Похожие презентации:
Фенолы
1.
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ«КРАСНОЯРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ ИМЕНИ ПРОФЕССОРА В.Ф. ВОЙНО-ЯСЕНЕЦКОГО»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАЦЕВТИЧЕСКИЙ КОЛЛЕДЖ
Тема: «Фенолы»
Преподаватель химии: Агафонова Н.В.
1
2.
План лекции:1.Фенолы.
2.Физические свойства.
3.Химические свойства.
4.Получение.
5.Применение.
2
3.
Фенол – органическое соединение,содержащее гидроксильную группу,
непосредственно связанную с бензольным
кольцом.
• фенолы – производные ароматических
углеводородов;
• фенолы – спирты, в которых группа –ОН связана
с бензольным кольцом.
Фенол
C6H5OH
3
4.
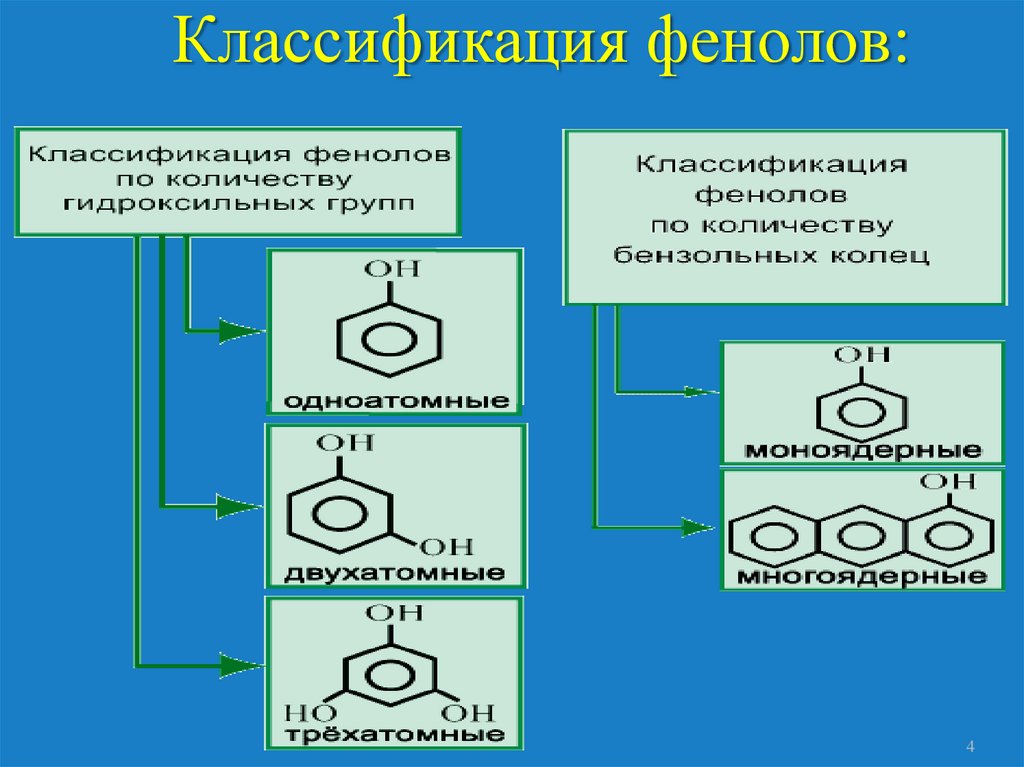
Классификация фенолов:4
5.
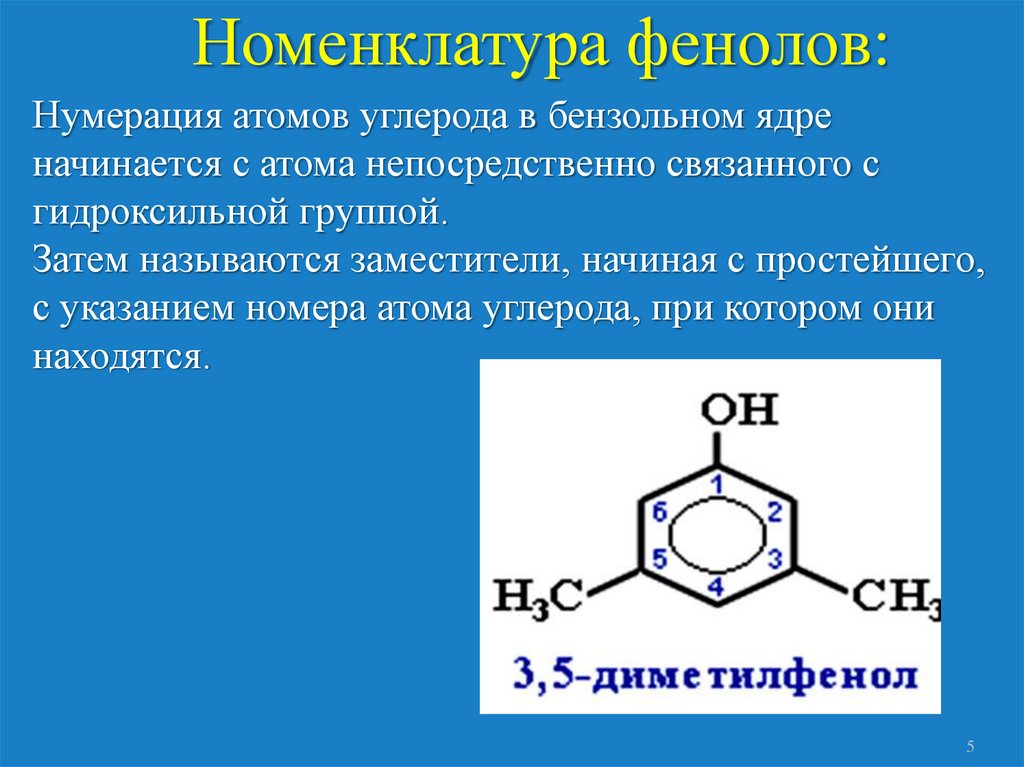
Номенклатура фенолов:Нумерация атомов углерода в бензольном ядре
начинается с атома непосредственно связанного с
гидроксильной группой.
Затем называются заместители, начиная с простейшего,
с указанием номера атома углерода, при котором они
находятся.
5
6.
Фенолы можно называть по ароматическойноменклатуре
6
7.
78.
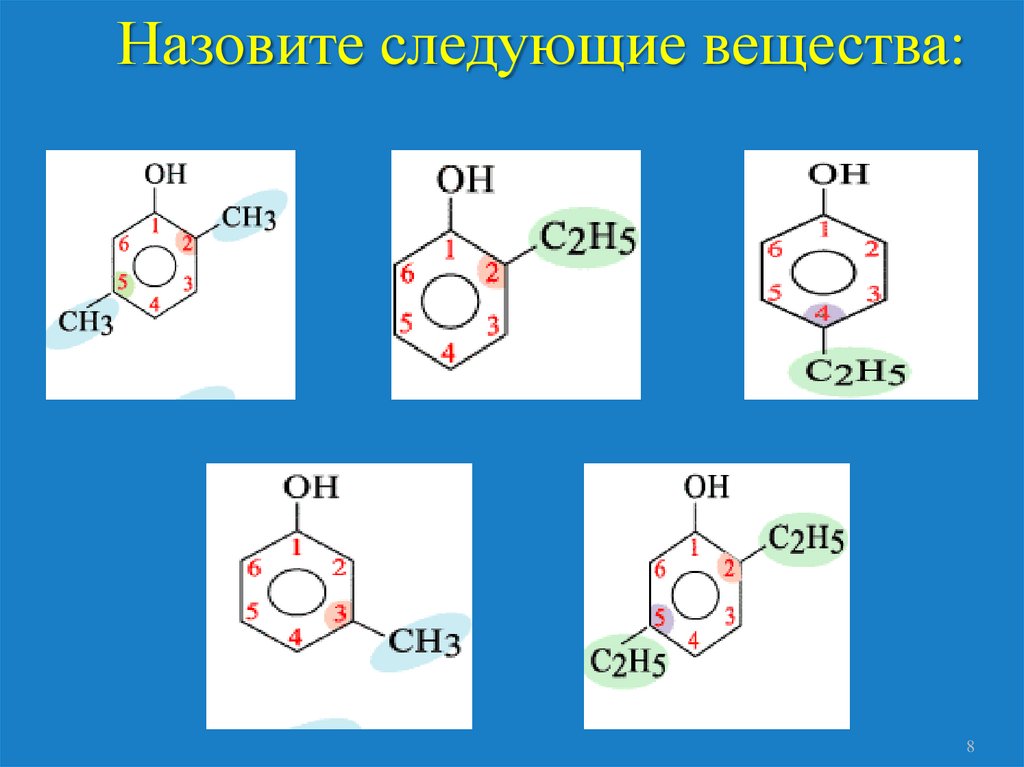
Назовите следующие вещества:8
9.
Физические свойства фенола:Фенол – бесцветное кристаллическое вещество.
Кристаллы фенола имеют игольчатую структуру. На
воздухе фенол окисляется и приобретает розовый
оттенок. Обладают специфическим запахом гуаши.
Фенол плавится при температуре 43 С, а кипит при
температуре 181ºС. Мало растворяется в воде при
комнатной температуре, однако быстро растворяется
при 60-70 ºС.
Фенол ядовит, при попадании на кожу
вызывает ожоги, одновременно он
всасывается через кожу и может вызвать
отравление.
9
10.
Химическиесвойства
10
11.
Химическиесвойства обусловлены
наличием:
1. Гидроксильной группы.
2. Бензольного кольца.
11
12.
Химические свойства обусловленныеналичием гидроксильной группы
1. Диссоциация фенола
12
13.
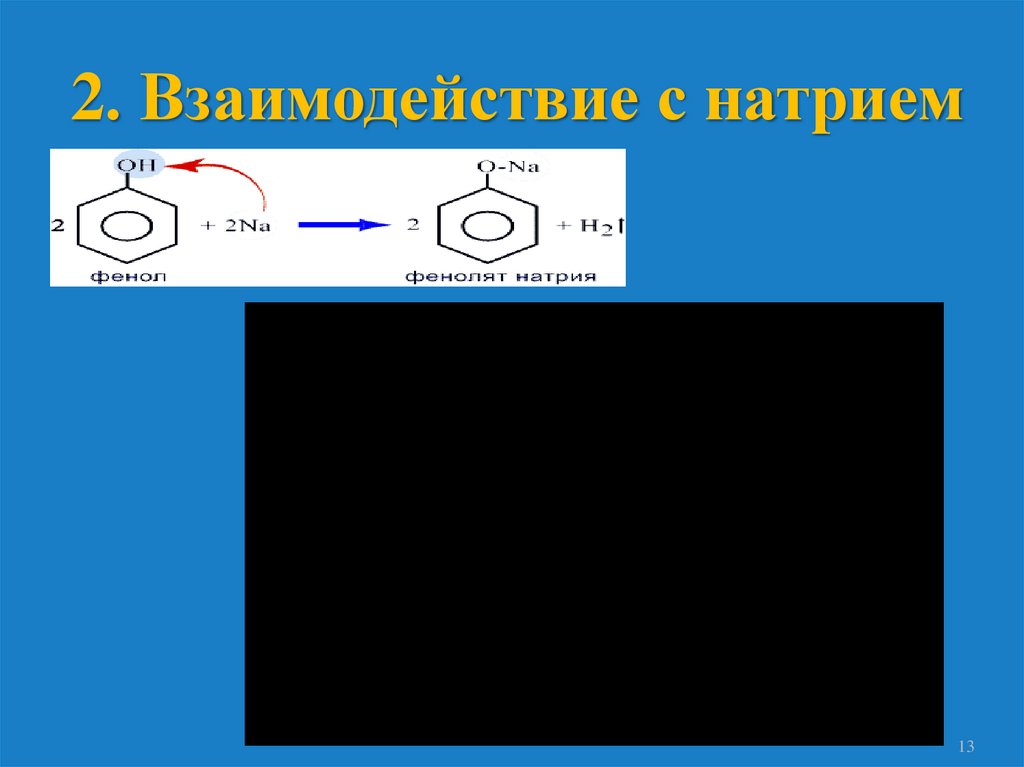
2. Взаимодействие с натрием13
14.
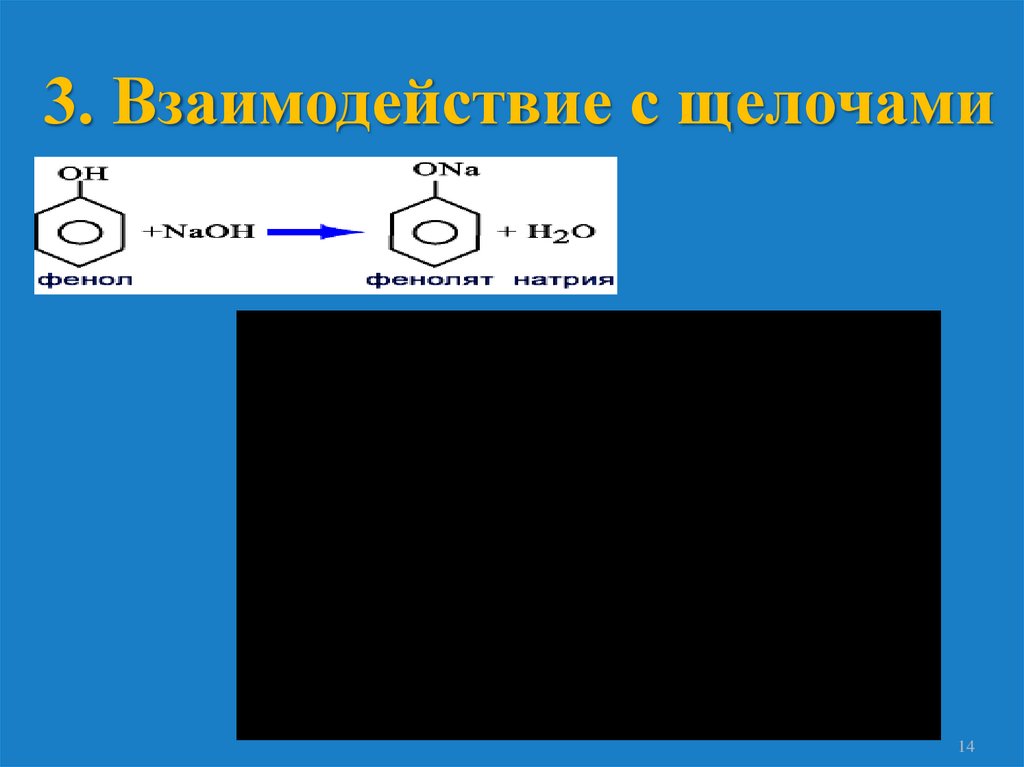
3. Взаимодействие с щелочами14
15.
При действии кислот фенолятаразлагаются с образованием
фенола и соли:
C6H5ONa + HCl C6H5OH + NaCl
15
16.
4. Взаимодействие с солямиВзаимодействие с хлоридом железа (III)
(качественная реакция на фенол)
C6H5OH + FeCl3 → [C6H5OFe](Cl)2 + HCl
16
17.
Химические свойства обусловленные наличиембензольного ядра
1. Реакции окисления
Фенол окисляется
кислородом воздуха,
приобретая розовую
окраску
17
18.
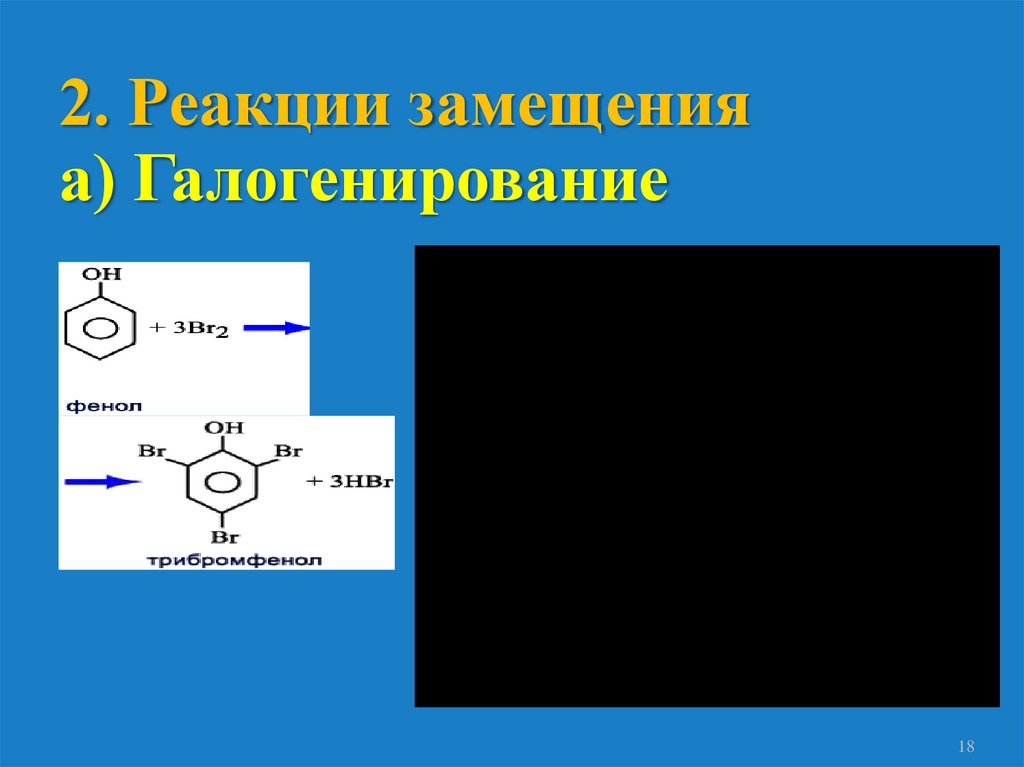
2. Реакции замещенияа) Галогенирование
18
19.
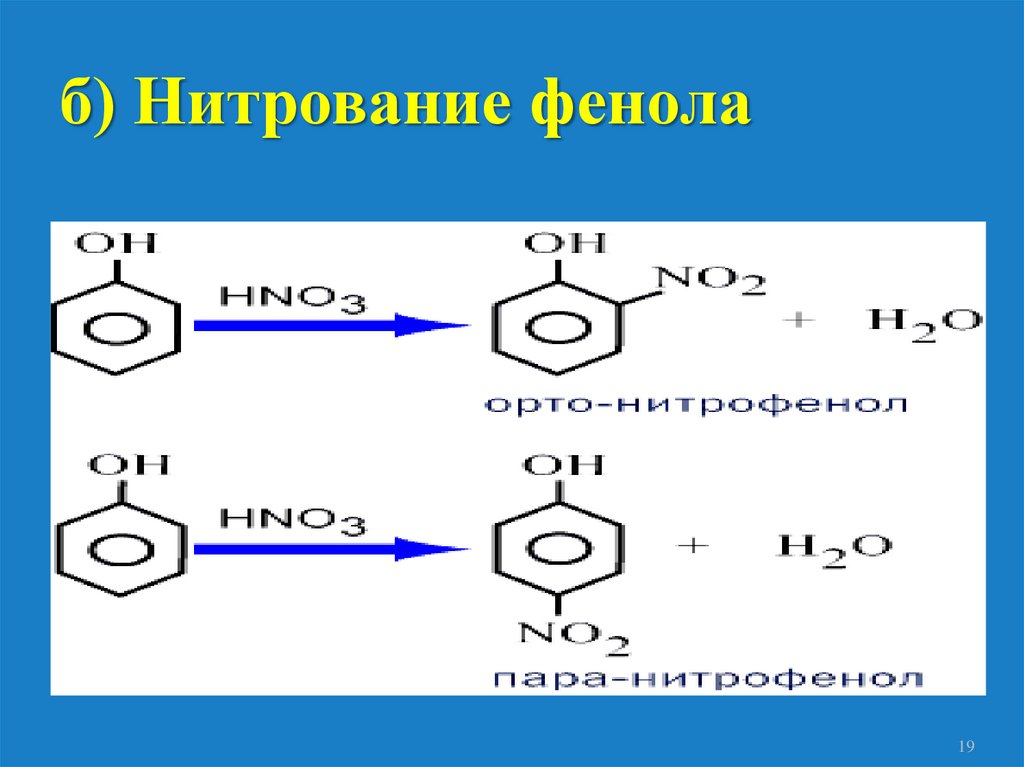
б) Нитрование фенола19
20.
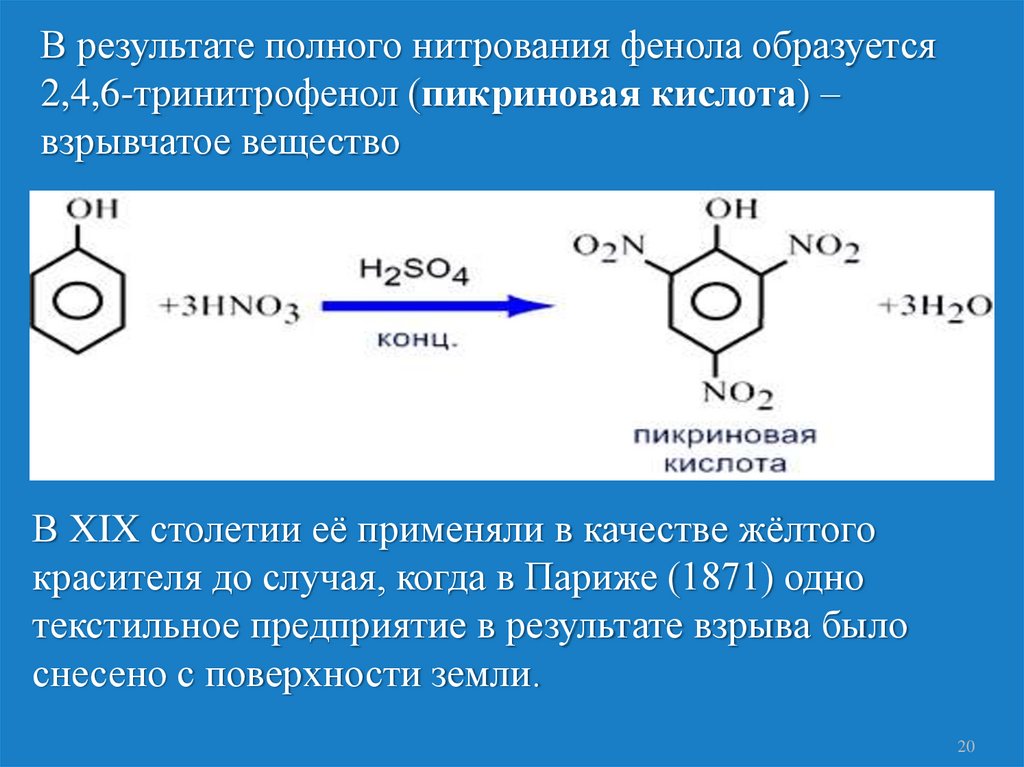
В результате полного нитрования фенола образуется2,4,6-тринитрофенол (пикриновая кислота) –
взрывчатое вещество
В XIX столетии её применяли в качестве жёлтого
красителя до случая, когда в Париже (1871) одно
текстильное предприятие в результате взрыва было
снесено с поверхности земли.
20
21.
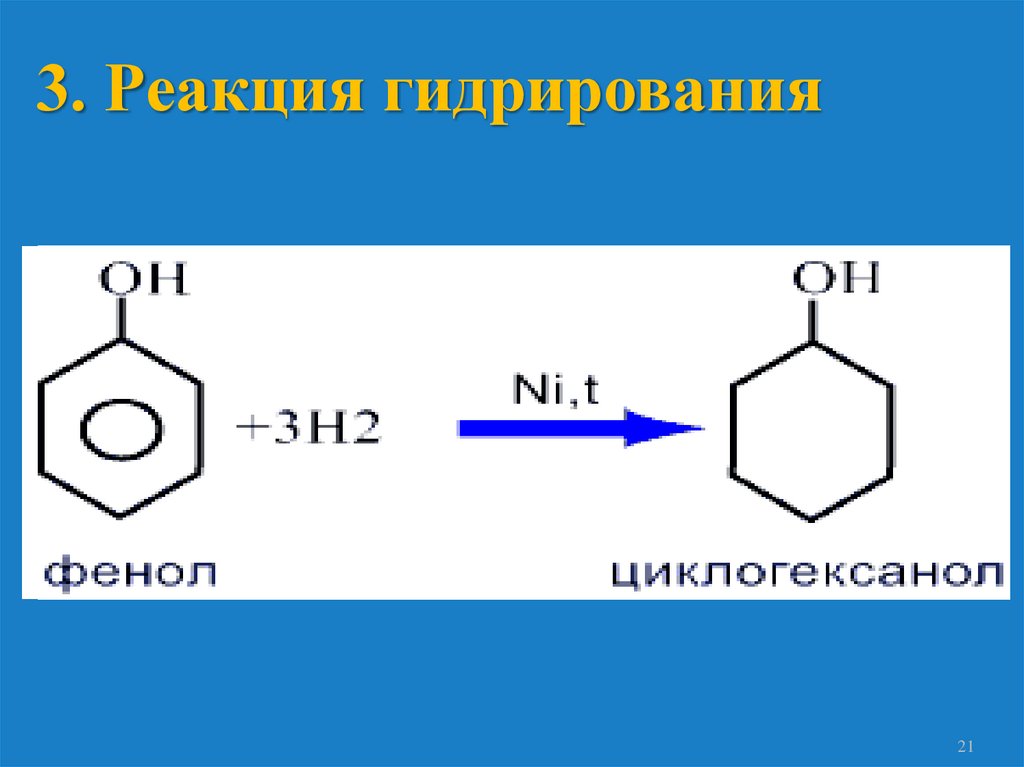
3. Реакция гидрирования21
22.
Получение фенола22
23.
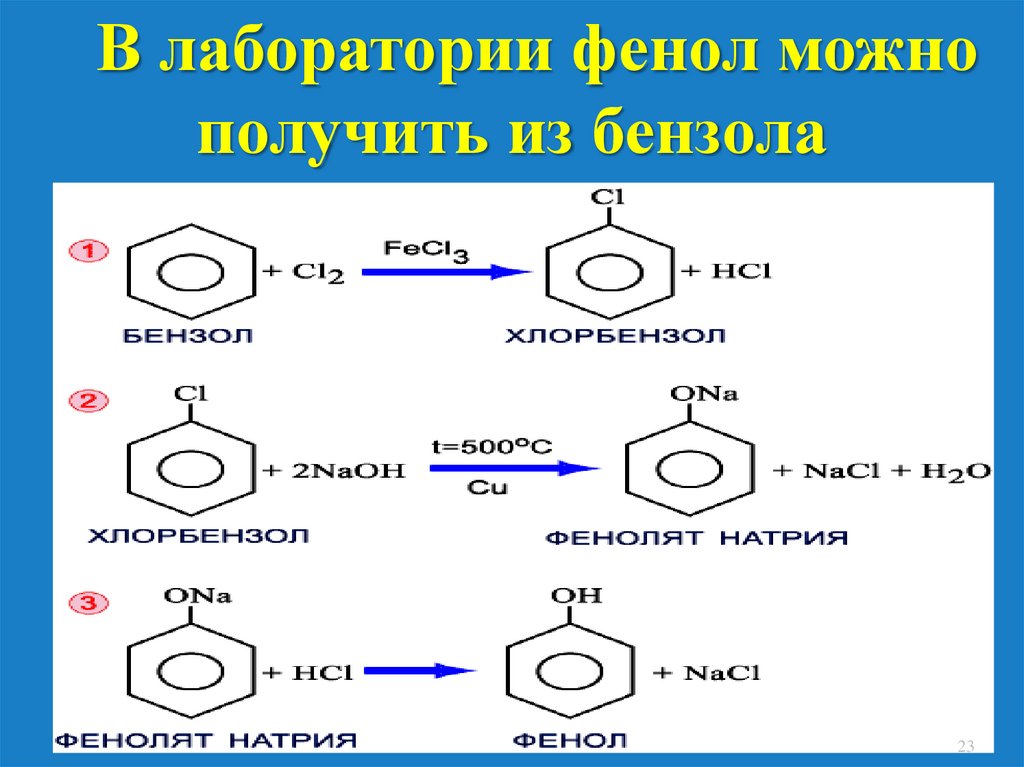
В лаборатории фенол можнополучить из бензола
23
24.
ПрименениеФенол в больших количествах используется
изготовления пластмасс, красителей, лекарственных
веществ.
Фенол – антисептическое и дезинфицирующее
средство. Применяемое для лечения некоторых
кожных заболеваний. Используется в синтезе
многих лекарственных средств.
24
25.
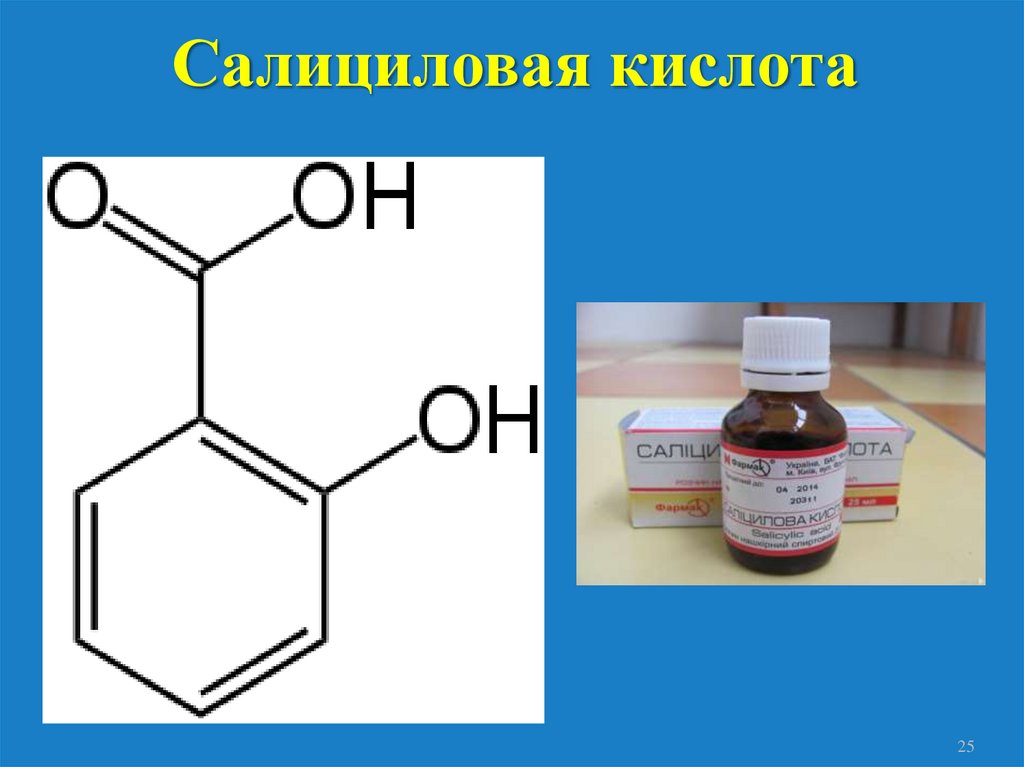
Салициловая кислота25
26.
Метилсалицилат26
27.
Салол(фениловый эфир
салициловой кислоты)
27
28.
Аспирин(ацетилсалициловая кислота
28
29.
Парацетамол29
30.
Фенолфталеин (пурген)C20H14O4
30
31.
Резорцин31
32.
ФЕНОЛ является одним из наиболее опасных дляздоровья человека веществ, и, к сожалению
достаточно широко распространенным
32
33.
Закрепление1. Выберите верное утверждение:
1) фенолы диссоциируют в большей степени, чем
спирты;
2) фенолы проявляют основные свойства;
3) фенолы и их производные не обладают
токсическим действием;
4) атом водорода в гидроксильной группе фенола не
может быть замещен на катион металла под
действием оснований.
33
34.
2. Фенол не взаимодействует с:1)
2)
3)
4)
метаналем;
метаном;
азотной кислотой;
бромной водой.
34
35.
3. Фенол взаимодействует c:1)
2)
3)
4)
соляной кислотой;
этиленом;
гидроксидом натрия;
метаном.
35
36.
4. Фенол в водном растворе является:1) сильной кислотой;
2) слабой кислотой;
3) слабым основанием;
4) сильным основанием.
36
37.
5. фенолов состава С7Н8О существует%1)
2)
3)
4)
один;
четыре;
три;
два.
37
38.
Спасибо за внимание38



























 Химия
Химия








