Похожие презентации:
Теория электролитической диссоциации
1.
2.
Вопросы темы1
Электролиты и неэлектролиты
2
Положения теории электролитической диссоциации
3
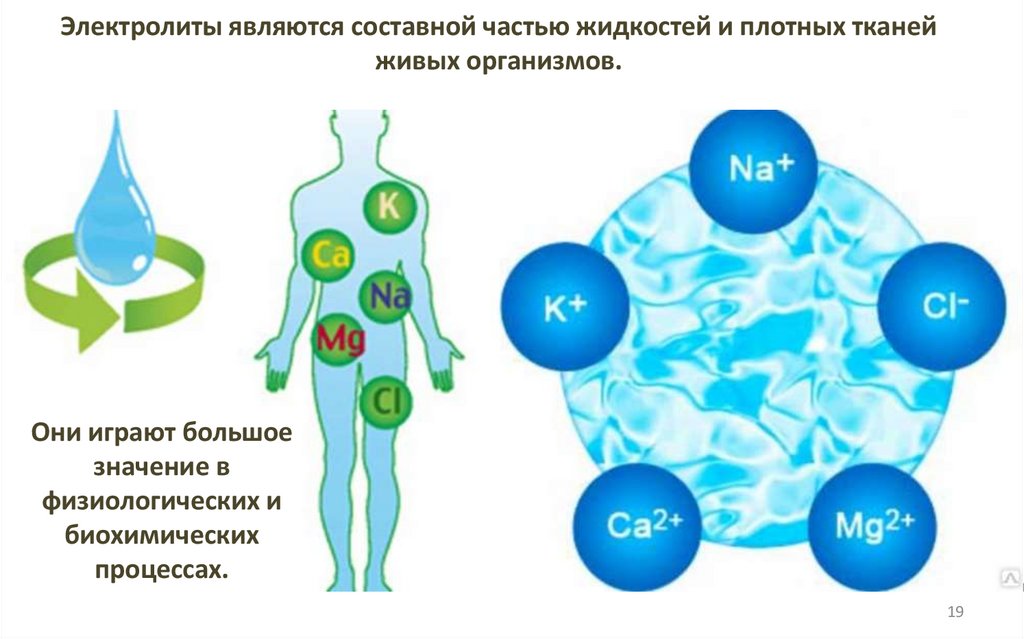
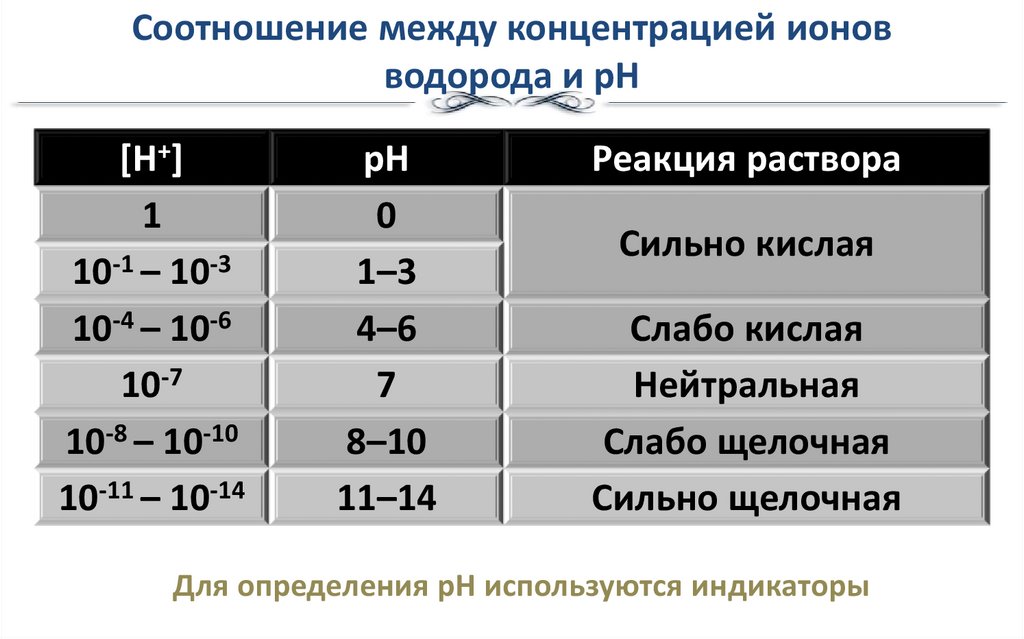
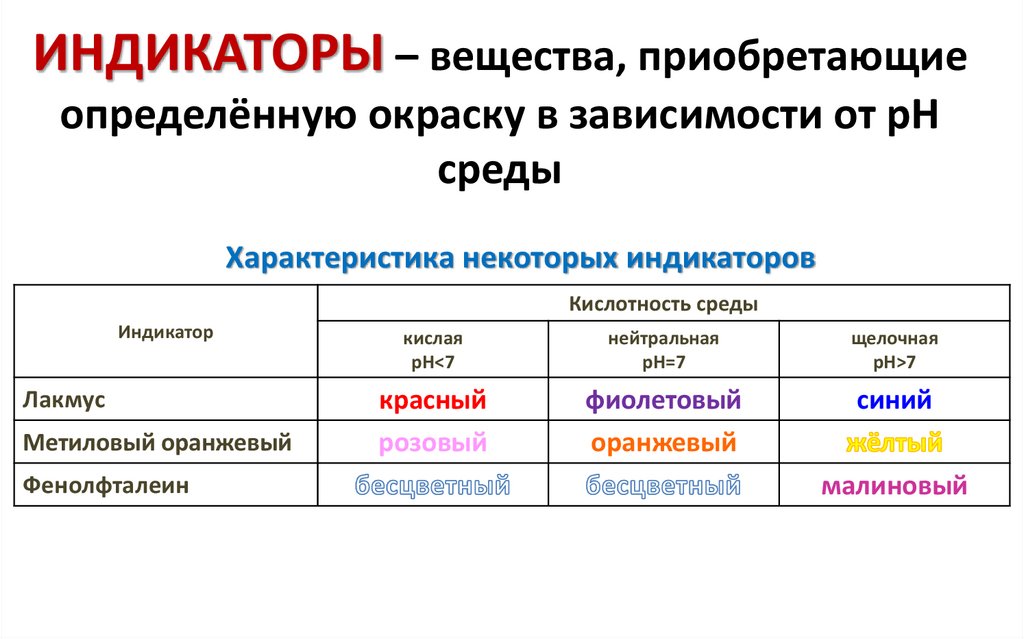
Кислотность и основность растворов
4
Диссоциация основных классов неорганических соединений
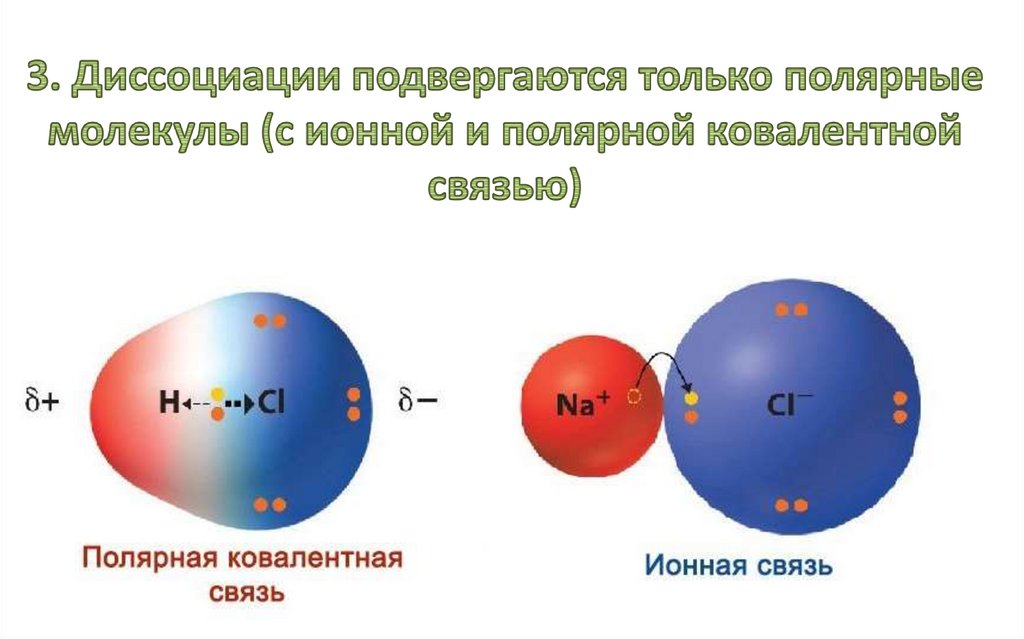
3.
34.
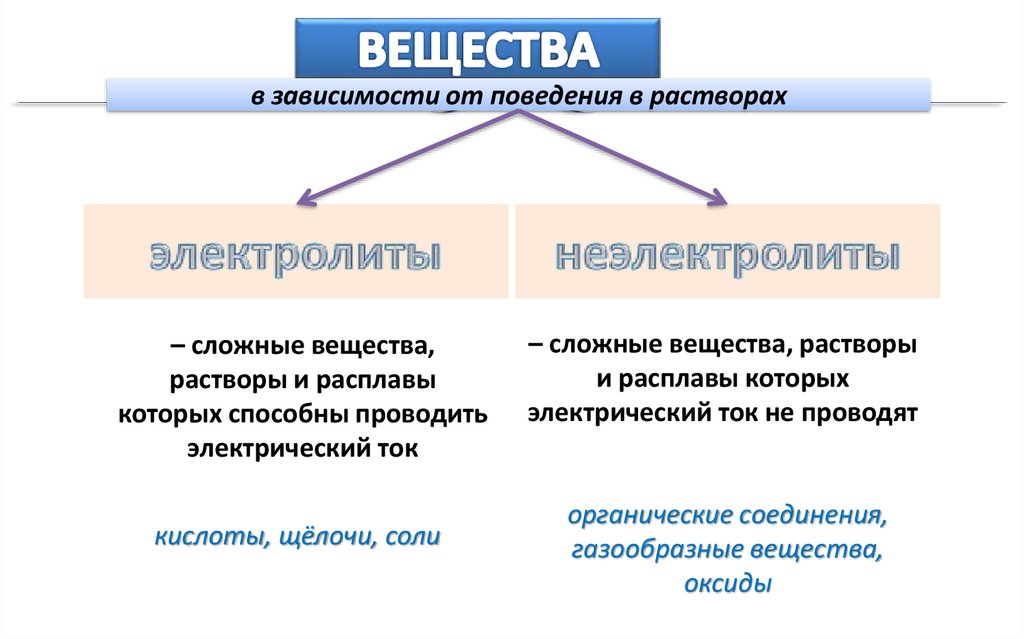
в зависимости от поведения в растворах– сложные вещества,
растворы и расплавы
которых способны проводить
электрический ток
кислоты, щёлочи, соли
– сложные вещества, растворы
и расплавы которых
электрический ток не проводят
органические соединения,
газообразные вещества,
оксиды
5.
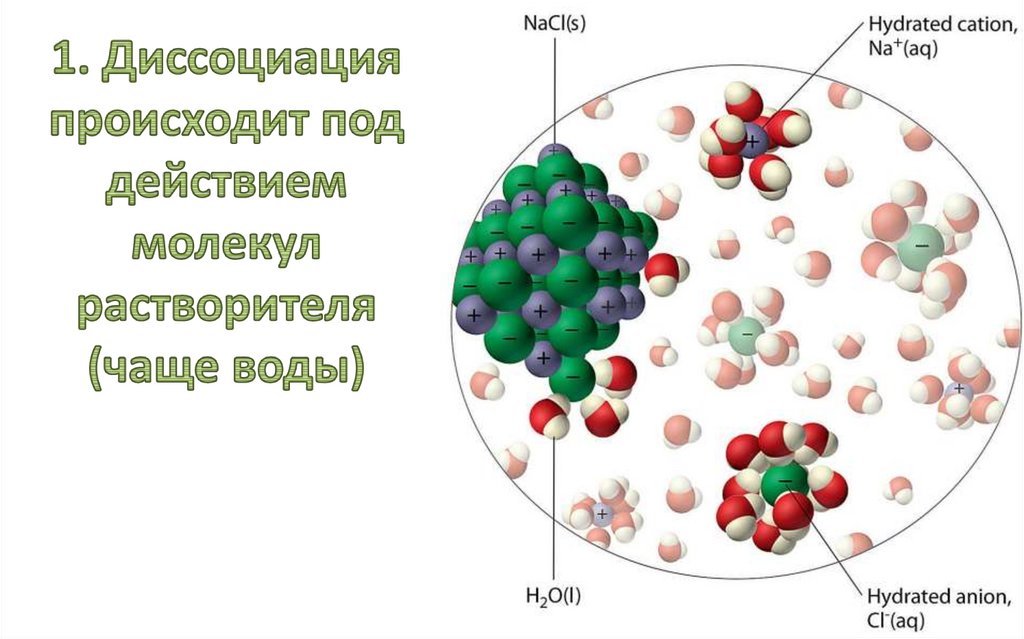
ЭЛЕКТРОЛИТИЧЕСКАЯДИССОЦИАЦИЯ
(ионизация) — процесс
распада веществ на ионы при
растворении или плавлении
6.
Для объяснения свойств водныхрастворов электролитов С. Аррениус в
1887 году предложил теорию
электролитической диссоциации
(ТЭД). Эта теория объясняла, почему
растворы некоторых веществ проводят
электрический ток, но не отвечала на
вопрос, почему одни вещества
являются электролитами, а другие —
нет.
Сва́нте А́вгуст
Арре́ниус
Svante August Arrhenius
19.02.1859 — 02.10.1927
— шведский физико-химик,
автор теории
электролитической
диссоциации, лауреат
Нобелевской премии по
химии (1903).
6
7.
Причину электролитическойдиссоциации объяснили
российские химики И.А.
Каблуков и В.А. Кистяковский
(1890–1891), которые опирались
на химическую теорию
растворов Д.И. Менделеева
(1887).
Иван Алексеевич
Каблуков
Владимир Александрович
Кистяковский
21.08.1857 — 05.05.1942
30.09.1865 — 19.10.1952
— российский и советский
физикохимик, академик АН
СССР (1929, членкорреспондент с 1925).
— советский физикохимик.
7
8.
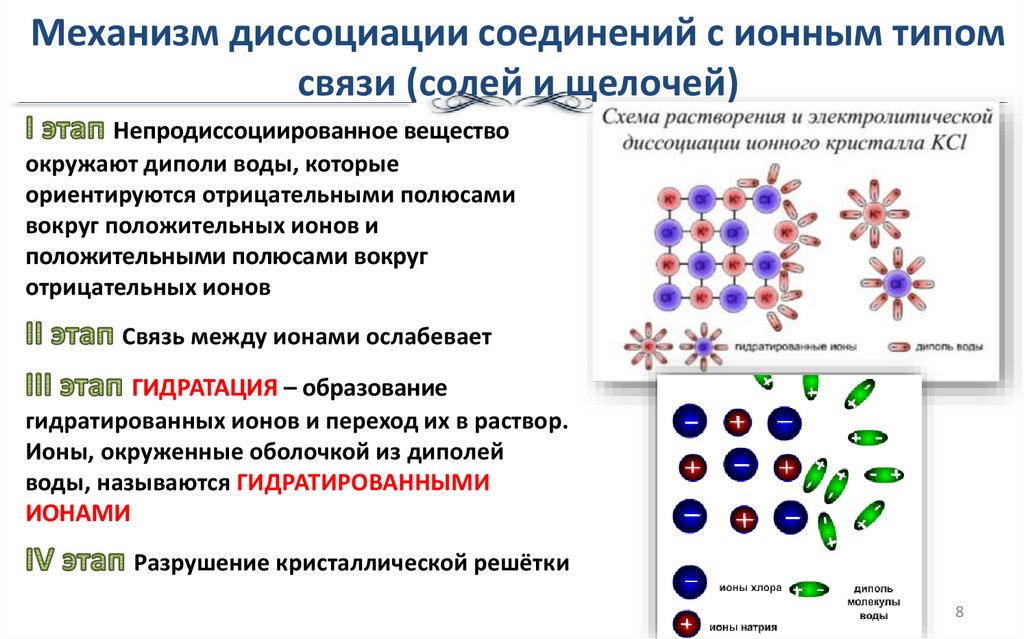
Механизм диссоциации соединений с ионным типомсвязи (солей и щелочей)
Непродиссоциированное вещество
окружают диполи воды, которые
ориентируются отрицательными полюсами
вокруг положительных ионов и
положительными полюсами вокруг
отрицательных ионов
Связь между ионами ослабевает
ГИДРАТАЦИЯ – образование
гидратированных ионов и переход их в раствор.
Ионы, окруженные оболочкой из диполей
воды, называются ГИДРАТИРОВАННЫМИ
ИОНАМИ
Разрушение кристаллической решётки
8
9.
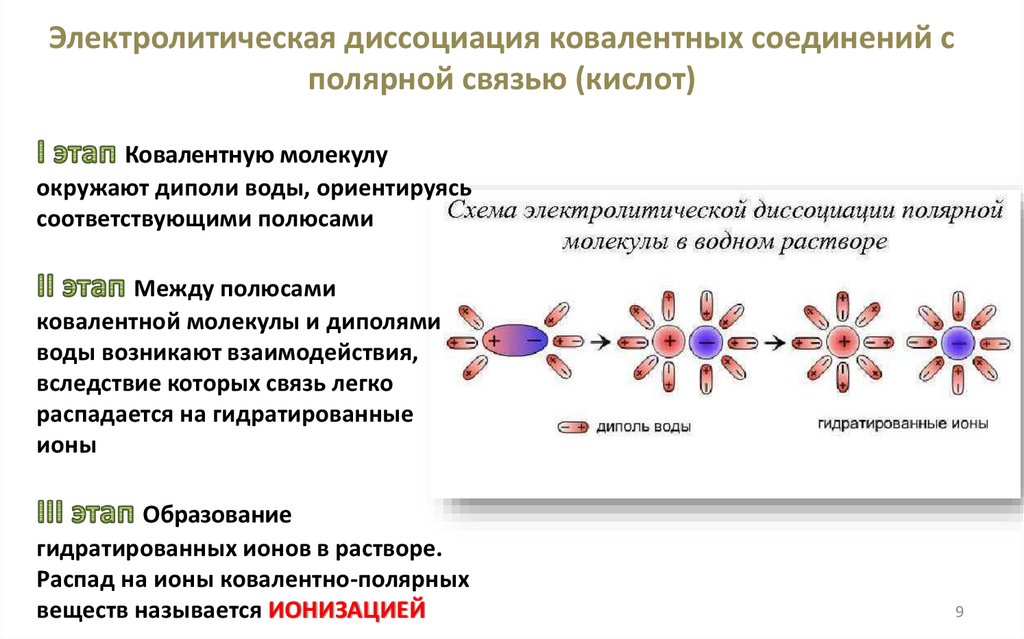
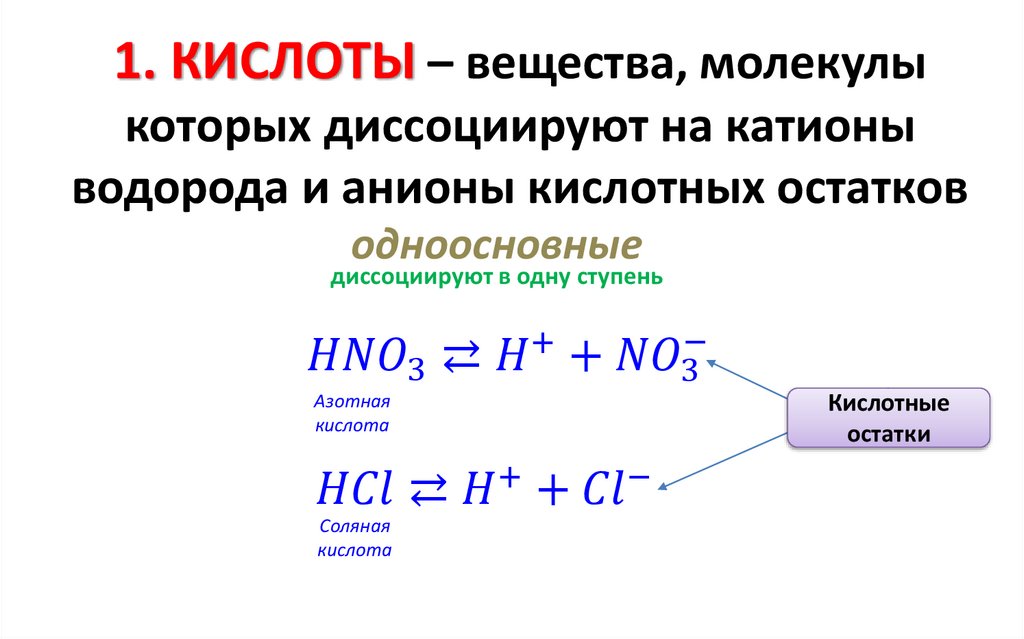
Электролитическая диссоциация ковалентных соединений сполярной связью (кислот)
Ковалентную молекулу
окружают диполи воды, ориентируясь
соответствующими полюсами
Между полюсами
ковалентной молекулы и диполями
воды возникают взаимодействия,
вследствие которых связь легко
распадается на гидратированные
ионы
Образование
гидратированных ионов в растворе.
Распад на ионы ковалентно-полярных
веществ называется ИОНИЗАЦИЕЙ
9
10.
1011.
12.
диссоциация+



















 Химия
Химия








