Похожие презентации:
Карбоновые кислоты
1.
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ«КРАСНОЯРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ ИМЕНИ ПРОФЕССОРА В.Ф. ВОЙНО-ЯСЕНЕЦКОГО»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАЦЕВТИЧЕСКИЙ КОЛЛЕДЖ
Преподаватель химии: Агафонова Н.В.
2.
План:1. Состав и классификация.
2. Номенклатура.
3. Изомерия.
4. Физические свойства.
5. Строение карбоксильной группы.
6. Химические свойства.
7. Получение карбоновых кислот.
8. Физиологическая активность и
применение в медицине.
2
3.
34.
Благодаря работам выдающегося шведскогохимика Карла Вильгельма Шееле к концу XVIII
стало известно около десяти различных
органических кислот он выделил и описал
лимонную, молочную, щавелевую и другие
кислот.
К.В. Шееле
4
5.
Уксусная кислота была известна еще в древнем мире ввиде уксуса, образующегося при скисании вина. Это
была единственная известная в то время кислота. Ее
способность растворять жемчуг и известняк
послужила основой для легенды о том, что Александр
Македонский во время своих походов устранял скалы
с пути, разрушая их уксусом.
5
6.
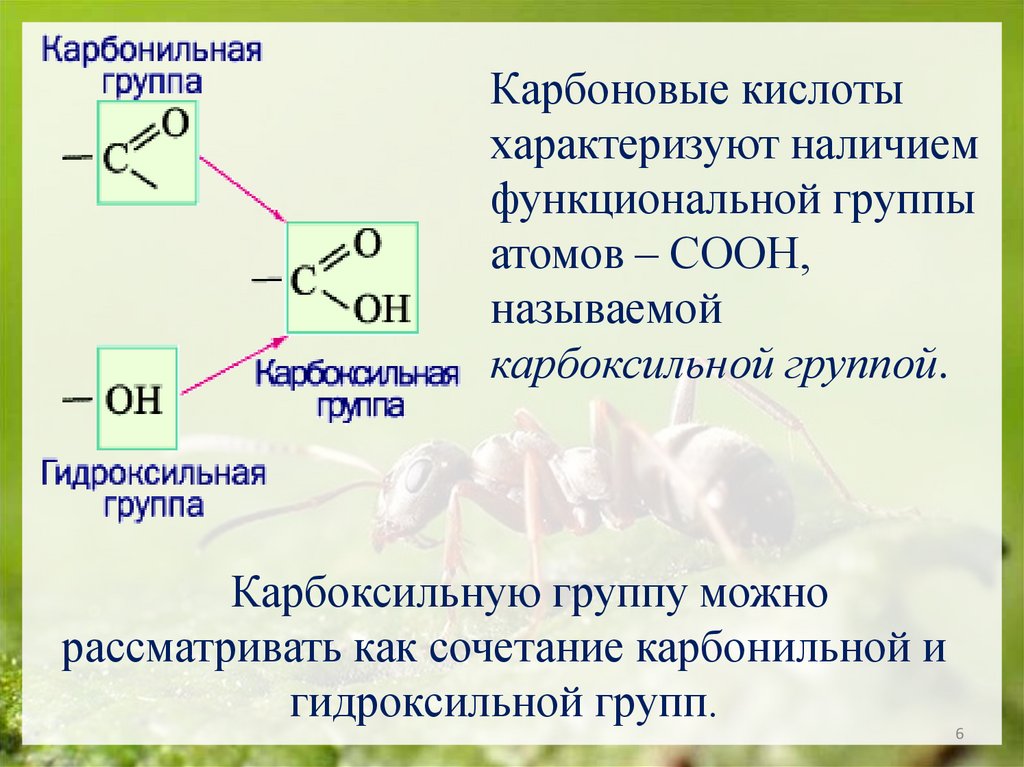
Карбоновые кислотыхарактеризуют наличием
функциональной группы
атомов – СООН,
называемой
карбоксильной группой.
Карбоксильную группу можно
рассматривать как сочетание карбонильной и
гидроксильной групп.
6
7.
Карбоновые кислоты – органическиевещества, молекулы которых содержат одну или
несколько карбоксильных групп, соединенных с
углеводородным радикалом (исключение –
муравьиная кислота)
7
8.
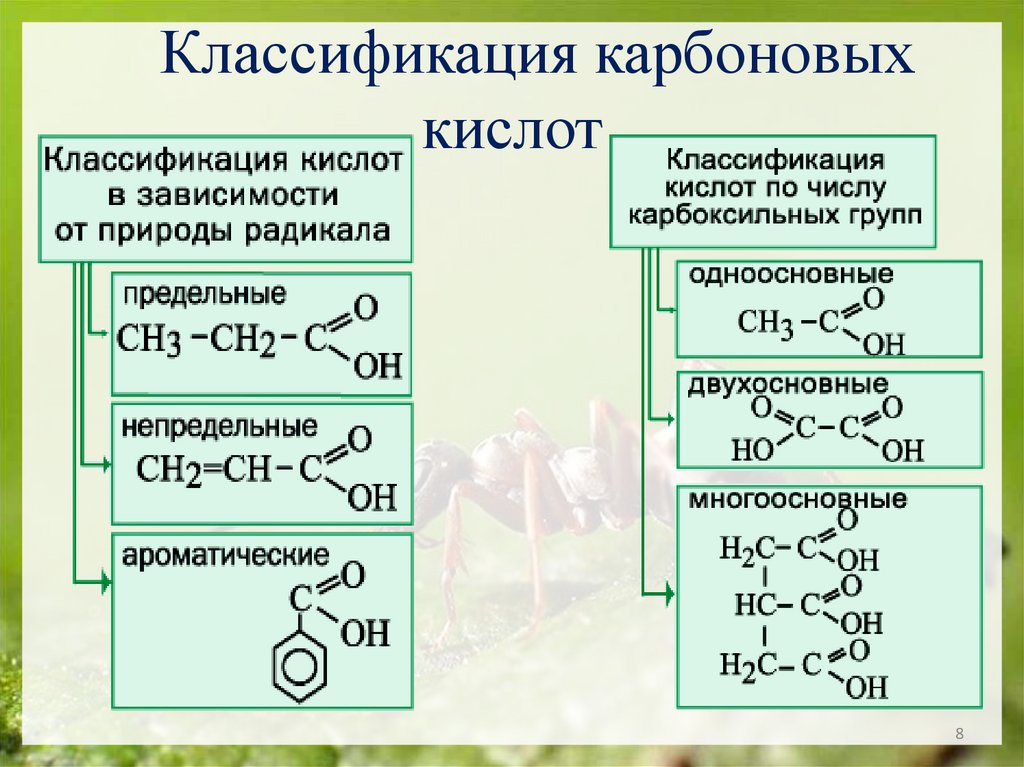
Классификация карбоновыхкислот
8
9.
910.
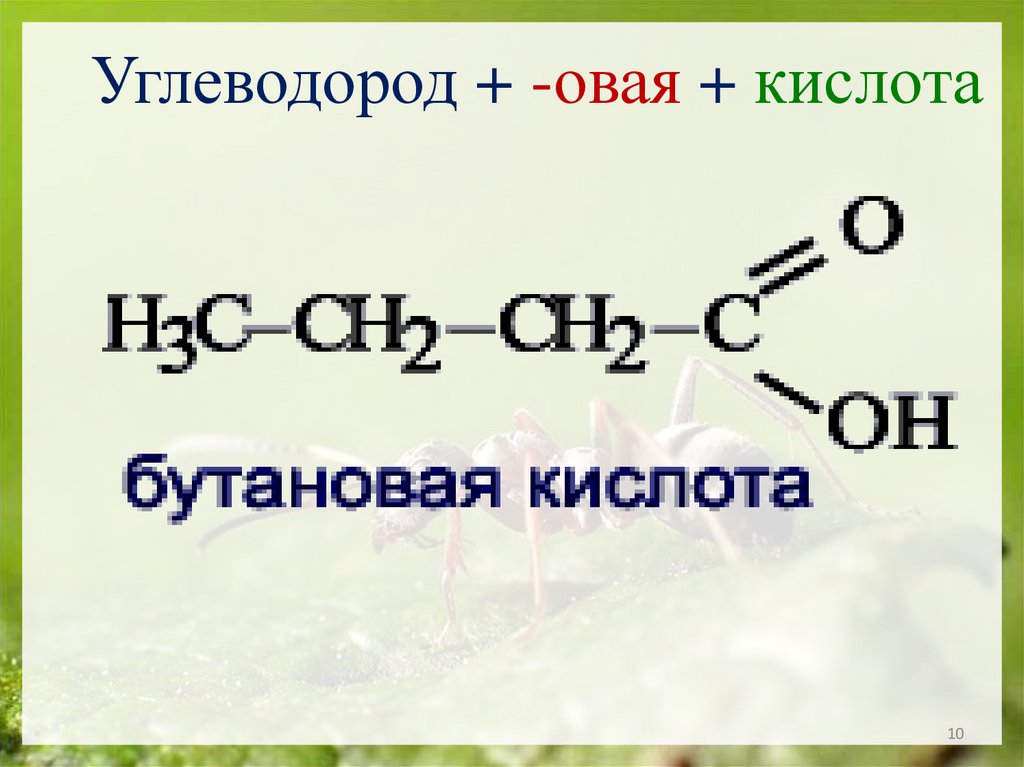
Углеводород + -овая + кислота10
11.
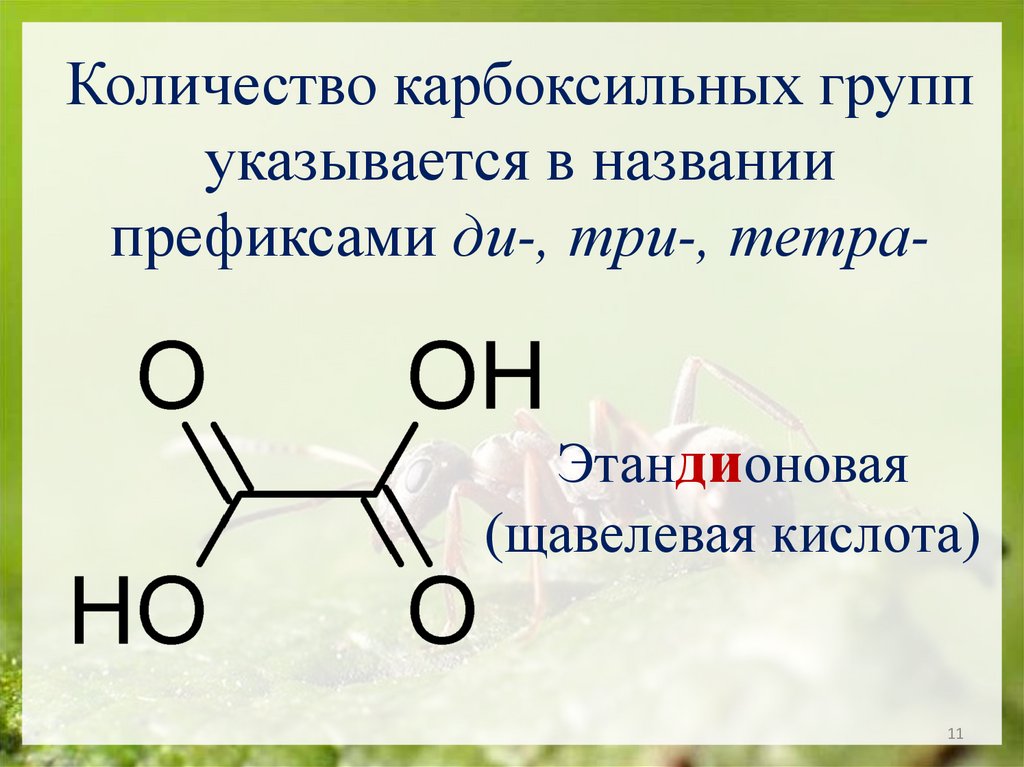
Количество карбоксильных группуказывается в названии
префиксами ди-, три-, тетраЭтандионовая
(щавелевая кислота)
11
12.
Насыщенные одноосновные кислотысодержат одну карбоксильную группу и
образуют гомологический ряд с общей
формулой CnH2n+1COOH.
12
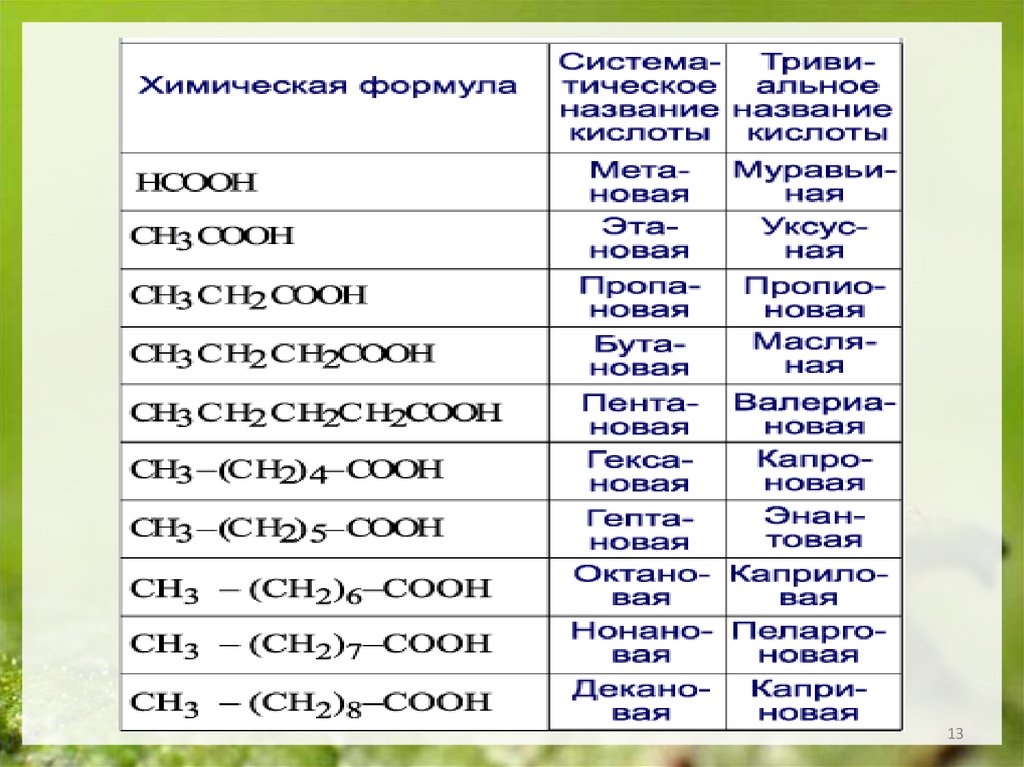
13.
1314.
1415.
Начиная с четвертого членагомологического ряда возможна
изомерия углеродного скелета.
Нумерация атомов углерода
начинают с углерода карбоксильной
группы.
2-метилпропановая
кислота
15
16.
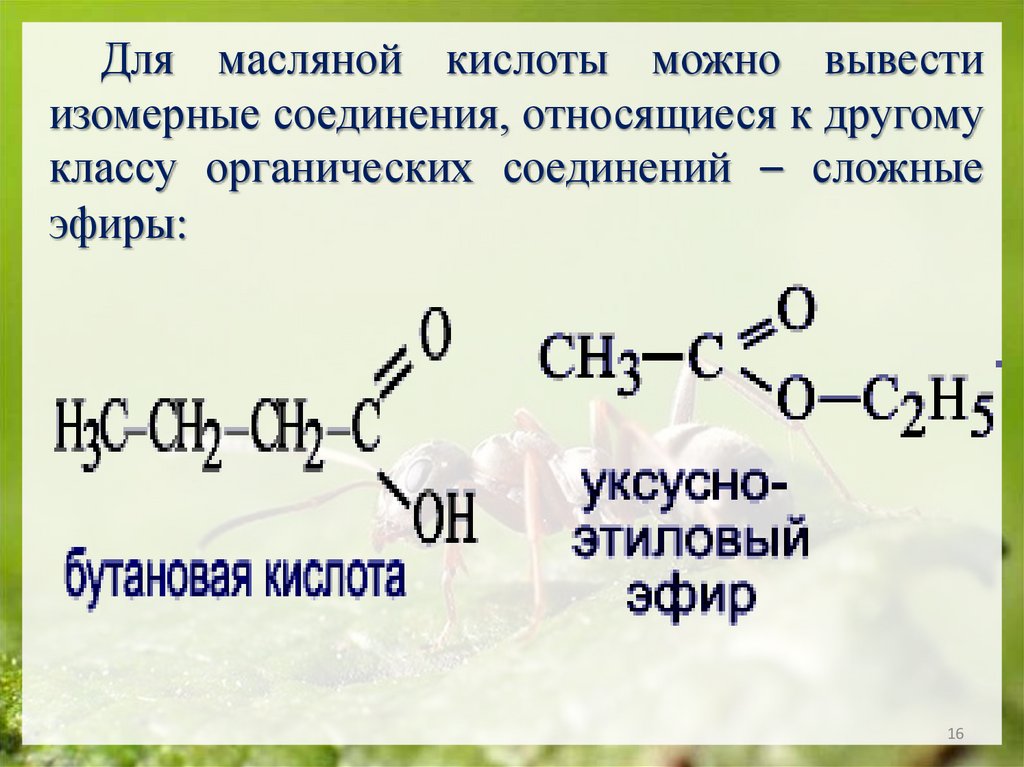
Для масляной кислоты можно вывестиизомерные соединения, относящиеся к другому
классу органических соединений – сложные
эфиры:
16
17.
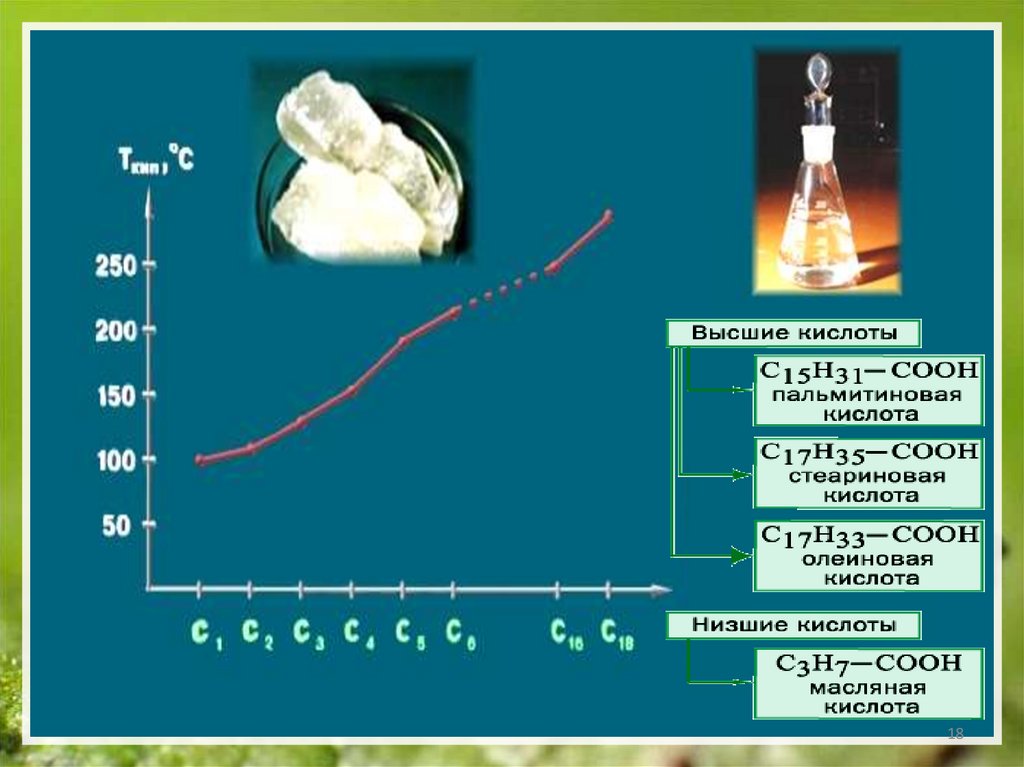
1718.
1819.
1920.
Электронная плотность смещена катому кислороду как более
электроотрицательного элемента. В
следствии этого карбонильный атом
углерода приобретает частично
положительный заряд.
Чтобы его компенсировать карбонильный атом углерода
притягивает электроны атома кислорода гидроксильной
группы. Электронная плотность на атоме углерода
понижается, и он смещает в свою сторону электронную
плотность связи –О-Н. Полярность связи в
гидроксильной группе возрастает, водород становится
более подвижным и легче отщепляется в виде протона.
20
21.
2122.
1. Диссоциация кислотВ водном растворе они диссоциируют с
образованием протонов и кислотных
остатков:
Раствор имеет кислый вкус и изменяет цвет
индикатора.
22
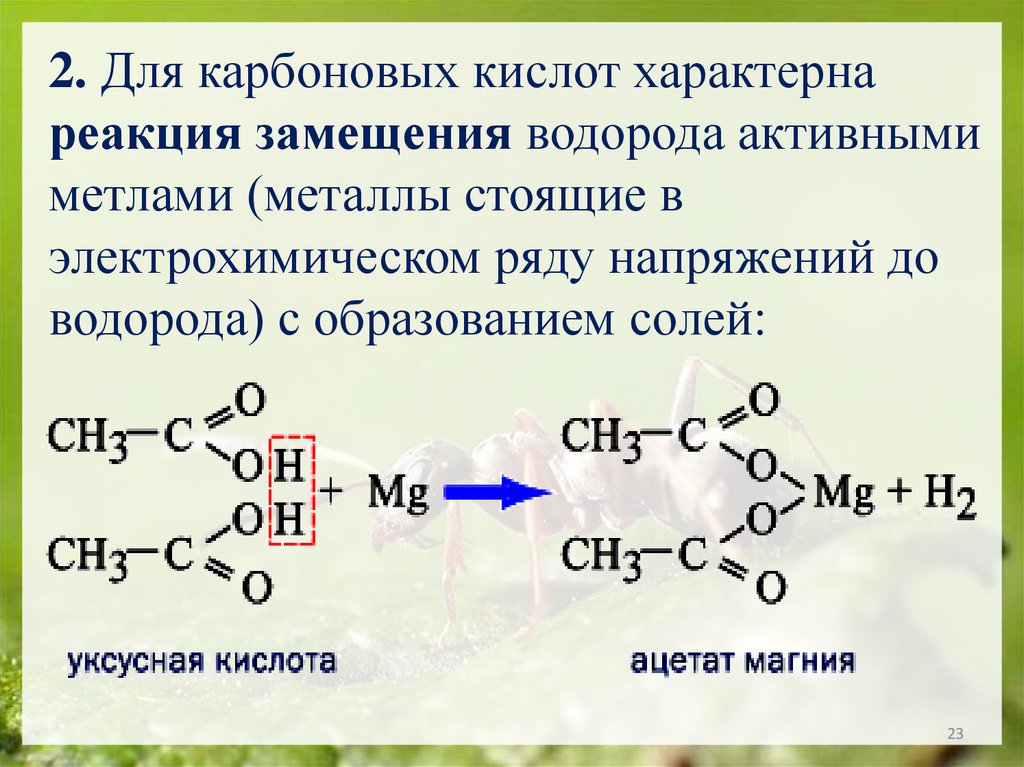
23.
2. Для карбоновых кислот характернареакция замещения водорода активными
метлами (металлы стоящие в
электрохимическом ряду напряжений до
водорода) с образованием солей:
23
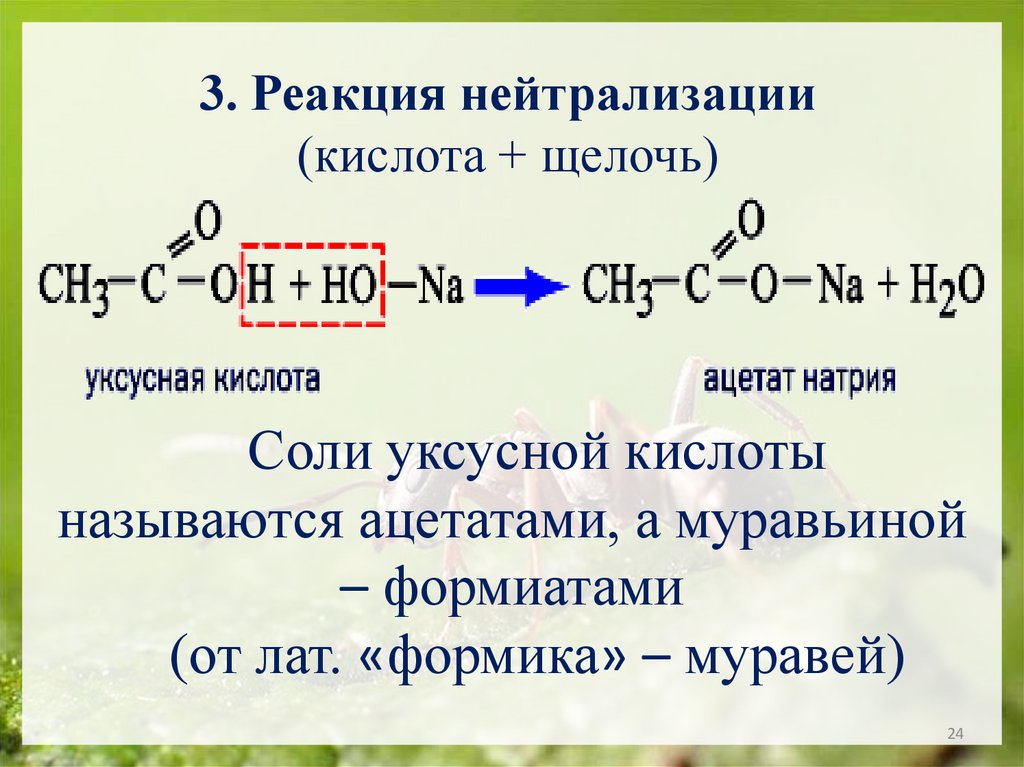
24.
3. Реакция нейтрализации(кислота + щелочь)
Соли уксусной кислоты
называются ацетатами, а муравьиной
– формиатами
(от лат. «формика» – муравей)
24
25.
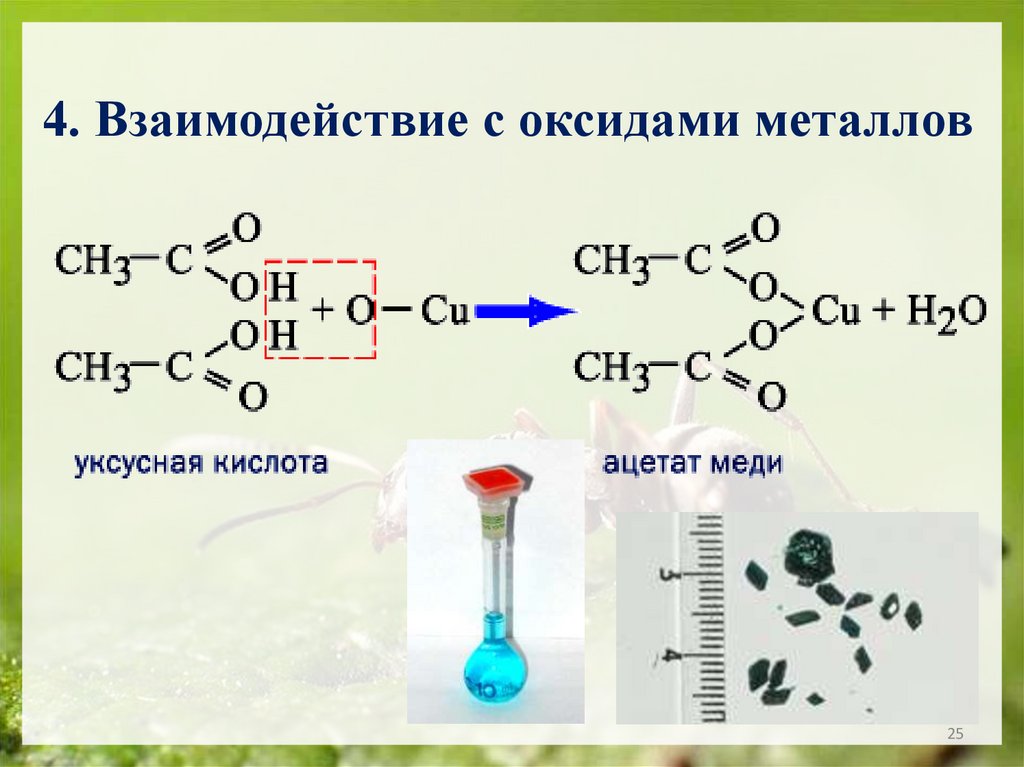
4. Взаимодействие с оксидами металлов25
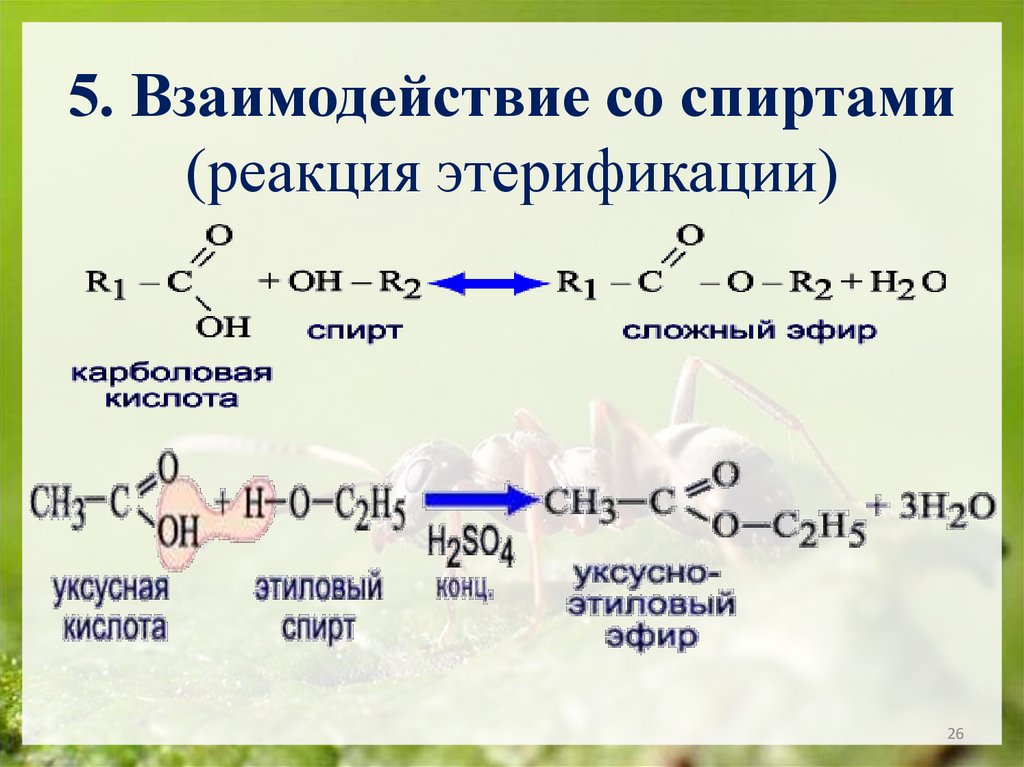
26.
5. Взаимодействие со спиртами(реакция этерификации)
26
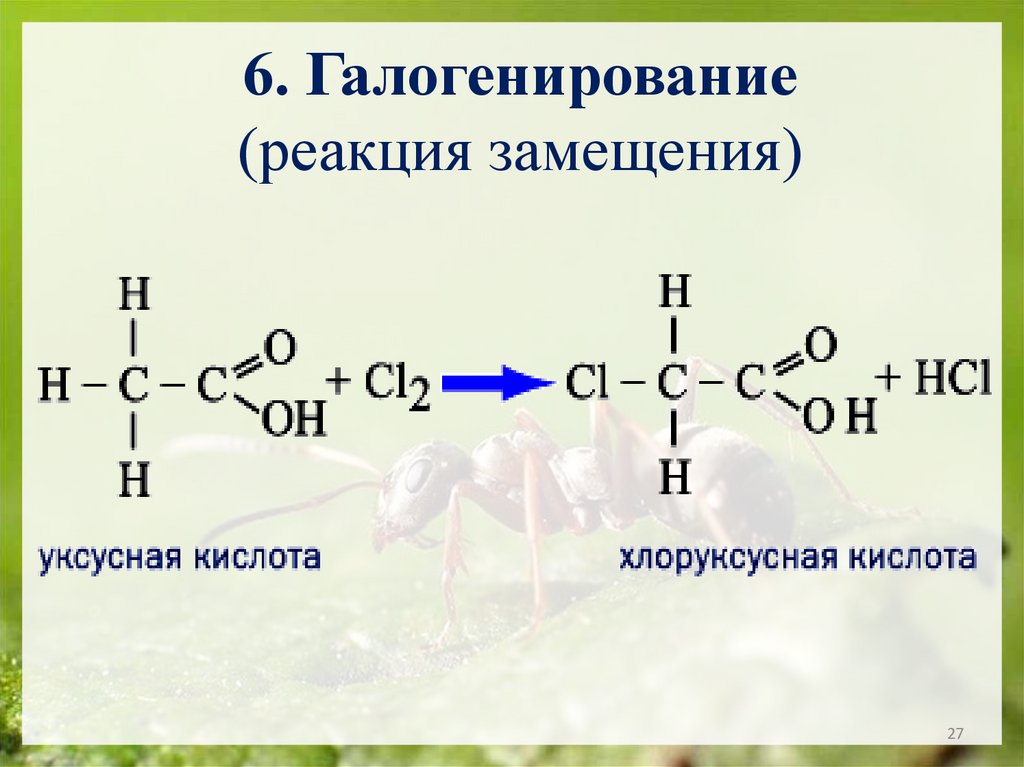
27.
6. Галогенирование(реакция замещения)
27
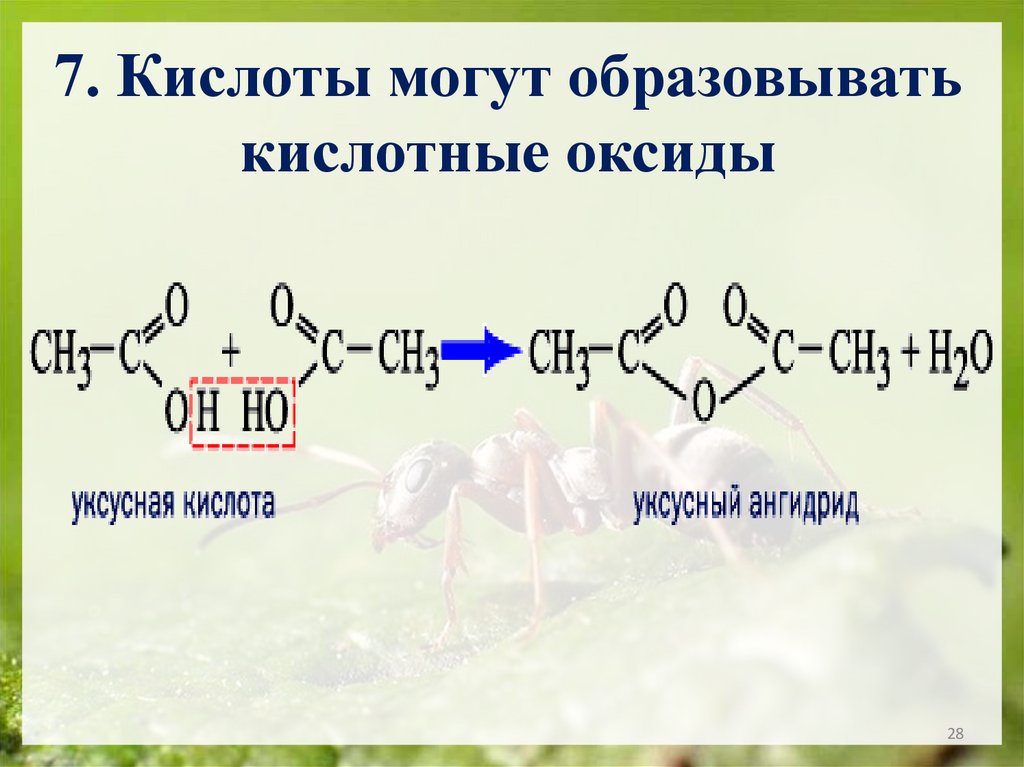
28.
7. Кислоты могут образовыватькислотные оксиды
28
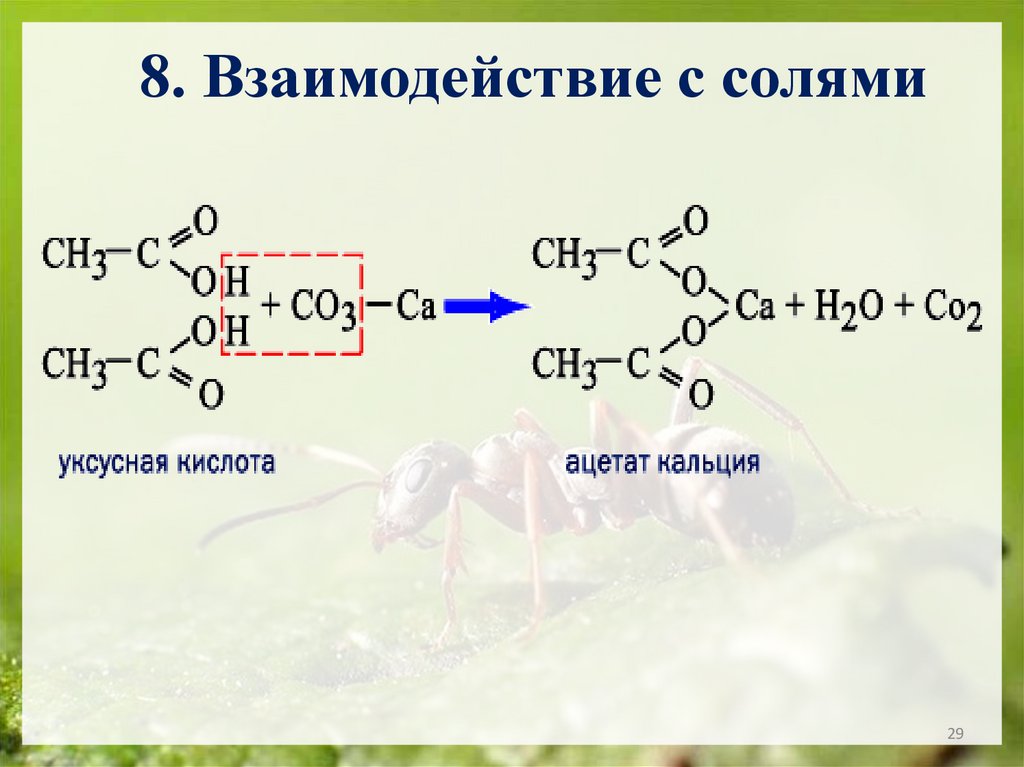
29.
8. Взаимодействие с солями29
30.
Горение паров уксусной кислоты30
31.
Химические свойства уксусной кислоты31
32.
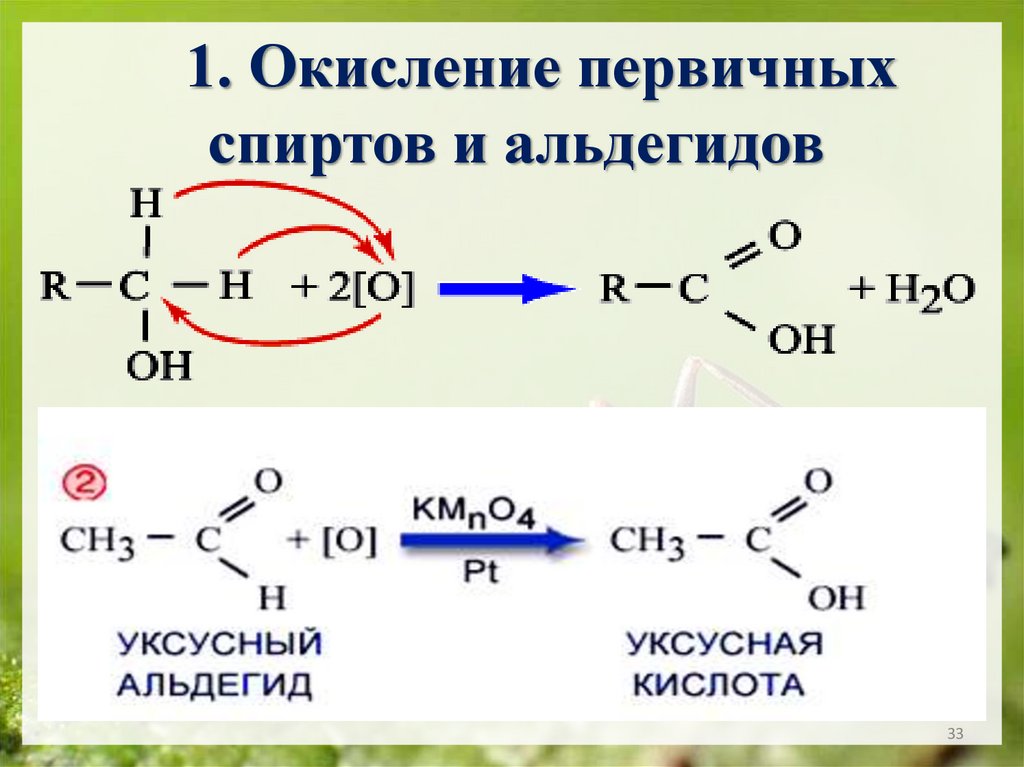
3233.
1. Окисление первичныхспиртов и альдегидов
33
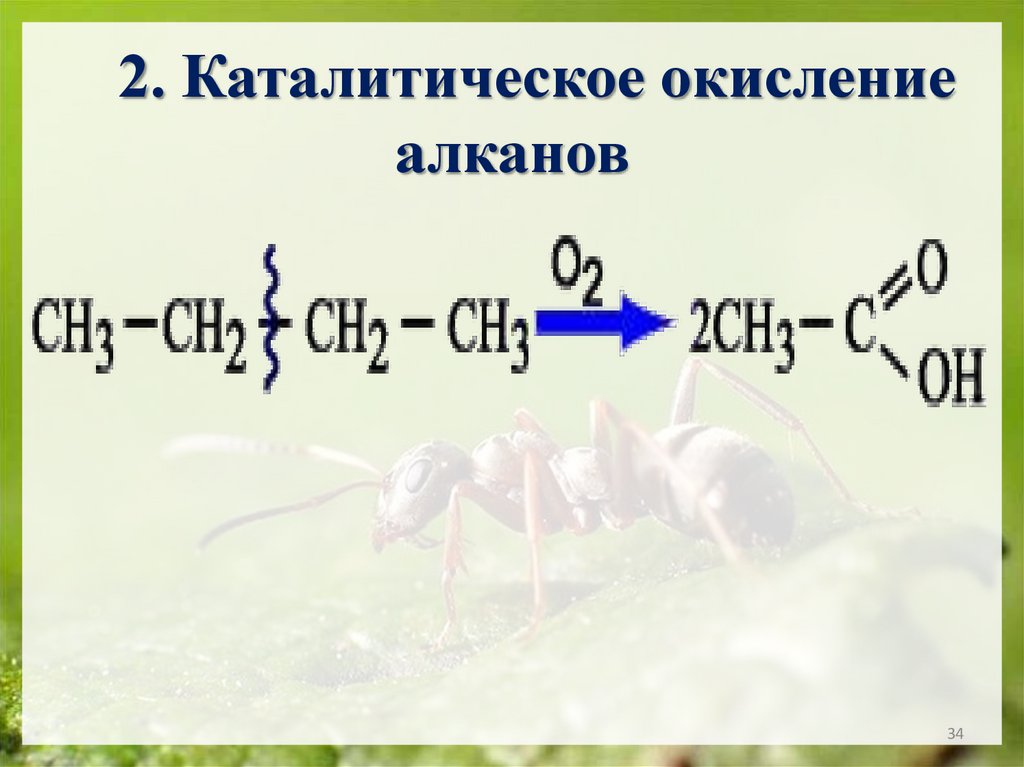
34.
2. Каталитическое окислениеалканов
34
35.
Получение уксусной кислоты35
36.
3637.
Молочная кислота (2-гидроксипропионовая)Образуется из содержащегося в свежем молоке
молочного сахара (лактозы) под действием бактерий.
Молочная кислота накапливается в мышцах при
недостатке кислорода: человек ощущает общую
слабость и тяжесть в мышцах.
В пищевой промышленности используется как
консервант, пищевая добавка Е270
37
38.
Лимонная кислота(2-гидрокси- 1,3,5 – пропантрикарбоновая кислота)
Важный продукт обмена веществ в живых
организмах.
Используется в фармацевтической промышленности как
компонент многих лекарственных средств т.к. является
антикоагулянтом.
38
39.
Муравьиная (метановая) кислотаВызывает ожоги!
В медицине применяется в виде 1,25%
спиртового раствора в качестве
раздражающего наружного средства (при
ревматических болях). Этот препарат
называют муравьиным спиртом. Это сильный
яд, его нельзя принимать внутрь.
Используется при крашении тканей и бумаги.
39
40.
Уксусная (этановая) кислотаБезводная уксусная кислота – кристаллическое вещество, такая
кислота называется «ледяной». Водный раствор (70-80 %-й)
кислоты называется уксусной эссенцией, а 6-9 %-й водный
раствор – столовым уксусом.
Используется для синтеза лекарственных веществ (аспирина).
40
41.
Валериановая (пентановая) иизовалериановая кислоты
Настойка валерианы используется при
сердечнососудистых заболеваниях.
Изовалериановая кислота
применяется в фармации для
синтеза лекарств (бромизовала,
валидола).
41
42.
Соли пальмитиновой и стеариновой кислот42
43.
Спасибо за внимание43



























 Химия
Химия