Похожие презентации:
Тромбогеморрагические синдромы
1.
Тромбогеморрагическиесиндромы
Кафедра фундаментальной
медицины,
проф. С.Н.Шилов
2.
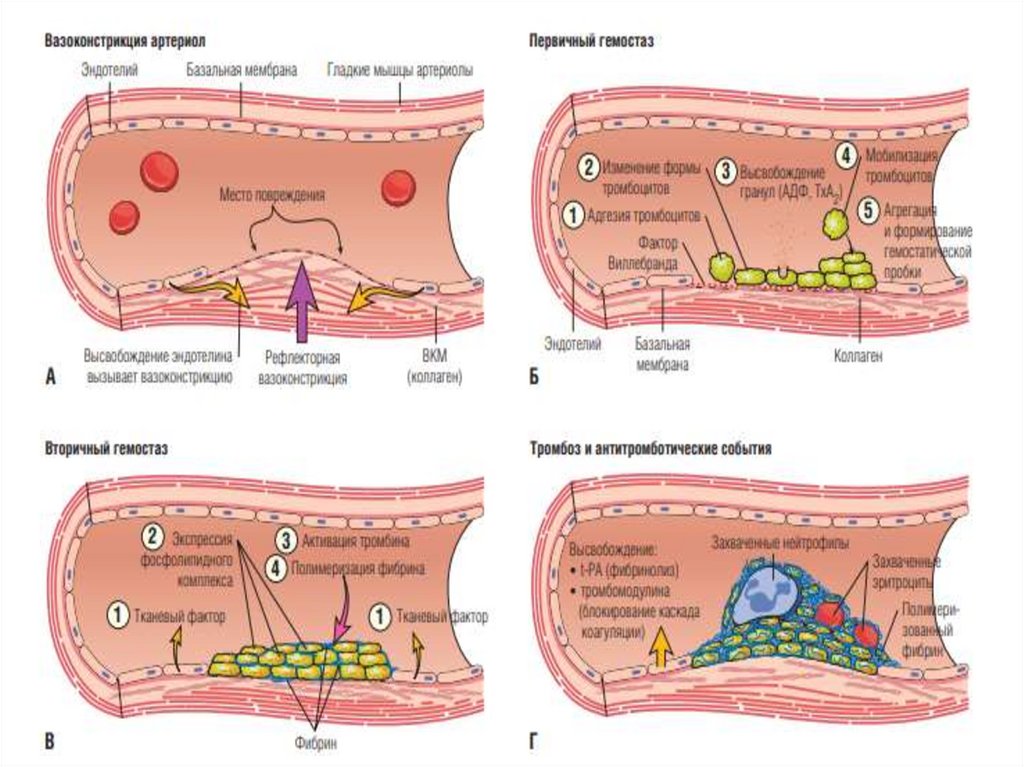
Механизмы гемостаза• Механизмы, обеспечивающие гемостаз, реализуются не только при
повреждении всей стенки сосудов, но и при любом повреждении
интимы сосудистой стенки, вызванном физическими (например,
катетеризация), гемодинамическими, химическими факторами,
воспалением, действием иммунных комплексов, нарушением
метаболизма (атеросклероз, коллагенозы) и т. д.
• Гемостаз происходит в основном благодаря образованию
пристеночного, или закупоривающего (интрамурального), тромба в
результате взаимодействия компонентов плазмы, тромбоцитов
и сосудистой стенки (рис.).
• Различают два механизма гемостаза:
— тромбоцитарно-сосудистый (первичный);
— коагуляционный (вторичный).
• Преобладание того или иного механизма в основном зависит от
калибра поврежденного сосуда и скорости кровотока.
• Эффективный гемостаз возможен только при нормальном
функционировании обоих механизмов.
• Функциональная неполноценность системы гемостаза может
привести к локальной или генерализованной кровоточивости из
сосудов (независимо от степени наполнения их кровью).
3.
4.
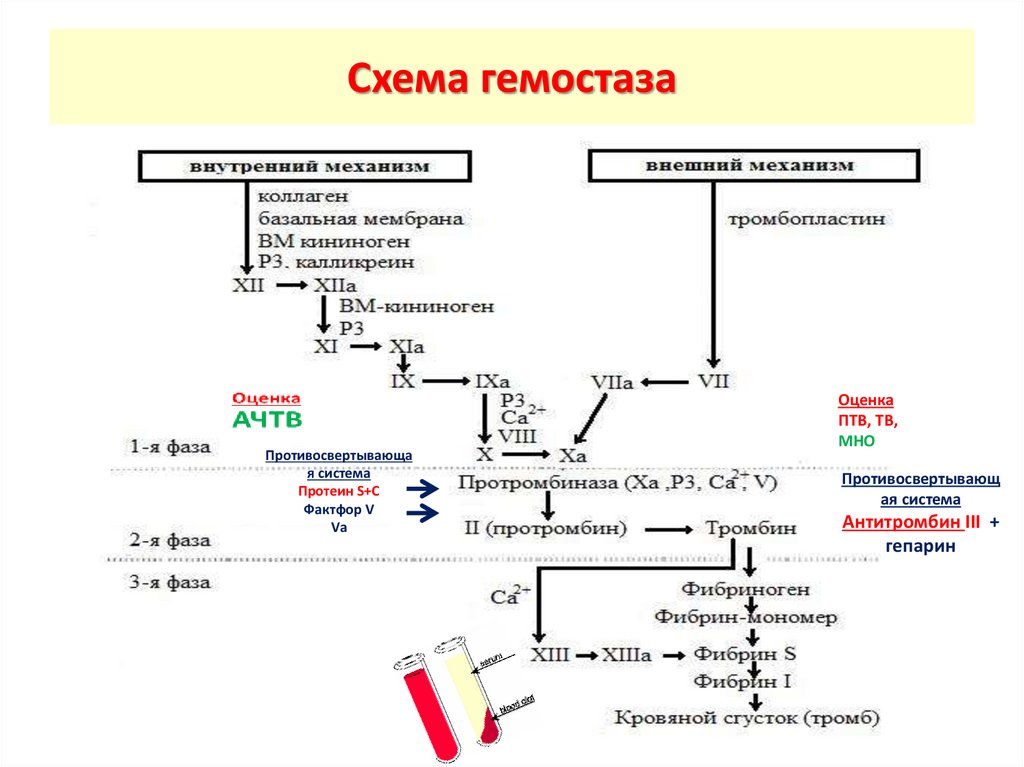
Схема гемостазаПротивосвертывающа
я система
Протеин S+С
Фактфор V
Vа
Оценка
ПТВ, ТВ,
МНО
Противосвертывающ
ая система
Антитромбин III +
гепарин
5.
Расстройства гемостаза• Возникают в результате нарушений метаболизма, структуры, функций
и механизмов регуляции трех взаимосвязанных систем:
— сосудистой (чаще всего при повреждении интимы сосудов);
— клеток крови (главным образом патологии тромбоцитов);
— плазмы крови (факторы свертывающей, антисвертывающей и
фибринолитической систем).
Патология системы гемостаза связана с тремя видами расстройств:
— повреждением эндотелиальной клетки флогогенами и дисрегуляцией ее
противосвертывающих, антиадгезивных и антиагрегационных механизмов,
которые в физиологических условиях сбалансированы
— нарушениями периферического кровообращения и, в частности,
микроциркуляции;
— в системе коагуляции крови и равновесия в состоянии ее свертывающей и
антисвертывающей систем.
6.
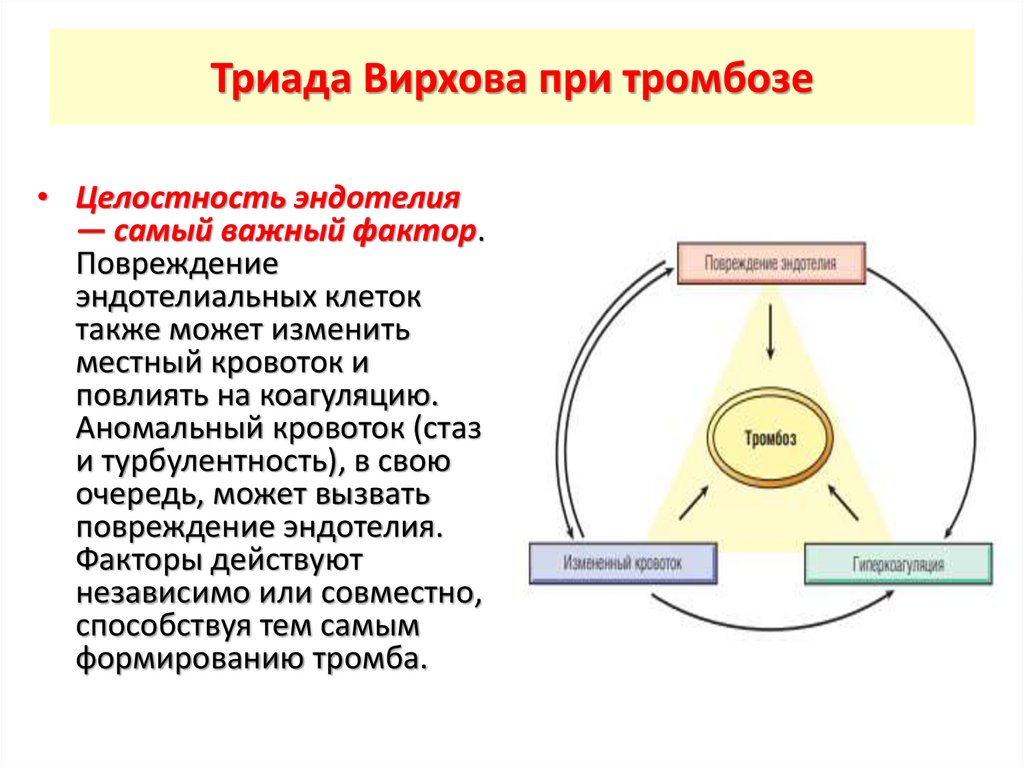
Триада Вирхова при тромбозе• Целостность эндотелия
— самый важный фактор.
Повреждение
эндотелиальных клеток
также может изменить
местный кровоток и
повлиять на коагуляцию.
Аномальный кровоток (стаз
и турбулентность), в свою
очередь, может вызвать
повреждение эндотелия.
Факторы действуют
независимо или совместно,
способствуя тем самым
формированию тромба.
7.
Нарушения в стенках микрососудов• Эндотелий принимает активное участие в регуляции тонуса
сосудов, вырабатывая различные вазоконстрикторы и
вазодилататоры. На эндотелий воздействуют также
вазоактивные вещества, которые продуцируются
тромбоцитами, лейкоцитами, тучными клетками или
активируются в плазме крови.
• Образование вазоактивных веществ в эндотелии регулируется
преимущественно двумя основными механизмами: действием
биологически активных веществ и напряжением сдвига.
• Эндотелийзависимая вазодилатация связана с синтезом трех
веществ — оксида азота, эндотелиального
гиперполяризующего фактора и простациклина, еще - оксид
азота, натрийуретический пептид С, адреномедуллин,
анандамид, АТФ, кинины.
• Эндотелийзависимая вазоконстрикция может быть связана с
синтезом в эндотелии эндотелина1, 20НЕТЕ
(20гидроксиэйкозатетраеновая кислота) и ангиотензина.
8.
• Адгезия тромбоцитов к эндотелию это начальный этап гемостаза итромбоза.
• Вторым фактором, влияющим на образование вазоактивных
веществ, является напряжение сдвига. Значительное изменение
этого показания происходит преимущественно в артериальных
сосудах при изменении скорости кровотока. Увеличение напряжения
сдвига приводит к усилению образования в эндотелии всех основных
вазодила таторов.
• Взаимодействие лейкоцитов с эндотелием происходит посредством
специальных адгезивных молекул, имеющихся как на
эндотелиоцитах, так и на лейкоцитах (вспоминаем!). Выделяют три
класса таких молекул: селектины, молекулы семейства
иммуноглобулинов и интегрины.
• Ряд селектинов (Е, Р) индуцируются цитокинами, при их участии
происходит «роллинг» — частичная задержка лейкоцитов на
поверхности эндотелия (прокатывание лейкоцитов вдоль эндотелия).
• Стимуляция эндотелия или его повреждения приводят к
дополнительной экспрессии молекул адгезии (катгерины, Р-селектин,
гликопротеин (GP) что завершает остановку лейкоцитов или их
плотную адгезию.
• Процесс адгезии завершатся миграцией лейкоцитов за пределы
сосудов. Данная стадия происходит в результате активации
интегринов — эндотелиальных молекул адгезии.
9.
Нарушение микроциркуляции и синдромсладжа
• Нарушения в стенках микрососудов наиболее часто
проявляются повышением проницаемости сосудистой
стенки, которое может вызвать прилипание (адгезию) к ее
поверхности форменных элементов крови, опухолевых клеток,
инородных частиц.
• Внутрисосудистые нарушения разнообразны и наиболее часто
связаны с агрегацией эритроцитов, тромбоцитов и других
форменных элементов крови, что приводит к нарушениям
реологических свойств крови. Крайней степенью агрегации
форменных элементов является синдром сладжа. В кровотоке
при сладже наступает разделение крови на клетки и плазму.
• Кратковременный стаз, как правило, явление обратимое.
Длительный стаз сопровождается распадом тромбоцитов
с последующим выпадением фибрина и образованием
тромба.
10.
Нарушение микроциркуляции и синдромсладжа (2)
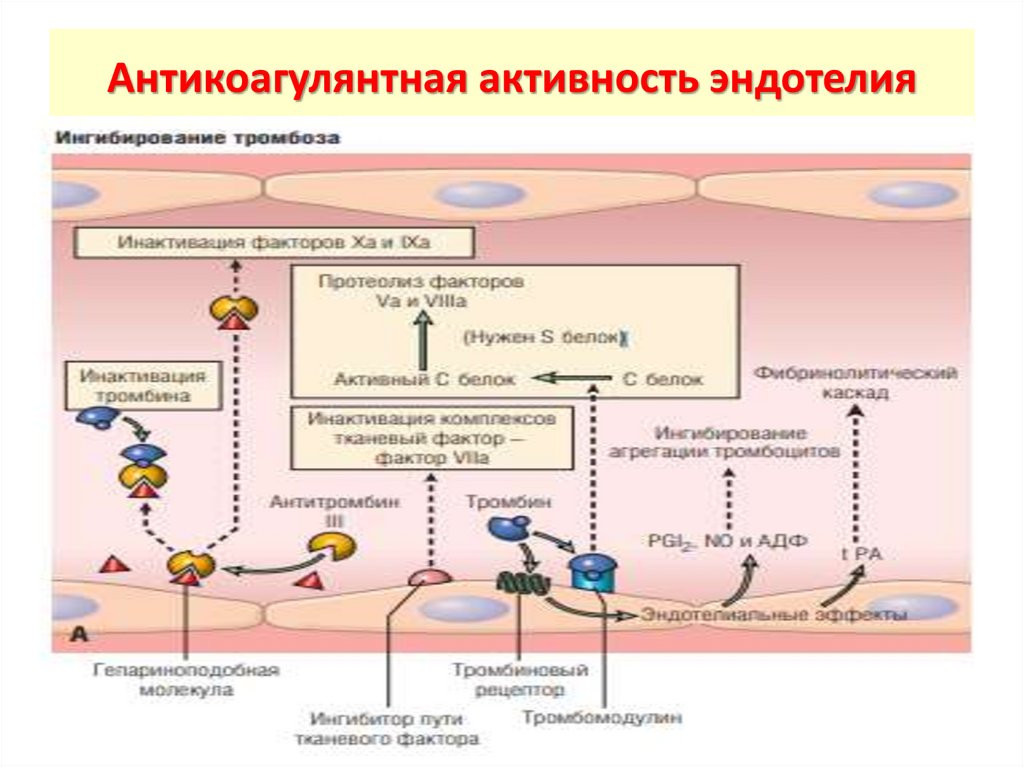
• эндотелиальная клетка экспрессирует и
высвобождает антикоагулянты и коагулянты.
• К антикоагулянтам относят: 1) простациклин,
который тормозит агрегацию тромбоцитов; 2)
гепариноподобные молекулы; 3) антитромбин,
который связывает тромбин; 4) тромбомодулин,
активирующий белок С, и др.
• Группу коагулянтов составляют: 1) тканевый фактор
свертывания; 2) фактор Виллебранда, участвующий в
адгезии тромбоцитов; 3) тромбоспондин, который
облегчает адгезию тромбоцитов
субэндотелиальными клетками сосудистой стенки.
11.
• В связи с закупоркой терминальных артериол капиллярыначинают пропускать только плазму.
• Процесс усугубляется местным ацидозом, действием
местных метаболитов и БАВ (серотонин, гистамин, гепарин),
поступающих в кровь в результате массовой дегрануляции
базофилов окружающей соединительной ткани.
• Повышение проницаемости сосудистой стенки и выход
жидкости усиливают сгущение крови и повышают ее вязкость,
что создает условия для образования множественных
гемокоагуляционных микротромбов с прогрессированием
микроциркуляторных расстройств.
• На заключительном этапе сладж характеризуется
выраженными нарушениями метаболизма и функций тканей и
органов, недостаточным обеспечением тканей кислородом,
пластическим и энергетическим материалом. В связи с этим
сладж называют капиллярнотрофической недостаточностью.
• Феномен сладжа, возникающий как местная реакция на
повреждение, в дальнейшем может приобрести характер
системной реакции организма.
12.
• Кратко вспомним сосудисто-тромбоцитарный гемостазВ норме количество тромбоцитов колеблется от 150 до 400 × 10х9/л, чаще — от 180
до 350 × 10х9/л. Нормальная продолжительность жизни тромбоцита составляет 6—12
сут.
• 15—25 % тромбоцитов ежесуточно поглощается эндотелием сосудов, что
обеспечивает ангиотрофическую и эндотелиоподдерживающую функции
тромбоцитов.
• Тромбоциты способствуют реэндотелизации в месте повреждения с участием
секреции факторов роста. В связи с чем тромбоциты справедливо называют
«физиологическими кормильцами эндотелия».
• В образовании тромбоцитарного тромба (в артериях) выделяют следующие
стадии:
— активация тромбоцитов и адгезия их к сосудистой стенке;
— агрегация тромбоцитов;
— реакция высвобождения ФАВ;
— тромбоцитарного тромба.
Уплотнение тромбоцитарного тромба. Во время агрегации активируется
сократительный белок тромбоцитов — тромбостенин, который изменяет форму
тромбоцитов и обеспечивает их максимальное приближение друг к другу в агрегатах,
становящихся плотными и малопроницаемыми для компонентов крови.
• Таким образом, ведущую роль в механизмах гемостаза играют тромбоциты.
Выделение ими тромбопластина способствует активации внешнего пути
свертывания крови
13.
Коагуляционный гемостаз• При повреждении более крупных сосудов (артерий и вен)
гемостаз осуществляется не только при участии тромбоцитов,
но и благодаря свертыванию крови и образованию
коагуляционного тромба.
• Необходимое условие для возникновения коагуляционного
тромба — это взаимодействие не только плазменных и
тромбоцитарных, но и тканевых факторов.
• Фосфолипиды тромбоцитарных мембран (ф. III тромбоцитов) —
место, где происходит фиксация прокоагулянтов и их активация.
• Свертывание крови — сложный аутокаталитический процесс,
при котором происходит последовательная активация
неактивных плазменных факторов и образование сериновых
протеаз.
• Напомню, выделяют три последовательные стадии
коагуляционного гемостаза:
• 1) образование активной протромбиназы;
• 2) образование тромбина;
• 3) образование фибрина.
14.
Стадии образования фибринаСтадии
Механизм
Первая Происходит протеолиз фибриногена тромбином (пептиды А и В
отщепляются от аминокислотного участка α- и β-цепей) и
образуется фибрин-мономер
Вторая Характеризуется полимеризацией фибрина-мономера и
образованием растворимого фибринаполимера,
чувствительного к плазмину
Третья Возникает стабилизация растворимого фибрина под влиянием ф.
ХIII и образование нерастворимого фибрина, устойчивого к
плазмину. Ф. ХIII (фибринстабилизирующий фактор)
синтезируется в печени и находится в плазме, тромбоцитах,
эритроцитах и сосудистой стенке.
15.
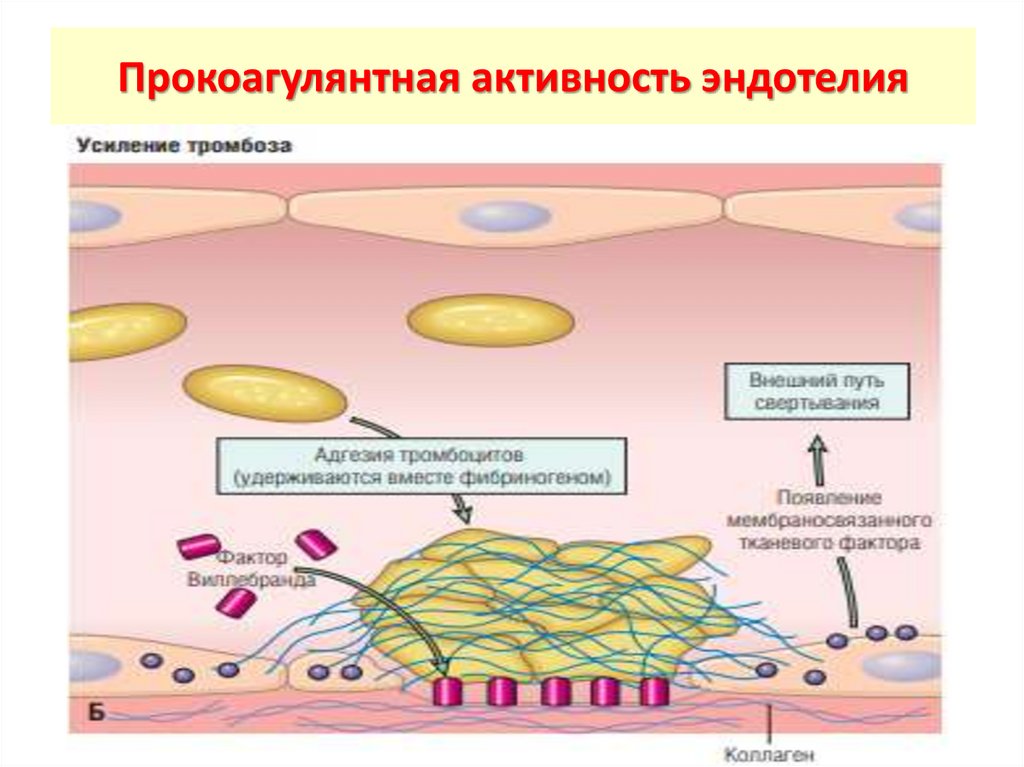
Прокоагулянтная активность эндотелия16.
Антикоагулянтная система крови• Первичные естественные антикоагулянты постоянно образуются
в организме и поступают в кровь, где взаимодействуют с активной
формой прокоагулянтов и ингибируют их.
• К первичным антикоагулянтам относят антитромбин III, гепарин,
кофактор II гепарина, протеин С, протеин S, тромбомодулин, α2 макроглобулин и еще:
• Протеин C (ПрC) — витамин К-зависимый белок, образующийся в
печени. Антикоагулянтные свойства проявляет только активная форма
протеина С (А-ПрC). Естественным активатором ПрC служит тромбин.
В организме активация ПрC осуществляется на поверхности мембран
эндотелиоцитов.
• Протеин S (ПрS) — гликопротеин, образуется в печени и эндотелии,
содержится в гранулах тромбоцитов. ПрS значительно усиливает
антикоагулянтное действие А-ПрC.
• Помимо антикоагулянтной активности, А-ПрC и ПрS обладают
профибринолитическим действием.
• Таким образом, активированная тромбином система ПрC—ПрS, с
одной стороны, ингибирует гемокоагуляцию, а с другой — повышает
фибринолитическую активность крови. Активацию этой системы
рассматривают как первичный антикоагуляционный механизм
17.
Вторичные естественные антикоагулянты• Эти антикоагулянты образуются в процессе
свертывания крови и фибринолиза.
• К ним относят:
— антитромбин — фибрин, сорбирует тромбин и ф.
Xa, превращает их в неактивные формы;
— антитромбин IV — продукт расщепления
протромбина тромбином, нарушает активацию
протромбина протромбиназой;
— антитромбин VI — продукты деградации
фибрина (ПДФ), нарушают полимеризацию фибринмономера, ингибируют агрегацию тромбоцитов, ф. Ха,
тромбин.
18.
Антикоагулянтная активность эндотелия19.
Фибринолитическая система крови• В системе ферментативного фибринолиза центральное место занимает
процесс активации плазминогена с образованием активного плазмина .
Вещества, вызывающие эту реакцию, называют активаторами плазминогена.
• Выделяют два типа тканевых активаторов плазминогена (ТАП) — тканевой
(ТАП 1) и урокиназный (ТАП 2).
• Наибольшее количество активатора образуется в матке, щитовидной железе,
надпочечниках, легких, предстательной железе.
• ТАП 1 синтезируется в моноцитах, гистиофагах и выделяется в кровь в
небольшом количестве.
• В эпителиальных клетках почечных канальцев образуется урокиназа (ТАП 2),
вызывающая активацию циркулирующего плазминогена и определяющая 15
% внешней фибринолитической активности (против 85 %, отмечаемой у ТАП 1).
• Самостоятельной фибринолитической активностью обладают протеазы
лейкоцитов.
• При стрессе, физической нагрузке, введении некоторых фармакологических
препаратов (например, АДГ, катехоламины, препараты, содержащие
никотиновую кислоту) активность активатора плазминогена в циркулирующей
крови быстро возрастает.
• Мощные стимуляторы выделения ТАП 1 — вазоактивные вещества, особенно
адреналин и гистамин.
20.
Фибринолитическая система крови (2)• Протеазы, высвобождающиеся из гранул
активированных лейкоцитов, особенно нейтрофилов,
протеазы микроорганизмов и грибов (стрептокиназа),
протеазы поджелудочной железы (трипсин,
химотрипсин) обладают самостоятельной
фибринолитической активностью.
• Активация фибринолиза происходит также под
действием ФНО-α, ИЛ-1 и др.
• Существует комплемент-опосредованный фибринолиз
(при активации фрагмента С8, приводящей к
превращению плазминогена в плазмин).
• При патологических процессах возможна первичная и
вторичная активация фибринолиза.
21.
Ингибиторы фибринолиза• Фибринолитическая активность крови зависит не только от
содержания плазминогена и его активаторов, но и от ингибиторов
фибринолиза.
• Ингибиторы фибринолиза делят на антиактиваторы и
антиплазмины. Антиактиваторы бывают первого (1) и второго (2)
типов.
• Ингибиторы активатора плазминогена типа 1 синтезируются
эндотелиоцитами, гепатоцитами и связывают ТАП. Их образование
повышено у больных инфарктом миокарда, при воспалительных
процессах.
• Ингибитор активатора плазминогена типа 2, образующийся в
эндотелиоцитах, моноцитах и гистиофагах (в том числе плаценты),
угнетает урокиназную активность. Большое количество ингибитора
активатора плазминогена типа 2 образуется в клетках
злокачественных опухолей.
• Антиактиваторы тормозят активацию плазминогена, оказывая
преимущественно местное действие.
• Определенное значение придают ингибитору фибринолиза,
активируемому тромбином (TAFI — англ. thrombin activator fibrinolys
inhibitor). Он представлен белком, после активации тромбином,
приобретающим антифибринолитическую активность.
22.
Ингибиторы фибринолиза (2)• Антиплазмины инактивируют плазмин и находятся в плазме в
избытке. К ним относят α2 -макроглобулин, α1 -антитрипсин, комплекс АТ
III—гепарин и др. Наибольшее значение как физиологический ингибитор
плазмина имеет антиплазмин — α2 -гликопротеид, образующийся в
печени.
• Кроме фибринолиза, связанного с действием плазмина, выделяют
гепаринзависимый фибринолиз.
• Гепаринзависимый фибринолиз развивается после образования
комплексов, содержащих в своем составе АТ III—гепарин, тромбин,
плазминоген, плазмин, фибриноген, катехоламины, серотонин, ф. ХIII,
тироксин.
• Эти комплексы обладают литическим действием на нестабильный фибрин,
препятствуют полимеризации фибрина-мономера и стабилизации его ф.
ХIII.
• Считают, что ε-аминокапроновая кислота тормозит именно
гепаринзависимый фибринолиз.
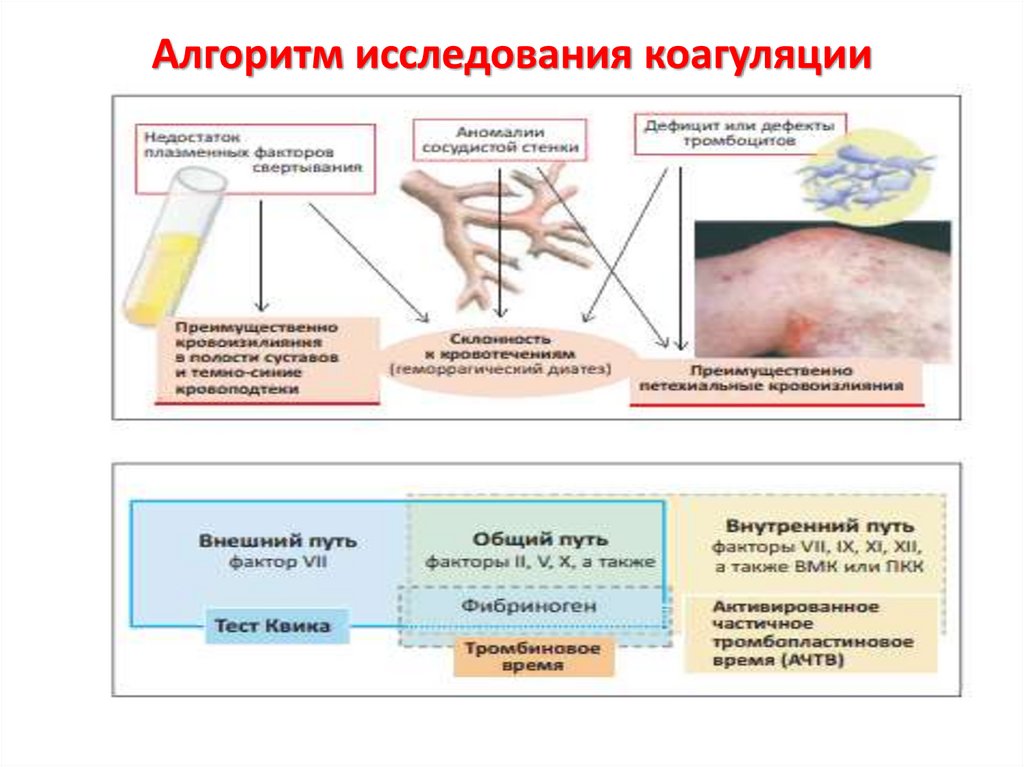
23.
Алгоритм исследования коагуляции24.
• Протромбин (по Квику) определяется в процентномсоотношении при сравнении образца крови пациента со
стандартной плазмой (определяется в %, 70-120).
Факторы протромбинового комплекса синтезируются в
печени.
• Для большей сопоставимости результатов разных
лабораторий определяется показатель
международного нормализованного отношения
(МНО, N 0,85-1,35).
• Исследование времени Квика – это способ
исследования факторов свертывания внешней системы в
присутствии избыточного тканевого тромбопластина.
Нормальное значение 13-15 сек.
• Удлинение времени Квика говорит о наличии
недостатка того или иного фактора внешней
системы или угнетающего фактора
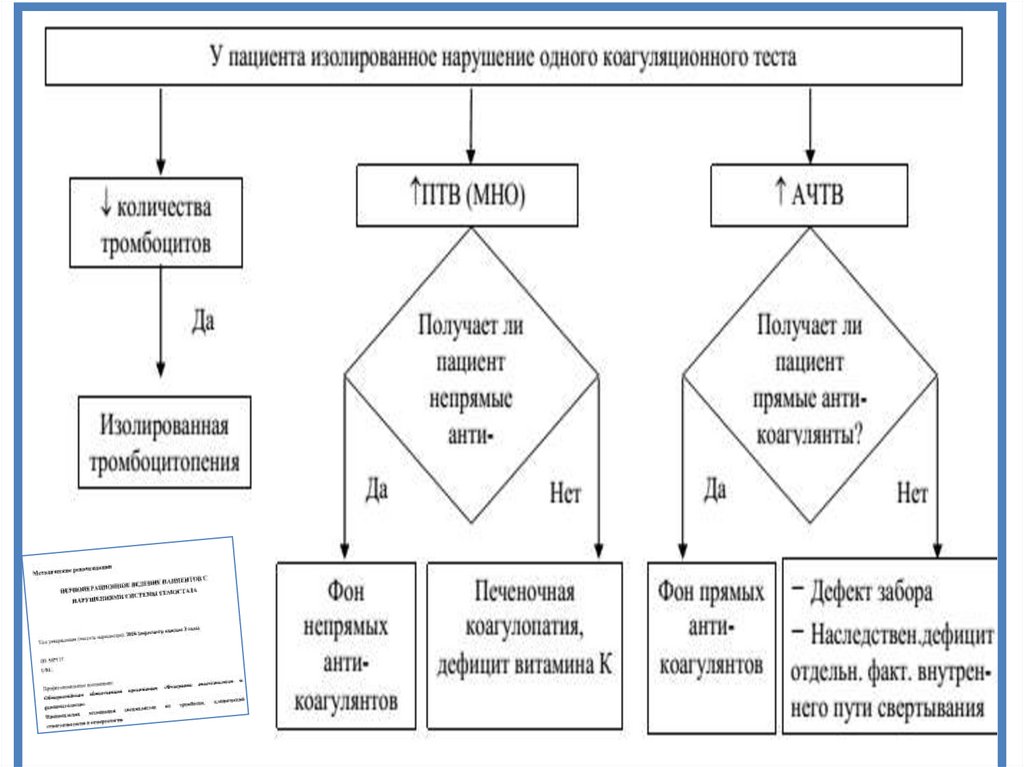
25.
Алгоритм исследования коагуляции26.
Тромбофилия и ее механизмы• Тромбофилия — состояние, характеризующееся
предрасположенностью
к
развитию
тромбообразования (тромбозу).
• Для развития тромбофилии имеют значение:
- повреждения сосудистых стенок, особенно
их интимы (повышение тромбогенной активности и
снижение тромборезистентности сосудов),
- тромбоцитарные
(повышение
функциональной активности тромбоцитов и
тромбоцитозы) и
- плазменные (увеличение содержания активных
коагулянтов
в
крови,
приводящее
к
гиперкоагуляции)
механизмы,
уменьшение
антикоагулянтной активности крови и угнетение
фибринолиза.
27.
Изменения тромбогенной и тромборезистентнойактивности сосудистой стенки
• В физиологических условиях образование и выделение тромбогенных (ФАТ,
тромбоксан А2 и др.) в сосудистой стенке ограничено, а при ее повреждении
или активации эндотелия БАВ значительно увеличивается.
• В механизме повышения тромбогенности сосудов большое значение имеет
интрамуральный тромбоз, развивающийся при микроповреждениях
интимы.
• При этом из тромбоцитов высвобождаются различные факторы, в том числе
и фактор роста (ф. IV), вызывающий пролиферацию гладкомышечных клеток
и фибробластов, миграцию их в интиму, усиление секреции коллагена и
других компонентов соединительной ткани, обладающих тромбогенными
свойствами.
• Этот механизм повреждения сосудистой стенки наиболее выражен при
сахарном диабете и атеросклерозе.
• Эндотелиальные клетки служат одновременно продуцентами и
эффекторами ИЛ-1, ИЛ-6, ИЛ-8, ФНО-α, увеличение их синтеза отмечают при
сепсиcе, опухолях, воспалении, что является неспецифическим ответом на
повреждение эндотелия →возникают тромбозы.
28.
Изменения тромбогенной и тромборезистентнойактивности сосудистой стенки (2)
• Сейчас широко обсуждают значение синдрома антифосфолипидных
антител (АТ) в патогенезе тромбозов и гиперкоагуляции.
• Впервые эти АТ обнаружили у больных системной красной волчанкой,
у которых были отмечены тромбозы не только вен, но и артерий.
• Антифосфолипидные АТ имеют определенное значение в патогенезе
ишемической болезни сердца (ИБС).
• В механизме повреждения эндотелия сосудов большое значение
придают ↓ образования NO и увеличению выделения
эндотелиоцитами вазоконстрикторов, а также ↓ ангиопротективной
роли ЛПВП из-за уменьшения их синтеза в печени.
• В патогенезе повреждения сосудистой стенки большое значение
также придают гипергомоцистеинемии, ее часто (в 10—15 % случаев)
выявляют в европейской популяции.
• Происходит инициация оксидативного стресса с последующим
повреждением эндотелия, а также стимуляция пролиферации
гладкомышечных клеток сосудов, что способствует развитию
атеросклероза.
29.
Повышение функциональной активноститромбоцитов и тромбоцитозы.
Повышенная склонность тромбоцитов к адгезии и агрегации характерна для
атеросклероза, сахарного диабета, ГБ и других заболеваний.
Усиление агрегации тромбоцитов может быть первичным, связанным, например, с
чрезмерным образованием тромбоксана А2 (при СД1, позднем гестозе беременных,
злокачественных опухолях и др.).
Гипергликемия и гиперлипидемия особенно за счет ЛПНП и ЛПОНП способствуют
повышению агрегационной активности тромбоцитов и их чувствительности к
индукторам агрегации.
Увеличение содержания в крови адреналина, β-липопротеинов, свободных
жирных кислот, фактора фон Виллебранда сопровождается значительным ↑
агрегационной активности тромбоцитов.
↓ простациклина как основного антиагрегантного вещества также характеризуется
гиперагрегацией тромбоцитов.
Тромбоцитозы, особенно при количестве тромбоцитов > 600 × 109/л, обычно
вызывают тромбофилию (при некоторых миелопролиферативных заболеваниях
например, болезнь Вакеза, миелофиброз), после спленэктомии, при дефиците
железа и т. д.
30.
Гиперкоагуляция и ее механизмы• В некоторых случаях, например после острой
кровопотери, повышение свертываемости крови бывает
компенсаторной реакцией организма. Однако
длительная и выраженная гиперкоагуляция создает
условия для активации тромбообразования
(тромбофилии).
• Гиперкоагуляцию и тромбофилию обнаруживают при
многих заболеваниях и патологических процессах.
• К их развитию могут привести следующие механизмы:
- Увеличение содержания прокоагулянтов в крови;
- Снижение антикоагулянтной активности крови;
- Угнетение фибринолиза.
31.
Гипокоагуляция и ее механизмы• Гипокоагуляция, очень часто сопровождающаяся
кровоточивостью, — важнейший симптом и
осложнение многих заболеваний.
• Наиболее частыми причинами нарушений гемостаза,
обусловленных развитием гипокоагуляции, бывают:
- тромбоцитопении,
- тромбоцитопатии,
- дефицит плазменных прокоагулянтов,
- повышение антикоагулянтной активности крови,
- гиперфибринолиз ,
(остановимся лишь на некоторых механизмах, остальные материал 3 курса)
32.
Виды тромбоцитопатийВиды
Механизмы развития
Первичные
Обусловлены генетическими нарушениями рецепторного аппарата тромбоцитов
или дефицитом определенных пулов тромбоцитов. В этих случаях снижается
интенсивность адгезии и агрегации тромбоцитов.
Тромбоцитопатии, связанные с дефицитом тромбоцитарных факторов (чаще 3 и 4),
проявляются нарушением реакции высвобождения и снижением их адгезивной и
агрегационной активности. При этом даже на фоне нормального количества
тромбоцитов возможно нарушение тромбоцитарно-сосудистого гемостаза, что
проявляется значительным удлинением времени кровотечения, особенно из
сосудов микроциркуляторного русла
Вторичные
Возникают при применении НСПВ (например, салицилаты, ибупрофен),
антидепрессантов (ингибиторов МАО), сердечных гликозидов, адреноблокаторов,
антибиотиков (например, хлорамфеникол, карбенициллин, большие дозы
препаратов пенициллинового ряда), тиазидных диуретиков, антигистаминных
средств. Механизм действия этих лекарственных средств сводится к ↓
образования и истощению пулов хранения некоторых тромбоцитарных
факторов.
Быстрое истощение этих пулов хранения происходит в тромбоцитах
консервированной крови уже в течение первых суток после ее приготовления.
33.
Болезнь Виллебранда• Это , возникающее у лиц с дефицитом ф. W и наследуемое по
аутосомно-доминантному, реже аутосомно-рецессивному
типу. Частота колеблется от 1:10 до 1:20 тыс. Латентное
течение болезни Виллебранда отмечают у 1 % населения.
• Описано несколько типов болезни Виллебранда:
— I и III типы обусловлены количественным дефицитом
неизмененного ф. W;
— IIa и IIb типы связаны с синтезом аномальных молекул ф. W.
• Клинически заболевание характеризуется возникновением
кровотечения сразу после повреждения, кровоточивостью
из сосудов микроциркуляторного русла, появлением
петехиальных кровоизлияний, везикул с геморрагическим
содержимым в ротовой полости, у женщин —
гиперполименореей.
34.
Гиперфибринолиз• Первичный гиперфибринолиз происходит при
массивном поступлении в кровоток ТАП и резком
уменьшении образования антиплазминов.
• Увеличение образования ТАП → в случаях
прогрессирования опухолевого процесса и тяжелой
печеночной недостаточности. В период обильной
менструальной
кровопотери,
при
обширных
механических и термических травмах,
• Способностью активировать фибринолиз обладают и
ферменты бактериального происхождения.
• Уменьшение образования антиплазминов и повышение
фибринолитической активности нередко обнаруживают
у больных с поражениями печени, для них характерна
выраженная склонность к кровоточивости.
• Это же явление отмечают при генетическом дефекте
образования α2 -антиплазмина (болезнь Миасато).
35.
Гиперфибринолиз (2)• Вторичный гиперфибринолиз возникает в
ответ на увеличение образования фибрина и
развивается на фоне ДВС-синдрома. Нарушение
гемостаза при гиперфибринолизе объясняют
растворением фибрина и невозможностью
образования коагуляционного тромба.
• Продукты деградации фибрина (ПДФ) оказывают
ингибирующее влияние на агрегацию тромбоцитов и
на все стадии свертывания крови.
• Увеличение ПДФ характерно как для первичного, так и
для вторичного гиперфибринолиза.
• Геморрагические заболевания и синдромы обычно
сопровождаются следующими видами (типами)
кровоточивости (табл. ниже)
36.
ТипХарактеристика
Капиллярный
Характеризуется петехиальными высыпаниями и синяками,
локализованными чаще на коже и слизистых оболочках, сочетается с
носовыми и маточными кровотечениями. Возможны кровоизлияния во
внутренние органы, среди них наиболее тяжелыми бывают
кровоизлияния в головной мозг. Такой тип кровоточивости характерен
для тромбоцитопении (болезнь Верльгофа), тромбоцитопатии
(тромбастении Гланцмана, болезнь фон Виллебранда), недостаточности
факторов протромбинового комплекса (V, VII, X, II) и др.
Гематомный
Характеризуется болезненными кровоизлияниями в ткани (подкожную
клетчатку, мышцы, суставы, брюшную полость, желудок, почки и др.).
Возникает при гемофилиях, особенно гемофилии А и В, дефиците
фактора III тромбоцитов, появлении ингибиторов факторов VIII, IX и др.
Капиллярногематомный
Происходит развитие повторных, строго локализованных кровотечений (в
частности, в местах телеангиэктазий, ангиом). Возникает при болезнях
Рандю — Ослера, Шенлейна — Геноха и др.
Васкулитнопурпурный
Характеризуется геморрагическими высыпаниями. Возникает при
воспалительных, инфекционных, токсических и иммунных заболеваниях
37.
Синдром ДВС крови• Это типовой патологический процесс, характеризующийся
генерализованной активацией системы гемостаза и
фибринолиза, при котором происходит рассогласование систем
регуляции агрегантного состояния крови. ДВС – частный случай
тромботической микроангиопатии.
• ДВС-синдром — сложное и грозное осложнение следующих
заболеваний, патологических процессов и синдромов:
— шок любого генеза (в 90—100 % случаев);
— септические состояния (в 70 % случаев);
— бактериемия и вирусемия (в 30 % случаев);
— опухоли, в первую очередь лейкозы (в 100 % случаев при остром
промиелоцитарном лейкозе, в 60—75 % — при других
диссеминированных опухолях);
— обширные и глубокие термические ожоги;
— краш-синдром ;
38.
Синдром ДВС крови (2)— акушерская патология (преждевременная отслойка
плаценты, тяжелый поздний гестоз беременных, ручное
отделение плаценты, кесарево сечение, обильные
кровотечения);
— острый внутрисосудистый гемолиз и цитолиз
(геморрагические лихорадки, малярия, переливание
несовместимой крови, действие ядов змей и грибов);
— травматические операции на паренхиматозных органах
(печени, селезенке, предстательной железе, легком),
сопровождающиеся выраженными кровопотерями;
— эндопротезирование сосудов, операции на клапанном
аппарате сердца;
— использование аппарата искусственного кровообращения;
— трансплантация органов и тканей.
Смертность при развитии острого ДВС-синдрома составляет
30—50 %. По течению выделяют острый и хронический ДВСсиндром
39.
Классификация ДВС-синдрома1. «Явный» ДВС-синдром,
геморрагическая
(фибринолитическая) форма
2. «Неявный» ДВС-синдром,
тромботическая форма.
.
40.
ГШ ≠ ДВС41.
ПАТОГЕНЕЗ ДВС-СИНДРОМАПути реализации
Внешний механизм
активации коагуляции
Внутренний механизм
активации коагуляции
Характеристика патогенеза
Осуществляется при массивном поступлении в кровь ф. III у больных с обширными
ожогами, распадом опухолей, эмболией околоплодными водами,
преждевременной отслойкой плаценты, синдроме мертвого плода.
При выраженном повреждении эндотелия отмечают инициацию
внутрисосудистой агрегации тромбоцитов (контакт с коллагеном и
другими активаторами агрегации), что происходит, например, при
гиперменингококцемии.
В процессе агрегации и гибели тромбоциты выделяют большое
количество ф. III, что поддерживает гемокоагуляцию по внешнему пути.
Повреждение эндотелия бывает вызвано иммунными комплексами,
активирующими каскад системы комплемента.
Компоненты системы комплемента С3а и (особенно) С5а усиливают
образование свободных кислородных радикалов путем активирования
нейтрофилов и выделения ИЛ-1, ФНО-α из моноцитов.
Активированные
нейтрофилы
выделяют
серинэластазу,
непосредственно повреждающую эндотелий.
Наиболее демонстративны эти повреждения при сепсисе.
Повреждение эндотелия возможно также за счет «осмотического
удара», отмечаемого при гипергликемиях.
42.
Стадии острого ДВС-синдрома(вспомним их коротко)
• Первая стадия — гиперкоагуляция — продолжается в среднем 15—20 мин.
При стремительном течении ДВС-синдрома она может резко сокращаться. Выраженное
генерализованное внутрисосудистое свертывание крови сопровождается усиленным
потреблением не только факторов свертывания, но также антикоагулянтов и
тромбоцитов (в процессе их необратимой агрегации). Гиперкоагуляция характеризуется
тем, что кровь сворачивается в игле.
В клинической картине ведущие симптомы — похолодание конечностей, резкая
бледность кожных покровов, одышка с инспираторным компонентом,
приводящая к развитию тяжелой гипоксии тканей и метаболического ацидоза.
• Вторая стадия — коагулопатия потребления — протекает в виде двух
подстадий.
Подстадия 2а характеризуется истощением факторов свертывания крови
вследствие их усиленного потребления без избыточной активации фибринолиза. В
условиях кислородного голодания нарастает выделение из сосудистой стенки
тканевого тромбопластина, происходит дальнейшая активация свертывания
крови, вновь потребляются прокоагулянты и усиливается кровоточивость.
Подстадия 2б характеризуется прогрессирующей активацией фибринолиза в
сочетании с нарастающей гипокоагуляцией.
Клинически эта стадия характеризуется появлением кровоточивости в
зонах повреждения (например, в операционной ране, в полости матки, в
месте инъекций).
43.
Стадии острого ДВС-синдрома (2)Третья стадия — гипокоагуляция — характеризуется истощением всех факторов
свертывания и антикоагулянтов, выраженной гипофибриногенемией, тромбоцитопенией, а
также
патологическим
усилением
фибринолитической
активности
(вторичный
гиперфибринолиз). Одновременно идет и фибринолиз, и фибриногенолиз, что приводит к
росту в десятки и сотни раз содержания ПДФ в крови.
Активация калликреин-кининовой системы плазмы, вызванная наличием активированных
форм ф. XIIa, приводит к↑ проницаемости сосудистой стенки и снижению ее тонуса.
Накопление активированных протеаз, в том числе поздних компонентов системы комплемента
С5–С9, вызывает повреждение мембран эритроцитов и появление в периферическом
кровотоке полигональных плотных эритроцитов и шизоцитов (фрагментированные,
разорванные эритроциты).
Клинически данная стадия характеризуется прогрессирующими кровотечениями в зонах
повреждения и ранее интактных тканях (например, слизистых оболочек глаз,
желудочно-кишечного тракта, мочеполовой системы, дыхательных путей).
Четвертая стадия — стадия исходов. Стадия остаточных проявлений блокады сосудов
микротромбами.
ДВС-синдром может стать одной из причин развития полиорганной несостоятельности,
характеризующейся развитием острой почечной недостаточности, гемолитико-уремического
синдрома (синдрома Гассера), респираторного дистресссиндрома, острой надпочечниковой
недостаточности (синдром Уотерхауса — Фридериксена).
44.
Хронический ДВС-синдром (неявный)• Часто встречают у больных на различных стадиях опухолевого процесса,
с хроническим сепсисом, на начальном этапе почечной
недостаточности (в том числе в условиях камнеобразования), при
пневмониях, замедлении кровотока в системе воротной вены, гриппе и
других ОРВИ.
• ХДВС-синдром характеризуется длительной локальной
гиперкоагуляцией и флеботромбозами в венах нижних конечностей,
реже в венах малого таза и верхних конечностей (синдром Труссо).
• ХДВС-синдром чаще развивается у больных со злокачественными
опухолями легкого, яичников, карциномой молочной железы,
карциномой простаты, диссеминированной нейробластомой,
метастатической аденокарциномой желудка, карциномой толстой
кишки.
• Процесс метастазирования плотных опухолей в 75 % случаев
сопровождается мигрирующими флеботромбозами.
• Для
клинициста
появление
признаков
персистирующего
флеботромбоза на фоне нормального соматического статуса и
состоятельности венозного русла всегда должно служить
основанием для дополнительного обследования больного и
исключения онкологической патологии
45.
Стадии хронического ДВС-синдромаСтадии
Патогенез
ГемолитикоОбнаруживают при вирусной, бактериальной инфекции у детей и родивших их
уремический
женщин. Образующиеся микротромбы, состоящие в основном из тромбоцитов,
синдром
закупоривают микрососуды почек и инициируют развитие острой
(синдром
преренальной почечной недостаточности и острой надпочечниковой
Гассера)
недостаточности. Смертность больных составляет свыше 70 %
Тромботическая Фактически повторяет картину гемолитико-уремического синдрома: лихорадка,
тромбоцитопени геморрагический синдром, острая почечная недостаточность,
ческая пурпура микроангиопатическая гемолитическая анемия.
(болезнь
Внутрисосудистое свертывание крови происходит во всех органах
Мошковича)
Болезнь
Шенлейна —
Геноха
Развитие ДВС-синдрома обусловлено формированием генерализованного
микротромбоваскулита, в основе которого лежит повреждение микрососудов
циркулирующими иммунными комплексами и активированными
компонентами системы комплемента. Мембраноатакующий комплекс
приводит к осмотическому лизису клеток, в том числе и эндотелиальных, что
активирует внутренний путь свертывания крови и тромбоцитарно-сосудистый
гемостаз. Маркером эндотелиального повреждения служит рост содержания
ф. W, это используют в клинической практике
46.
Хронический ДВС-синдром (2)• Микроангиопатии или макроангиопатии у больных
сахарным диабетом — условие развития ХДВС-синдрома.
Этому способствует гиперкоагуляция в сочетании с
гипофибринолизом и высокой реактивностью тромбоцитов.
• В патогенезе ХДВС-синдрома имеет значение длительное
локализованное внутрисосудистое свертывание крови в
различных органах, как правило поврежденных
воспалительным процессом.
• Это особенно характерно для гломерулонефрита, острых
пневмоний, некоторых диффузных повреждений паренхимы
печени, метроэндометритов, аднекситов.
• Сосуды микроциркуляторного русла этих органов постепенно
заполняются микротромбами, что способствует истощению
коагуляционного потенциала и активации фибринолиза с
развитием в дальнейшем гипокоагуляции.
• Отмечена возможность развития ДВС-синдрома при
циркуляции в кровотоке значительного количества
стрептококков, способных поступать в системный кровоток из
микрососудов.
47.
ДВСКлиника + лабораторные показатели
Показатели свертывания крови:
«Прикроватный тест» - (2 мл. венозной крови в
пробирку, закрыть, взять в руки чтобы согреть, через 4 мин.
наклонить и смотреть образовался ли сгусток, наклоняют
каждую мин. и смотрят., образование сгустка > 7 мин. →
подозрение на коагулопатию ),
Гемостазиограмма. Скрининг.
ПТВ (МНО), АЧТВ, фибриноген, количества
тромбоцитов, ТЭГ
48.
• АЧТВ - скрининг врождённых или приобретённыхкоагулопатий. Оценка внутреннего пути
свертывания. Мониторинг гепаринотерапии
(нефракционированный гепарин)
• Протромбиновое время (ПВ) и его производные: ПТИ,
международное нормализованное отношение (МНО).
Оценка внешнего пути свертывания, общего
гемостаза, терапии варфарином, синтез печеночных
факторов свертывания.
• Фибриноген — важнейший белок гемостаза, его
продукты деградации - ПДФ, Д-димер характерны для
тромботических состояний.
• Тромбоэластография (ТЭГ, ROTEM) — метод оценки
системы гемостаза, который позволяет измерить
формирование фибринового сгустка в цельной крови.
49.
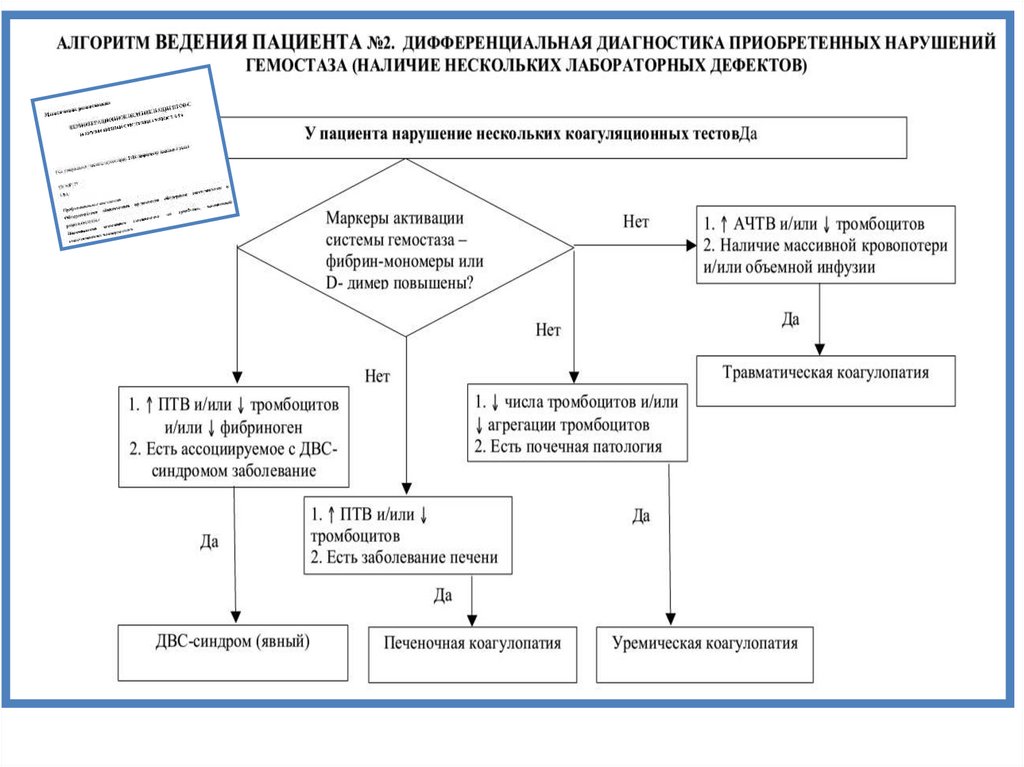
ДВС1.Обнаружение не менее двух нарушений в
скрининговых гемостазиологических тестах.
2.Повышение уровня маркеров
тромбообразования: ПДФ, D-димер.
3.Наиболее достоверные критерии наличия
ДВС-синдрома – удлинение ПТВ (МНО) и/или
снижение количества тромбоцитов.
50.
51.
52.
Три основных критерия:1. Клиника критического состояния,
2. Кровотечение и/или полиорганная недостаточность
3. Лабораторные показатели
53.
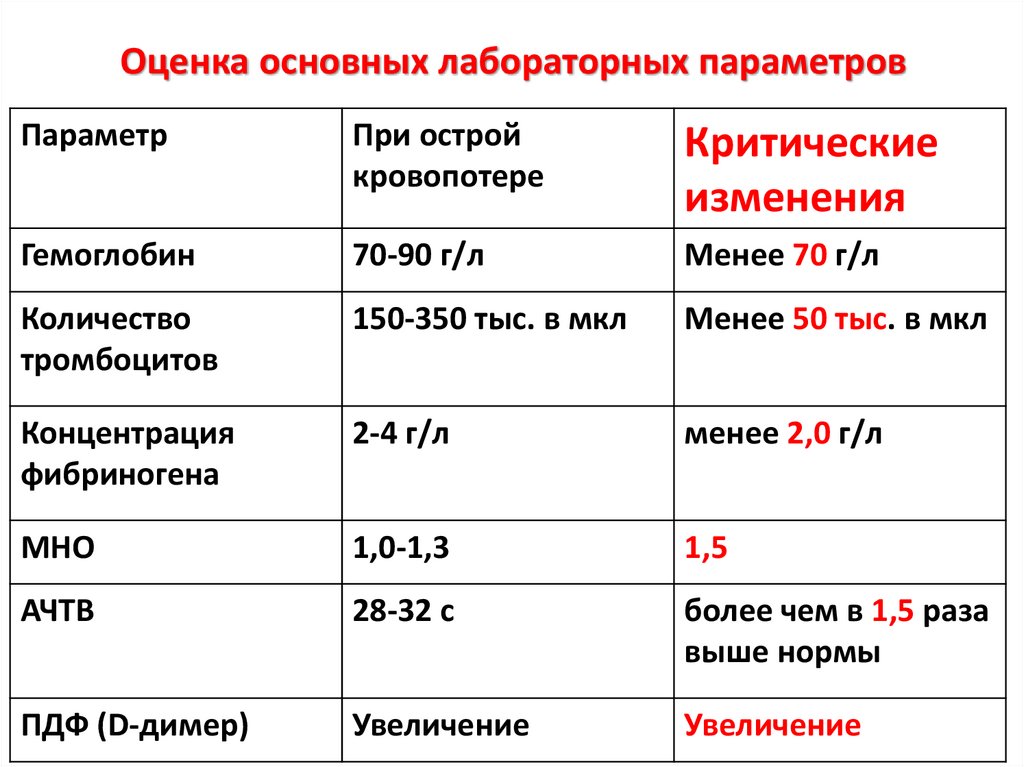
Оценка основных лабораторных параметровПараметр
При острой
кровопотере
Критические
изменения
Гемоглобин
70-90 г/л
Менее 70 г/л
Количество
тромбоцитов
150-350 тыс. в мкл
Менее 50 тыс. в мкл
Концентрация
фибриногена
2-4 г/л
менее 2,0 г/л
МНО
1,0-1,3
1,5
АЧТВ
28-32 с
более чем в 1,5 раза
выше нормы
ПДФ (D-димер)
Увеличение
Увеличение
54.
Принципы терапии форм геморрагическихсиндромов
• Лечение гемофилии сложное и недостаточно эффективное. Оно предполагает
переливание нативной, антигемофильной плазмы, тромбоцитарной массы и цельной свежей
крови, введение препаратов, содержащих антигемофильный глобулин, а также витаминов (С,
РР, В12), и проведение плазмафереза и гемодиализа.
• Лечение гипопротромбинемии обычно этиотропное, включает использование
витамина K. Лечение дефицита ф. V (акселератора-глобулина) в крови проводят, как правило,
во время кровотечений.
Оно состоит в переливаниях больному свежей крови или плазмы. Основу лечения
гипопротромбинемии составляет переливание свежей крови, введение тромбина.
Применение витамина K малоэффективно.
Лечение гипофибринемии включает переливание крови, сухой плазмы, фибриногена,
введение препаратов кальция, витаминов (аскорбиновой кислоты и др.).
При первичном гипофибринолизе используют антифибринолитические препараты типа
антипротеаз (апротинин, аминокапроновая кислота и др.), а также препараты
аминометилбензойной кислоты.
• Лечение тромбоцитопений (хронической тромбоцитопенической пурпуры, болезни
Верльгофа) включает переливание нативной плазмы, гемотрансфузии, осторожно проводимую
терапию аминокапроновой кислотой, глюкокортикоидами, андрогенами, витаминами В12 и В6
, синтетическими противозачаточными средствами, а также спленэктомию.
55.
Принципы терапии формгеморрагических синдромов (2)
• Лечение тромбастении →использование средств, повышающих адгезивно-
агрегационную активность тромбоцитов (препараты Сa2+, АДФ, адреналина,
серотонина, тромбина, фибриногена и другие, а также применение
противоинфекционных и антитоксических средств).
Лечение тромбоцитопатий → переливание свежей тромбоцитарной массы,
введение глюкокортикоидов и других иммунодепрессантов (например, азатиоприн
и др.), противомикробных и детоксицирующих средств, антигемофильного
глобулина, фактора фон Виллебранда, препаратов АТФ; проведении
симптоматической терапии аминокапроновой кислотой.
Спленэктомия возможна, но не всегда показана. Викасол и соли кальция не
назначают.
В лечении геморрагического васкулита (болезни Шенлейна — Геноха) →
отмена препаратов, вызвавших заболевание. Проводят неспецифическую
десенсибилизирующую терапию. Назначают рутозид, препараты кальция,
серотонина, адреналина. Показаны ацетилсалициловая кислота, другие
дезагреганты, гепарин, плазмаферез.
Лечение тромбофилического синдрома направлено на устранение или
ослабление основного заболевания, вызвавшего развитие этого состояния.
Показаны антикоагулянты прямого и непрямого действия,
фибринолитические средства, плазмозамещающие растворы.
56.
Лечение ДВС-синдрома• Крайне сложное и не всегда эффективное.
• Часто отмечают остаточные явления нарушения как гемостаза, так и
других видов гомеостаза.
• Лечение
больных
с
ДВС-синдромом
осуществляют
в
реанимационном отделении. Этиотропная терапия ДВС-синдрома
направлена на уменьшение или ликвидацию причинного фактора
(бактериемии, септицемии, гемолиза и др.).
• Патогенетическое лечение назначают с учетом фазы и тяжести
развития ДВС-синдрома.
• При
развитии
гиперкоагуляции
используют
экстренную
гепаринотерапию (гепарин обладает свойствами антикоагулянта и
фибринолитика), затем — противошоковые средства (натрия хлорид,
солевые растворы, декстран [мол. масса 30—40 кДА], нативная
плазма,
минералои/или
глюкокортикоиды)
вместе
с
антиагрегантами
(α-адреноблокаторами),
дезагрегантами
(ацетилсалициловой кислотой, дипиридамолом, пентоксифиллином
и др.), а также гемодиализ и обязательно (в целях быстрого
восстановления ОЦК и метаболических процессов) — массивное
переливание свежей совместимой крови.
57.
Лечение ДВС-синдрома (2)• При развитии гипокоагуляции показаны ингибиторы
плазменных протеаз, инфузионная терапия
свежезамороженной плазмы, плазмаферез,
гемосорбция (с целью уменьшения иммунных комплексов,
продуктов деградации фибрина, токсических веществ).
• При геморрагическом синдроме, обычно
сочетающемся с тромобоцитопенией, внутривенно
вводят тромбоцитарную массу.
• Во все фазы ДВС-синдрома назначаются мероприятия и
средства, восстанавливающие газовый состав и КОС
крови, внешнее дыхание, кровообращение, особенно
деятельность сердца (путем использования
искусственной вентиляции, кислородотерапии,
дыхательных аналептиков, сердечнососудистых,
адаптогенных и других средств).
58.
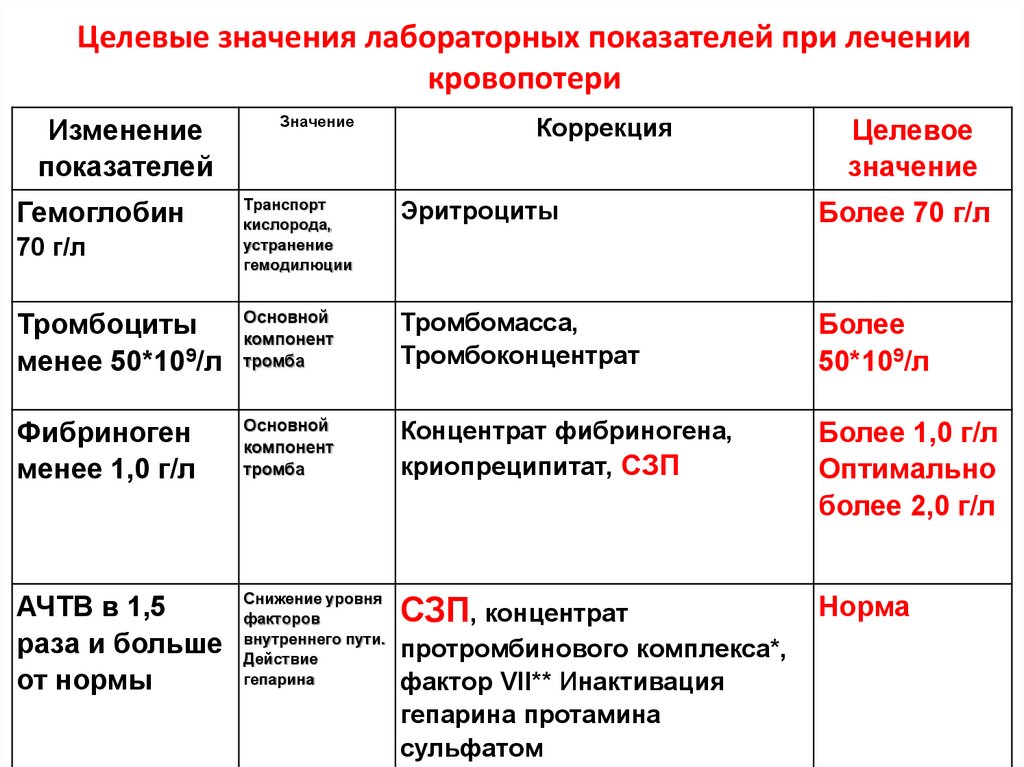
Целевые значения лабораторных показателей при лечениикровопотери
Изменение
показателей
Значение
Коррекция
Целевое
значение
Транспорт
кислорода,
устранение
гемодилюции
Эритроциты
Более 70 г/л
Тромбоциты
менее 50*109/л
Основной
компонент
тромба
Тромбомасса,
Тромбоконцентрат
Более
50*109/л
Фибриноген
менее 1,0 г/л
Основной
компонент
тромба
Концентрат фибриногена,
криопреципитат, СЗП
Более 1,0 г/л
Оптимально
более 2,0 г/л
АЧТВ в 1,5
раза и больше
от нормы
Снижение уровня
факторов
внутреннего пути.
Действие
гепарина
СЗП, концентрат
Норма
Гемоглобин
70 г/л
протромбинового комплекса*,
фактор VII** Инактивация
гепарина протамина
сульфатом
59.
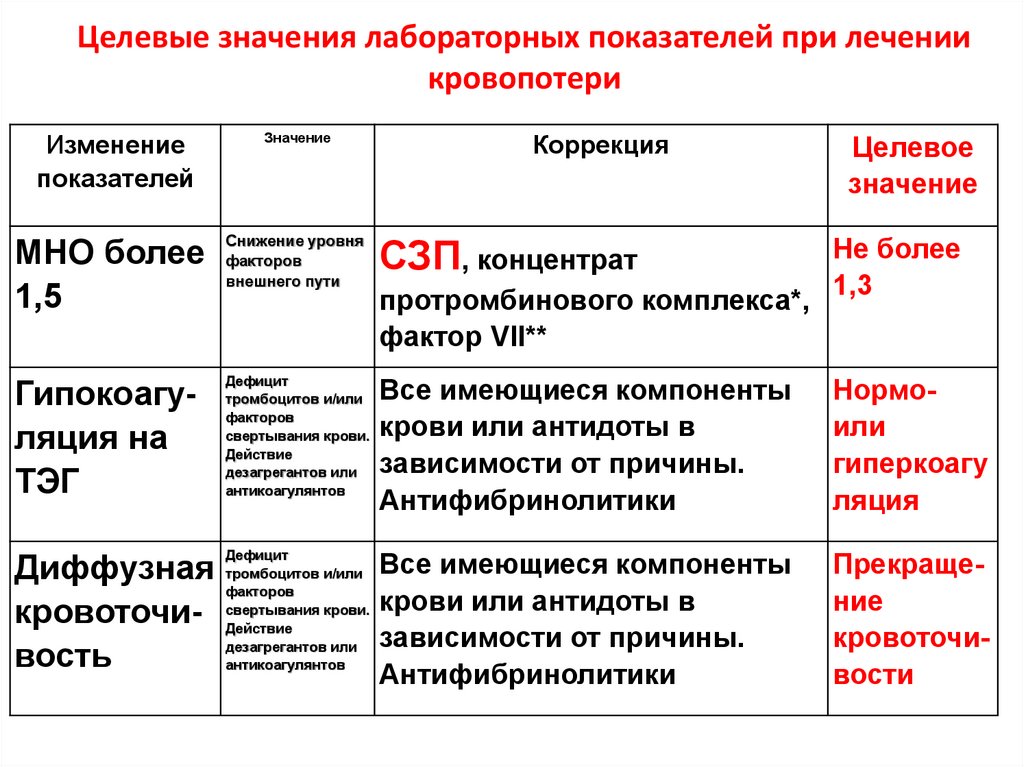
Целевые значения лабораторных показателей при лечениикровопотери
Изменение
показателей
Значение
Снижение уровня
МНО более факторов
внешнего пути
1,5
Дефицит
тромбоцитов и/или
факторов
свертывания крови.
Действие
дезагрегантов или
антикоагулянтов
Коррекция
СЗП, концентрат
протромбинового комплекса*,
фактор VII**
Целевое
значение
Не более
1,3
Все имеющиеся компоненты
крови или антидоты в
зависимости от причины.
Антифибринолитики
Нормоили
гиперкоагу
ляция
Диффузная тромбоцитов и/или Все имеющиеся компоненты
факторов
крови. крови или антидоты в
кровоточи- свертывания
Действие
зависимости от причины.
дезагрегантов или
вость
антикоагулянтов
Антифибринолитики
Прекращение
кровоточивости
Гипокоагуляция на
ТЭГ
Дефицит
60.
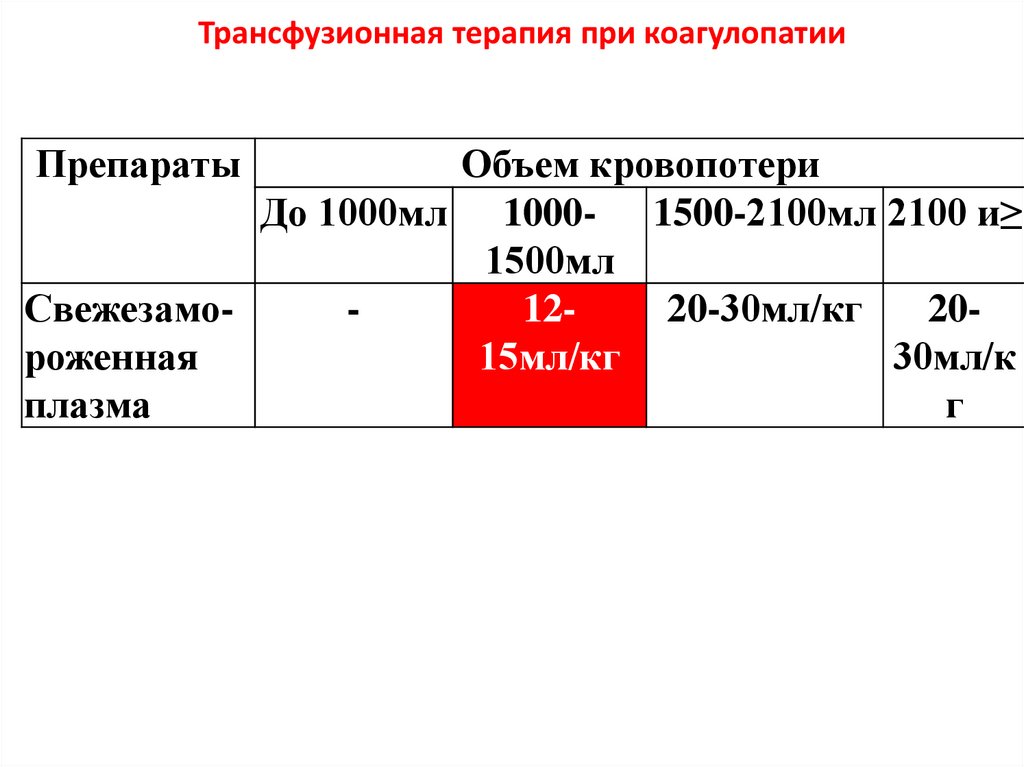
Трансфузионная терапия при коагулопатииПрепараты
Объем кровопотери
До 1000мл 1000- 1500-2100мл 2100 и≥
1500мл
Свежезамо1220-30мл/кг
20роженная
15мл/кг
30мл/к
плазма
г
61.
62.
Лабораторный контроль показателей входе инфузионной терапии:
• гемоглобин, гематокрит, уровень
эритроцитов и тромбоцитов;
• КЩС (pH, HCO3, SaO2, PaO2);
• Электролиты (калий, кальций, натрий,
хлор);
• уровень глюкозы;
• уровень фибриногена, АЧТВ, МНО.
63.
Критерии эффективности терапии прикровотечении
• Кровотечение остановлено за 3-4 часа
• Отсутствует геморрагический синдром
• Отсутствуют клинические и лабораторные
признаки коагулопатии;
• Сатурация более 70%;
• Восстанавливается сознание и адекватное
спонтанное дыхание.
• Восстановление сознания, прекращение ИВЛ
• Отсутствие признаков ОРДС и/или пневмонии.

















































 Медицина
Медицина








