Похожие презентации:
Омыляемые и неомыляемые липиды
1.
Омыляемые и неомыляемыелипиды
Общая и органическая химия
для специальности 31.05.01 Лечебное дело
Институт фундаментальных основ и
информационных технологий в медицине
Лектор - канд.хим.наук Задорожная А.Н.
2.
План лекции1. Триацилглицерины. Строение, химические свойства, биороль.
2. Сложные липиды: фосфолипиды, липопротеины, гликопротеины. Строение,
свойства, роль в метаболизме.
3. Насыщенные и полиненасыщенные жирные кислоты (НЖК, ПНЖК)компоненты липидов, простагландины. Структура, участие в обменных процессах
организма.
4. Классификация неомыляемых липидов.
5. Терпены: строение, применение их в качестве лекарственных препаратов.
6. Стерины, витамины группы «Д»: химические формулы, участие в процессах
жизнедеятельности.
7. Желчные кислоты: структура, биороль.
8. Стероидные гормоны: строение, участие в метаболизме.
3.
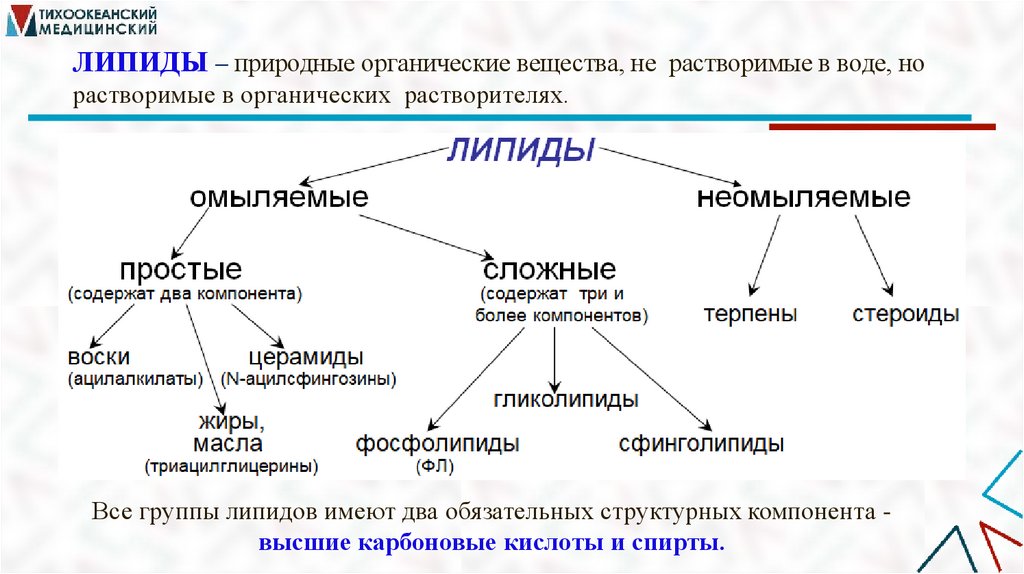
ЛИПИДЫ – природные органические вещества, не растворимые в воде, норастворимые в органических растворителях.
Все группы липидов имеют два обязательных структурных компонента высшие карбоновые кислоты и спирты.
4.
Участие липидов в процессах жизнедеятельности1. Структурная функция – 20% массы - печень 5%, жировая ткань 90%,
клетки мозга – 50%.
2. Энергетическая функция – 39 кДж или 9,3 ккал выделяется при
окислении 1г жира.
3. Запасные питательные вещества (подкожный жир в брюшной
полости).
4. Процессы терморегуляции (запас на зиму).
5. Предохраняют кожу от высыхания.
6. Предохраняют органы от сотрясения (почки).
7. Источники эндогенной воды.
8. Источники «ЖК», участвующих в построении клеточных мембран.
9. Суточная потребность в жирах – 60-80 г (30 г растительного масла).
5.
Жиры и масла – триацилглицерин(д)ы (ТАГ)Жиры и масла (триацилглицерины, триацилглицериды, триацилглицеролы) сложные эфиры глицерина (глицерола) и высших жирных кислот.
6.
Высшие жирные кислоты (ВЖК) –структурные компоненты ТАГ
Биологически важные жирные кислоты могут быть насыщенными и ненасыщенными.
Общие структурные признаки:
• являются монокарбоновыми;
• содержат неразветвленную углеродную цепь;
• включают четное число атомов углерода в цепи;
• имеют цис-конфигурацию двойных связей (если они присутствуют).
Ближайшая к карбоксильной группе двойная связь обычно расположена между
атомами С-9 и С-10. Если двойных связей несколько, то они отделены друг от
друга метиленовой группой СН2.
7.
Номенклатура ненасыщенных ВЖК1. У символа атома углерода числом обозначают общее число атомов С в молекуле
кислоты, через двоеточие число двойных связей.
2. Концевой атом углерода, независимо от длины цепи, обозначается буквой греческого
алфавита ω (омега). Отсчет положения двойных связей производится не от карбоксильной
группы, а от метильной группы.
олеиновая к-та С 18:1 ω-9
линолевая к-та С 18:2 ω-6
арахидоновая к-та С 20:4 ω-6
ВЖК в зависимости от расположения двойных связей составляют семейства:
• ω-3 (у 3-го атома углерода, семейство линоленовой к-ты);
• ω-6 ( у 6-го атома С , линолевой к-ты);
• ω-9 (у 6-го атома С , семейство олеиновой к-ты).
8.
Номенклатура ненасыщенных ВЖКДля нормальной жизнедеятельности человека большое значение имеет правильный баланс
липидов трех типов кислот: ω-3 (льняное масло, рыбий жир), ω-6 (подсолнечное, кукурузное
масла) и ω-9 (оливковое масло) в рационе питания.
Следует подчеркнуть роль полиненасыщенных линолевой и линоленовой кислот как
соединений, незаменимых для человека («витамин F»). В организме они не синтезируются и
должны поступать с пищей в количестве около 3-5 г в день. В природе эти кислоты
содержатся в основном в растительных маслах. Они способствуют нормализации липидного
профиля плазмы крови.
Из насыщенных кислот в липидах человеческого организма наиболее важны пальмитиновая
С 16:0 и стеариновая С 18:0 , а из ненасыщенных - олеиновая С 18:1, линолевая С
18:2, линоленовая С 18:3 и арахидоновая С 20:4
9.
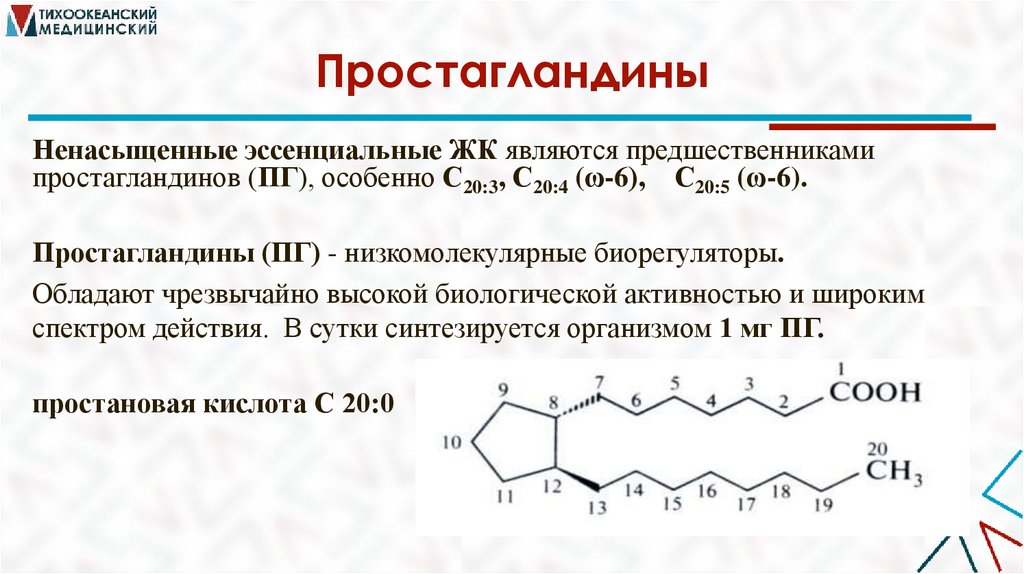
ПростагландиныНенасыщенные эссенциальные ЖК являются предшественниками
простагландинов (ПГ), особенно С20:3, С20:4 (ω-6), С20:5 (ω-6).
Простагландины (ПГ) - низкомолекулярные биорегуляторы.
Обладают чрезвычайно высокой биологической активностью и широким
спектром действия. В сутки синтезируется организмом 1 мг ПГ.
простановая кислота С 20:0
10.
БИОРОЛЬ ПРОСТАГЛАНДИНОВ1. Регулируют кровяное давление
2. Ингибируют свертывание крови и выделение желудочного сока
3. Стимулируют работу кишечника, легких, бронхов, синтез
гликогена
4. Влияют на процессы нервного возбуждения
5. Оптимизируют половой цикл у женщин
6. Вызывают болевые ощущения и повышение температуры.
11.
Свойства липидови их структурных компонентов
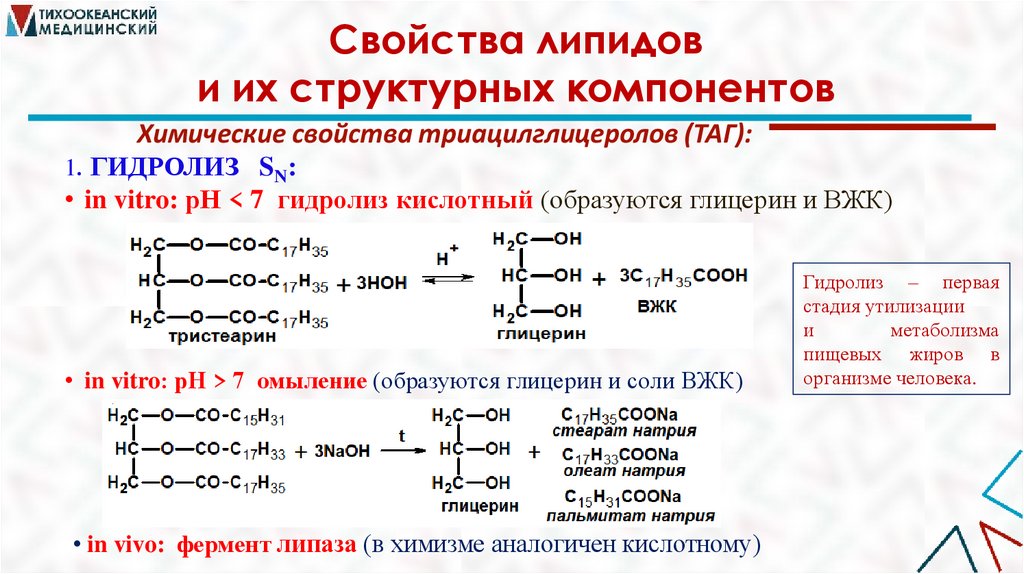
Химические свойства триацилглицеролов (ТАГ):
1. ГИДРОЛИЗ SN:
• in vitro: рН < 7 гидролиз кислотный (образуются глицерин и ВЖК)
• in vitro: рН > 7 омыление (образуются глицерин и соли ВЖК)
• in vivo: фермент липаза (в химизме аналогичен кислотному)
Гидролиз – первая
стадия утилизации
и
метаболизма
пищевых жиров в
организме человека.
12.
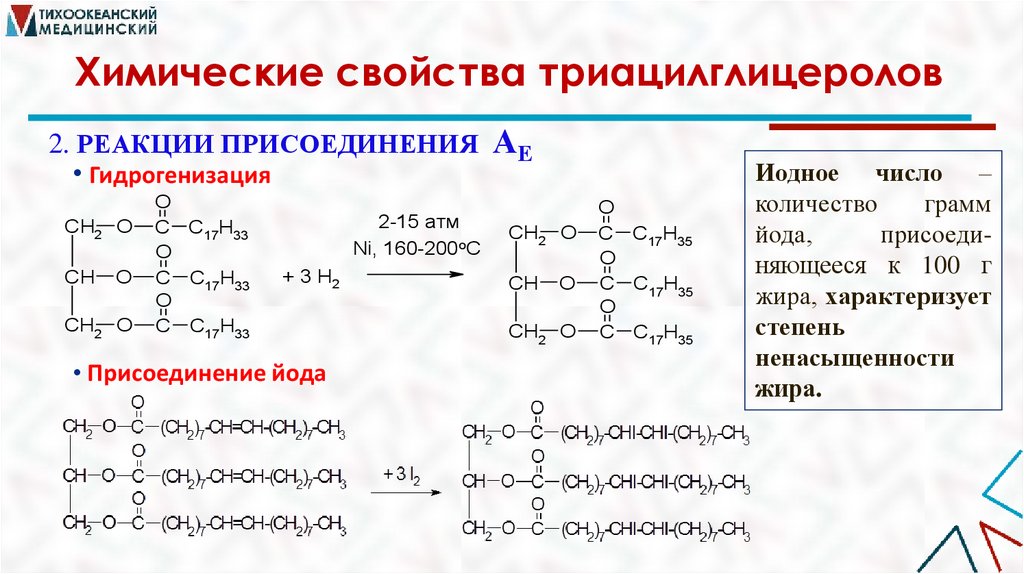
Химические свойства триацилглицеролов2. РЕАКЦИИ ПРИСОЕДИНЕНИЯ АЕ
• Гидрогенизация
CH2 O
CH
O
CH2 O
O
C C17H33
O
C C17H33
O
C C17H33
2-15 атм
Ni, 160-200oC
+ 3 H2
• Присоединение йода
CH2 O
CH
O
CH2 O
O
C C17H35
O
C C17H35
O
C C17H35
Иодное число –
количество
грамм
йода,
присоединяющееся к 100 г
жира, характеризует
степень
ненасыщенности
жира.
13.
Химические свойства триацилглицеролов(ТАГ) и ВЖК
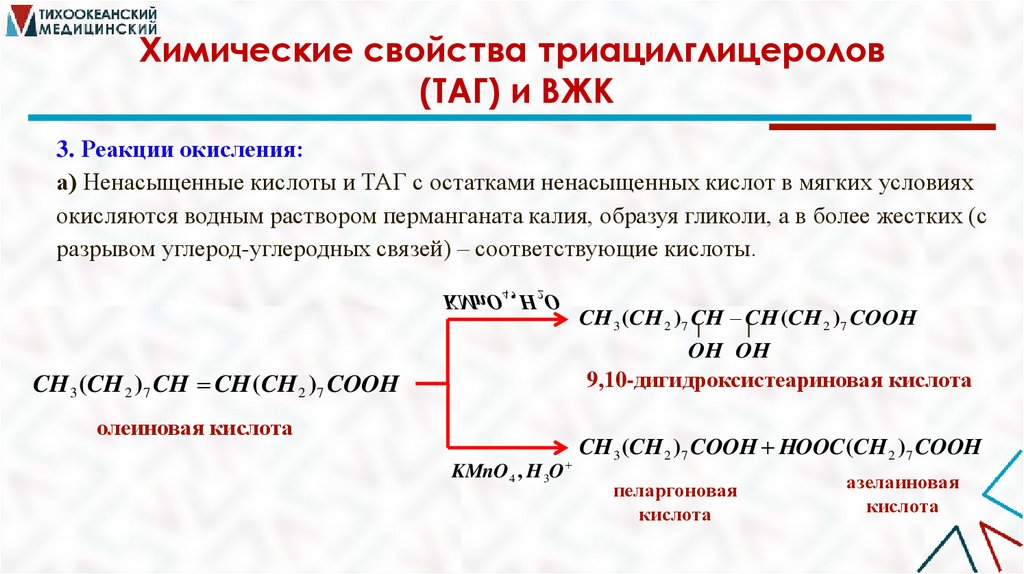
3. Реакции окисления:
а) Ненасыщенные кислоты и ТАГ с остатками ненасыщенных кислот в мягких условиях
окисляются водным раствором перманганата калия, образуя гликоли, а в более жестких (с
разрывом углерод-углеродных связей) – соответствующие кислоты.
KMnO4 , H 2O
CH 3 (CH 2 )7 CH CH (CH 2 )7 COOH
OH OH
9,10-дигидроксистеариновая кислота
CH 3 (CH 2 )7 CH CH (CH 2 )7 COOH
олеиновая кислота
KMnO 4 , H 3O
CH3 (CH 2 )7 COOH HOOC (CH 2 )7 COOH
пеларгоновая
кислота
азелаиновая
кислота
14.
Химические свойстватриацилглицеролов (ТАГ) и ВЖК
б) Окисление кислородом воздуха ненасыщенных ТАГ при
(автоокисление), сопровождаемое гидролизом, является частью
известного как прогоркание масла.
хранении
процесса,
Кислотное число – количество мг щелочи, способное нейтрализовать
свободные жирные кислоты в 1 г жира.
Первичными продуктами взаимодействия ТАГ с молекулярным кислородом
являются гидропероксиды ЖК, образующиеся в результате цепного
свободнорадикального процесса.
H
O2
LH
L H
L
LOO
L O O H
HX
L
липид
гидропероксид
15.
Химические свойства ВЖК:окисление in vivo
.
.
.
в) β-окисление окисление насыщенных
ЖК протекает в митохондриях при участии
коферментов – НSКоА, НАД+, ФАД.
г) пероксидное окисление липидов (ПОЛ):
Один из наиболее важных окислительных процессов в
организме. Он является основной причиной
повреждения клеточных мембран (например, при
лучевой болезни).
Обусловлено окислением ненасыщенных ЖК в
мембранах при участии АФК:
О ,.Оˉ , НО., Н О и др.
2
2
2
2
16.
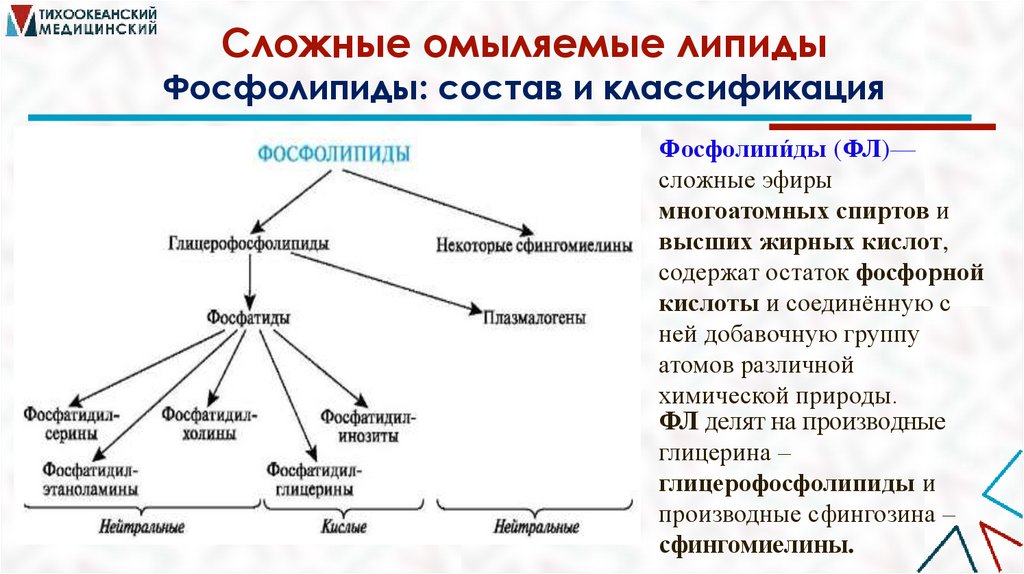
Сложные омыляемые липидыФосфолипиды: состав и классификация
Фосфолипи́ды (ФЛ)—
сложные эфиры
многоатомных спиртов и
высших жирных кислот,
содержат остаток фосфорной
кислоты и соединённую с
ней добавочную группу
атомов различной
химической природы.
ФЛ делят на производные
глицерина –
глицерофосфолипиды и
производные сфингозина –
сфингомиелины.
17.
Глицерофосфолипиды –производные L-фосфатидных кислот
Структурная формула
L-фосфатидной кислоты:
Структурная формула
глицерофосфолипида:
Х - группа атомов различной химической природы.
В условиях организма рН =7, 4 ионные
группировки в фосфатидах ионизированы.
18.
Фосфолипиды: строениеГлицерофосфолипиды – бифильные вещества,
которые включают: полярную – гидрофильную
часть (остаток глицерола, карбонильные и
фосфатная группы, полярная группировка – X);
неполярную – гидрофобную часть (остатки
ВЖК).
Фосфолипиды формируют липидный бислой структурную основу мембран;
• участвуют в регуляции активности
ферментов;
• служат «якорем» для мембранных белков;
• участвуют в передаче гормональных сигналов.
19.
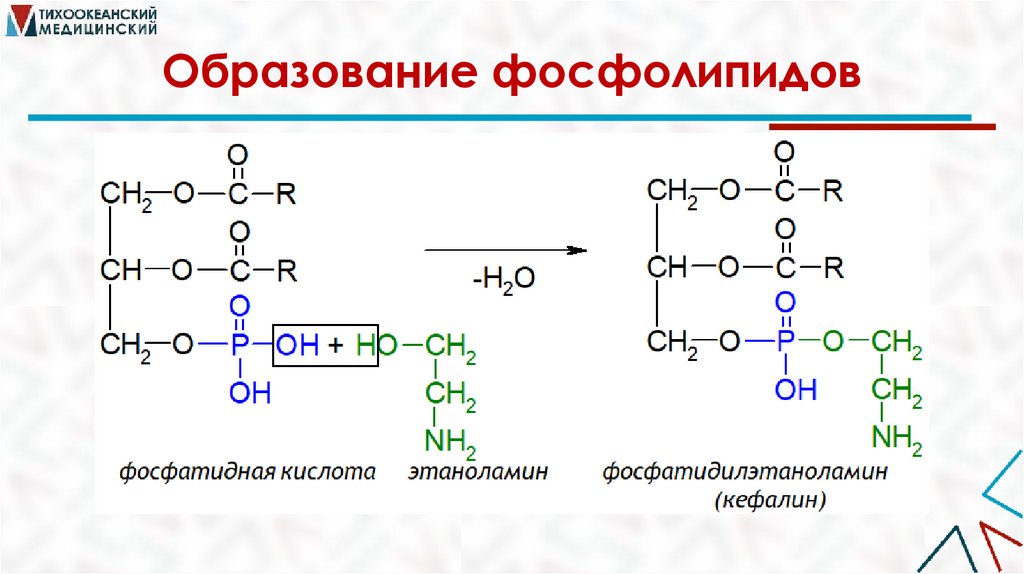
Образование фосфолипидов20.
Классификация глицерофосфолипидов,биологическая роль
1. Фосфатидилэтаноламины (ФЭ, коламинкефалины) – производные
L-фосфатидных кислот и этаноламина.
….от общего количества
фосфолипидов составляет
25%.
В клетке содержится не в
свободном виде, а в виде
комплексов с белками.
Входит в состав мембран
митохондрий.
21.
Классификация глицерофосфолипидов,биологическая роль
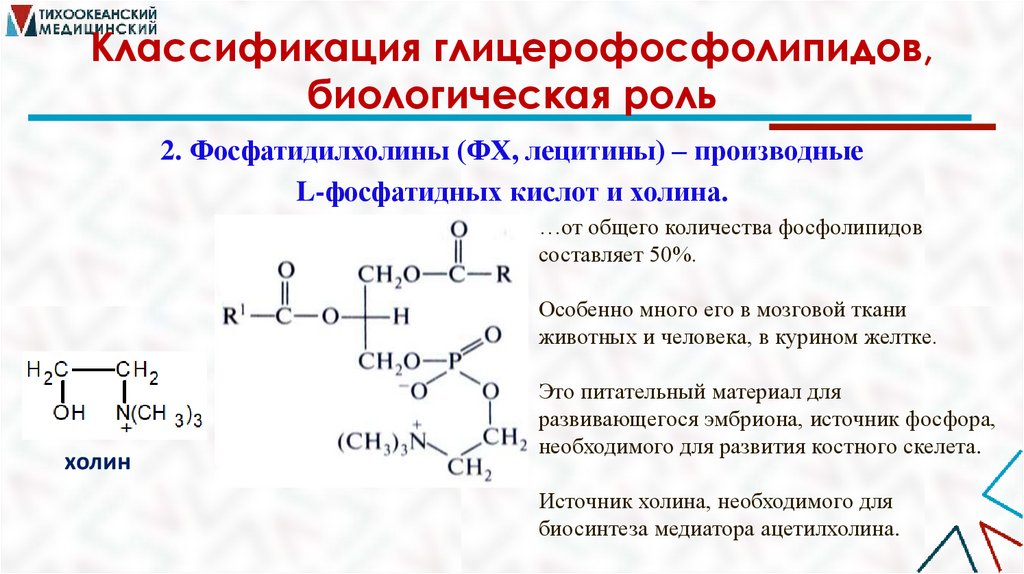
2. Фосфатидилхолины (ФХ, лецитины) – производные
L-фосфатидных кислот и холина.
…от общего количества фосфолипидов
составляет 50%.
Особенно много его в мозговой ткани
животных и человека, в курином желтке.
холин
Это питательный материал для
развивающегося эмбриона, источник фосфора,
необходимого для развития костного скелета.
Источник холина, необходимого для
биосинтеза медиатора ацетилхолина.
22.
Классификация глицерофосфолипидов,биологическая роль
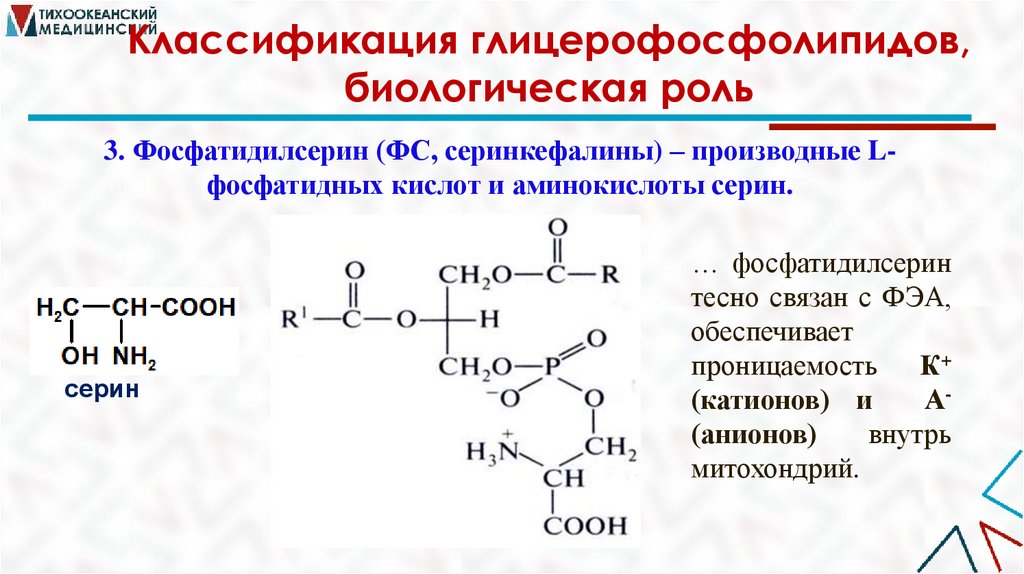
3. Фосфатидилсерин (ФС, серинкефалины) – производные Lфосфатидных кислот и аминокислоты серин.
серин
… фосфатидилсерин
тесно связан с ФЭА,
обеспечивает
проницаемость К+
(катионов) и
А(анионов)
внутрь
митохондрий.
23.
Классификация глицерофосфолипидов,биологическая роль
4. Фосфатидилинозиты – производные L-фосфатидных кислот и
спирта инозитола (инозита).
Фосфатидилинозитолы
содержится в ткани мозга,
обусловливают процессы,
связанные с общим обменом
жиров, белков и углеводов.
Фосфорилированные
производные фосфатидилинозитола
относят к внутриклеточной
системе мессенджеров , в
частности инозитол-1,4,5-трифосфат.
24.
Свойства липидови их структурных компонентов
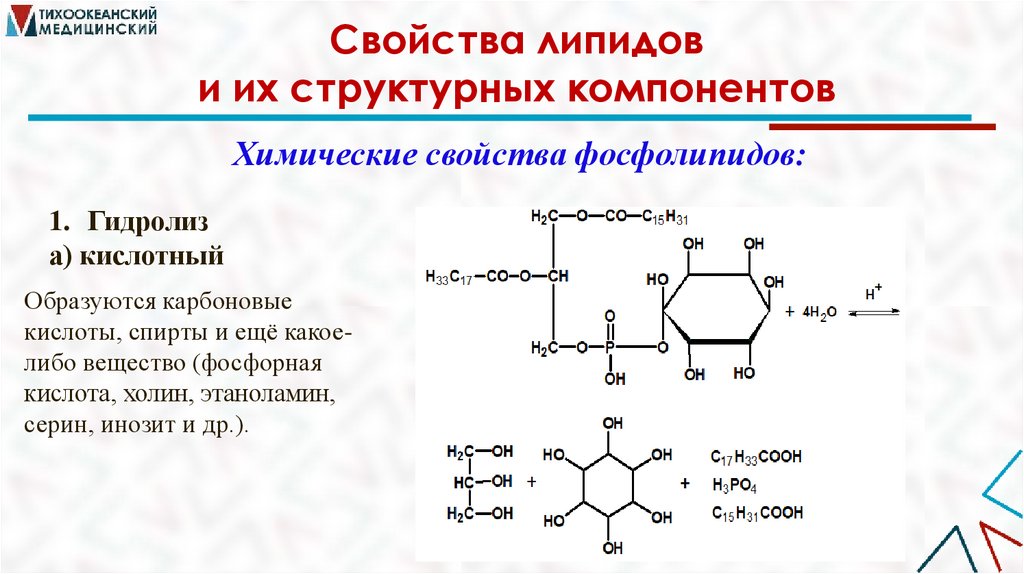
Химические свойства фосфолипидов:
1. Гидролиз
а) кислотный
Образуются карбоновые
кислоты, спирты и ещё какоелибо вещество (фосфорная
кислота, холин, этаноламин,
серин, инозит и др.).
25.
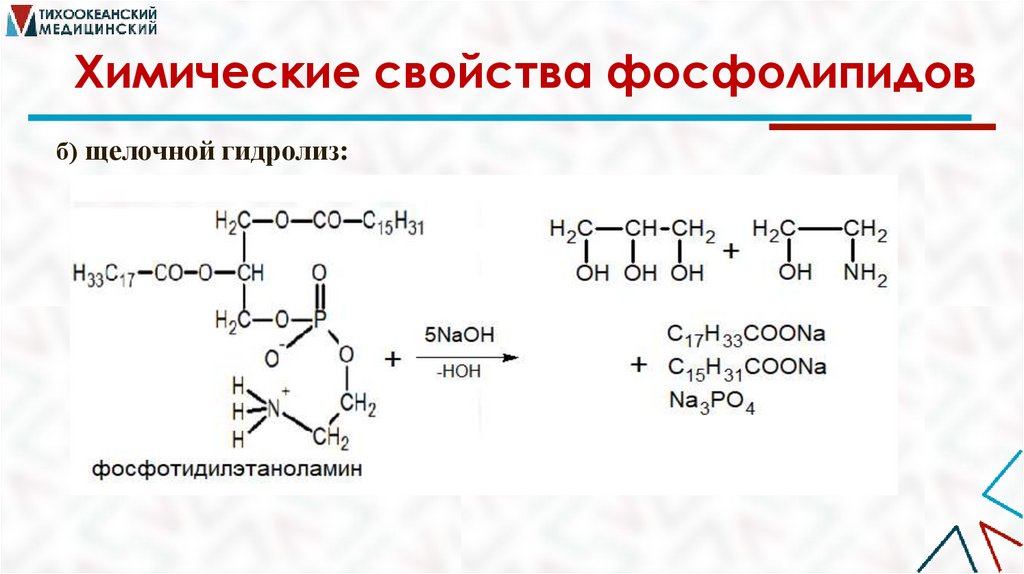
Химические свойства фосфолипидовб) щелочной гидролиз:
26.
Неомыляемые липиды.Терпены. Стероиды
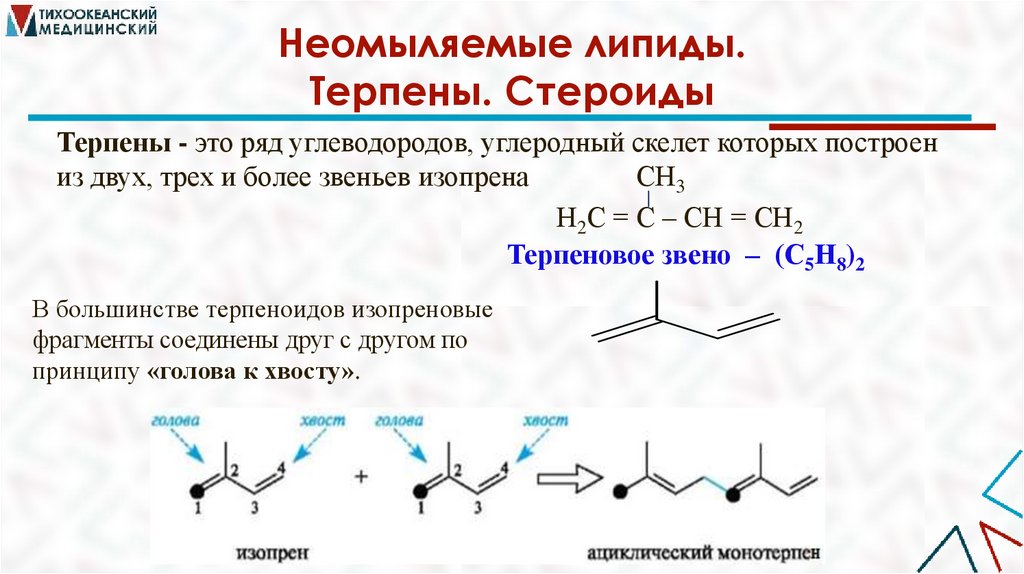
Терпены - это ряд углеводородов, углеродный скелет которых построен
из двух, трех и более звеньев изопрена
СН3
Н2С = С – СН = СН2
Терпеновое звено – (С5Н8)2
В большинстве терпеноидов изопреновые
фрагменты соединены друг с другом по
принципу «голова к хвосту».
27.
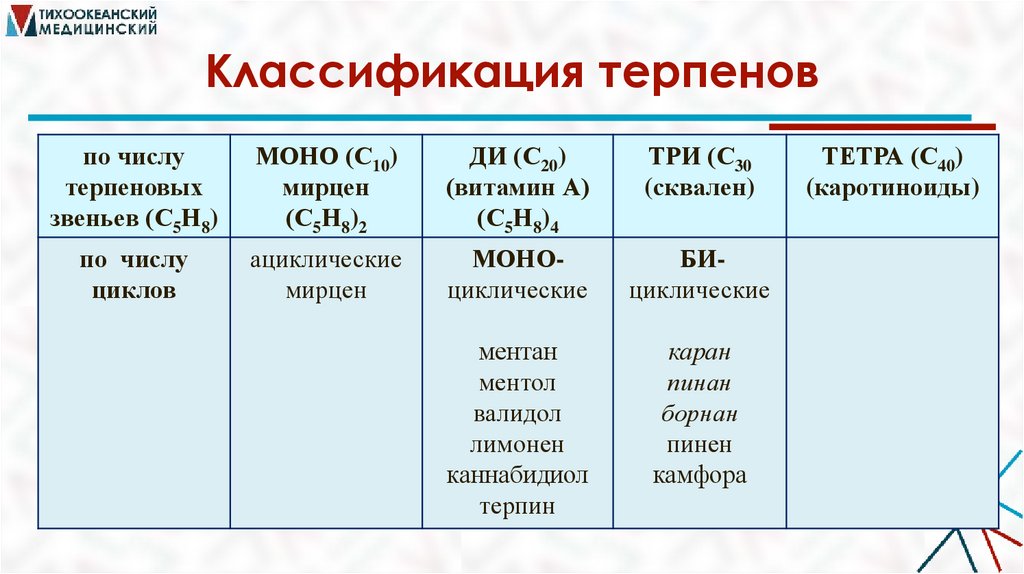
Классификация терпеновпо числу
терпеновых
звеньев (С5Н8)
МОНО (С10)
мирцен
(С5Н8)2
ДИ (С20)
(витамин А)
(С5Н8)4
ТРИ (С30
(сквален)
по числу
циклов
ациклические
мирцен
МОНОциклические
БИциклические
ментан
ментол
валидол
лимонен
каннабидиол
терпин
каран
пинан
борнан
пинен
камфора
ТЕТРА (С40)
(каротиноиды)
28.
Характеристика терпеновАЦИКЛИЧЕСКИЕ:
МИРЦЕН (С10Н16) …построен по правилу «голова – хвост»
Содержится в эфирных маслах ХМЕЛЯ, ЛАВРА. ГЕРАНИОЛ (эфирные масла
герани, розы).
ЦИТРАЛЬ (эфирные масла
лимона, лекарство).
Цитраль и гераниол выделяются в небольших
количествах рабочими пчелами при поиске пищи
и привлекают других пчел. Соединения
цитраль
гераниол
подобного действия называют феромонами.
29.
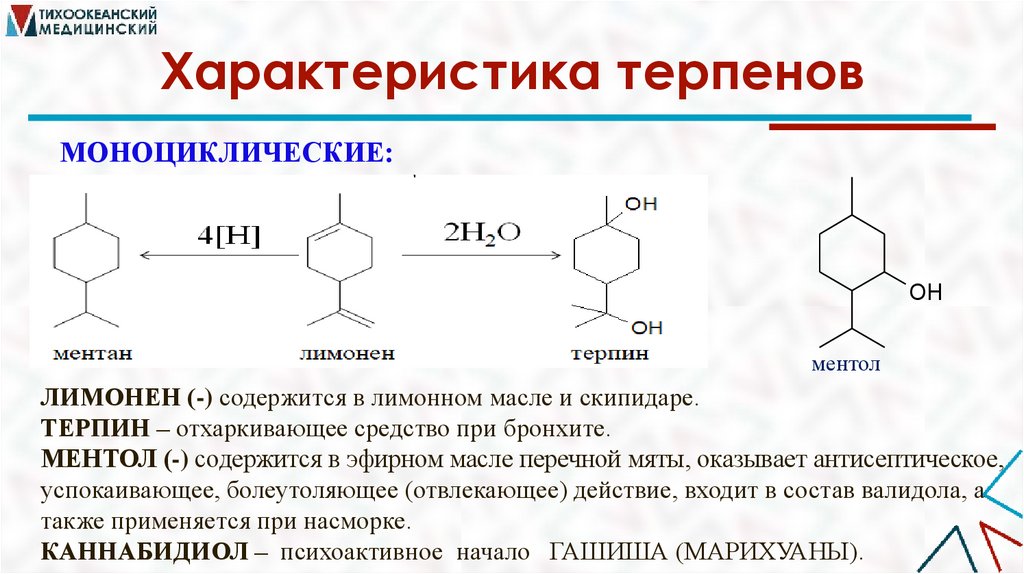
Характеристика терпеновМОНОЦИКЛИЧЕСКИЕ:
OH
ментол
ЛИМОНЕН (-) содержится в лимонном масле и скипидаре.
ТЕРПИН – отхаркивающее средство при бронхите.
МЕНТОЛ (-) содержится в эфирном масле перечной мяты, оказывает антисептическое,
успокаивающее, болеутоляющее (отвлекающее) действие, входит в состав валидола, а
также применяется при насморке.
КАННАБИДИОЛ – психоактивное начало ГАШИША (МАРИХУАНЫ).
30.
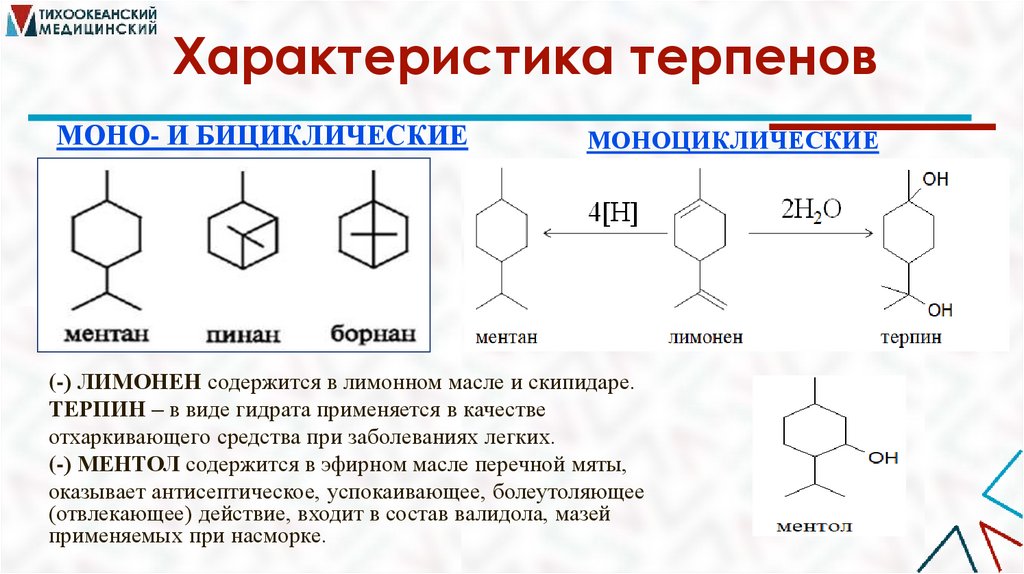
Характеристика терпеновМОНО- И БИЦИКЛИЧЕСКИЕ
МОНОЦИКЛИЧЕСКИЕ
(-) ЛИМОНЕН содержится в лимонном масле и скипидаре.
ТЕРПИН – в виде гидрата применяется в качестве
отхаркивающего средства при заболеваниях легких.
(-) МЕНТОЛ содержится в эфирном масле перечной мяты,
оказывает антисептическое, успокаивающее, болеутоляющее
(отвлекающее) действие, входит в состав валидола, мазей
применяемых при насморке.
31.
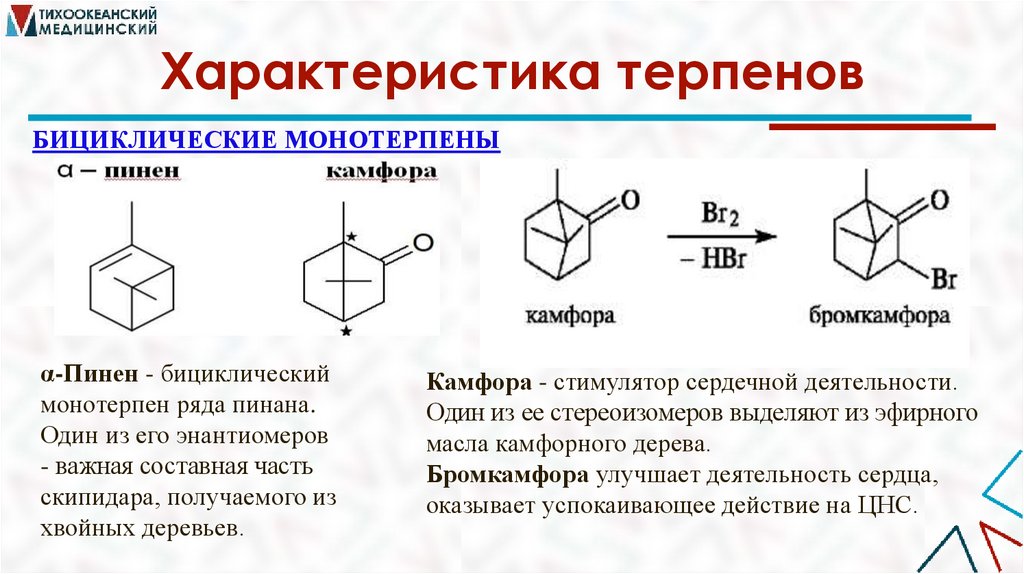
Характеристика терпеновБИЦИКЛИЧЕСКИЕ МОНОТЕРПЕНЫ
α-Пинен - бициклический
монотерпен ряда пинана.
Один из его энантиомеров
- важная составная часть
скипидара, получаемого из
хвойных деревьев.
Камфора - стимулятор сердечной деятельности.
Один из ее стереоизомеров выделяют из эфирного
масла камфорного дерева.
Бромкамфора улучшает деятельность сердца,
оказывает успокаивающее действие на ЦНС.
32.
Характеристика терпеновДИ-, ТРИ-, ТЕТРА- ТЕРПЕНЫ
ВИТАМИН «А»
Принимает участие в процессе
зрительного восприятия
и особенно важен для
обеспечения остроты зрения
при слабой освещенности.
СКВАЛЕН
Промежуточный продукт при
синтезе холестерина.
33.
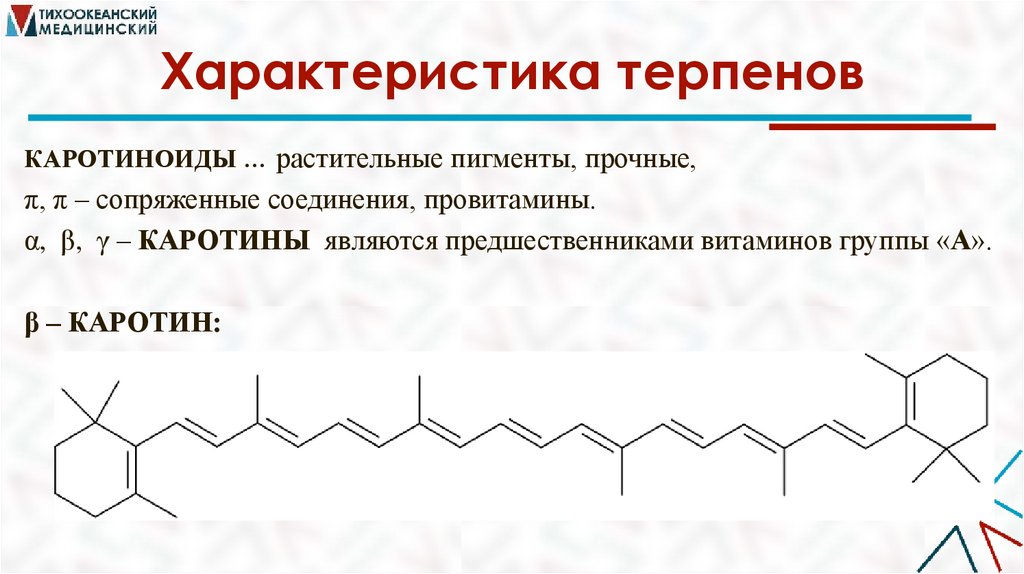
Характеристика терпеновКАРОТИНОИДЫ … растительные пигменты, прочные,
π, π – сопряженные соединения, провитамины.
α, β, γ – КАРОТИНЫ являются предшественниками витаминов группы «А».
β – КАРОТИН:
34.
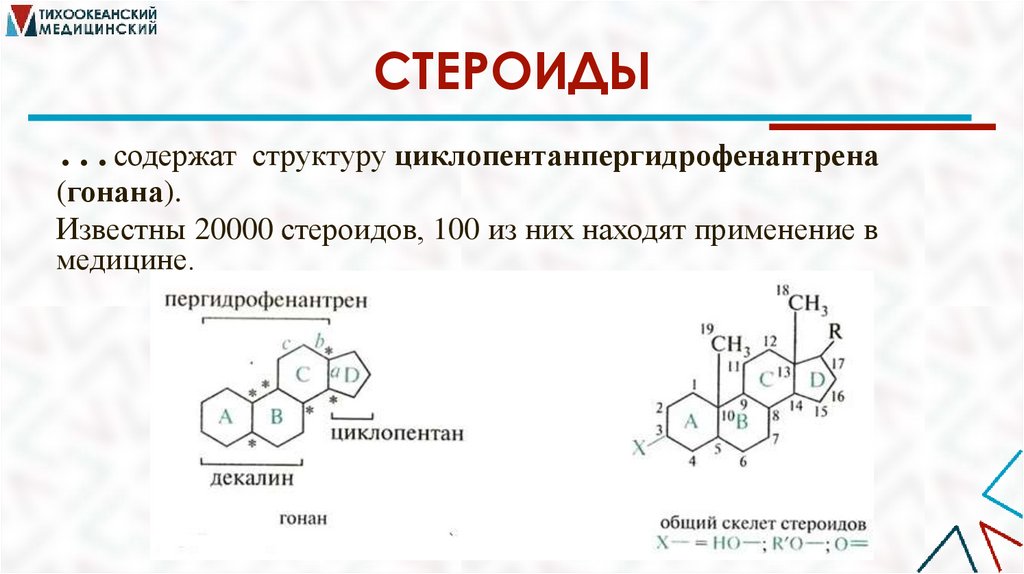
СТЕРОИДЫ…содержат структуру циклопентанпергидрофенантрена
(гонана).
Известны 20000 стероидов, 100 из них находят применение в
медицине.
35.
Общие особенностихимического строения стероидов:
1) С10 и С13 атомы углерода стерановой основы имеют метильные
заместители (ангулярные, т.е. угловые, метильные группы);
2) у С3 атома углерода, обычно, присутствует кислородсодержащая
функциональная группа (гидрокси-, оксо-группы);
3) у С17 атома углерода углеводородный заместитель может
отсутствовать или иметь разный состав; может содержать кратные
связи.
Углеводородная природа этого заместителя является главным
признаком, различающим родоначальные стероидные углеводороды,
которые служат основой химической классификации стероидов.
36.
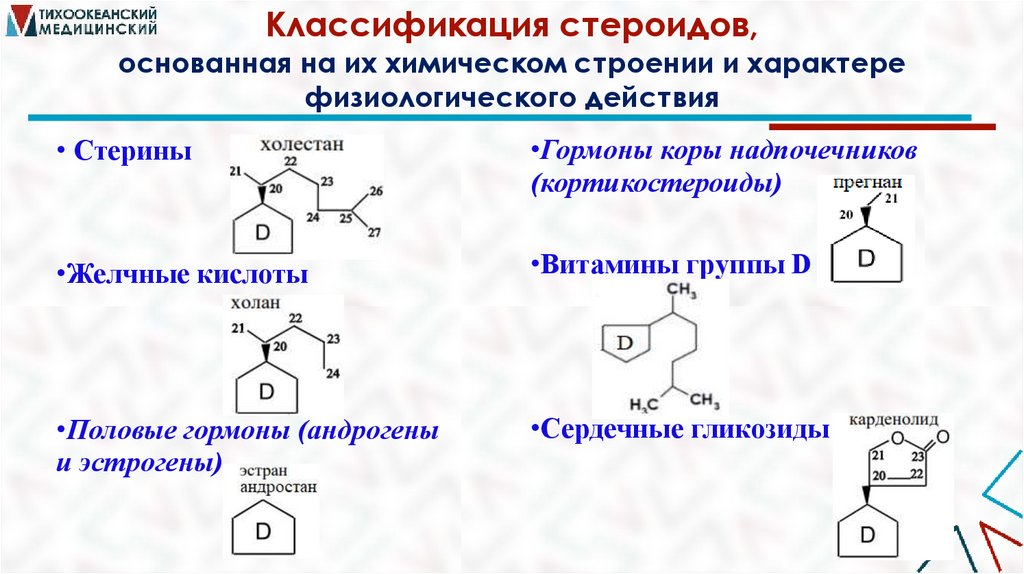
Классификация стероидов,основанная на их химическом строении и характере
физиологического действия
• Стерины
•Гормоны коры надпочечников
(кортикостероиды)
•Желчные кислоты
•Витамины группы D
•Половые гормоны (андрогены
и эстрогены)
•Сердечные гликозиды
37.
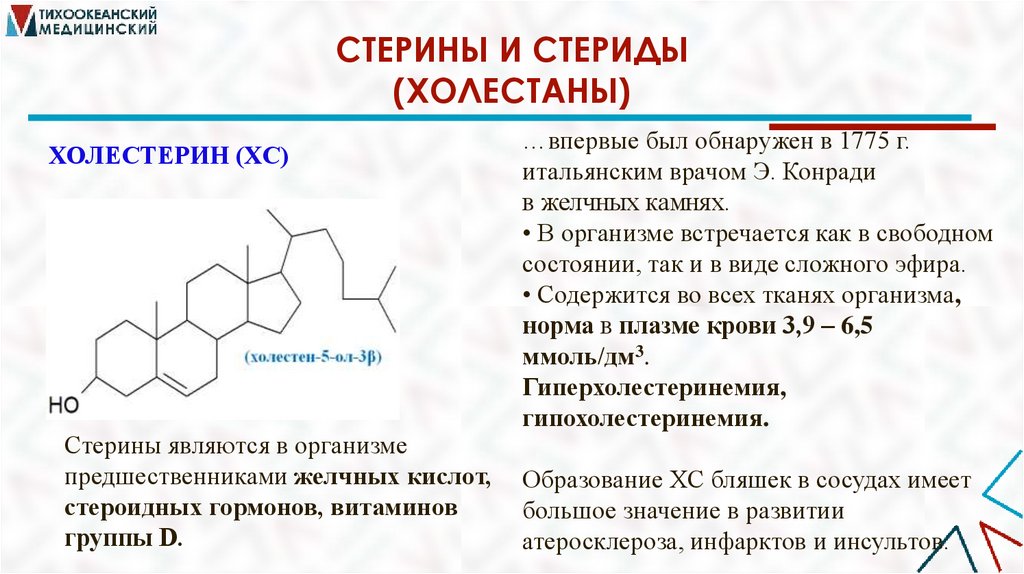
СТЕРИНЫ И СТЕРИДЫ(ХОЛЕСТАНЫ)
ХОЛЕСТЕРИН (ХС)
Стерины являются в организме
предшественниками желчных кислот,
стероидных гормонов, витаминов
группы D.
…впервые был обнаружен в 1775 г.
итальянским врачом Э. Конради
в желчных камнях.
• В организме встречается как в свободном
состоянии, так и в виде сложного эфира.
• Содержится во всех тканях организма,
норма в плазме крови 3,9 – 6,5
ммоль/дм3.
Гиперхолестеринемия,
гипохолестеринемия.
Образование ХС бляшек в сосудах имеет
большое значение в развитии
атеросклероза, инфарктов и инсультов.
38.
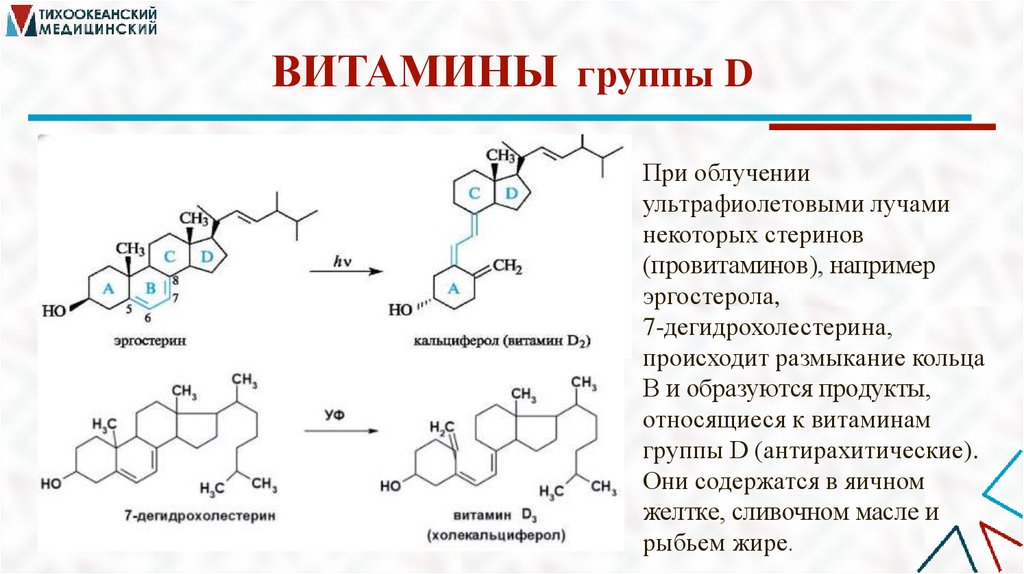
ВИТАМИНЫ группы DПри облучении
ультрафиолетовыми лучами
некоторых стеринов
(провитаминов), например
эргостерола,
7-дегидрохолестерина,
происходит размыкание кольца
В и образуются продукты,
относящиеся к витаминам
группы D (антирахитические).
Они содержатся в яичном
желтке, сливочном масле и
рыбьем жире.
39.
ВИТАМИНЫ группы D…относятся к группе жирорастворимых, впервые заболевание, обусловленное
гиповитаминозом «D», было описано Ф. Глиссоном (1650 г.) – поражение скелета
– рахит.
Синтез: из холестерина под действием УФО.
Биороль: - регуляция синтеза белка, обеспечивающего всасывание
из кишечника «Са»
- усвоение «Р» и лимонной кислоты
- регуляция «Р-Са» обмена и формирование костной ткани.
Нарушение указанных процессов приводит к возникновению заболеваний рахита и остеопороза.
40.
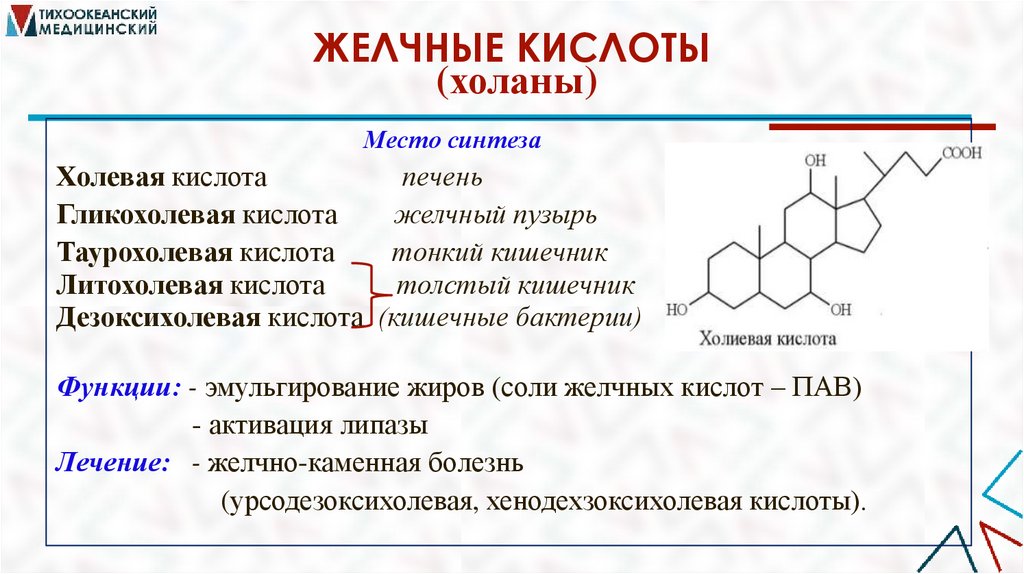
ЖЕЛЧНЫЕ КИСЛОТЫ(холаны)
Место синтеза
Холевая кислота
печень
Гликохолевая кислота
желчный пузырь
Таурохолевая кислота
тонкий кишечник
Литохолевая кислота
толстый кишечник
Дезоксихолевая кислота (кишечные бактерии)
Функции: - эмульгирование жиров (соли желчных кислот – ПАВ)
- активация липазы
Лечение: - желчно-каменная болезнь
(урсодезоксихолевая, хенодехзоксихолевая кислоты).
41.
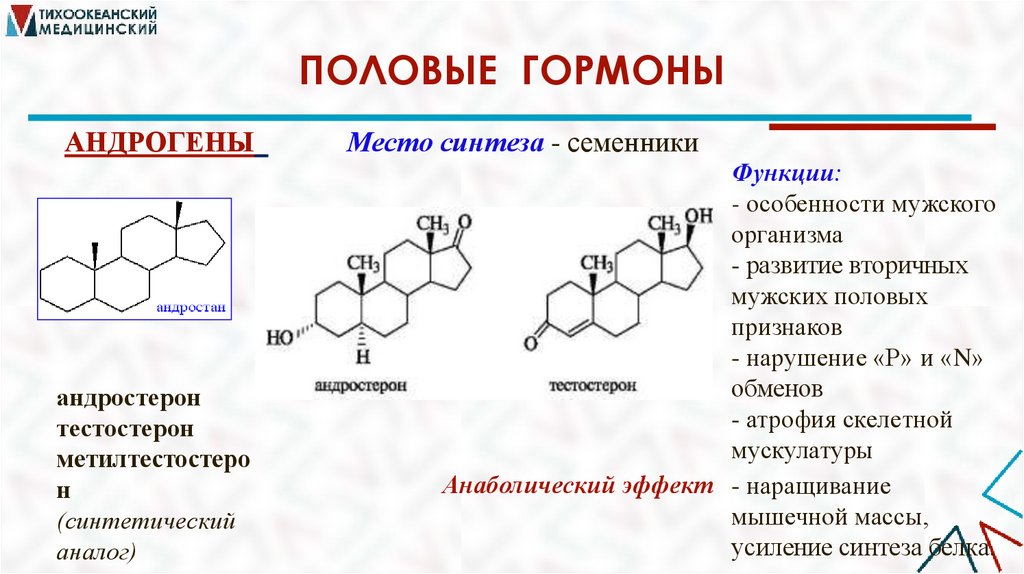
ПОЛОВЫЕ ГОРМОНЫАНДРОГЕНЫ
андростерон
тестостерон
метилтестостеро
н
(синтетический
аналог)
Место синтеза - семенники
Функции:
- особенности мужского
организма
- развитие вторичных
мужских половых
признаков
- нарушение «Р» и «N»
обменов
- атрофия скелетной
мускулатуры
Анаболический эффект - наращивание
мышечной массы,
усиление синтеза белка.
42.
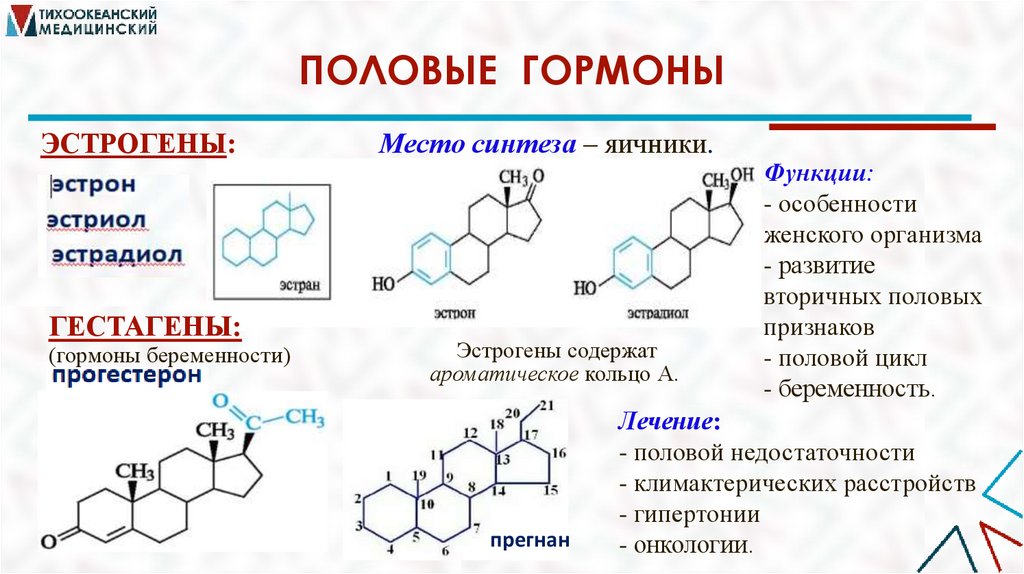
ПОЛОВЫЕ ГОРМОНЫЭСТРОГЕНЫ:
ГЕСТАГЕНЫ:
(гормоны беременности)
Место синтеза – яичники.
Эстрогены содержат
ароматическое кольцо А.
прегнан
Функции:
- особенности
женского организма
- развитие
вторичных половых
признаков
- половой цикл
- беременность.
Лечение:
- половой недостаточности
- климактерических расстройств
- гипертонии
- онкологии.
43.
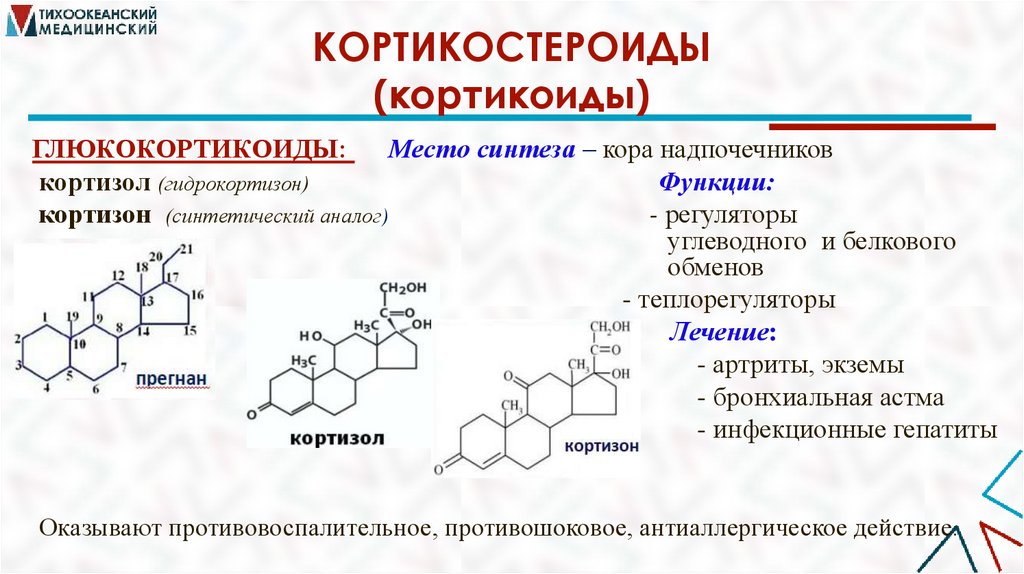
КОРТИКОСТЕРОИДЫ(кортикоиды)
ГЛЮКОКОРТИКОИДЫ:
Место синтеза – кора надпочечников
кортизол (гидрокортизон)
Функции:
кортизон (синтетический аналог)
- регуляторы
углеводного и белкового
обменов
- теплорегуляторы
Лечение:
- артриты, экземы
- бронхиальная астма
- инфекционные гепатиты
Оказывают противовоспалительное, противошоковое, антиаллергическое действие.



















 Химия
Химия








