Похожие презентации:
Радиойодтерапия. Радиойодрезистентность. Таргетная терпия
1.
Радиойодтерапия.Радиойодрезистентность.
Таргетная терпия.
Слащук К.Ю.
врач-эндокринолог, онколог, к.м.н.
2.
3.
Стратификация риска рецидива РЖЩВедение пациента на всех этапах лечения зависит от стратификации риска рецидива, которую можно
условно разделить на три основных этапа:
• Дооперационная стратификация риска для определения показаний и оптимального объема операции
• Послеоперационная стратификация риска для определения адекватности объема операции,
показаний к терапии радиоактивным йодом и супрессивной терапии левотироксином
• Динамическая стратификация риска для оценки ответа на проведенное лечение и определения
оптимальной тактики ведения пациента (в т.ч. отсроченного решения вопроса о проведении РЙТ)
4.
Основные вопросы послеоперационноговедения пациентов с ДРЩЖ
• Оценка выполненного объема операции
• Необходимость радиойодтерапии
• Необходимость супрессивной терапии левотироксином
• Динамическая оценка/переквалификация риска на основании наблюдения
• Периодичность наблюдения при различных результатах лечения
5.
Протокол послеоперационного морфологическогоисследования при ДРЩЖ должен включать:
• Гистологический вариант РЩЖ
• Наличие инвазии в капсулу ЩЖ
• Наличие сосудистой инвазии и количество вовлеченных сосудов (более или менее 4)
• Наличие лимфатической (лимфоваскулярной) инвазии
• Количество и размер удаленных и метастатических лимфоузлов раздельно по зонам шеи
• Оценка экстратиреоидной инвазии – минимальная /распространенная
Минимальная ЭТИ не является стадией Т3b !
распространенная мышечная инвазия – Т3b
• Размер наибольшего метастатического лимфоузла
• Наличие или отсутствие экстранодального/инвазивного роста метастаза за пределы л/у
• Хирургический край резекции (R0, R1, R2)
• Т4 - наличие инвазии в трахею, гортань, пищевод, ВГН
• дополнительное ИГХ-исследование по показаниям
6.
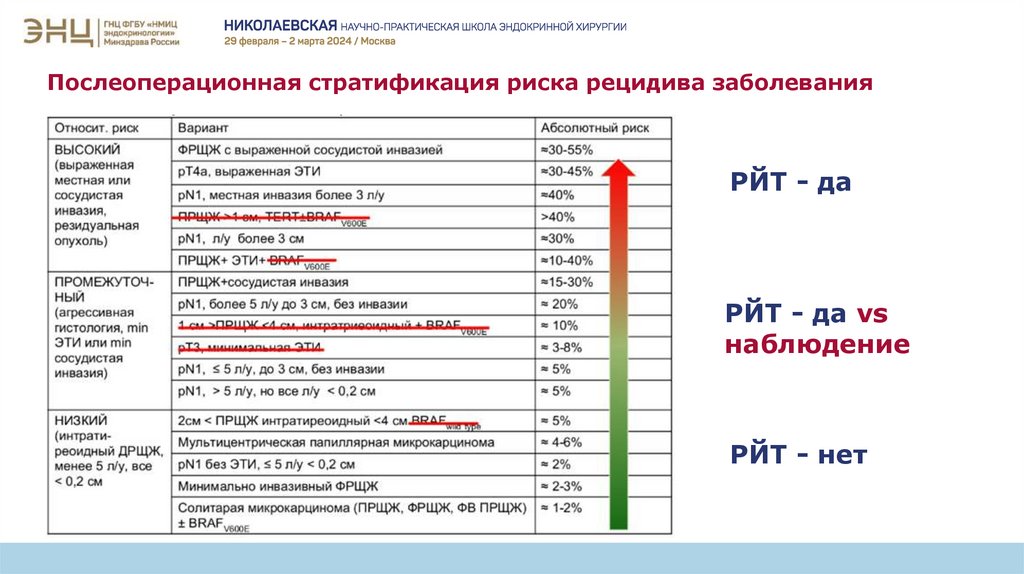
Послеоперационная стратификация риска рецидива заболеванияРЙТ - да
РЙТ - да vs
наблюдение
РЙТ - нет
7.
Алгоритм ведения пациентов после операции• Низкий риск – наблюдение, контроль ТТГ, ТГ, АТ к ТГ через 3-6 месяцев после операции.
Заместительная терапия Л-Т4. Визуализация (УЗИ, КТ) по показаниям.
• Промежуточный риск – наблюдение или РЙТ, контроль ТТГ, ТГ, АТ к ТГ через 3 месяца после
операции.
Мягкая супрессия ТТГ 0,1 – 0,5
+ УЗИ ложа щитвоидной железы и л/у шеи, КТ органов грудной клетки.
Решение вопроса о проведении РЙТ или продолжении наблюдения через 3-6 мес. после
операции
• Высокий риск – планирование РЙТ (возможен пересмотр в случае биохимической и структурной
ремиссии через 3 месяца после операции, по результатам обследования в инд. порядке).
8.
Показания к РЙТ:Отдаленные метастазы дифференцированного рака щитовидной железы
Признаки биохимического и/или структурного рецидива рака щитовидной железы
Высокая группа риска рецидива, по данным послеоперационного гистологического исследования
Повышение чувствительности и специфичности определения ТГ и АТ к ТГ
Риски осложнений:
Постлучевое повреждение слюнных желез (сиалоаденит) - до 50 % острый ~ 2-5 % хронический
Постлучевое повреждение протоков слезных желез (облитерация, дакриоцистит) – 5-10 %
Вторичные ЗНО - 1 % ( ? ОМЛ и ХМЛ)
Постлучевой гастрит, колит, фиброз легких - < 1 %
Протоколы РЙТ
• РЙТ с целью аблации остаточной ткани ЩЖ 1,1 – 3,7 ГБк
• РЙТ с целью терапии отдаленных метастазов 3,7 – 5,5 ГБк (при костных до 7,4 – 11,1 ГБк)
Расчет терапевтической активности I-131 у детей и подростков:
37-92 МБк (~ 55 МБк) на 1 кг массы тела
9.
Подготовка к радиойдотерапииЭндогенная
отмена Левотироксина натрия
на 3-4 недели
Экзогенная
рчТТГ (Тироджин)
I. Стимуляция ТТГ
> 30 мМЕ/л
II. Обеспечение условий дефицита йода в организме:
• Исключить йод-содержащие лек. в-ва. (контраст)
• Йод-ограниченная диета в течение 7-14 дней
(основные источники йода: йодированная соль,
морская рыба, морепродукты, клюква, фейхоа и пр.)
10.
Пациентка А. 18 летПРЩЖ pT4аN1bM1 pul
Ремиссия
РЙТ 131I 5,5 ГБк
Январь 2018
ТГ > 5000 нг/мл
Июль 2018
ТГ 0,09 нг/мл
Январь 2024
11.
ТиреоглобулинНеопределяемый уровень ТГ имеет высокое отрицательное прогностическое значение
В идеале должен оцениваться в одной лаборатории (на одном и том же оборудовании)
Обязательно определение вместе с АТ к ТГ
Возможно определение базального ТГ (на фоне приема левотироксина) или после эндогенной или
экзогенной стимуляции ТТГ (отмена левотироксина/инъекции рчТТГ)
Высокочувствительный анализ базального ТГ (< 0,2 нг/мл) также можно использовать для
подтверждения ремиссии заболевания (полный ответ на лечение) [II, B] [55]
После ТТЭ и РЙА, стимулированный уровень ТГ в сыворотке <1 нг/мл, с высокой вероятностью
говорить об эффективности проводимого лечения, дальнейшее определение стимулированного ТГ
не целесообразно [54]
Повышение уровня ТГ крайне подозрительно в отношении персистенции/рецидива ДРЩЖ, то же
самое актуально и при повышении уровня АТ к ТГ
Короткое время удвоение ТГ (< 1 год) ассоциировано с плохим прогнозом [95]
Filetti S, Durante C, Hartl D, Leboulleux S, Locati LD, Newbold K, Papotti MG, Berruti A; ESMO Guidelines Committee. Electronic address: clinicalguidelines@esmo.org.
Thyroid cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up†. Ann Oncol. 2019 Dec 1;30(12):1856-1883. doi: 10.1093/annonc/mdz400.
PMID: 31549998.
12.
Ультразвуковое исследование• УЗИ шеи является наиболее эффективным методом для выявления местного рецидива
заболевания
• Находки по УЗИ могут быть классифицированы как неопределенные или
подозрительные [62, 63]
• К недостаткам УЗИ можно отнести существенную оператор-зависимость [60], высокую
частоту неспецифических находок [61]
• Диагностическая точность результатов УЗИ, ТАБ (+смыв на ТГ) в сочетании с
уровнем ТГ, может достигать 100% [58,59]
Filetti S, Durante C, Hartl D, Leboulleux S, Locati LD, Newbold K, Papotti MG, Berruti A; ESMO Guidelines Committee. Electronic address: clinicalguidelines@esmo.org.
Thyroid cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up†. Ann Oncol. 2019 Dec 1;30(12):1856-1883. doi: 10.1093/annonc/mdz400.
PMID: 31549998.
13.
Дополнительные методы визуализации(КТ, МРТ, эндоскопия)
• Другие методы визуализации следует назначать, при известных местных и/или
отдаленных метастазах [IV, A] или при подозрении (на основании повышения уровня
ТГ или АТ к ТГ) [IV, B] [8]
• Выбор метода лучевой диагностики зависит от анатомической области:
- КТ с к/у используется для исследования лимфатических узлов шеи и средостения,
нативное КТ для легких
- МРТ для исследования печени, костей и головного мозга [64], МРТ шеи как правило
менее информативно чем КТ
• Подозрение на поражение дыхательных путей/пищевода всегда следует оценивать
эндоскопически (+биопсия)
Filetti S, Durante C, Hartl D, Leboulleux S, Locati LD, Newbold K, Papotti MG, Berruti A; ESMO Guidelines Committee. Electronic address: clinicalguidelines@esmo.org.
Thyroid cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up†. Ann Oncol. 2019 Dec 1;30(12):1856-1883. doi: 10.1093/annonc/mdz400.
PMID: 31549998.
14.
Дополнительные методы визуализации123/131I СВТ (ОФЭКТ/КТ), 18F-ФДГ (ПЭТ/КТ)
У пациентов с биохимической ремиссией после РЙТ проведение плановой СВТ не
показано (так как чувствительность дСВТ низкая (25-55%) [IV, A] [64]
СВТ показано через 6-12 мес. после РЙА у пациентов группы высокого и
промежуточного риска без достижения биохимической ремиссии
Однофотонная эмиссионная компьютерная томография + КТ (ОФЭКТ/КТ)
существенно превосходит планарную СВТ [64]
ПЭТ/КТ с 18ФДГ является более чувствительным методом чем СВТ, для выявления
персистирующего заболевания у пациентов с отрицательными данными по УЗИ, КТ +
повышенным уровнем ТГ (более 10 нг/мл) и/или агрессивными гистотипами опухоли
(например, агрессивные варианты ПРЩЖ, низкодифференцированный РЩЖ, широко
инвазивный фолликулярный РЩЖ) [67]
Захват ФДГ ассоциирован с худшим прогнозом и резистентностью к лечению
радиоактивным йодом [68, 69], но не является надежным предиктором роста опухоли [70]
Filetti S, Durante C, Hartl D, Leboulleux S, Locati LD, Newbold K, Papotti MG, Berruti A; ESMO Guidelines Committee. Electronic address: clinicalguidelines@esmo.org.
Thyroid cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up†. Ann Oncol. 2019 Dec 1;30(12):1856-1883. doi: 10.1093/annonc/mdz400.
PMID: 31549998.
15.
СтратификацияБиохимическая и
структурная
ремиссия
Критерии оценки
Нестимул. TГ < 0,2 нг/мл
Стимул. TГ < 1,0 нг/мл
Отриц. данные УЗИ, КТ, СВТ
Нестимул. TГ > 1 нг/мл
Неполная
биохимическая
ремиссия
Стимул. TГ > 10 нг/мл
Вираж АТ к ТГ
Отриц. данные УЗИ, КТ, СВТ
Структурный
рецидив
Структурные признаки опухоли
при любом ТГ и/или АТ к ТГ
Неспец. топические данные,
Низкий захват 123/131I в ложе
Неопределенный
опухолевый
статус
0,2 < Нестимул. TГ < 1,0 нг/мл
1,0 < Стимул. TГ < 10 нг/мл
АТ к ТГ стабильны или снижаются
Риск
Тактика лечения
Рецидив 1-4%
Специфич. смертность < 1%
Снизить периодичность
наблюдения и не проводить
супрессию ТТГ
Около 30% - спонтанное снижение
б/х показателей
20% - ремиссия после
дополнительного лечения
20% - структурный рецидив
Специфич. смертность < 1%
Стабильный или снижающийся
ТГ/АТ к ТГ– наблюдение.
Рост ТГ и/или АТ к ТГ –
обследование / лечение.
(«Мягкая») супрессия ТТГ у
большинства больных
50-58% сохраняют персистенцию,
несмотря на дополнительное
лечение.
Специфич. смертность при
шейных метастазах ~ 10%,
при отдаленных ~ 50%
Лечение зависит от: размера,
локализации, скорости роста,
захвата 131I или 18FDG,
гистологического варианта
опухоли. Супрессия ТТГ
Структурный рецидив 15-20%
Неспецифические изменения могут
быть стабильны или исчезнуть
Специфич. смертность < 1%
Продолжить наблюдение
(топика, ТГ). Подозрительные
изменения - дополнительная
визуализация и биопсия.
(«Мягкая») супрессия ТТГ
16.
Критерии резистентности ДРЩЖк терапии радиоактивным йодом для
взрослых пациентов
1
Наличие одного (или более) очага не
накапливающего 131I на посттерапевтической
сцинтиграфии всего тела при адекватно
выполненной РЙТ
РЙР
ДРЩЖ
Прогрессирование опухолевого процесса
в течение ≤ 12 месяцев согласно системе
RECIST 1.1 на фоне РЙТ активностью не
менее 100 мКи (3,7 ГБк)
1
2
2
3
Румянцев П.О., Фомин Д.К., Румянцева У.В. Критерии резистентности
высокодифференцированного рака щитовидной железы к терапии
радиоактивным йодом. Опухоли головы и шеи №3, 2014
Отсутствие регрессии очагов опухоли
3 при суммарной лечебной активности
131I более 600 мКи (22 ГБк)
17.
Выживаемость пациентов сраспространенным РЙР ДРЩЖ
127 пациентов
1.0
0.9
Группа 1
Изначально накапливающие I131 , с ответом
на лечение (контроль методами визуализации)
Возраст < 55 лет
Чаще высокодифференцированные формы
Малые размеры метастазов
1
Выживаемость (%)
0.8
0.7
0.6
0.5
Группа 2
Изначально накапливающие I131 , но
прогрессирующие
168 пациентов
0.4
2
0.3
132 пациента
Группа 3
Изначально рефрактерные к I131
0.2
3
0.1
0.0
0
5
10
15
20
25
Годы после выявления метастазов
Durante C, et al. J Clin Endocrinol Metab. 2006;91(8):2892–2899.
30
35
40
18.
ОСНОВНЫЕКритерии для назначения
таргетной терапии при РЙР-ДРЩЖ
Прогрессирование опухоли в течение 12 месяцев или менее, согласно критериям
RECIST 1.1. ≥20% и/или появление новых очагов опухоли
Большая опухолевая нагрузка
ДОПОЛНИТЕЛЬНЫЕ
Симптоматические проявления или риск прогрессирования
(сдавление/инвазия нервов, сосудов, трахеи, пищевода, др. структур)
Хороший функциональный статус пациента (ECOG, возраст, коморбидность) – отсутствие
противопоказаний; приверженность пациента терапии и возможность наблюдения
18F-ФДГ позитивные метастазы с высокой метаболической активностью
Время удвоения тиреоглобулина <2 лет / нарастание антител к тиреоглобулину
Адаптировано из Berdelou, A., Lamartina, L., Klain, M., Leboulleux, S., Schlumberger, M., & on behalf of the
TUTHTYREF Network. (2018). Treatment of refractory thyroid cancer, Endocrine-Related Cancer, 25(4), R209-R223.
19.
Одобрено FDAТип рака
Возраст
пациента
Объективный
ответ
опухоли
РЙР ДРЩЖ
РЙР ДРЩЖ
РЙР ДРЩЖ
> 18 лет
> 18 лет
> 18 лет
60 %
12 %
28%
NTRK
Ларотректиниб
Энтректиниб
Любой солидный
Любой солидный
Любой
≥ 12 лет
86 %
54 %
RET
Селперкатиниб
Пралсетиниб
Любой солидный
Любой солидный
≥ 12 лет
≥ 12 лет
79 %
89 %
BRAF
Дабрафениб/Траметиниб
Любой солидный
≥ 12 лет
69 %
Таргетная терапия
Мутация не имеет
значения
1-2 линия Ленватиниб
1-2 линия Сорафениб
2-3 линия Кабозантиниб
20.
Молекулярные мишени сигнальных каскадов в клетках ДРЩЖBuffet C et al., 2020
21.
8 (495) 500-00-64rnt@endocrincentr.ru




















 Медицина
Медицина








