Похожие презентации:
Виды химических связей
1.
Виды химическихсвязей
2.
Под химической связью понимаютсяэлектрические силы притяжения, удерживающие
частицы друг около друга. Частицами могут быть
атомы, ионы, молекулы.
3.
Причина образования химической связи —стремление атомов посредством взаимодействия с
другими атомами достичь более устойчивого
состояния.
Электроотрицательность (ЭО) – способность
притягивать электроны.
Если атомы обладают одинаковой ЭО, возникает
ковалентная неполярная связь;
Если атомы обладают ЭО разной, но не резко
отличаются, разность в ЭО < 1,7 – возникает
ковалентная полярная связь;
Если атомы обладают ЭО разной, резко отличаются,
разность в ЭО > 1,7 – возникает ионная связь.
4.
Ионная связь - это связь междуположительно и отрицательно
заряженными ионами. Характеризуется
прочностью и высокими
температурами плавления и кипения.
Соли, основания и оксиды металлов
образованы ионной химической
связью.
5.
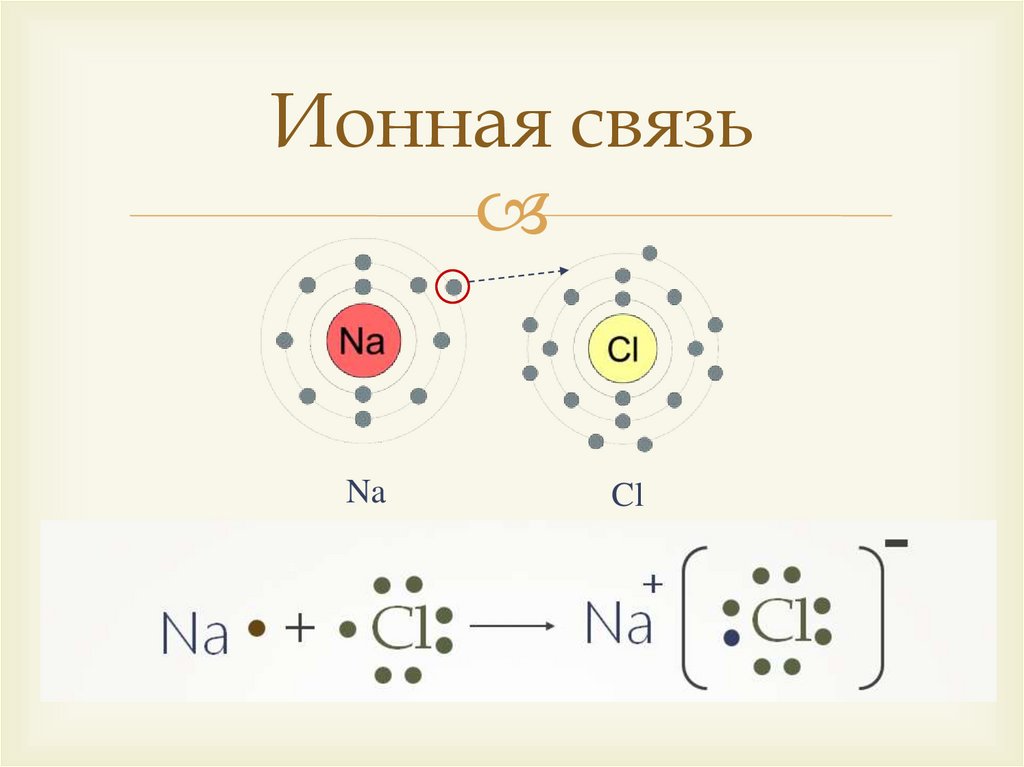
Ионная связьNa
Cl
6.
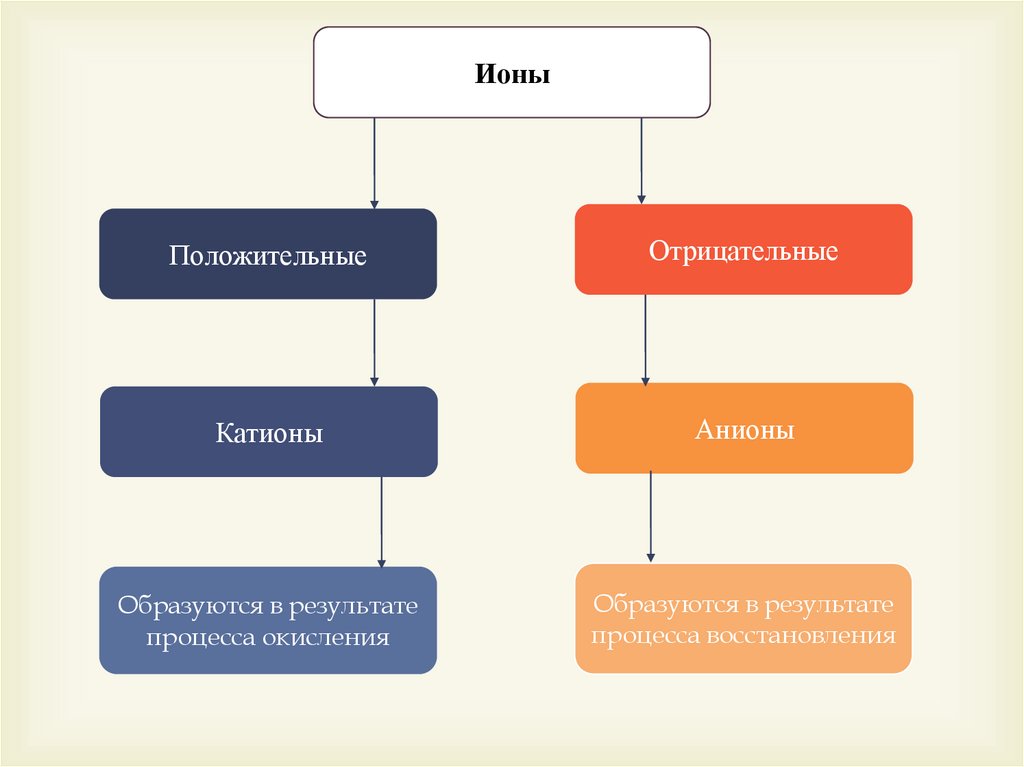
ИоныПоложительные
Отрицательные
Катионы
Анионы
Образуются в результате
процесса окисления
Образуются в результате
процесса восстановления
7.
Как правило, ионная связь возникает междуатомами типичных металлов и типичных
неметаллов.
8.
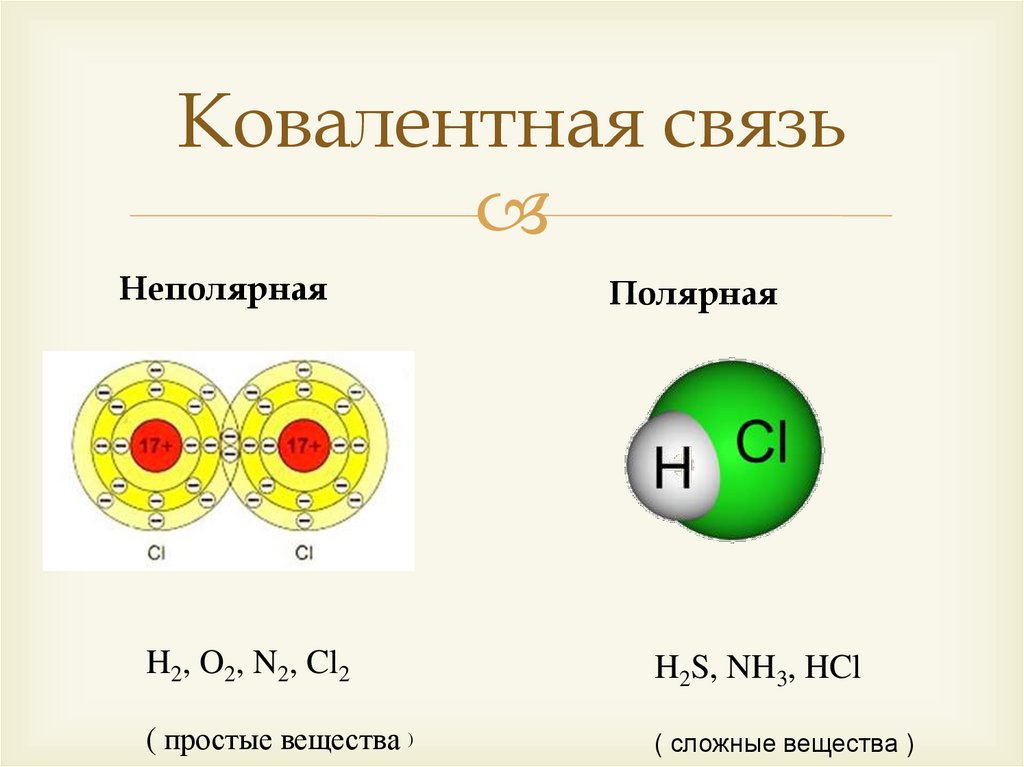
Ковалентная связьНеполярная
Полярная
H2, O2, N2, Cl2
H2S, NH3, HCl
( простые вещества )
( сложные вещества )
9.
Ковалентная связь -это химическая связь, возникающая за
счет образования общих электронных
пар.
(электронами внешнего уровня )
Возникает только между атомами
неметаллов
10.
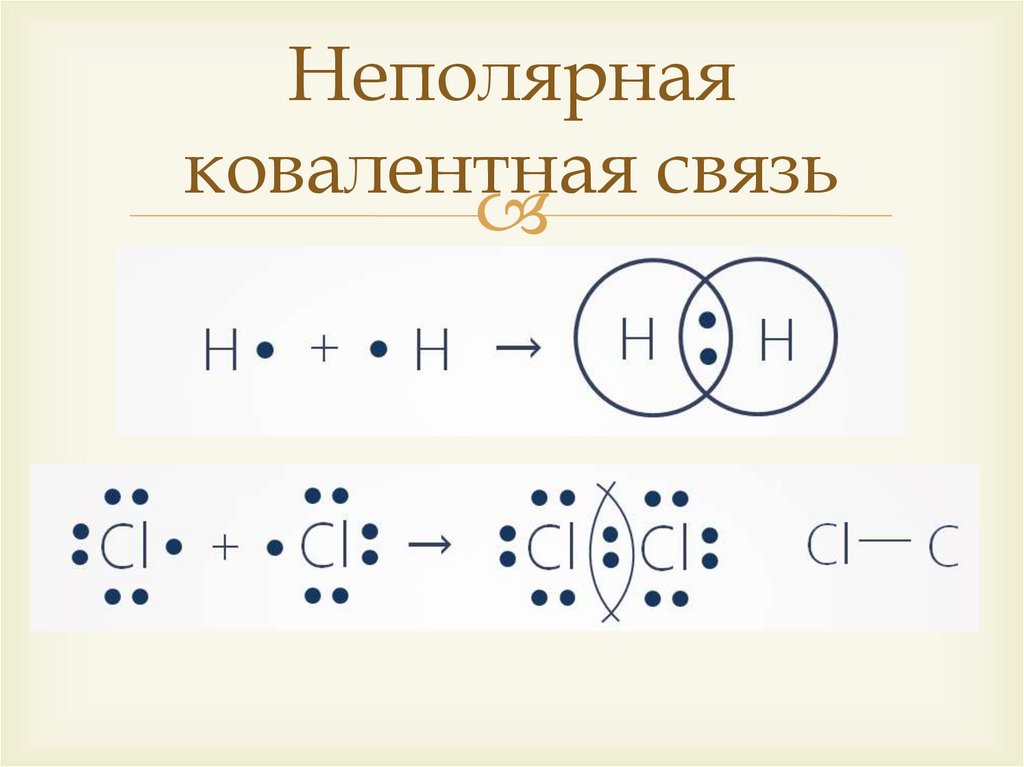
Неполярнаяковалентная связь
11.
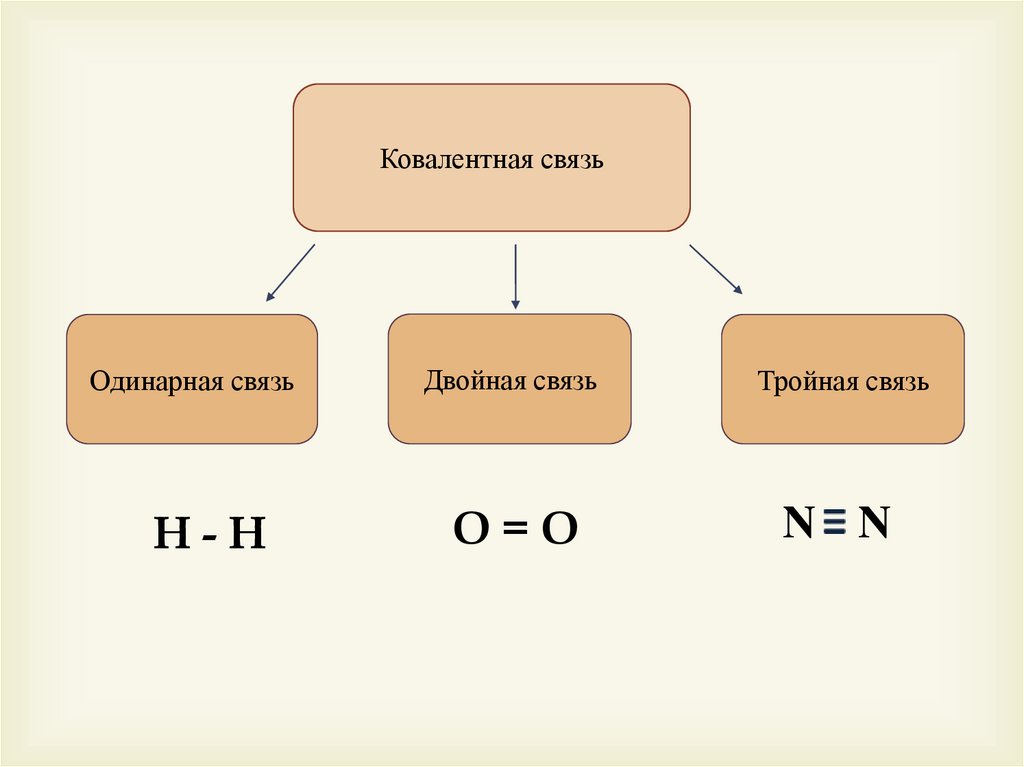
Ковалентная связьОдинарная связь
Двойная связь
Тройная связь
Н-Н
О=О
N N
12.
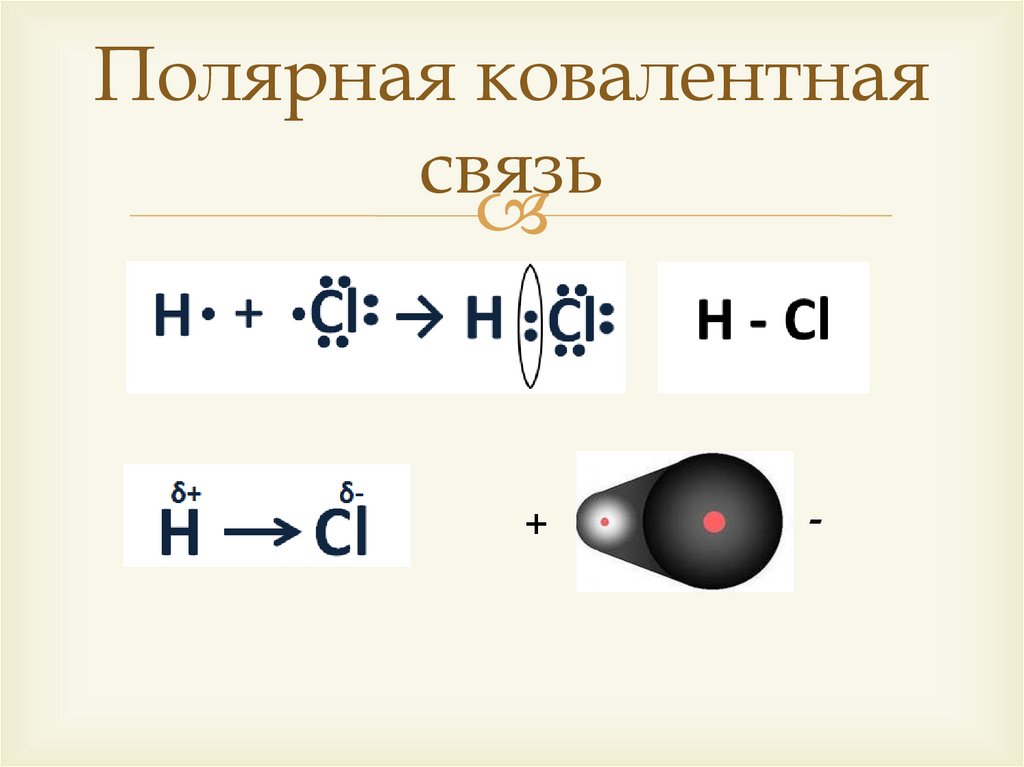
Полярная ковалентнаясвязь
+
-
13.
Ковалентная полярная связь образуетсямежду атомами неметаллов разных
химических элементов.
Возникающие общие электронные пары
смещаются к более электроотрицательному
элементу. Поэтому у него образуется избыток
отрицательного заряда. А со стороны
элемента с меньшей ЭО возникает область
положительного заряда.
Молекула вытянута и имеет два полюса :
+ и -
14.
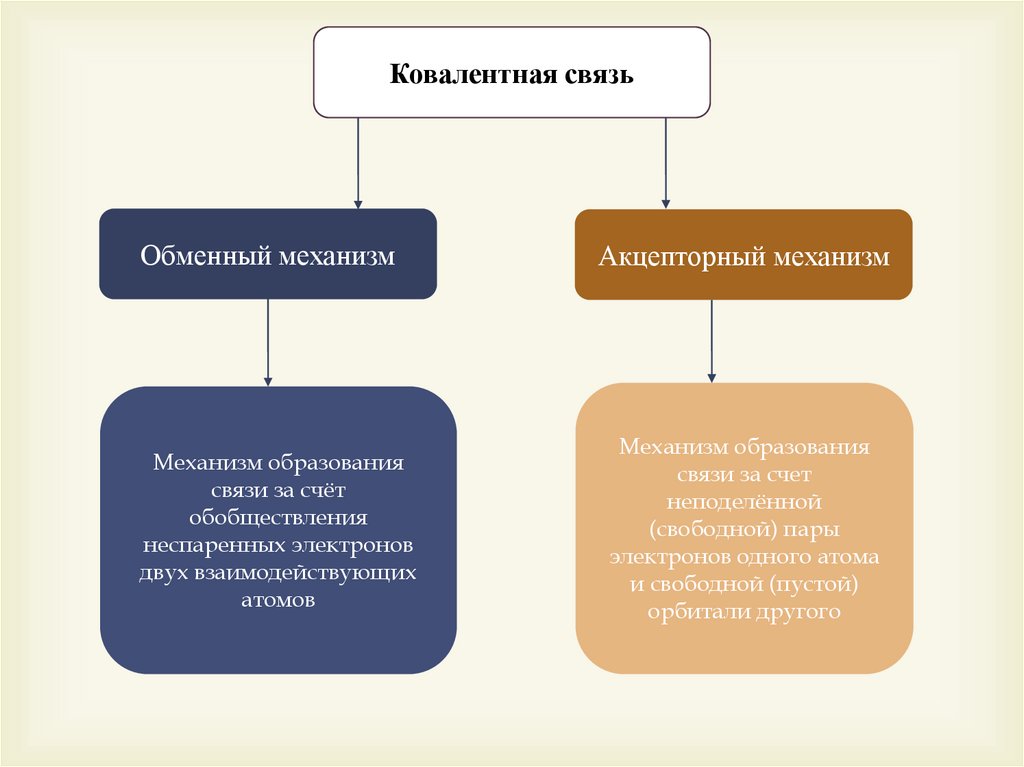
Ковалентная связьОбменный механизм
Акцепторный механизм
Механизм образования
связи за счёт
обобществления
неспаренных электронов
двух взаимодействующих
атомов
Механизм образования
связи за счет
неподелённой
(свободной) пары
электронов одного атома
и свободной (пустой)
орбитали другого
15.
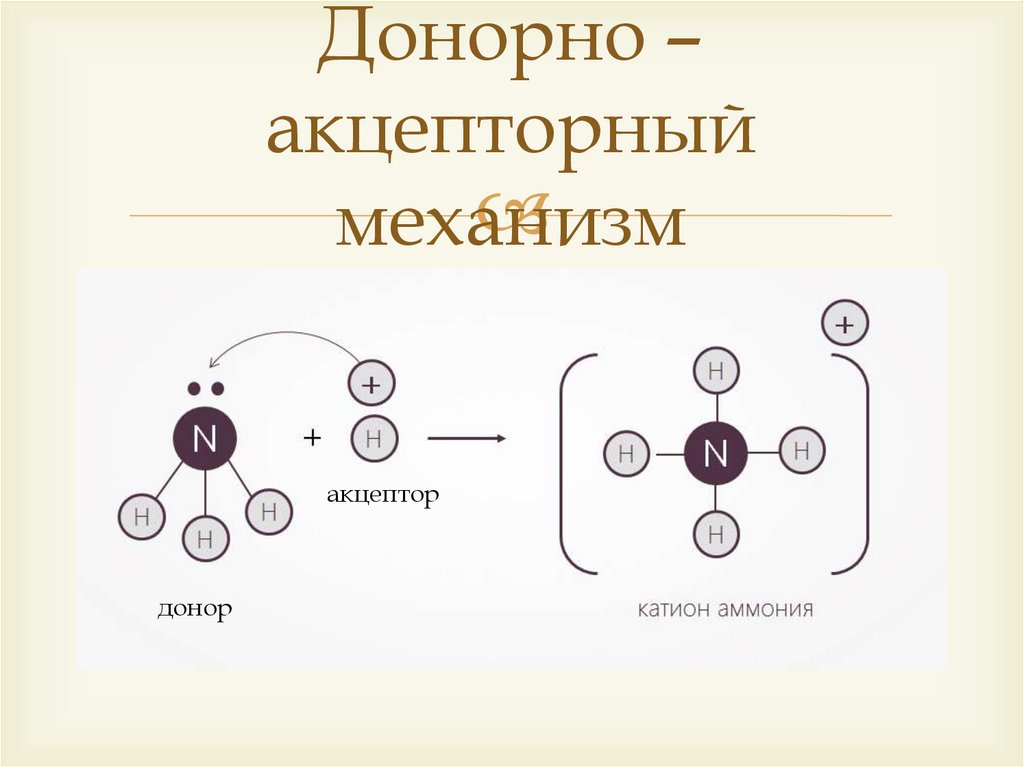
Донорно –акцепторный
механизм
акцептор
донор
16.
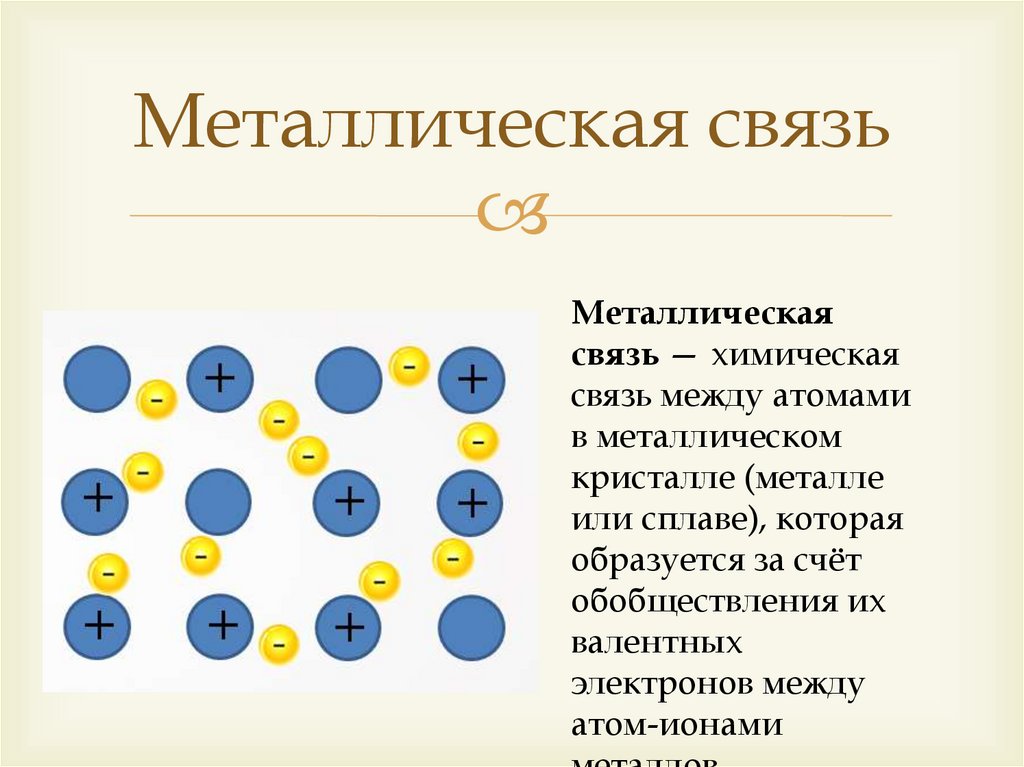
Металлическая связьМеталлическая
связь — химическая
связь между атомами
в металлическом
кристалле (металле
или сплаве), которая
образуется за счёт
обобществления их
валентных
электронов между
атом-ионами
17.
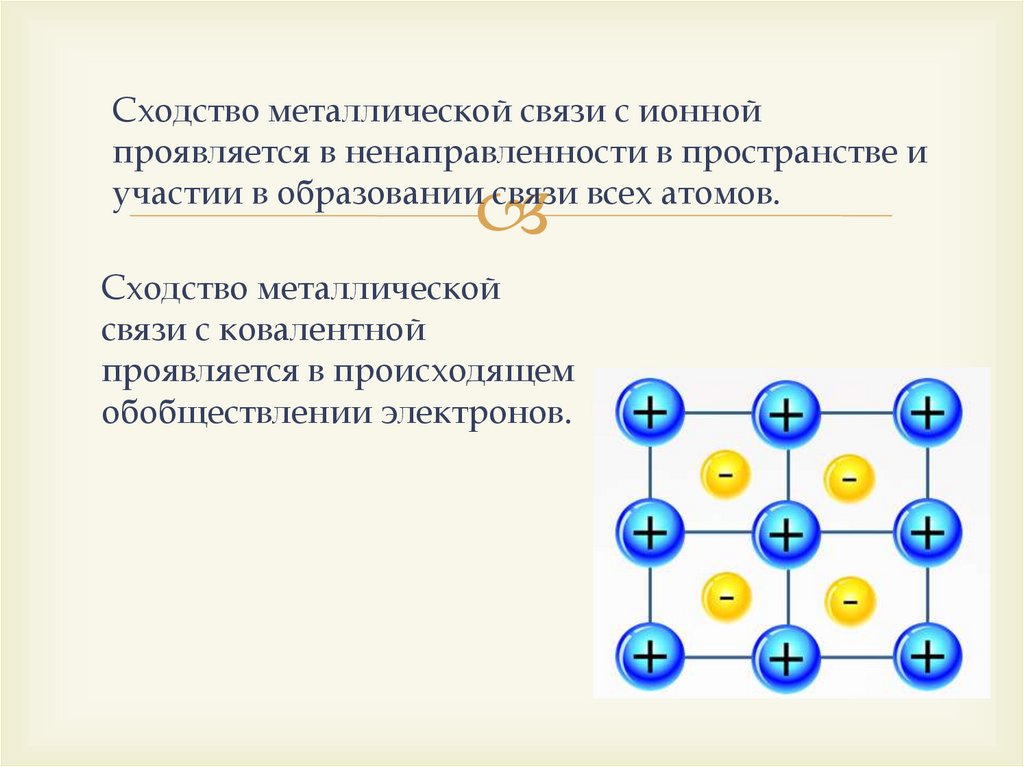
Сходство металлической связи с ионнойпроявляется в ненаправленности в пространстве и
участии в образовании связи всех атомов.
Сходство металлической
связи с ковалентной
проявляется в происходящем
обобществлении электронов.
18.
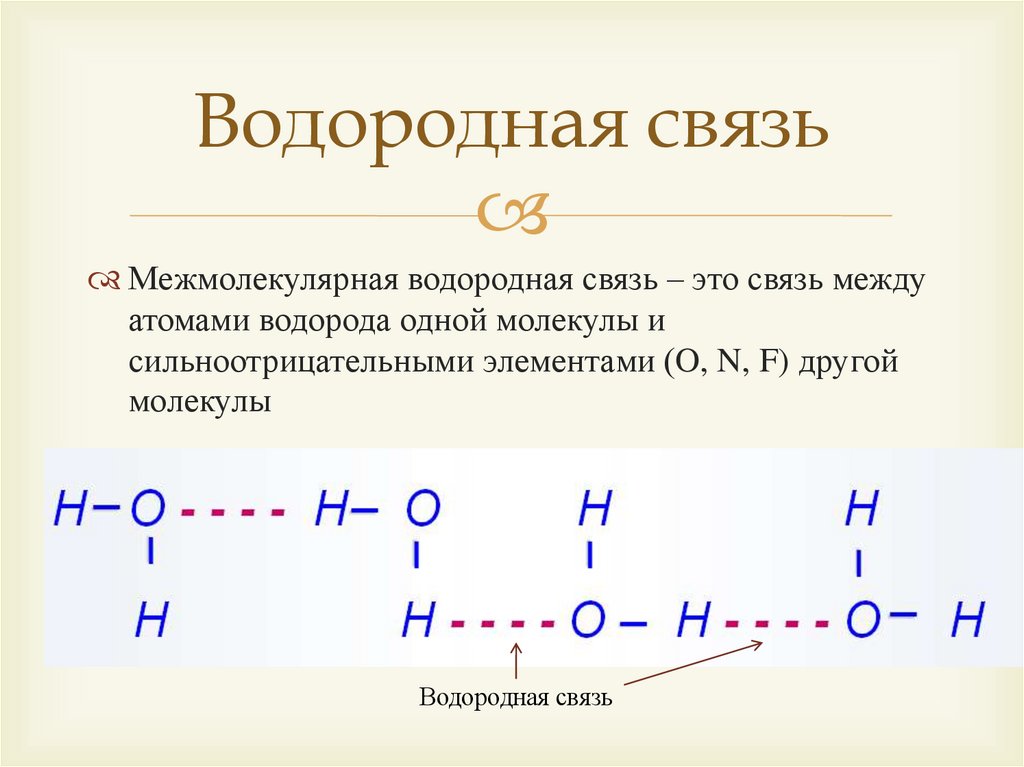
Водородная связьМежмолекулярная водородная связь – это связь между
атомами водорода одной молекулы и
сильноотрицательными элементами (O, N, F) другой
молекулы
Водородная связь
19.
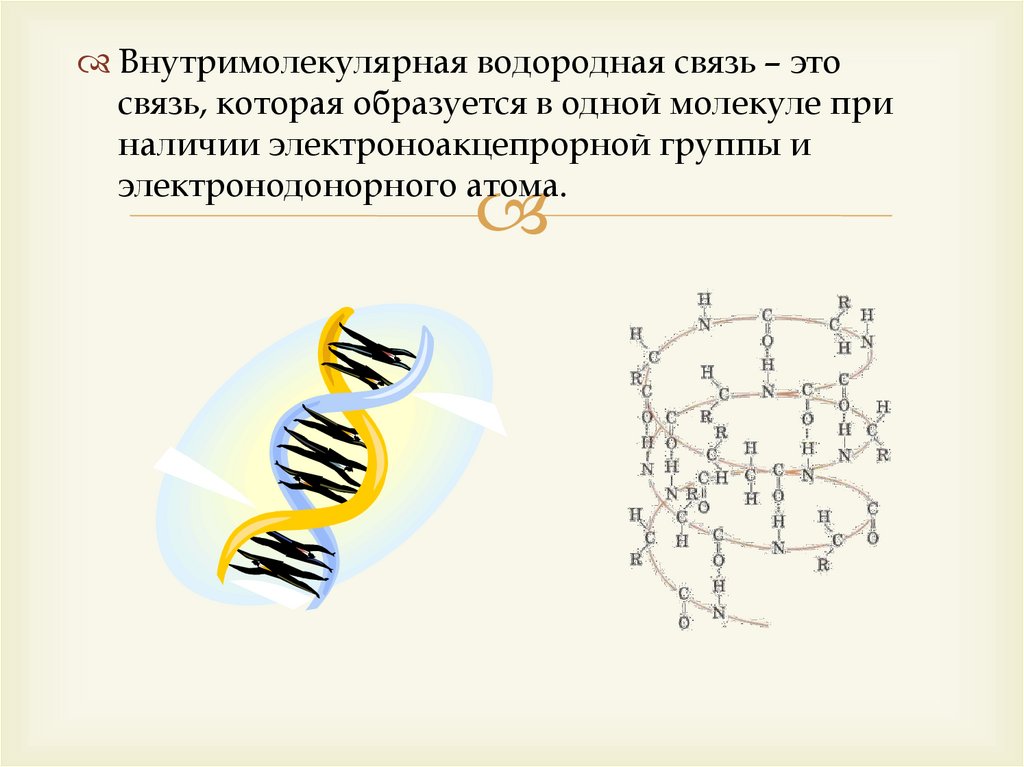
Внутримолекулярная водородная связь – этосвязь, которая образуется в одной молекуле при
наличии электроноакцепрорной группы и
электронодонорного атома.






 Химия
Химия








