Похожие презентации:
Рак молочной железы
1.
Рак молочной железы.Доцент кафедры онкологии
ФГБОУ ВО НГМУ Минздрава России, к.м.н.
Ткачук Ольга Анатольевна
2. Актуальность проблемы:
Ежегодный прирост заболеваемости за последние 10лет составляет 5,8%.
Ежегодно в мире выявляется не менее 1,3 млн. новых
случаев РМЖ.
В России, как и во всем мире РМЖ среди женского
населения вышел на 1 место среди всех
злокачественных опухолей.
27,2 % занимает III и IV стадия процесса
Заболеваемость РМЖ в странах Европейского союза
составляет 50-120 женщин, а смертность 20,3 на 100
000 женского населения в год.
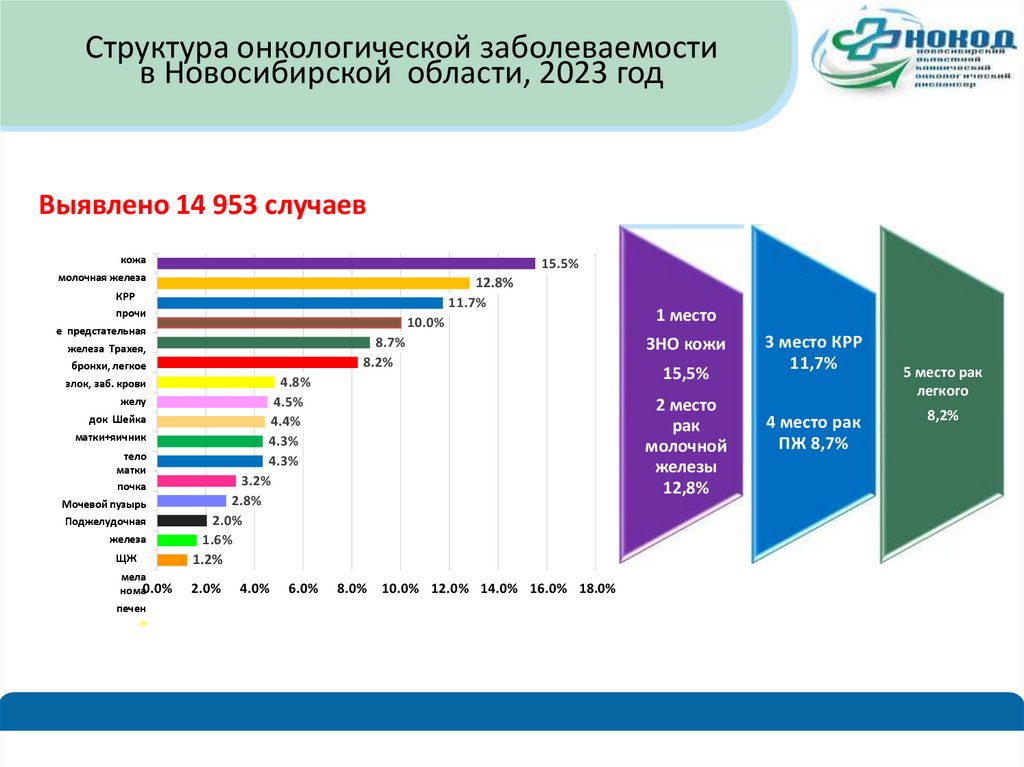
3. Структура онкологической заболеваемости в Новосибирской области, 2023 год
Выявлено 14 953 случаевкожа
15.5%
молочная железа
12.8%
11.7%
КРР
прочи
10.0%
е предстательная
8.7%
8.2%
железа Трахея,
бронхи, легкое
ЩЖ
4.8%
4.5%
4.4%
4.3%
4.3%
3.2%
2.8%
2.0%
1.6%
1.2%
мела
нома0.0%
2.0%
злок, заб. крови
желу
док Шейка
матки+яичник
тело
матки
почка
Мочевой пузырь
Поджелудочная
железа
печен
ь
2023
4.0%
6.0%
1 место
ЗНО кожи
15,5%
2 место
рак
молочной
железы
12,8%
8.0% 10.0% 12.0% 14.0% 16.0% 18.0%
3 место КРР
11,7%
4 место рак
ПЖ 8,7%
5 место рак
легкого
8,2%
4. Статистические данные
Рак молочной железы – наиболее частое злокачественное заболевание у женщин в
РФ. В 2018 году зарегистрировано 70 682 новых случая, что составляет 20,9 % в
структуре заболеваемости злокачественными новообразованиями у женщин.
Средний возраст заболевших составил 61,5 года. Среднегодовой темп прироста
заболеваемости (стандартизованный показатель) составил 1,97 % за последние 10
лет. Кумулятивный риск развития РМЖ в 2018 году составил 5,87 % при
продолжительности жизни 74 года. В последние годы увеличивается количество
пациентов, у которых заболевание диагностировано в I–II стадиях. Так, в 2018 году
этот показатель составил 71,2 %, тогда как 10 лет назад равнялся 62,7 %.
Стандартизованный показатель смертности снизился с 2008 по 2018 гг. с 17,05 до
14,02 соответственно. Риск умереть от рака молочной железы у женщин в 2018 г.
составил 1,6 %. Доля женщин, состоящих на учете 5 и более лет, составляет 59,8 %.
В структуре смертности женского населения РМЖ также находится на первом
месте, составляя 16,2 %.
РМЖ у мужчин составляет менее 1 % опухолей этой локализации, занимая 0,3 % в
структуре заболеваемости. Принципы диагностики и лечения РМЖ у мужчин не
отличаются от таковых у женщин
5. Классификация МКБ-10
Карцинома in situ молочной железы (D05):D05.0 – Дольковая карцинома in situ.
D05.1 – Внутрипротоковая карцинома in situ.
D05.7 – Другая карцинома in situ молочной железы.
D05.9 – Карцинома in situ молочной железы
неуточненная.
6. Риск развития рака молочной железы (РМЖ) в различных регионах мира
• США− 1 из 8; в Европе − 1 из 12; в России 1 из 18; вЯпонии 1 из 80 женщин в течение жизни.
• В России заболеваемость РМЖ 46 на 100 000 женщин,
диффузная мастопатия ( 30-70-98,6%)
• Первый пик заболеваемости приходится на возраст 30-40
лет (80-100 случаев на 100 000 женщин).
• Второй пик заболеваемости приходится на возраст > 65
лет (за счет локальных механизмов, независимых от
функции яичников).
7. Значимость известных факторов риска рака молочной железы
Относительный риск повышен Относительный рискнезначительно: 1<2
повышен: 2-4
Относительный риск
значительно повышен: >4
Раннее менархе
Родственник первой линии с
РМЖ
Мутации генов
предрасположенности**
Применение гормональных
контрацептивов*
Возраст первых родов >35 лет
Дольковая карцинома in situ
Отсутствие родов
Пролиферативные
заболевания молочной
железы без атипии
Атипичная гиперплазия
Поздняя менопауза
Высокая рентгенологическая
плотность молочных желез
Радиационное воздействие на
молочные железы в возрасте
до 30 лет
Постменопаузальное
ожирение
Употребление алкоголя
Примечание: * - повышение вероятности тройного негативного РМЖ;
** - количественную оценку риска осуществляет врач-генетик.
8. АНАТОМИЯ Молочные железы – это железистые гормонозависимые органы, входящие в репродуктивную систему женщины, которые
развиваются и начинают функционировать подвлиянием гормонов:
Гипоталамус (рилизинг - факторы);
Гипофиз (ФСГ - фоликулостимулирующий и ЛГ лютеинизирующий гормоны, пролактин, тиреотропный
гормон и гонадотропин);
Щитовидная железа (Т3,Т4, ТТГ);
Надпочечники (кортикостероиды)
Поджелудочная железа (инсулин)
Яичники (эстрогены, прогестероны и андрогены)
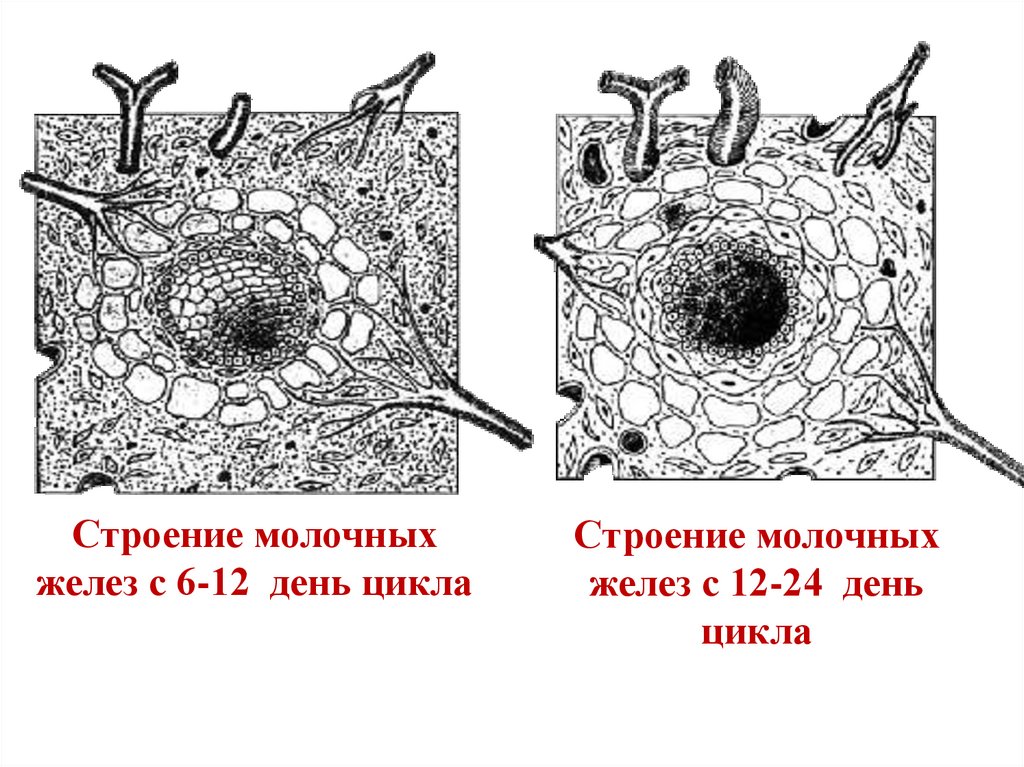
9.
Строение молочныхжелез с 6-12 день цикла
Строение молочных
желез с 12-24 день
цикла
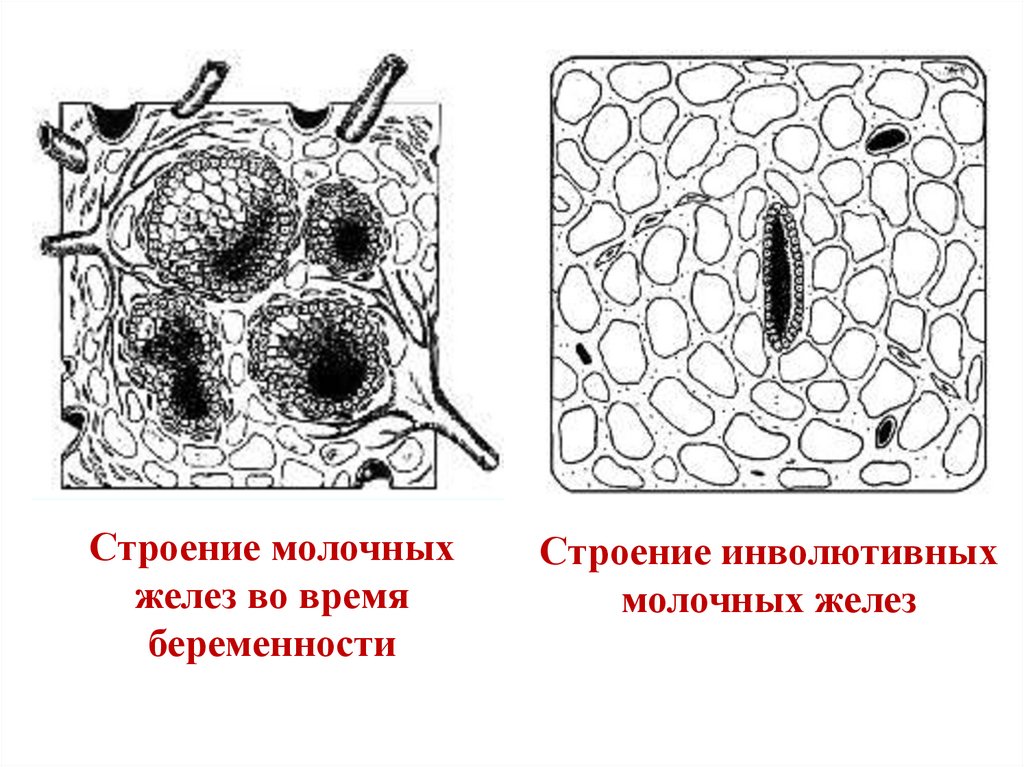
10.
Строение молочныхжелез во время
беременности
Строение инволютивных
молочных желез
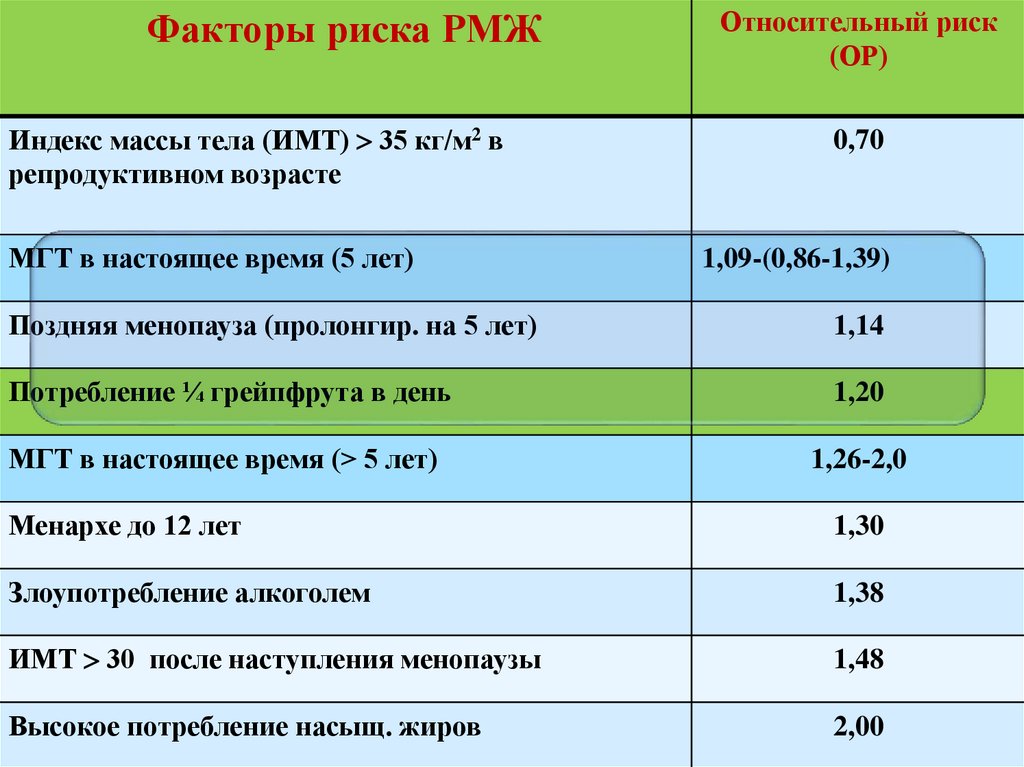
11.
Факторы риска РМЖИндекс массы тела (ИМТ) 35 кг/м2 в
репродуктивном возрасте
МГТ в настоящее время (5 лет)
Относительный риск
(ОР)
0,70
1,09-(0,86-1,39)
Поздняя менопауза (пролонгир. на 5 лет)
1,14
Потребление ¼ грейпфрута в день
1,20
МГТ в настоящее время (> 5 лет)
1,26-2,0
Менархе до 12 лет
1,30
Злоупотребление алкоголем
1,38
ИМТ 30 после наступления менопаузы
1,48
Высокое потребление насыщ. жиров
2,00
12.
5-10% случаев рака молочнойжелезы и яичников
Риск развития рака яичников
- BRCA1 18-60%
- BRCA2 45%
Наследственные
мутации BRCA1,
BRCA 2,CHEK 2
NBS1, TP53.
Риск РМЖ у носительниц
мутаций генов
- BRCA1 - 54-85%
- BRCA2 - 45%
Воздействие эстрогенов на
изменение риска рака молочной
железы у носительниц BRCA не
выяснено*
13. Рекомендуется с диагностической целью проведение генетического тестирования BRCA1/2 у больных РМЖ:
с первично множественным РМЖ у пациентки
включая, но не ограничиваясь установленным
диагнозом
рака
поджелудочной
железы,
контралатеральной МЖ, рака яичников или маточных
труб;
в возрасте до 45 лет всем и до 60 лет при ТН РМЖ;
РМЖ у близких родственников≤50 лет, рак яичников,
маточных труб, рак поджелудочной железы, РМЖ у
мужчин, метастатического рака предстательной железы
при тройном негативном фенотипе опухоли;
РМЖ у мужчин дополнительно определяем поломку в
генах BRCA1/2.
14. Методы диагностики
ПальпацияМаммография
УЗИ молочных желез
Магнитно-резонансная томография
Цитологический метод
Трепанобиопсия (cor-биопсия)
15. Оценка общей распространенности процесса
Сканирование костей скелетаСканирование и/или УЗИ печени
УЗИ органов малого таза
Рентгенография легких
ПЭТ
Консультация гинеколога
МРТ головного мозга
16. Маркеры на РМЖ
• СА 15,3 опухолевый антиген ассоциированный с РМЖ.Повышен у 70-80% больных с диссеминацией и лишь у 2040% больных с вновь диагностируемым ранним РМЖ.
Чувствительность
63%,
специфичность—
89%.
Используется для мониторинга больных, у которых нет
измеряемых проявлений.
• СА-27,29 опухолевый антиген, ассоциированный с
РМЖ, мало известен в России, эффективен в предсказании
рецидива
болезни.
Чувствительность
-57,7%,
специфичность - 97,9%.
• СЕА карцино-эмбриональный антиген повышен у 4050% больных метастатическим РМЖ. Высокие уровни
маркера отмечаются при метастазах в кости, печень и при
множественных проявлениях болезни; повышение маркера
после операции может указывать на риск рецидива.
Чувствительность-54%, специфичность -97%.
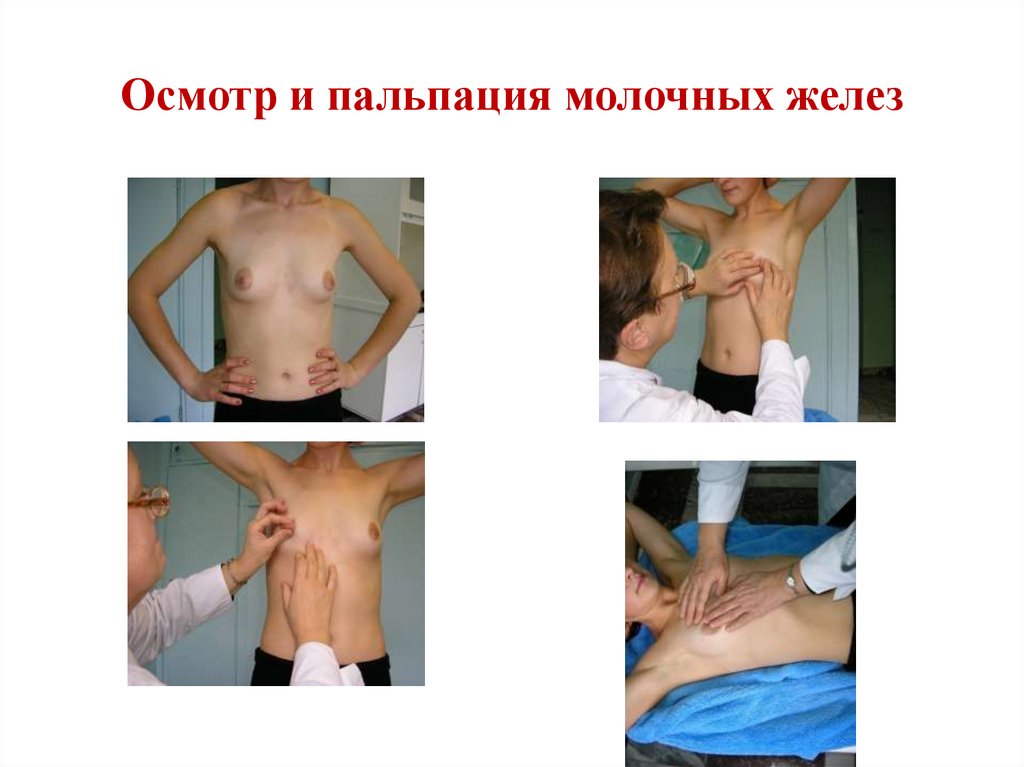
17. Осмотр и пальпация молочных желез
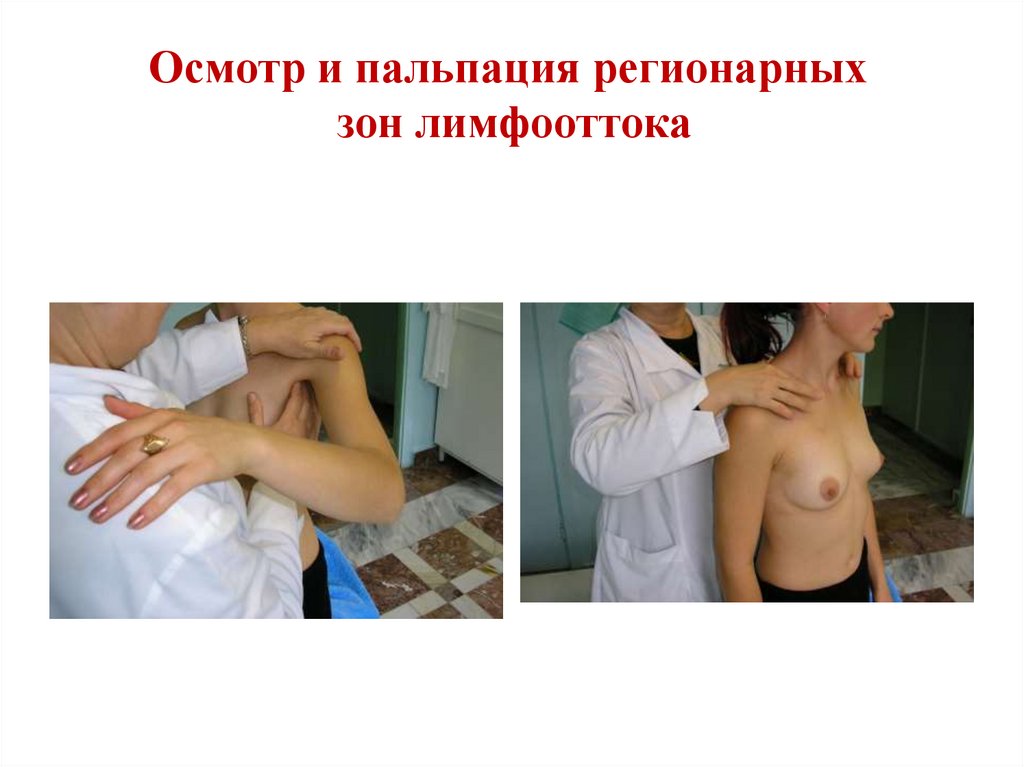
18. Осмотр и пальпация регионарных зон лимфооттока
19.
При осмотре необходимо оценивать симметриюмолочных желез, состояние сосково-ареолярного
комплекса, состояние кожи желез.
Пальпацию молочных желез и регионарных
лимфоузлов необходимо проводить в положении
пациентки стоя и положении лежа.
Требуется оценивать наличие узловых и
инфильтративных образований молочных желез
с
указанием
пальпаторных
размеров,
консистенции,
смещаемости;
определять
наличие, размер и консистенцию лимфоузлов
20. Что необходимо перед инструментальным обследованием?
• результаты самообследования молочных желез иливрачебного осмотра и жалобы пациентки;
• фаза менструального цикла;
• наследственная отягощенность по РМЖ;
• перенесенные заболевания молочных желез,
выполненные хирургические вмешательства, в том
числе пластические и реконструктивные;
• акушерско-гинекологический анамнез по числу
беременностей, в том числе наличие текущей
беременности;
начало
и
регулярность
менструаций, состояние климакса.
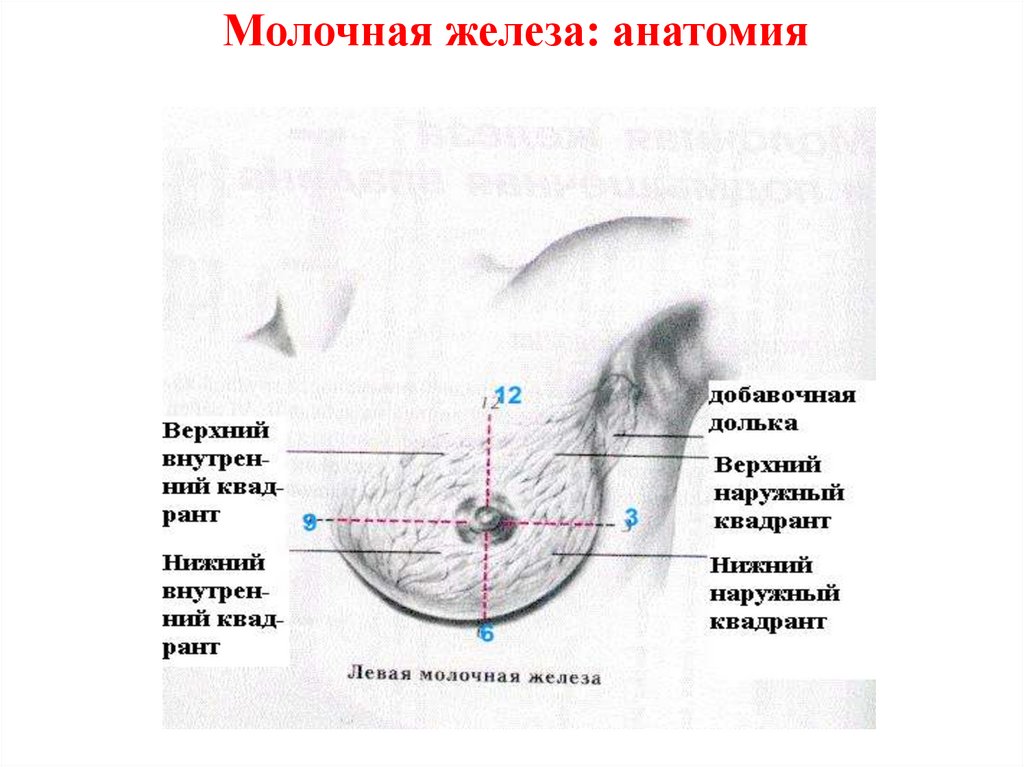
21.
Молочная железа: анатомия22.
УЛЬТРАЗВУКОВАЯ МАММОГРАФИЯNB!!! Применение соноэластографии повышает специфичность
УЗИ почти до 95%, чувствительность для не определяемых при
пальпации опухолей - до уровня выше 85%, общую точность - около
90%.
23.
ПОКАЗАНИЯ К УЛЬТРАЗВУКОВОЙМАММОГРАФИИ
1. Дифференциальная диагностика кист и солидных
образований, выявленных при пальпации и РМ
(рентгеновская маммография).
2. Обследование рентгенологически плотных молочных
желез.
3. Обследование молочных желез у беременных и
кормящих матерей.
4. Обследование молочных желез у женщин до 30 лет.
5. Обследование молочных желез у детей и подростков
обоего пола.
24. ПОКАЗАНИЯ К УЛЬТРАЗВУКОВОЙ МАММОГРАФИИ
6. Обследование молочных желез в острый периодтравмы или воспаления.
7. Оценка состояния силиконовых протезов молочных
желез при невозможности МРТ.
8. Ультразвуковой контроль при пункционой биопсии
пальпируемых и непальпируемых образований в
молочных железах и окружащих тканях.
9. Обследование грудных желез у мужчин.
10. Оценка уплотнений неясной этиологии в молочных
железах.
11. Как дополнение к РМ в группе женщин
предменопаузального периода.
12. Как дополнение к РМ при неоднозачных
рентгенологических заключениях
25. Недостатки УЗИ молочной железы
Субъективность получения изображения, зависящаяот положения датчика;
Малоинформативна при жировой инволюции;
Отсутствие
визуализации
более
60%
непальпируемого рака в виде скопления
микрокальцинатов, в виде локальной тяжистой
перестройке структуры, рака внутри протоков.
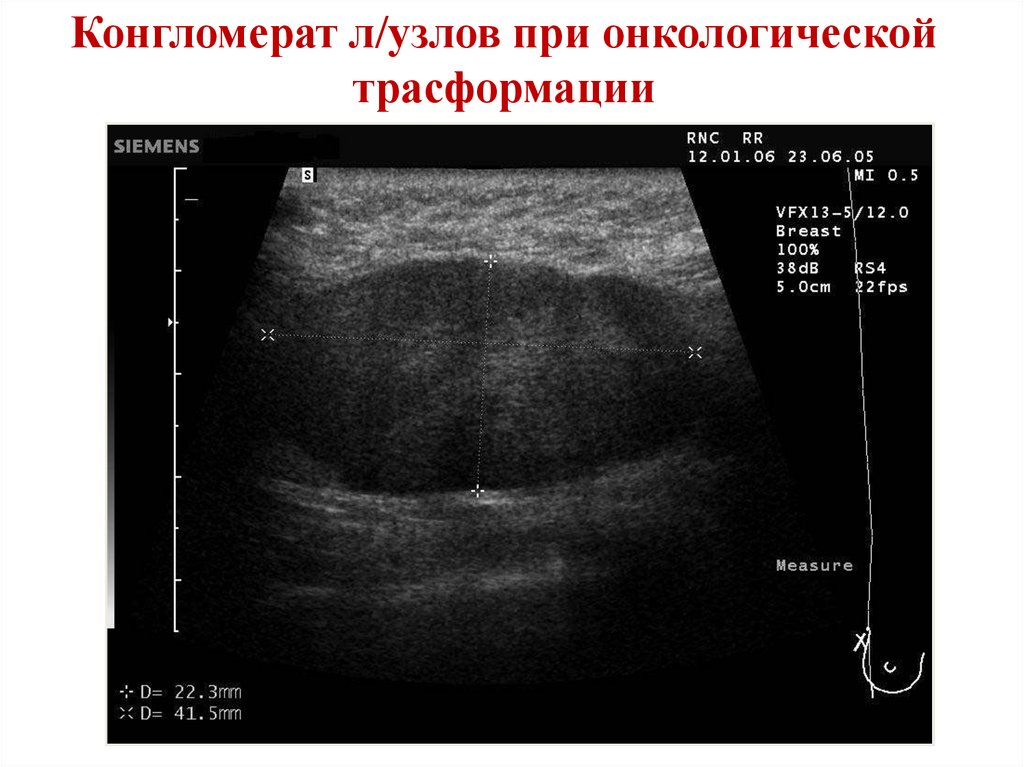
26.
Конгломерат л/узлов при онкологическойтрасформации
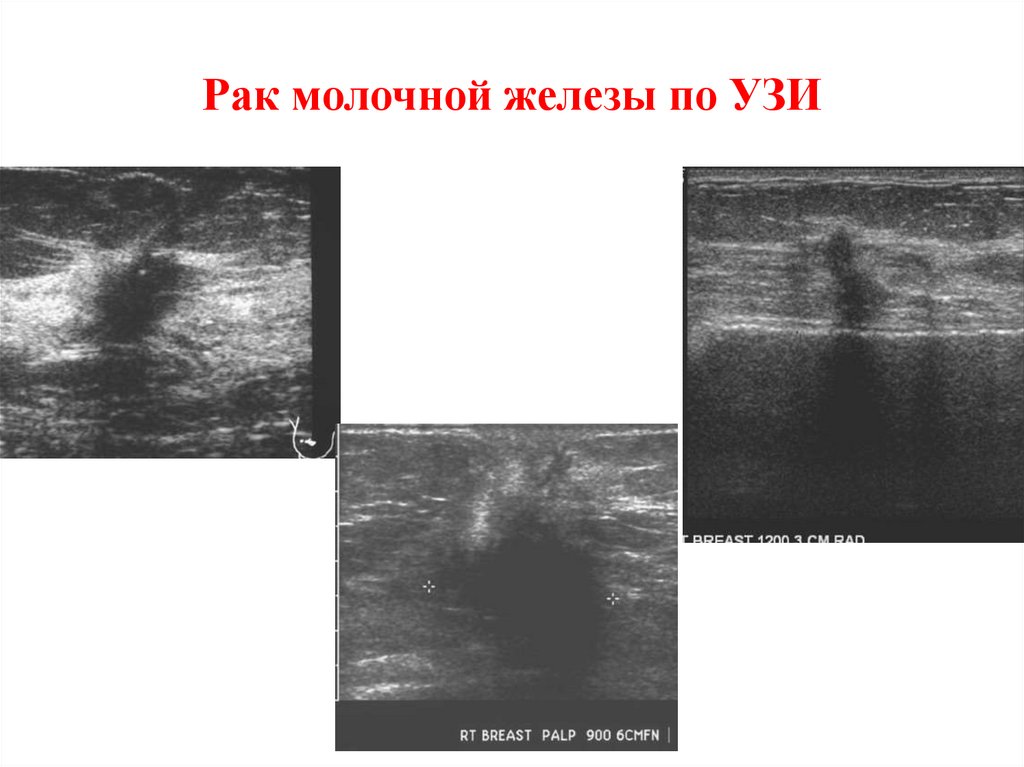
27. Рак молочной железы по УЗИ
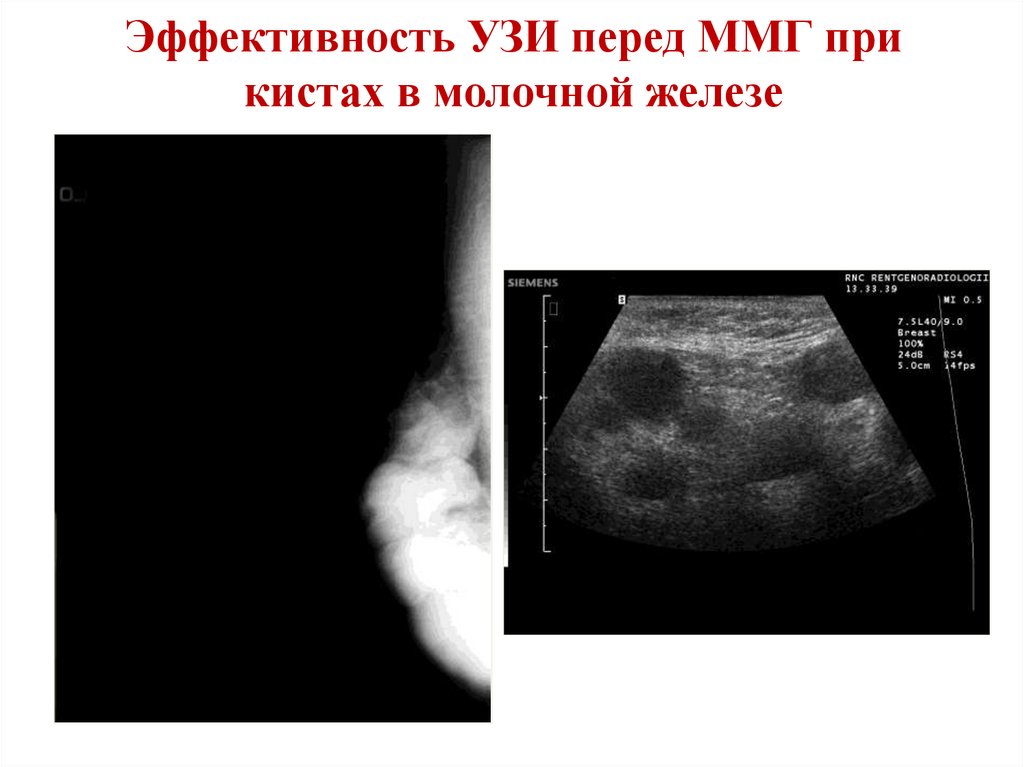
28. Эффективность УЗИ перед ММГ при кистах в молочной железе
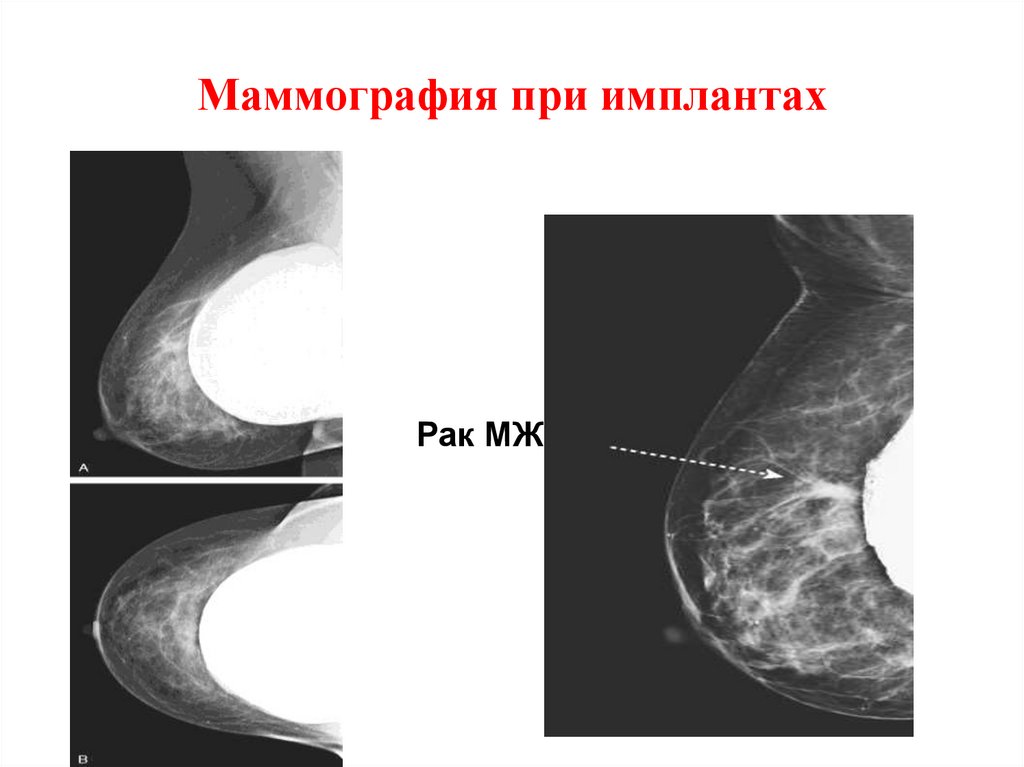
29. Маммография при имплантах
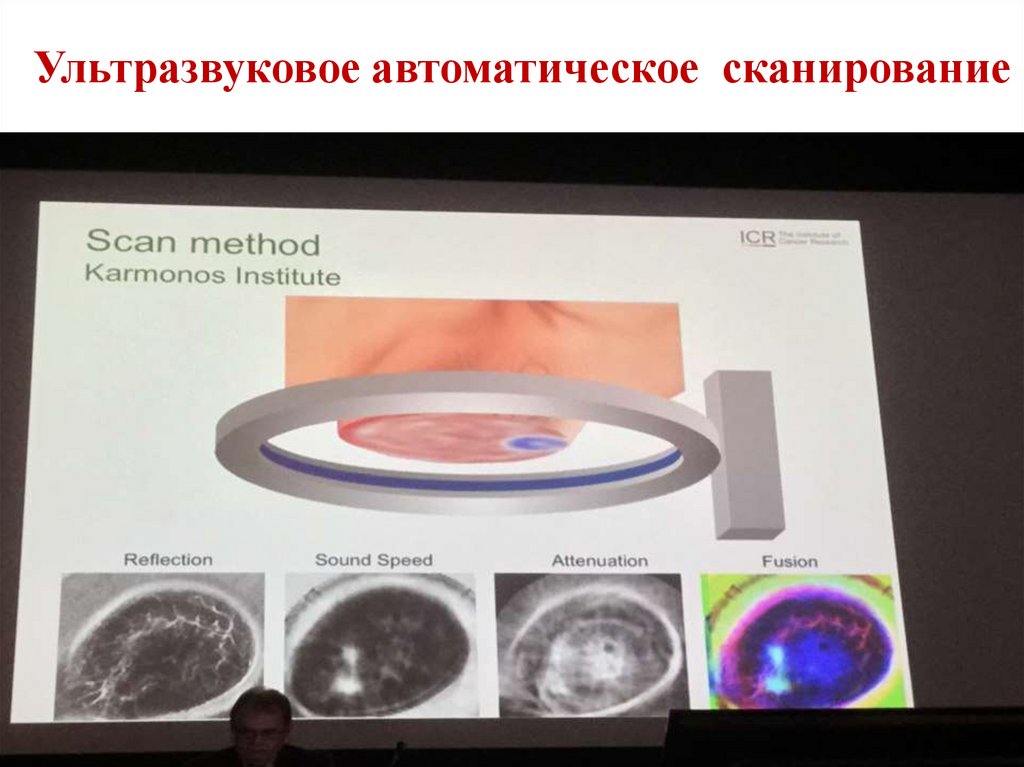
Рак МЖ30. Ультразвуковое автоматическое сканирование
31. Маммография
Маммография – основной метод ранней диагностикимолочных
желез.
Чувствительность
маммографии
составляет 73-95%, специфичность 94-97%.
Маммография
выполняется
в
первой
фазе
менструального цикла с 6 по 12 день менструального
цикла.
Если речь идет о подозрении на рак молочной железы,
исследование проводится независимо от дня цикла.
Всем женщинам в возрасте от 30 до 50лет рекомендовано
проведение маммографии один раз в два года, а в возрасте
старше 50 лет – ежегодно. Женщинам, относящимся к
группам риска, рекомендована ежегодная маммография
NB!!!
До 30 лет маммография не разрешена (ВОЗ).
32.
Рак в виде узлаРентгенологические признаки:
• симптом лучистости
• радиарное расположение лучей
• преобладание солидных участков
в опухоли обусловливает полицикличность
контуров.
• нечеткость контуров (если размер образования
>1см),
• скоплением микрокальцинатов в центре и по
периферии узла
• отсутствие грубой тяжистости по краям узла,
• структура новообразования - неоднородная
33. Рак в виде узла
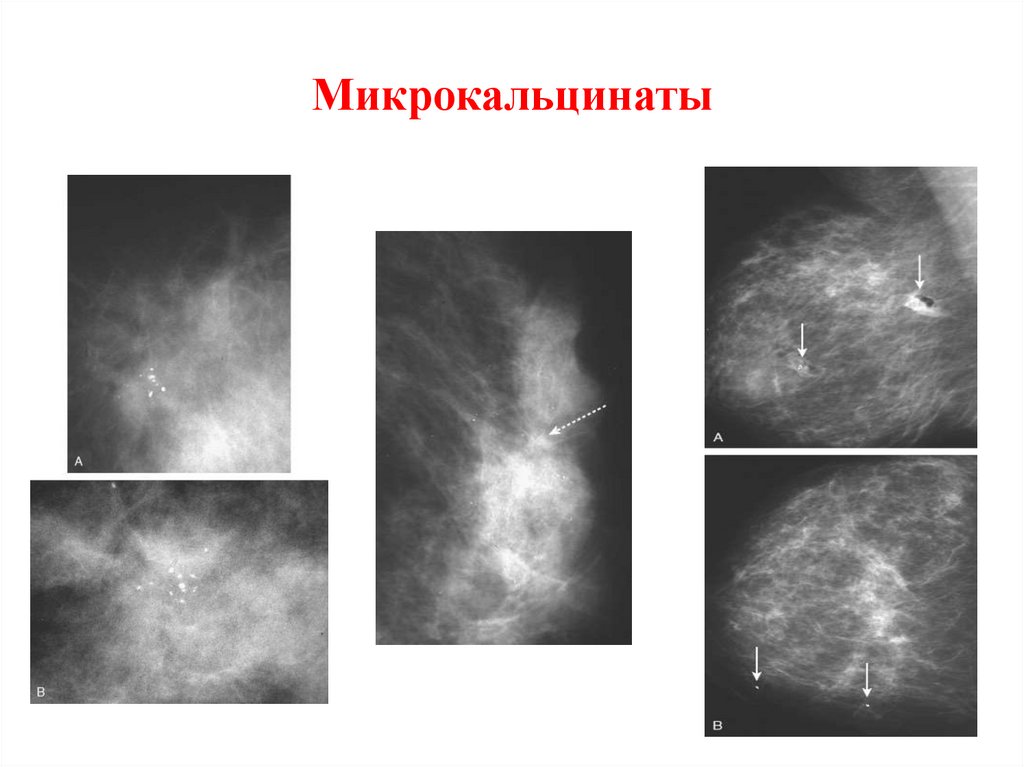
34. Микрокальцинаты
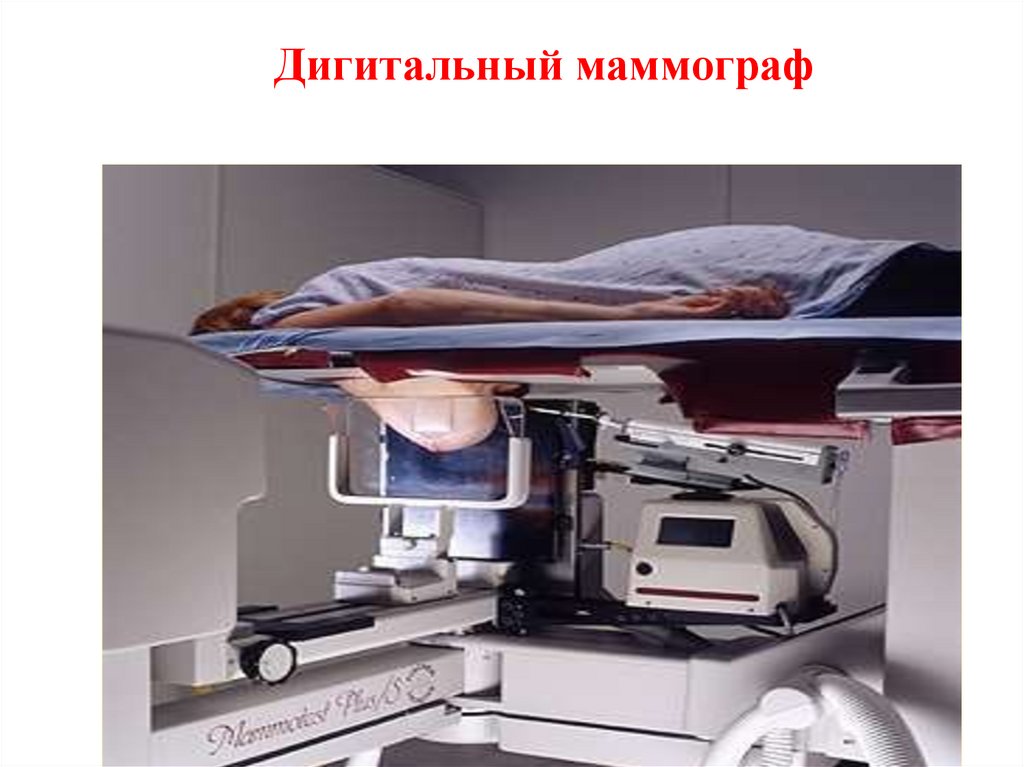
35.
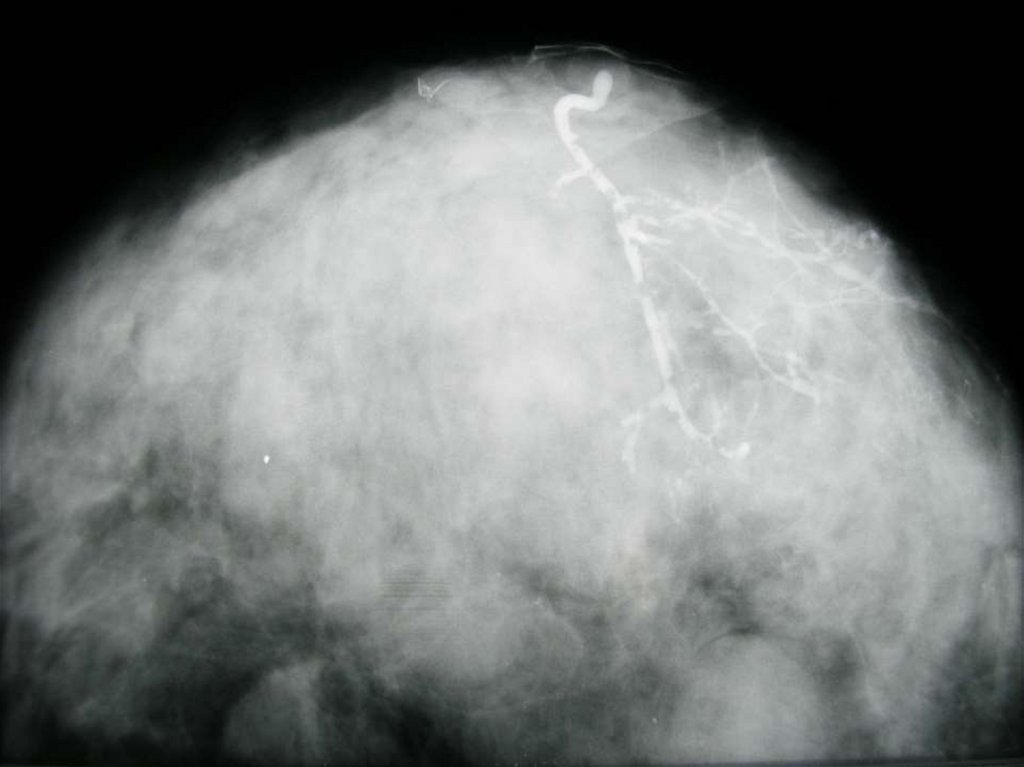
Дигитальный маммограф36. Дуктография (анат. ductus проток + греч. grapho писать, изображать) - рентгенография протоков каких-либо органов
(преимущественно желез)после введения в них контрастных веществ, син.
галактофорография (галакто- + греч. рhorosнесущий + grapho- писать)
37.
38.
39.
40.
41.
42.
43.
44.
45.
46.
47.
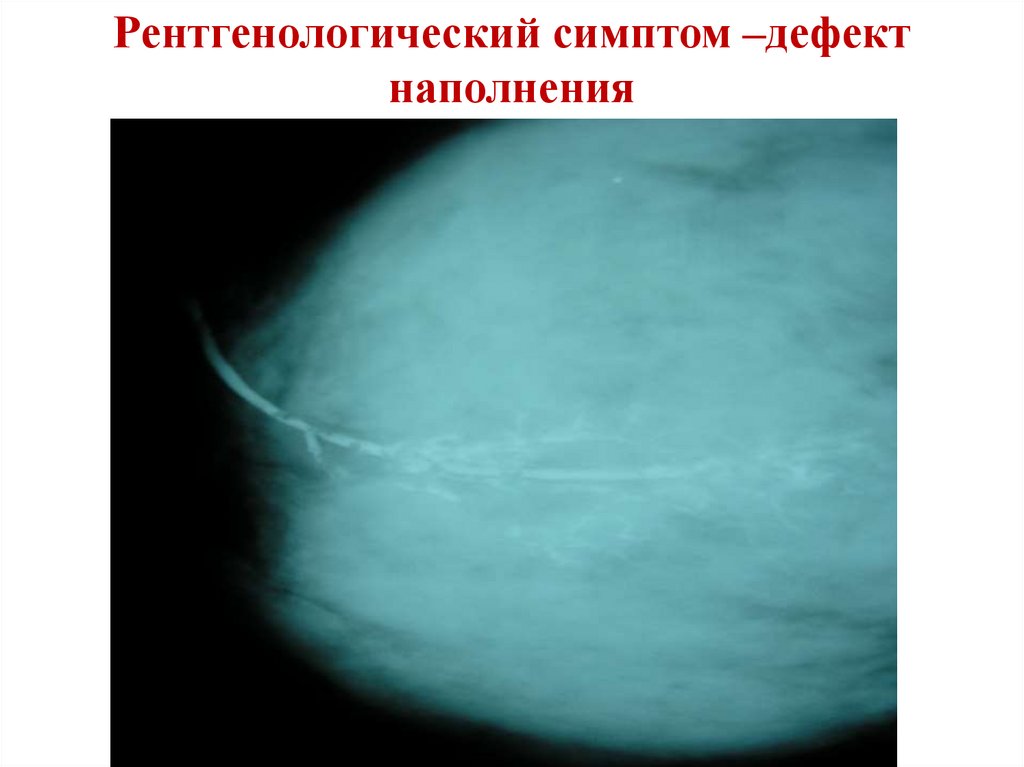
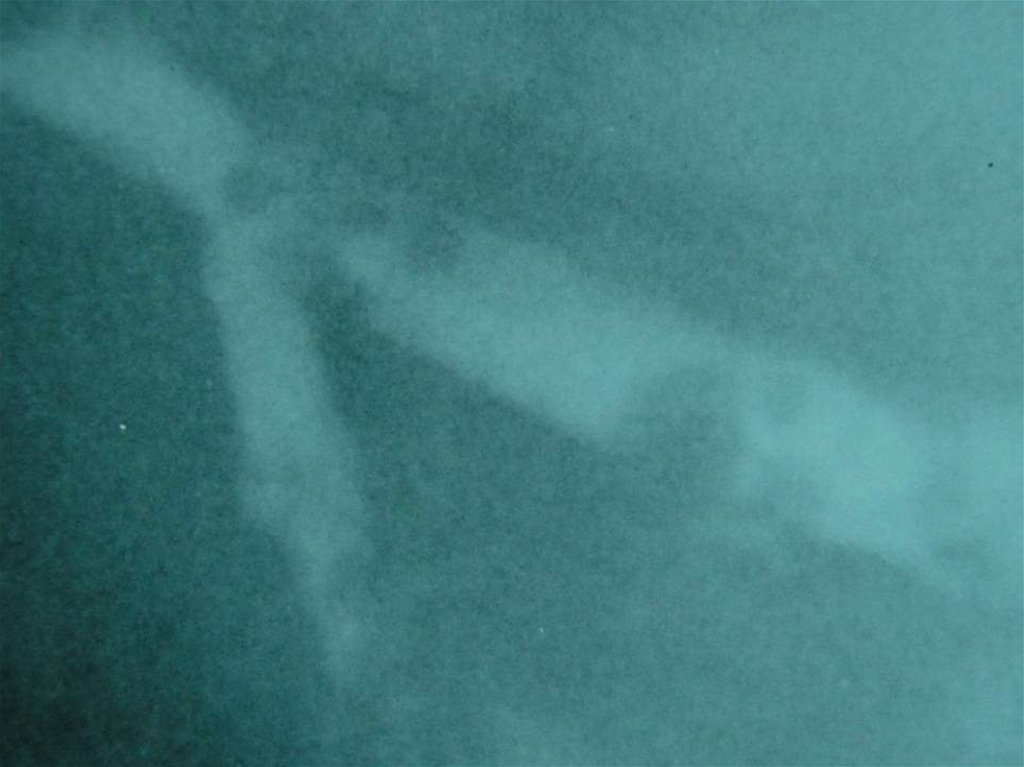
Рентгенологический симптом –дефектнаполнения
48.
49. Показания к выполнению МРТ молочных желез:
1. Возраст до 30 лет2. Наличие мутаций в генах BRCA1, BRCA2, CHECK, NBS1, tP53
3. Высокая рентгенологическая плотность молочных желез
4. Наличие имплантатов молочных желез при невозможности
выполнения
качественного маммографического исследования
5. Признаки или подозрение на мультицентричный РМЖ
6. Оккультный РМЖ: метастазы РМЖ в аксиллярные лимфоузлы
без выявленного
первичного очага
7. Первичная отечно-инфильтративная форма РМЖ
8. Внутрипротоковый РМЖ.
http://www.abvpress.ru/project/www.abvpress.ru/KR_ROOM_2020.pdf
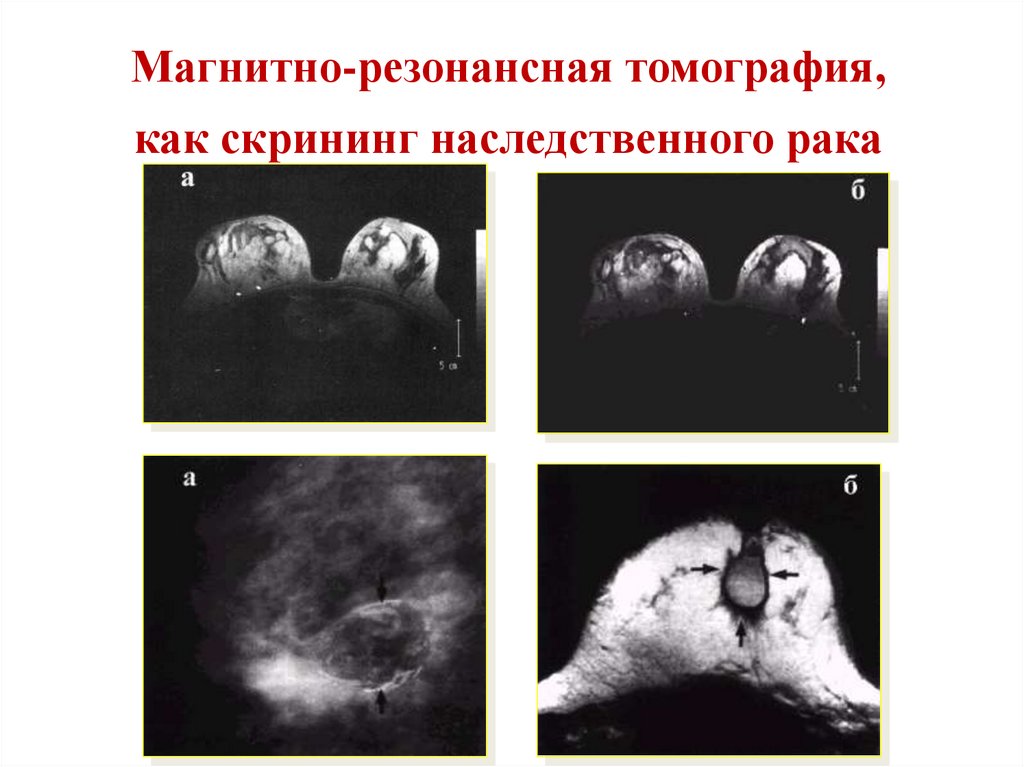
50.
Магнитно-резонансная томография,как скрининг наследственного рака
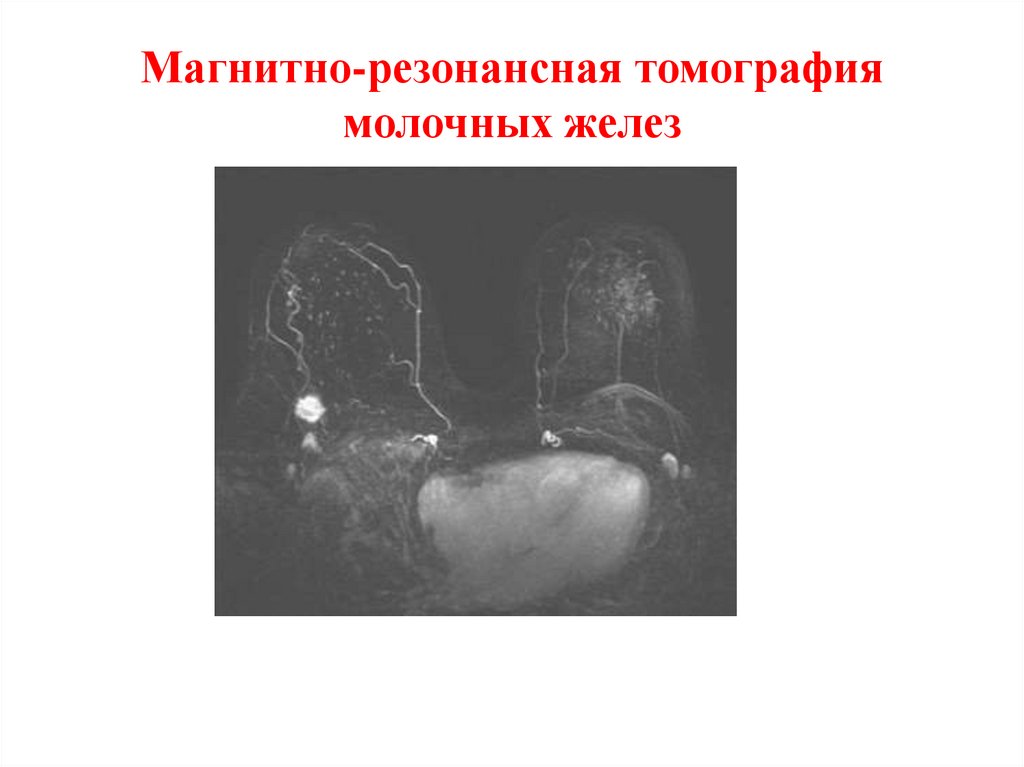
51. Магнитно-резонансная томография молочных желез
52.
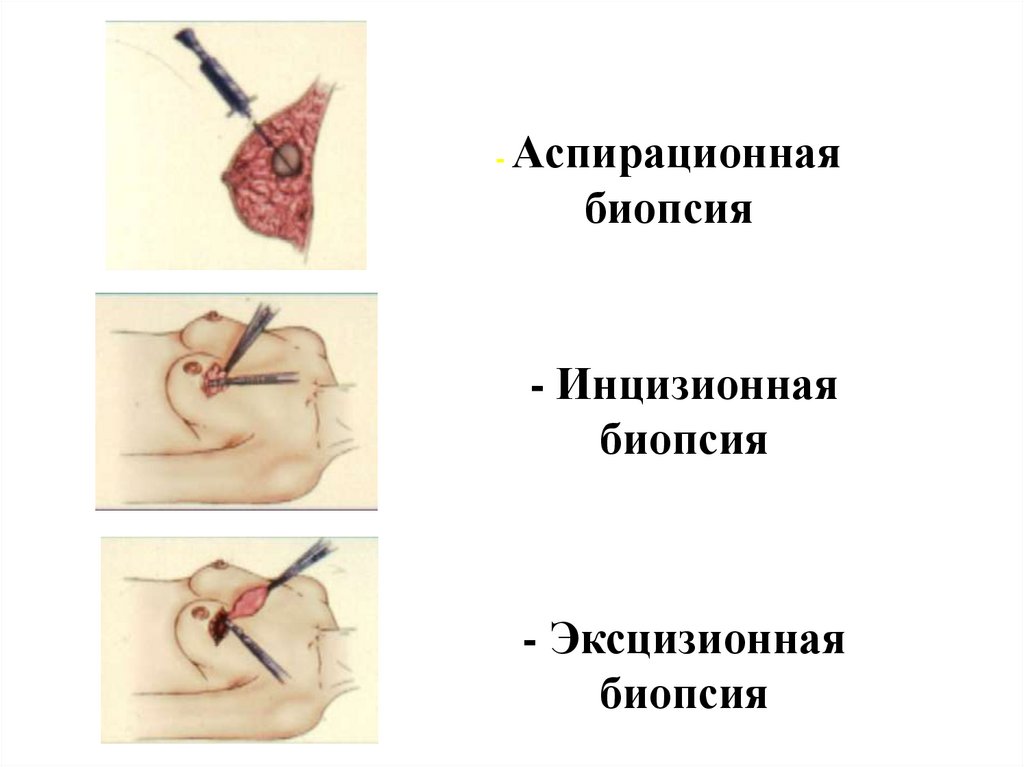
- Аспирационнаябиопсия
- Инцизионная
биопсия
- Эксцизионная
биопсия
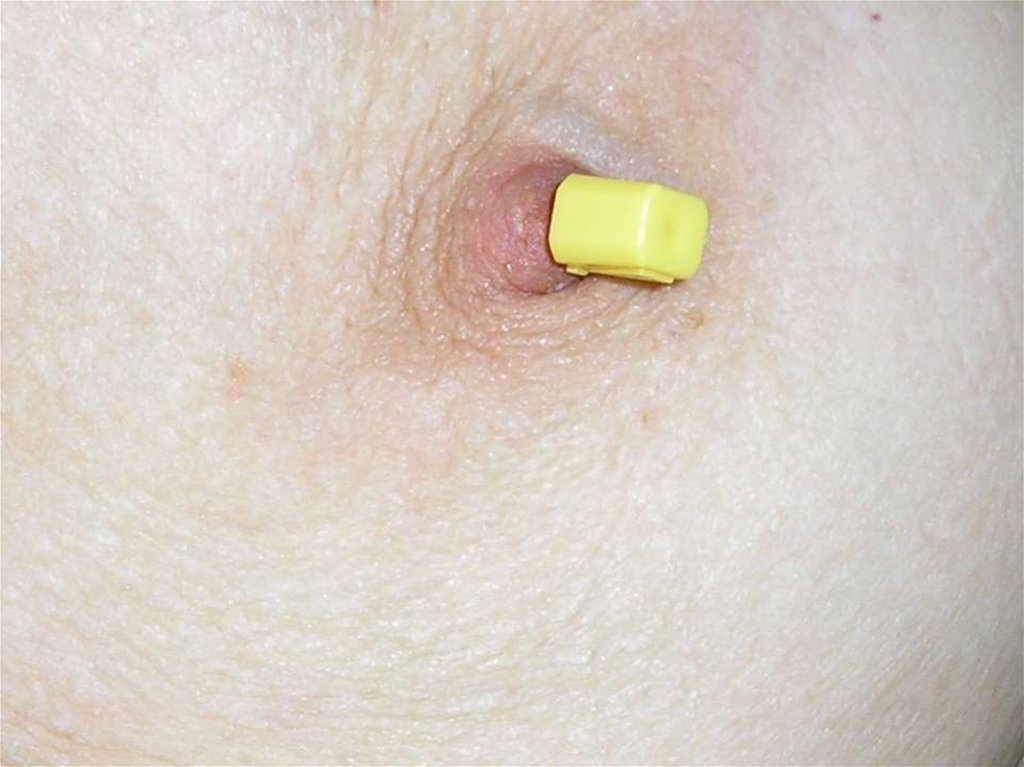
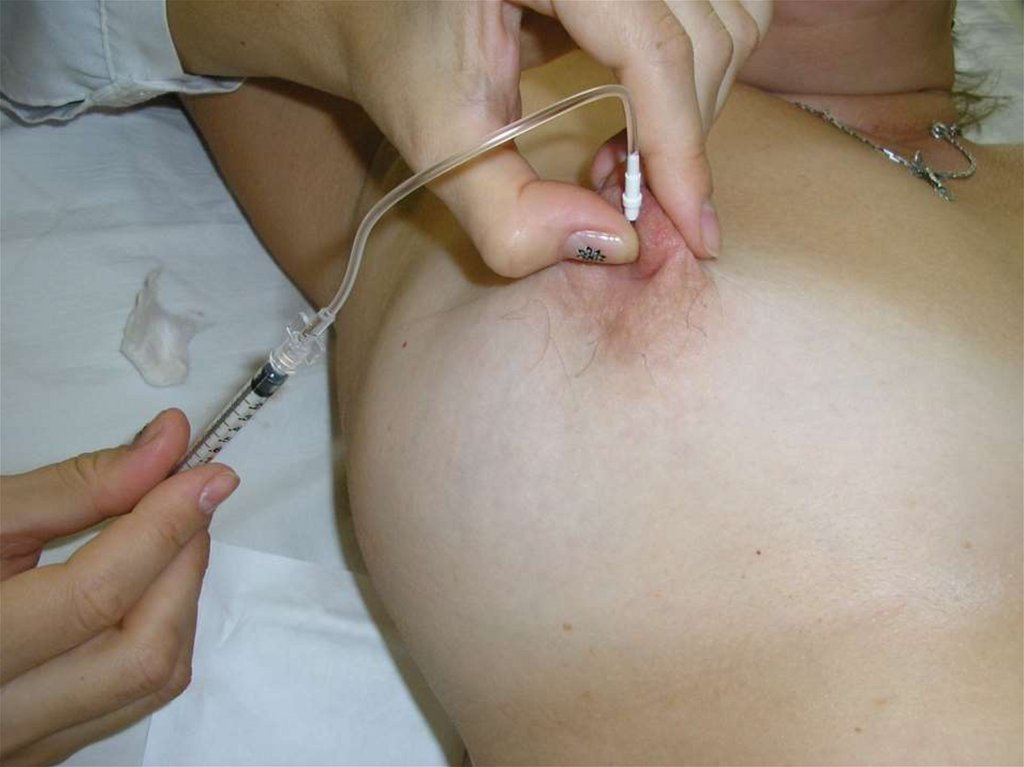
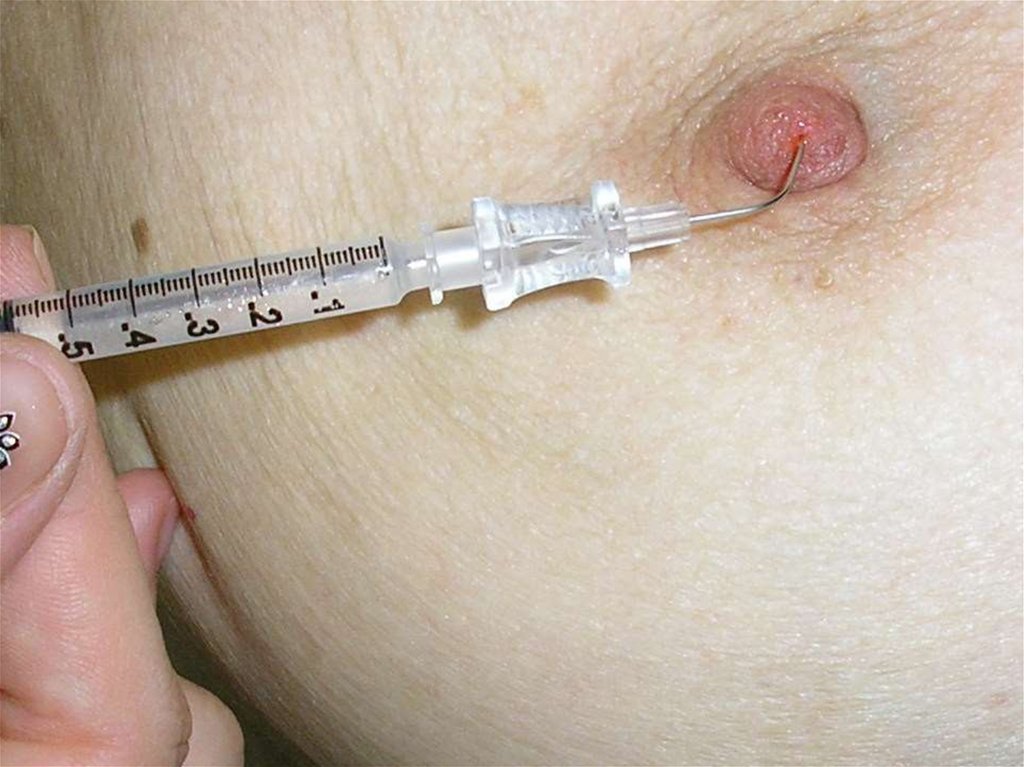
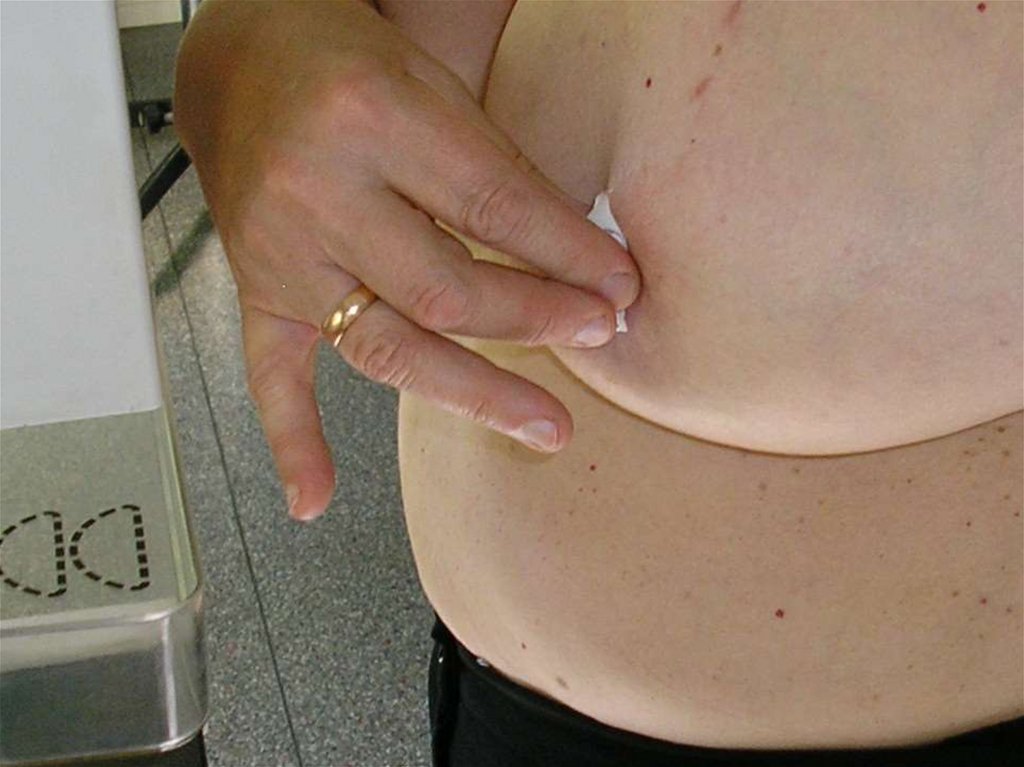
53.
Техника проведения тонкоигольнойаспирационной биопсии
54. Цитологическое исследование
55.
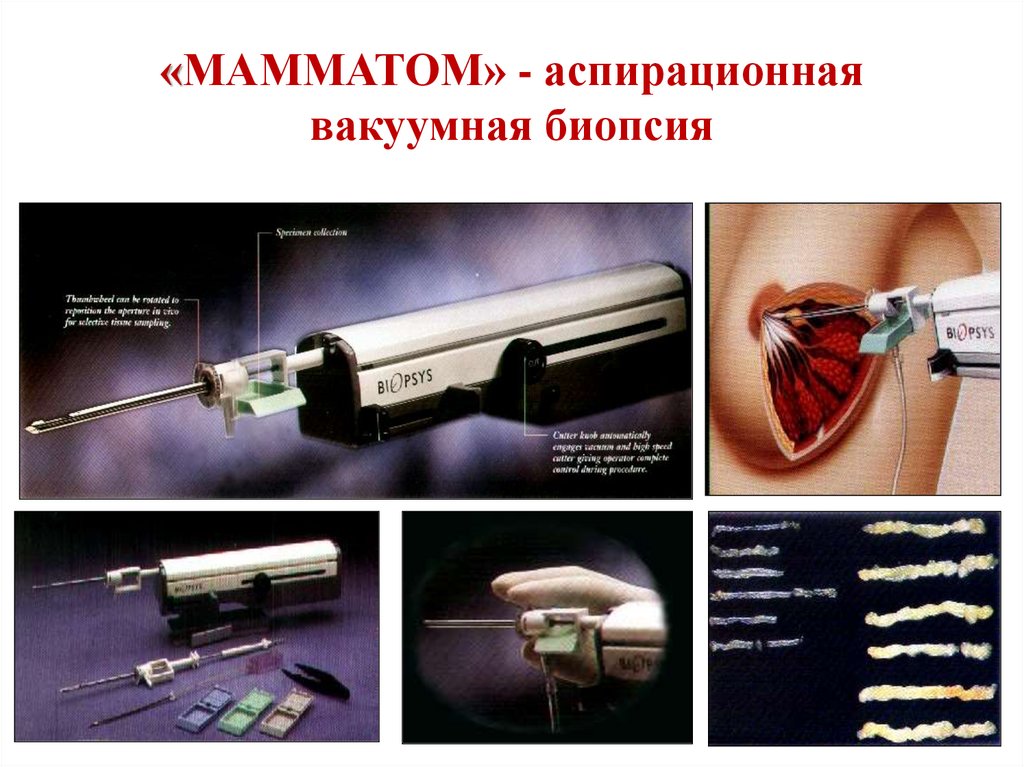
«МАММАТОМ» - аспирационнаявакуумная биопсия
56.
Высокая диагностическая точность благодарябольшему размеру образцов
Размеры игл 12G, 10G и 7G
Вес образцов до 130 мг
позволяет проводить более
точную диагностику
заболеваний молочной железы
57.
При исследовании биопсийногоматериала в заключении должны быть
указаны:
• гистологический вариант,
• степень дифференцировки опухоли,
• результаты
суррогатного
иммуногистохимического
определения РЭ/РП, HER2 и Ki67.
58.
При оценке уровня экспрессии РЭ/РП следует использовать 8-ибалльную шкалу Allred Scoring Guideline.
Расчетный интегративный показатель позволяет определить
исследуемый случай в одну из четырех основных групп: в группу
с уровнем экспрессии 0 баллов (полное отсутствие окрашенных
ядер, индекс = 0),
группу со слабым уровнем окраски (индекс от 2 до 4 баллов),
группу со средним уровнем экспрессии (индекс от 5 до 6 баллов),
группу с высоким уровнем экспрессии (индекс составляет от 7 до
8 баллов).
Указывается
также
процент
опухолевых
клеток,
экспрессирующих РЭ/РП.
Положительной реакция считается при ER и/или PR –
позитивные ≥ 1%, однако по рекомендациям значения ER между
1% и 9% следует расценивать как сомнительные (Консенсус СанГаллена, 2017).
59.
При определении одной из 4 категорий уровнейэкспрессии HER2 (0, 1+, 2+, 3+) следует
руководствоваться обновленными рекомендациями
АSCO/CAP, 2013.
HER2–статус, оцененный как 0 и 1+, следует считать
негативным,
оцененный как 3+ является позитивным,
при
неопределенном
уровне
HER2
статуса
(оцененный как 2+) следует дополнительно провести
молекулярно-генетическое исследование методом in
situ гибридизации (FISH, CISH, SISH HER2), для
установления наличия или отсутствия в клетках
амплификации гена HER2.
Наличие амплификации позволяет говорить о
позитивном HER2 статусе опухоли.
60.
Экспрессия Ki67 оценивается в инвазивном компоненте напериферии роста опухоли.
В каждом случае должно исследоваться не менее 500 опухолевых
клеток. При наличии, так называемых, «горячих точек
пролиферации» их дополнительно включают в обсчет (например: 5
полей + одна «горячая точка»). Оценивается только ядерное
окрашивание, учитываются все окрашенные ядра опухолевых
клеток независимо от интенсивности окраски. Оценка Ki67 должна
интерпретироваться с учётом особенностей местных лабораторных
показателей (например, если в лаборатории среднее значение Ki67
при гормонрецептор-положительном РМЖ равняется 20%, значение
в 30% или выше может считаться высоким, а 10% или менее –
низким (Консенсус Сан-Галлена, 2017).
Молекулярно-генетические исследования должны проводиться в
сертифицированных
лабораториях
с
подтвержденной
квалификацией.
61.
• У пациенток с метастатическим ТН РМЖ, неполучавших лечение по поводу метастатической
болезни, рекомендовано определение теста
Ventana SP 142 уровня экспрессии PD-L1 на
иммунокомпетентных клетках.
• У пациенток с первично метастатическим
HER+HER2- РМЖ или при прогрессировании
болезни рекомендовано определение наличие
мутаций гена PIK3CA
• В
отдельных
случаях
определяют
–
микросателлитную нестабильность опухоли(MSI)
и мутацию в генах NTRK1, NTRK2, NTRK3
62. КЛИНИКО-АНАТОМИЧЕСКАЯ КЛАССИФИКАЦИЯ РМЖ
Узловая формаДиффузная форма:
а) Отечно-инфильтративная
б) Маститоподобная
в) Рожистоподобная
г)Панцирная.
Редкие формы:
а) Рак Педжета
б) Атипичные и др. формы
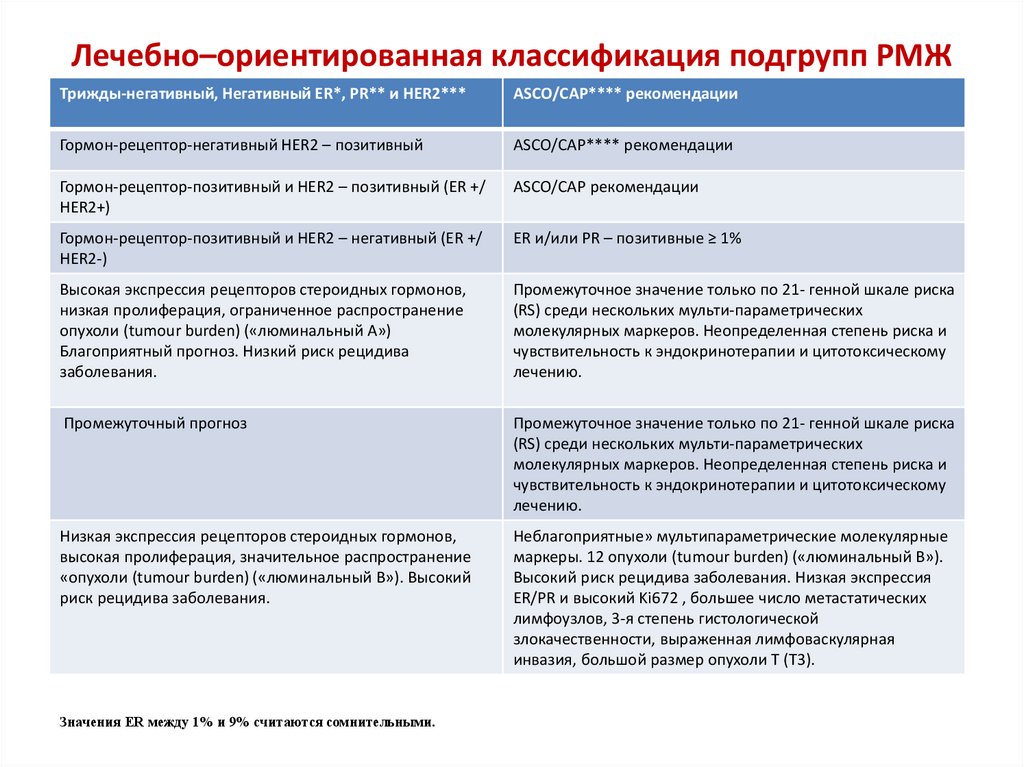
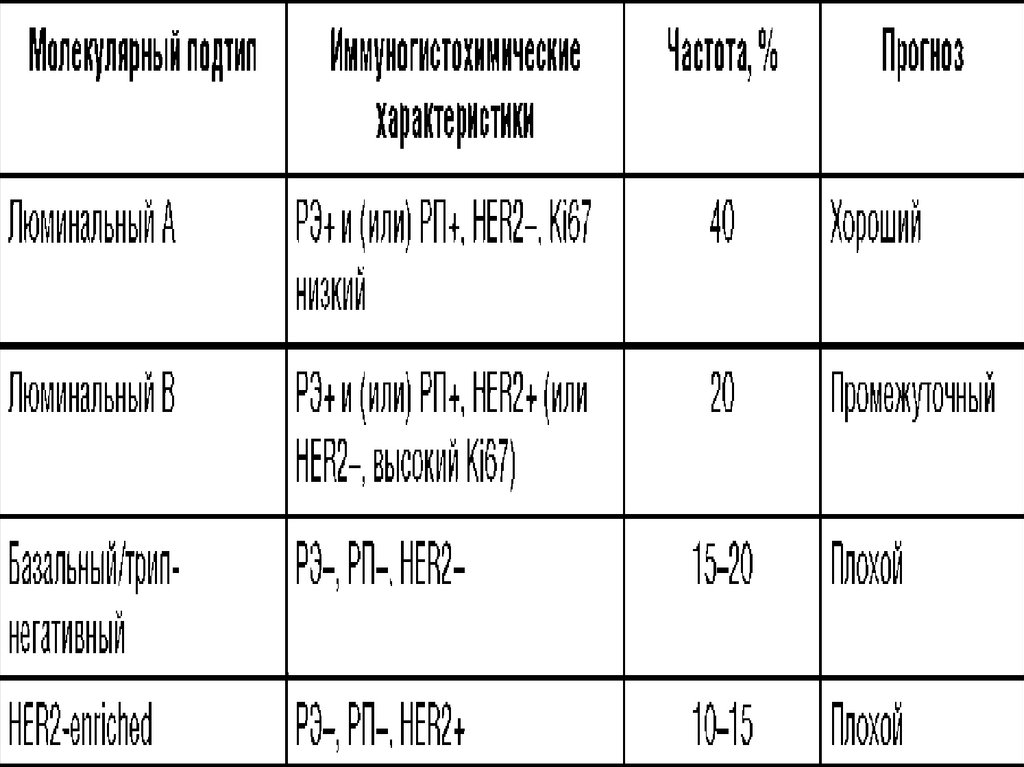
63. Лечебно–ориентированная классификация подгрупп РМЖ
Трижды-негативный, Негативный ER*, PR** и HER2***ASCO/CAP**** рекомендации
Гормон-рецептор-негативный HER2 – позитивный
ASCO/CAP**** рекомендации
Гормон-рецептор-позитивный и HER2 – позитивный (ER +/
HER2+)
ASCO/CAP рекомендации
Гормон-рецептор-позитивный и HER2 – негативный (ER +/
HER2-)
ER и/или PR – позитивные ≥ 1%
Высокая экспрессия рецепторов стероидных гормонов,
низкая пролиферация, ограниченное распространение
опухоли (tumour burden) («люминальный А»)
Благоприятный прогноз. Низкий риск рецидива
заболевания.
Промежуточное значение только по 21- генной шкале риска
(RS) среди нескольких мульти-параметрических
молекулярных маркеров. Неопределенная степень риска и
чувствительность к эндокринотерапии и цитотоксическому
лечению.
Промежуточный прогноз
Промежуточное значение только по 21- генной шкале риска
(RS) среди нескольких мульти-параметрических
молекулярных маркеров. Неопределенная степень риска и
чувствительность к эндокринотерапии и цитотоксическому
лечению.
Низкая экспрессия рецепторов стероидных гормонов,
высокая пролиферация, значительное распространение
«опухоли (tumour burden) («люминальный В»). Высокий
риск рецидива заболевания.
Неблагоприятные» мультипараметрические молекулярные
маркеры. 12 опухоли (tumour burden) («люминальный В»).
Высокий риск рецидива заболевания. Низкая экспрессия
ER/PR и высокий Ki672 , большее число метастатических
лимфоузлов, 3-я степень гистологической
злокачественности, выраженная лимфоваскулярная
инвазия, большой размер опухоли Т (Т3).
Значения ER между 1% и 9% считаются сомнительными.
64. Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической
классификации болезней и проблем,связанных со здоровьем
Злокачественное новообразование молочной железы (С50):
C50.0 – соска и ареолы
C50.1 – центральной части молочной железы
C50.2 – верхневнутреннего квадранта молочной железы
C50.3 – нижневнутреннего квадранта молочной железы
C50.4 – верхненаружного квадранта молочной железы
C50.5 – нижненаружного квадранта молочной железы
C50.6 – подмышечной задней части молочной железы
C50.8 – поражение молочной железы, выходящее за пределы одной и
более вышеуказанных локализаций
• C50.9 – молочной железы неуточненной части
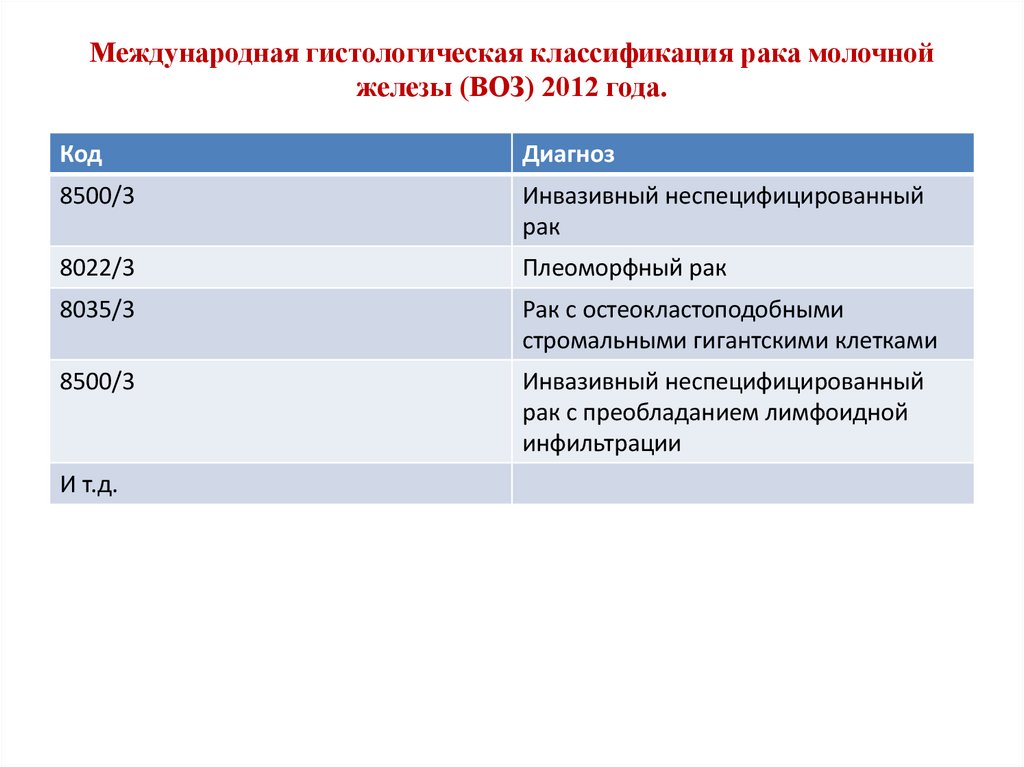
65. Международная гистологическая классификация рака молочной железы (ВОЗ) 2012 года.
КодДиагноз
8500/3
Инвазивный неспецифицированный
рак
8022/3
Плеоморфный рак
8035/3
Рак с остеокластоподобными
стромальными гигантскими клетками
8500/3
Инвазивный неспецифицированный
рак с преобладанием лимфоидной
инфильтрации
И т.д.
66. Стадирование РМЖ
• Для стадирования РМЖ следует использоватьTNM-8
классификацию
Союза
по
международному противораковому контролю
(Union for International Cancer Control, UICC).
• Выделяют клиническую и патоморфологическую
стадии РМЖ, которые могут существенно
различаться.
• Клиническое стадирование осуществляют на
основании
результатов
клинического
обследования, патоморфологическое – на
основании
заключения
морфолога
после
операции.
67. Т
Т – первичная опухоль;
Тх – недостаточно данных для оценки опухоли;
T0 – нет признаков первичной опухоли;
Тis (DCIS) – протоковый рак in situ;
Тis (Paget) – рак Педжета (соска) без признаков опухоли (при наличии опухоли оценку проводят по ее размеру);
Т1mic – микроинвазия[1] ≤0,1 см в наибольшем измерении
. Примечание:
Т1а – опухоль >1 мм, но ≤5 мм в наибольшем измерении;
Т1б – опухоль >5 мм, но ≤10 мм в наибольшем измерении;
Т1с – опухоль >10 мм, но ≤20 мм в наибольшем измерении;
Т2 – опухоль >20 мм, но ≤50 мм в наибольшем измерении;
ТЗ – опухоль >50 мм в наибольшем измерении;
Т4 – опухоль любого размера с прямым распространением на грудную стенку[2] и/или кожу;
Т4а – прорастание грудной стенки, исключая инвазию только в грудные мышцы;
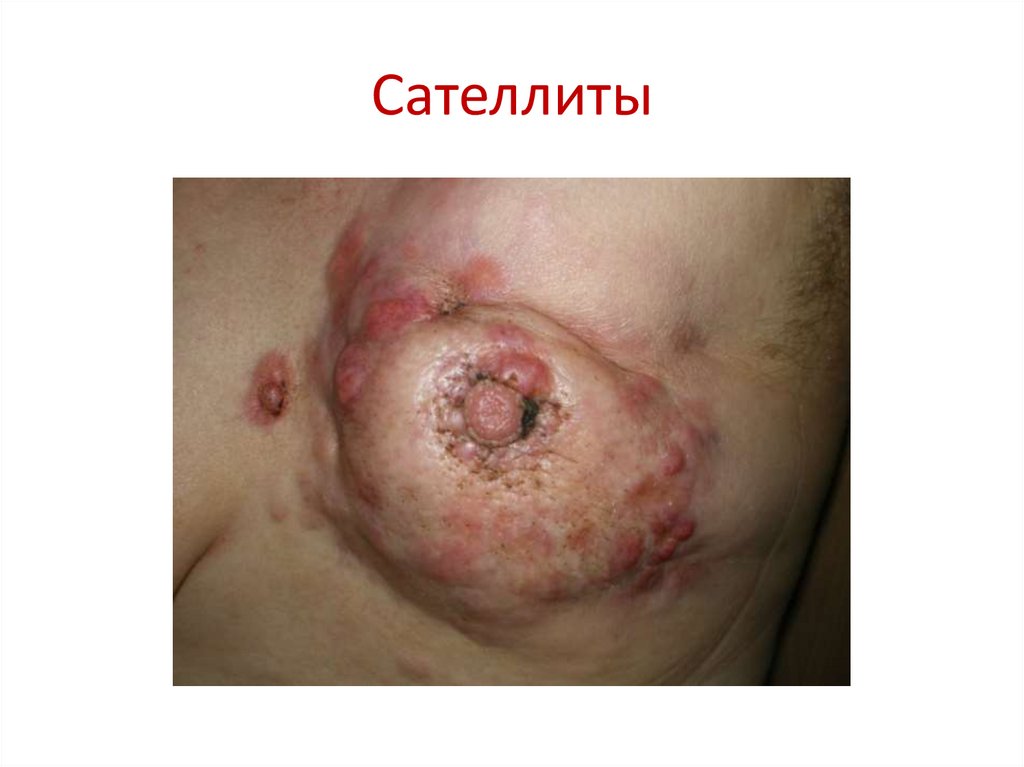
Т4б – отек (включая «апельсиновую корочку») или изъязвление кожи молочной железы либо сателлиты в коже железы;
Т4с – признаки, перечисленные в пунктахТ4а и Т4б;
Т4d – воспалительный (отечный) рак[3];
68. N
Nх – недостаточно данных для оценки поражения регионарных лимфатических узлов;
N0 – нет признаков поражения метастазами регионарных лимфатических узлов;
N1 – метастазы в смещаемых подмышечных лимфатических узлах (на стороне поражения);
N2 – метастазы в подмышечных лимфатических узлах на стороне поражения, спаянные между собой или
фиксированные, либо клинически определяемые метастазы во внутренних маммарных (парастернальных)
лимфатических узлах при отсутствии клинически явного поражения подмышечных лимфатических узлов;
N2а – метастазы в подмышечных лимфатических узлах на стороне поражения, спаянные между собой или
фиксированные;
N2b – клинически определяемые метастазы во внутренних маммарных (парастернальных) лимфатических узлах
при отсутствии клинически явного поражения подмышечных лимфатических узлов;
N3 – метастазы в подключичных лимфатических узлах на стороне поражения, либо клинически определяемые
метастазы во внутренних маммарных (парастернальных) лимфатических узлах при наличии клинически явного
поражения подмышечных лимфатических узлов, либо метастазы в надключичных лимфатических узлах на
стороне поражения (независимо от состояния подмышечных и внутренних маммарных лимфатических узлов);
N3а – метастазы в подключичных лимфатических узлах на стороне поражения;
N3b – метастазы во внутренних маммарных (парастернальных) лимфатических узлах при наличии клинически
явного поражения подмышечных лимфатических узлов;
N3c – метастазы в надключичных лимфатических узлах на стороне поражения.
69. М – отдаленные метастазы
• М0 – нет признаков отдаленныхметастазов;
• М1 – имеются отдаленные метастазы
• легкое – pul, кости – oss, печень – hep,
плевра – ple, брюшина – per, костный мозг –
mar, головной мозг – bra, кожа – ski,
надпочечники – adr, лимфатические узлы –
lym, другие – оth.
70. G-степень дифференцировки ткани опухоли
• Gх – степень дифференцировки нельзя установить;• G1 – высокая степень дифференцировки ткани, 3–5 баллов по шкале
SBR[6];
• G2 – умеренная степень дифференцировки ткани, 6–7 баллов по
шкале SBR;
• G3 – низкая степень дифференцировки ткани, 8–9 баллов по шкале
SBR;
• G4 – недифференцированная опухоль;
71. Стадирование
ypT – состояние первичной опухоли после лекарственного лечения;
ypN – состояние регионарных лимфатических узлов после лекарственного
лечения;
ypN – после лечения должно быть оценено так же, как и до лечения
(клинически N).
Обозначение (sn) используют в том случае, если оценка «сторожевого» узла
была проведена после лечения. Если обозначение (sn) отсутствует, то
предполагают, что оценка подмышечных узлов была выполнена после их
диссекции.
Рубрикацию Х (ypNХ) нужно использовать, если не была выполнена оценка
ypN после лечения (sn) или диссекции подмышечных лимфатических узлов.
Категория N аналогична тем, которые используют для рN.
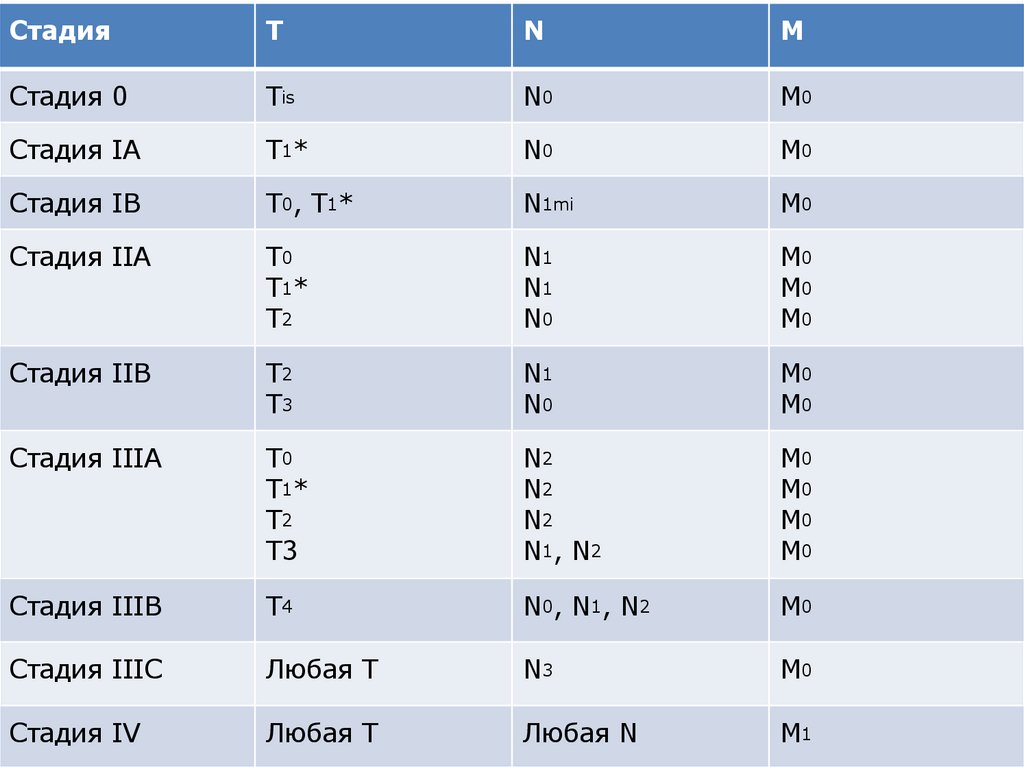
72.
СтадияT
N
M
Cтадия 0
Tis
N0
M0
Стадия IА
T1*
N0
M0
Стадия IВ
Т0, Т1*
N1mi
M0
Стадия IIА
T0
T1*
T2
N1
N1
N0
M0
M0
M0
Стадия IIВ
T2
T3
N1
N0
M0
M0
Стадия IIIА
T0
T1*
T2
T3
N2
N2
N2
N1, N2
M0
M0
M0
M0
Cтадия IIIВ
Т4
N0, N1, N2
M0
Cтадия IIIС
Любая Т
N3
M0
Стадия IV
Любая T
Любая N
M1
73. Стадирование
• Воспалительнаяформа
РМЖ
характеризуется
диффузным
утолщением кожи с плотными краями, обычно без подлежащей
пальпируемой массы. Если биопсия кожи отрицательна и нет
локализованной
опухолевой
массы,
при
патологической
классификации употребляют категорию рТх, а при клинической – Т4d.
При оценке категории рТ определяют инвазивный компонент.
Втяжение кожи, ретракция соска или другие кожные изменения, за
исключением относящихся к Т4б и Т4d, могут оцениваться как Т1, Т2 и
Т3, не влияя на стадирование.
• Индексы (sn) или (f) должны быть добавлены к категории N для
обозначения способа подтверждения метастатического поражения
лимфоузлов — с помощью БСЛУ (sn) или тонкогоигольной
аспирационной / core-биопсии (f) (без последующего удаления
лимфоузлов) соответственно
74.
Клиническая картина рака молочной железывключает
в
себя
как
симптомы,
обусловленные
локо-регионарными
изменениями (изменение размеров и формы
молочной железы, изменения кожи и
сосково-ареолярного комплекса), так и
симптомы, обусловленные генерализацией
процесса и наличием паранеопластических
синдромов.
75. К клиническим симптомам ранних форм относятся следующие:
• наличие опухолевого узла в ткани молочной железы;• плотная консистенция опухоли (опухоль может быть
деревянистой или даже каменистой плотности);
• ограниченная подвижность либо полное ее отсутствие; как
правило, безболезненность опухоли, наличие симптома
«умбиликации» – втяжения кожи над опухолью,
определяемого при сдвигании кожи;
• наличие
одиночного
плотного
подвижного
лимфатического узла в подмышечной области на стороне
опухоли, либо нескольких аналогичных лимфоузлов, не
спаянных между собой;
• возможны кровянистые выделения из соска, которые
встречаются лишь при внутрипротоковом раке и
внутрипротоковой папилломе.
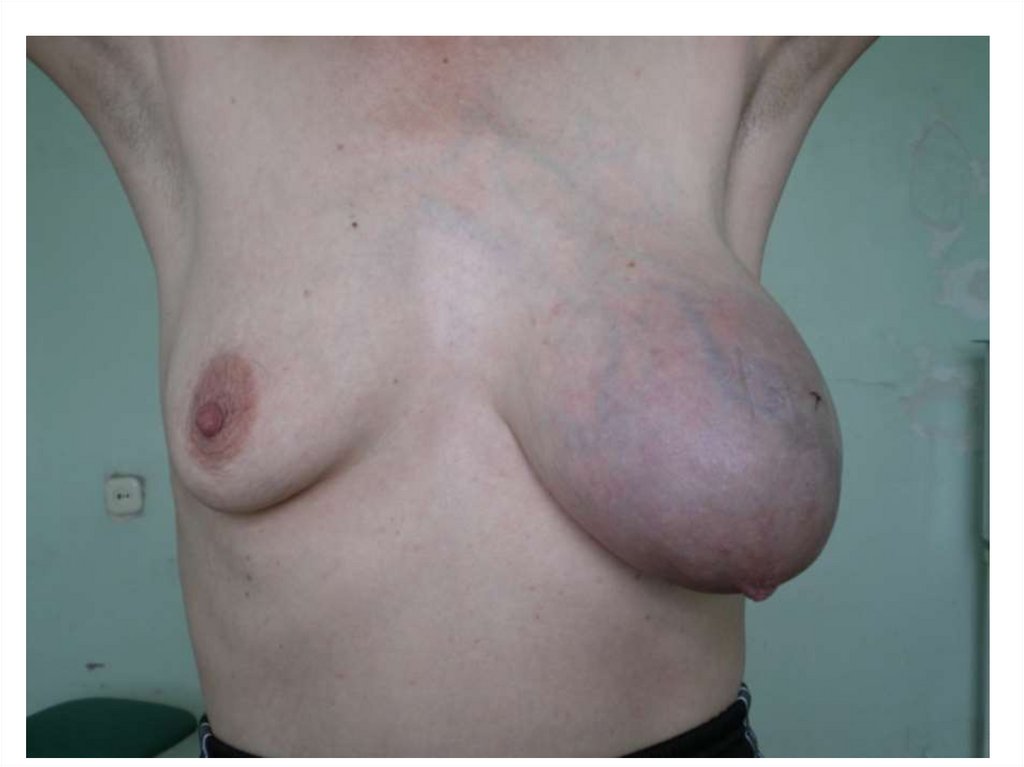
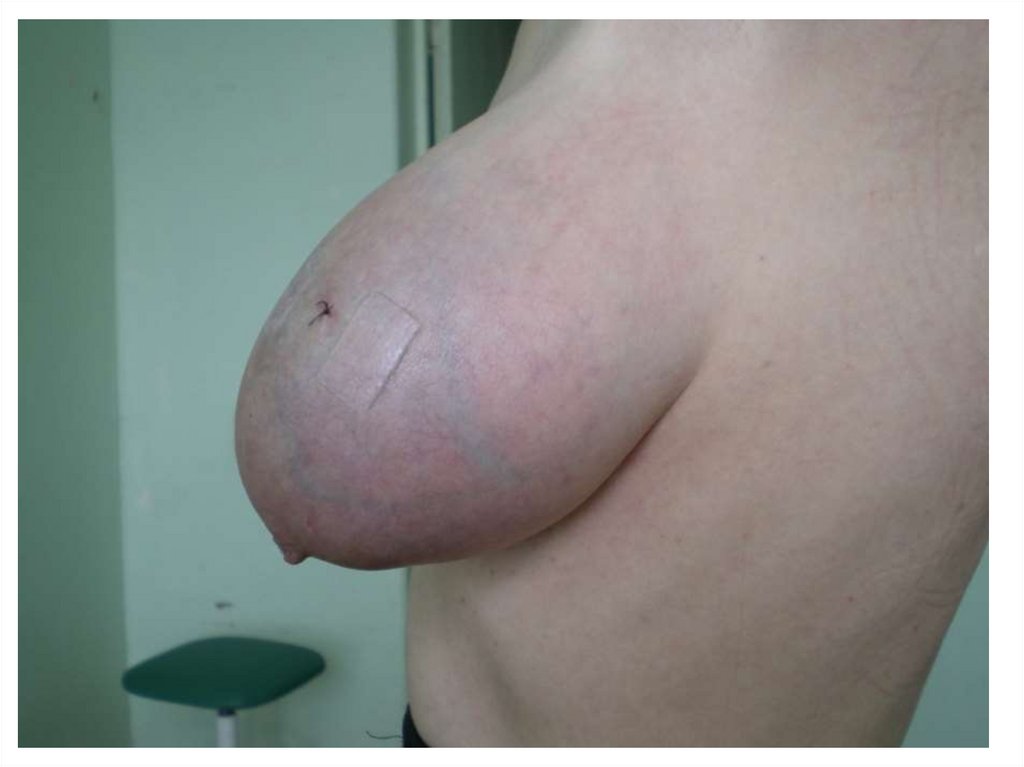
76. К симптомам, характерным для более распространенных форм опухоли, относятся:
заметная на глаз деформация кожи молочной железы над определяемой
опухолью (особенно при осмотре с поднятыми вверх руками);
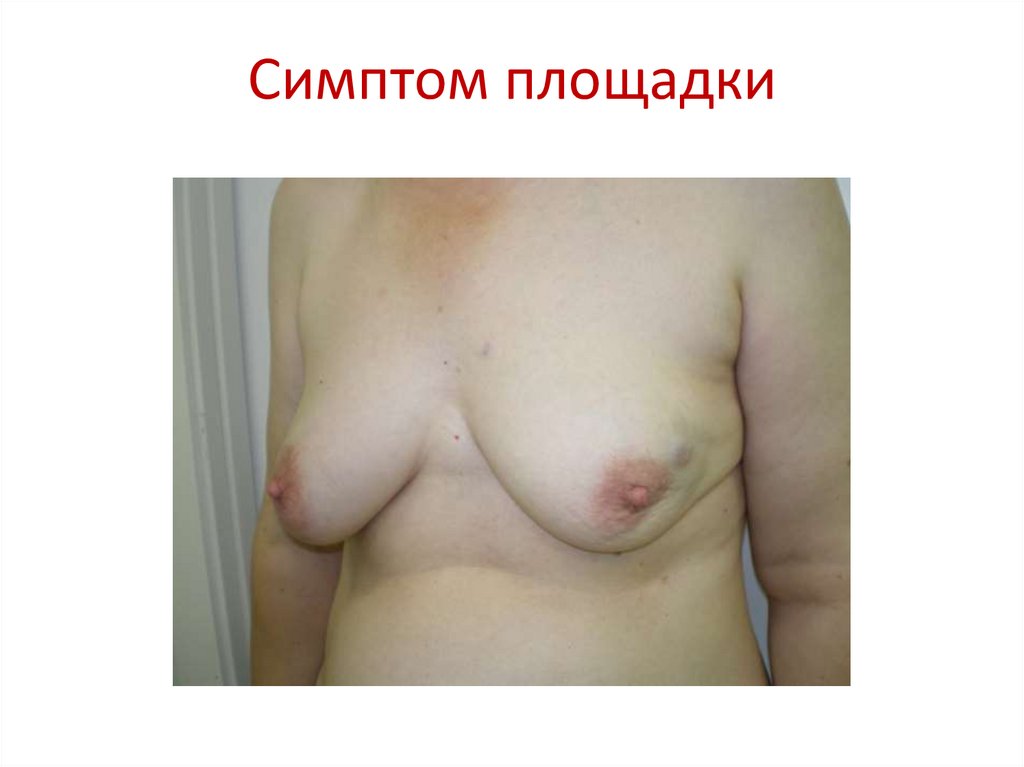
выраженный симптом «умбиликации» (втяжения) кожи над опухолью;
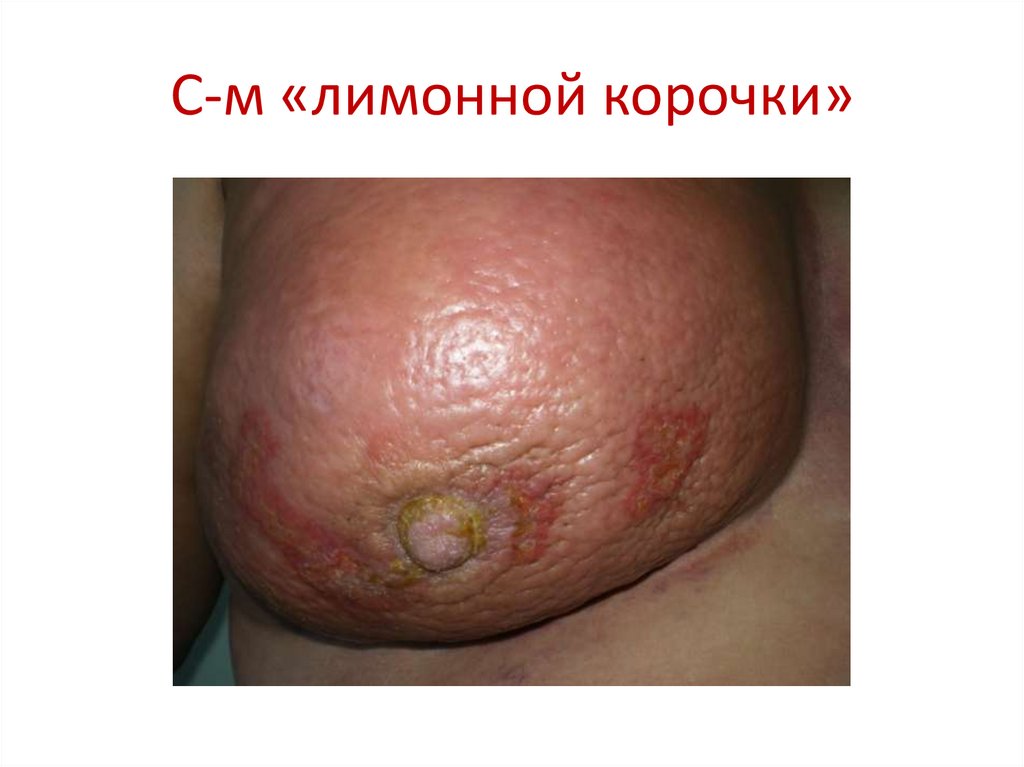
явления лимфостаза – симптом «лимонной корочки» над опухолью или за ее
пределами;
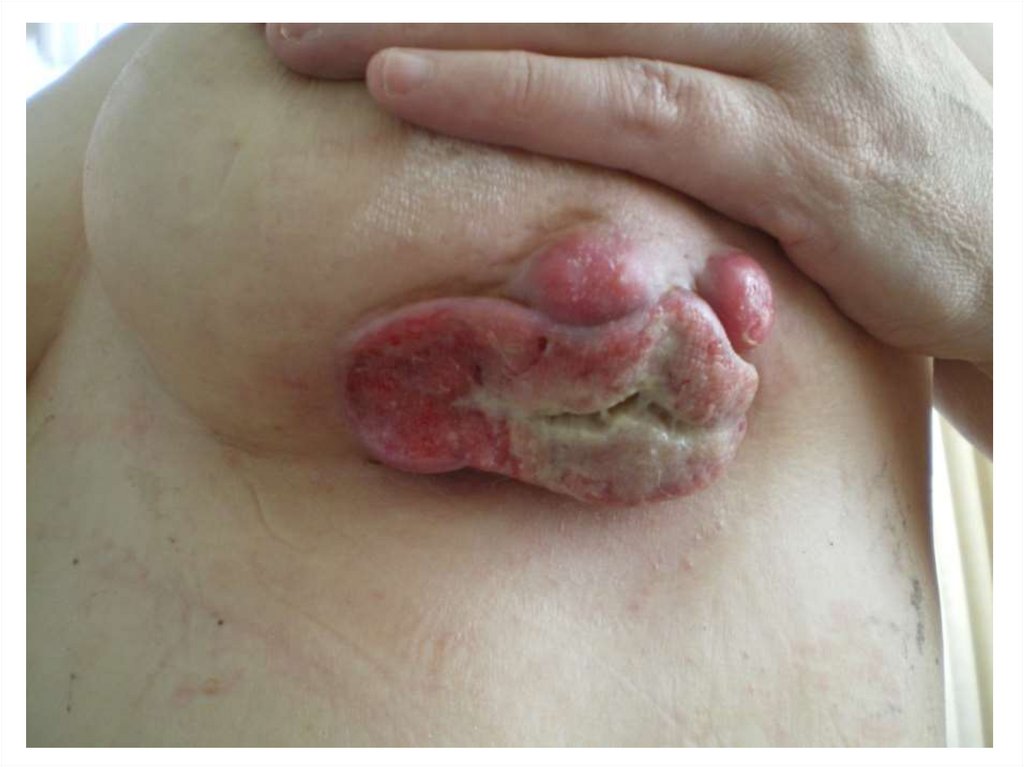
прорастание кожи опухолью и/или изъязвление опухоли;
выраженное утолщение соска и складки ареолы (симптом Краузе);
втяжение и фиксация соска;
деформация молочной железы, уменьшение или увеличение ее размеров,
подтягивание ее вверх, фиксация к грудной стенке;
множественные плотные малоподвижные или неподвижные лимфатические
узлы в подмышечной области на стороне опухоли, иногда сливающиеся в
конгломераты;
плотные надключичные лимфатические узлы на стороне поражения.
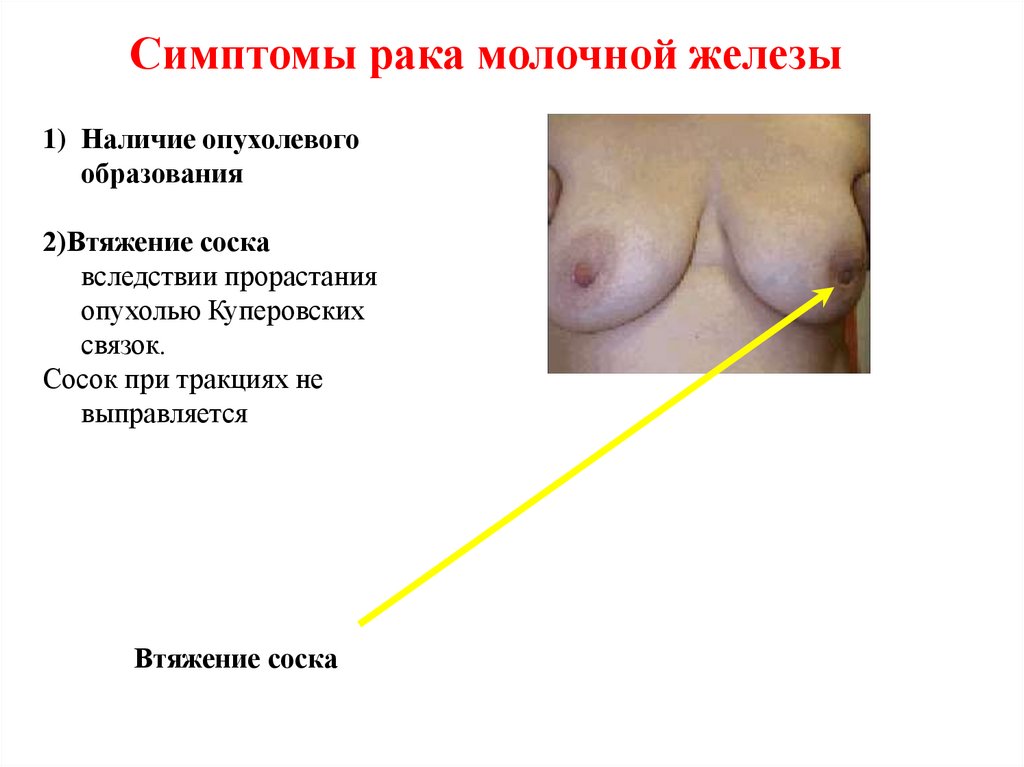
77.
Симптомы рака молочной железы1) Наличие опухолевого
образования
2)Втяжение соска
вследствии прорастания
опухолью Куперовских
связок.
Сосок при тракциях не
выправляется
Втяжение соска
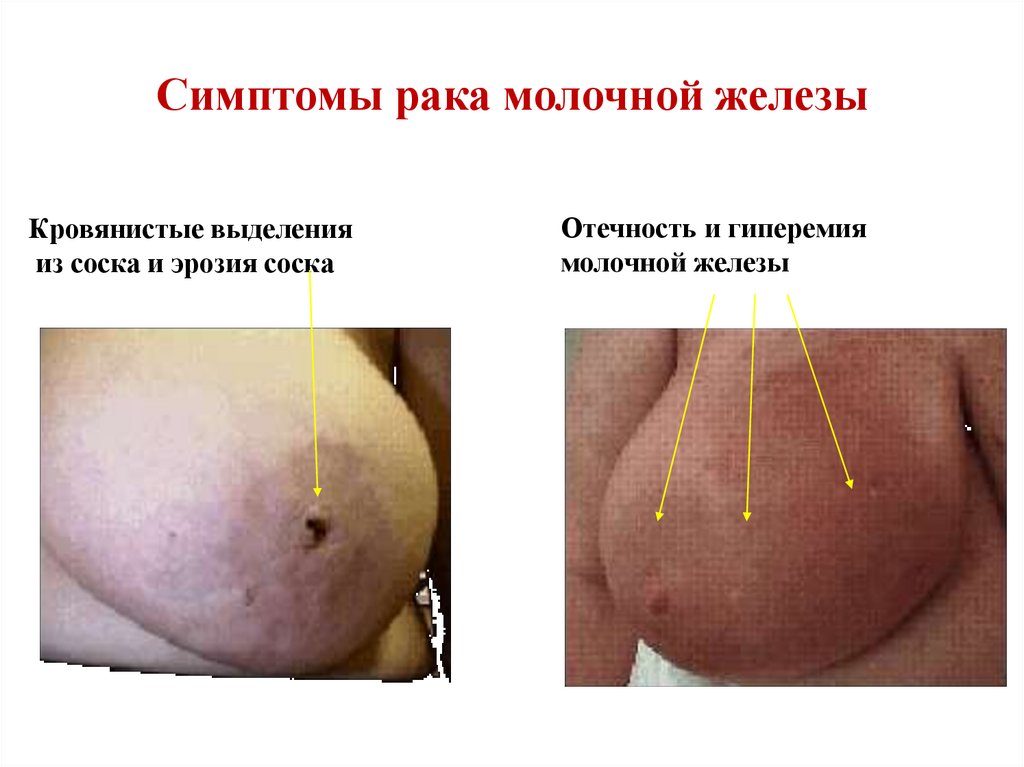
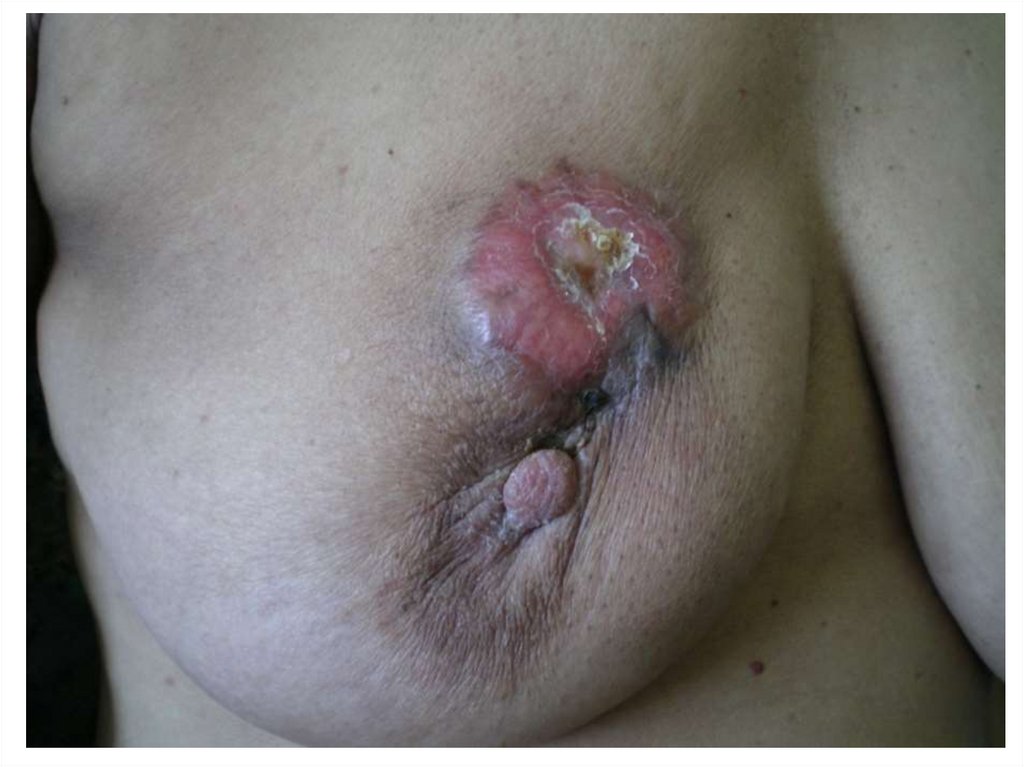
78. Симптомы рака молочной железы
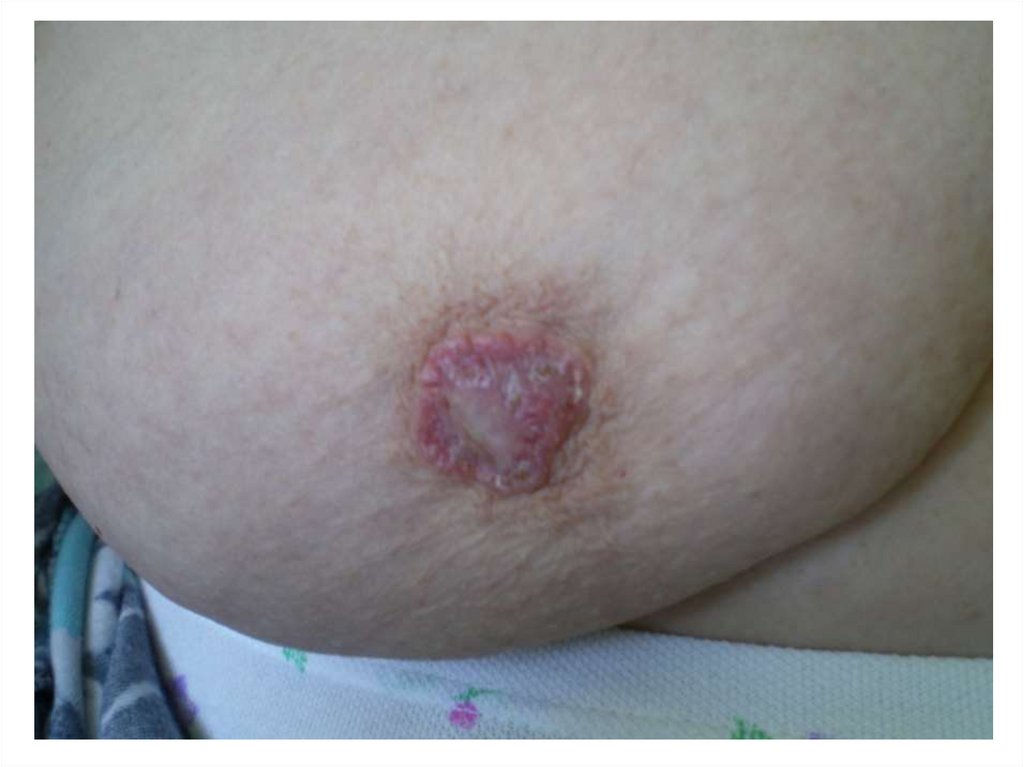
Кровянистые выделенияиз соска и эрозия соска
Отечность и гиперемия
молочной железы
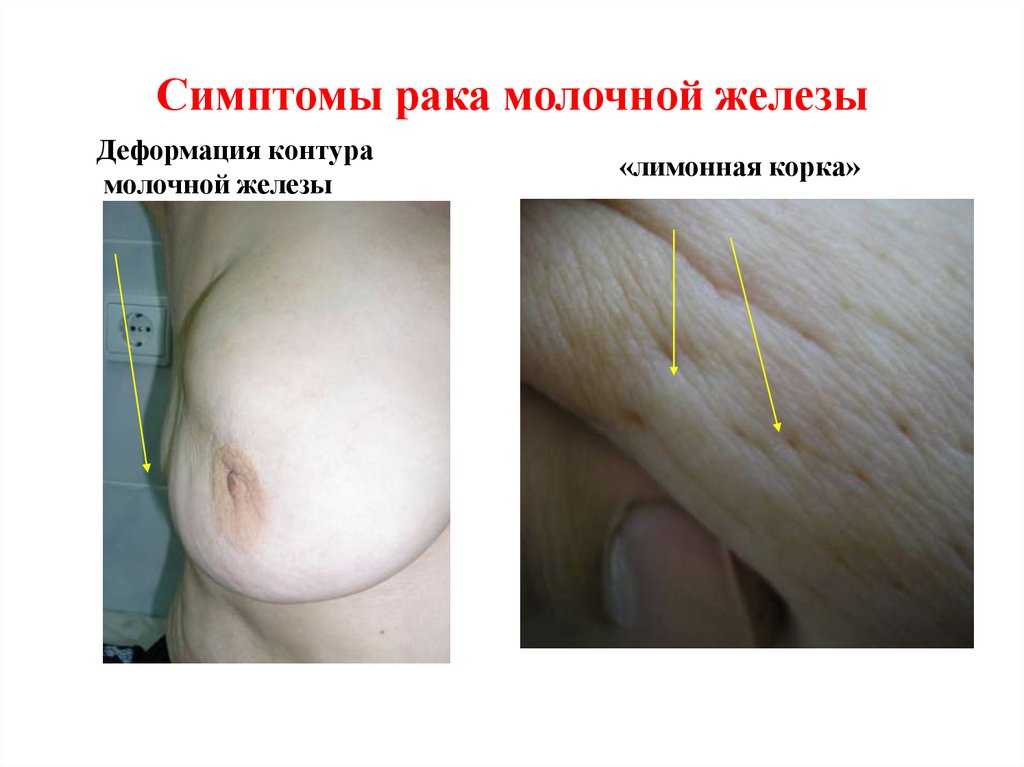
79. Симптомы рака молочной железы
Деформация контурамолочной железы
«лимонная корка»
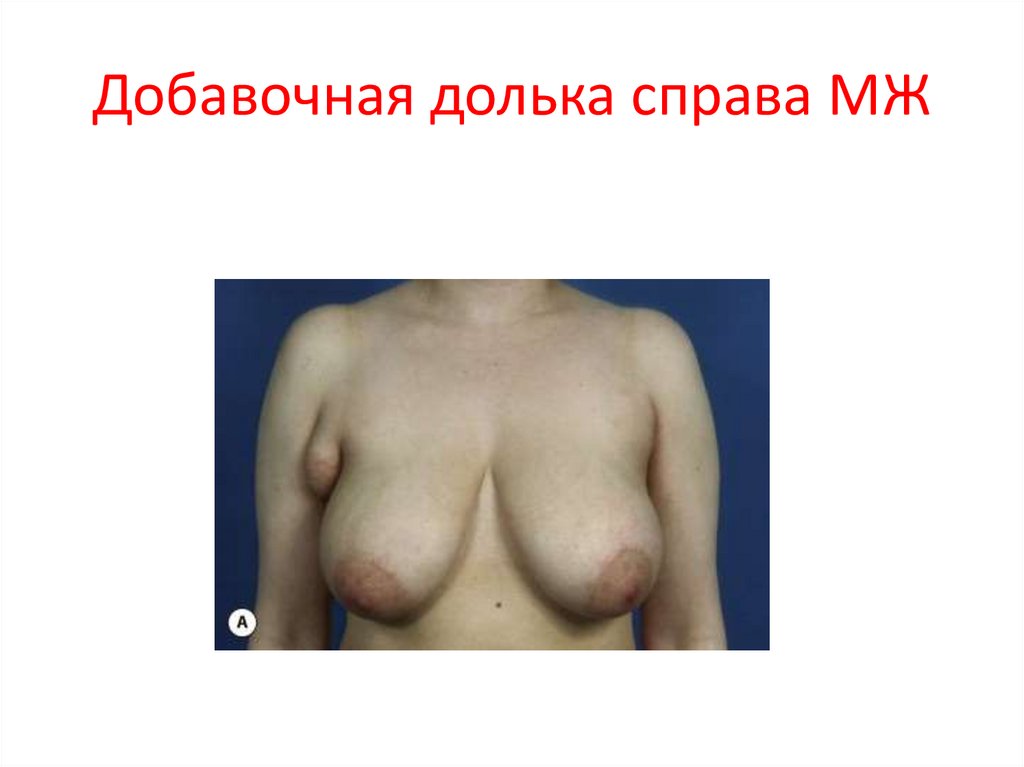
80. Добавочная долька справа МЖ
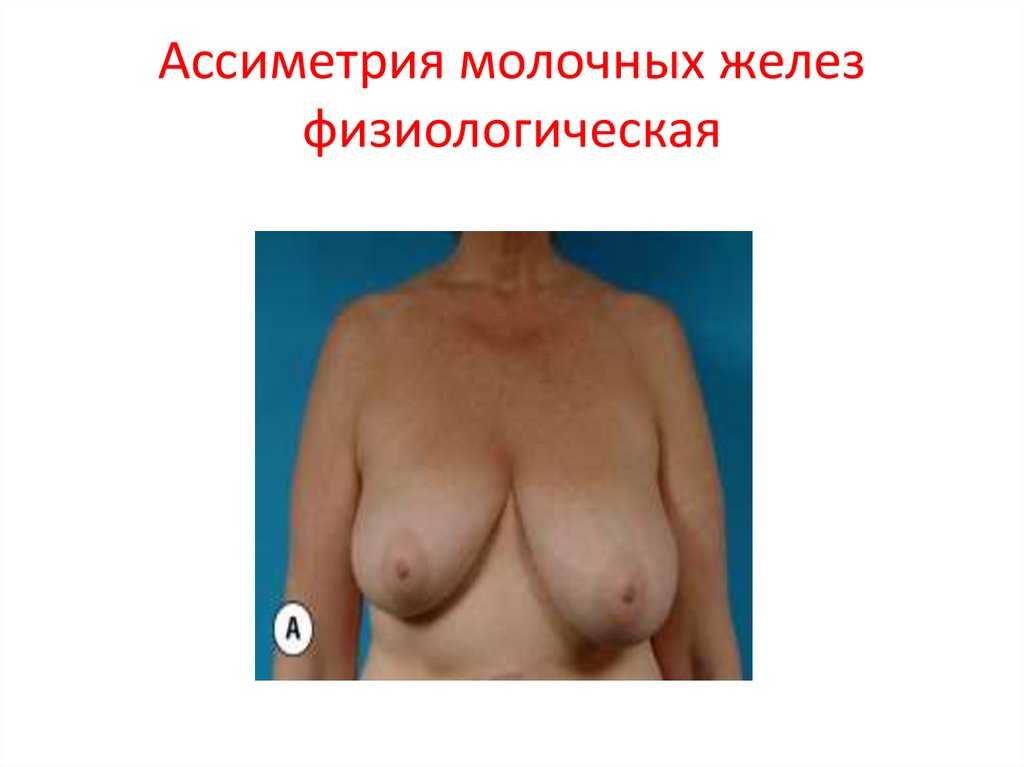
81. Ассиметрия молочных желез физиологическая
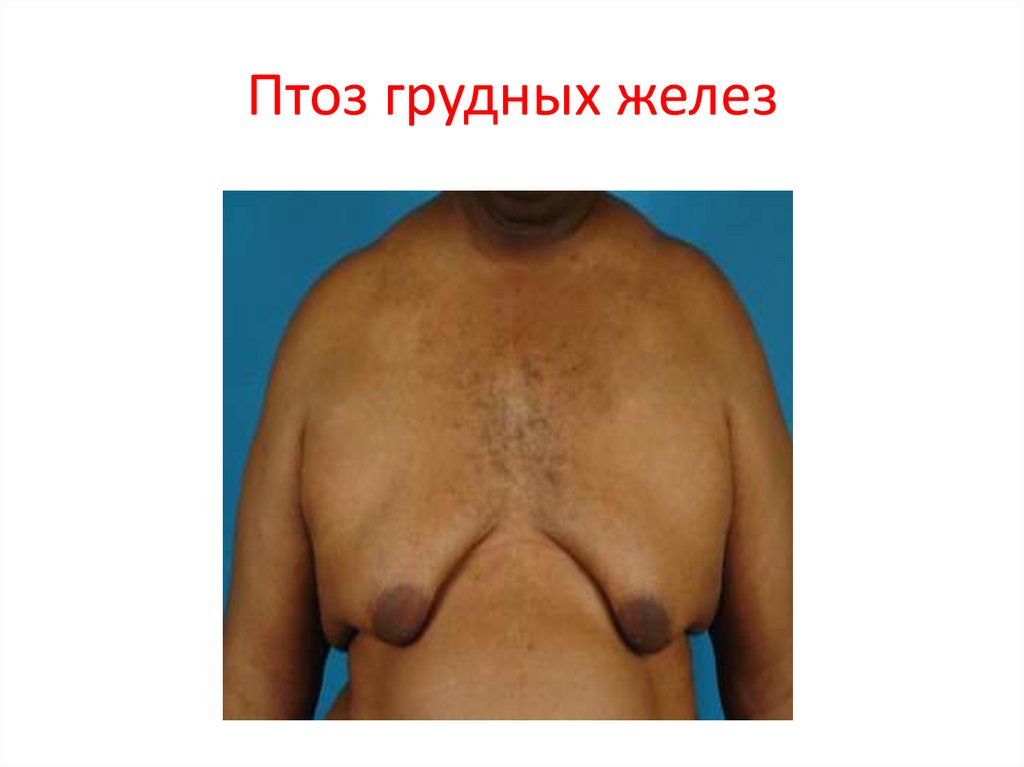
82. Птоз грудных желез
83.
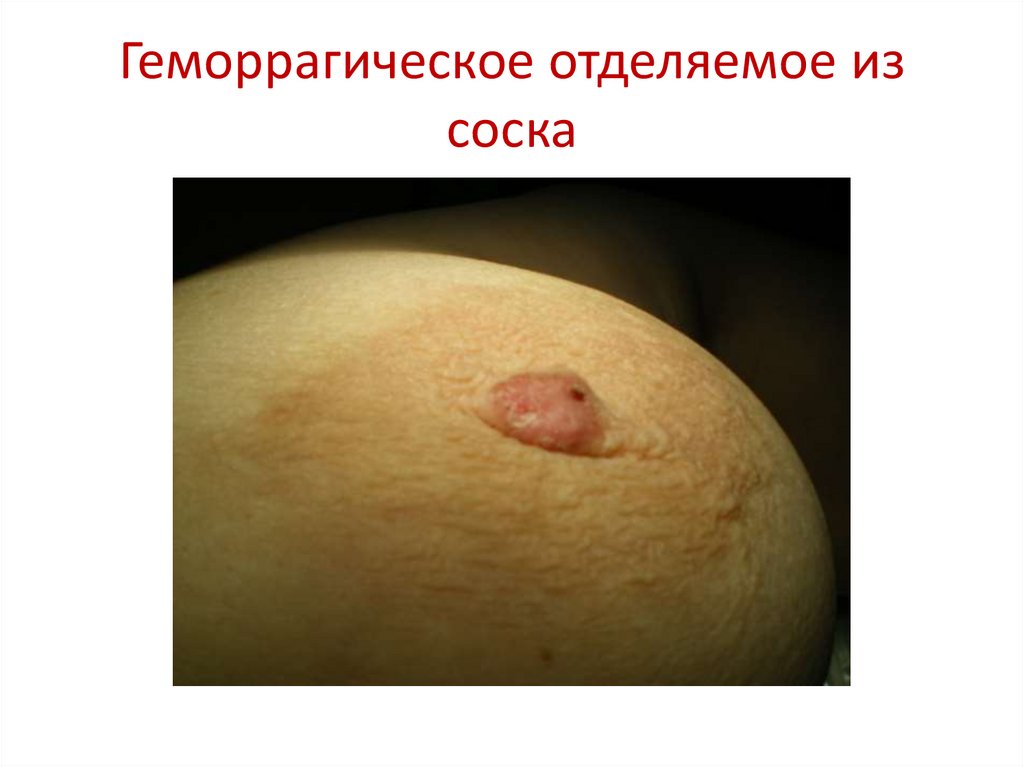
84. Геморрагическое отделяемое из соска
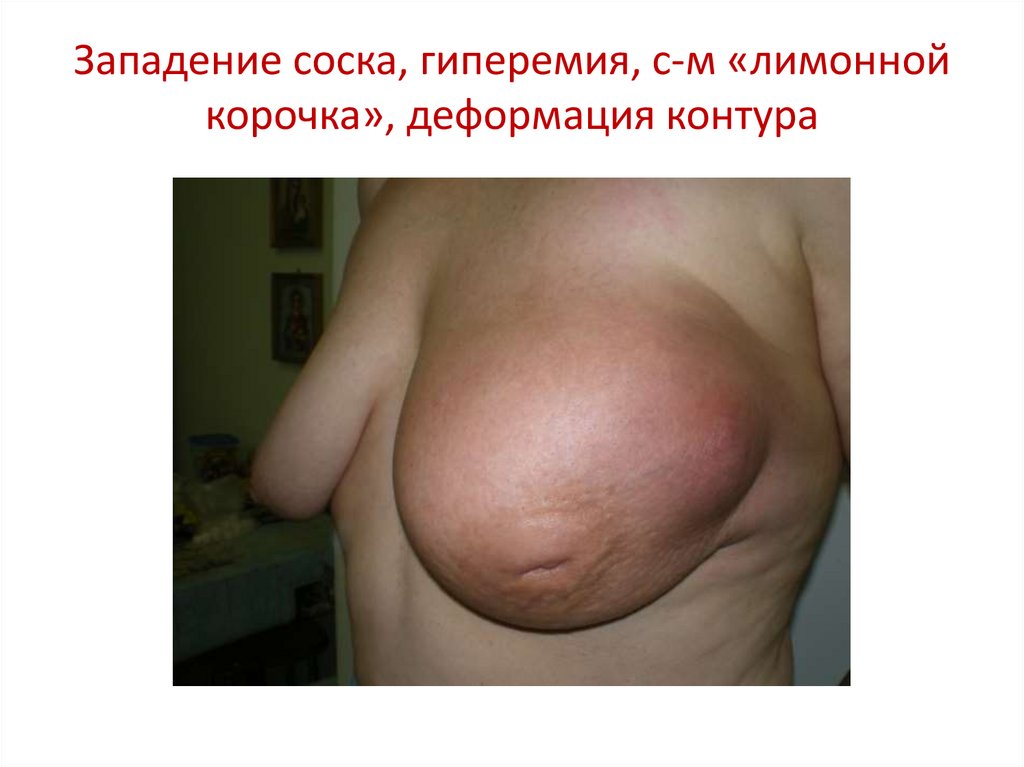
85. Западение соска, гиперемия, с-м «лимонной корочка», деформация контура
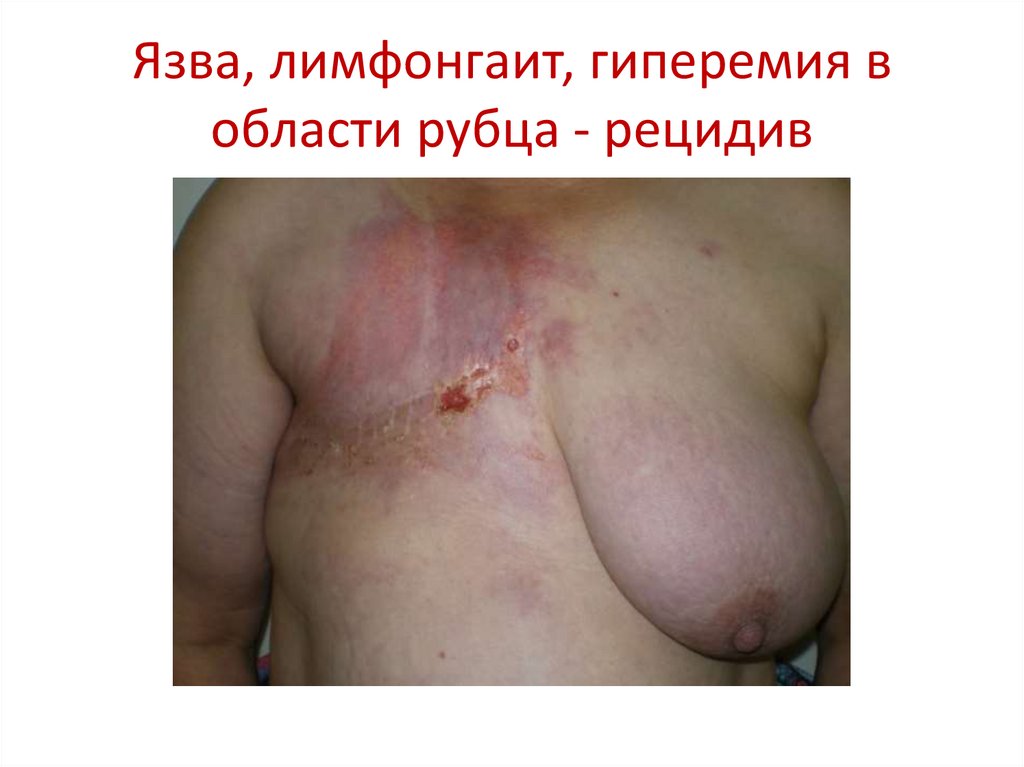
86. Язва, лимфонгаит, гиперемия в области рубца - рецидив
87. Симптом площадки
88. Ассиметрия молочных желез за счет опухоли справа
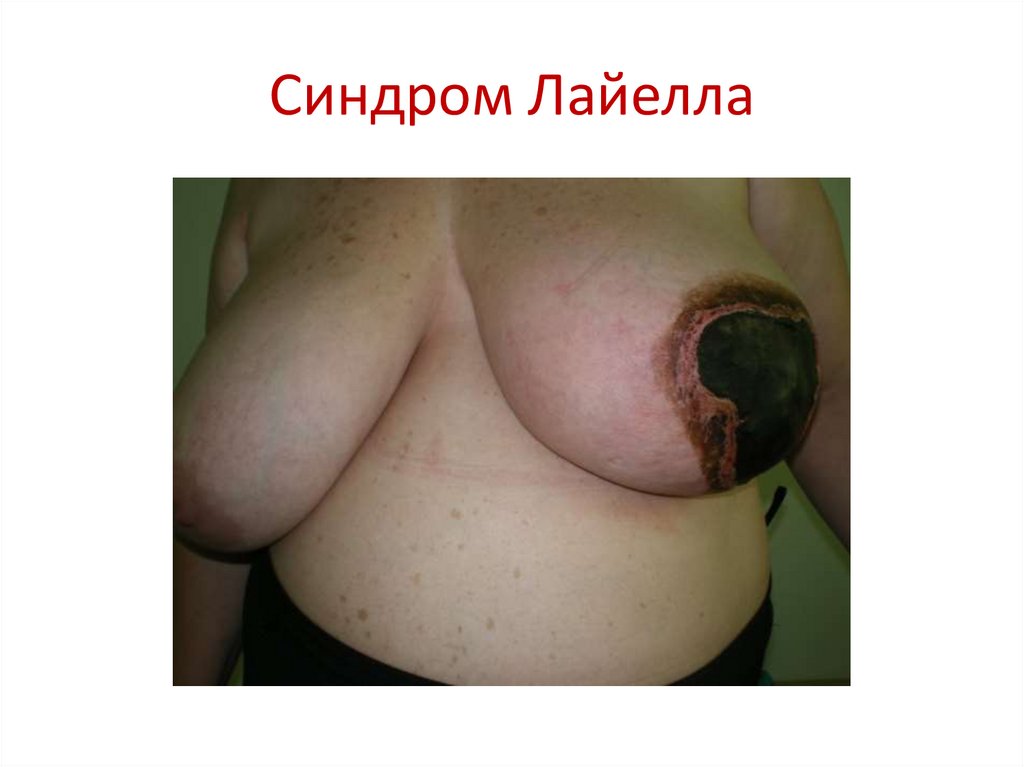
89. Синдром Лайелла
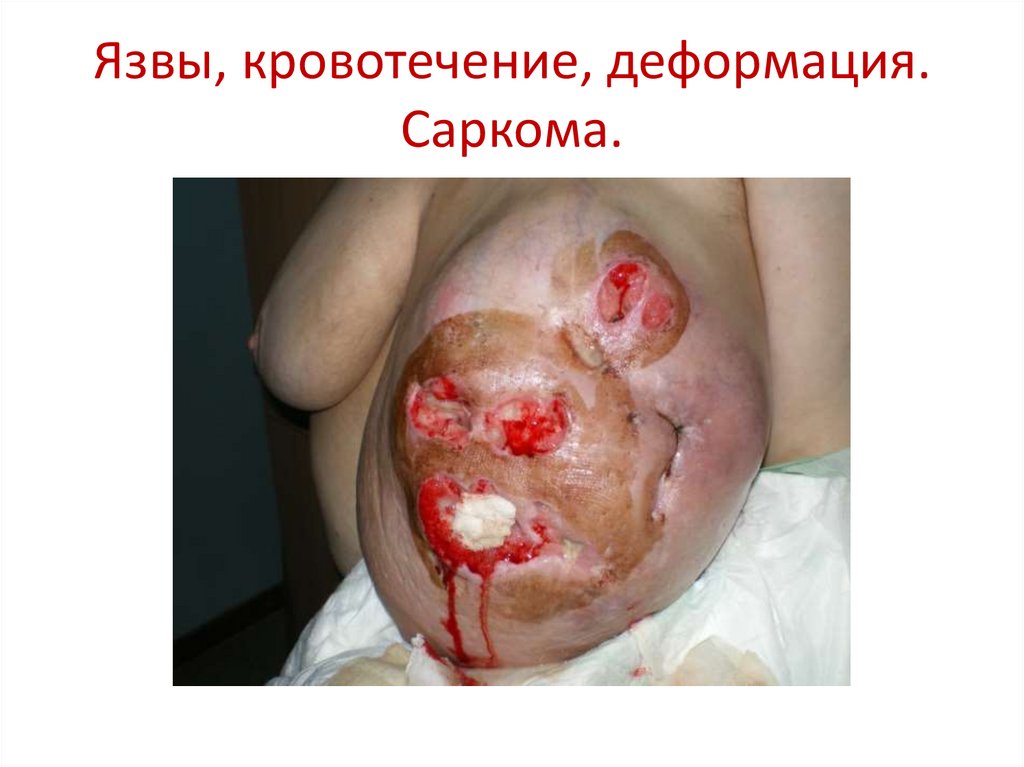
90. Язвы, кровотечение, деформация. Саркома.
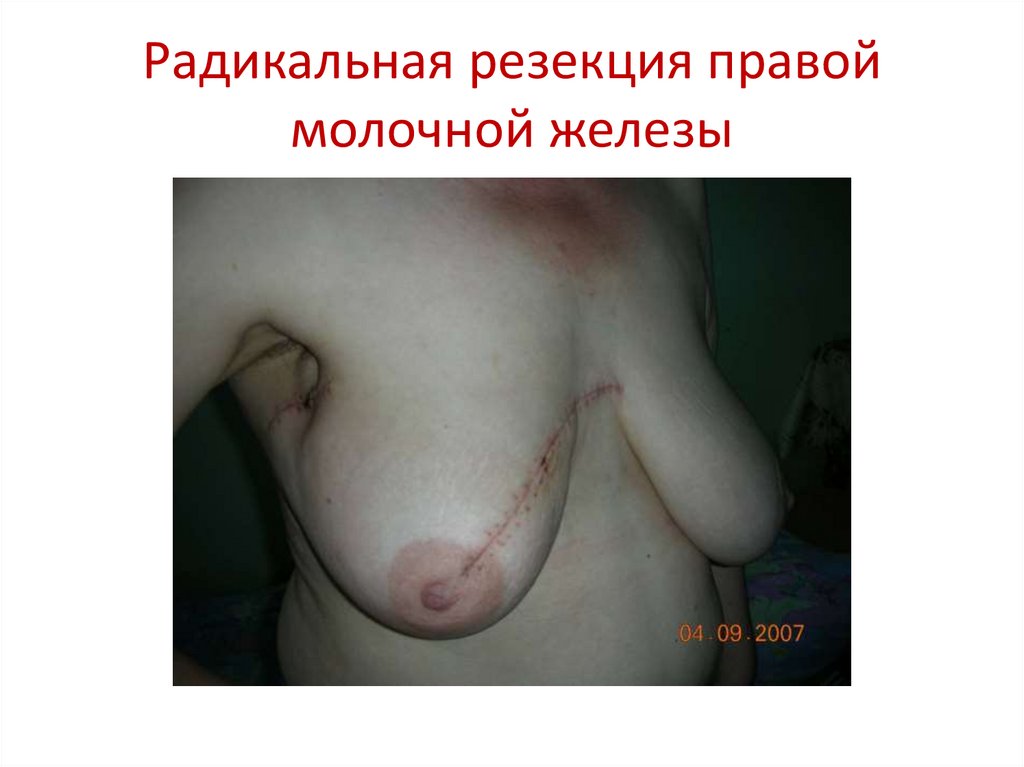
91. Радикальная резекция правой молочной железы
92. Пластика собственными тканями
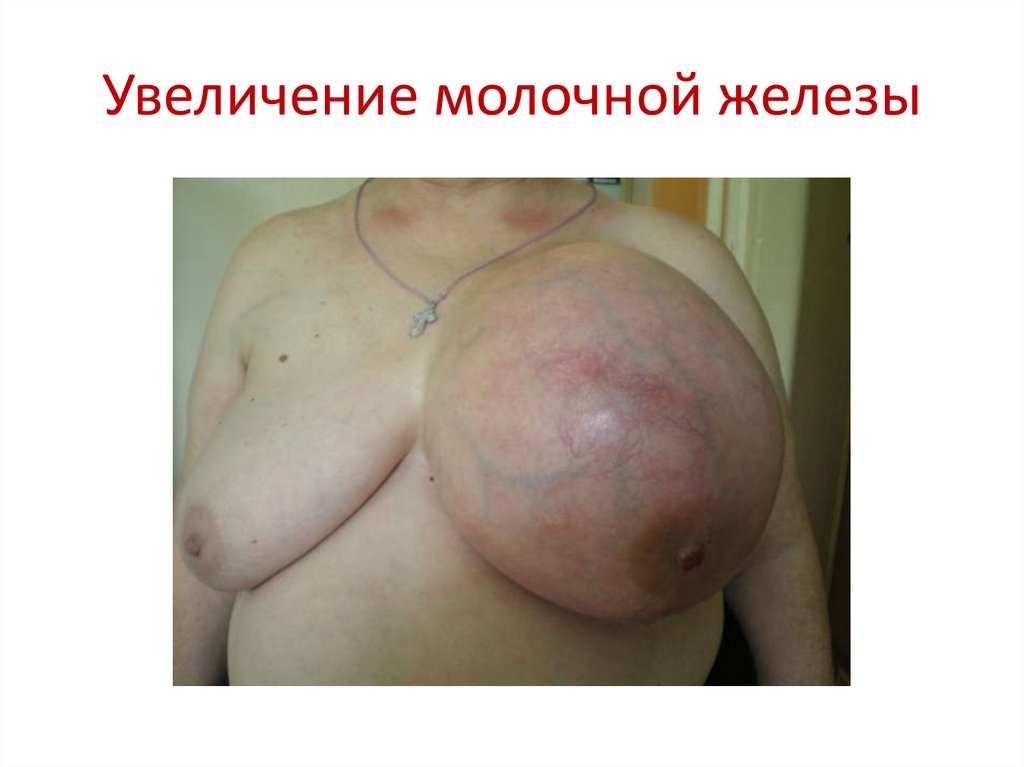
93. Увеличение молочной железы
94. Увеличение молочной железы
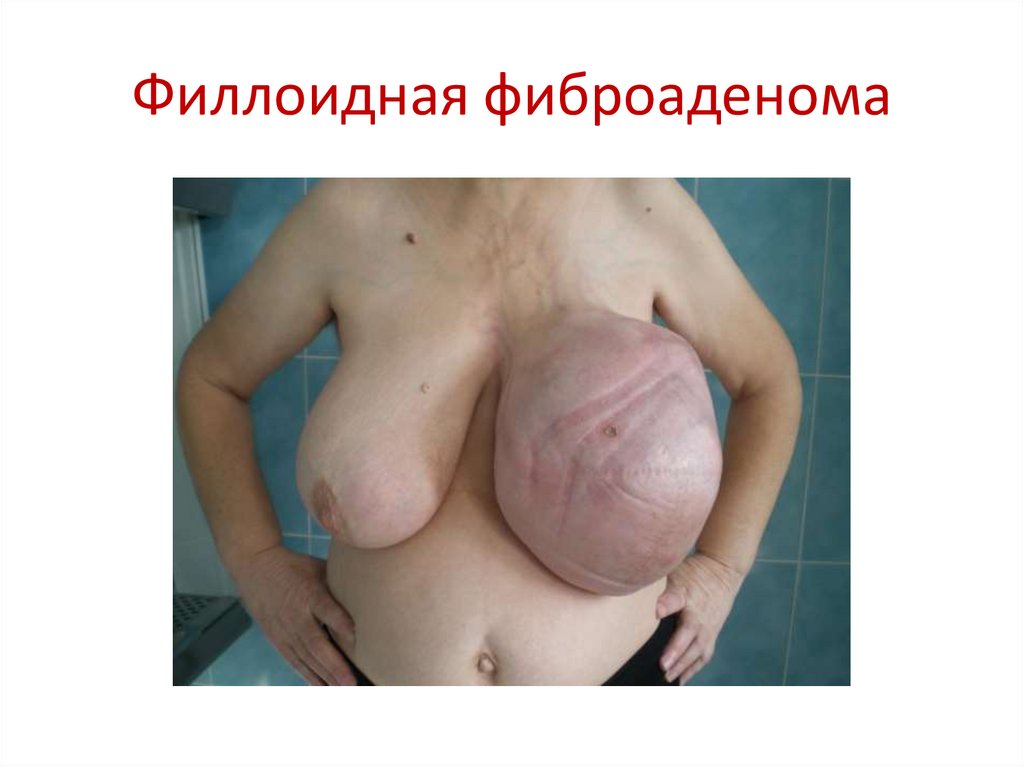
95. Филлоидная фиброаденома
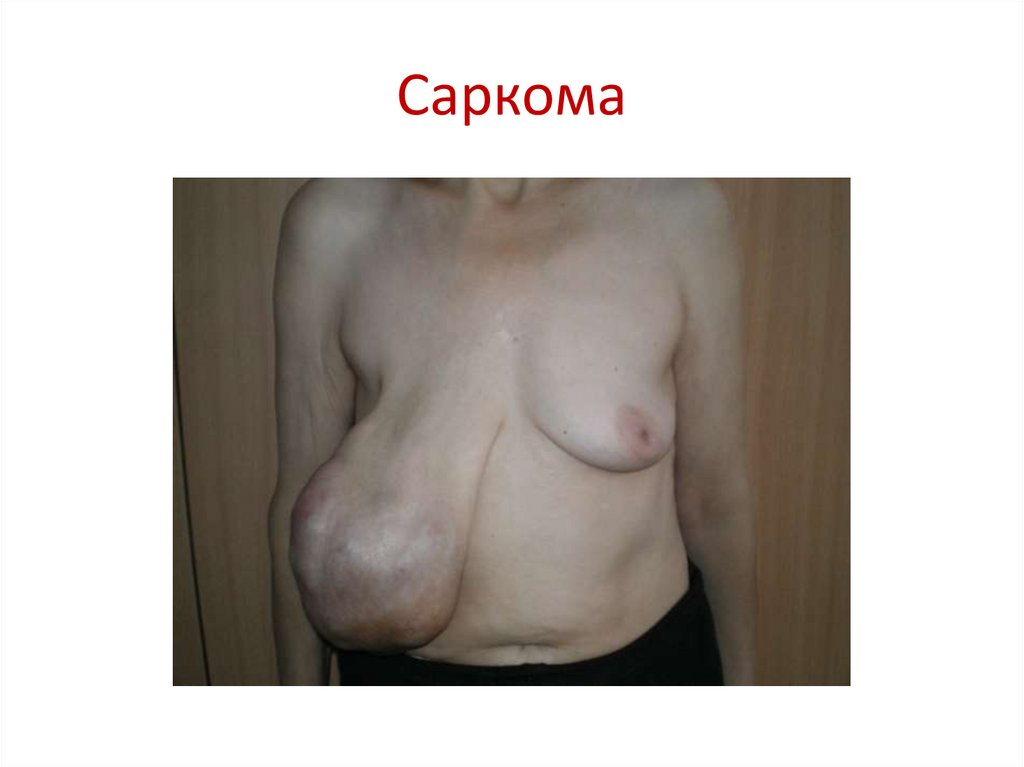
96. Саркома
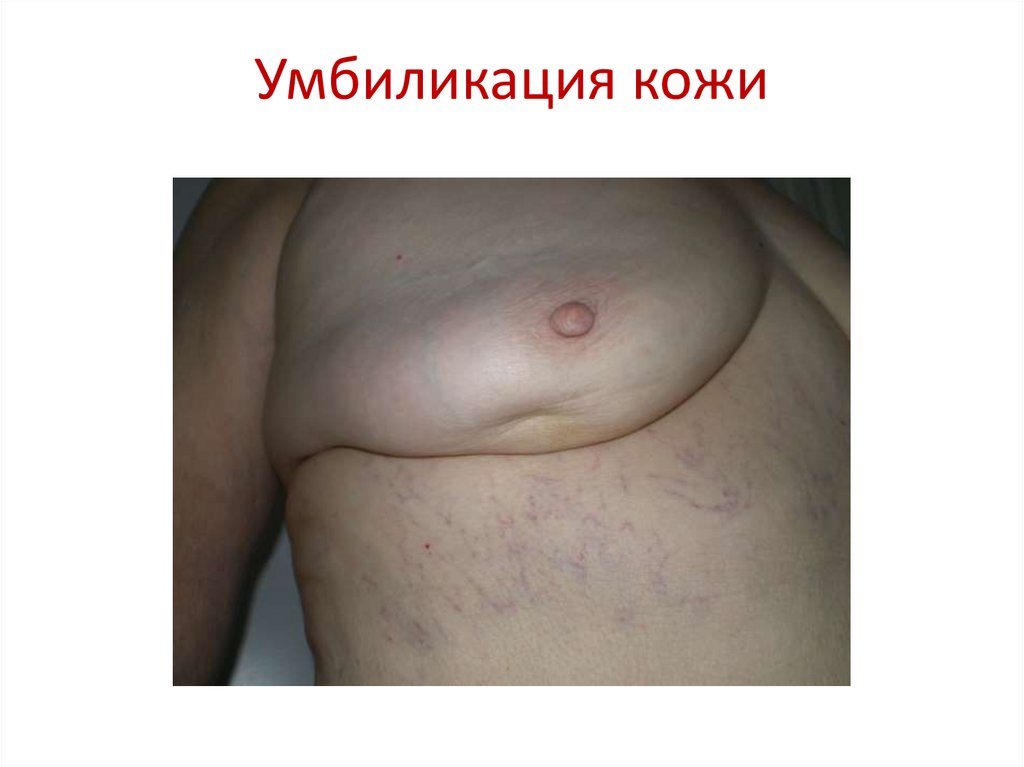
97. Умбиликация кожи
98. Увеличение молочной железы
99. Сателлиты
100. С-м «лимонной корочки»
101.
102.
103.
104.
105.
106.
Выделяют клиническую и патоморфологическую стадии РМЖ, которые могутсущественно различаться. Клиническое стадирование (обозначается
префиксом «с», от англ. «clinical») проводится на основании результатов
клинического обследования, патоморфологическое (определяется префиксом
«р», от англ. «pathologic») – на основании заключения морфолога после
операции.
Патоморфологическое стадирование по значимости превосходит клиническое.
Категории Т и N, оцениваемые после неоадъювантной терапии, обозначаются
префиксом «y»: «ус» – при клиническом стадировании или «yp» – при
патоморфологическом стадировании, например, «ypT» или «ypN».
Префиксы для категорий TNM:
• m (множественные опухолевые узлы инвазивного рака);
• r (рецидив);
• y (после неоадъювантной терапии);
• sn (сторожевой лимфатический узел).
107.
Рекомендуется с целью определения тактикиведения больных РМЖ исходить из
принципов мультидисциплинарного подхода.
Рекомендуется планирование лечения в
рамках консилиума с участием хирурга,
химиотерапевта и радиотерапевта.
Выбор
тактики
возможен
после
морфологического подтверждения диагноза,
- гистологического или гистологического +
иммуногистохимического.
108. Лечение РМЖ
1.2.
3.
4.
5.
Перед лечением необходимо определить:
Стадию процесса
Гистологию
Биологический (ИГХ) подтип
Менопаузальный статус по ВОЗ (пременопаузарепродуктивный период, перименопаузанерегулярные месячные, но уровень ФСГ, ЛГ и
эстродиола соответствует репродуктивному)
BRCA-1
109. Биологический (ИГХ) подтип РМЖ
Люминальный АНаличие всех факторов:
• РЭ и РП положительные
• HER2 отрицательный
• Ki67<20%
• показатель низкого риска рецидива при
мультигенном анализе (если доступен)
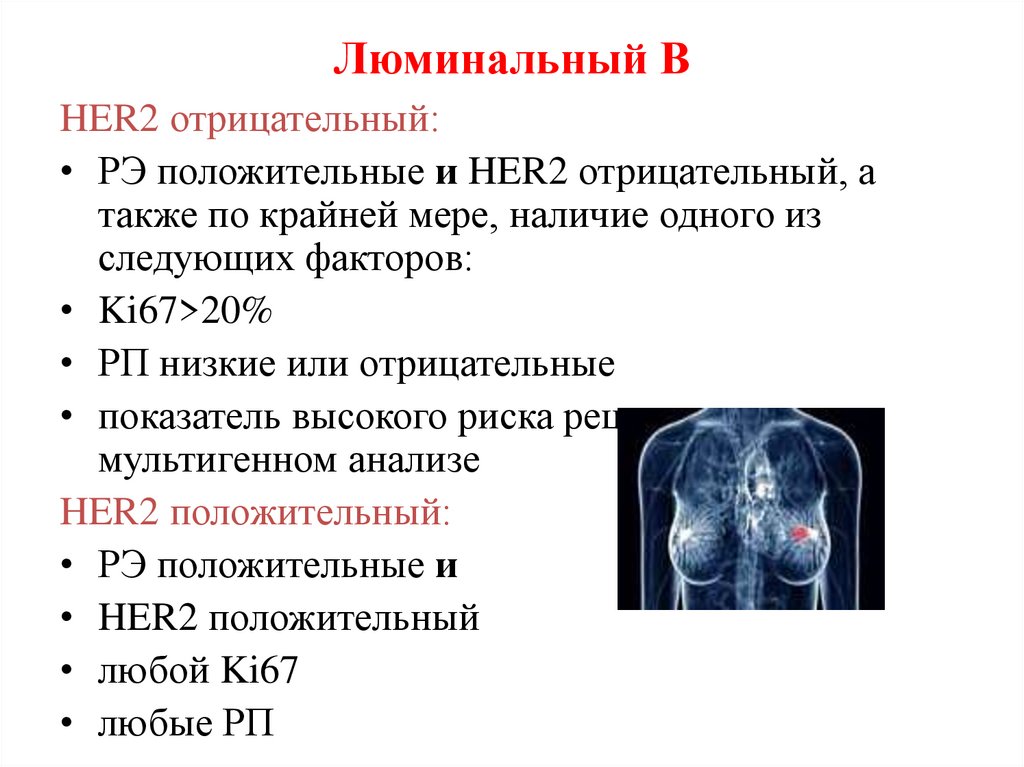
110. Люминальный В
HER2 отрицательный:• РЭ положительные и HER2 отрицательный, а
также по крайней мере, наличие одного из
следующих факторов:
• Ki67>20%
• РП низкие или отрицательные
• показатель высокого риска рецидива при
мультигенном анализе
HER2 положительный:
• РЭ положительные и
• HER2 положительный
• любой Ki67
• любые РП
111. С гиперэкспрессией HER2
HER2 положительный (не люминальный)• гиперэкспрессия HER2 и/или амплификация
HER2
• РЭ и РП отрицательные
112. Базальноподобный
Тройной негативный• РЭ, РП и HER2 отрицательные
113.
114. Обследование
Обследование
сбор анамнеза и осмотр;
осмотр включает бимануальную пальпацию молочных желез и лимфоузлов
регионарных зон, а также выявление симптомов, подозрительных в отношении
отдаленных метастазов;
общий анализ крови с подсчетом лейкоцитарной формулы и количества тромбоцитов;
биохимический анализ крови с определением показателей функции печени, почек,
уровня щелочной фосфатазы, кальция, глюкозы;
билатеральную маммографию + УЗИ молочных желез и ре- гионарных зон; МРТ
молочных желез – по показаниям1 ;
R-графию органов грудной клетки; КТ/МРТ органов грудной клетки – по показаниям;
УЗИ органов брюшной полости и малого таза, КТ/МРТ органов брюшной полости
и малого таза с контрастированием – по показаниям ;
радиоизотопное исследование скелета + рентгенографию и/или КТ/МРТ зон
накопления радиофармпрепарата – по показаниям;
биопсию опухоли с патоморфологическим исследованием опухолевой ткани;
определение в опухолевой ткани рецепторов эстрогенов (РЭ) и прогестерона (РП),
HER2 и Ki67;
оценку функции яичников (см. раздел 2.2.1.3, критерии менопаузы);
консультацию медицинского генетика; определение мутаций BRCA1/2 показано: – при
отягощенном наследственном анамнезе; – пациенткам моложе 40 лет; – пациенткам
моложе 50 лет с тройным негативным фенотипом РМЖ.
115.
Способы лечения рака молочной железы• Хирургическое
• Лучевое
• Лекарственное: химиотерапия,
гормонотерапия, таргетная терапия
• Комбинированное
• Комплексное
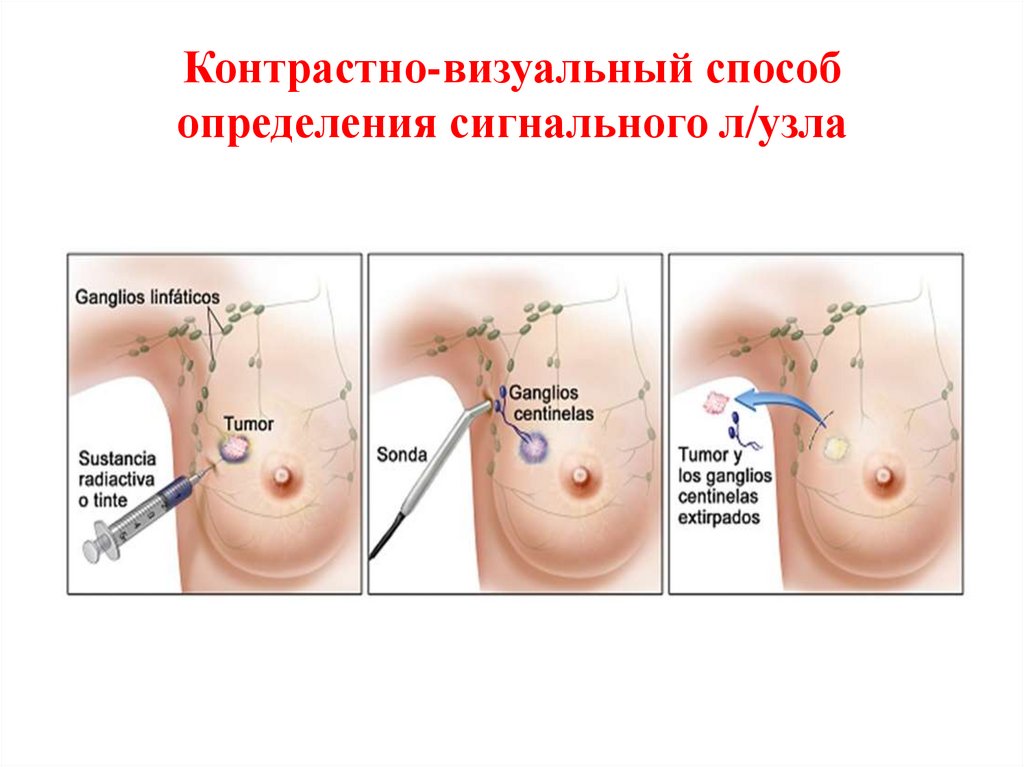
116. Способы идентификации сигнальных лимфатических узлов
Сигнальные лимфоузлы можно обнаружить,используя синий контраст или радиоизотоп, или с
помощью комбинации «краситель и изотоп».
Синий краситель помогает обнаружить сигнальные
лимфоузлы у 80% пациентов, радиоизотоп – у
89% пациентов. Комбинация красителя и
изотопов
повышает
частоту
обнаружения
сигнальных лимфоузлов до 96% [1].
1. Семиглазов В.Ф., Канаев С.В., Пожарисский К.М. и др. Органосохраняющее лечение ранних стадий инвазивного рака
молочной железы. Методические указания. – СПб, 2001.
117. Контрастно-визуальный способ определения сигнального л/узла
118. Показаниями для биопсии сторожевого л/у (БСЛУ)
• Рак молочной железы ранних стадий сотсутствием
признаков
поражения
регионарных лимфатических узлов;
• Пациенткам, имеющим резектабельный
рак, но с мультицентричной или протоковой
карциномой in situ и не имевшим
оперативного вмешательства на молочной
железе в анамнезе.
Противопоказаниями
для
данной
манипуляции
принято
считать
распространенные формы РМЖ (Т3/Т4/N1-и
более).
119.
Хирургическое лечение рака молочнойжелезы
•Лампэктомия
•Радикальная резекция молочной железы
•Радикальная мастэктомия по Маддену
•Радикальная мастэктомия по Пейти
•Радикальная мастэктомия по Холстеду
•Расширенная радикальная мастэктомия по Урбану Холдину
120.
Критерии к выполнениюорганосохраняющих операций:
• размер опухоли до 3 см в диаметре;
• отсутствие метастазов в регионарных лимфатических
узлах или наличие единичных метастатических
аксиллярных лимфатических узлов;
удаленность опухоли от сосково-ареолярного
комплекса не менее чем на 3-4 см;
• отсутствие мультицентричности;
благоприятные соотношения объема опухоли и
объема молочной железы;
• желание пациентки сохранить молочную железу.
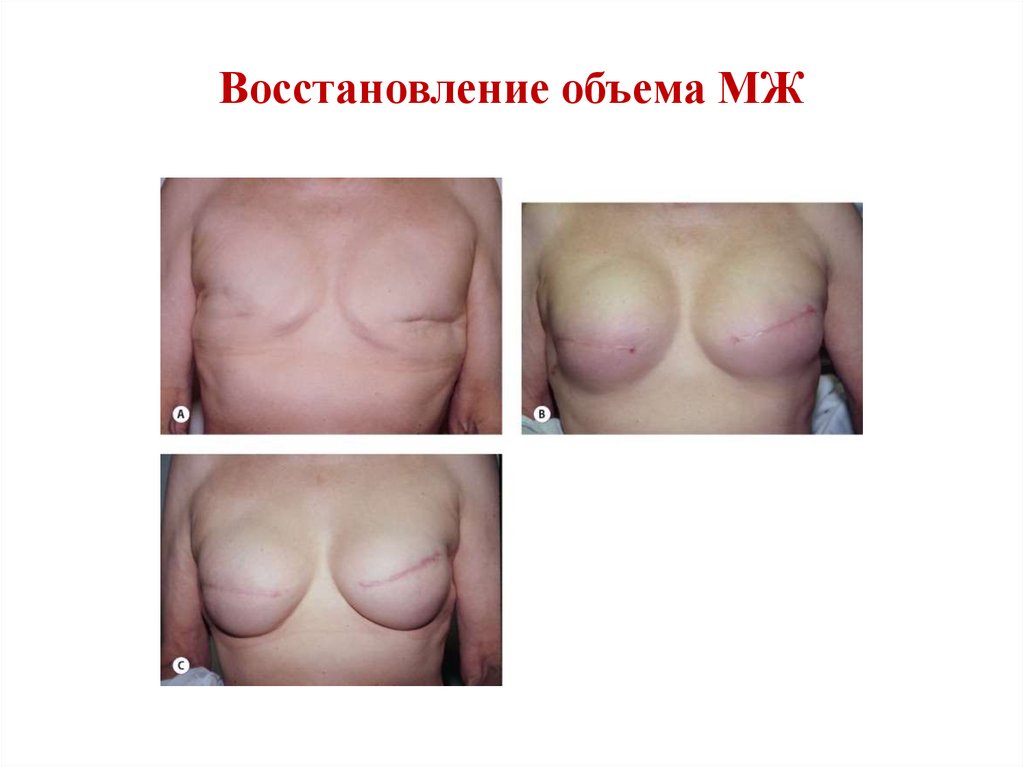
121. Восстановление объема МЖ
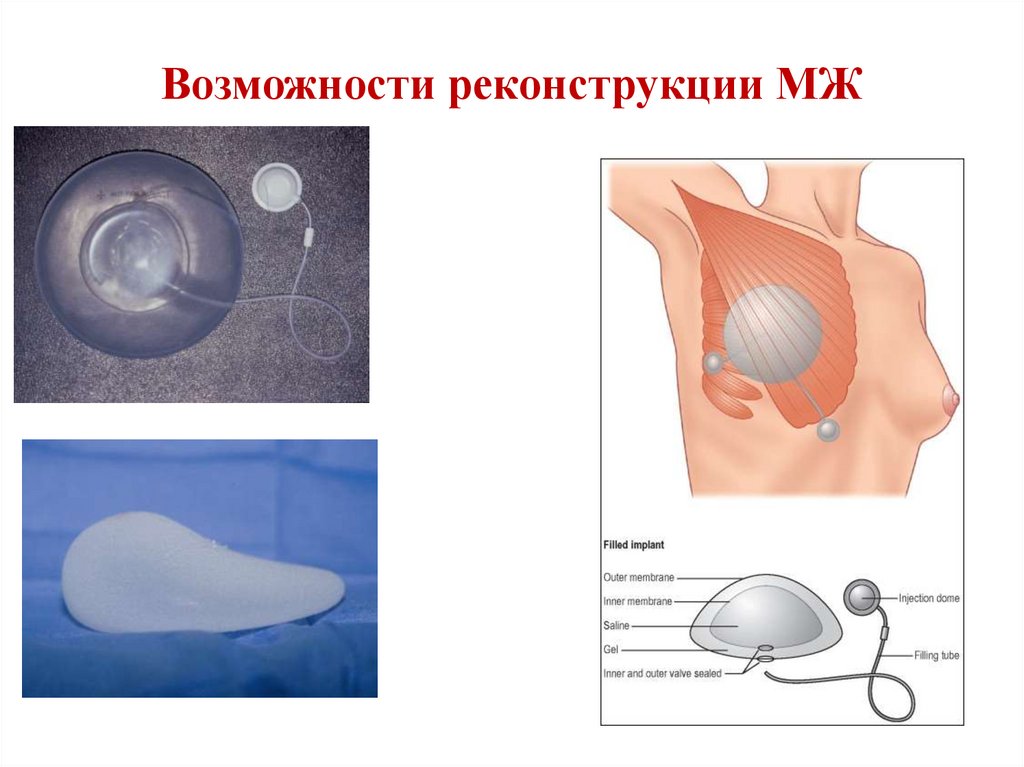
122. Возможности реконструкции МЖ
123. При исследовании операционного материала в заключении должны быть указаны:
1.Расстояние до ближайшего края резекции2. Состояние краев резекции
3. Размеры опухоли в трех взаимно-перпендикулярных измерениях
4. Гистологическое строение опухоли
5. Степень дифференцировки опухоли
6. рТ
7. рN (с указанием общего числа исследованных и поражённых
лимфоузлов)
8. Наличие лимфоваскулярной, периневральной инвазии,
экстракапсулярного распространения (в том числе и отрицательный
результат)
9. Степень патоморфологического ответа опухоли по шкале RCB (при
проведении неоадъювантного лечения)
10. Экспрессия РЭ/РП, статус HER2 и Ki67, при необходимости (при
неопределенном уровне HER2 - результаты молекулярно-генетического
исследования (ISH HER2).
124. Показания к радикальной кожесохранной мастэктомии с одномоментной реконструкцией
1.Преинвазивная карцинома DCIS,2. Рак молочной железы I ст. сТ1N0M0; IIA ст. сТ2N0M0, cT1N1M0; IIB
ст. сT2N1M0
3. Рак молочной железы IIB ст. сT3N0M0, IIIA ст. cT1N2M0, cT2N2M0,
cT3N1M0 после неоадъювантного лечения с частичной или полной
регрессией (PR, CR)
4. Расстояние опухоли до проекционного кожного лоскута менее 1 см
5. Наличие птоза молочной железы
6. Близкая локализация опухоли до САК, наличие опухолевых клеток в
подсосковой области при срочном интраоперационном морфологическом
исследовании
125. Противопоказания к радикальной подкожной/кожесохранной мастэктомии с одномоментной реконструкцией
1.Рак молочной железы сT4bN0-3M0-12. Рак молочной железы IIB ст. сT3N0M0, IIIA
ст. cT1N2M0, cT2N2M0, cT3N1M0 после
неоадъювантного лечения при отсутствии
эффекта (NR)
3. Поражение кожных покровов (хронические
дерматиты, рубцовые деформации, наличие
келоидных рубцов)
4. Тяжелые сопутствующие заболевания
5. Психические расстройства
126. Общая схема лечения
Первично операбельный рак I, IIА, IIВ:Оперативные пособия: радикальная резекция;
радикальная мастэктомия по Маддену
Неоадъювантная химиотерапия, гормонотерапия
при IIВ
Лучевая терапия после органносохранной операции,
более 4 пораженных MTS лимфоузлов.
Адъювантная химиогормонотерапия (люминальный
А, I и IIА стадии не показана ПХТ, а HER2позитивный нелюминальный - гормонотерапия)
127. Адъювантная терапия(АТ)
• Вариант адъювантнойлекарственной терапии(АЛТ) зависит от
молекулярно-биологического подтипа и стадии РМЖ
• АЛТ должна начинаться с ХТ, если показана
• Не вводят одновременно антрациклины и анти-HER2 препаратыкардиотоксичность высокая
• АЛТ таксаносодержащими режимами должна проводиться одновременно
с анти HER2 терапией, если она показана
• Гормонотерапия(ГТ) начинается после завершения ХТ и может
проводиться одновременно с анти-HER2 терапией
• Лучевая терапия начинается после завершения ХТ и может проводиться
совместно с ГТ и анти-HER2 терапией
• Следует соблюдать дозовые режимы
• Избегать редукции доз и интервалов между курсами
• Последовательно использовать антрациклины и таксаны
• При назначении паклитаксела предпочтительно еженедельное введение,
особенно при тройном негативном раке
128. Адъювантная гормонотерапия(АГ)
• АГ показана всем пациенткам с РЭ ≥1%• Выбор ГТ зависит от функции яичников (определить в
крови ЛГ, ФСГ, эстрадиол до начала ХТ).
• Пациенткам в постменопаузе или с подавлением
функции яичников показано на фоне ГТ для
профилактики остеопороза остеомодифицирующие
агенты (золендронат 4 мг в/в 1 раз в 6 мес или
Деносумаб 60 мг п/к 1 раз в 6 мес) в течении 2-3
лет+ Вит D 800 МЕ/сут внутрь ежедневно+ кальций
1500 мг/сут внутрь ежедневно; под контролем
минеральной плотности костей (денситометрия) 1
раз в год
129. Неоадъювантная терапия(НТ)
• При первично операбельном РМЖ очередностьлекарственного и хирургического лечения не
влияет
на
безрецедивную
и
общую
выживаемость.
• Неоадъювантная лекарственная терапия (НЛТ)
первично операбельного РМЖ позволяет: 1.
выполнить органосохраняющую операцию и/или
улучшить косметический эффект; 2. оценить
выраженность патоморфологического ответа и
назначить
дополнительную
адъювантную
терапию; 3. в случае местного прогрессирования
во время НЛТ ее прекращают и выполняют
радикальную операцию
130. Неоадъювантная терапия(НТ)
• При I стадии проведение НЛТ не показано• При первично-неоперабельном РМЖ основной целью НЛТ
является уменьшение размеров опухоли с целью
достижения операбельного состояния
• Все курсы ХТ проводим до операции –цель полный
патоморфологический регресс
• Если все курсы провели до операции адъювантную ХТ не
проводят
• Пациенткам
с
ТНРМЖ
и
HER2+
получившим
неоадъювантно антрациклины и таксаны в полном
объеме и имеющие резидуальную опухоль назначается
адъювантно капицетабин при ТНРМЖ и транстузумабэмтанзим (Кадсила) при HER2+
131. Неоадъювантная терапия(НТ)
• Если по каким-либо причинам на дооперационном этапене удалось провести все запланированные курсы ХТ, то
недостающие курсы проводятся после операции.
• Оптимальный промежуток от начала лечения до оценки
результатов, не должен превышать 6-8 недель и теми
методами которые были первоначально
• При получении «быстрого» (2-4 курса ХТ) клинического
эффекта не следует сокращать объем лечения менее чем
до 6-8- курсов
• После завершения НЛТ при отсутствии клинических
признаков прогрессирования оценку эффекта производят
теми же методами, что были первоначально до лечения
132. Лучевая терапия при первично операбельном РМЖ (0, I, IIA, IIB, IIIA (T3N1M0) стадии) после органосберегающего лечения
Рекомендуется проводить адъювантную лучевую терапию после органосберегающего
лечения у больных раком молочной железы TisN0M0, Т1-3N0-1M0 стадий
Объемы облучения после органосберегающего лечения:
Tis (протоковый рак in situ - DCIS): оставшаяся часть молочной железы
Т1-3N0-1М0: o при N1 (поражении 1-3 л/узлов): оставшаяся часть молочной железы +/дополнительное облучение ложа удалённой опухоли, рассмотреть целесообразность
проведения ЛТ на надподключичную область, ипсилатеральные парастернальные
лимфатические узлы, на часть подмышечной области (как зону риска возникновения
рецидива)
при N0: оставшаяся часть молочной железы +/- дополнительное облучение ложа
удалённой опухоли
• рассмотреть целесообразность проведения ЛТ на надподключичную область и
ипсилатеральные
парастернальные
лимфатические
узлы
у
больных
с
центральной/медиальной локализацией опухоли или опухолью размерами > 2см и
наличием факторов риска возникновения рецидива опухоли
133. Лучевая терапия при первично операбельном РМЖ (0, I, IIA, IIB, IIIA (T3N1M0) стадии) после органосберегающего лечения
• ЛТ должна быть начата через 4-12 недель послеорганосберегающей
операции
без
проведения
адъювантной полихимиотерапии (при полном заживлении
операционной раны) или через 3-4 недели после
завершения всей запланированной адъювантной
химиотерапии в случае её назначения. Проведение
лучевой терапии возможно одновременно с эндокринной
или таргетной терапией
• ЛТ после органосберегающих операций можно не
проводить больным РМЖ старше 70 лет, T1N0M0, Grade III, при отсутствии опухолевых клеток в краях резекции,
РЭ+ статусе опухоли при условии назначения
гормонотерапии
134. Лучевая терапия при первично операбельном РМЖ (0, I, IIA, IIB, IIIA (T3N1M0) стадии) после органосберегающего лечения
Дозы и режимы ЛТ: на оставшуюся часть молочной железы– в режиме классического фракционирования– РОД-2Гр,
СОД - 46-50Гр или гипофракционированный режим ЛТ
(возможен при условии проведения 3D конформной лучевой
терапии) - РОД - 2,67-2,66 Гр до СОД - 40-42,56 Гр за 15-16
фракций. На зоны лимфооттока ЛТ проводится в режиме
классического фракционирования РОД 2Гр, СОД – 46-50Гр
Дополнительное облучение ложа удалённой опухоли
проводится с помощью 3Dконформной лучевой терапии,
брахитерапиии, интраоперационной лучевой терапии.
Рекомендуется при проведении дистанционной ЛТ
использовать РОД-2-2,5Гр, СОД 10- 16Гр [70,71] Лучевая
терапия проводится 5 раз в неделю.
135. Показания к дополнительному облучению ложа опухоли («boost») у больных РМЖ
• возраст ≤ 50 лет• у больных в возрасте старше 51 года - Grade III, положительный или близкий
(менее 1 мм) край резекции (при отказе от повторной операции)
• лимфоваскулярная инвазия учитывается как дополнительный фактор риска в
сомнительных случаях
• чёткими ориентирами для определения ложа удалённой опухоли являются
послеоперационная серома, рентгеноконтрастные клипсы, устанавливаемые
хирургами во время операции.
• Можно не проводить дополнительное облучение ложа удалённой опухоли
(«boost») у больных ранним РМЖ в возрасте ≤ 50 лет с опухолью G1 и/или в
случае благоприятного молекулярного подтипа при планируемой
адъювантной эндокринной терапии
136. Показания для ЛТ после мастэктомии
• рТ1-3N1 (1-3 поражённых лимфатических узла +наличие одного или нескольких факторов риска
рецидива опухоли)
• рТ3N0 (опухоль ˃5 см)
• рТ1-2N0 – при наличии опухолевых клеток на
расстоянии менее 1 мм от края резекции или при
центральной/медиальной локализации опухоли,
при размерах опухоли >2 см, при трижды
негативном подтипе опухоли в сочетании с
наличием факторов риска развития рецидива
опухоли
137. Факторы риска возникновения рецидива РМЖ
• Возраст до 50 лет• Grade III
• Опухолевые клетки в краях резекции
• Лимфоваскулярная инвазия - учитывается
как дополнительный фактор риска в
сомнительных случаях
ЛТ должна быть начата через 4-6 недель после операции (при полном
заживлении операционной раны) или через 3-4 недели после
завершения всей запланированной адъювантной химиотерапии.
Проведение лучевой терапии возможно одновременно с эндокринной
или таргетной терапией.
138. Объемы облучения после мастэктомии:
• рТ1-3N1(1-3 поражённых лимфатических узла) + факторы риска рецидиваопухоли (один или несколько) - мягкие ткани передней грудной стенки +
дополнительное облучение зоны риска развития рецидива в области
послеоперационного рубца, надподключичная область, ипсилатеральные
парастернальные лимфатические узлы, любая часть подмышечной, области (как
зона риска развития рецидива)
• рТ3N0(опухоль ˃5 см): мягкие ткани передней грудной стенки +
дополнительное облучение зоны риска развития рецидива в области
послеоперационного рубца, рассотреть целесообразность ЛТ на шейнонадподключичную зону, ипсилатеральные парастернальные лимфатические узлы
• рТ1-2N0 при наличии опухолевых клеток на расстоянии менее 1 мм от края
резекции, при центральной/медиальной локализации опухоли или размере
опухоли >2 см, или трижды негативном подтипе опухоли + наличии факторов
развития рецидива опухоли: мягкие ткани передней грудной стенки +
дополнительное облучение зоны риска развития рецидива в области
послеоперационного рубца, +/- надподключичная зона и ипсилатеральные
парастернальные лимфатические узлы
139. Дозы и режимы ЛТ: на мягкие ткани передней грудной стенки (+ реконструированная молочная железа) и зоны лимфооттока
ЛТ проводится методом РОД - 2Гр, СОД - 46-50Гр. Дополнительноеоблучение зоны риска в области послеоперационного рубца проводится с
помощью 3D-конформной лучевой терапии, брахитерапиии, при
дистанционной ЛТ - РОД - 2Гр, СОД - 10Гр.
Лучевая терапия проводится 5 раз в неделю
Следует рассмотреть целессобразность применения специального
болюса при облучении мягких тканей передней грудной стенки или
послеоперационного рубца для обеспечения адекватной кожной дозы в
облучаемом объёме.
Комментарий: показания к ЛТ после неоадъювантной химиотерапии и
радикальной мастэктомии определяются исходными критериями Т и N и
не зависят от ответа на системную терапию
Перед выполнением онкопластических операций целесообразно
совместное обсуждение плана лечения хирургом и радиотерапевтом, при
наличии показаний к послеоперационной ЛТ операцию по
реконструкции молочной железы целесообразно выполнить по
завершении курса ЛТ
140. Местнораспространенный первично не операбельный рак IIIА, IIIВ, IIIС
• Предоперацианная лекарственная терапия• Вопрос об овариоэктомии?
• Альтернативная лучевая терапия
• Радикальная мастэктомия по Маддену, Холстеду
• Адъювантная химиогормонотерапия
• Таргетное лечение
141. Оценка результатов
• Объективный эффект: существенное уменьшениеразмеров и/или количества опухолевых очагов;
является показанием для продолжения проводимой
терапии в отсутствие серьезной токсичности;
• Стабилизация болезни: отсутствие значимых изменений
размеров и количества опухолевых очагов; при
удовлетворительном общем состоянии и хорошей
переносимости лечение может быть продолжено;
• Прогрессирование заболевания является показанием
к смене лечения. При подозрении на прогрессирование
болезни по данным осмотра необходимо выполнить
уточняющие обследования, в т.ч. с оценкой зон, не
обследовавшихся до начала терапии.
142. Признаки прогрессирования
Появление и/или усугубление симптомов, обусловленных опухолевым ростом(например, боли или одышки);
Существенное увеличение размеров или появление новых опухолевых очагов,
выявляемых при осмотре;
Ухудшение общего состояния (дифференцировать с токсичностью лечения);
Немотивированная потеря веса (дифференцировать с токсичностью лечения);
Повышение ЩФ, АЛТ, АСТ, билирубина (дифференцировать с токсичностью
лечения);
Гиперкальциемия;
Появление новых и/или существенное увеличение имевшихся ранее очагов по
данным объективных методов обследования;
При оценке результатов сканирования костей следует иметь в виду, что
репарация метастазов в костях, начавшаяся в результате эффективной
противоопухолевой терапии (в сочетании с остеомодифицирующими
агентами) и сопровождающаяся повышенным метаболизмом, может
создавать формальную картину прогрессирования за счет появления на
сканограммах новых очагов и увеличения накопления радиофармпрепарата
в имевшихся очагах, особенно при первом оценочном исследовании.
143. Таргетное лечение РМЖ
• Трастузумаб (герцептин) - гуманизированные антителаподавляют рост и сигнальные свойства Нег-2 системы.
Трастузумаб вводится в/в еженедельно, в 1-ую неделю 4
мг/кг, в последующем 2 мг/кг еженедельно или через
неделю.
• Лапатиниб – ингибитор тирозинкиназы рецепторов
эпидермального фактора роста (EGFR), 1 (HER-1) и 2
(HER-2/neu). Рекомедуемая доза лапатиниба составляет
1250 мг 1 раз/сут, ежедневно. Лапатиниб принимают за 1 ч
до или через 1 ч после приема пищи.
• Бевацизумаб (авастин) – обладает антиангиогенными
свойствами и воздействует на лиганд рецептора
сосудистого эндотелиального фактора роста (VEGF).
Препарат назначают в дозе 10 мг/кг 1 раз в 2 недели в виде
в/в инфузии (90 минут), длительно.
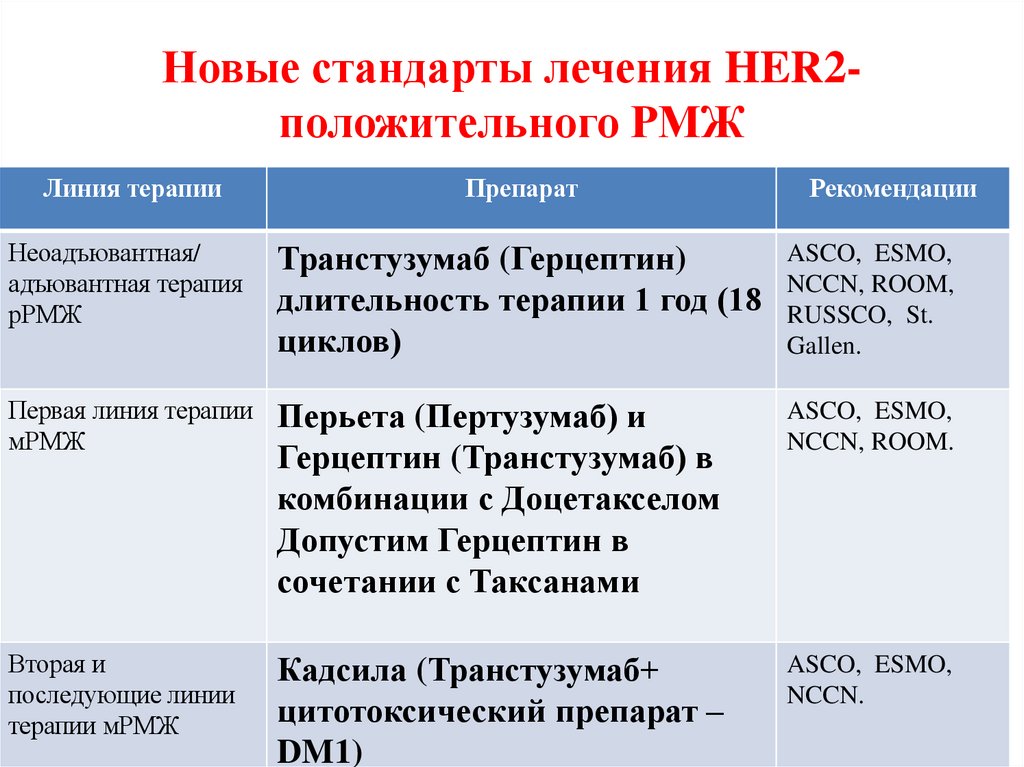
144. Новые стандарты лечения HER2-положительного РМЖ
Новые стандарты лечения HER2положительного РМЖЛиния терапии
Препарат
Рекомендации
Неоадъювантная/
адъювантная терапия
рРМЖ
Транстузумаб (Герцептин)
длительность терапии 1 год (18
циклов)
ASCO, ESMO,
NCCN, ROOM,
RUSSCO, St.
Gallen.
Первая линия терапии
мРМЖ
Перьета (Пертузумаб) и
Герцептин (Транстузумаб) в
комбинации с Доцетакселом
Допустим Герцептин в
сочетании с Таксанами
ASCO, ESMO,
NCCN, ROOM.
Вторая и
последующие линии
терапии мРМЖ
Кадсила (Транстузумаб+
цитотоксический препарат –
DM1)
ASCO, ESMO,
NCCN.
145. Критериями менопаузы являются:
• билатеральная овариэктомия;• возраст > 60 лет;
• возраст < 60 лет в отсутствие терапии тамоксифеном или
торемифеном и супрессии функции яичников: аменорея в
течение > 12 мес в сочетании с постменопаузальными
уровнями ФСГ, ЛГ и эстрадиола;
• возраст < 60 лет в процессе терапии тамоксифеном или
торемифеном: постменопаузальные уровни ФСГ, ЛГ и
эстрадиола.
• оценка функции яичников в период лечения аналогами
ГРГ невозможна.
• при сохранной менструальной функции на момент начала
химиотерапии (например, адъювантной) аменорея не
является достоверным признаком достижения менопаузы
и для назначения препаратов, разрешенных к применению
только у больных в менопаузе, необходимо выключение
функции яичников с помощью любого доступного способа
либо регулярное определение уровней ФСГ, ЛГ и
эстрадиола.
146. Факторы неблагоприятного прогноза
• Возраст ≤ 35 лет,• сохранная функция яичников после
адъювантной химиотерапии,
• Т3–4,
• поражение ≥ 4 подмышечных лимфоузлов,
• III степень злокачественности;
• положительный HER2,
• высокий Ki67.
NB – Назначаем гормонотерапию 10 лет
147. Бисфосфонаты в адъюванте
Больным гормонозависимым РМЖ в менопаузе(в т.ч. получающим овариальную супрессию)
могут
быть
назначены
бисфосфонаты
(золедронат 4 мг в/в 1 раз в 6 мес. в течение 3–
5 лет) как с целью профилактики остеопороза,
так и с целью снижения риска рецидива
болезни.
148. TisN0M0 (DCIS) Протоковая карцинома in situ
Рекомендуется с целью проведения хирургического лечения:органосохраняющая операция или мастэктомия. При
выполнении мастэктомии не требуются дополнительные
лучевая терапия или системная терапия.
При органосохраняющей операции возможно проведение
адъювантной гормонотерапии и адъювантной лучевой
терапии.
Проведение адъювантной цитотоксической терапии не
рекомендуется, если у больных DCIS.
149. Болезнь Педжета соска
Объём вмешательства на молочное железе зависит от объёмавыявленного поражения.
С учётом высокой частоты периферического поражения и
мультицентричности рекомендуется в качестве дополнительного
диагностического метода МРТ молочных желёз с контрастным
усилением.
Мастэктомия может выполняться как без реконструкции, так и с
первичной реконструкцией. В случае с первичной реконструкцией
мастэктомия выполняется в варианте кожесохраняющей мастэктомии (с
удалением соска и ареолы).
При наличии технической возможности показана биопсия сигнального
лимфатического узла, при отсутствии такой возможности не
рекомендуется выполнение подмышечной лимфаденэктомии.
150. Стадии I (Т1N0М0), IIa (Т2N0М0)
Первично операбельный РМЖ. Тактические вопросы, которые нужнорешить: возможность выполнения органосохраняющей операции,
возможность сохранения основной группы подмышечных и
подключичных лимфатических узлов с использованием технологии
биопсии сигнального лимфатического узла. При относительно крупной
первичной опухоли и невозможности выполнения органосохраняющей
операции с приемлемым эстетическим результатом рекомендовано
проведение неоадъювантной системной терапии.
Перенос химиотерапии на предоперационный период рекомендован
также в случаях планирования первичной реконструкции, поскольку
позволяет снизить частоту послеоперационных осложнений. В
абсолютном большинстве случаев показано проведение системной
адъювантной терапии; при выполнении органосохраняющих операций
и/или поражении лимфатических узлов показана лучевая терапия.
151. Стадии IIa (Т1N1М0), IIb (Т2N1М0, T3N0M0) и T3N1M0
Рекомендовано тактику лечения, определять с учетом биологическогоподтипа.
При трижды-негативном и HER2+ типах опухоли неоадъювантная
химиотерапия обладает высокой эффективностью – большая вероятность
достижения полного морфологического регресса и уменьшения объема
операции.
При отсутствии такового разработаны схемы адъювантной терапии,
позволяющие улучшить отдаленные результаты лечения у этой группы
больных.
При люминальных типах опухоли лечебная тактика определяется
индивидуально и основная задача неоадъювантного лечения – возможное
уменьшение объема операции.
В ряде случаев возможно выполнение кожесохраняющей мастэктомии с
возможной
одномоментной
реконструкцией
и
последующей
адъювантной системной терапией.
152. Стадии IIIa (Т0-3N2М0), IIIb (Т4N0-2М0), IIIc (T0-4N3M0)
Первичноиноперабельный
РМЖ.
Первым
этапом
лечения
рекомендовано проведение предоперационной системной терапии.
Оценка операбельности после системной терапии основывается на
оценке динамики размеров проявлений опухолевого процесса (первичной
опухоли, отёка кожи, регионарных метастазов).
План адъювантной системной терапии вырабатывается с учётом
исходных
и
послеоперационных
гистологических
и
иммуногистохимических характеристик опухоли.
Лучевая терапия показана во всех случаях.
153. Стадия IV. T0-4N0-3M1
Диссеминированная болезнь.Основное значение имеет системная терапия. Удаление
первичной опухоли с «чистыми» краями резекции
рекомендуется в случаях при метастатическом поражении
костей и наличии ответа на системное лечение.
Рекомендуется лучевая терапия в случаях осложнённого
метастатического поражения костей, метастатического
поражения головного мозга.
154. Лечения метастатического РМЖ
Единого стандарта лечения метастатического РМЖне существует.
Выбор варианта лекарственной терапии
осуществляется с учетом биологических маркеров
(РЭ и РП, HER2, Ki67), факторов риска и
клинико-анамнестических особенностей
больного.
Лечение метастатической болезни обычно
включает химио- и (или) гормонотерапию,
которые должны дополняться таргетной
терапией по показаниям
155. HER2+местнорецидивирующий или метастатический РМЖ
HER2+ мРМЖ:• 1-я линия – транстузумаб+пертузумаб+доцетаксел;
• 2-я линия –
транстузумаб эмтанзин
• 3-я линиялапатиниб+капецитабин
• 4-я лини и последующие линии- клинические
исследования, (Энхерту)
Каждая линия терапии проводится до однозначного
прогрессирования или неприемлемой токсичности. Эхокардиография 1 раз в 3 мес.
156. HER2+местнорецидивирующий или метастатический РМЖ
HER2+ мРМЖ:С солидными метастазами в головной мозг
показано хирургическое лечение и/или лучевое.
При наличии метастазов в другие органы
продолжить схемы ХТ.
При костных метастазах – введение бисфосфонатов
или деносумаба
Лекарственнными
опциями
с
доказанной
эффективностью при метастазах в головной мозг
являются tucatinib- или neratinib-cодержащие схемы
ХТ –нет регистрации в РФ
157. HR+HER2-местнорецидивирующий или метастатический РМЖ
HR+HER2- мРМЖ: определение подтипа именструального статуса
Мутацию гена PIK3CA
При сохраненной функции яичников – овариальная
супрессия
При наличии мутаций гена PIK3CA и резистентности
к ГТ рекомендуется терапия ингибиторами PIK3CA с
фульвестрантом (при нормальном уровне глюкозы
крови)
3-я линия монотерапия абемациклибом
158. HR+HER2- мРМЖ
1-я линия-при раннем рецидиве менее 1 года после окончанияадъювантного лечения -Ингибиторы CDK4/6 (паблоциклиб+фульвестрант;
рибоциклиб+ фульвестрант;абемациклиб+фульвестрант(Mts гол мозг);
алпелесиб+фульвестрант (для PIK3CA+); эверолимус+экземестан;
эверолимус+фулвестрант)
При позднем рецидиве (паблоциклиб+ингибиторы ароматазы;
рибоциклиб+ингибиторы ароматазы/фульвестрант (младше 65 лет);
абемациклиб+ингибиторы
ароматазы
(Mts
гол
мозг);
моногормонотерапия (тамоксифен, экземестан, торемифен, летрозол,
анастразол, фульвестрант)
2-я линия- паблоциклиб+фульвестрант; рибоциклиб+фульвестрант;
абемациклиб+фульвестрант (мts в гол мозг); алпелисиб+фульвестрант
(для PIK3CA+); эверолимус+экземестан; эверолимус+фульвестрант;
фульвестрант
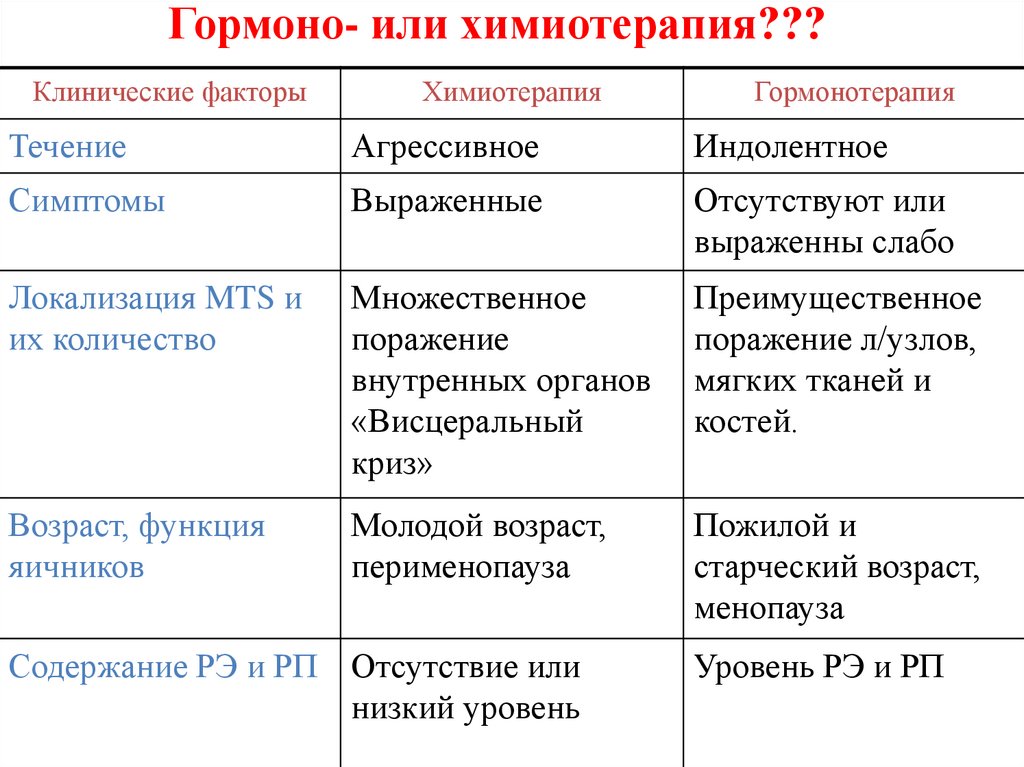
159. Гормоно- или химиотерапия???
Клинические факторыХимиотерапия
Гормонотерапия
Течение
Агрессивное
Индолентное
Симптомы
Выраженные
Отсутствуют или
выраженны слабо
Локализация MTS и
их количество
Множественное
поражение
внутренных органов
«Висцеральный
криз»
Преимущественное
поражение л/узлов,
мягких тканей и
костей.
Возраст, функция
яичников
Молодой возраст,
перименопауза
Пожилой и
старческий возраст,
менопауза
Содержание РЭ и РП Отсутствие или
низкий уровень
Уровень РЭ и РП
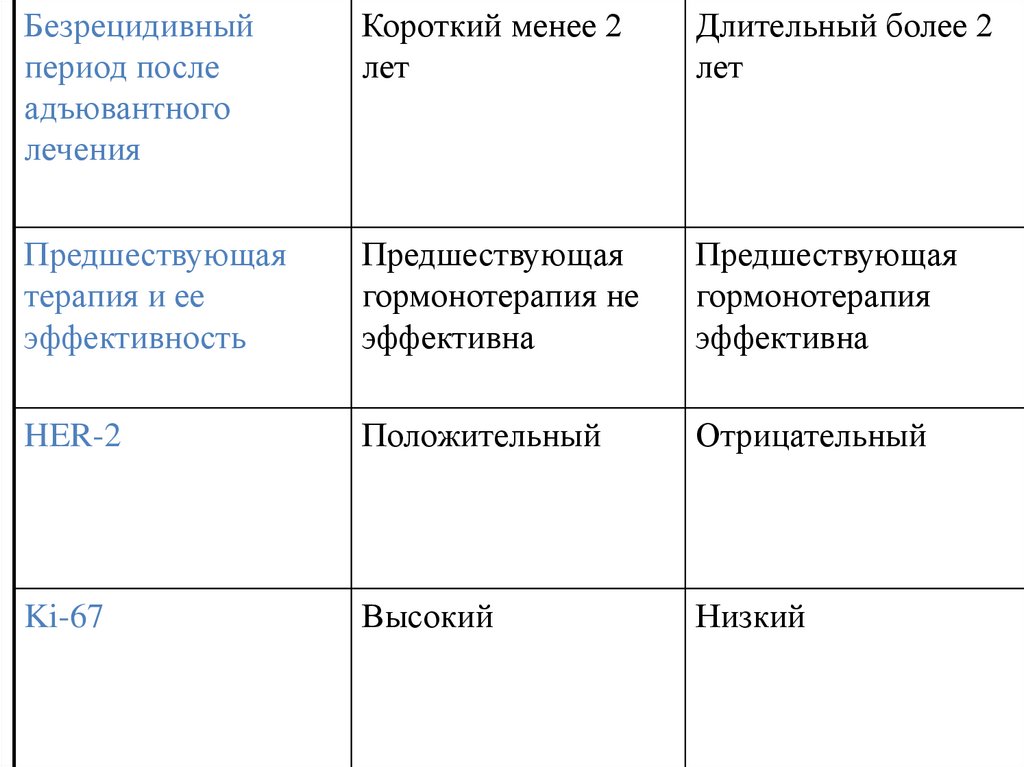
160.
Безрецидивныйпериод после
адъювантного
лечения
Короткий менее 2
лет
Длительный более 2
лет
Предшествующая
терапия и ее
эффективность
Предшествующая
гормонотерапия не
эффективна
Предшествующая
гормонотерапия
эффективна
HER-2
Положительный
Отрицательный
Ki-67
Высокий
Низкий
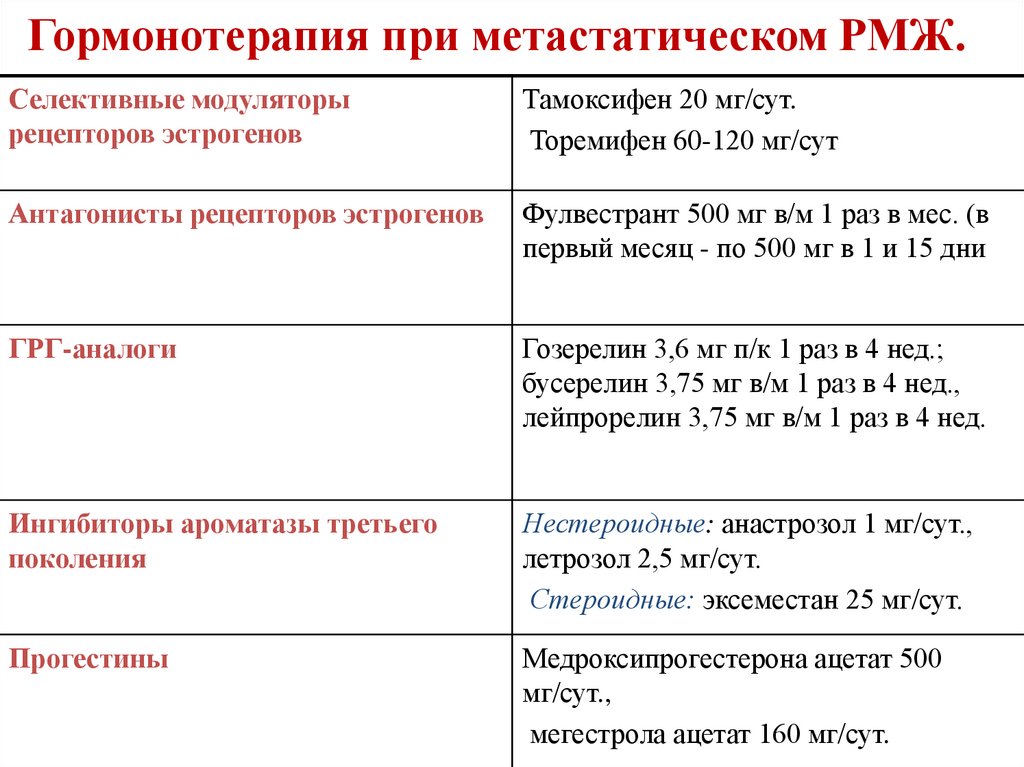
161. Гормонотерапия при метастатическом РМЖ.
Селективные модуляторырецепторов эстрогенов
Тамоксифен 20 мг/сут.
Торемифен 60-120 мг/сут
Антагонисты рецепторов эстрогенов
Фулвестрант 500 мг в/м 1 раз в мес. (в
первый месяц - по 500 мг в 1 и 15 дни
ГРГ-аналоги
Гозерелин 3,6 мг п/к 1 раз в 4 нед.;
бусерелин 3,75 мг в/м 1 раз в 4 нед.,
лейпрорелин 3,75 мг в/м 1 раз в 4 нед.
Ингибиторы ароматазы третьего
поколения
Нестероидные: анастрозол 1 мг/сут.,
летрозол 2,5 мг/сут.
Стероидные: эксеместан 25 мг/сут.
Прогестины
Медроксипрогестерона ацетат 500
мг/сут.,
мегестрола ацетат 160 мг/сут.
162. Гормонотерапия при метастатическом РМЖ.
Фулвестрант + палбоциклибФулвестрант 500 мг в/м 1 раз в мес.
(в первый месяц – по 500 мг в 1-й и
15-й дни) + палбоциклиб 125 мг/сут.
внутрь в 1–21-й дни, интервал 1 нед.
Летрозол + палбоциклиб
Летрозол 2,5 мг/сут. внутрь
ежедневно + палбоциклиб 125 мг/сут.
внутрь в 1-21-й дни, интервал 1 нед.
Ингибиторы ароматазы
третьего поколения
(стероидные)
Эксеместан 25 мг/сут. внутрь
ежедневно
Эксеместан + эверолимус
Эксеместан 25 мг/сут. внутрь
ежедневно + эверолимус 10 мг/сут.
внутрь ежедневно
163.
Прогрессирование болезни в результате трехпоследовательных линий гормонотерапии
свидетельствует об устойчивости к данному
виду лечения и необходимости назначения
химиотерапии
164.
Метастатический трижды негативный РМЖ (мТНРМЖ)(HR-HER2-мРМЖ)
У пациенток не получающих терапию по поводу метастазов
необходимо определить с помощью теста Ventana SP142
уровень экспрессии PD-L-1≥1% на иммунокомпетентных
клетках – назначаем атезолизумаб+наб-паклитаксел
Если + BRCA1/2 – олапариб или талазопариб при
предлеченных метастазах.
Если нет мутаций, то бевацизумаб+таксаны+платина
165. Стоимость лечения РМЖ
По данным ФОМС г. Москвы, лечение запущенногорака молочной железы III и IV стадии в 14 раз
дороже.
166. А Вы прошли обследование молочных желез ???
167. Основные принципы лечения РМЖ на фоне беременности
Выбор метода лечения в зависимости от стадиизаболевания, биологического подтипа опухоли,
гестационного возраста плода и решения матери о
сохранении беременности;
Комплексный подход, важнейшим этапом которого
является хирургическое лечение;
Планирование лечения с учетом мнения онколога,
химиотерапевта, акушера, неонатолога, пациентки и
ее супруга.
168. Обследование
сбор анамнеза и осмотр;
общий и биохимический анализы крови;
ЭКГ, ЭХО-КГ (по показаниям);
УЗИ молочных желез и регионарных зон;
УЗИ брюшной полости и малого таза;
билатеральную маммографию (возможна при абдоминальной защите плода);
R-графию грудной клетки (возможна при абдоминальной защите плода) –по
показаниям;
МРТ молочных желез без контрастирования (возможна по показаниям во II и III
триместрах);
МРТ органов грудной и брюшной полости без контрастирования (возможна по
показаниям во II и III триместрах);
КТ, радиоизотопное исследование костей, ПЭТ-КТ в период беременности
противопоказано. Возможно выполнение МРТ без контрастирования для
диагностики метастазов в костях;
биопсия опухоли с патоморфологическим и ИГХ исследованием опухолевой ткани
проводится на любом сроке беременности;
генетическое обследование с определением возможных мутаций генов BRCA1/2,
CHEK2 у всех беременных пациенток;
консультация психолога – по показаниям.
169. Рак и беременность
Вид леченияВозможный объем лечения
Хирургический
Радикальная мастэктомия (сторожевой л/узел –меченные
коллоиды?)
Лучевая терапия (не более 6
мес. после РМЭ)
По рекомендациям ESMO (2013) и NCCN (2014) лучевая
терапия
с
адъювантной
целью
как
этап
комбинированного/комплексного лечения может быть
проведена больным РМЖ только после родоразрешения
Химиотерапия
I – тератогенез, самопроизвольный аборт, ВЗРП и т.д. ПХТ
проводят начиная со II (12-14 нед) триместра до 34-35
недель, родоразрешение не менее 2 недель после
окончания ПХТ.
Назначение паклитаксела 1 раз в 7 дней не требует
введения высоких доз дексаметазона в целях пре- и
постмедикации, а также гранулоцитарного
колониестимулирующего фактора (G-CSF)
Гормонотерапия
После родоразрешения
170. Алгоритм выбора терапии
ТриместрХирургическое лечение
Адъювантная лекарственная терапия
I
При желании сохранения Адъювантная химиотерапия во II триместре ±
беременности –
адъювантная лучевая терапия после р/р ±
мастэктомия
адъювантная гормонотерапия после р/р
II/III ранний
Мастэктомия, или
органосохраняющая
операция, или
неоадъювантная
химиотерапия
Адъювантная химиотерапия + адъювантная
лучевая терапия после р/р ± адъювантная антиHER-2-терапия после р/р + адъювантная
гормонотерапия после р/р
III поздний
Мастэктомия или
органосохраняющая
операция
Адъювантная химиотерапия + адъювантная
лучевая терапия после р/р ± адъювантная антиHER- 2-терапия после р/р ± адъювантная
гормонотерапия после р/р
171. Скрининг РМЖ в РФ
в 20-39 лет - самообследование молочной
железы ежемесячно, ежегодно ультразвуковое
исследование (УЗИ), особенно если женщина
входит в группу риска;
• однократно в возрасте 35-39 лет выполнить
маммографию;
с 40 лет - самообследование ежемесячно,
ежегодно – маммографию в двойном прочтении.
В рамках реализации Национального проекта «Здоровье» Министерством здравоохранения и социального
развития 15.03.2006 г. по приказу №154 «О мерах по оказанию медицинской помощи при заболеваниях молочной
железы»







































































































 Медицина
Медицина








