Похожие презентации:
Бес мүшелі гетерофункциялық қосылыстар
1.
ҚАЗАҚСТАН-РЕСЕЙ МЕДИЦИНАЛЫҚУНИВЕРСИТЕТІ
ТАҚЫРЫП:БЕС МҮШЕЛІ ГЕТЕРОФУНКЦИЯЛЫҚ
ҚОСЫЛЫСТАР
ОРЫНДАҒАН: АЛПАМЫС НҰРТІЛЕУ, ҚАЛИБЕК
АЛДИЯР, ХАБИБУЛЛАЕВ МҰРАТЖАН, ӘЛІХАН
БОТАХАН, САЛИК АРАЙ, МҰСТАФА ӘСЕЛ
ФАКУЛЬТЕТ: МЕДИЦИНА
ТОП: 102Б
2.
БЕС МҮШЕЛІ ГЕТЕРОФУНКЦИЯЛЫҚҚОСЫЛЫСТАР ЖАЛПЫ
СИПАТТАМАСЫ
Тұйық тізбектің құрамында көміртегі атомдарынан басқа бір немесе бірнеше басқа атомдар
болатын қосылыстар гетероциклды қосылыстар деп аталады. Олар әртүрлі болуы мүмкін,
табиғатта кең тараған гетероциклдарға бес және алты мүшелілер жатады.
Гетероатомның ролін азот, күкірт, оттегі және т.б. атқаруы мүмкін. Гетероциклдар қаныққан,
қанықпаған және ароматты болып бөлінеді. Олардың ішінде физиологиялық белсенді заттардың
және дәрі дәрмектердің құрамында кездесетін ароматтылар табиғатта кең тараған. Бес мүшелі
бір гетероатомды гетероциклдарға пиррол, фуран және тиофен жатады. Олар өзара генетикалық
байланыста болатын ароматты қосылыстар болып табылады.
3.
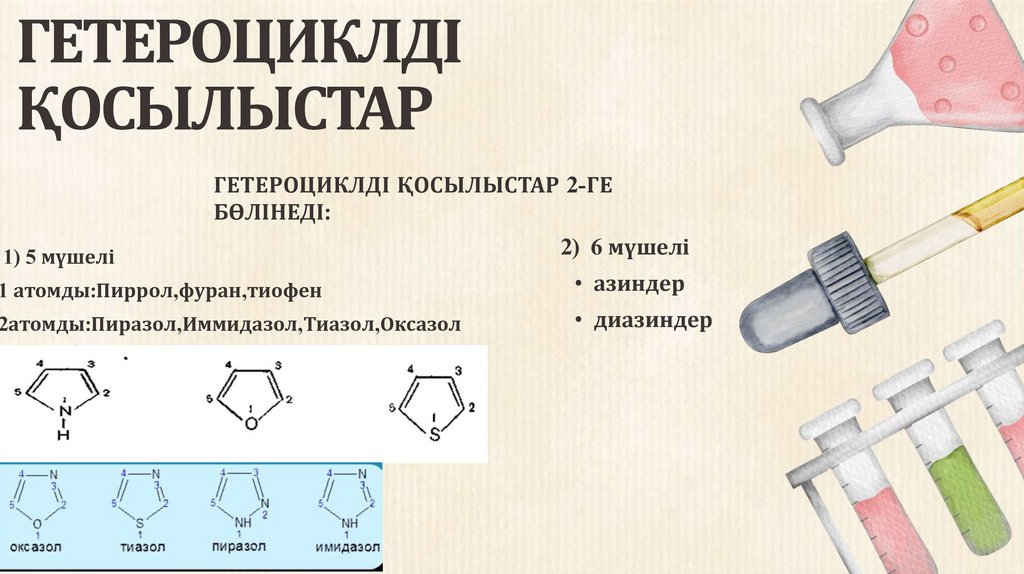
ГЕТЕРОЦИКЛДІҚОСЫЛЫСТАР
ГЕТЕРОЦИКЛДІ ҚОСЫЛЫСТАР 2-ГЕ
БӨЛІНЕДІ:
1) 5 мүшелі
2) 6 мүшелі
1 атомды:Пиррол,фуран,тиофен
• азиндер
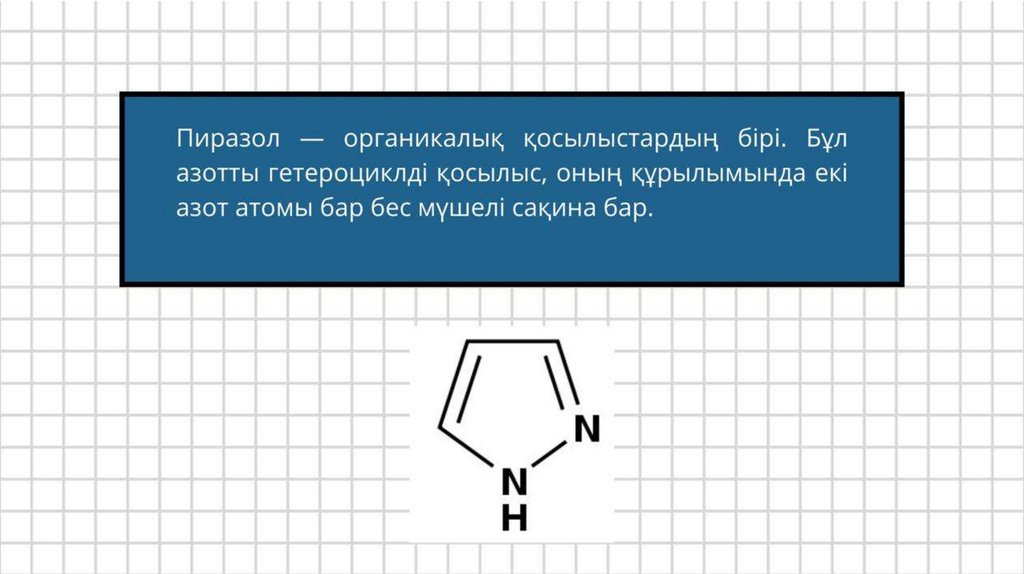
2атомды:Пиразол,Иммидазол,Тиазол,Оксазол
• диазиндер
4.
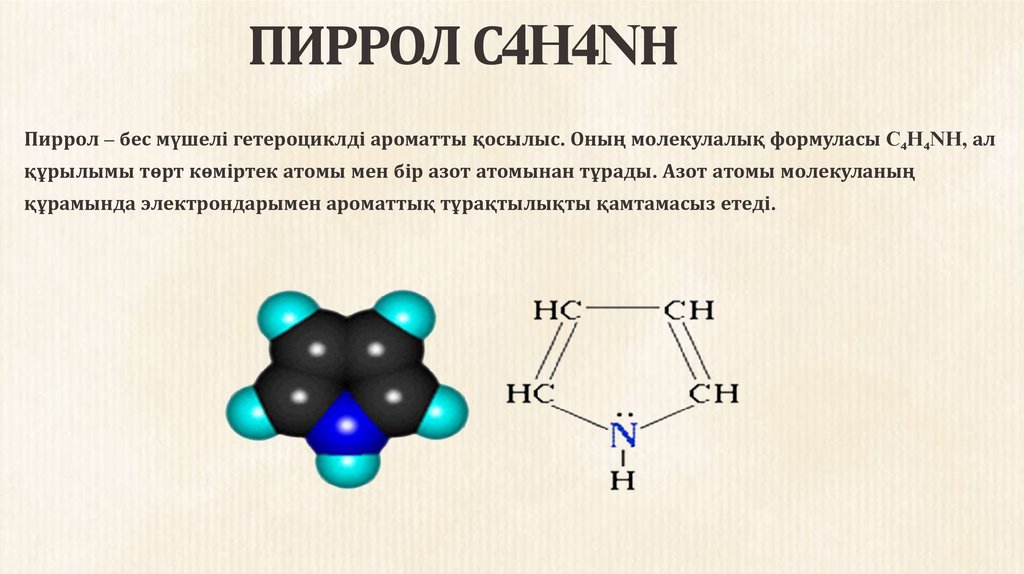
ПИРРОЛ С4H4NНПиррол – бес мүшелі гетероциклді ароматты қосылыс. Оның молекулалық формуласы C₄H₄NH, ал
құрылымы төрт көміртек атомы мен бір азот атомынан тұрады. Азот атомы молекуланың
құрамында электрондарымен ароматтық тұрақтылықты қамтамасыз етеді.
5.
6.
7.
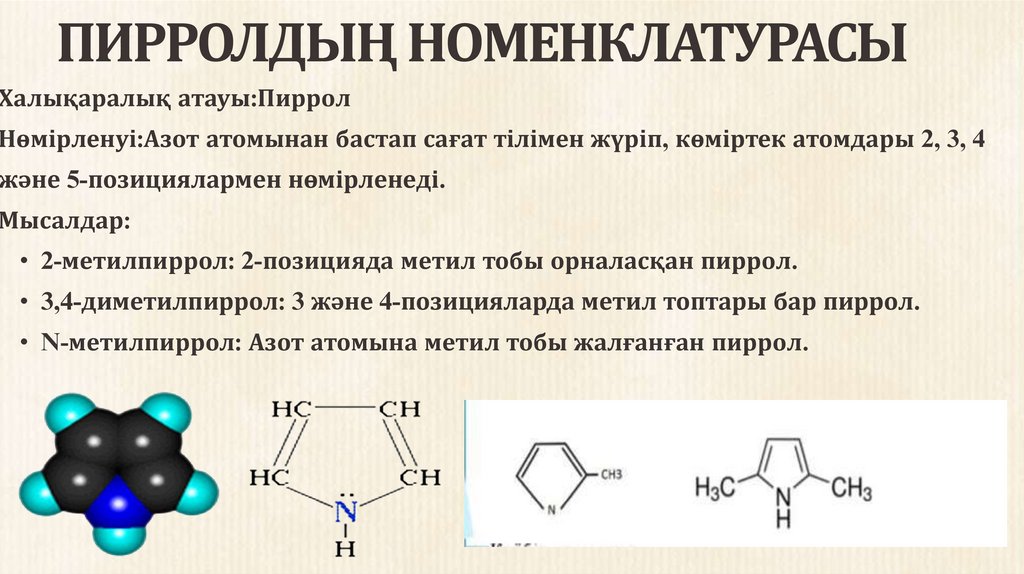
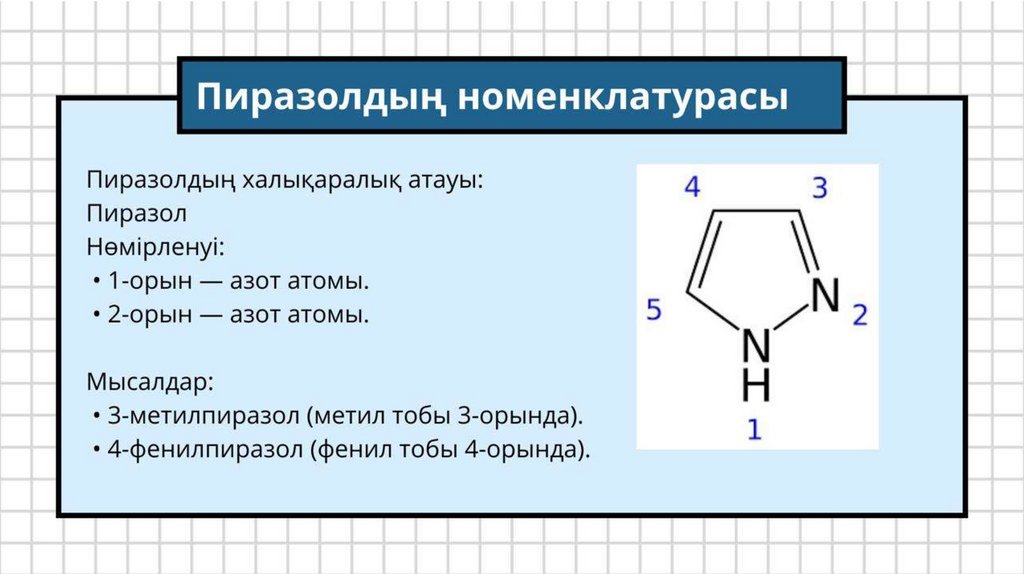
ПИРРОЛДЫҢ НОМЕНКЛАТУРАСЫХалықаралық атауы:Пиррол
Нөмірленуі:Азот атомынан бастап сағат тілімен жүріп, көміртек атомдары 2, 3, 4
және 5-позициялармен нөмірленеді.
Мысалдар:
• 2-метилпиррол: 2-позицияда метил тобы орналасқан пиррол.
• 3,4-диметилпиррол: 3 және 4-позицияларда метил топтары бар пиррол.
• N-метилпиррол: Азот атомына метил тобы жалғанған пиррол.
8.
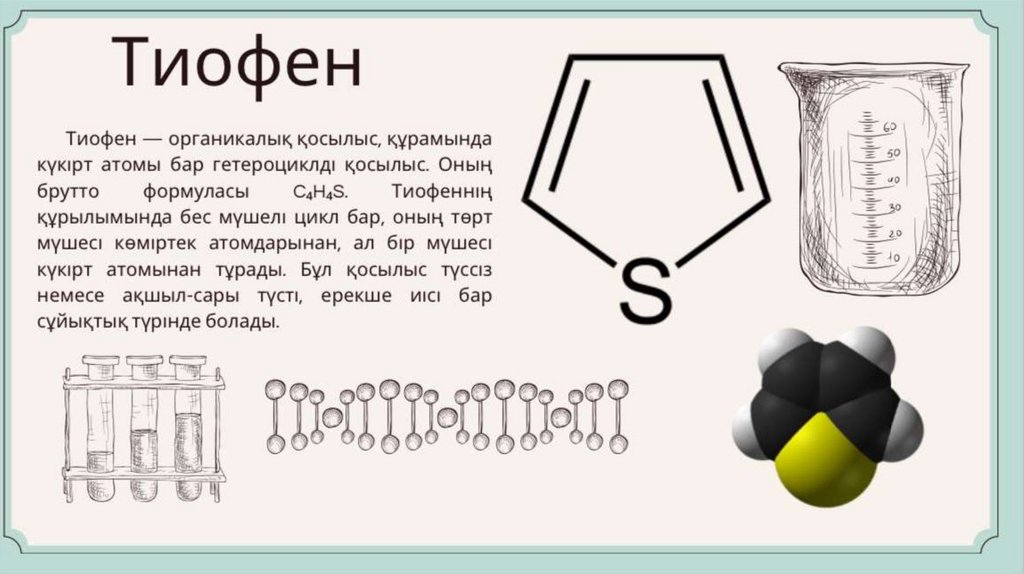
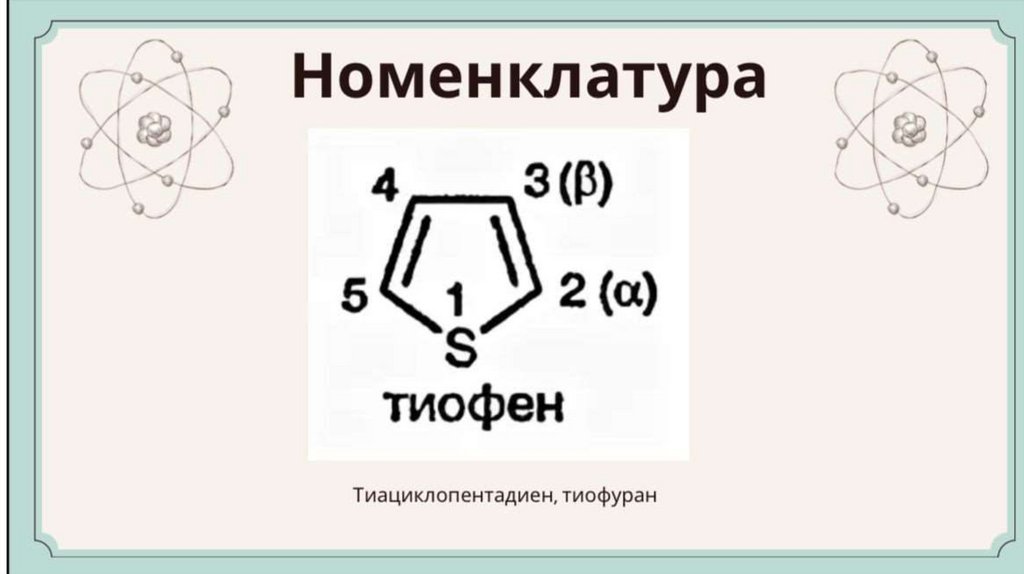
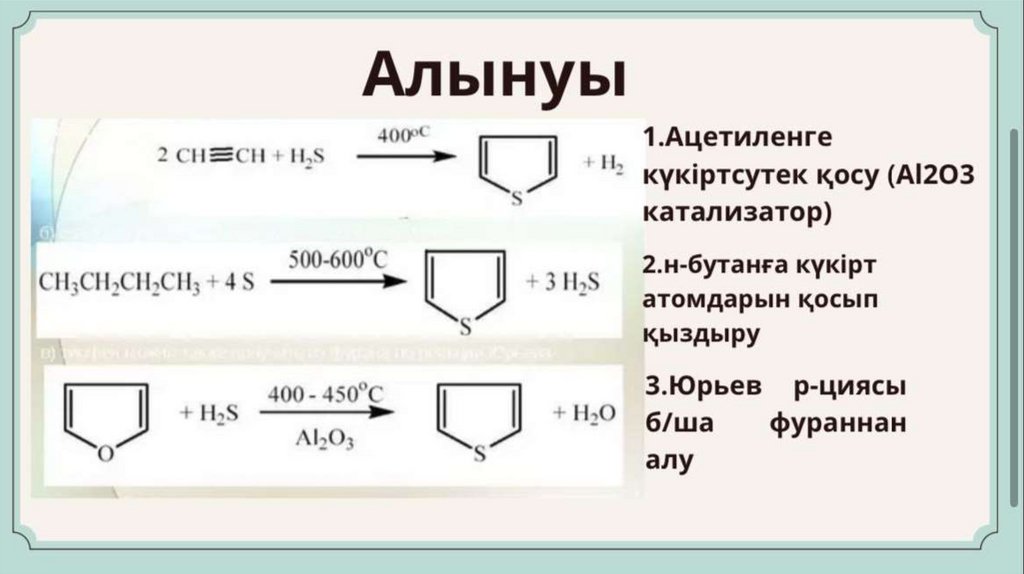
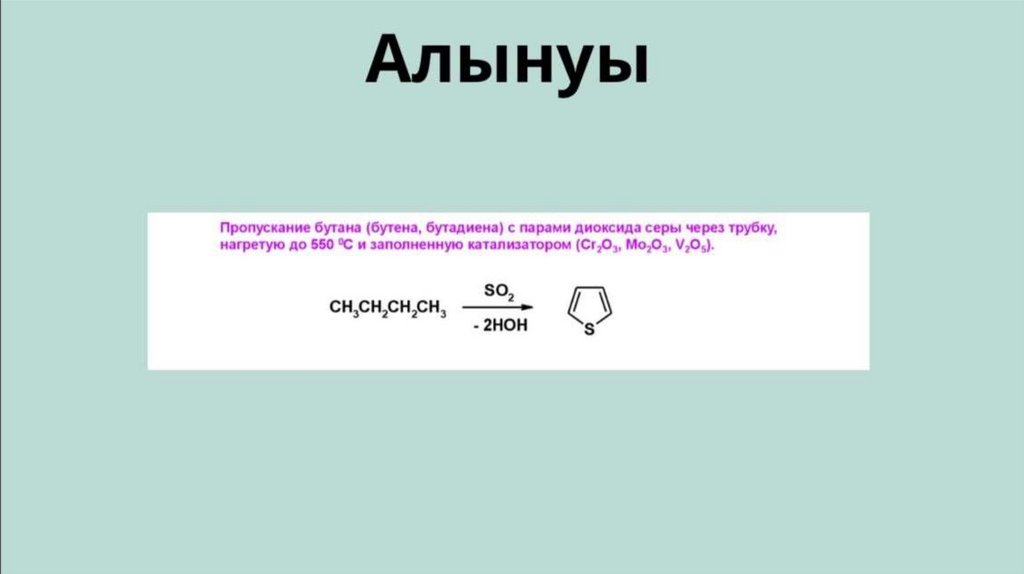
ТИОФЕН/Номенклатура ережелері1. Сақинадағы атомдарды нөмірлеу:
• Нөмірлеу күкірт атомынан басталады (ол әрдайым №1 позиция).
• Көміртек атомдары күкірт атомынан бастап 2, 3, 4 деп белгіленеді.
2. Субституенттердің орналасуын көрсету:
• Субституенттер сақинадағы нөмірленген позициялар арқылы
көрсетіледі.
Мысалы, 2-метилтиофен, 3-бромтиофен.
• Егер бірнеше орынбасар болса, олардың орналасу реті нөмірлермен
және алфавиттік тәртіппен көрсетіледі.
9.
10.
11.
ПИРРОЛДЫҢ ФИЗИКАЛЫҚ ҚАСИЕТТЕРІ• Күйі: Түссіз сұйықтық, ауада уақыт өте сарғыш түске айналуы мүмкін.
• Иісі: Әлсіз жағымсыз иіс, сәл аммиакты еске түсіреді.
• Тығыздығы: 0,967 г/см³
• Еруі:
⚬ Суда нашар ериді, себебі пирролдың полярлығы төмен.
⚬ Органикалық еріткіштерде (этанол, эфир) жақсы ериді.
• Балқу температурасы: -23°C.
• Қайнау температурасы: 129°C.
Пирролдың физикалық қасиеттері оның биологиялық және химиялық қолданылу мүмкіндіктерін
анықтайды. Органикалық синтезде және электрохимияда оның ерігіштігі мен реактивтілігі
маңызды рөл атқарады.
12.
13.
14.
15.
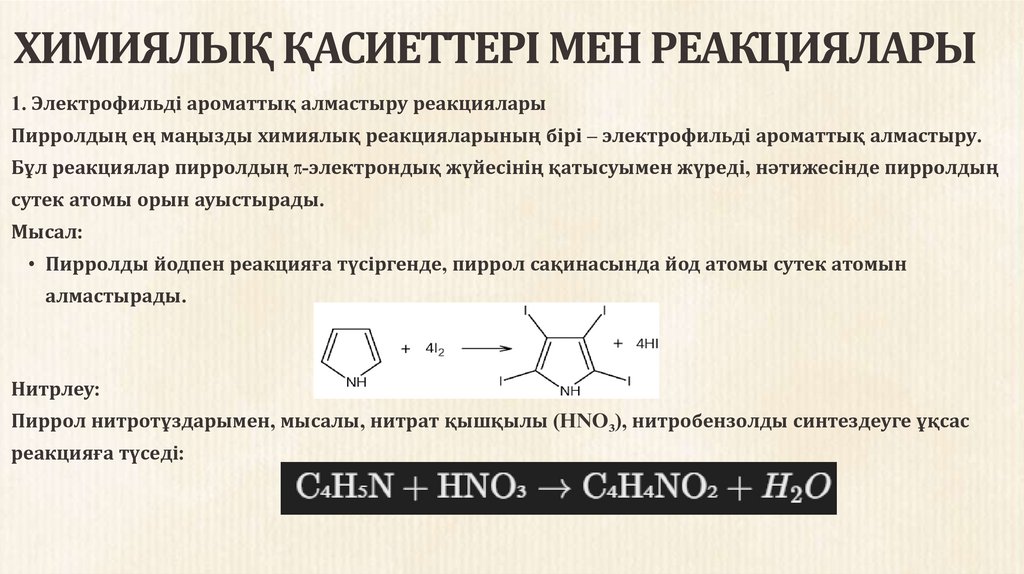
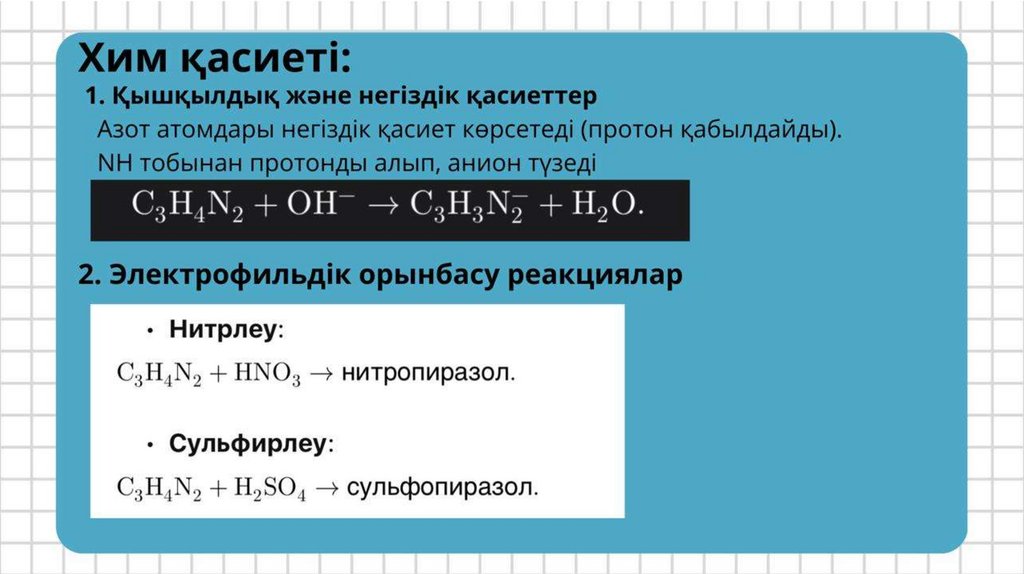
ХИМИЯЛЫҚ ҚАСИЕТТЕРІ МЕН РЕАКЦИЯЛАРЫ1. Электрофильді ароматтық алмастыру реакциялары
Пирролдың ең маңызды химиялық реакцияларының бірі – электрофильді ароматтық алмастыру.
Бұл реакциялар пирролдың π-электрондық жүйесінің қатысуымен жүреді, нәтижесінде пирролдың
сутек атомы орын ауыстырады.
Мысал:
• Пирролды йодпен реакцияға түсіргенде, пиррол сақинасында йод атомы сутек атомын
алмастырады.
Нитрлеу:
Пиррол нитротұздарымен, мысалы, нитрат қышқылы (HNO₃), нитробензолды синтездеуге ұқсас
реакцияға түседі:
16.
ХИМИЯЛЫҚ ҚАСИЕТТЕРІ МЕН РЕАКЦИЯЛАРЫ2. Нуклеофильді алмастыру реакциялары
Пиррол молекуласында азот атомының жалғыз жұп электрондары оны нуклеофильді етеді, және ол
бірқатар қосылыстармен нуклеофильді алмастыру реакцияларына қатыса алады.
Мысал:
• Метилдеу:
Пиррол азотына метил тобы қосылғанда N-метилпиррол түзілетіні белгілі.
3.Қалпына келтіру реакциялары
Пирролдың азот атомындағы электрондар оның қалпына келтіру реакцияларында маңызды рөл
атқарады.
Қалпына келтіру:
Пиррол редукторлармен (мысалы, сутек) әрекеттесіп, пирролдың қаныққан туындыларын (мысалы,
дигидропиррол) түзуі мүмкін.
17.
ХИМИЯЛЫҚ ҚАСИЕТТЕРІ МЕН РЕАКЦИЯЛАРЫ4. Аминоқышқылдармен реакциялар
Пиррол азот атомының жалғыз жұп электрондарымен аминоқышқылдармен немесе аминдермен
реакцияға түсіп, пирроламиндер немесе пиррол туындыларын түзуі мүмкін.
Мысал:
• Аминдермен әрекеттесу:
• Пирролды аминдермен реакцияға түсіргенде аминопирролдар түзіледі.
18.
19.
20.
21.
22.
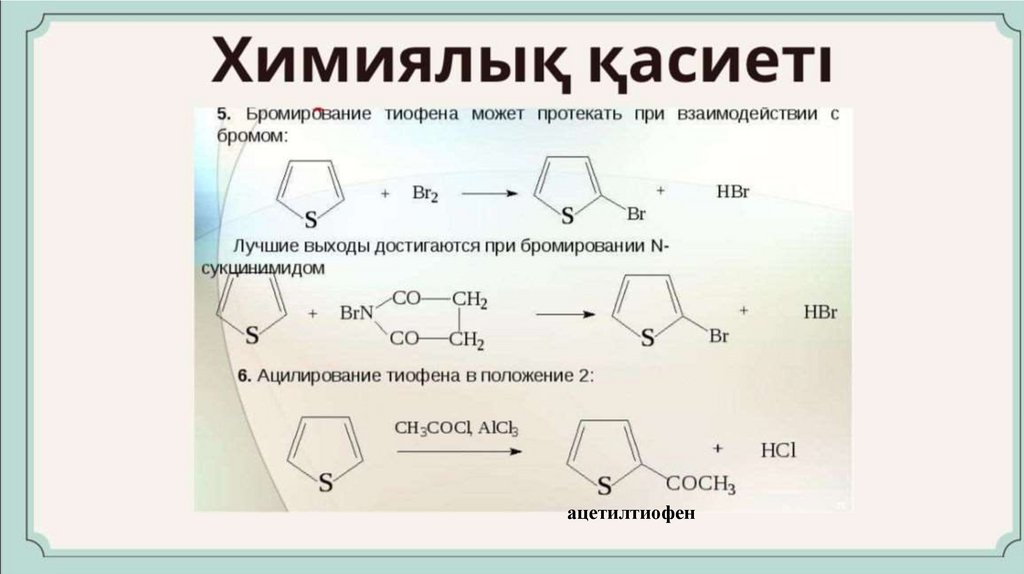
ацетилтиофен23.
ПИРРОЛДЫҢ ИЗОМЕРИЯСЫПирролдың изомериясы оның туындыларының құрылымына және орынбасарлардың орналасуына
байланысты. Өйткені пирролдың өзі қарапайым бес мүшелі сақина, онда изомерия түрлері
шектеулі. Бірақ оның туындылары үшін бірнеше негізгі изомерия түрлері байқалады.
1. Құрылымдық изомерия:
Бұл изомерия пиррол сақинасына жалғанған орынбасарлардың әртүрлі позицияларда орналасуына
байланысты болады.
Мысал:
• 2-метилпиррол: Метил тобы 2-позицияда.
• 3-метилпиррол: Метил тобы 3-позицияда.
Бұл екі қосылыс пиррол сақинасында метил тобының орналасуына қарай ажыратылады.
24.
ПИРРОЛДЫҢ ИЗОМЕРИЯСЫ2. Позициялық изомерия:
Орынбасарлардың пиррол сақинасындағы орналасуы әртүрлі болған кезде байқалады.
Мысал:
• 2,4-диметилпиррол: Метил топтары 2 және 4-позицияда орналасқан.
• 2,3-диметилпиррол: Метил топтары 2 және 3-позицияда орналасқан.
3. Таутомерлік изомерия:
Пирролда азот атомындағы сутек атомы сақина ішіндегі көміртек атомына ауыса алады. Бұл
процесс көбінесе субститутталған пирролдарда кездеседі және таутомерлік изомерия деп аталады.
Мысал:
• Пирролдың таутомерлері:
25.
ПИРРОЛДЫҢ ИЗОМЕРИЯСЫ4. Функционалдық изомерия:
Бұл изомерия пиррол туындыларындағы әртүрлі функционалдық топтардың орналасуымен
байланысты.
Мысал:
• 2-карбоксипиррол және 3-карбоксипиррол: Карбоксил тобы (–COOH) 2 немесе 3-позицияда
орналасқан.
5. Стереоизомерия:
Пиррол
сақинасының
өзінде
стереоизомерия
болмайды,
бірақ
пиррол
туындыларында
стереоизомерия байқалуы мүмкін. Бұл көбінесе сақинаға жалғанған орынбасарлар болғанда орын
алады.
26.
27.
28.
29.
ПИРРОЛДЫҢ АЛЫНУЫПирролды жануарлардың сүйектерін құрғақ айдағанда бөлініп алынған. 1834ж. Рунге аз мөлшерде
тас көмір шайырында болатынын анықтаған, одан фракциялық айдау арқылы алынады.
Пирролдың құрылымын 1870ж. А. Байер дәлелдеген. Өндірісте фуран мен аммиакты әрекеттестіріп
алады. Пирролда екіншілік азот атомы бар, екіншілік аминдерге ұқсас болғанымен, негіздік қасиеті
әлсіз, қышқылдармен тұрақты тұз түзбейді. Себебі, азот атомының жұп электроны ароматтыэлектронды жүйе құруға қатысады Пиррол түссіз сұйықтык, суда нашар ериді, ауада тез тотығып,
қоңырайып кетеді.
30.
ПИРРОЛДЫҢ АЛЫНУЫ1. Аммоний тұздарын және фурфуролды қолдану
Бұл ең кең тараған және өндірістік маңызы бар әдістердің бірі.
• Фурфурол (C₅H₄O₂) аммоний тұздарымен қыздырылғанда пиррол түзіледі:
• Шарттары:
• Реакция
200–300°C
температурада,
катализаторлардың
(қышқылдар
қатысуымен жүреді.
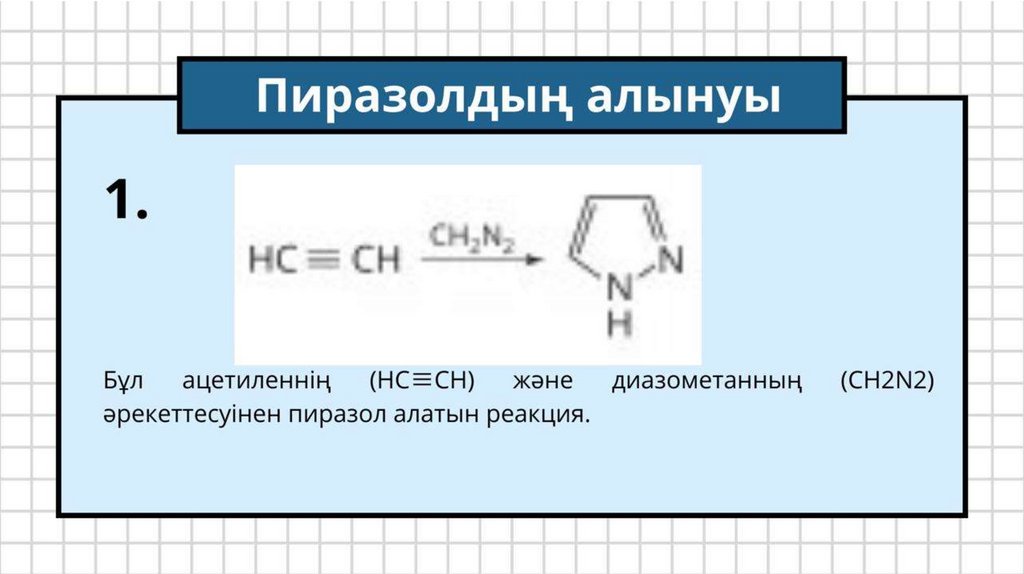
2. Ацетиленді және аммиакты қолдану
Ацетиленнің аммиакпен әрекеттесуі пиррол алудың тиімді әдістерінің бірі.
Ацетилен (C₂H₂) аммиакпен қыздырылғанда пиррол түзіледі:
немесе
негіздер)
31.
ПИРРОЛДЫҢ АЛЫНУЫ3. Пирролидонның дегидрленуі
Пирролидон пирролға дейін дегидрленіп, оны алу әдісі ретінде қолданылуы мүмкін.
Бұл реакция катализатордың қатысуымен (мысалы, платина) және жоғары температурада жүреді.
4. Табиғи көздерден алу
Пиррол табиғи қосылыстардың (мысалы, гемоглобин, хлорофилл) деградациясы арқылы алынуы
мүмкін.
Процесс:
• Табиғи қосылыстарды ферментативті немесе химиялық әдістермен ыдырату арқылы пиррол
алынады. Бұл әдіс көбінесе зертханалық деңгейде қолданылады.
32.
33.
34.
35.
36.
37.
БИОЛОГИЯЛЫҚ ҚАСИЕТІПиррол – табиғи және синтетикалық қосылыстардың құрамында кездесетін маңызды гетероциклді қосылыс. Оның
биологиялық маңызы көптеген табиғи молекулалардың құрамында болуымен және олардың қызметіне тікелей әсер
етуімен сипатталады.
1. Пирролдың табиғи қосылыстардағы рөлі
Гем тобы:
Пиррол сақиналарының төрт бірлігінен тұратын порфирин сақинасы мен темір атомы гем молекуласының негізін құрайды.
Гем:
• Гемоглобиннің құрамында болып, қан арқылы оттегіні тасымалдауға қатысады.
• Миоглобиннің құрамында бұлшықет тіндерінде оттегіні сақтау қызметін атқарады.
Хлорофилл молекуласы өсімдіктерде кездеседі және фотосинтез процесінде күн сәулесін сіңіріп, оны химиялық энергияға
түрлендіруге қатысады. Оның құрамында порфирин сақинасы мен магний ионы бар.
Витамин B12 (кобаламин) – құрамында пиррол сақинасы бар күрделі қосылыс. Ол қанның дұрыс түзілуіне, ДНҚ синтезіне
және нерв жүйесінің қызметін реттеуге қатысады.
Пиррол сақинасы табиғи алкалоидтардың құрамында болады.
Мысалы:
• Никотин – нерв жүйесіне әсер етеді.
• Пилокарпин – көз ауруларын емдеуде қолданылады.
38.
БИОЛОГИЯЛЫҚ ҚАСИЕТІ2. Пиррол негізіндегі пигменттер
• Билирубин және билевердин – гемнің ыдырауынан түзілетін пиррол туындылары.
• Билирубиннің деңгейі бауырдың жағдайын көрсетсе, билевердин антиоксиданттық қасиетке ие.
3. Ферменттер мен коферменттер
• Цитохромдар: Тыныс алу процесінде электрондарды тасымалдайды.
• Ферредоксиндер: Азотты байланыстыру және энергияны тасымалдау процестерінде маңызды рөл
атқарады.
4. Полимерлер және биосенсорлар
Пирролдан алынатын полимерлер (мысалы, полипиррол) биосенсорлар мен медициналық құрылғыларда
қолданылады. Олар биоүйлесімді және электр өткізгіш қасиетке ие.
5. Қосымша биологиялық рөлдері
• Иммундық жүйеде пиррол сақинасы бар молекулалар антиденелердің жұмысын жақсартады.
• Пиррол негізіндегі қосылыстар антиоксиданттық қасиетке ие, бұл бос радикалдарды бейтараптандыруда
маңызды.
• Гормондар биосинтезінде пиррол құрылымдары аралық өнім ретінде қатысады.
39.
40.
41.
МЕДИЦИНАЛЫҚ ҚАСИЕТІ1.Пиррол негізіндегі қосылыстардың қатерлі ісіктерді емдеудегі потенциалы да зерттелуде. Олар жасушалар
арасындағы байланыстарды бұзып, ісік жасушаларының өсуін тежейді.
2.Пиррол сақиналары бар молекулалар қабынуға қарсы әсер етуімен танымал. Олар қабыну белгілерін
төмендетуге және ауруды жеңілдетуге көмектеседі. Бұл әсер әсіресе буын ауруларында және тері
ауруларында пайдалы.
3.Пирролдың туындысы пирролидон молекулалары белгілі бір дәрілік препараттар ретінде қолданылады,
мысалы, ауырсынуды жеңілдету немесе қабынуды басу үшін. Бұл қосылыстардың тыныштандыратын
әсері бар.
4.Пиррол құрылымын қамтитын кейбір синтетикалық қосылыстар антибиотик ретінде қолданылуы мүмкін.
Олар бактерияларға қарсы әсер көрсетіп, инфекцияларды емдеуде қолданылады.
42.
43.
44.
45.
46.
47.
48.
49.
50.
51.
52.
53.
54.
55.
56.
57.
58.
59.
60.
61.
62.
63.
64.
65.
66.
67.
68.
69.
70.
71.
72.
73.
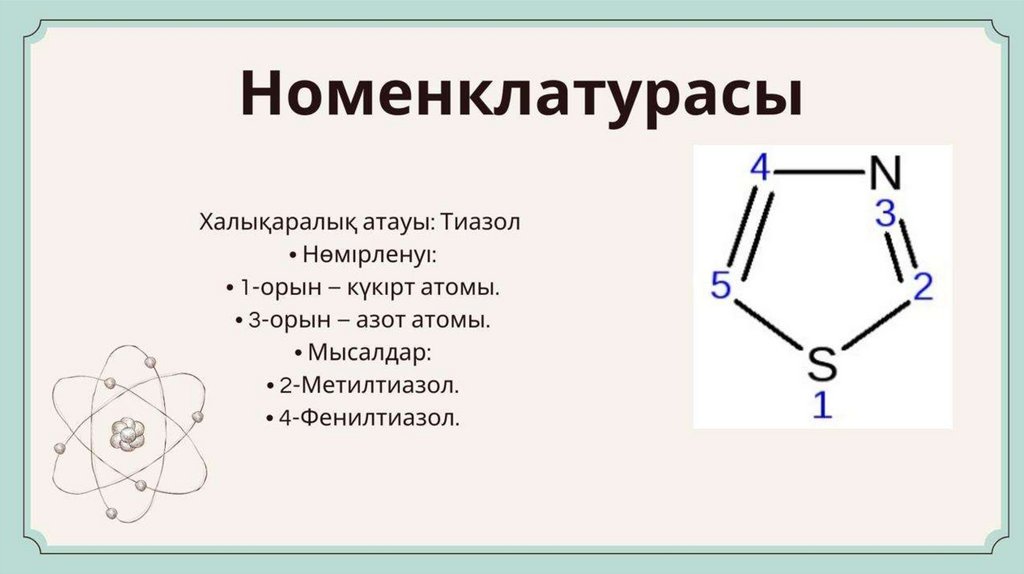
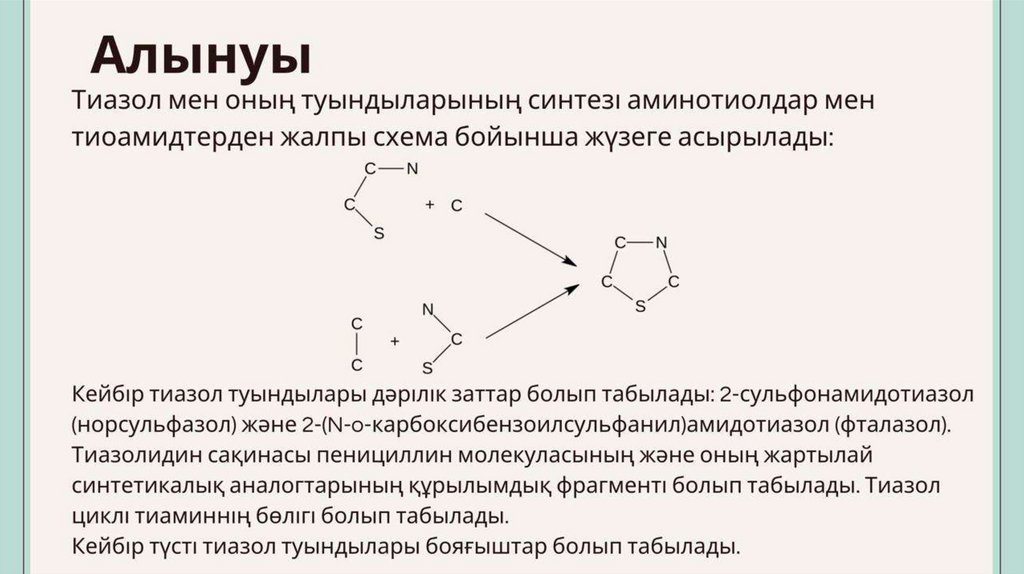
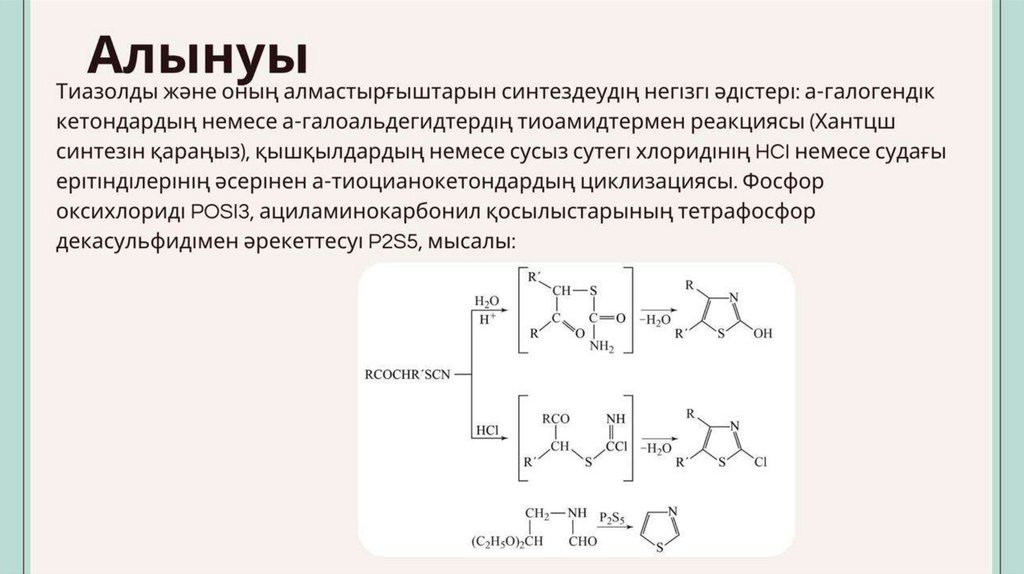
Тиазол74.
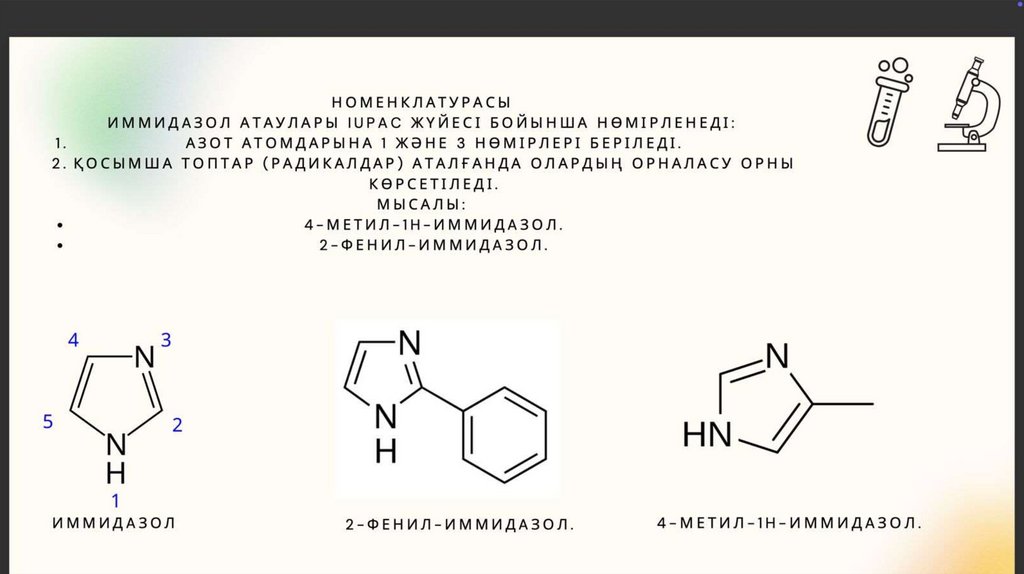
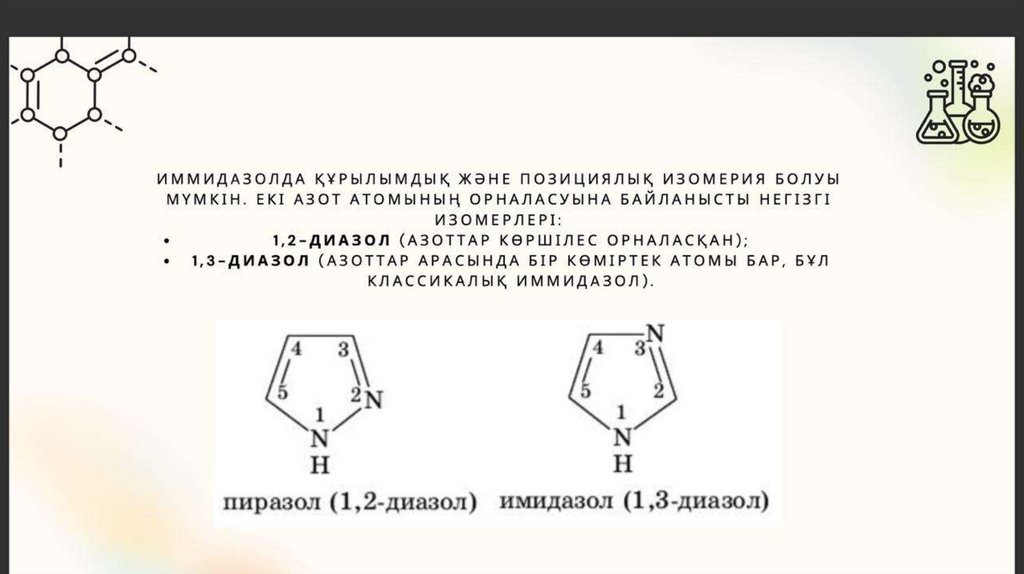
Имидазол75.
76.
77.
78.
79.
80.
81.
82.
83.
84.
85.
86.
87.
88.
89.
90.
91.
92.
ПАЙДАЛАНЫЛҒАН ӘДЕБИЕТТЕР1. Е. Жұбанов, Р. Жанғабылов. Органикалық химия. – Алматы: Мектеп, 2012.
2. Қ. А. Базарбаев, С. К. Ермұқанов. Органикалық қосылыстар химиясы. – Алматы:
Қазақ университеті, 2019.
3. Е. Баймағанбетов, А. Ахметов. Физикалық және органикалық химия. – Алматы:
Рауан, 2008.
4. Г. М. Железная, В. В. Титов. Гетероциклические соединения в органической химии.
– Санкт-Петербург: Лань, 2016.






























































 Химия
Химия








