Похожие презентации:
Анти-краун-эфиры
1.
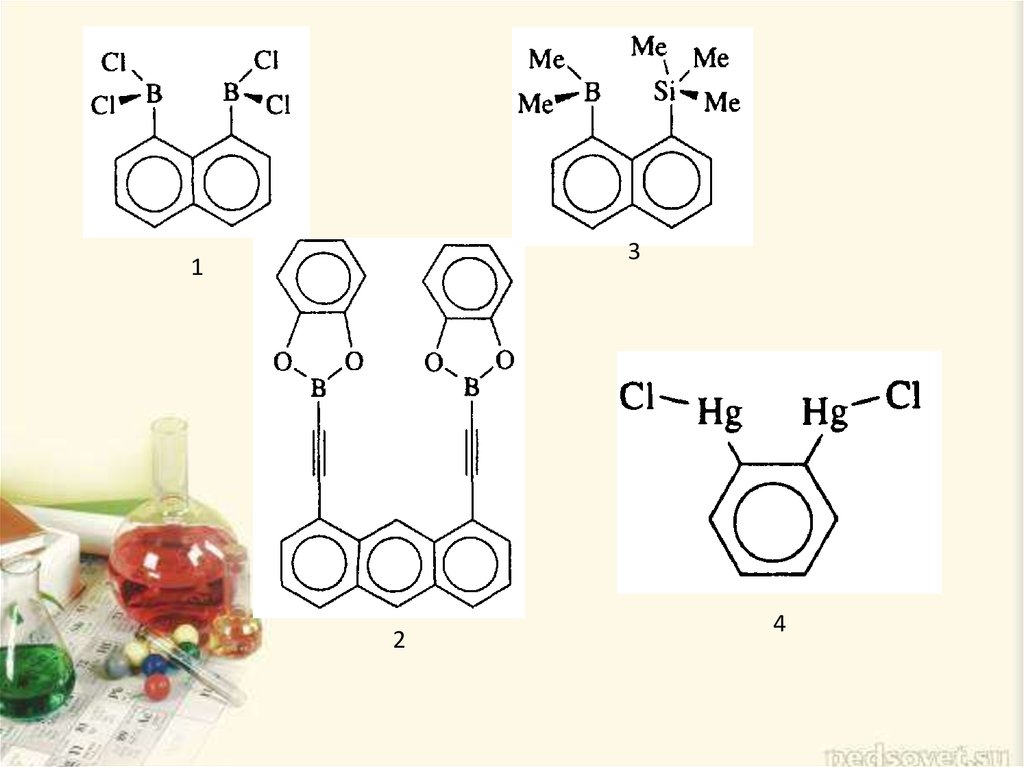
2. Бидентатное координационное поведение таких хелатирующих лиган- дов на основе кислот Льюиса, как (1-4), предполагает, что очень сильное анио
Бидентатное координационное поведение таких хелатирующих лигандов на основе кислот Льюиса, как (1-4), предполагает, что очень сильноеанионное связывание может быть достигнуто, когда группы, представляющие
собой кислоты Льюиса, являются частью кольца макроцикла. В
противоположность основаниям Льюиса в обычных краун-эфирах, аналог краунэфира, собранный из электроноакцепторных групп, может быть представлен как
«антикраун» из-за его альтернативных комплексообразующих свойств, т.е. из-за
его сродства к анионам — основаниям Льюиса, а не к кислотам Льюиса, например
к катионам щелочных металлов. Будучи частью системы макроциклического
кольца, антикрауны должны повышать стабильность комплекса за счет
макроциклического и хелатного эффектов, а также более строгой
предорганизации.
3.
31
2
4
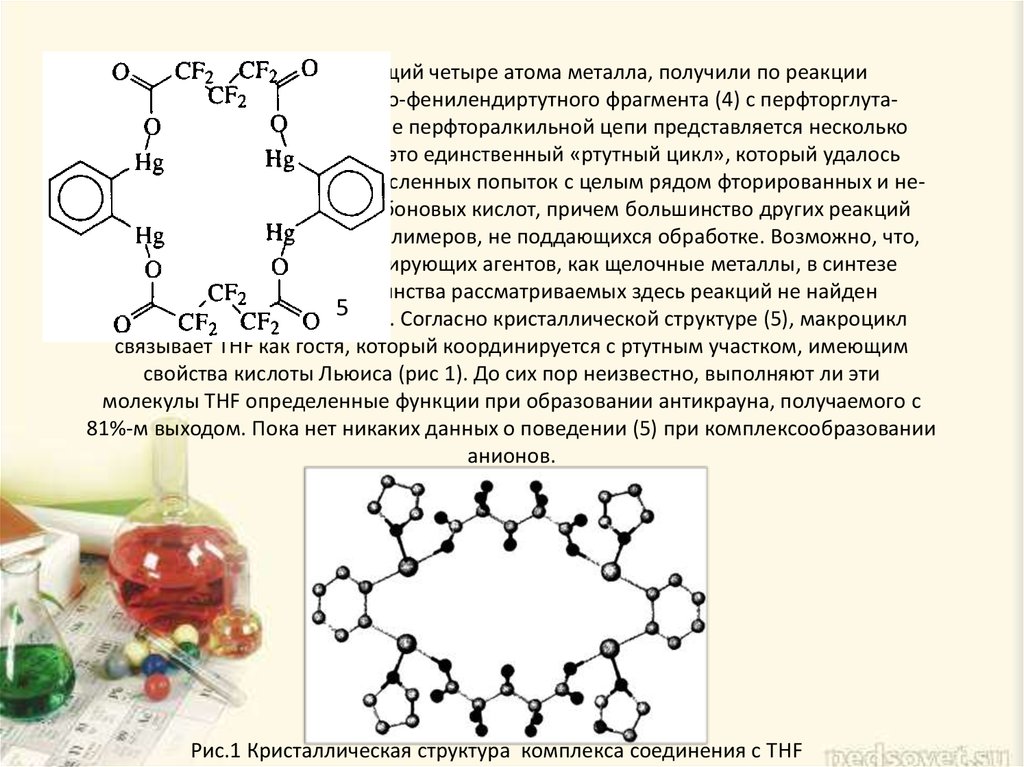
4. Антикраун (5), содержащий четыре атома металла, получили по реакции оксо-мостикового аналога о-фенилендиртутного фрагмента (4) с перфторглут
Антикраун (5), содержащий четыре атома металла, получили по реакцииоксо-мостикового аналога о-фенилендиртутного фрагмента (4) с перфторглутаровой кислотой. Встраивание перфторалкильной цепи представляется несколько
необычным, тем не менее это единственный «ртутный цикл», который удалось
синтезировать после многочисленных попыток с целым рядом фторированных и нефторированных α,Ѡ -дикарбоновых кислот, причем большинство других реакций
приводило к образованию полимеров, не поддающихся обработке. Возможно, что,
в отличие от таких темплатирующих агентов, как щелочные металлы, в синтезе
краунэфиров для большинства рассматриваемых здесь реакций не найден
5
подходящий «антитемплат».
Согласно кристаллической структуре (5), макроцикл
связывает THF как гостя, который координируется с ртутным участком, имеющим
свойства кислоты Льюиса (рис 1). До сих пор неизвестно, выполняют ли эти
молекулы THF определенные функции при образовании антикрауна, получаемого с
81%-м выходом. Пока нет никаких данных о поведении (5) при комплексообразовании
анионов.
Рис.1 Кристаллическая структура комплекса соединения с ТHF
5. Вслед за (5) был получен ряд других циклических ртутьсодержа- щих краун-соединений, которые ведут себя подобным образом при комплексообразо
Вслед за (5) был получен ряддругих циклических ртутьсодержащих краун-соединений, которые
ведут себя подобным образом при
комплексообразовании с галогенидионами. Соединение (6)
дает 1:1-полимер с бромид-анионом в
твердом состоянии, в котором
анионы Вr~ располагаются над
плоскостью Hg3 (структура типа
«насест»).
Длина связи Hg—Вr, равная
3.07-3.39 Å, значительно больше
длины обычной ковалентной связи
Hg-Br (-2.54 Å).
Аналогичный хлоридный комплекс
имеет
стехиометрию 3:2, что предполагает
трехпалубный сэндвич типа
[(6)-Сl-(6)-С1-(6)]2-.
Сэндвичевый полимер комплекса
соединения (6) с Вг-.)
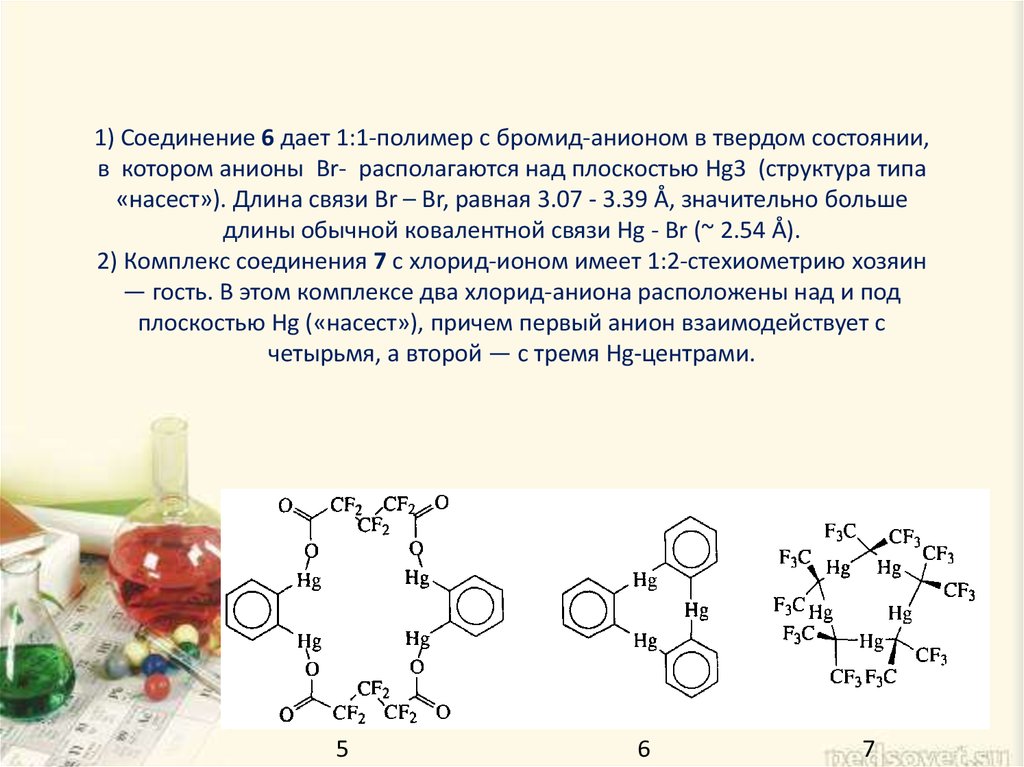
6. 1) Соединение 6 дает 1:1-полимер с бромид-анионом в твердом состоянии, в котором анионы Br- располагаются над плоскостью Hg3 (структура типа «нас
1) Соединение 6 дает 1:1-полимер с бромид-анионом в твердом состоянии,в котором анионы Br- располагаются над плоскостью Hg3 (структура типа
«насест»). Длина связи Br – Br, равная 3.07 - 3.39 Å, значительно больше
длины обычной ковалентной связи Hg - Br (~ 2.54 Å).
2) Комплекс соединения 7 с хлорид-ионом имеет 1:2-стехиометрию хозяин
— гость. В этом комплексе два хлорид-аниона расположены над и под
плоскостью Hg («насест»), причем первый анион взаимодействует с
четырьмя, а второй — с тремя Hg-центрами.
5
6
7
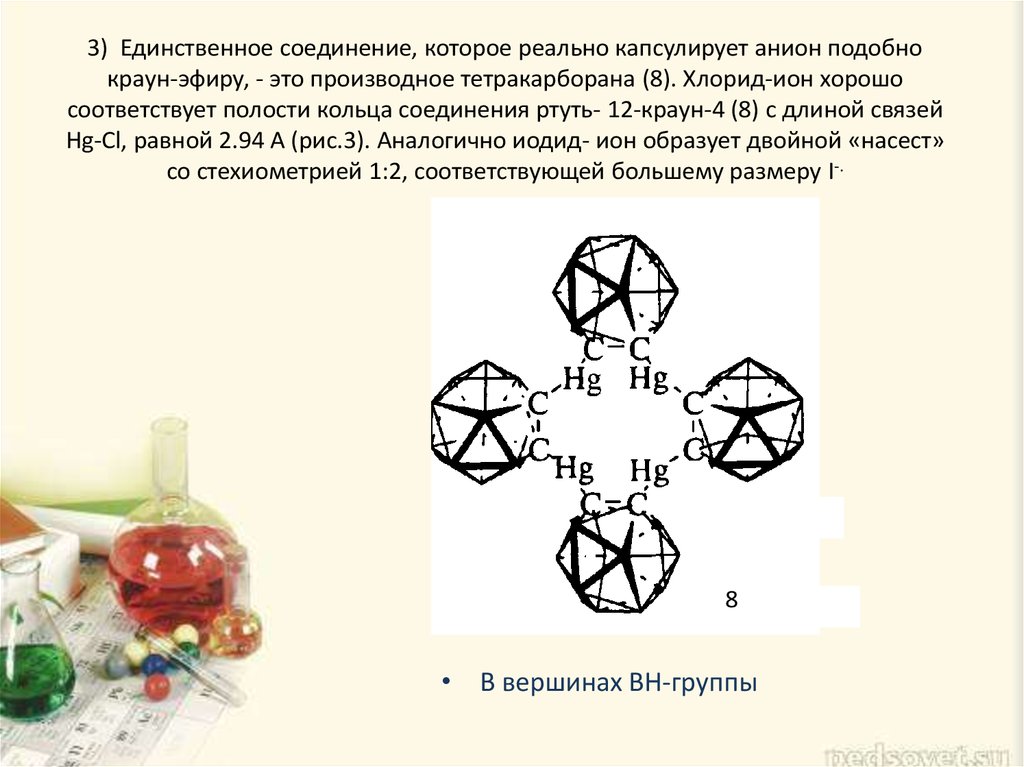
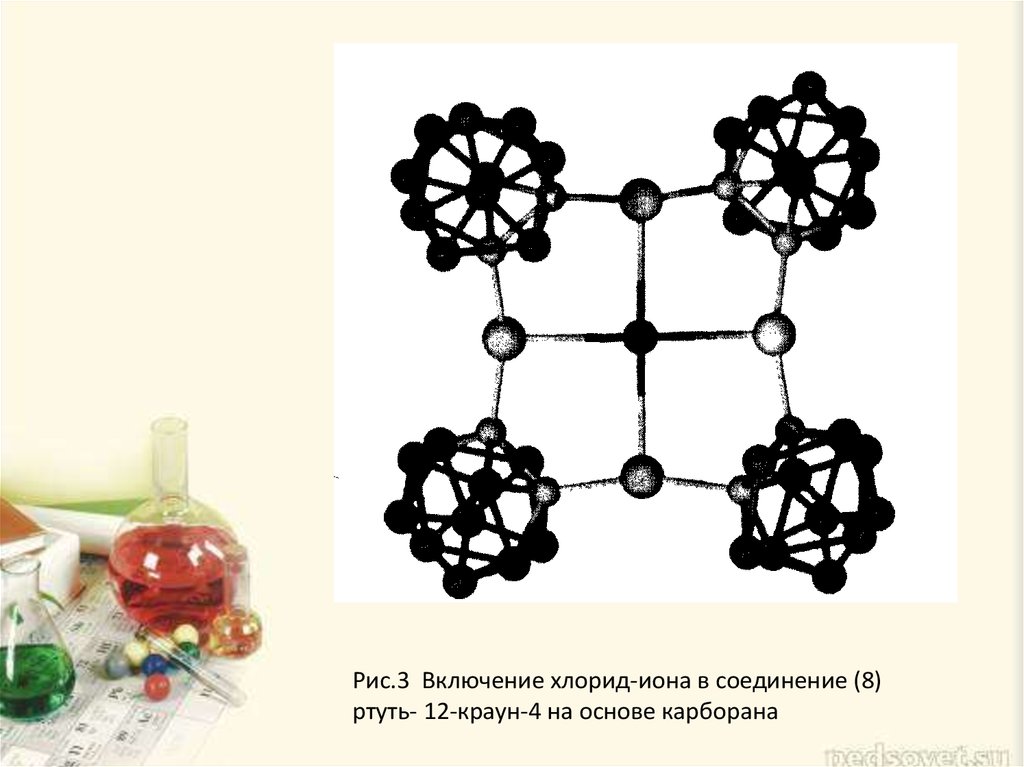
7. 3) Единственное соединение, которое реально капсулирует анион подобно краун-эфиру, - это производное тетракарборана (8). Хлорид-ион хорошо со
3) Единственное соединение, которое реально капсулирует анион подобнокраун-эфиру, - это производное тетракарборана (8). Хлорид-ион хорошо
соответствует полости кольца соединения ртуть- 12-краун-4 (8) с длиной связей
Hg-Cl, равной 2.94 А (рис.3). Аналогично иодид- ион образует двойной «насест»
со стехиометрией 1:2, соответствующей большему размеру I-.
8
• В вершинах BH-группы
8.
Рис.3 Включение хлорид-иона в соединение (8)ртуть- 12-краун-4 на основе карборана
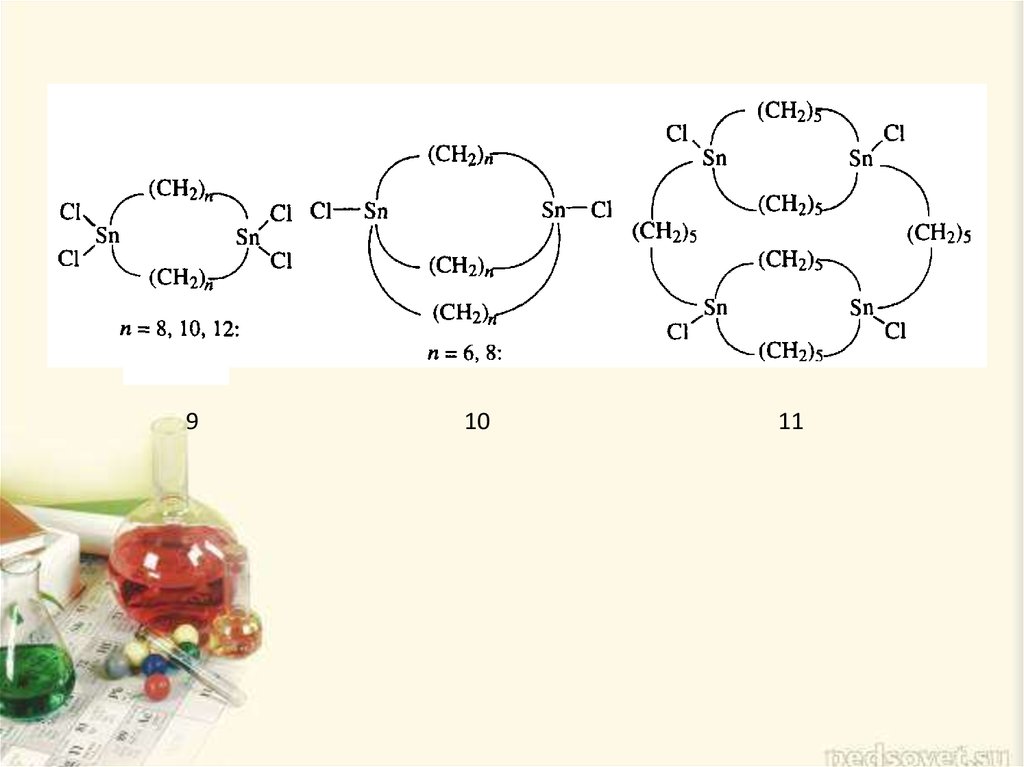
9. Олово(IV), как кремний и ртуть, тоже способно расширять свою координационную сферу от четырех до пяти центров и вести себя как кислота Льюиса
Олово(IV), как кремний и ртуть, тоже способно расширять своюкоординационную сферу от четырех до пяти центров и вести себя как кислота Льюиса.
Учитывая это, М. Ньюкомб с сотрудниками из Техасского
университета (США) приготовил ряд содержащих олово антикраунов и антикриптандов
(9) — (11), отчасти напоминающих катапинанды.
Соединение (9) связывает хлорид-ион в растворе ацетонитрила, однако его
константа связывания всего лишь в 2 раза больше константы его аналогов с
открытой цепью и не зависит от размера кольца, что свидетельствует о невысоком
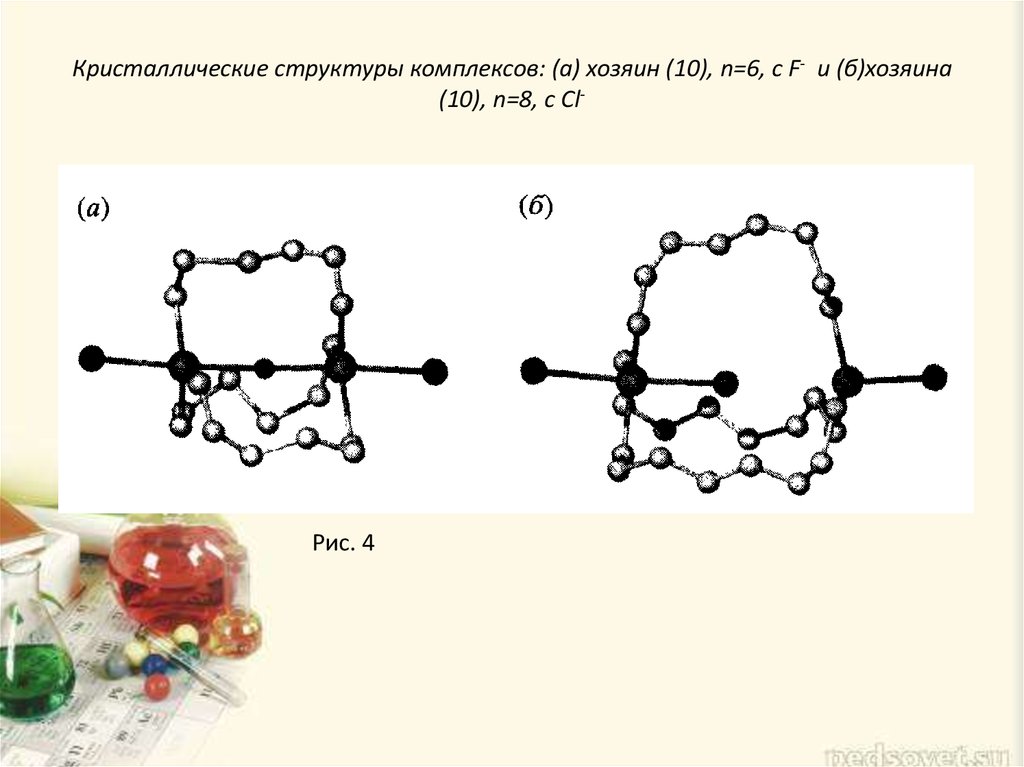
сродстве компонентов. Был проведен рентгеноструктурный анализ комплексов макробициклического соединения (10) со фторид- (n = 6) и хлорид-ионами (n = 8). В
первом случае фторид-анион располагается почти симметрично, образуя мостик
между двумя атомами олова с длинами связей Sn-F 2.12 и 2.28 А (рис.4 а). Этот
хозяин прочно связывает фторид-ион (K1= 104 М-1) и, вероятно из-за размерного
несоответствия, вообще не взаимодействует с хлорид-ионом. В хлоридном
комплексе большего хозяина (n = 8) хлорид-ион внутри макробицикла
скоординирован только с одним центром олова (длины связей Sn-Cl равны 2.610 и
3.388 А), из чего следует, что полость макроцикла слишком велика для аниона. Если
тенденция к образованию линейных мостиков в случае хлорид-иона и существует, то
она недостаточно сильна, чтобы инициировать необходимую перестройку хозяина
(рис. 4 б). Интересно, что даже при -100 °С анион Сl- в растворе быстро перескакивает
от одного металлического центра к другому и обратно. Константа
связывания очень мала и сравнима только с константой связывания единичного Snцентра в ациклических системах.
10.
910
11





 Химия
Химия








