Похожие презентации:
Л7 Нуклеиновые кислоты
1.
НУКЛЕИНОВЫЕКИСЛОТЫ (НК)
- высокомолекулярные соединения
(биополимеры), играющие главную роль в
передаче наследственной информации и
управлении процессом биосинтеза белка.
2.
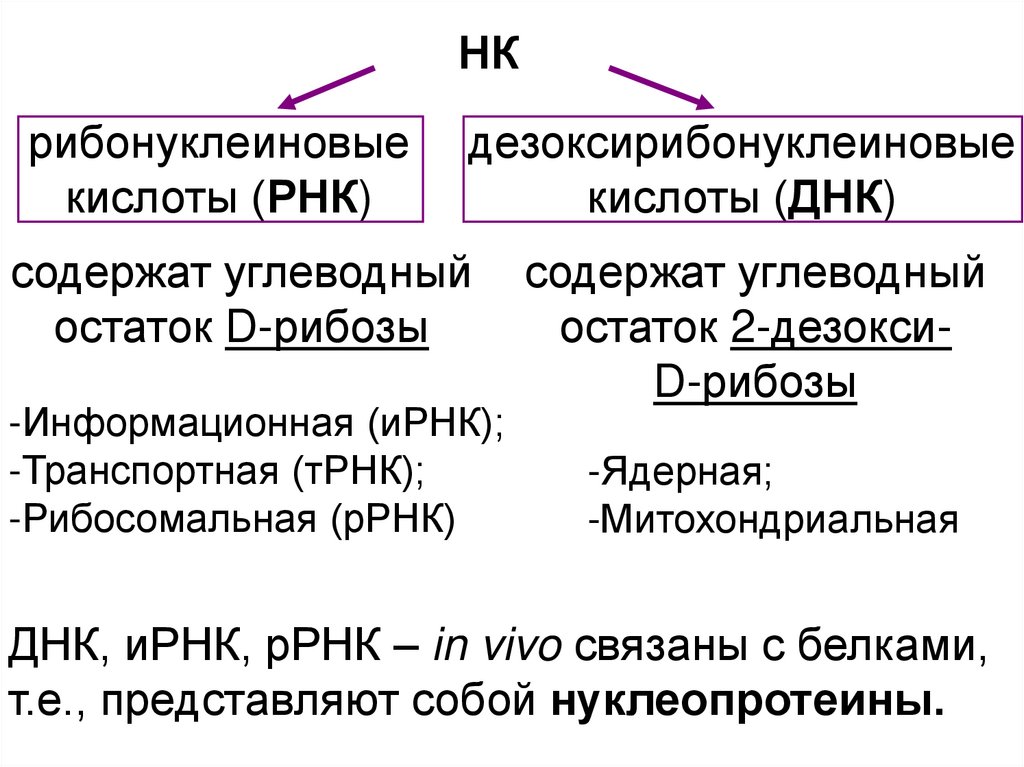
НКрибонуклеиновые
кислоты (РНК)
дезоксирибонуклеиновые
кислоты (ДНК)
содержат углеводный
остаток D-рибозы
-Информационная (иРНК);
-Транспортная (тРНК);
-Рибосомальная (рРНК)
содержат углеводный
остаток 2-дезоксиD-рибозы
-Ядерная;
-Митохондриальная
ДНК, иРНК, рРНК – in vivo связаны с белками,
т.е., представляют собой нуклеопротеины.
3.
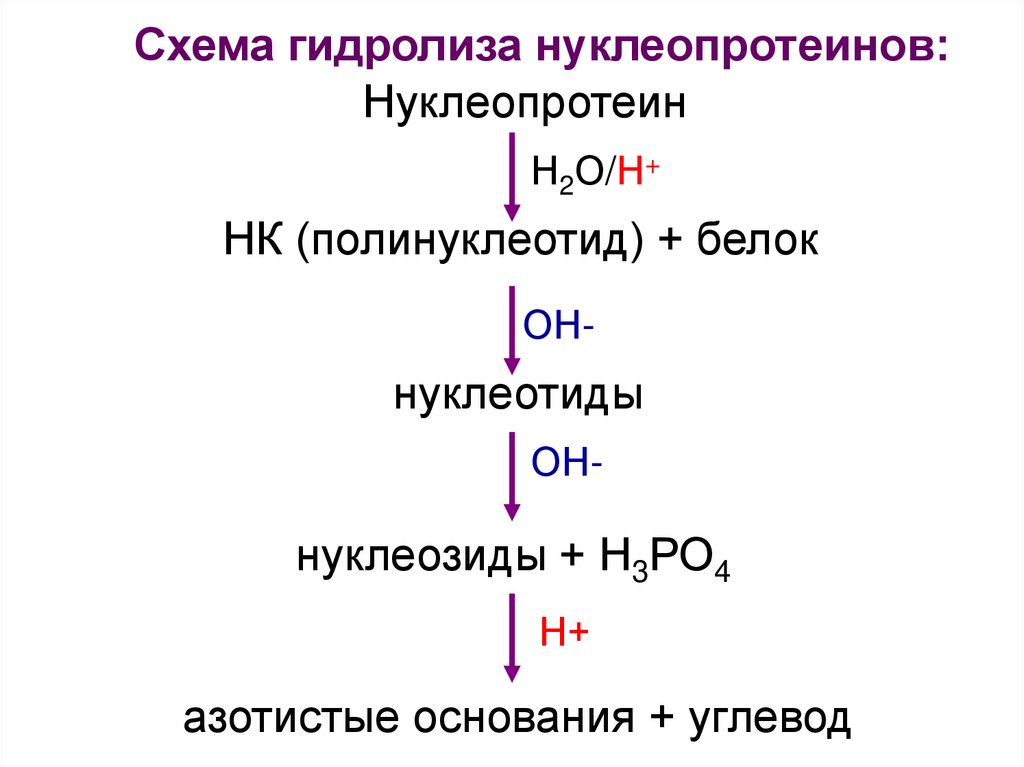
Схема гидролиза нуклеопротеинов:Нуклеопротеин
Н2О/Н+
НК (полинуклеотид) + белок
ОН-
нуклеотиды
ОН-
нуклеозиды + Н3РО4
Н+
азотистые основания + углевод
4.
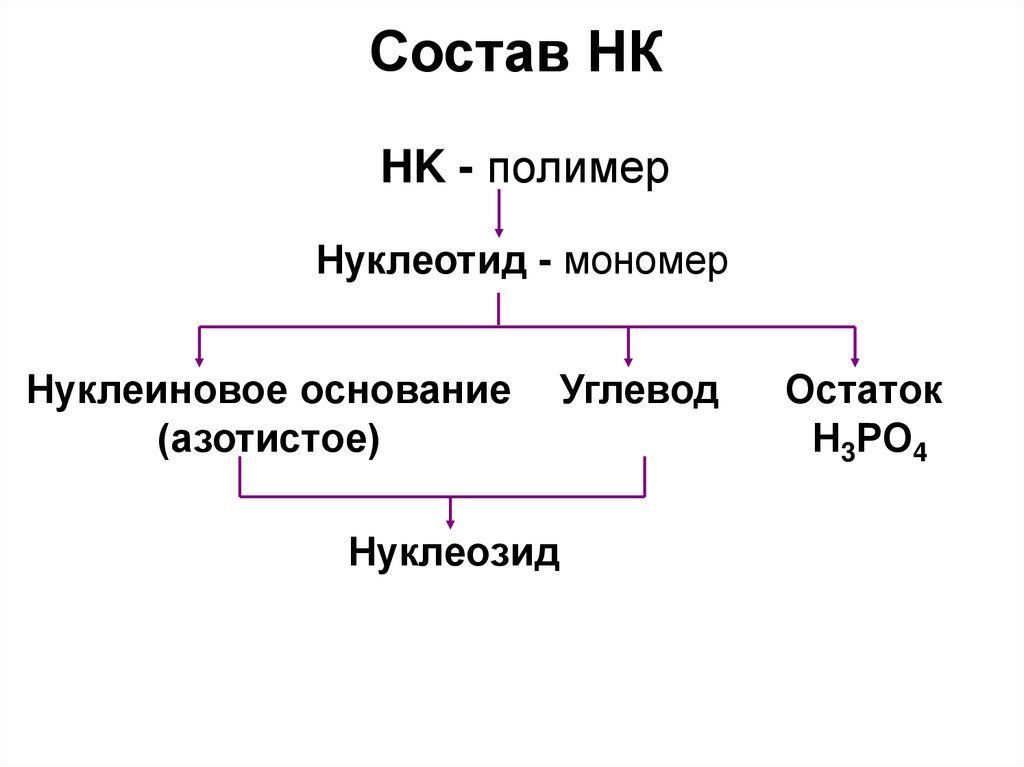
Состав НКHK - полимер
Нуклеотид - мономер
Нуклеиновое основание
(азотистое)
Нуклеозид
Углевод
Остаток
Н3РО4
5.
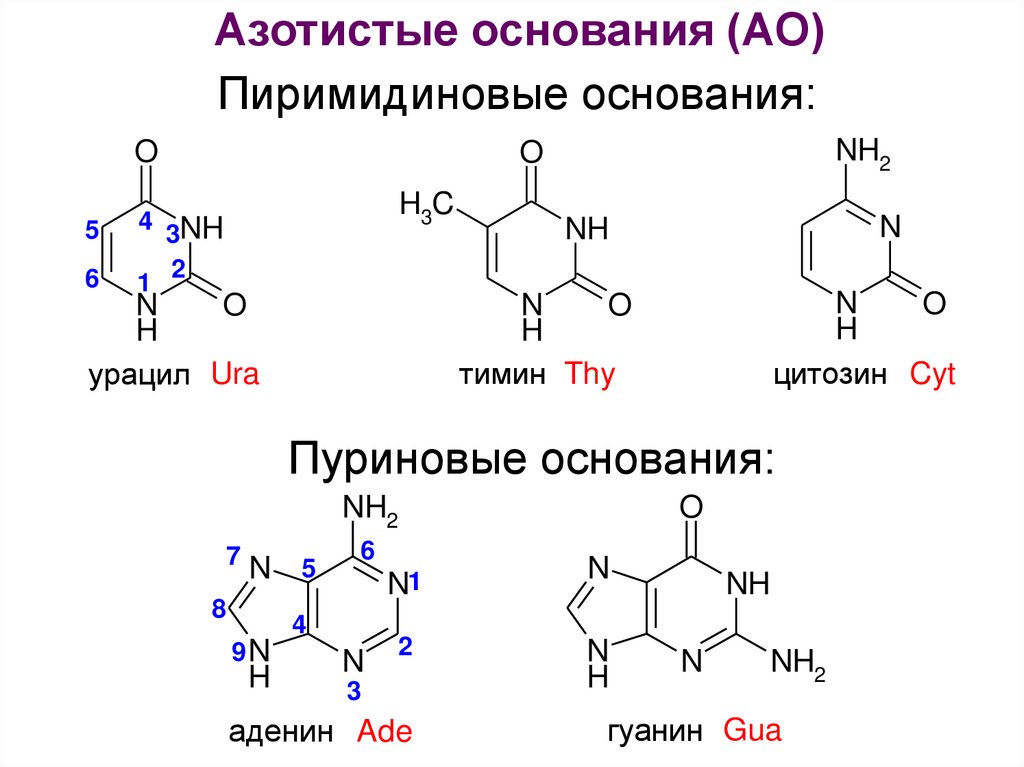
Азотистые основания (АО)Пиримидиновые основания:
O
5
4
6
1
NH2
O
H3C
3NH
2
N
O
H
урацил Ura
N
NH
N
O
H
цитозин Cyt
N
O
H
тимин Thy
Пуриновые основания:
NH2
7
N 5
8
6
N1
4
9N
H
N
2
3
аденин Ade
O
N
N
H
NH
N
NH2
гуанин Gua
6.
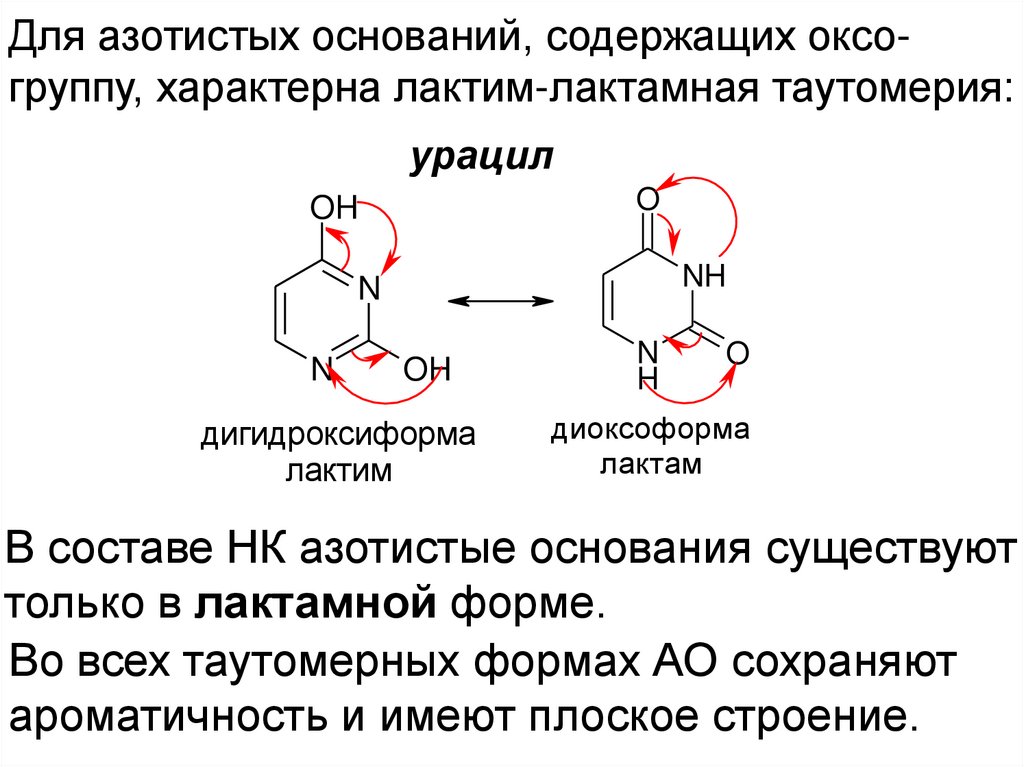
Для азотистых оснований, содержащих оксогруппу, характерна лактим-лактамная таутомерия:урацил
O
OH
NH
N
N
OH
дигидроксиформа
лактим
N
H
O
диоксоформа
лактам
В составе НК азотистые основания существуют
только в лактамной форме.
Во всех таутомерных формах АО сохраняют
ароматичность и имеют плоское строение.
7.
НК различаются входящими в их составазотистыми основаниями:
РНК
урацил
цитозин
аденин
гуанин
ДНК
тимин
цитозин
аденин
гуанин
8.
НУКЛЕОЗИДЫУглевод связывается с азотистым основанием
за счет β-N-гликозидной связи.
В зависимости от природы углеводного остатка
различают рибонуклеозиды и
дезоксирибонуклеозиды.
В зависимости от природы азотистого
основания нуклеозиды делятся на пуриновые
и пиримидиновые.
9.
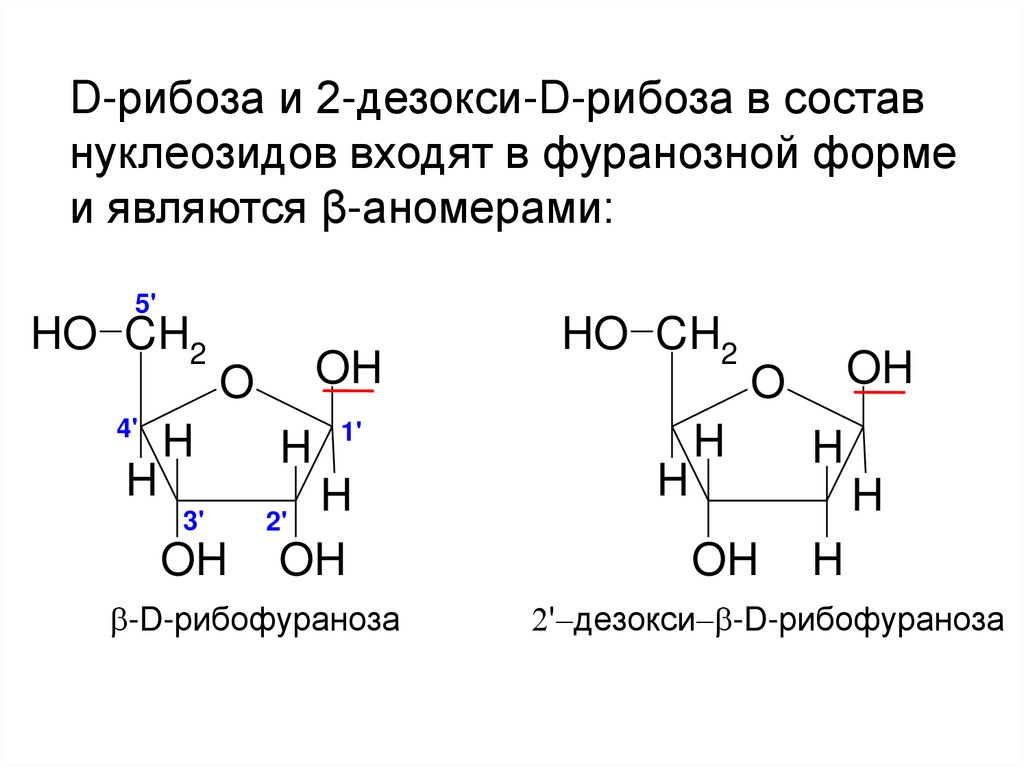
D-рибоза и 2-дезокси-D-рибоза в составнуклеозидов входят в фуранозной форме
и являются β-аномерами:
5'
HO CH2
4'
H
H
OH
O
H
HO CH2
1'
H
3'
2'
OH OH
-D-рибофураноза
H
OH
O
H
H
H
OH
H
' дезокси -D-рибофураноза
10.
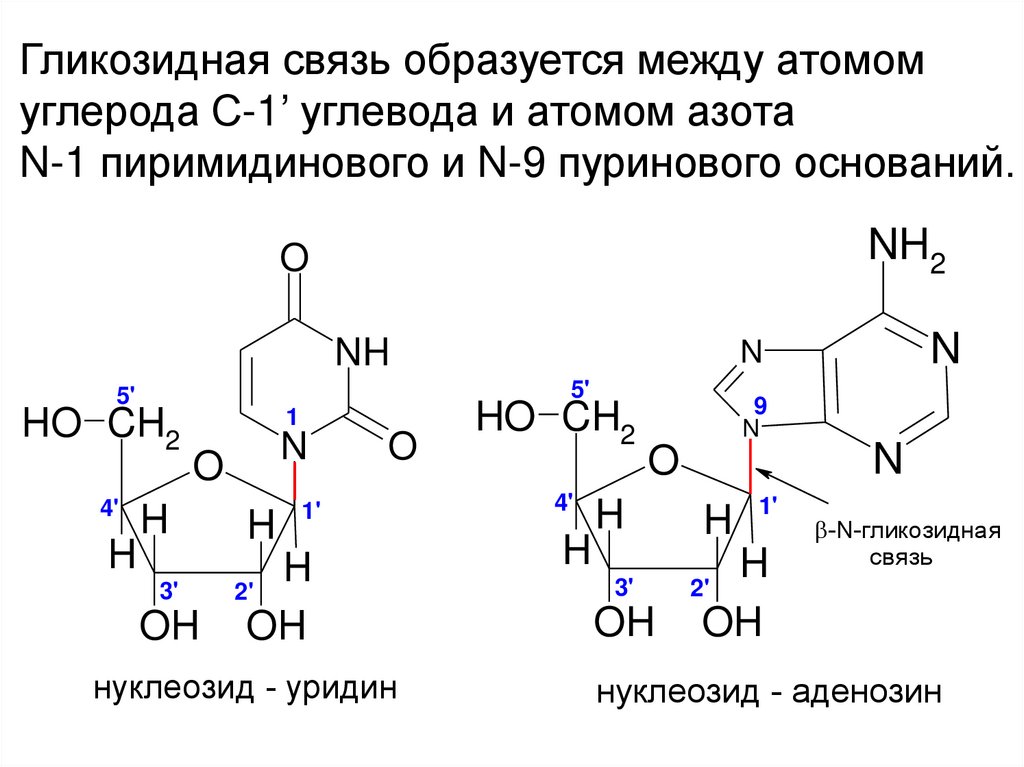
Гликозидная связь образуется между атомомуглерода С-1’ углевода и атомом азота
N-1 пиримидинового и N-9 пуринового оснований.
NH2
O
NH
5'
5'
HO CH2
4'
H
1
N
O
H
3'
OH
H
O
1'
H
OH
2'
нуклеозид - уридин
N
N
HO CH2
4'
9
N
O
H 1'
H
H
3'
2'
OH OH
H
N
-N-гликозидная
связь
нуклеозид - аденозин
11.
Номенклатура нуклеозидовНазвания строят от тривиального названия
соответствующих азотистых оснований
с суффиксами –идин у пиримидиновых,
и -озин у пуриновых нуклеозидов.
Цитозин + рибоза = цитидин
Цитозин + дезоксирибоза = дезоксицитидин
Аденин + рибоза = аденозин
Аденин + дезоксирибоза = дезоксиаденозин
Исключение: Тимин + дезоксирибоза = тимидин
тимин + рибоза = тимидинрибозид
12.
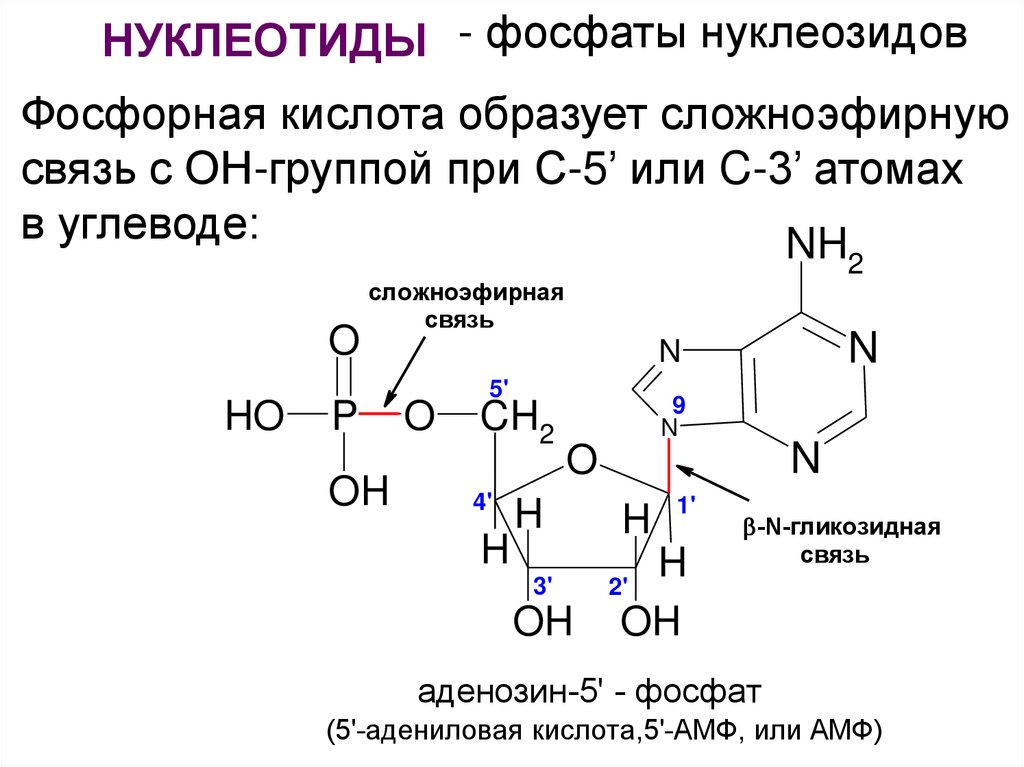
НУКЛЕОТИДЫ - фосфаты нуклеозидовФосфорная кислота образует сложноэфирную
связь с ОН-группой при С-5’ или C-3’ атомах
в углеводе:
NH
O
HO
2
сложноэфирная
связь
P
OH
N
N
O
5'
CH2
4'
9
N
H 1'
H
H
3'
2'
OH OH
H
N
O
-N-гликозидная
связь
аденозин-5' - фосфат
(5'-адениловая кислота,5'-АМФ, или АМФ)
13.
NH2N
N
HO
5'
CH2
4'
H
O
HO
H
3'
O
9
N
N
O
H
1'
H
OH
2'
P
OH
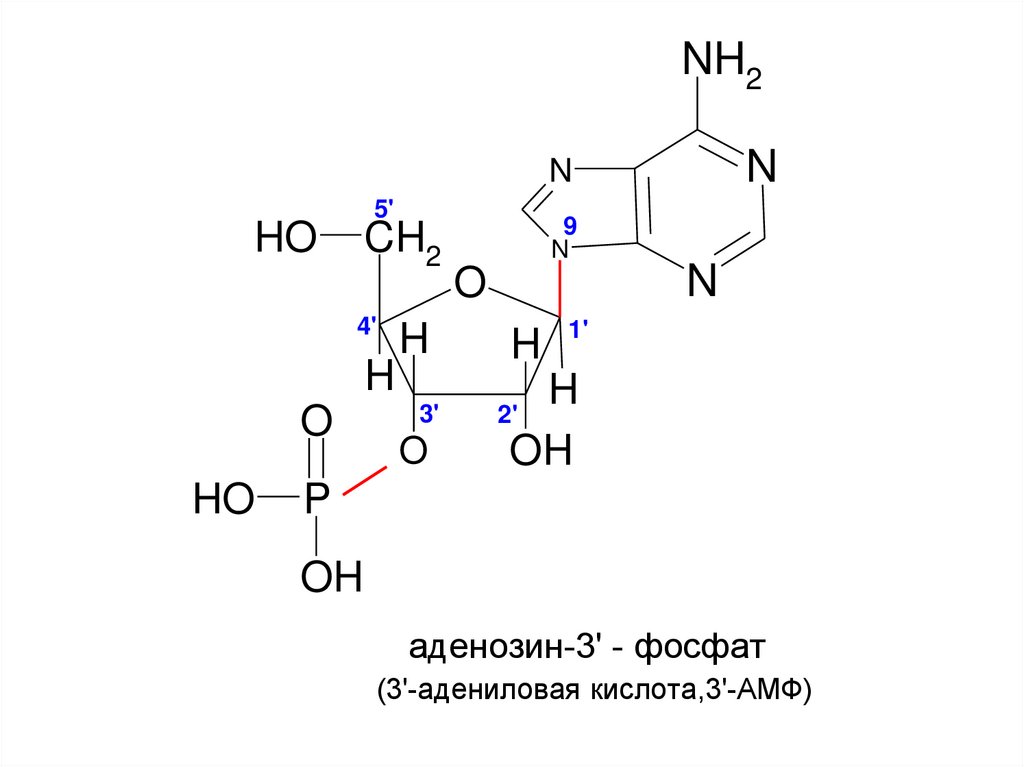
аденозин-3' - фосфат
(3'-адениловая кислота,3'-АМФ)
14.
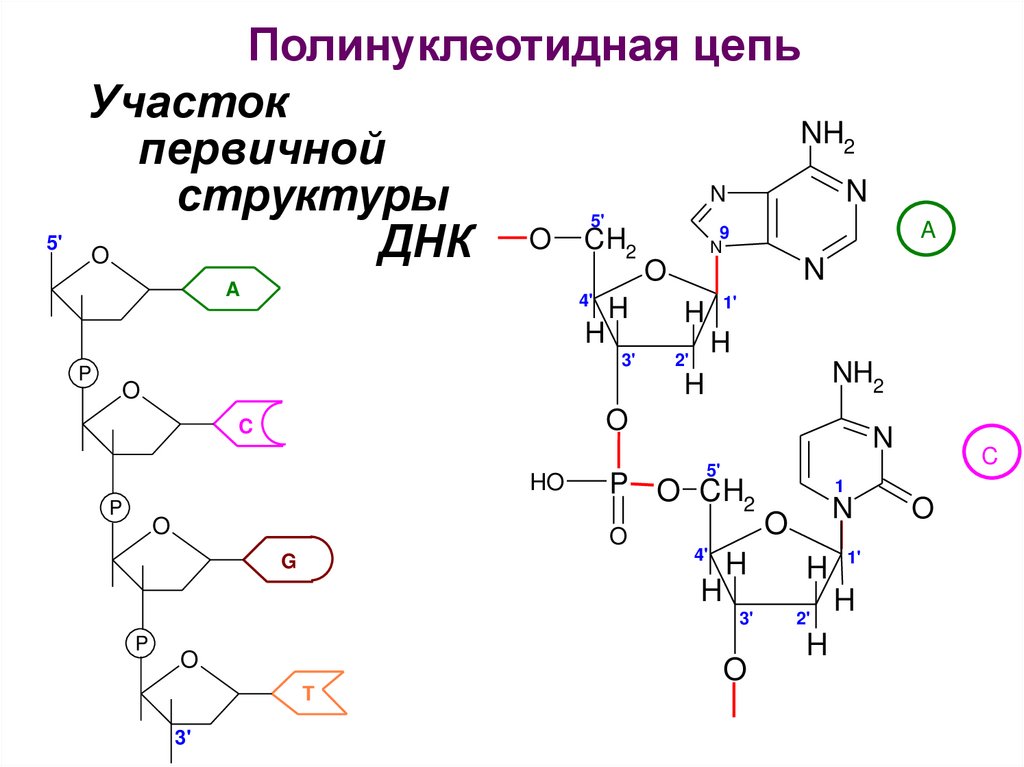
Полинуклеотидная цепьУчасток
NH2
первичной
N
N
структуры
5'
ДНК O CH2
O
N
5'
O
A
4'
H
P
H
3'
O
H 1'
H
2'
H
NH2
O
C
HO
P
O
N
5'
P O CH
2
O
G
4'
H
H
3'
P
O
T
3'
A
9
N
O
C
1
O
N
H 1'
H
2'
H
O
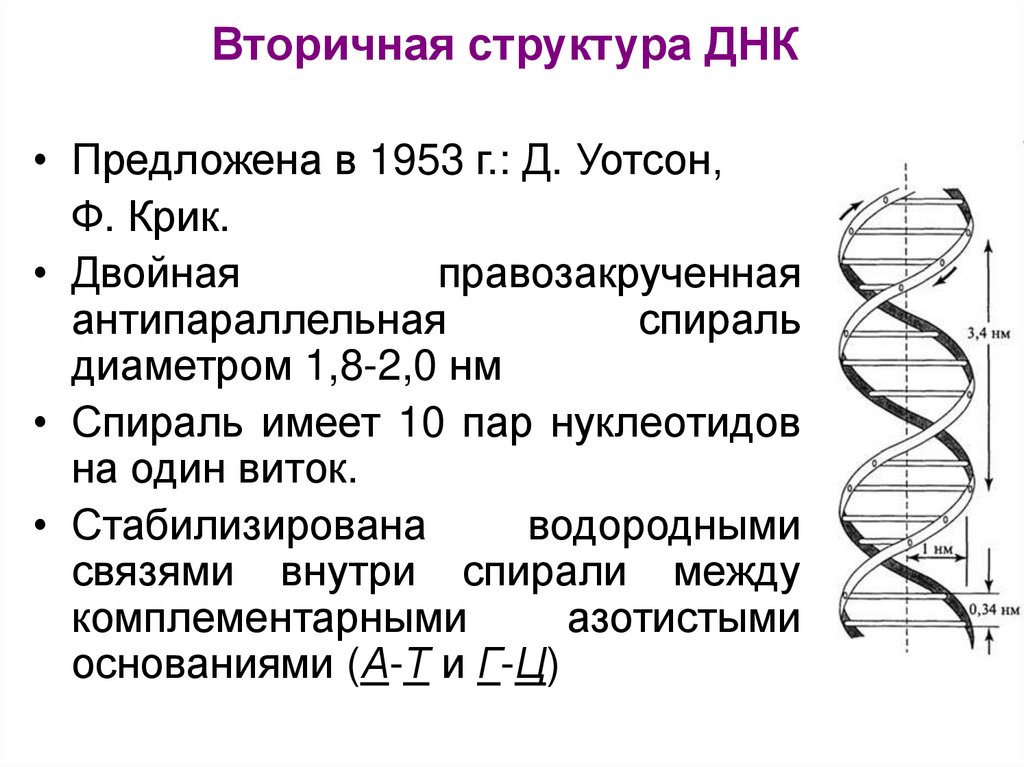
15. Вторичная структура ДНК
• Предложена в 1953 г.: Д. Уотсон,Ф. Крик.
• Двойная
правозакрученная
антипараллельная
спираль
диаметром 1,8-2,0 нм
• Спираль имеет 10 пар нуклеотидов
на один виток.
• Стабилизирована
водородными
связями внутри спирали между
комплементарными
азотистыми
основаниями (А-Т и Г-Ц)
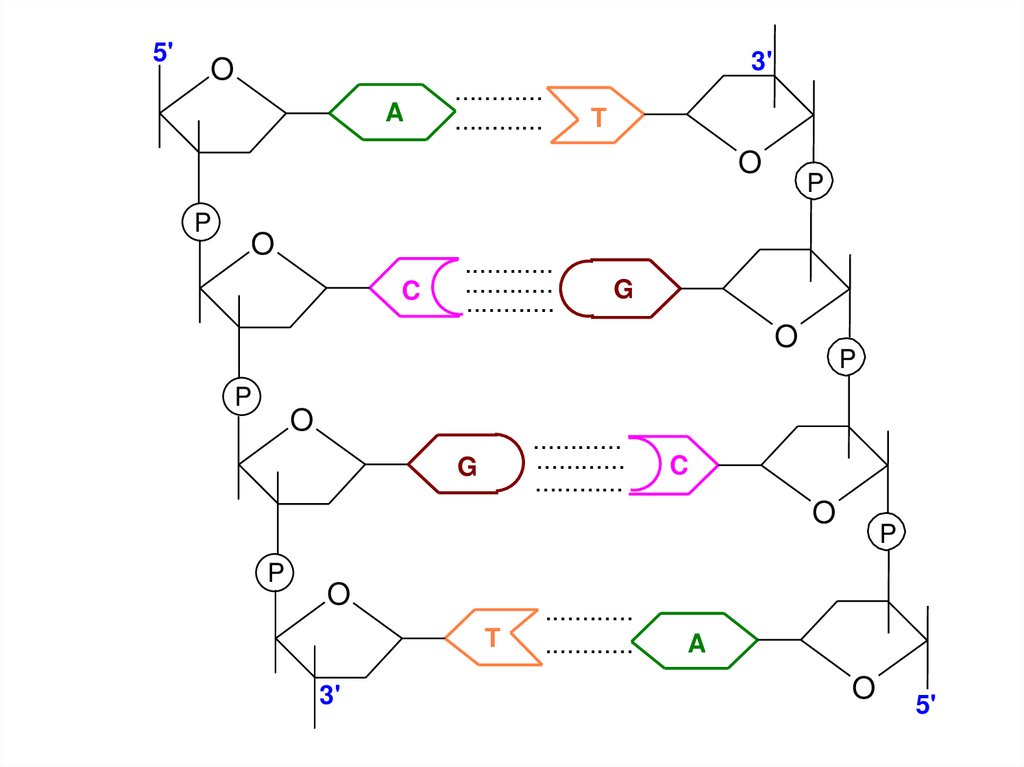
16.
5'3'
O
A
............
............
T
O
P
O
C
............
............
............
P
G
O
P
O
............
............
............
G
P
C
O
P
O
T
3'
............
............
P
A
O
5'
17.
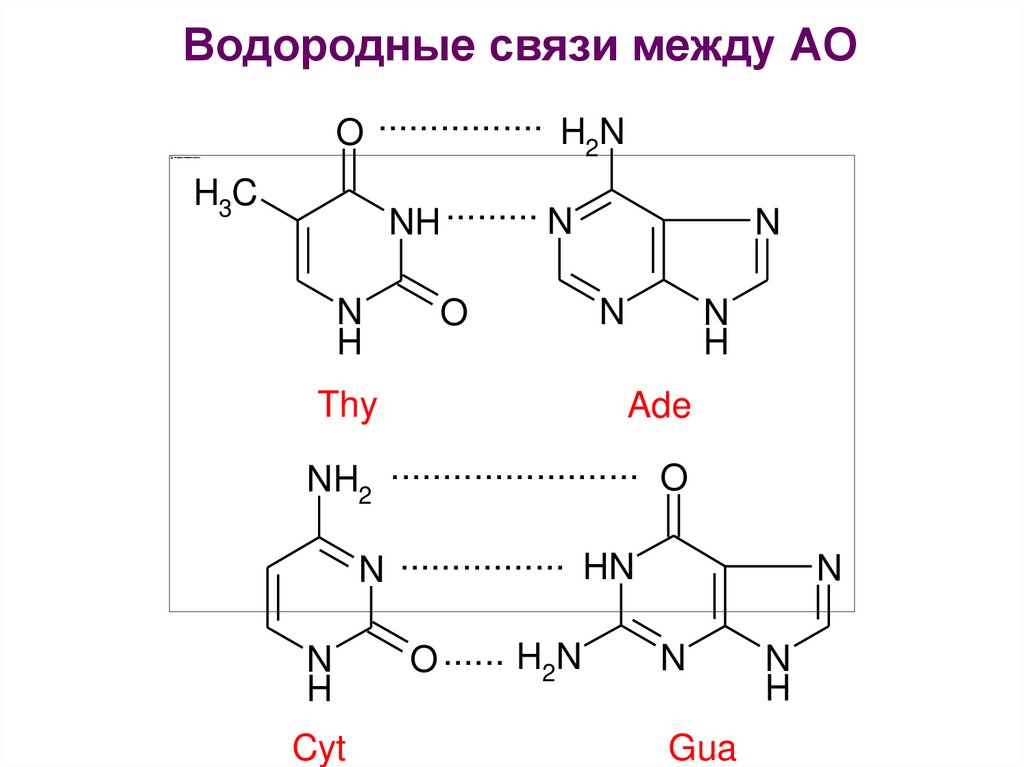
Водородные связи между АОO ................ H2N
H3C
NH ......... N
N
H
O
Thy
N
N
N
H
Ade
NH2 ........................ O
N ................ HN
N
H
Cyt
O ...... H2N
N
N
Gua
N
H
18.
Состав ДНК подчиняется правилам Чаргаффа:- количество А равно количеству Т,
а количество Г – количеству Ц (А = Т, Г = Ц),
- количество пуриновых оснований равно
количеству пиримидиновых (А + Г = Т + Ц),
(А + Ц =Т+Г).
Транспортные и рибосомальные РНК не
подчиняются правилам Чаргаффа.
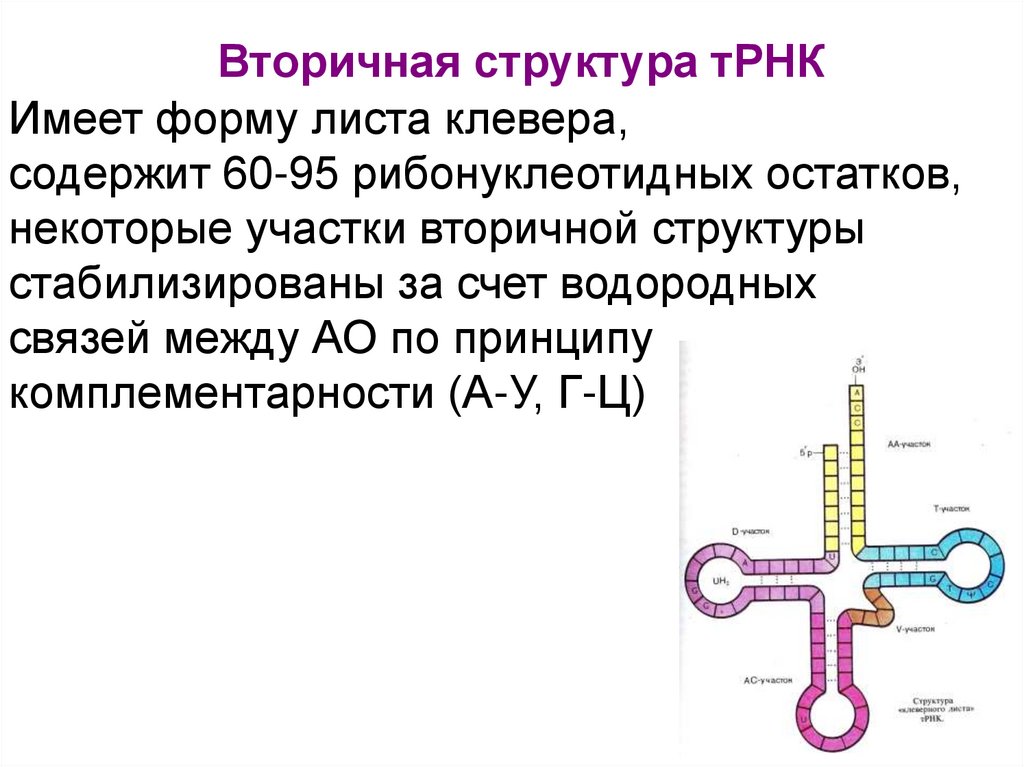
19. Вторичная структура тРНК
Имеет форму листа клевера,содержит 60-95 рибонуклеотидных остатков,
некоторые участки вторичной структуры
стабилизированы за счет водородных
связей между АО по принципу
комплементарности (А-У, Г-Ц)
20.
Метаболизм пуриновых соединений in vivoСинтезируемые в организме и поступающие
с пищей пуриновые основания в конечном
итоге превращаются в мочевую кислоту:
аденин
гипоксантин
ксантин
гуанин
мочевая кислота
21.
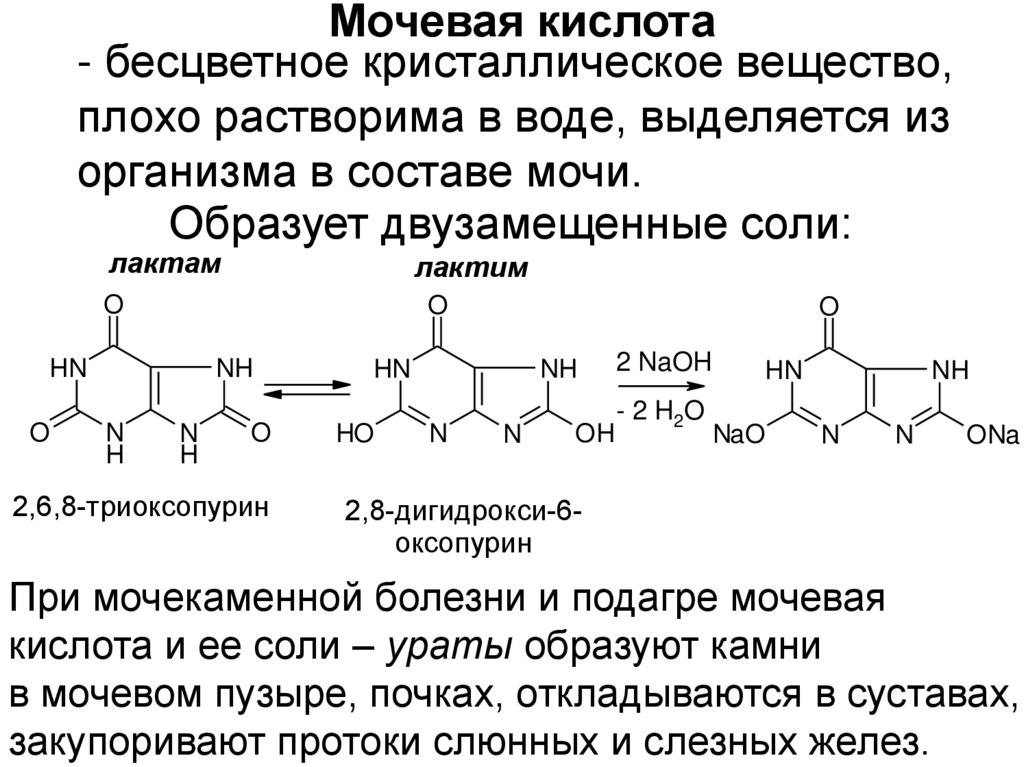
Мочевая кислота- бесцветное кристаллическое вещество,
плохо растворима в воде, выделяется из
организма в составе мочи.
Образует двузамещенные соли:
лактам
лактим
O
O
HN
O
NH
N
H
N
H
O
2,6,8-триоксопурин
O
HN
HO
NH
N
N
OH
2 NaOH
- 2 H2O
HN
NaO
NH
N
N
ONa
2,8-дигидрокси-6оксопурин
При мочекаменной болезни и подагре мочевая
кислота и ее соли – ураты образуют камни
в мочевом пузыре, почках, откладываются в суставах,
закупоривают протоки слюнных и слезных желез.
22.
Свободные нуклеотидыIn vivo выполняют роль коферментов
нуклеозидфосфаты никотинамиднуклеотиды
Аденозинмонофосфат (АМФ) НикотинамидаденинАденозиндифосфат (АДФ)
динуклеотид (НАД) и
Аденозинтрифосфат (АТФ)
его фосфат (НАДФ)
Гуанозинтрифосфат (ГТФ)
Уридинтрифосфат (УТФ)
Цитидинтрифосфат (ЦТФ)
специальные нуклеотиды
Фосфоаденозилфосфосульфат ФАСФ, УДФ-глюкоза,
Флавинадениндинуклеотид (ФАД)
23. Биологическая роль нуклеозидов и азотистых оснований
• Составляющие компоненты нуклеотидов иНК.
• Модифицированные
синтетические
и
полусинтетические азотистые основания
(5-фторурацил, 6-меркаптопурин и др.) и
нуклеозиды (фторафур, 3'-азидотимидин,
рибавирин и др.) – большая группа
лекарственных
препаратов
(противоопухолевые,
противовирусные,
противогрибковые
и
антибактериальные
средства).
24. Биологическая роль свободных нуклетидов
• Нуклеозидтрифосфаты (АТФ, ГТФ, ЦТФ и др.)используются в биосинтезе НК и специальных
нуклеотидов (УДФ-глюкоза, ФАФС).
• Используются
для
регуляции
метаболических
процессов, АМФ и АДФ стимулируют выработку
энергии в клетках, ц-АМФ и ц-ГМФ передают
гормональный сигнал в клетку.
• УДФ-глюкоза используется для синтеза гликогена,
УДФ-глюкуроновой кислоты.
• УДФ-глюкуроновая кислота и ФАФС используются для
детоксикации ксенобиотиков и в биосинтезе
полисахаридов - ГАГ соединительной ткани.
25.
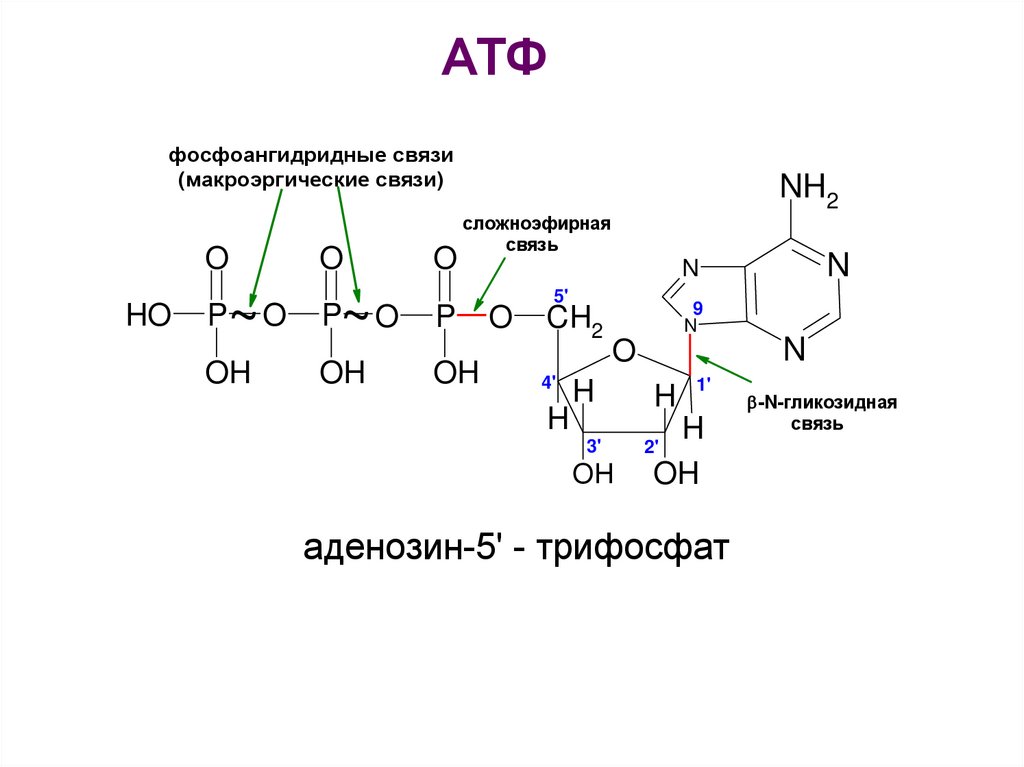
АТФфосфоангидридные связи
(макроэргические связи)
O
HO
O
O
NH2
сложноэфирная
связь
5'
~ O P~ O P O CH O
P
OH
2
OH
OH
N
N
4'
9
N
H 1'
H
H
3'
2'
OH OH
H
аденозин-5' - трифосфат
N
-N-гликозидная
связь
26.
Важнейшее макроэргическое соединениечеловеческого организма, используется для
кратковременного запасания энергии (<1 мин.),
скорость обмена ~ 50 кг/сут.
Образуется при тканевом дыхании
(окислительное фосфорилирование)
и при субстратном фосфорилировании.
Используется для активации и биосинтеза
метаболитов, биосинтеза НК и циклических
нуклеотидов (цАМФ), для энергообеспечения
физиологических процессов (секреция,
клеточное деление и движение, мышечное
сокращение и др.).










 Химия
Химия








