Похожие презентации:
Эмиссия
1. На изучение учебной дисциплины отводится 108 часов (3 зачетные единицы), в том числе 70 аудиторных, из них на лекции – 46 часов
Физическая электроникаНа изучение учебной дисциплины отводится 108
часов (3 зачетные единицы), в том числе 70
аудиторных, из них на лекции – 46 часов (из них
УСР – 14), на лабораторные работы – 24 часа.
Форма отчетности – зачет в 7 семестре.
2.
Физическая электроника – область науки и техники, занимающаясяисследованием физических явлений, составляющих основу для
разработок и создания новых электронных приборов и устройств.
Область исследования
1. Эмиссионная электроника, включая процессы на поверхности, определяющие
явления эмиссии, эмиссионную спектроскопию и все виды эмиссии заряженных частиц.
2. Твердотельная электроника, в том числе СВЧ-электроника, полупроводниковая
электроника,
акустоэлектроника,
сверхпроводниковая
электроника,
спиновая
электроника, оптоэлектроника, криоэлектроника.
3. Вакуумная электроника, включая методы генерирования потоков заряженных частиц,
электронные и ионные оптические системы, релятивистскую электронику.
4. Физические явления в твердотельных микро- и наноструктурах, молекулярных
структурах и кластерах; проводящих, полупроводниковых и тонких диэлектрических
пленках и покрытиях.
5. Плазменная электроника, включая физические процессы в плазменных электронных
приборах: СВЧ-генераторах, усилителях, плазменных (коллективных) ускорителях,
плазменно-пучковых разрядах.
6. Изучение физических основ плазменных и лучевых (пучковых) технологий, в том
числе модификации свойств поверхности, нанесение тонких пленок и пленочных
структур
3.
Эмиссия электроновРабота, которую нужно затратить для удаления электрона из металла в
вакуум, называется работой выхода. Причины появления работы выхода
электрона
1. Если электрон по какой-то причине удаляется из металла, то в том месте,
которое электрон покинул, возникает избыточный положительный заряд и
электрон притягивается к индуцированному им самим положительному
заряду.
+2. Отдельные электроны, покидая металл, удаляются от него на расстояния
порядка атомных и создают тем самым над поверхностью металла
«электронное облако», плотность которого быстро убывает с расстоянием.
Это облако вместе с наружным слоем положительных ионов решетки
образует двойной электрический слой, поле которого подобно полю плоского
конденсатора. Толщина этого слоя равна нескольким межатомным
расстояниям (10-10 - 10-9 м). Он не создает электрического поля во внешнем
пространстве, но препятствует выходу свободных электронов из металла.
4.
Эмиссия электроновВблизи от поверхности образуется электронное
облако, и на границе раздела формируется
двойной электрический слой с разностью
потенциалов (φвн. – φпов.).
За пределами металла электрон приобретает энергию W0. Это энергия
притяжения W0 < 0. Для того, чтобы покинуть металл, электрон должен
преодолеть потенциальный барьер и совершить работу
Aвых =e(φвн - φпов). Эту работу называют работой выхода электрона из
металла. Для ее совершения электрону необходимо сообщить достаточную
энергию W ≥ Aвых.
Наименьшая энергия, которую необходимо сообщить
электрону для того, чтобы удалить его из твердого или
жидкого тела в вакуум, называется работой выхода А.
5.
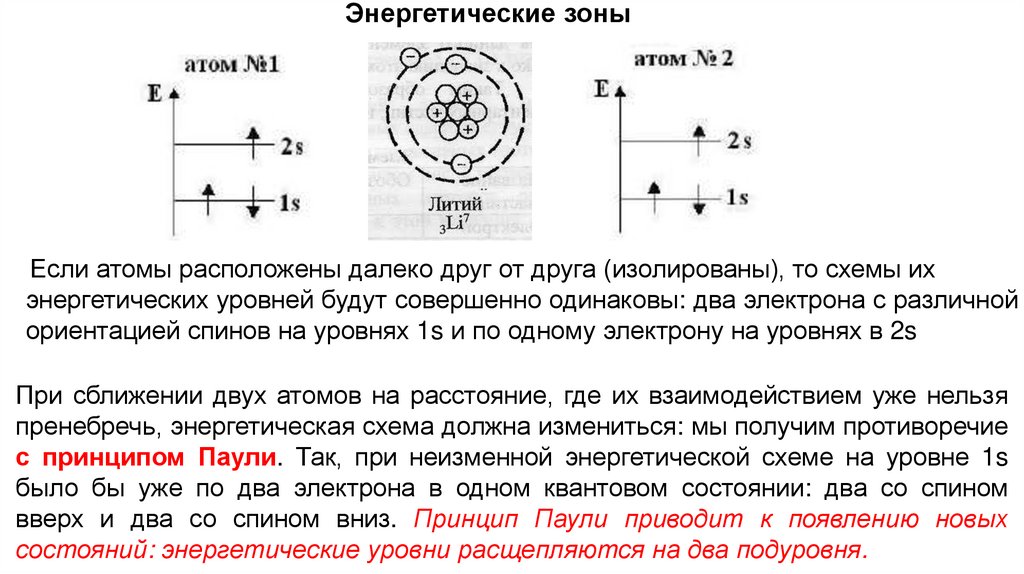
Энергетические зоныЕсли атомы расположены далеко друг от друга (изолированы), то схемы их
энергетических уровней будут совершенно одинаковы: два электрона с различной
ориентацией спинов на уровнях 1s и по одному электрону на уровнях в 2s
При сближении двух атомов на расстояние, где их взаимодействием уже нельзя
пренебречь, энергетическая схема должна измениться: мы получим противоречие
с принципом Паули. Так, при неизменной энергетической схеме на уровне 1s
было бы уже по два электрона в одном квантовом состоянии: два со спином
вверх и два со спином вниз. Принцип Паули приводит к появлению новых
состояний: энергетические уровни расщепляются на два подуровня.
6.
Принцип ПаулиВ атоме не может быть двух электронов с одинаковым значением
четырех квантовых чисел. При одинаковых n, l и m электроны должны
отличаться
спиновым
квантовым
числом.
1. На каждой орбитали, характеризующейся определенными значениями
квантовых чисел (n, l, m), может находиться не более 2-х электронов, спины
которых имеют противоположные знаки.
2. Количество электронов на подуровне равно 2(2l + 1).
3. Количество электронов на энергетическом уровне равно 2n2 , где n – номер
энергетического уровня.
Орбитали
Энергетиче Число
ский
подуров
уровень
ней
Обозначение
подуровня
Максимальное
число
электронов
s
2
↑↓
p
6
↑↓ ↑↓ ↑↓
d
f
10
14
Тип
Число
Максимальн
Количес ое число
тво
электронов
электро на уровне
нов
n=1 (K)
1
1s
1
2
2
↑↓ ↑↓ ↑↓ ↑↓
↑↓
n=2 (L)
2
2s
2p
1
3
2
6
8
↑↓ ↑↓ ↑↓ ↑↓
↑↓ ↑↓ ↑↓
n=3 (M)
3
3s
3p
3d
1
3
5
2
6
10
18
7.
Энергетические зоныТеперь на подуровнях 1s, в полном соответствии с
принципом Паули, разместились четыре электрона, по
одному в каждом квантовом состоянии. Верхний
подуровень 2s оказался свободным.
Величина расщепления уровней ∆E зависит от
расстояния между атомами. При сближении атомов ∆E
растет. Величина ∆E1 < ∆E2, так как в состоянии 1s
электроны сильнее связаны с ядром, чем в
состоянии 2s.
Минимальное расстояние между
атомами – постоянная
кристаллической решетки a –
неизменно.
Величина расщепления (∆E1 и ∆E2) будет той же
самой, как и для системы из двух атомов (∆E зависит
от минимального расстояния
между
атомами).
Третий энергетический уровень расположился между
двумя крайними.
8.
Энергетические зоныПри этом величина расщепления ∆E не будет зависеть от числа
атомов, так как минимальное расстояние между атомами в кристалле
остается неизменным. Следовательно, расстояние между соседними
подуровнями будет уменьшаться с ростом N – числа атомов в кристалле.
Число атомов N имеет порядок числа Авогадро NA = 6,02 · 1023 1/моль.
Максимальное расщепление уровней ∆E по порядку величины составляет
∆
































































































































 Химия
Химия








