Похожие презентации:
Презентация РиМСК
1.
Компания по производству БАДов «ARYS»:СМК ISO 9001, 22000 и принципы GMP
Практическая работа по дисциплине
«Российские и международные стандарты качества»
Выполнили:
Студенты группы №182302:
А.К.Мавлянкул уулу
Д.В.Тартычный
2.
ЦЕЛЬ И РЕЗУЛЬТАТЫЦель работы и итоговые результаты
Цель работы
Результаты работы
продемонстрировать на примере СМК виртуальной организации
Контекст и заинтересованные стороны
разработку элементов СМК с учетом видов деятельности
Цели, политика и план целей СМК
Организационная структура
Карта процессов
Процесс «Производство БАДов» (этапы и точки контроля)
Анализ рисков
Документы (ДП/СОП/рабочая инструкция/ДИ)
План контроля качества
Нормативная база
организации.
3.
О компанииКомпания ARYS и продуктовая линейка
4.
МИССИЯ«Мы укрепляем здоровье
людей и улучшаем их жизнь,
соединяя инновации, науку,
доступность и доверие»
Связь миссии с СМК
Безопасность — приоритет №1
Доверие — через прозрачность и сертификацию
Стабильность качества — контроль на всех этапах
Ориентация на потребителя — основа ISO 9001
Миссия компании определяет стратегические цели СМК
и задаёт вектор развития всех процессов — от
разработки рецептур до выпуска готовой продукции
5.
Анализ контекстаКонтекст организации: внутренние и внешние факторы
Внутренние факторы
Внешние факторы
Ресурсы и персонал: высококвалифицированные
технологи, фармацевты, химики-аналитики
Инфраструктура: современное оборудование,
сертифицированные лаборатории, автоматизированные
линии
Документация: внедрённые системы ISO 9001, GMP*, HACCP
Культура качества: ориентация на непрерывное улучшение
ИТ-системы: интегрированная ERP-система*, CRM*, LIMS*
Научно-исследовательский потенциал: разработка новых
рецептур
Требования законодательства: Роспотребнадзор, СанПиН,
ТР ТС, обязательная маркировка
Ожидания потребителей: рост интереса к ЗОЖ и
профилактике заболеваний
Рынок и конкуренция: рост рынка БАДов 10–15% в год,
высокая насыщенность
Поставщики: зависимость от импортного сырья, колебания
валют
Логистика: региональные особенности доступности поставок
Риски сырья: необходимость диверсификации поставщиков
*HACCP - это международная система управления безопасностью пищевых продуктов,
расшифровывающаяся как «Анализ рисков и критические контрольные точки».
*GMP - это международный стандарт "Надлежащей производственной практики", система правил и требований к производству,
которая гарантирует, что продукция (лекарства, косметика, продукты питания, медицинские изделия) выпускается стабильно качественной,
безопасной и эффективной, контролируя все этапы от сырья до готового продукта
*ERP-система - комплексная система для планирования и управления ресурсами предприятия.
*CRM - система управления взаимоотношениями с клиентами.
*LIMS - система управления лабораторной информацией..
6.
Управление ожиданиямиЗаинтересованные стороны и их требования
Потребители/клиенты
Руководство
Регуляторы
Персонал
Поставщики
Партнёры/дистрибуция
Требования: безопасность, эффективность, прозрачная информация о составе
Требования: соблюдение нормативов, своевременная отчётность, сертификация
Требования: стабильные заказы, своевременная оплата, долгосрочное
сотрудничество
Требования: финансовая устойчивость, рост компании, репутация
Требования: достойная оплата, безопасные условия труда, карьерный рост
Требования: стабильные поставки, конкурентные цены, маркетинговая
поддержка
Как требования закрываются в СМК
Контроль качества
Управление процессами
Непрерывное улучшение
Управление несоответствиями и CAPA*
Документирование всех процессов
Прослеживаемость через ERP/LIMS
Регулярные аудиты
Корректная маркировка
Обучение персонала
Анализ KPI
Входной контроль сырья
(COA* + лабораторные
испытания)
Внутриоперационный
контроль на критических
этапах
Выпускной контроль готовой продукции
*COA (Certificate of Analysis) - документ, подтверждающий результаты лабораторных испытаний сырья или готовой продукции и их соответствие установленным спецификациям
*CAPA (Corrective and Preventive Actions) - мероприятия по устранению причин выявленных несоответствий и предотвращению их повторного возникновения.
7.
Стратегические цели компании ARYS1
2
Рыночная цель
Тактическая цель
Достичь объёма продаж 500 млн
рублей и занять 5% рынка БАДов в СФО
к концу 2026 года.
Пройти сертификацию GMP и ISO 22000
до декабря 2025 года.
3
Инновационная цель
Разработать и вывести на рынок 5 новых продуктовых линеек в 2025-2026 годах.
8.
Политика в области качества ARYSСоответствие требованиям
Выполнение законодательства РФ и ЕАЭС, применение ISO 9001, 22000 и GMP.
Ориентация на потребителя и безопасность
Приоритет потребностям клиентов, гарантия безопасности и эффективности БАДов.
Непрерывное улучшение
Постоянное совершенствование процессов, продуктов и СМК.
Предотвращение проблем
Проактивный подход к управлению качеством, выявление рисков на ранних стадиях.
Развитие персонала
Инвестиции в обучение и профессиональный рост сотрудников.
9.
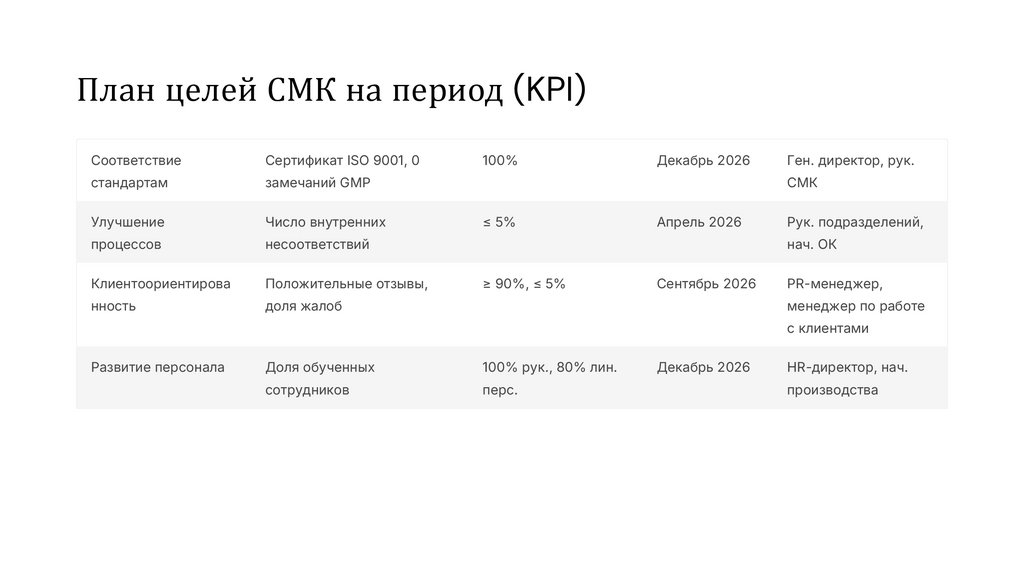
План целей СМК на период (KPI)Соответствие
Сертификат ISO 9001, 0
стандартам
замечаний GMP
Улучшение
Число внутренних
процессов
несоответствий
Клиентоориентирова
Положительные отзывы,
нность
доля жалоб
100%
Декабрь 2026
Ген. директор, рук.
СМК
≤ 5%
Апрель 2026
Рук. подразделений,
нач. ОК
≥ 90%, ≤ 5%
Сентябрь 2026
PR-менеджер,
менеджер по работе
с клиентами
Развитие персонала
Доля обученных
100% рук., 80% лин.
сотрудников
перс.
Декабрь 2026
HR-директор, нач.
производства
10.
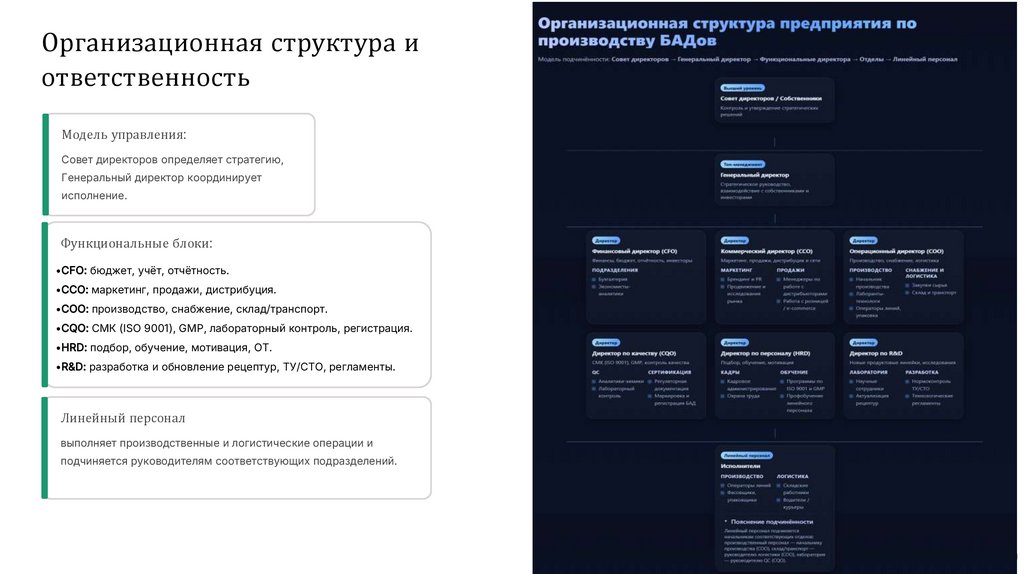
Организационная структура иответственность
Модель управления:
Совет директоров определяет стратегию,
Генеральный директор координирует
исполнение.
Функциональные блоки:
•CFO: бюджет, учёт, отчётность.
•CCO: маркетинг, продажи, дистрибуция.
•COO: производство, снабжение, склад/транспорт.
•CQO: СМК (ISO 9001), GMP, лабораторный контроль, регистрация.
•HRD: подбор, обучение, мотивация, ОТ.
•R&D: разработка и обновление рецептур, ТУ/СТО, регламенты.
Линейный персонал
выполняет производственные и логистические операции и
подчиняется руководителям соответствующих подразделений.
11.
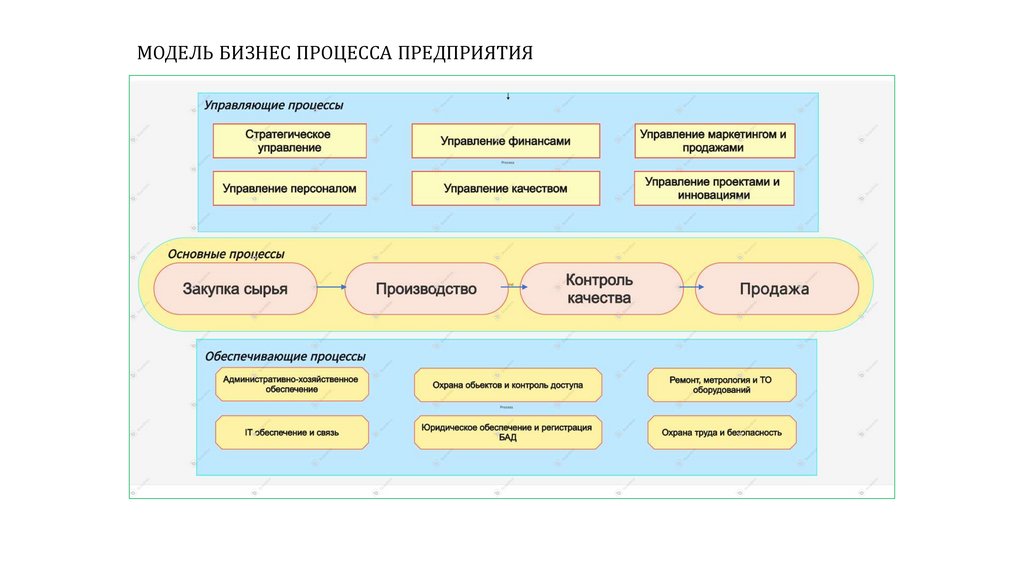
МОДЕЛЬ БИЗНЕС ПРОЦЕССА ПРЕДПРИЯТИЯ12.
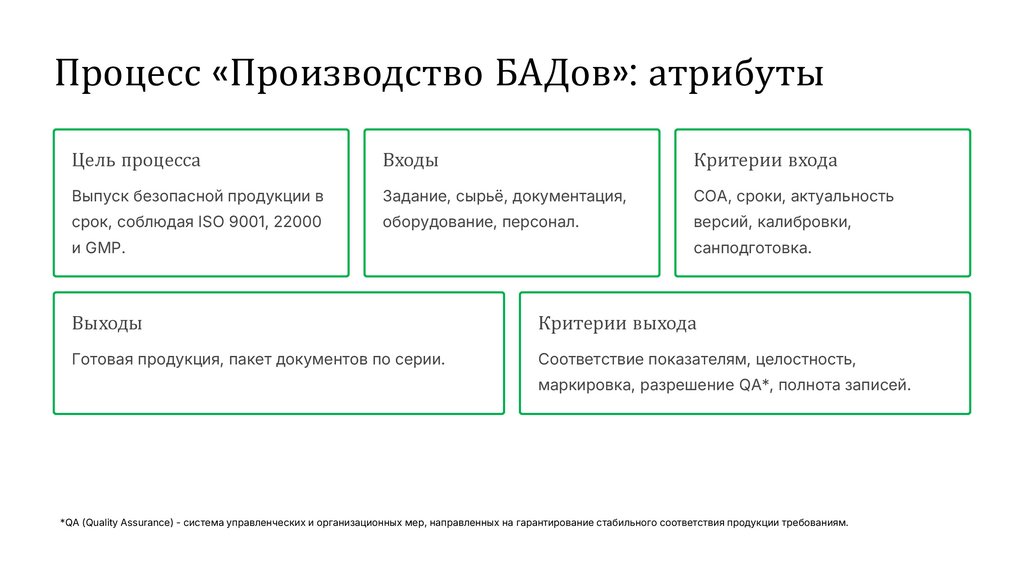
Процесс «Производство БАДов»: атрибутыЦель процесса
Входы
Критерии входа
Выпуск безопасной продукции в
Задание, сырьё, документация,
COA, сроки, актуальность
срок, соблюдая ISO 9001, 22000
оборудование, персонал.
версий, калибровки,
и GMP.
санподготовка.
Выходы
Критерии выхода
Готовая продукция, пакет документов по серии.
Соответствие показателям, целостность,
маркировка, разрешение QA*, полнота записей.
*QA (Quality Assurance) - система управленческих и организационных мер, направленных на гарантирование стабильного соответствия продукции требованиям.
13.
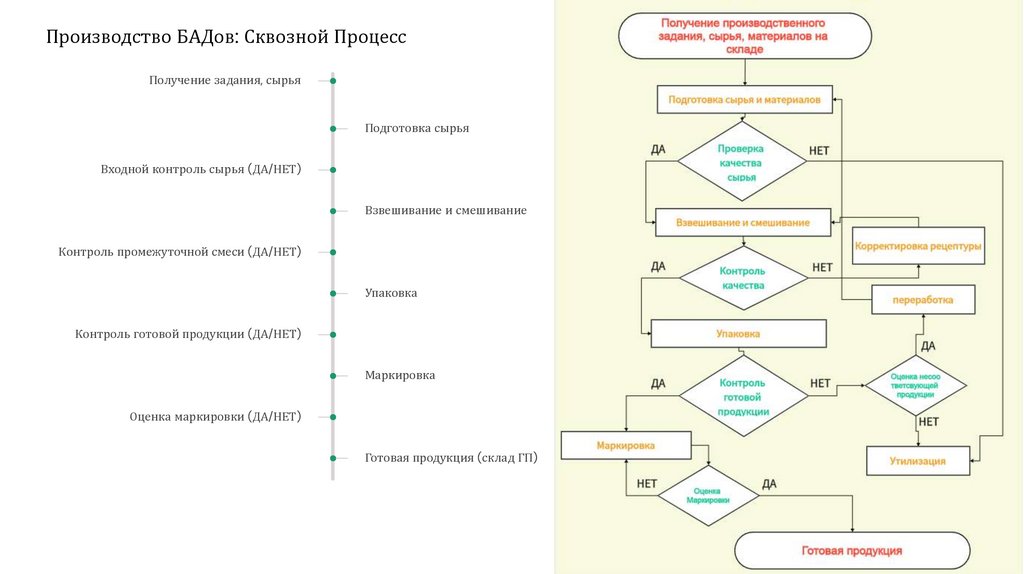
Производство БАДов: Сквозной ПроцессПолучение задания, сырья
Подготовка сырья
Входной контроль сырья (ДА/НЕТ)
Взвешивание и смешивание
Контроль промежуточной смеси (ДА/НЕТ)
Упаковка
Контроль готовой продукции (ДА/НЕТ)
Маркировка
Оценка маркировки (ДА/НЕТ)
Готовая продукция (склад ГП)
14.
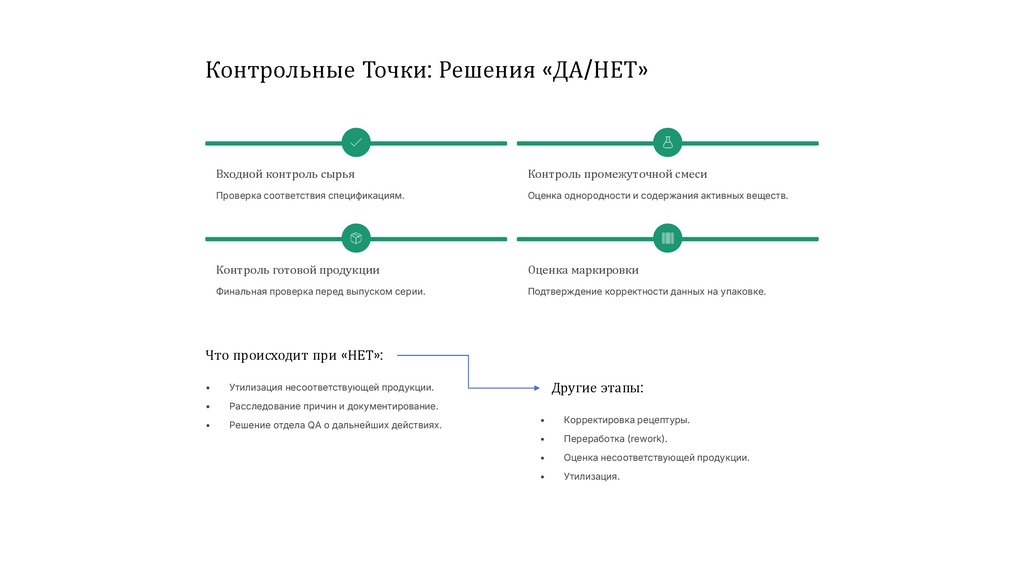
Контрольные Точки: Решения «ДА/НЕТ»Входной контроль сырья
Контроль промежуточной смеси
Проверка соответствия спецификациям.
Оценка однородности и содержания активных веществ.
Контроль готовой продукции
Оценка маркировки
Финальная проверка перед выпуском серии.
Подтверждение корректности данных на упаковке.
Что происходит при «НЕТ»:
Утилизация несоответствующей продукции.
Расследование причин и документирование.
Решение отдела QA о дальнейших действиях.
Другие этапы:
Корректировка рецептуры.
Переработка (rework).
Оценка несоответствующей продукции.
Утилизация.
15.
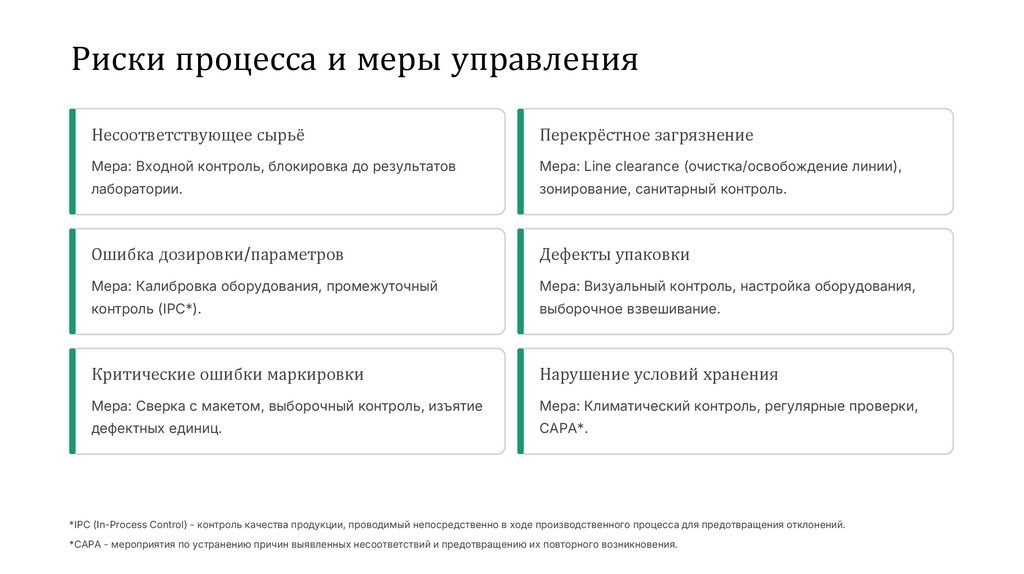
Риски процесса и меры управленияНесоответствующее сырьё
Перекрёстное загрязнение
Мера: Входной контроль, блокировка до результатов
Мера: Line clearance (очистка/освобождение линии),
лаборатории.
зонирование, санитарный контроль.
Ошибка дозировки/параметров
Дефекты упаковки
Мера: Калибровка оборудования, промежуточный
Мера: Визуальный контроль, настройка оборудования,
контроль (IPC*).
выборочное взвешивание.
Критические ошибки маркировки
Нарушение условий хранения
Мера: Сверка с макетом, выборочный контроль, изъятие
Мера: Климатический контроль, регулярные проверки,
дефектных единиц.
CAPA*.
*IPC (In-Process Control) - контроль качества продукции, проводимый непосредственно в ходе производственного процесса для предотвращения отклонений.
*CAPA - мероприятия по устранению причин выявленных несоответствий и предотвращению их повторного возникновения.
16.
ДП | СОП | РИ | ДИДокументы СМК: ДП, СОП, Рабочая и Должностная Инструкции
Документированная Процедура (ДП)
• Пример: Входной контроль сырья.
Стандартная Операционная Процедура
(СОП)
• Определяет: кто, что, когда, где фиксирует.
• Пример: Упаковка продукции.
• Регулирует: карантин, допуск, блокировку партий.
• Обеспечивает: единый порядок
выполнения, контроль, записи.
• Соответствует: требованиям GMP.
Рабочая Инструкция
Должностная Инструкция
• Пошаговое выполнение операций
(например, взвешивание/смешивание).
• Определяет ответственность и полномочия.
• Включает контрольные действия и записи.
• Устанавливает требования к квалификации
(например, оператор линии/мастер смены).
17.
18.
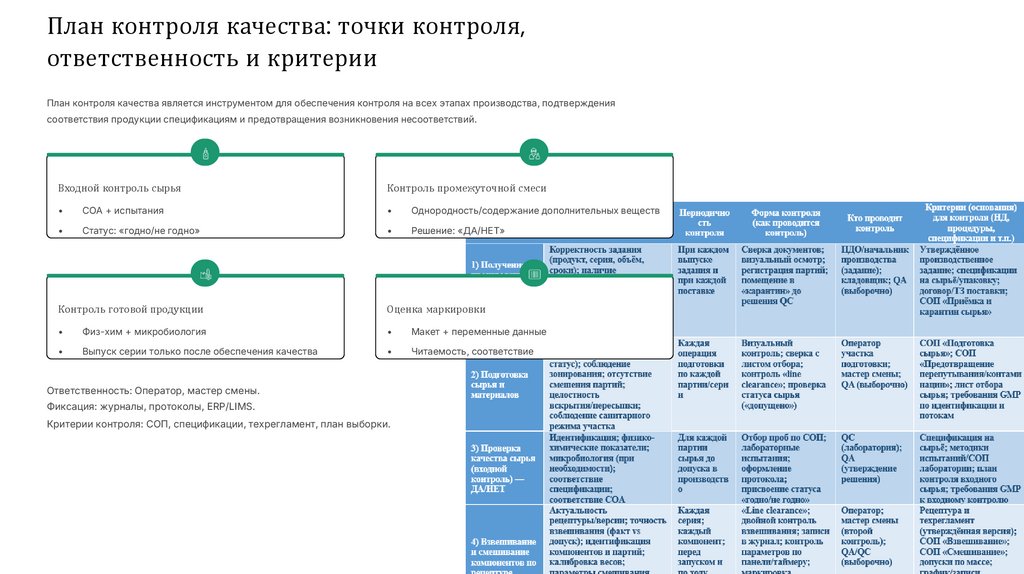
План контроля качества: точки контроля,ответственность и критерии
План контроля качества является инструментом для обеспечения контроля на всех этапах производства, подтверждения
соответствия продукции спецификациям и предотвращения возникновения несоответствий.
Входной контроль сырья
Контроль промежуточной смеси
COA + испытания
Однородность/содержание дополнительных веществ
Статус: «годно/не годно»
Решение: «ДА/НЕТ»
Контроль готовой продукции
Оценка маркировки
Физ-хим + микробиология
Макет + переменные данные
Выпуск серии только после обеспечения качества
Читаемость, соответствие
Ответственность: Оператор, мастер смены.
Фиксация: журналы, протоколы, ERP/LIMS.
Критерии контроля: СОП, спецификации, техрегламент, план выборки.
19.
Улучшение (PDCA): обратная связь + нормативныетребования
Анкета обратной связи
Сбор и анализ обратной связи от клиентов — важнейший элемент цикла PDCA (Plan-Do-Check-Act), позволяющий непрерывно
совершенствовать нашу продукцию и сервис.
Цель анкеты
Как используем
Ключевые показатели
Оценка качества и
стабильности партий.
Качество упаковки и
Анализ ответов для выявления
проблем.
корректирующих действий
Соблюдение сроков, работа
(CAPA).
менеджера.
партии к партии).
Инициирование
маркировки.
Стабильность качества (от
Отсутствие дефектов
упаковки/маркировки.
Соблюдение сроков (NPS: 0–10).
Непрерывное улучшение
процессов и сервиса.
Нормативная база
ФЗ от 07.06.2025 № 150-ФЗ “О внесении изменений в отдельные законодательные акты РФ”
ФЗ № 38 ФЗ «О рекламе»
ТР ЕАЭС 021/2011 «О безопасности пищевой продукции»
ТР ЕАЭС 022/2011 «Пищевая продукция в части её маркировки»
Постановления Правительства РФ № 886 об обязательной маркировке БАД и более новые версии
СанПиН 1.2.3685-21 «Гигиенические нормативы и требования»
ФЗ № 184 ФЗ «О техническом регулировании»
20.
ВыводВ ходе работы на примере виртуальной организации по производству БАДов были разработаны
ключевые элементы системы менеджмента качества с учетом видов деятельности предприятия.
Определены контекст и требования заинтересованных сторон, установлены цели и политика в
области качества, описана организационная ответственность и построена карта процессов.
Для основного процесса «Производство БАДов» выделены этапы и контрольные точки, выполнена
оценка рисков и определены меры управления, а также показана логика подтверждения
соответствия и выпуска продукции.
Предложенный подход обеспечивает управляемость процессов, прослеживаемость,
профилактику несоответствий и основу для постоянного улучшения по циклу PDCA.