Похожие презентации:
Многоатомные спирты
1.
Многоатомныеспирты
2.
Многоатомныеспирты —
это производные углеводородов, в
молекулах которых два и более атома
водорода замещены на гидроксильные
группы.
Многоатомные
спирты
3.
Представители многоатомных спиртовДвухатомные спирты (гликоли)
Трёхатомные спирты
HO – CH2 – CH2 – OH
СН2ОН – СНОН – СН2ОН
Этиленгликоль
Глицерин
Этандиол-1,2
Пропантриол-1,2,3
Этиленгликоль и глицерин – бесцветные вязкие жидкости, тяжелее
воды, неограниченно растворимы в воде, хорошо растворяются в
этаноле.
4.
Этиленгликоль:• ядовитое вещество;
• входит в состав антифризов;
• водные растворы не
кристаллизуются при низких
температурах.
Этиленгликоль
5.
Глицерин:• имеет сладковатый вкус;
• гигроскопичен;
• нелетуч.
Глицерин
6.
Карл ВильгельмШееле
(1742–1786 гг.)
Впервые в 1783 году получил
глицерин из оливкового масла.
7.
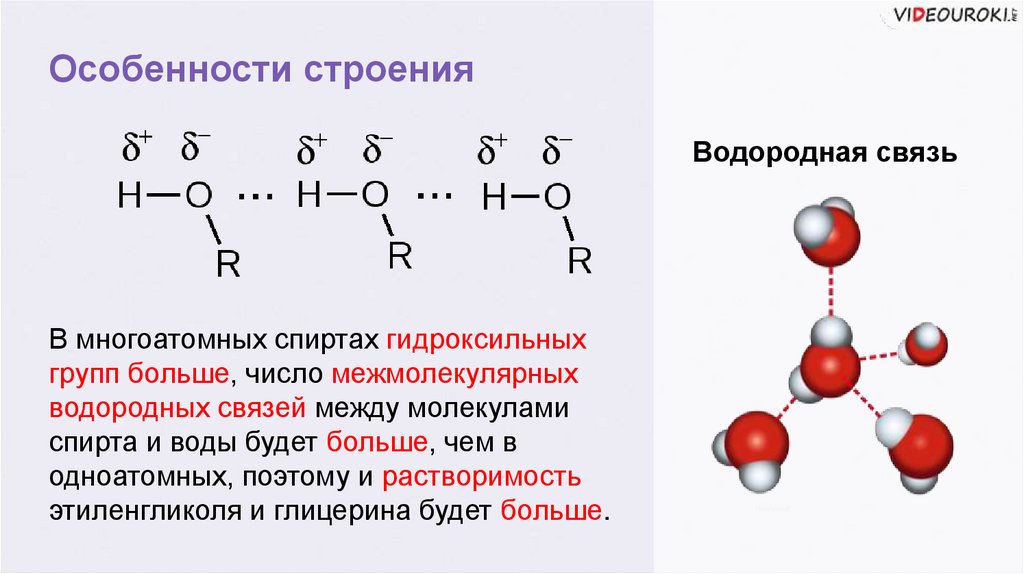
Особенности строенияВодородная связь
В многоатомных спиртах гидроксильных
групп больше, число межмолекулярных
водородных связей между молекулами
спирта и воды будет больше, чем в
одноатомных, поэтому и растворимость
этиленгликоля и глицерина будет больше.
8.
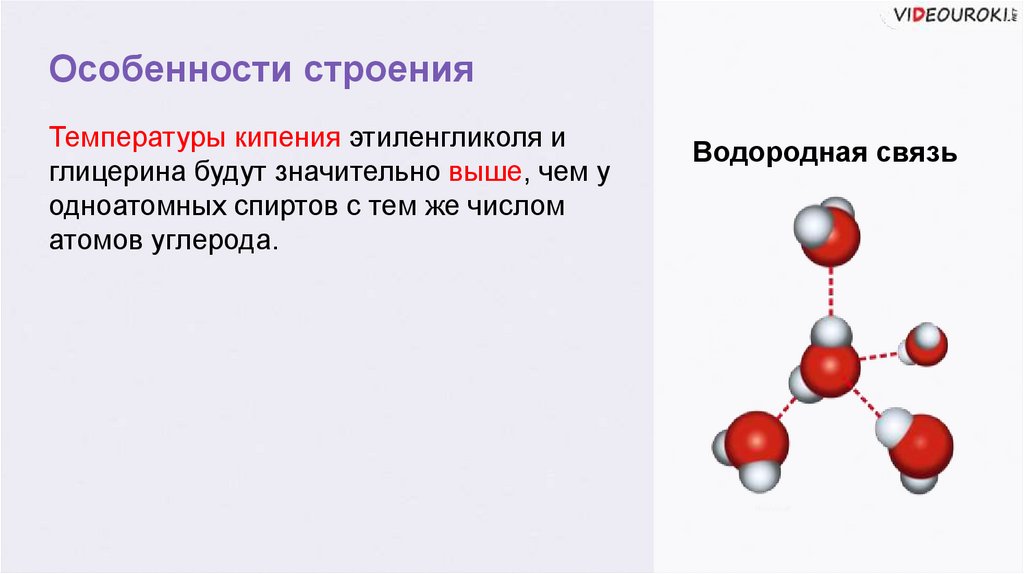
Особенности строенияТемпературы кипения этиленгликоля и
глицерина будут значительно выше, чем у
одноатомных спиртов с тем же числом
атомов углерода.
Водородная связь
9.
Химические свойства многоатомных спиртовДля многоатомных спиртов характерны свойства, обусловленные
наличием функциональной гидроксильной группы, а также
одновременным присутствием нескольких гидроксильных групп в
молекуле.
Реакции со
щелочными металлами
Динатрийгликолят
Кислотные свойства
CH2OH – CH2OH + 2Na → CH2ONa – CH2ONa + H2↑
2CH2OH – CHOH – CH2OH + 6Na → 2CH2ONa – CHONa – CH2ONa +
+3H2↑
Тринатрийглицерат
10.
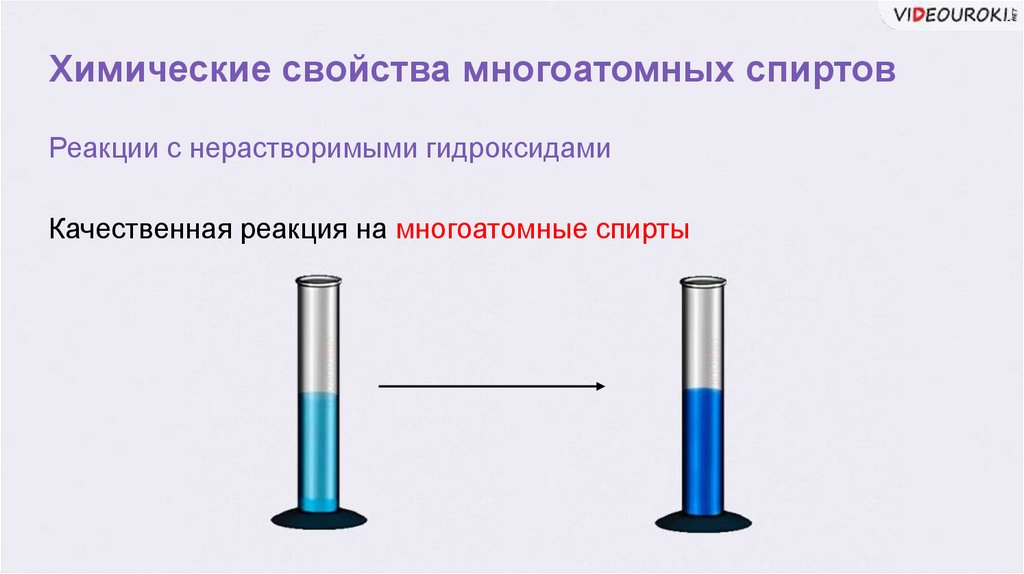
Химические свойства многоатомных спиртовРеакции с нерастворимыми гидроксидами
Качественная реакция на многоатомные спирты
11.
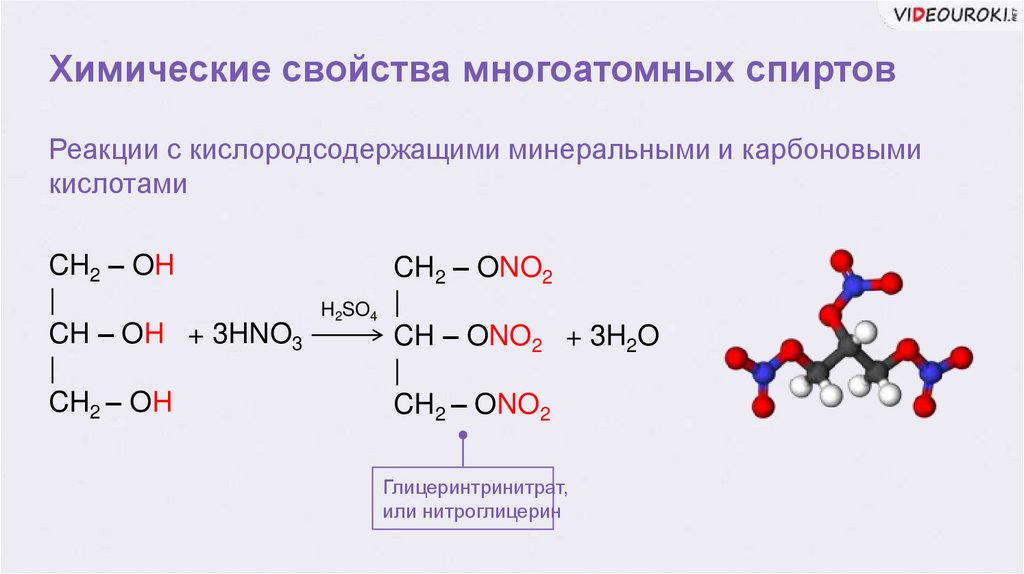
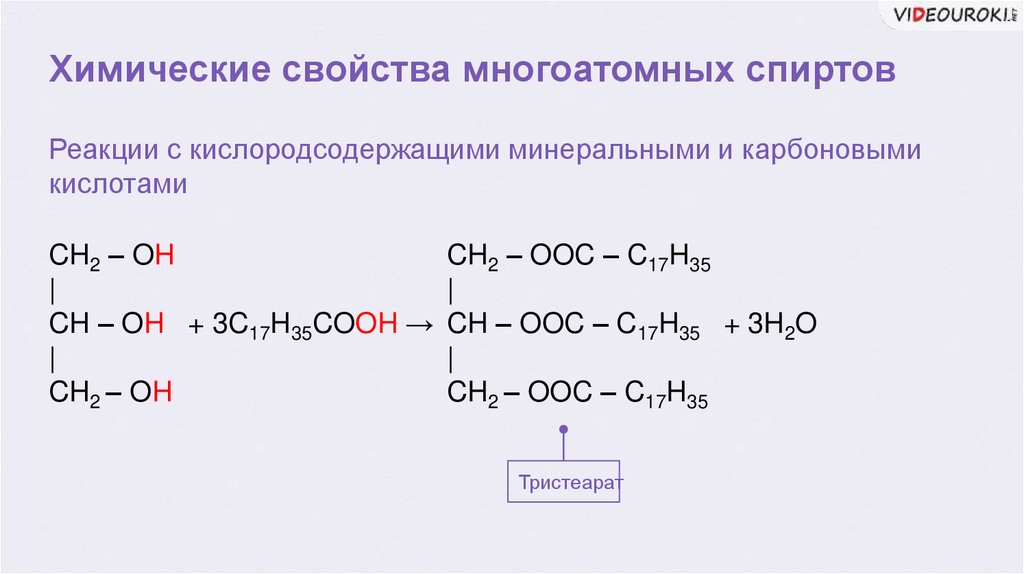
Химические свойства многоатомных спиртовРеакции с кислородсодержащими минеральными и карбоновыми
кислотами
CH2 – OH
CH2 – ONO2
|
H2SO4 |
CH – OH + 3HNO3
CH – ONO2 + 3H2O
|
|
CH2 – OH
CH2 – ONO2
Глицеринтринитрат,
или нитроглицерин
12.
Химические свойства многоатомных спиртовРеакции с кислородсодержащими минеральными и карбоновыми
кислотами
CH2 – OH
CH2 – OOC – C17H35
|
|
CH – OH + 3C17H35COOH → CH – OOC – C17H35 + 3H2O
|
|
CH2 – OH
CH2 – OOC – C17H35
Тристеарат
13.
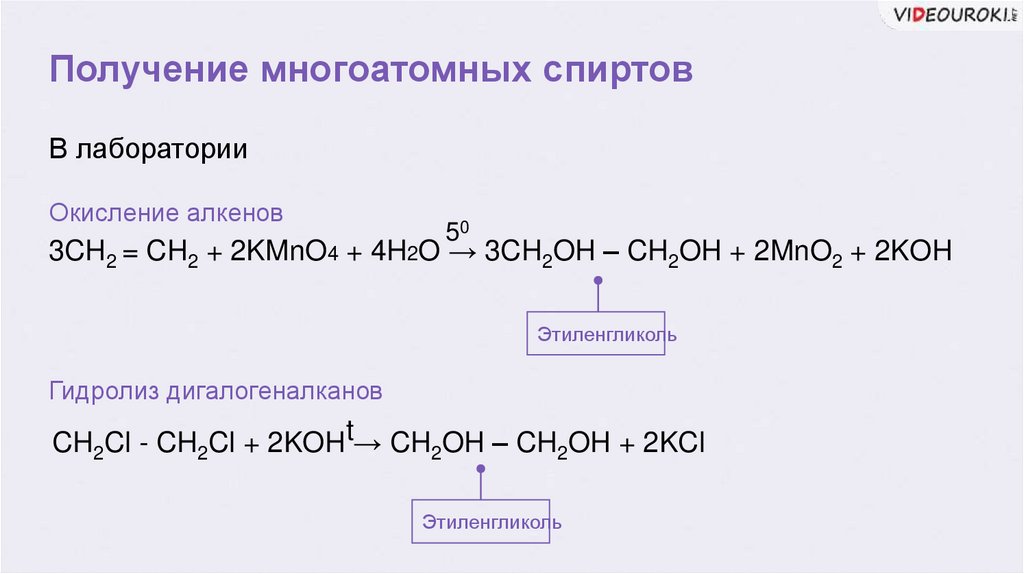
Получение многоатомных спиртовВ лаборатории
Окисление алкенов
50
3CH2 = CH2 + 2KMnO4 + 4H2O → 3CH2OH – CH2OH + 2MnO2 + 2KOH
Этиленгликоль
Гидролиз дигалогеналканов
CH2Cl - CH2Cl + 2KOHt→ CH2OH – CH2OH + 2KCl
Этиленгликоль
14.
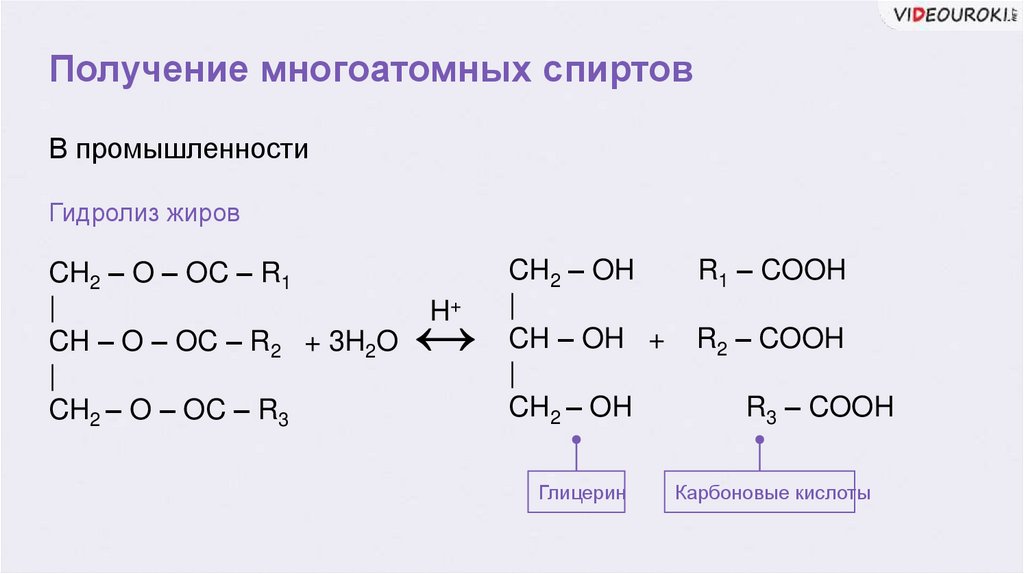
Получение многоатомных спиртовВ промышленности
Гидролиз жиров
CH2 – O – OC – R1
|
CH – O – OC – R2 + 3H2O
|
CH2 – O – OC – R3
H+
↔
CH2 – OH
|
CH – OH +
|
CH2 – OH
R1 – COOH
R2 – COOH
Глицерин
Карбоновые кислоты
R3 – COOH
15.
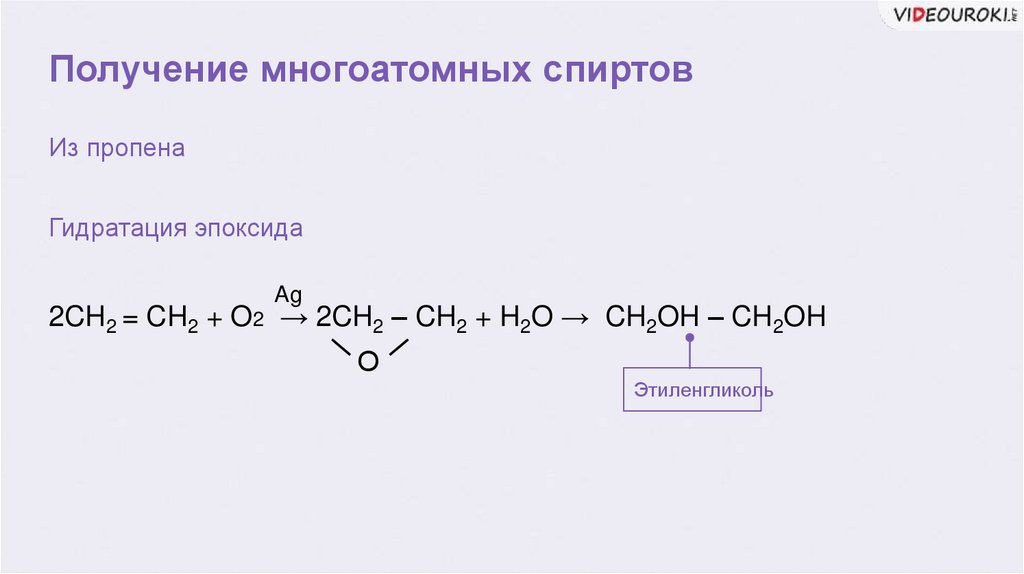
Получение многоатомных спиртовИз пропена
Гидратация эпоксида
Ag
2CH2 = CH2 + O2 → 2CH2 – CH2 + H2O → CH2OH – CH2OH
О
Этиленгликоль
16.
Применение этиленгликоляСинтез полимерных
материалов
Получение волокна
лавсана
В качестве
антифриза
17.
Применение этиленгликоляПолучение
пластификаторов
В лакокрасочной
промышленности
18.
Применение глицеринаПриготовление
мазей
В кожевенной
промышленности
В текстильной
промышленности
19.
Применение глицеринаВ косметических
средствах
Как добавка в
зубных пастах
Изготовления клея
20.
Применение глицеринаПолучение
антифризов
Получение
нитроглицерина
21.
Применение нитроглицеринаПолучение
бездымного пороха
Получение
динамита
Как лечебное
средство
22.
Альфред БернхардНобель
(1833–1896 гг.)
А. Нобель изобрёл динамит, он завещал
часть прибыли своих заводов по
производству динамита на выплату
Нобелевских премий за выдающиеся
достижения в науке и литературе.
23.
• Многоатомные спирты являются производнымиуглеводородов, в которых содержится несколько
гидроксильных групп.
• Многоатомные спирты взаимодействуют с активными
металлами, гидроксидами тяжёлых металлов,
кислотами.
• Качественной реакцией на многоатомные спирты
является реакция с гидроксидом меди (II).
• Многоатомные спирты имеют широкое применение во
многих областях народного хозяйства.















 Химия
Химия








