Похожие презентации:
Органические вещества
1.
РОССИЙСКИЙ ГОСУДАРСТВЕННЫЙ СОЦИАЛЬНЫЙ УНИВЕРСИТЕТФакультет информационных технологий и техносферной безопасности
КАФЕДРА СОЦИАЛЬНОЙ ЭКОЛОГИИ И ПРИРОДОПОЛЬЗОВАНИЯ
Биология
Органические вещества
к.п.н, доцент кафедры
социальной экологии
и природопользования
Гапоненко А.В.
Москва, 2015 г
2.
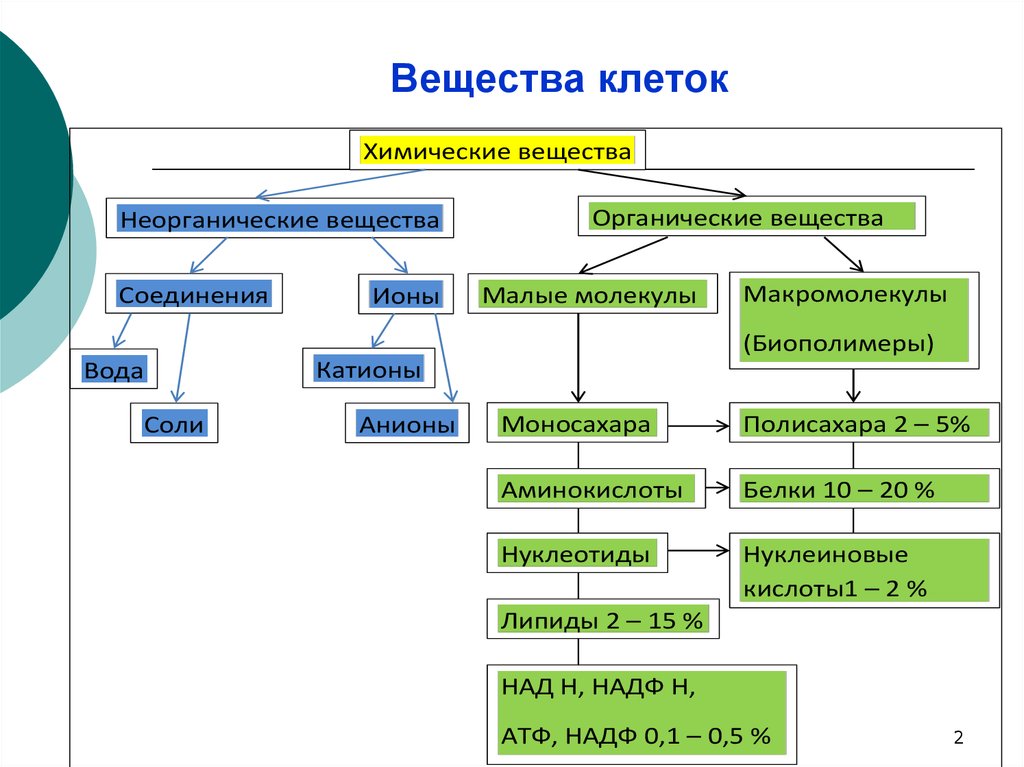
Вещества клетокХимические вещества
Неорганические вещества
Соединения
Ионы
Органические вещества
Малые молекулы
Макромолекулы
(Биополимеры)
Катионы
Вода
Соли
Анионы
Моносахара
Полисахара 2 – 5%
Аминокислоты
Белки 10 – 20 %
Нуклеотиды
Нуклеиновые
кислоты1 – 2 %
Липиды 2 – 15 %
НАД Н, НАДФ Н,
АТФ, НАДФ 0,1 – 0,5 %
2
3.
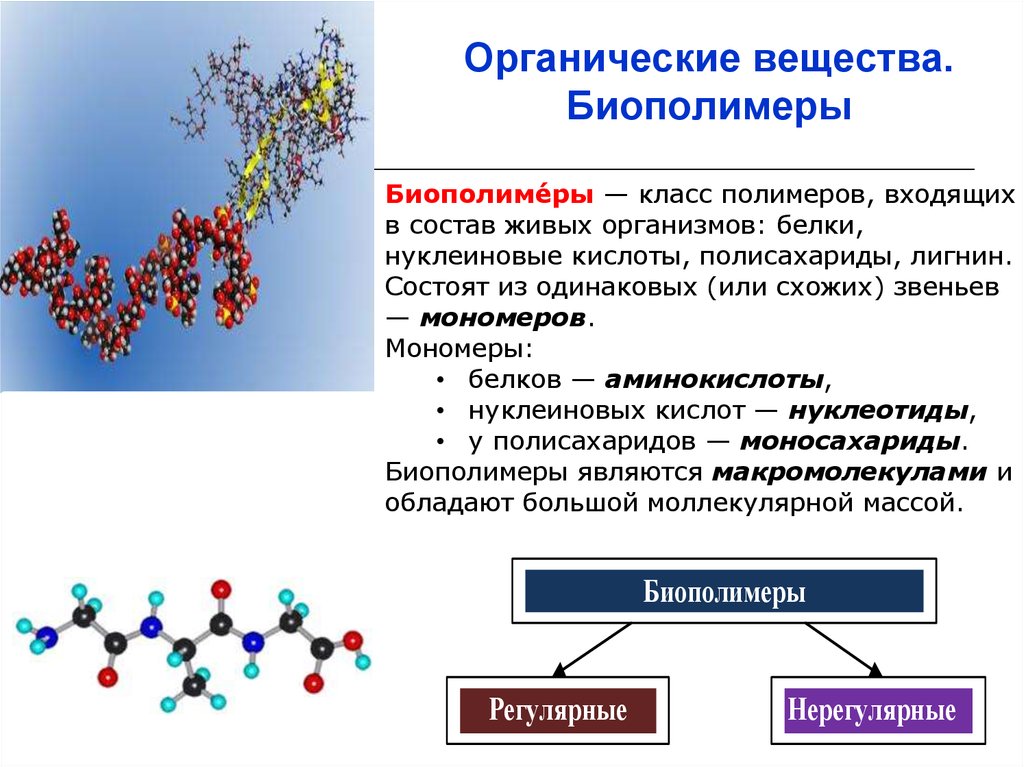
Органические вещества.Биополимеры
Биополиме́ры — класс полимеров, входящих
в состав живых организмов: белки,
нуклеиновые кислоты, полисахариды, лигнин.
Состоят из одинаковых (или схожих) звеньев
— мономеров.
Мономеры:
• белков — аминокислоты,
• нуклеиновых кислот — нуклеотиды,
• у полисахаридов — моносахариды.
Биополимеры являются макромолекулами и
обладают большой моллекулярной массой.
Биополимеры
Регулярные
Нерегулярные
3
4.
Органические вещества: белки«Повсюду, где мы встречаем жизнь, мы находим, что она связана с
каким-либо белковым телом, и повсюду, где мы встречаем какоелибо белковое тело, не находящееся в процессе разложения, мы
без исключения встречаем и явление жизни».
( К. Маркс, Ф.Энгельс. Собрание сочинений.Т.20).
Белки – это сложные высокомолекулярные природные соединения,
построенные из остатков а-аминокислот, соединенных
пептидными (амидными) связями ―СО ― NH ―.
4
5. История открытия белка
Первый белок, очищенный от примесей былполучен в 1728 г. Я. Беккари.
Это был белок пшеничного зерна клейковина
Белки стали называть
протеинами
(от греческого protos – первый)
6. Уровни структурной организации белков: 4 уровня
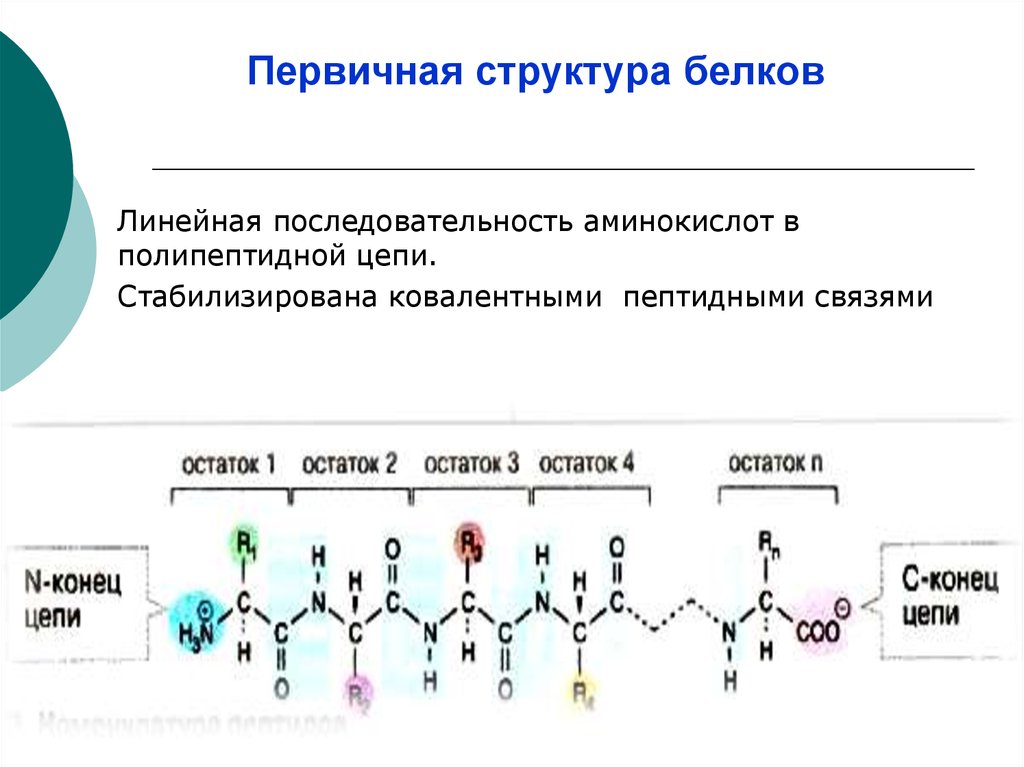
7. Первичная структура белков
Линейная последовательность аминокислот вполипептидной цепи.
Стабилизирована ковалентными пептидными связями
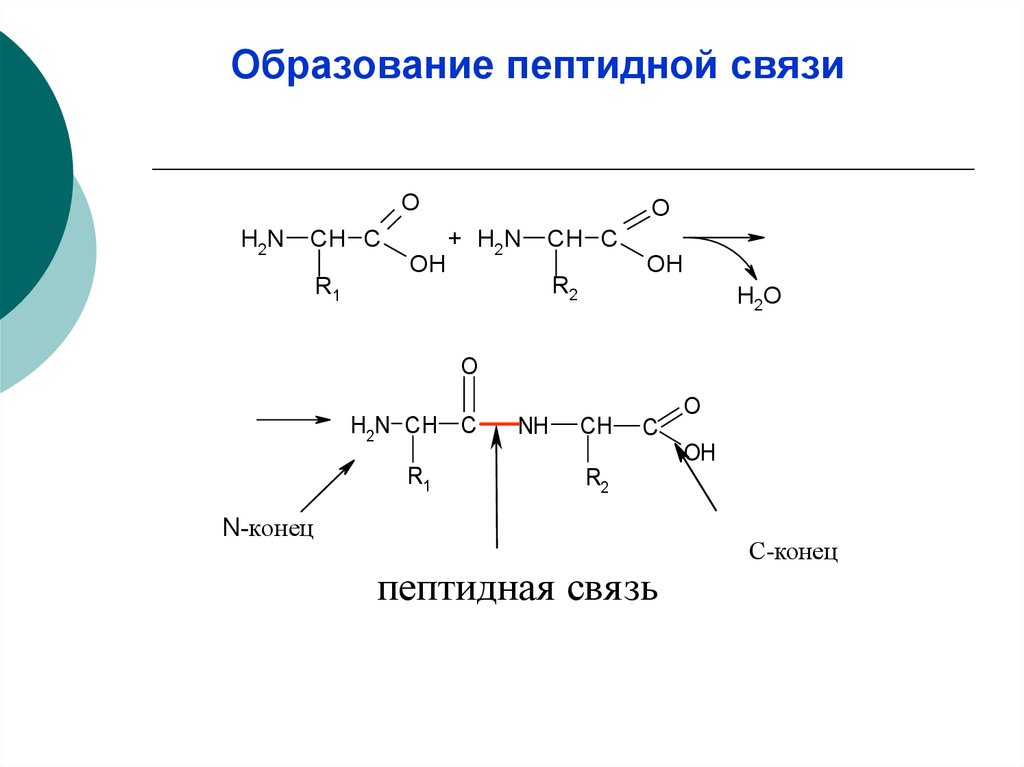
8. Образование пептидной связи
OH2N
CH C
OH
O
+ H2N
CH C
OH
R2
R1
H2O
O
H2N CH C
R1
NH
CH
C
O
OH
R2
N-конец
пептидная свя зь
С-конец
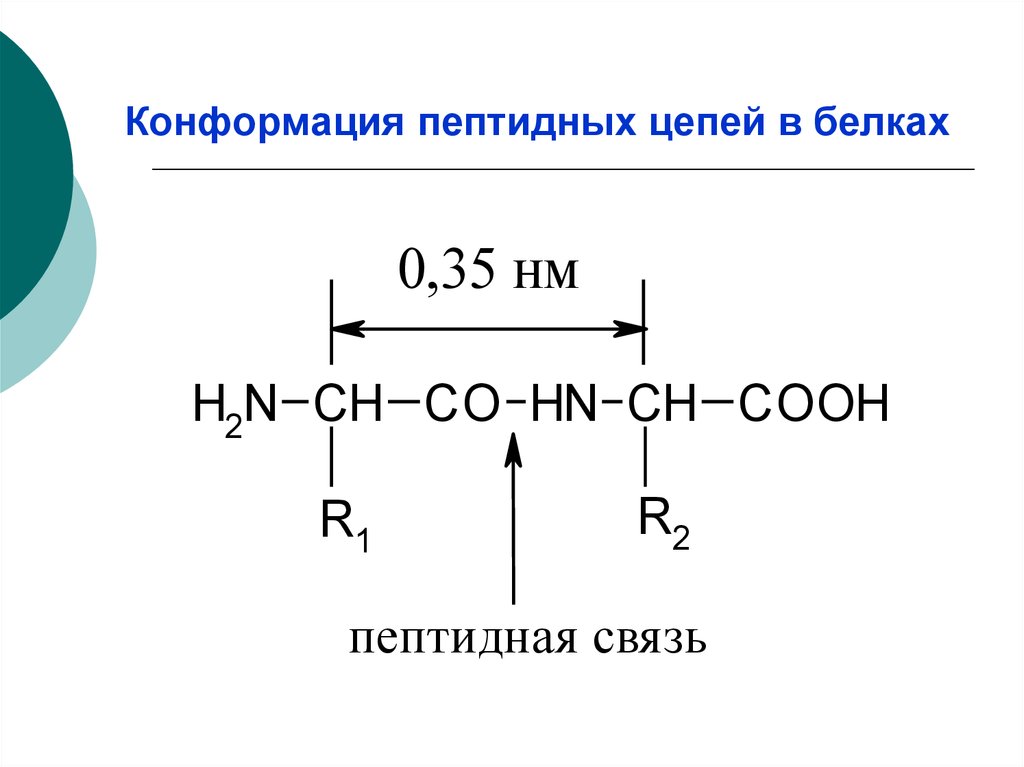
9. Конформация пептидных цепей в белках
0,35 нмH2N CH CO HN CH COOH
R1
R2
пептидная свя зь
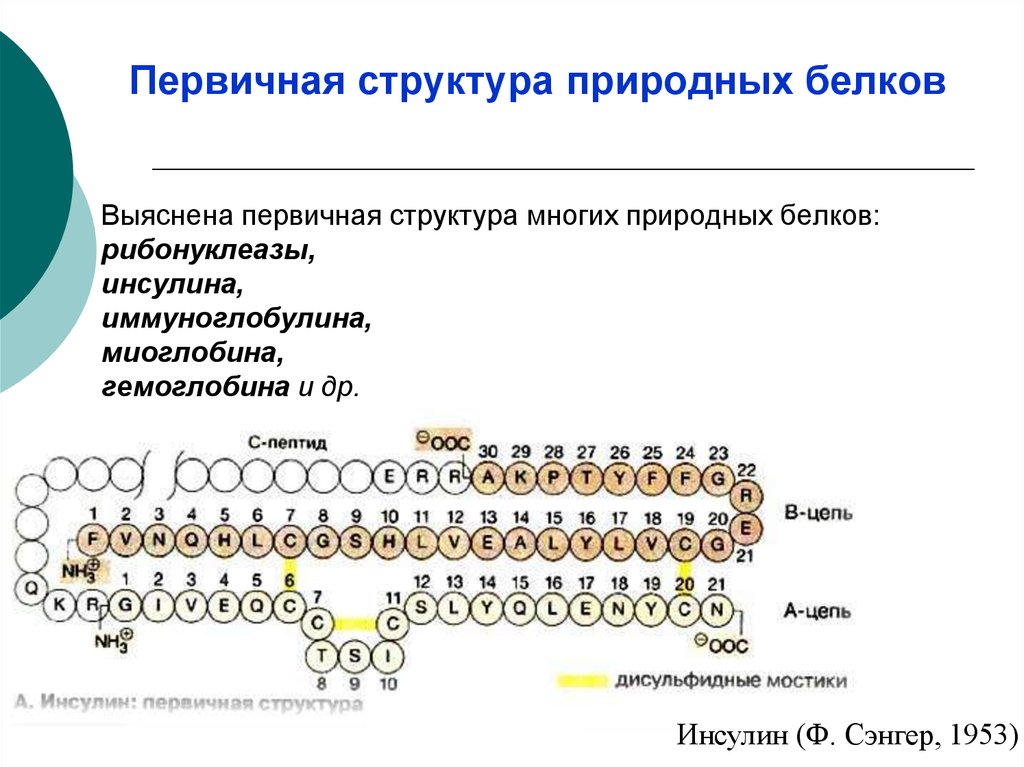
10. Выяснена первичная структура многих природных белков: рибонуклеазы, инсулина, иммуноглобулина, миоглобина, гемоглобина и др.
Первичная структура природных белковВыяснена первичная структура многих природных белков:
рибонуклеазы,
инсулина,
иммуноглобулина,
миоглобина,
гемоглобина и др.
Инсулин (Ф. Сэнгер, 1953)
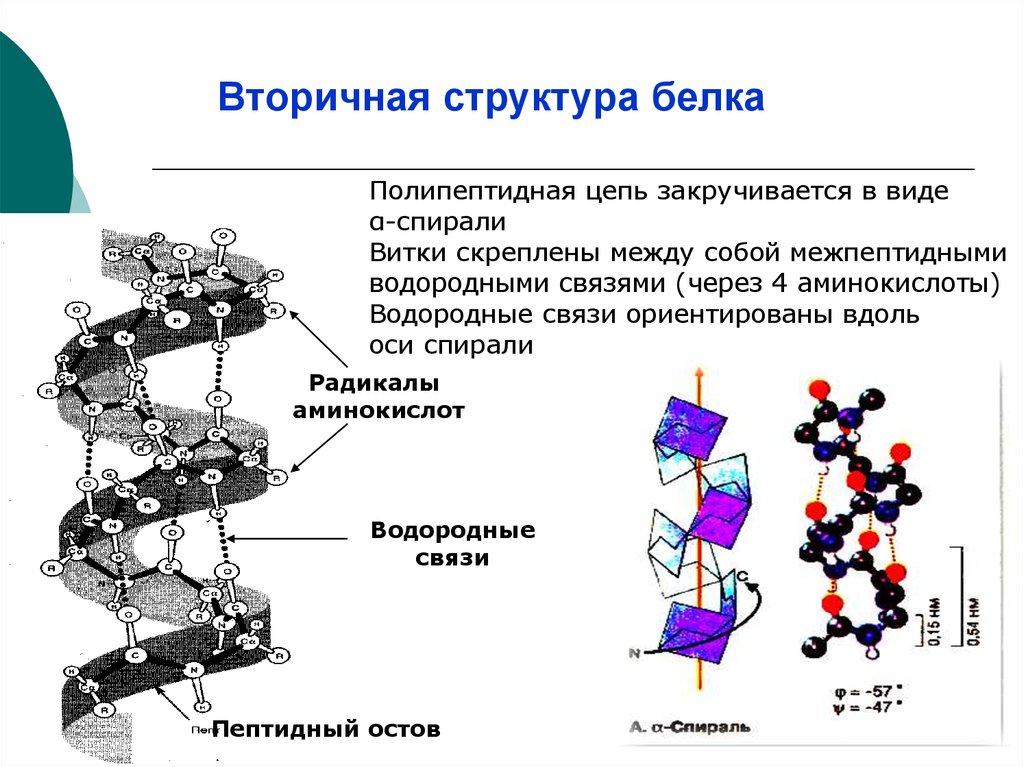
11. Вторичная структура белка
Полипептидная цепь закручивается в видеα-спирали
Витки скреплены между собой межпептидными
водородными связями (через 4 аминокислоты)
Водородные связи ориентированы вдоль
оси спирали
Радикалы
аминокислот
Водородные
связи
Пептидный остов
12. Третичная структура белка
Трехмерная пространственнаяструктура образуется за счет
взаимодействия между радикалами
аминокислот, которые располагаются
на значительном расстоянии друг от
друга в полипептидной цепи.
Стабилизирована ионными, водородными,
гидрофобными связями, дисульфидными
связями
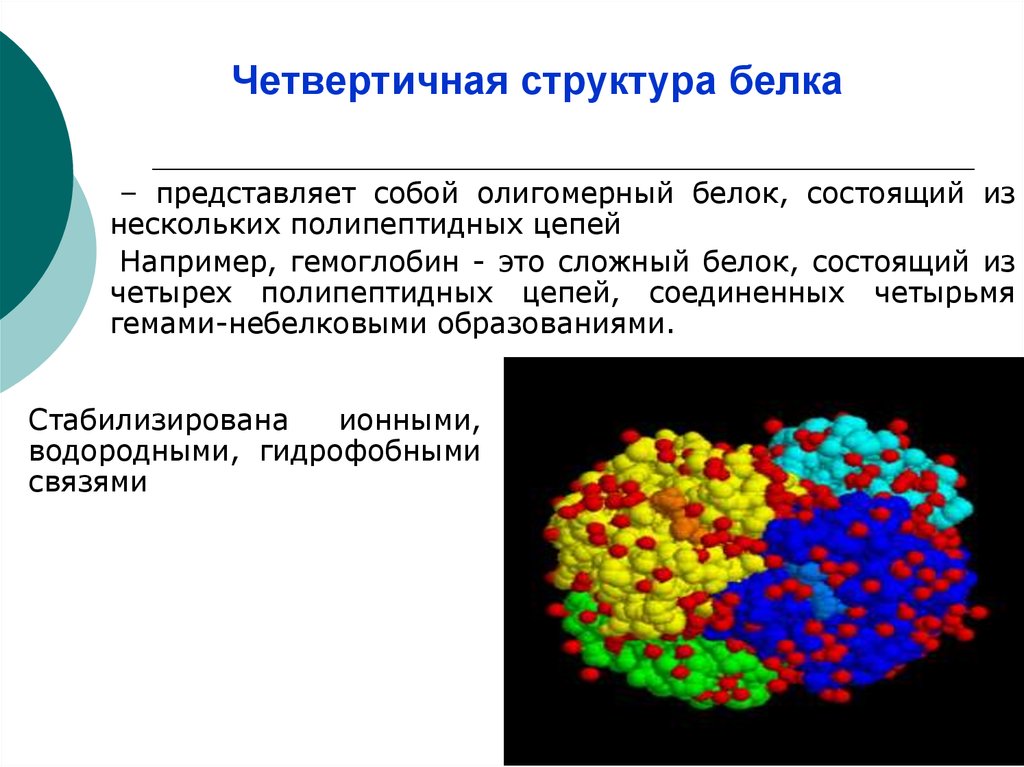
13. Четвертичная структура белка
– представляет собой олигомерный белок, состоящий изнескольких полипептидных цепей
Например, гемоглобин - это сложный белок, состоящий из
четырех полипептидных цепей, соединенных четырьмя
гемами-небелковыми образованиями.
Стабилизирована
ионными,
водородными, гидрофобными
связями
14. По форме молекул белки делятся на 2 группы:
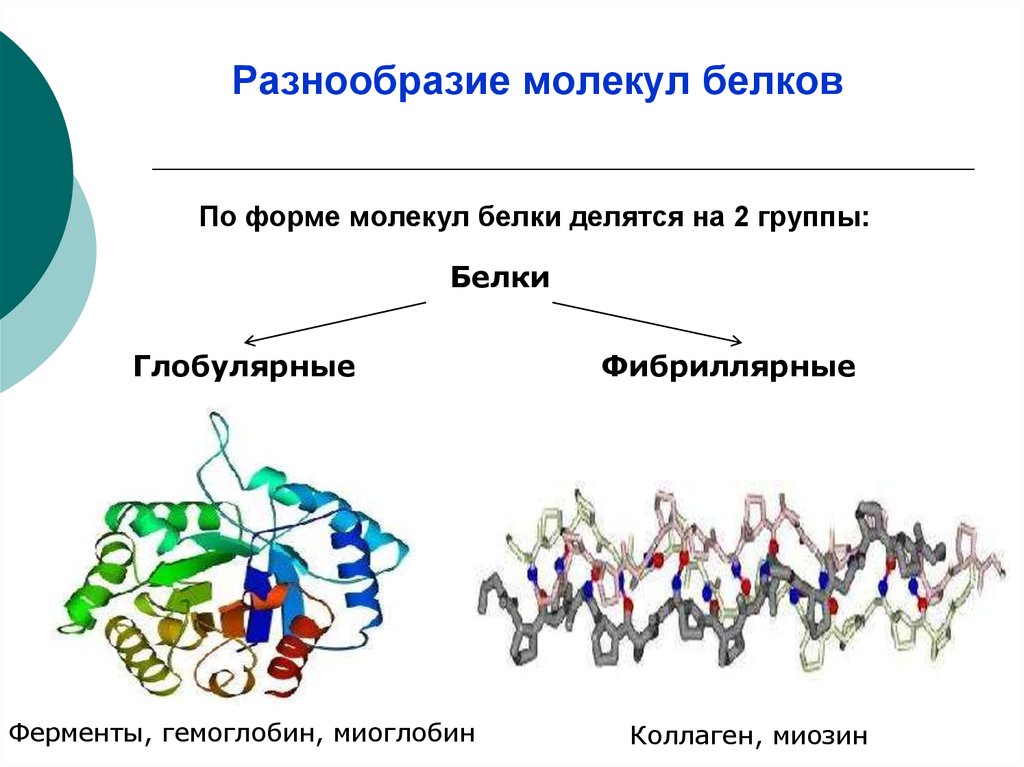
Разнообразие молекул белковПо форме молекул белки делятся на 2 группы:
Белки
Глобулярные
Ферменты, гемоглобин, миоглобин
Фибриллярные
Коллаген, миозин
15.
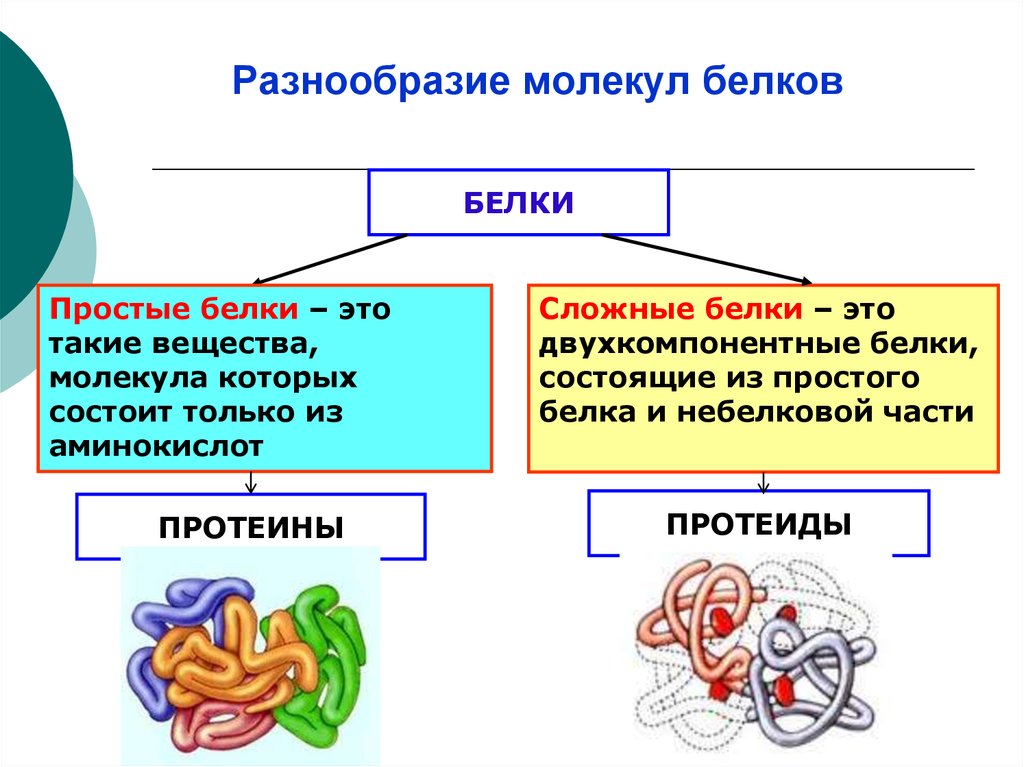
Разнообразие молекул белковБЕЛКИ
Простые белки – это
такие вещества,
молекула которых
состоит только из
аминокислот
ПРОТЕИНЫ
Сложные белки – это
двухкомпонентные белки,
состоящие из простого
белка и небелковой части
ПРОТЕИДЫ
16.
Свойства белковБелки представляют собой наиболее сложные коллоидные соединения.
1. В растворах белки обнаруживают очень низкое осмотическое
давление
2. Незначительная способность к диффузии
3. Высокая вязкость
4. Набухание в очень больших пределах с образованием гелей и
студней
5. Способность к адсорбции
6. Амфотерность
7. Ионизация, наличие заряда, электрофоретическая подвижность
8. Гидрофильность, растворимость в воде
9. Склонность к денатурации, осаждению
10. Способность к гидролизу с расщеплением пептидных связей
11. Растворы белков обладают способностью к светорассеянию и
способностью к поглощению УФ-излучения при 280 нм
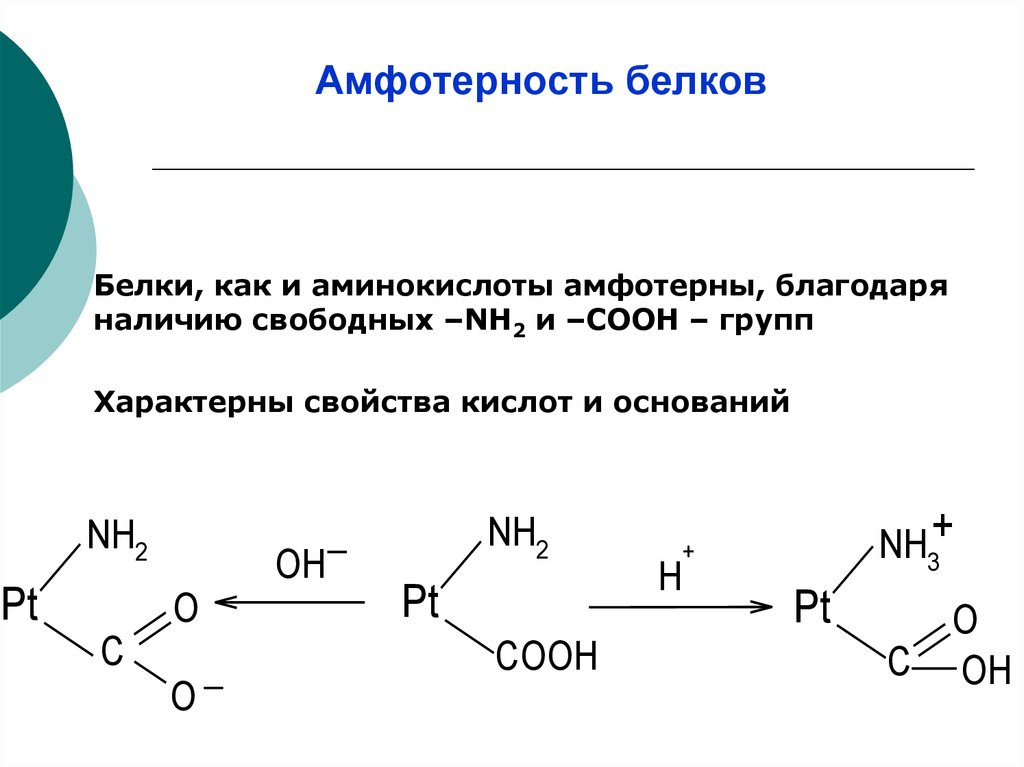
17. Амфотерность белков
Белки, как и аминокислоты амфотерны, благодаряналичию свободных –NH2 и –СООН – групп
Характерны свойства кислот и оснований
NH2
Pt
OH
O
C
NH2
Pt
COOH
O
NH3+
+
H
Pt
C
O
OH
18. Денатурация белков
В основе денатурации лежат глубокиевнутримолекулярные перестройки, приводящие к
изменению специфической конфигурации белковой
молекулы (вторичной, третичной структуры)
Денатурация
Физические агенты:
нагревание,
УФ-лучи,
рентгеновские лучи,
ультразвуковое излучение,
высокое давление
Химические агенты:
концентрированные кислоты и
щелочи,
соли тяжелых металлов,
алкалоидные реактивы,
многие органические
растворители
Необратимая
Обратимая
19. Гидролиз белков
Взаимодействие белков с водой, в ходе которогобелок утрачивает свою первичную структуру:
Белок
Н2О
Н2О
полипептиды
дипептиды
Н2О
Н2О
олигопептиды
аминокислоты
20. Цветные реакции на белки
1. Биуретовая (реакция Пиотровского)Белок + Cu(OH)2 → фиолетовая окраска →
реакция на пептидные связи
2. Ксантопротеиновая
Белок + HNO3(к) → желтая окраска →
реакция на ароматические циклы
3. Фоля
Белок + Pb(NO3)2 +NaOH → черный осадок →
реакция на серу
21. Биологическое значение белков
ФерментативнаяСтруктурная
Биологическое значение
Сигнальная
белков
Защитная
Сократительная
Транспортная
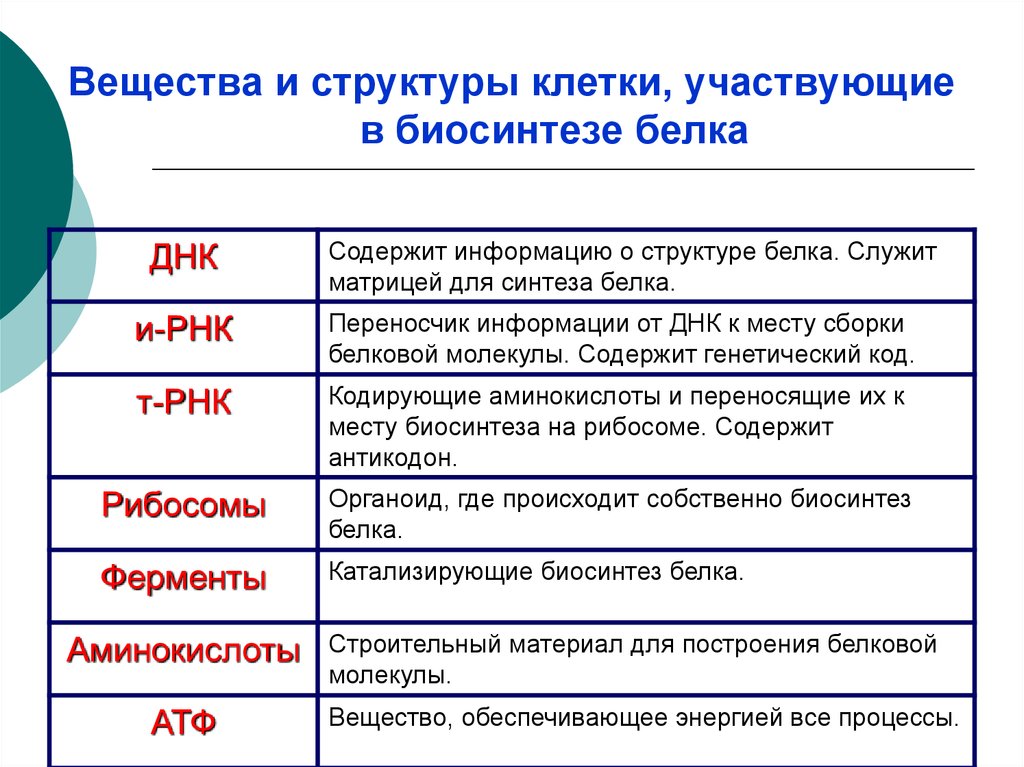
22. Вещества и структуры клетки, участвующие в биосинтезе белка
ДНКСодержит информацию о структуре белка. Служит
матрицей для синтеза белка.
и-РНК
Переносчик информации от ДНК к месту сборки
белковой молекулы. Содержит генетический код.
т-РНК
Кодирующие аминокислоты и переносящие их к
месту биосинтеза на рибосоме. Содержит
антикодон.
Рибосомы
Органоид, где происходит собственно биосинтез
белка.
Ферменты
Катализирующие биосинтез белка.
Аминокислоты
АТФ
Строительный материал для построения белковой
молекулы.
Вещество, обеспечивающее энергией все процессы.
23.
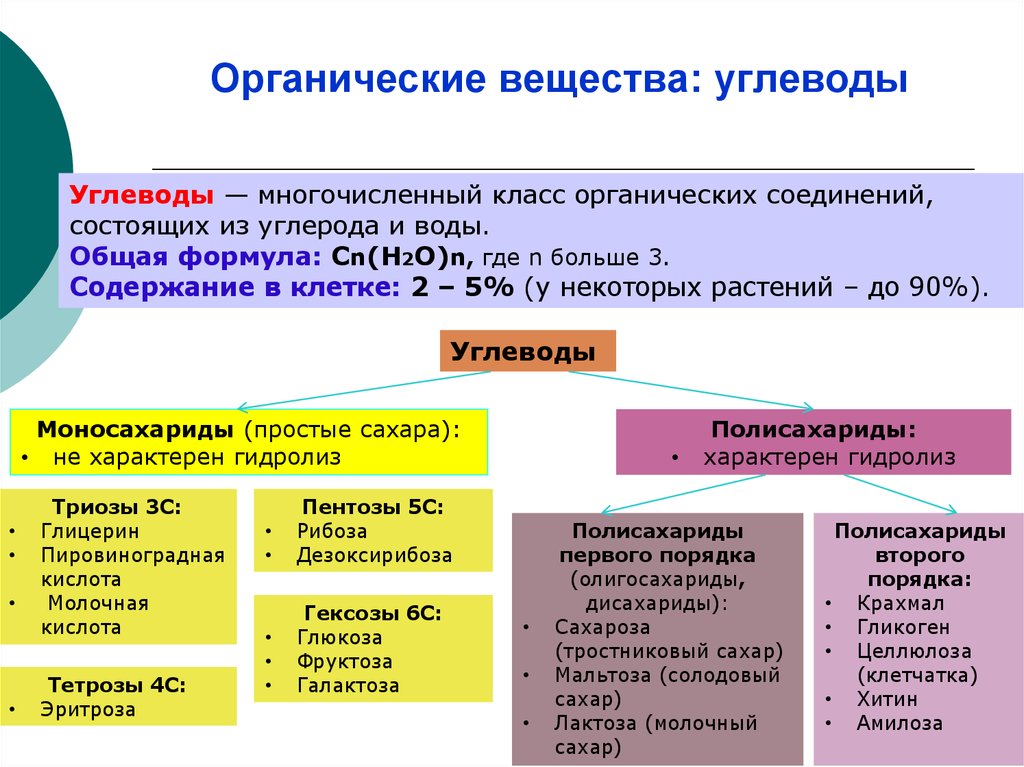
Органические вещества: углеводыУглеводы — многочисленный класс органических соединений,
состоящих из углерода и воды.
Общая формула: Сn(Н2О)n, где n больше 3.
Содержание в клетке: 2 – 5% (у некоторых растений – до 90%).
Углеводы
Моносахариды (простые сахара):
• не характерен гидролиз
Триозы 3С:
Глицерин
Пировиноградная
кислота
Молочная
кислота
Тетрозы 4С:
Эритроза
Пентозы 5С:
Рибоза
Дезоксирибоза
Гексозы 6С:
Глюкоза
Фруктоза
Галактоза
Полисахариды:
характерен гидролиз
Полисахариды
первого порядка
(олигосахариды,
дисахариды):
Сахароза
(тростниковый сахар)
Мальтоза (солодовый
сахар)
Лактоза (молочный
сахар)
Полисахариды
второго
порядка:
• Крахмал
• Гликоген
• Целлюлоза
(клетчатка)
• Хитин
• Амилоза
24.
Биологическое значениеуглеводов
• Энергетическая функция: 1г. углеводов – 17,6 кДж энергии.
• Запасающая (крахмал, гликоген).
• Пластическая функция: углеводы образуют в организме более сложные
вещества (АТФ, ДНК, пентозы и др.).
• Осмотическая функция: наличие углеводов в тканях организма
оказывает влияние на их осмотическое давление.
• Рецепторная функция: олигосахариды входят в состав рецепторов
клеточных мембран.
• Структурная и защитная функция: из углеводов состоит клеточная
стенка растений (целлюлоза), хитин входит в клеточную стенку грибов и
обеспечивает жёсткий экзоскелет насекомых.
24
25.
Органические вещества: липиды25
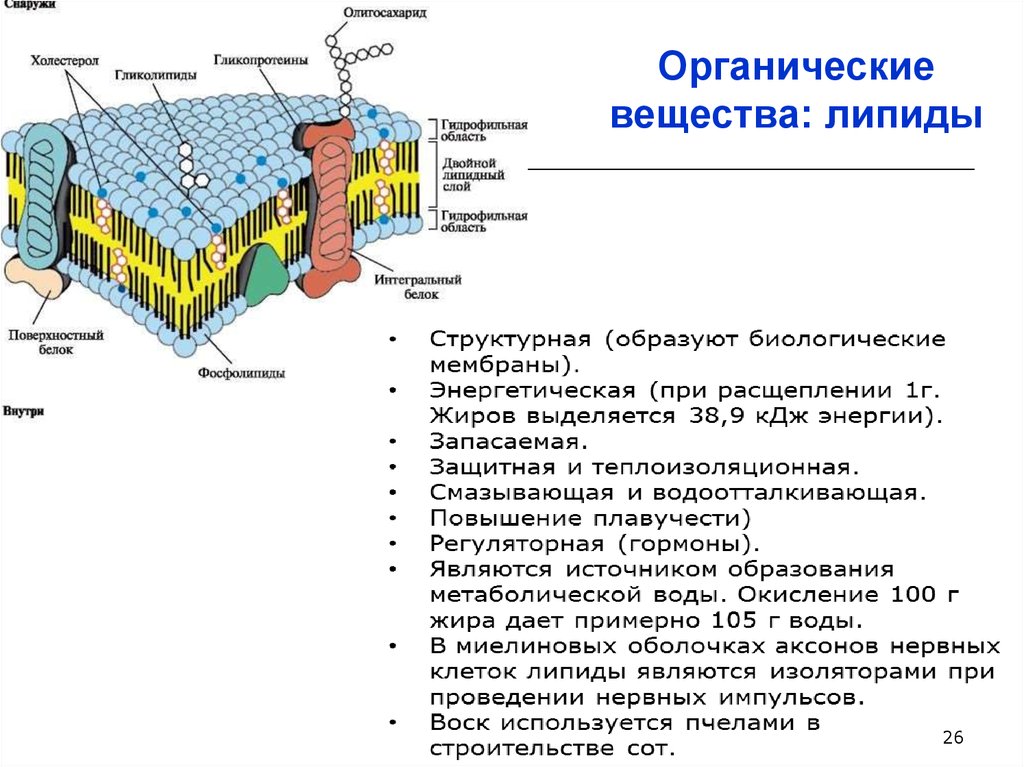
26.
Органическиевещества: липиды
26
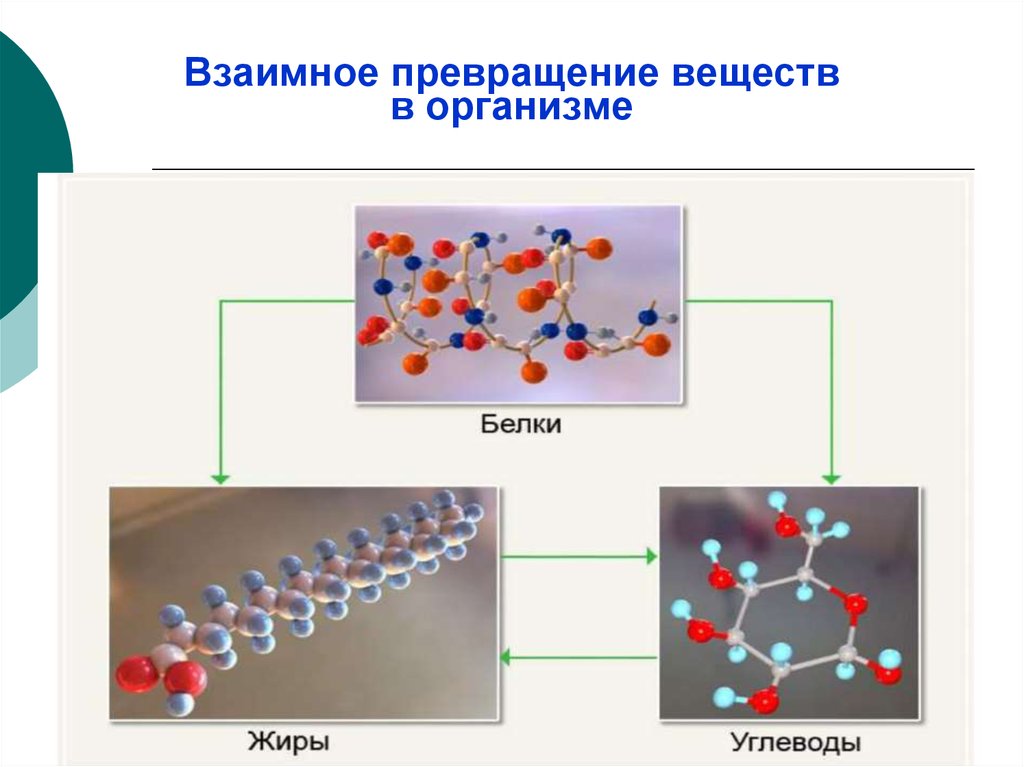
27. Взаимное превращение веществ в организме
28. В природе встречаются 2 вида нуклеиновых кислот: ДНК и РНК
Органические вещества:Нуклеиновые кислоты
В природе встречаются 2 вида нуклеиновых кислот: ДНК и РНК
В прокариотических и эукариотических организмах генетические
функции выполняют оба типа нуклеиновых кислот.
Вирусы всегда содержат:
РНК
или
ДНК
29.
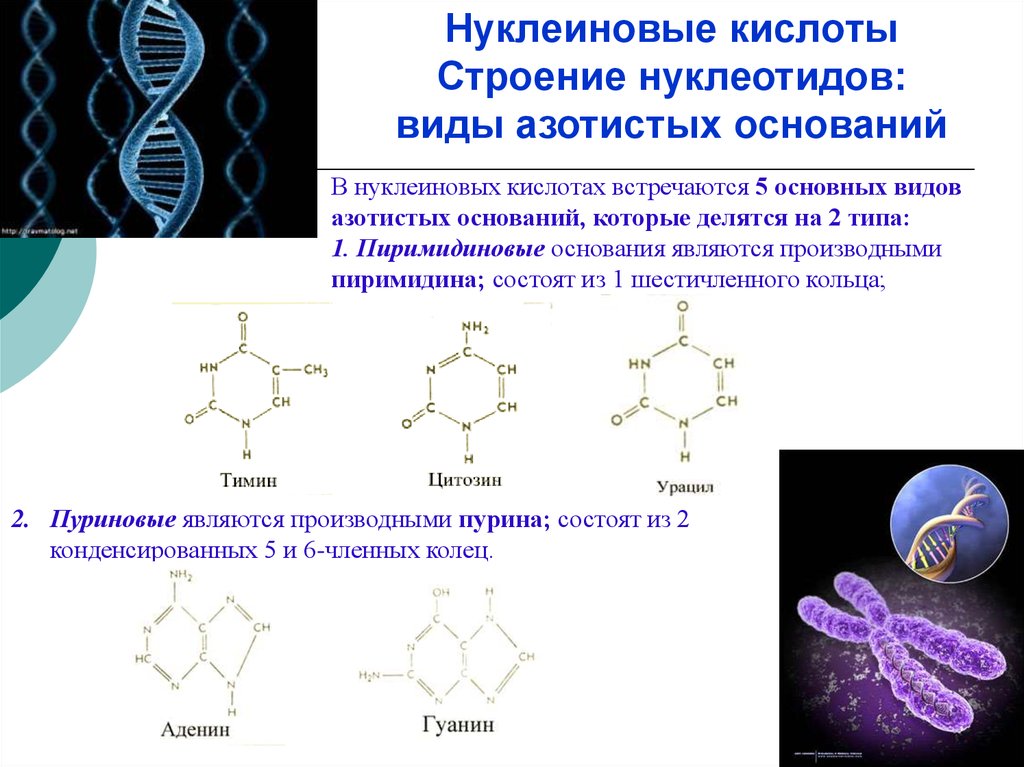
Нуклеиновые кислотыСтроение нуклеотидов:
виды азотистых оснований
В нуклеиновых кислотах встречаются 5 основных видов
азотистых оснований, которые делятся на 2 типа:
1. Пиримидиновые основания являются производными
пиримидина; состоят из 1 шестичленного кольца;
2. Пуриновые являются производными пурина; состоят из 2
конденсированных 5 и 6-членных колец.
29
30. ДНК – это полимерная молекула состоящая из 2х комплиментарных полинуклеотидных цепей соединенными водородными связями, имеют большие раз
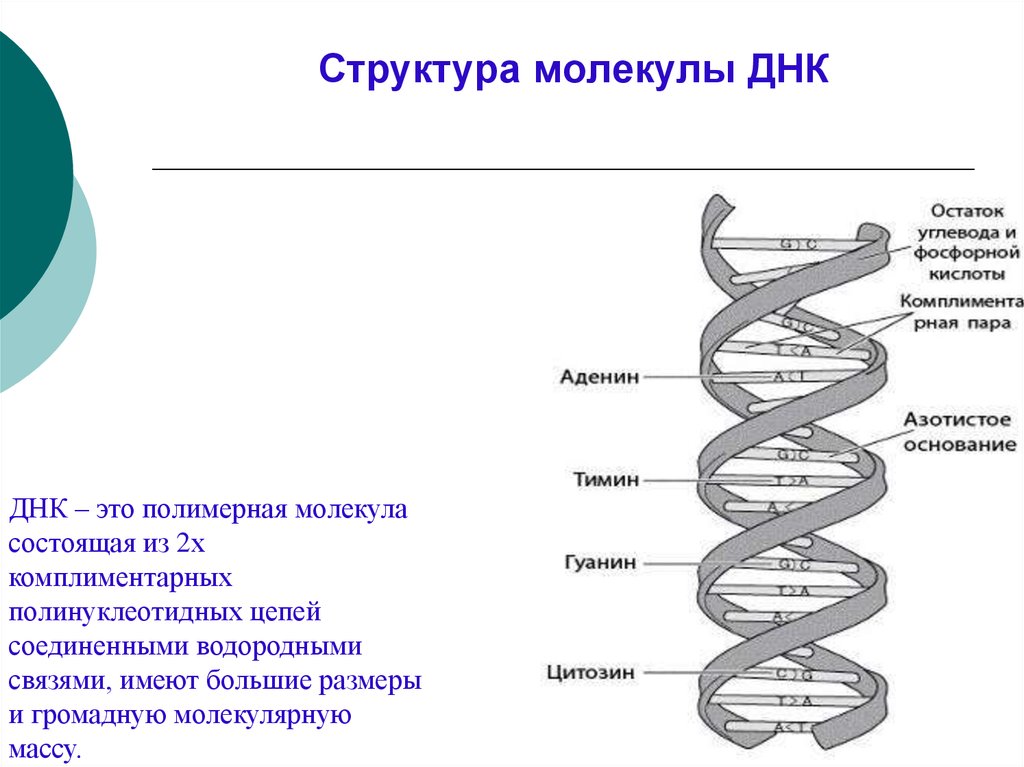
Структура молекулы ДНКДНК – это полимерная молекула
состоящая из 2х
комплиментарных
полинуклеотидных цепей
соединенными водородными
связями, имеют большие размеры
и громадную молекулярную
массу.
31. Первичную структуру ДНК составляет последовательность нуклеотидов в полинуклеотидной цепи. Молекула ДНК состоит из 4 видов нуклеотидов.
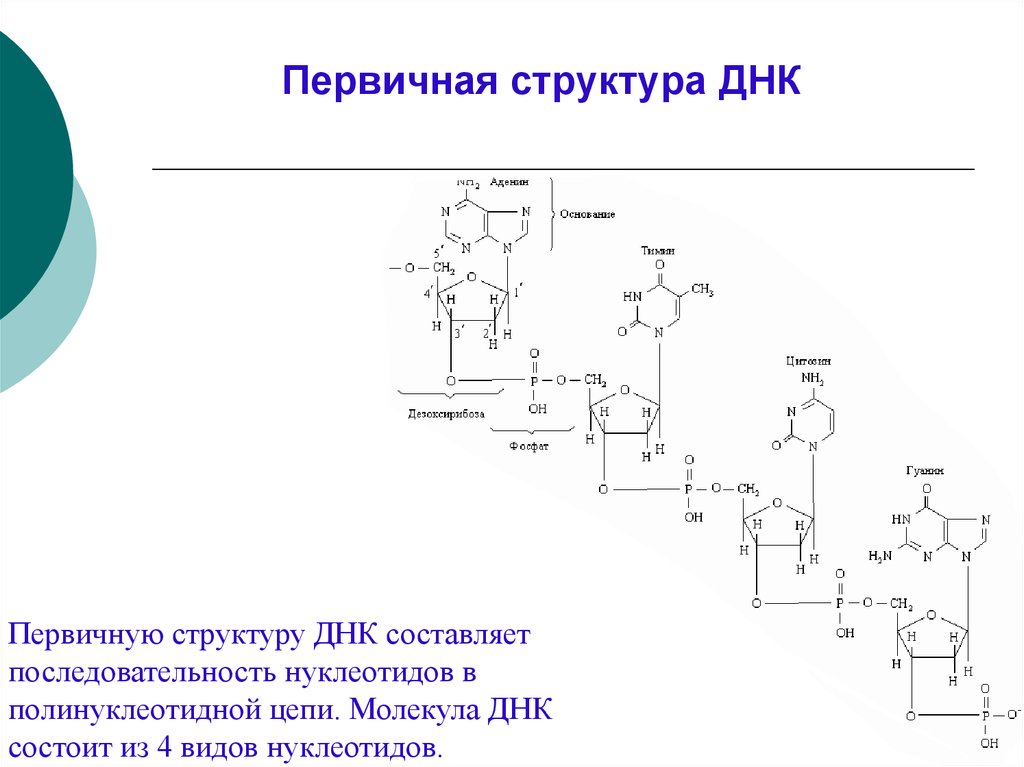
Первичная структура ДНКПервичную структуру ДНК составляет
последовательность нуклеотидов в
полинуклеотидной цепи. Молекула ДНК
состоит из 4 видов нуклеотидов.
32. Больших успехов в определении структуры ДНК достигли Эрвин Чаргафф и его сотрудники (1950г.) Используя метод хроматографии они впервые опред
Правила ЧаргаффаБольших успехов в определении структуры ДНК
достигли Эрвин Чаргафф и его сотрудники
(1950г.) Используя метод хроматографии они
впервые определили нуклеотидный состав ДНК.
Они установили, что соотношение азотистых
оснований ДНК подчиняется универсальным
законам.
1. Сумма пуриновых нуклеотидов
= сумме пиримидиновых нуклеотидов.
2. Молярное содержание аденинов = молярному содержанию тиминов и
их отношение =1.
3. Количество аденина = количеству цитозина, а количество гуанина =
количеству тимина, сумма аденина и цитозина = сумме гуанина и тимина.
33. Вторичная структура ДНК
В 1953г. Уотс и Крик установили, что ДНК представляет собойдвойную спираль, состоящую из 2-х антипаралельных
полинукислотных цепей.
Расстояние между азотистыми основаниями = 0,34 нм
34. Пуриновые и перемидиновые основания направлены внутрь двойной спирали и образуют пары А=Т, Г=Ц.
Вторичная структура ДНКПуриновые и перемидиновые
основания направлены внутрь
двойной спирали и образуют
пары А=Т, Г=Ц.
Малая
бороздка
Большая
бороздка
Виток
35. Это супер спираль или кольцо более высокого порядка; представляет собой дальнейшую спирализацию и суперспирализацию молекулы ДНК.
Третичная структура ДНКЭто супер спираль или кольцо более
высокого порядка; представляет собой
дальнейшую спирализацию и
суперспирализацию молекулы ДНК.
Хромосомы эукариот представляют собой
линейную молекулу ДНК.
Эукариотическая ДНК обматывает
белковые частицы- гистоны,
располагающиеся вдоль ДНК.
36. Комплексы участков ДНК и гистонов называются нуклеосомами.
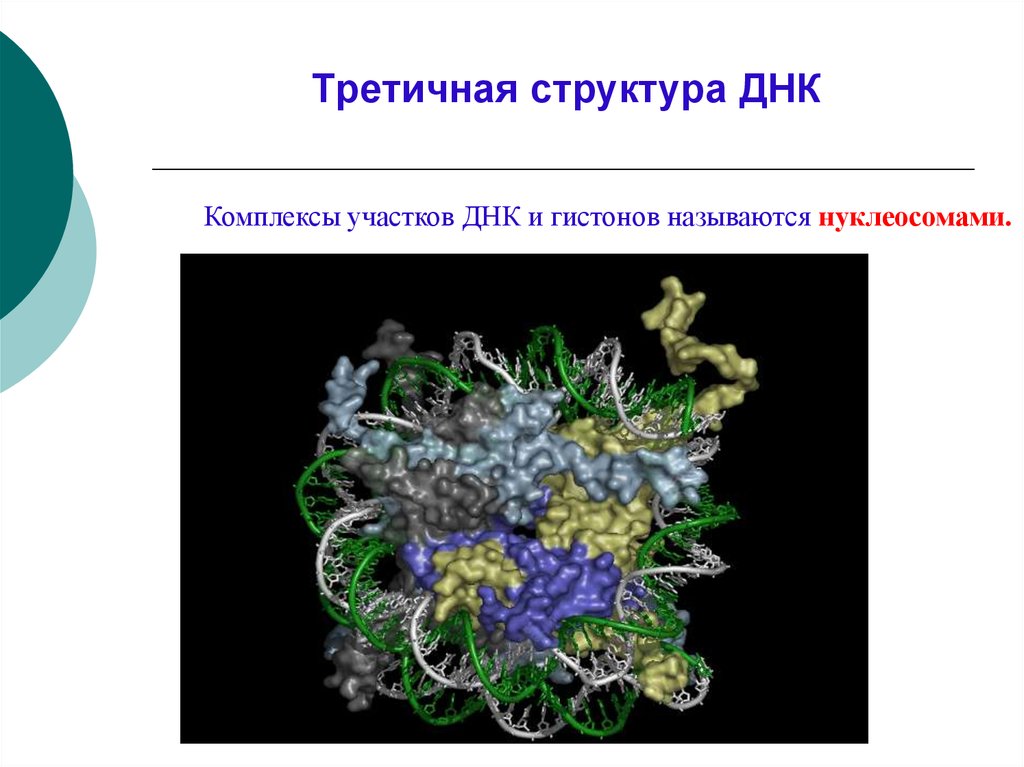
Третичная структура ДНККомплексы участков ДНК и гистонов называются нуклеосомами.
37.
Органические вещества: Малые органическиемолекулы: АТФ
37

















 Биология
Биология








