Похожие презентации:
Важнейшие классы неорганических соединений
1.
ВАЖНЕЙШИЕ КЛАССЫНЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
2.
КИСЛОТЫ– ЭТО СЛОЖНЫЕВЕЩЕСТВА, молекулы
которых состоят из
3
атомов водорода,
Кислотный
остаток
способных замещаться
на
атомы металла, и
кислотных остатков.
Na
Н NО
3.
КЛАССИФИКАЦИЯ КИСЛОТ1. По содержанию кислорода
кислоты
4.
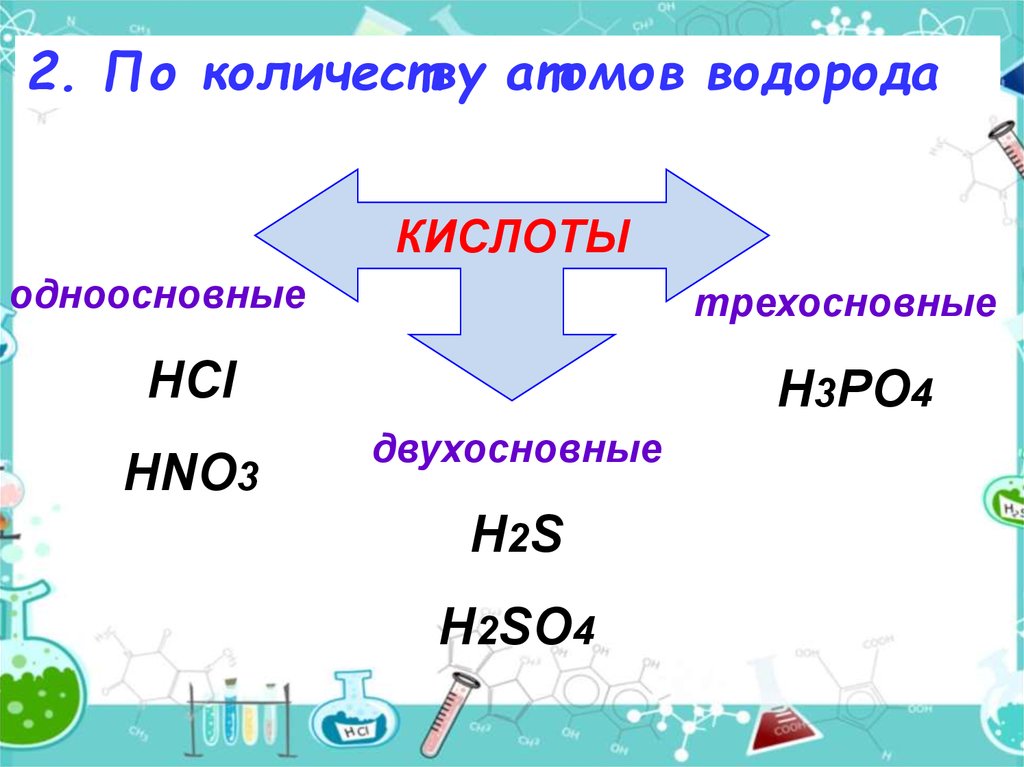
2. По количеству атомов водородаКИСЛОТЫ
одноосновные
трехосновные
HCl
HNO3
H3PO4
двухосновные
H2S
H2SO4
5. Химические свойства кислот
1. Действие на индикаторы2. Взаимодействие с основаниями
2NaOH + H2SO4 → Na2SO4 + 2H2O
основание + кислота
=
соль
+
вода
2Na++2OH-+2H++SO42-→2Na++SO42- + 2H2O
2H+ + 2OH- →2H2O
Реакция нейтрализации, реакция обмена
6. Химические свойства кислот
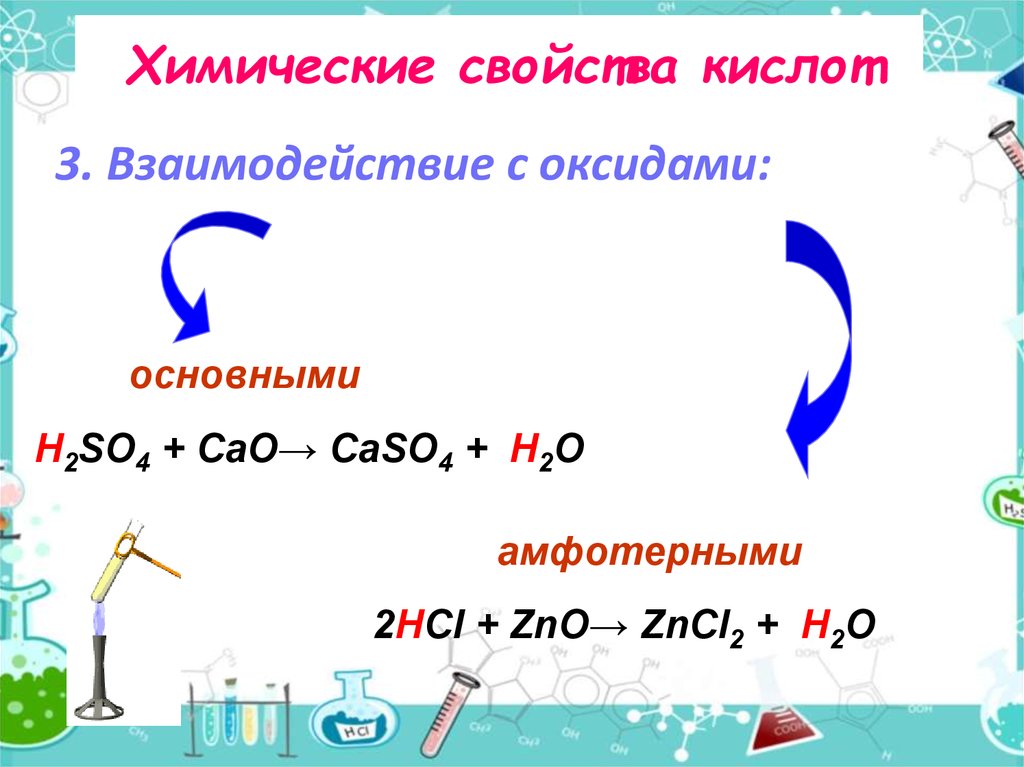
3. Взаимодействие с оксидами:основными
H2SO4 + CаO→ CаSO4 + H2O
амфотерными
2HCl + ZnO→ ZnCl2 + H2O
7. Химические свойства кислот
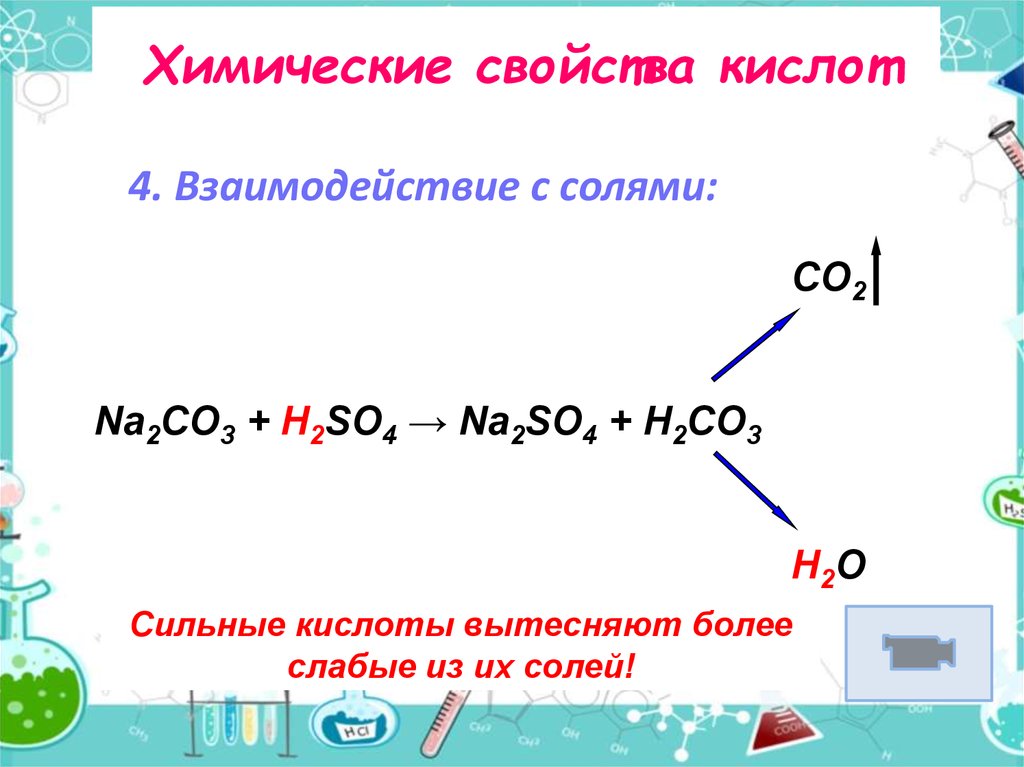
4. Взаимодействие с солями:CO2
Na2CO3 + H2SO4 → Na2SO4 + H2CO3
H2O
Сильные кислоты вытесняют более
слабые из их солей!
8. Химические свойства кислот
5. Взаимодействие с металлами:Zn + 2HCl → ZnCl2 + H2
Cu + HCl →
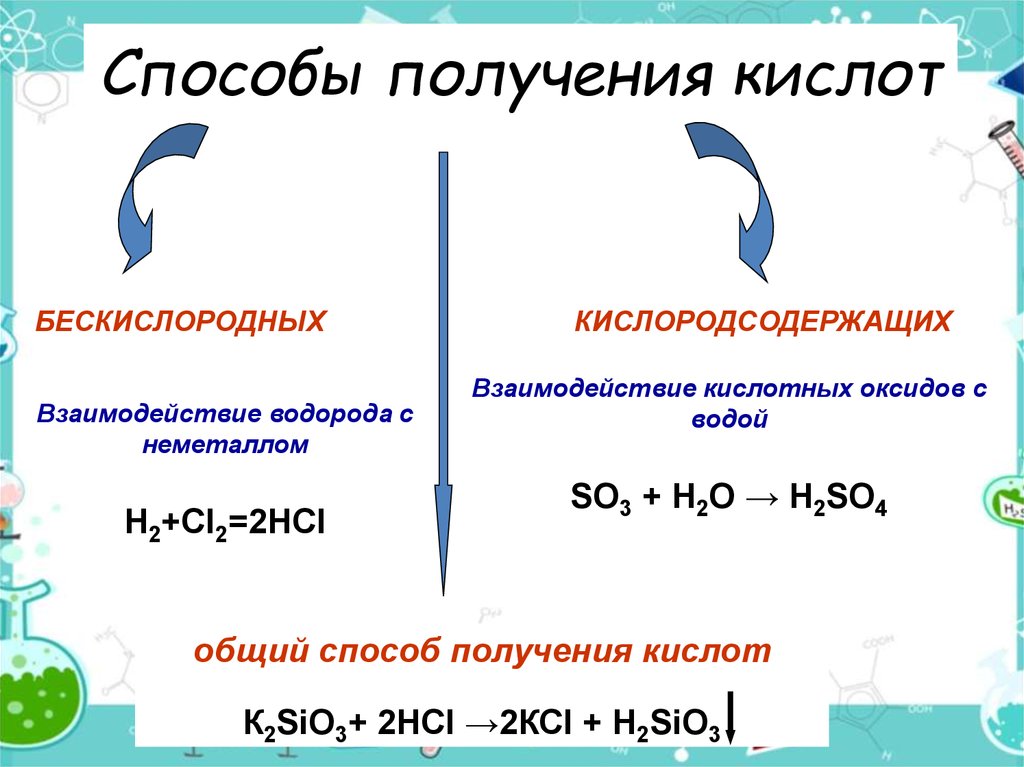
9. Способы получения кислот
БЕСКИСЛОРОДНЫХВзаимодействие водорода с
неметаллом
Н2+Сl2=2НСl
КИСЛОРОДСОДЕРЖАЩИХ
Взаимодействие кислотных оксидов с
водой
SO3 + H2O → H2SO4
общий способ получения кислот
К2SiO3+ 2НСl →2КСl + Н2SiO3
10. КИСЛОТЫ СОДЕРЖАТСЯ В ЖИВЫХ ОРГАНИЗМАХ
Молочная кислот аобразует ся в мышцах при
физической нагрузке
Соляная кислот а,
находящаяся в желудке,
помогает перевариват ь
пищу
11. КИСЛОТЫ ПРИМЕНЯЮТСЯ В МЕДИЦИНЕ
Аскорбиновая,фолиевая,
липоевая,
ацетилсалициловая
и другие
12. КИСЛОТЫ ПРИМЕНЯЮТСЯ В КУЛИНАРИИ
Уксусная кислот аЛимонная кислот а








 Химия
Химия








