Похожие презентации:
Феноло-альдегидные олигомеры и пластмассы на их основе
1. СИНТЕЗ РЕАКЦИОННОСПОСОБНЫХ ОЛИГОМЕРОВ И ПОЛИМЕРОВ НА ИХ ОСНОВЕ
ЛЕКЦИЯ № 4.22. План лекции
1. ФЕНОЛО-АЛЬДЕГИДНЫЕ ОЛИГОМЕРЫ ИПЛАСТМАССЫ НА ИХ ОСНОВЕ
МОНОМЕРЫ
ПОЛУЧЕНИЕ
КЛАССИФИКАЦИЯ
СВОЙСТВА
ПРИМЕНЕНИЕ
3. 1907 году Лео Хендрик Бакеланд изобрел фенолоформальдегидную смолу
первый синтетический реактопласт,легко формуется, легкий, прочный,
выдерживает нагревание,
обладает хорошими электроизолирующими свойствами,
недорого стоит,
7 декабря 1909 года может быть изготовлен из имеющегося на тот момент
U.S. Patent 0,942,809 сырья
General Bakelite Corp.
1910 год
Бакелит
открыл «эру пластмасс»
Материал
тысячи применений
Прогноз развития рынка ФФС
в Европе 2007-2015 гг.
4.
ФЕНОЛО-АЛЬДЕГИДНЫЕ ОЛИГОМЕРЫИ ПЛАСТМАССЫ НА ИХ ОСНОВЕ
Интерес и высокое техническое значение
определяются:
• низкой стоимостью исходного сырья и
его доступностью,
• простотой и высокой производительностью
технологических процессов получения и переработки
феноло-альдегидных олигомеров
• широтой ассортимента и
хорошими потребительскими качествами материалов
на их основе
5.
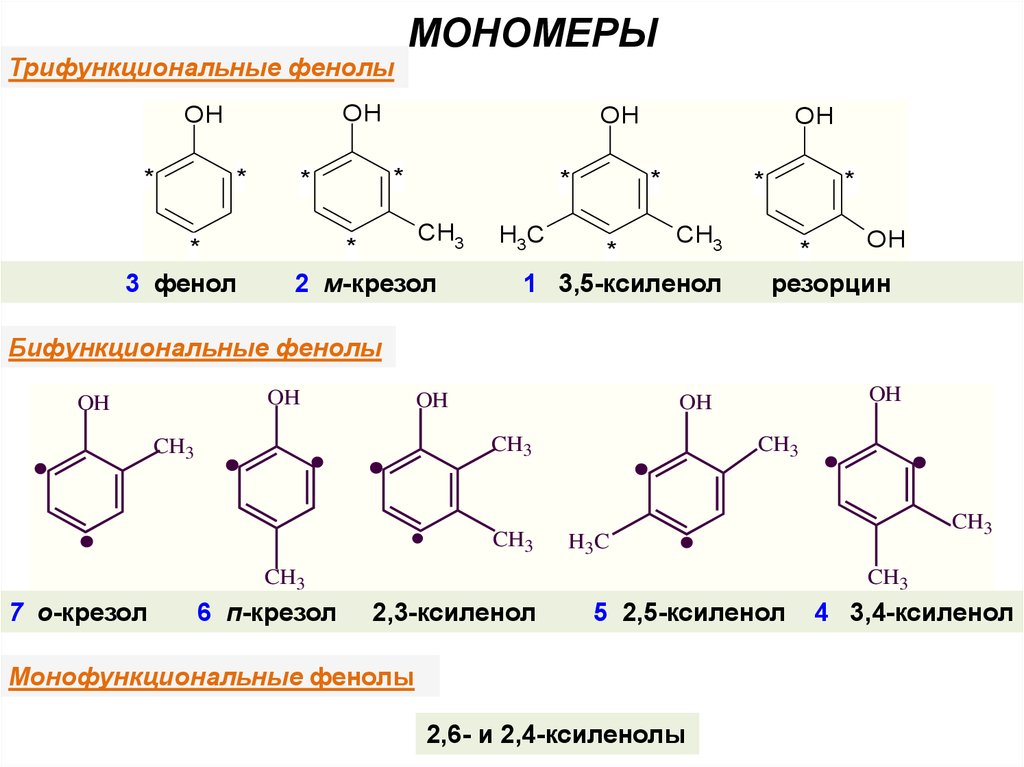
Трифункциональные фенолыOH
OH
*
*
МОНОМЕРЫ
*
*
*
CH3
*
*
3 фенол
OH
2 м-крезол
H3C
OH
*
*
*
*
CH3
1 3,5-ксиленол
*
OH
резорцин
Бифункциональные фенолы
OH
OH
OH
CH3
CH3
OH
OH
CH3
CH3
H3C
CH3
7 о-крезол
6 п-крезол
CH3
CH3
2,3-ксиленол
5 2,5-ксиленол
Монофункциональные фенолы
2,6- и 2,4-ксиленолы
4 3,4-ксиленол
6.
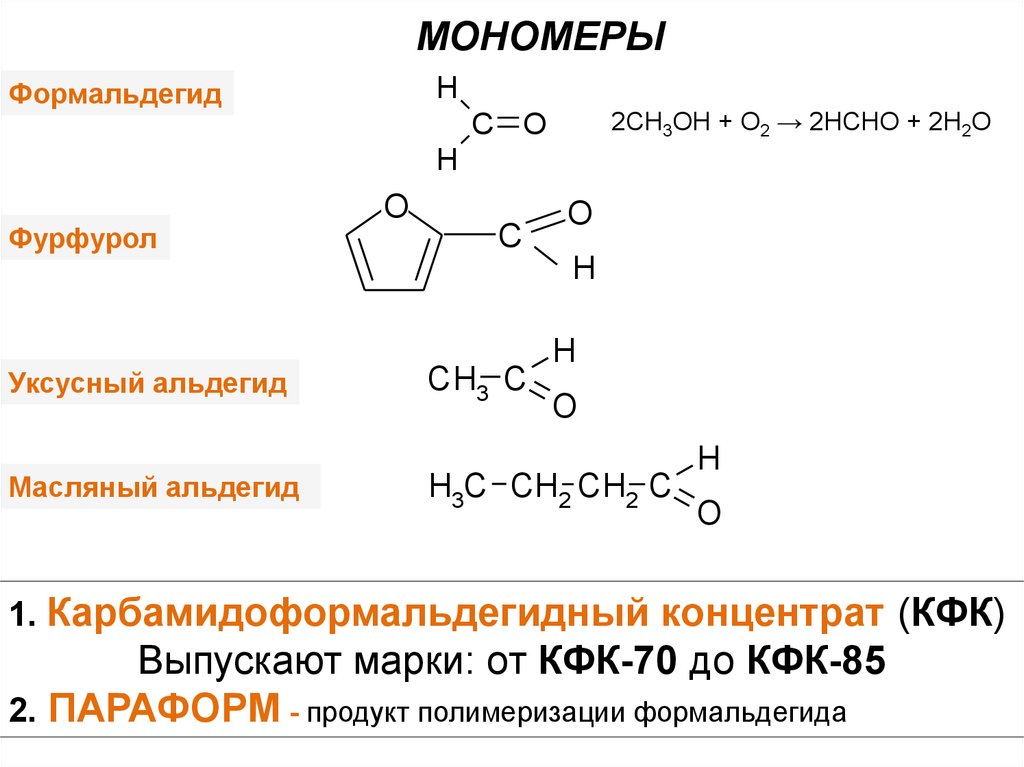
МОНОМЕРЫH
Формальдегид
2CH3OH + O2 → 2HCHO + 2H2O
C O
H
Фурфурол
O
C
O
H
Уксусный альдегид
Масляный альдегид
CH3 C
H
O
H3C CH2 CH2 C
H
O
1. Карбамидоформальдегидный концентрат (КФК)
Выпускают марки: от КФК-70 до КФК-85
2. ПАРАФОРМ - продукт полимеризации формальдегида
7.
ПОЛУЧЕНИЕреакции образования феноло-формальдегидных смол:
присоединение
конденсация
OH
OH
OH
CH2OH
+ CH2O
+ C6H5OH
OH
OH
OH
CH2
CH2
CH2OH
+ CH2O
+ CH2O
+ C6H5OH
OH
CH2OH
HOH2C
+ CH2O
реакции практически необратимы
(константы равновесия порядка 104)
реакции реализуются при участии
активных
атомов
водорода
фенольного ядра
OH
CH2OH
HOH2C
+ C6H5OH
HOH2C
тепловой эффект соединения
фенольных
ядер
метиленовыми
мостиками – 88 кДж/моль
8. факторы, определяющие механизм реакций, структуру и свойства фенолоформальдегидных олигомеров
ПОЛУЧЕНИЕфакторы, определяющие механизм реакций, структуру и свойства
фенолоформальдегидных олигомеров
Реакционная способность реагентов (функциональность
мономерных молекул)
Молярное соотношение Фенол : Формальдегид
Природа катализатора
основные катализаторы: NaOH, Ba(OH)2, NH4OH, Na2CO3
кислотные катализаторы: HCl, H2SO4, H2C2O4
pH среды
Концентрация катализатора
Температура реакции
Продолжительность реакции
9.
ПОЛУЧЕНИЕ1. в
OH
кислотной среде :
CH2OH
происходит протонизация молекулы формальдегида с образованием
нестойкого карбониевого иона, который атакует фенольное кольцо с
образованием фенолоспирта (метилольного производного)
OH
2. фенолоспирты превращаются
реагируют с другим
фенольным кольцом по
реакции электрофильного
замещения
4. в
+
CH2OH
в бензилкарбониевый ион
в присутствии H+
3. этот ион быстро
OH
C H2
+
OH
OH
+
+ H2O
H
OH
OH
+
C H2
CH2
+
+H
щелочной среде:
образуются хиноидные
структуры (нуклеофилы),
которые легко реагируют с
формальдегидом (электрофил)
с образованием различных по
строению анионов, что приводит
к получению смеси
фенолоспиртов
OH
O
O
O
C
C
+
10.
КЛАССИФИКАЦИЯ ОЛИГОМЕРОВ И ПОЛИМЕРОВOH
новолак
(новолачные олигомеры)
СКОРОСТЬ
присоединение << конденсация
H
OH
CH2
n=4-8
n
А) Если взаимодействие фенола с формальдегидом проводить в
присутствии кислотных катализаторов при избытке фенола (например,
Ф:ФА= 1:0,78÷0,86 моль),
Б) либо при большом избытке формальдегида (Ф:ФА=1:2÷2,5 моль) в
присутствии сильных кислот
Катализатор вводят в количестве 0,2-2,0% от массы фенола
Т=98-100 oC
Атмосферное давление
11. Изомерные положения метиленовых мостиков в новолаках
OHOH
10-25 %
CH2
OH
CH2OH
C6H5OH
OH
50-60 %
OH
CH2OH
CH2
OH
OH
C6H5OH
CH2OH
25-30 %
HO
CH2
OH
12.
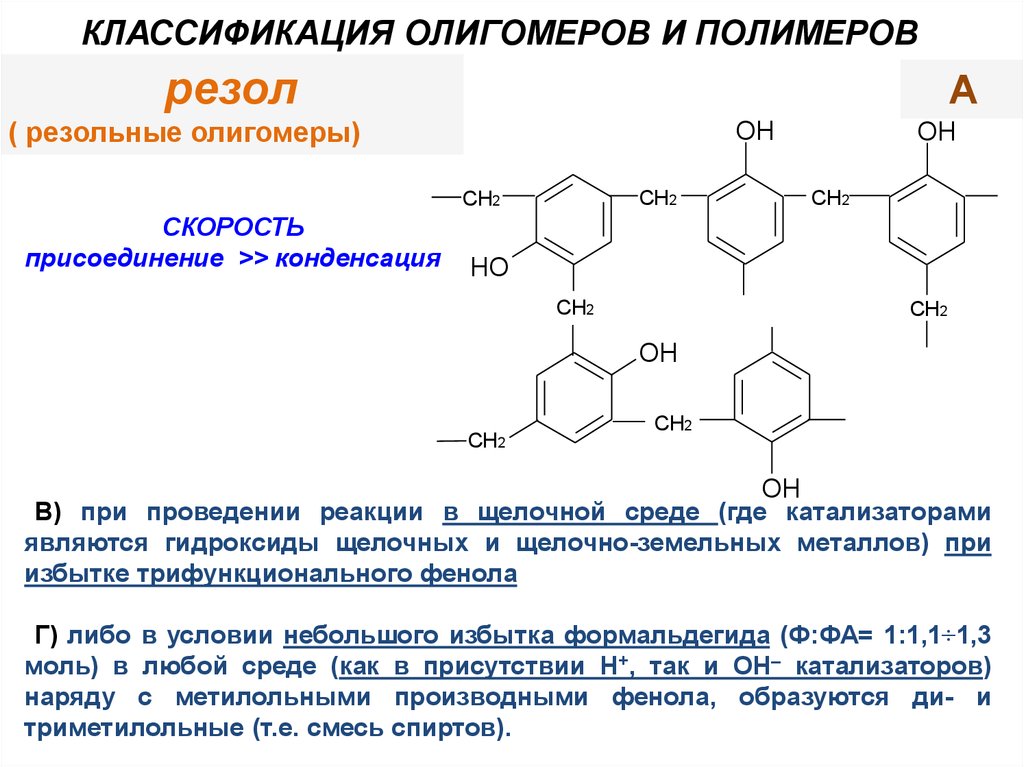
КЛАССИФИКАЦИЯ ОЛИГОМЕРОВ И ПОЛИМЕРОВрезол
А
( резольные олигомеры)
OH
CH2
CH2
СКОРОСТЬ
присоединение >> конденсация
OH
CH2
HO
CH2
CH2
OH
CH2
CH2
OH
В) при проведении реакции в щелочной среде (где катализаторами
являются гидроксиды щелочных и щелочно-земельных металлов) при
избытке трифункционального фенола
Г) либо в условии небольшого избытка формальдегида (Ф:ФА= 1:1,1÷1,3
моль) в любой среде (как в присутствии H+, так и OH– катализаторов)
наряду с метилольными производными фенола, образуются ди- и
триметилольные (т.е. смесь спиртов).
13.
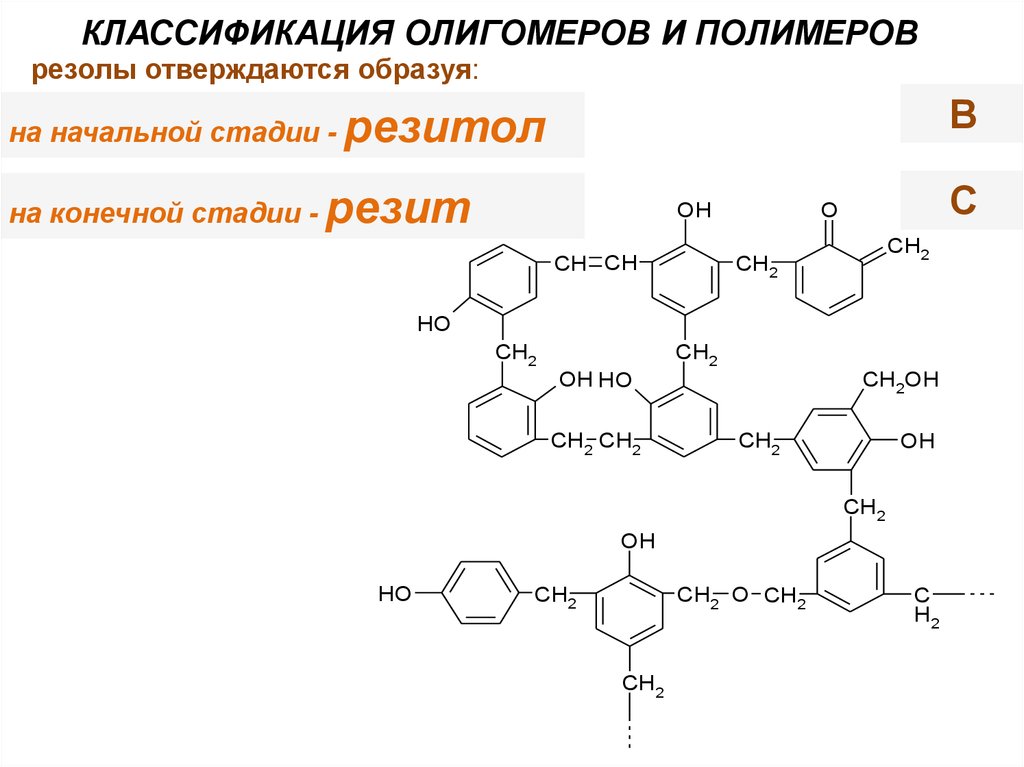
КЛАССИФИКАЦИЯ ОЛИГОМЕРОВ И ПОЛИМЕРОВрезолы отверждаются образуя:
В
на начальной стадии - резитол
на конечной стадии - резит
OH
CH CH
С
O
CH2
CH2
HO
CH2
CH2
CH2OH
OH HO
CH2 CH2
CH2
OH
CH2
OH
HO
CH2
CH2 O CH2
CH2
C
H2
14. новолачных олигомеров
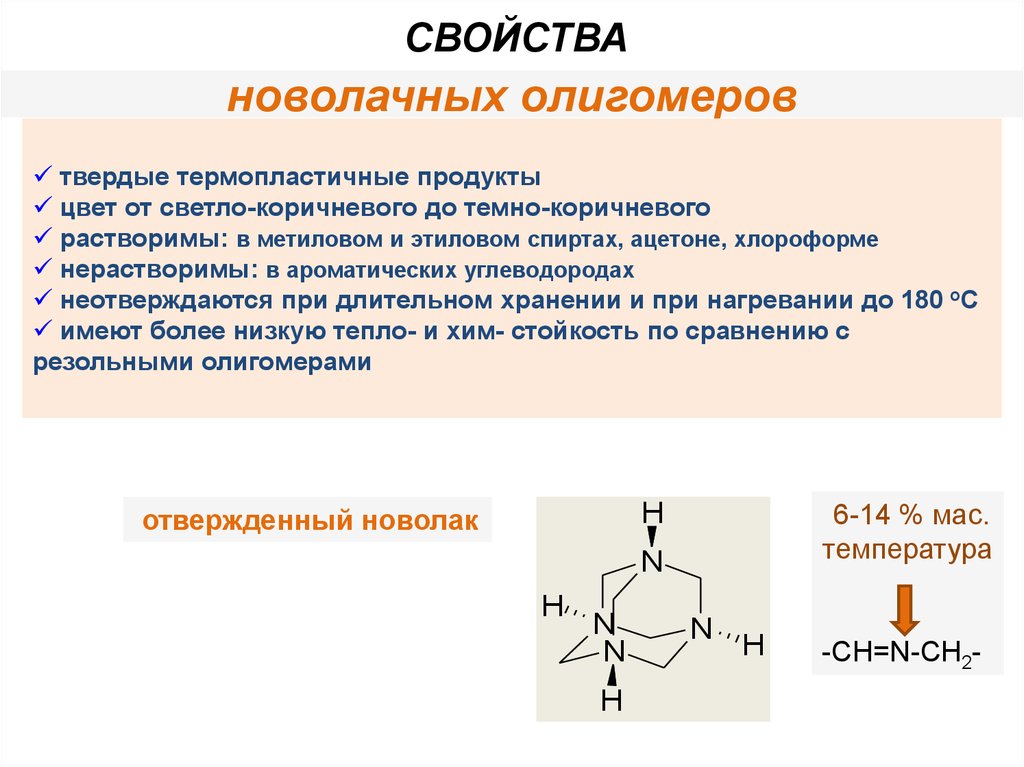
СВОЙСТВАноволачных олигомеров
твердые термопластичные продукты
цвет от светло-коричневого до темно-коричневого
растворимы: в метиловом и этиловом спиртах, ацетоне, хлороформе
нерастворимы: в ароматических углеводородах
неотверждаются при длительном хранении и при нагревании до 180 oC
имеют более низкую тепло- и хим- стойкость по сравнению с
резольными олигомерами
6-14 % мас.
температура
H
отвержденный новолак
N
H
N
N
H
N
H
-СН=N-СН2-
15.
СВОЙСТВАрезольных олигомеров
твердые или жидкие термореактивные продукты
цвет зависит от используемого катализатора
растворимы: в этиловом спирте, ацетоне, хлороформе
нерастворимы: в ароматических углеводородах
отверждаются при хранении даже при комнатной температуре
содержат большое количество свободного фенола, который снижает их
температуру плавления (по сравнению с новолачными олигомерами)
резит
неплавкий, не размягчающийся при нагревании продукт
нерастворимый и не набухающий в растворителях продукт
устойчив до T=250-280 OC
резиты
обладают
высокой
термической
стойкостью,
эксплуатироваться длительное время при температуре ниже 200 oС
могут
16.
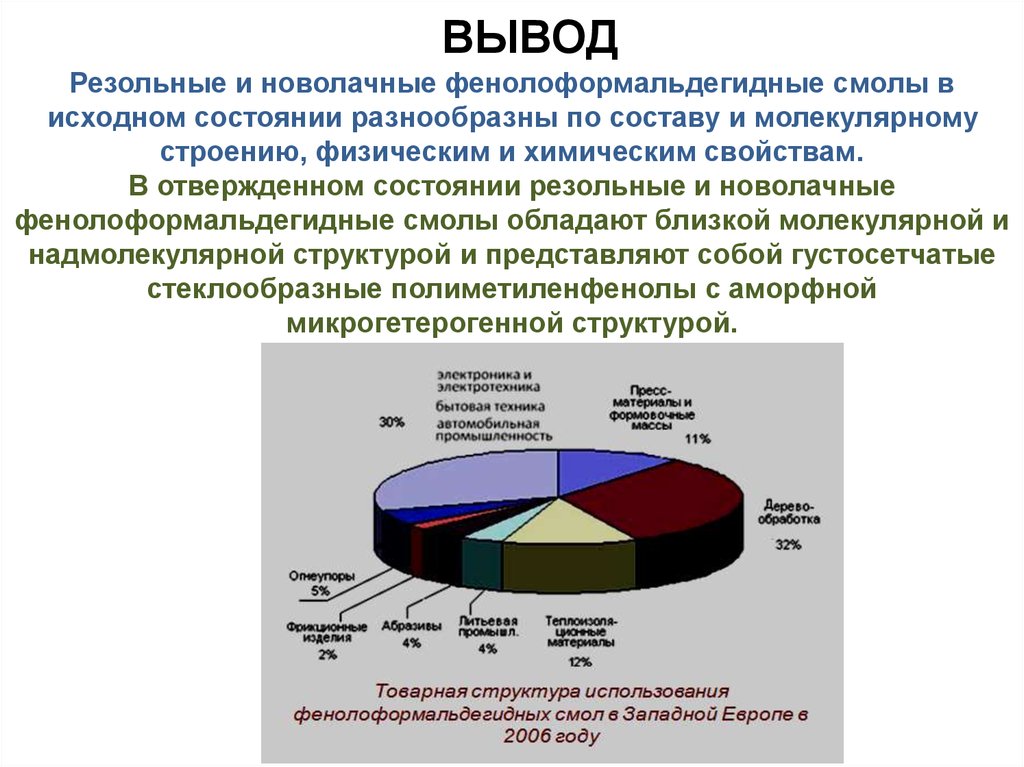
ВЫВОДРезольные и новолачные фенолоформальдегидные смолы в
исходном состоянии разнообразны по составу и молекулярному
строению, физическим и химическим свойствам.
В отвержденном состоянии резольные и новолачные
фенолоформальдегидные смолы обладают близкой молекулярной и
надмолекулярной структурой и представляют собой густосетчатые
стеклообразные полиметиленфенолы с аморфной
микрогетерогенной структурой.
17.
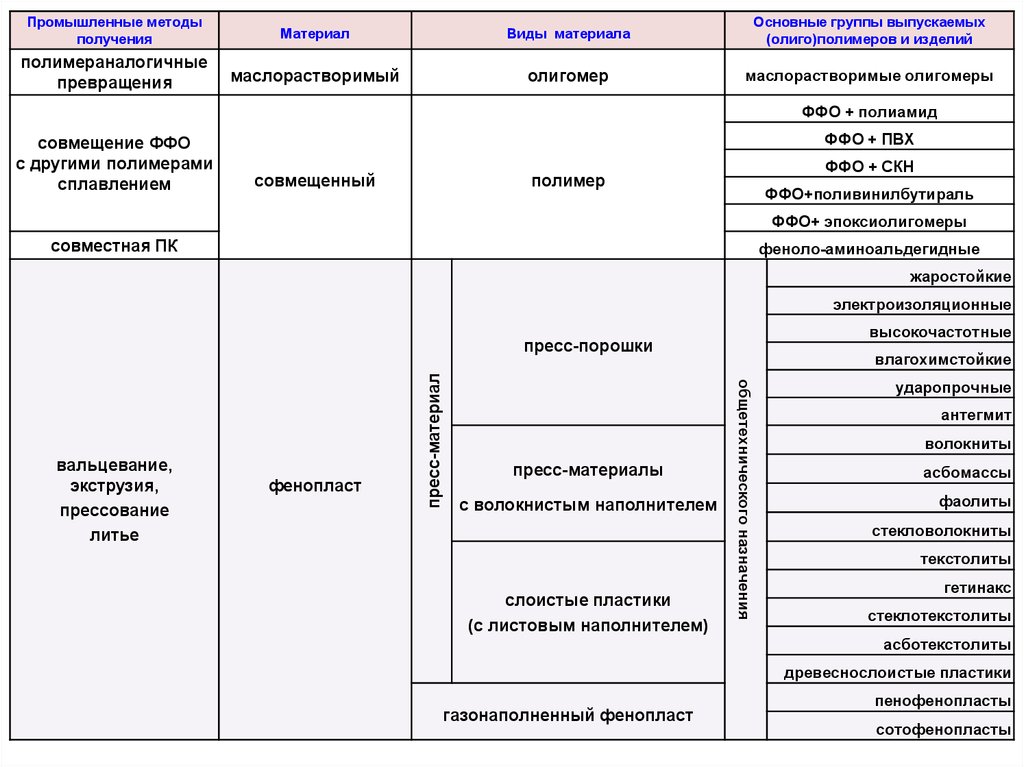
Промышленные методыполучения
Материал
Виды материала
Основные группы выпускаемых
(олиго)полимеров и изделий
полимераналогичные
превращения
маслорастворимый
олигомер
маслорастворимые олигомеры
ФФО + полиамид
совмещение ФФО
с другими полимерами
сплавлением
ФФО + ПВХ
совмещенный
ФФО + СКН
полимер
ФФО+поливинилбутираль
ФФО+ эпоксиолигомеры
совместная ПК
феноло-аминоальдегидные
жаростойкие
электроизоляционные
высокочастотные
фенопласт
пресс-материалы
с волокнистым наполнителем
слоистые пластики
(с листовым наполнителем)
влагохимстойкие
общетехнического назначения
вальцевание,
экструзия,
прессование
литье
пресс-материал
пресс-порошки
ударопрочные
антегмит
волокниты
асбомассы
фаолиты
стекловолокниты
текстолиты
гетинакс
стеклотекстолиты
асботекстолиты
древеснослоистые пластики
газонаполненный фенопласт
пенофенопласты
сотофенопласты
18.
НАПОЛНИТЕЛИ, ПРИМЕНЕНИЕН
А
минеральные вещества:
графит, слюда, асбест
природные материалы:
порошкообразный речной песок
органические вещества:
древесная мука
производство
профильных изделий, ширпотреба,
электротехнических изделий
П
О
Ф
Л
Ф
Н
С
И
Т
бумага
ткани
древесный шпон
производство мебели,
конструкционные и
электроизоляционные материалы
волокнистый
целлюлоза
стеклянное волокно
базальтовое волокно
асбест (длинноволокнистый)
производство
изделий повышенной прочности при
истирании, кручении, статическом
изгибе;
химической аппаратуры;
конструкционных изделий
газ (порофоры)
•твердые вещества + к-та
•низкокипящие
углеводороды
•органические вещества
производство тепло- и
звукоизоляции, заполнитель в
изделиях, подвергающихся вибрации
листовой
Е
Л
Ь











 Химия
Химия








