Похожие презентации:
Рак яичников при эндометриозе
1. Рак яичников при эндометриозе
РАК ЯИЧНИКОВ ПРИ ЭНДОМЕТРИОЗЕ2.
ПЛАН:1.Формулировка проблемы
-Цели и задачи
-гипотеза
2.Методы
-Выборка
-дизайн исследования
3.Результаты
4.Оценка
2
3. Цели и задачи статьи
1.ФОРМУЛИРОВКА ПРОБЛЕМЫЦели и задачи статьи
• Цель: выяснить причину возникновения рака
яичников при эндометриозе
Задачи :
1) Дать оценку молекулярно-гинитическим методам исследования,
при эндометриозе ;
2) Провести статистический анализ на проведенные ранее
клинические исследования, на наличие атипичных клеток при
эндометриозе;
3) Доказать роль оксидативного стресса и воспаления в
канцерогенезе , появившегося от эндометриоза
4) Выяснить значение эндометриоидных кист в канцерогенезе
5) Разработать патогенез трансформации эндометриоза в рак
яичников.
3
4.
1.ФОРМУЛИРОВКА ПРОБЛЕМЫ1) Среди злокачественных новообразований женских
половых органов опухоли яичника занимают третье
место после рака шейки и тела матки, их доля достигает
30% [1].
2) Источник возникновения рака яичек полностью не
изучен, поскольку средой его развития является
железистый эпителий, а в яичнике этот эпителий не
содержится
3) Исследования эндометриоза с позиции образования
рака яичек мало изучены
1)[Ahmed FY, Wilnshaw Е, H'Hern RP et al. Natural history of prognosis of untreated stage I epithelial ovarian carcinoma //J Clin Oncol
14:2968-75, 1996 ]
4
5. Ключевые слова:
1.ФОРМУЛИРОВКА ПРОБЛЕМЫКлючевые слова:
Рак яичников, эндометриоз, патогенез,
оксидативный стресс, микроматричный
анализ
Данные ключевые концепции определены четко и распределены в порядке
их значимости!
(+)Что касается литературы, то ее источники имеют прямое отношение к
данной статье, порядок расположения ссылок на них подобран строго по
плану самой статьи, использованная литература была достаточно новой,
учитывая, что сама статья 2009 года
(-) Там где указываются ссылки на проведенный статистический анализ, была
указана старая литература, а подобранная выборка не достаточна для ответа
на поставленный вопрос.
5
6. Гипотеза
1.ФОРМУЛИРОВКА ПРОБЛЕМЫГипотеза
1.Покровный эпителий яичников и эндометриоз являются
основными площадками развития рака;
2. Эндометриоз является фактором риска образования рака даже
после наступления менопаузы;
3. Роль гиперплазии в канцерогенезе;
4.Среда эндометриоидной кисты больше подвержена мутации, чем
среды других кист
6
7. А) С клинической точки зрения общей популяцией в данном исследований являлись пациенты страдающие эндометриозом
2.МЕТОДЫ [1](ВЫБОРКА)А) С клинической точки зрения общей популяцией в данном
исследований являлись пациенты страдающие эндометриозом
B) Популяция которую выбрали авторы для
исследования в статье вполне отвечает поставленным
перед исследователями задачам.
C) Выборка, предложенная в данном исследовании, достаточна для
ответа на поставленный вопрос? Нет, но она достаточна для
выводов, которые в дальнейшем помогут получить ответ, поскольку
проведенные в дальнейшем гистологические исследования могут
выявить частоту сродства эндометриоза к раку яичников , ключевую
роль здесь играют факторы риска ( возрост, статус постменопаузы,
этнические группы) и количество исследуемых.
7
8. А) Каким образом тестировалась гипотеза?
2.МЕТОДЫ [2](ДИЗАЙН ИССЛЕДОВАНИЯ)А) Каким образом тестировалась гипотеза?
Были проведены :
• Статистические;
• Молекулярно-генетические;
• Биохимические;
• Гистологические исседования.
8
9. Ограничения данного исследования :
2. МЕТОДЫ [2]ДИЗАЙН ИССЛЕДОВАНИЯОграничения данного исследования :
• Мало изученный механизм канцерогенеза при
эндометриозе;
• Все проведенные молекулярно-генетические
исследования не являются абсолютно специфичными
к раку яичников или по крайней мере к конкретному
из подтипов (светлоклеточный, эндометриозный)
рака
9
10. статистический анализ
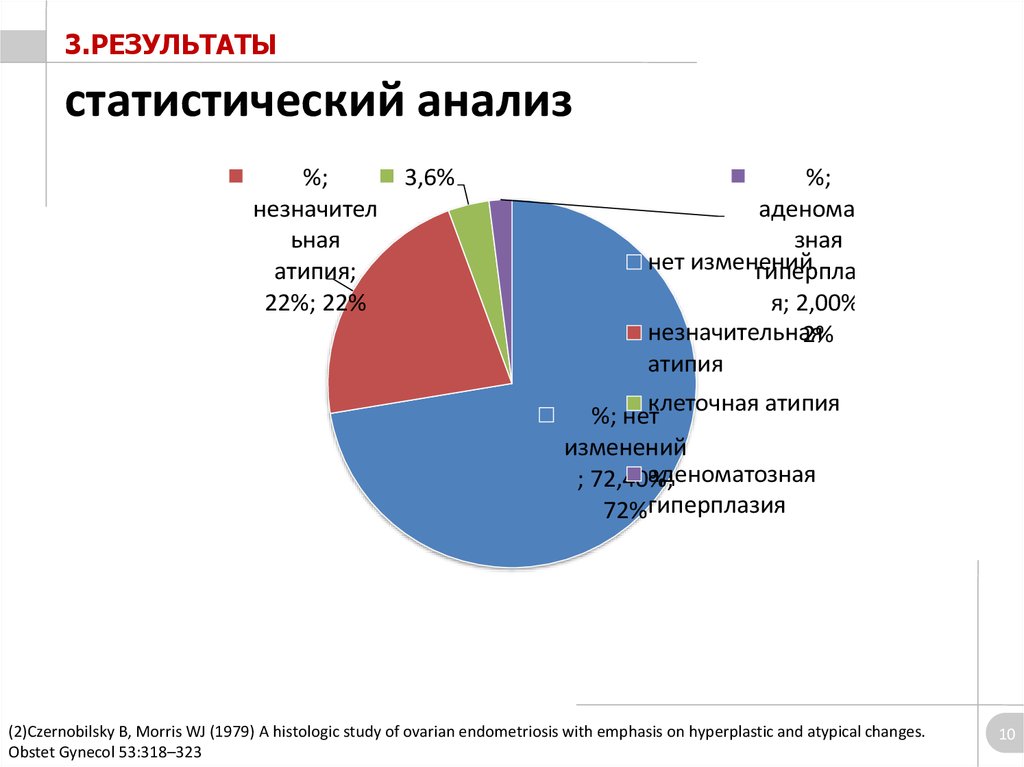
3.РЕЗУЛЬТАТЫстатистический анализ
%;
незначител
ьная
атипия;
22%; 22%
3,6%
%;
аденомато
зная
нет изменений
гиперплази
я; 2,00%;
незначительная
2%
атипия
клеточная атипия
%; нет
изменений
аденоматозная
; 72,40%;
72%гиперплазия
(2)Czernobilsky B, Morris WJ (1979) A histologic study of ovarian endometriosis with emphasis on hyperplastic and atypical changes.
Obstet Gynecol 53:318–323
10
11. Молекулярно-генетический анализ
3.РЕЗУЛЬТАТЫМолекулярно-генетический анализ
P-53 (антионкоген,
подовляющий опухоль)
Накопление p-53,
обнаружены в 17%
в доброкачественных
эндометриоидных
поражений приводящих к
карциноме , тогда как
аномальная коррозия
не была найдена при
эндометриозе без рака.
Частота мутаций p-53 при
раке составляет 40-50%
можно наблюдать при
серозной карциноме
яичника
LOH и генетическая
нестабильность
Сопровождается
генетической абберацией
которые могут внести свой
вклад в развитие самого
эндометриоза, тем не менее
некоторые генетические
события общие у
эндометриоза и рака
связанные со
злокачественной
трансформацией в связи с их
высокой
распроспространенностью в
последней. В 40%
наблюдается LOH в 10q
наблюдается при атипичном
эндометриозе
PTEN и К-ras(онкогены
расположенные на покровном
эпителии яичника, уомбинация
которых приводит к карциноме)
PTEN мутирует в 20%
эндометриоидный и 8%
мветлоклеточной карциноме.
Также PTEN в 15% случаев
(особенно в запущенных),
приводит к злокачественным
преобразованиям. Мутации К-ras
обнаружены в 1/12 (8,3%) в
эндометриоидной и 3/24 (12,5%)
в светлоклеточной карциноме
сопровождающейся
эндометриозом. Несмотря на это,
k-ras не был найден в
доброкачественном
эндометриозе , сопутствующим с
карциномой.
HNF-1B (гепатоцито-ядерный
фактор, являющийся
маркером светлоклеточной
карциномы)
HNF-1В был активен в
светлоклеточных карциномах,
(но не в других случаях) в 9 из
12 случаев светлоклеточных
карцином с эндометриозом.
Эндометриальный эпителий
был выстелан этим фактором.
В сопровождении с mRNA
стимулирует апоптоз .
Эффект эстрогена
В 31 случае рака яичника с эндометриозом как эндогенный так иэкзогенный гиперэстрогенизм являлся
значительным фактором риска. В некоторых случаях стимуляция эстрогена может быть связана со
злокачественным преобразованием эндометриоза, даже после абдоменальной гистерэктомии и
двухсторонней овариоэктомии. Злокачественные преобразования эндометриоза происходит под влиянием
эндогенных эстрогенов от опухоли яичников или экзогенного тамоксифена. Эстроген ассоциируется с
повышением риска рака яичников опровождающемся эндометриозом
11
12. Гистологические исследования
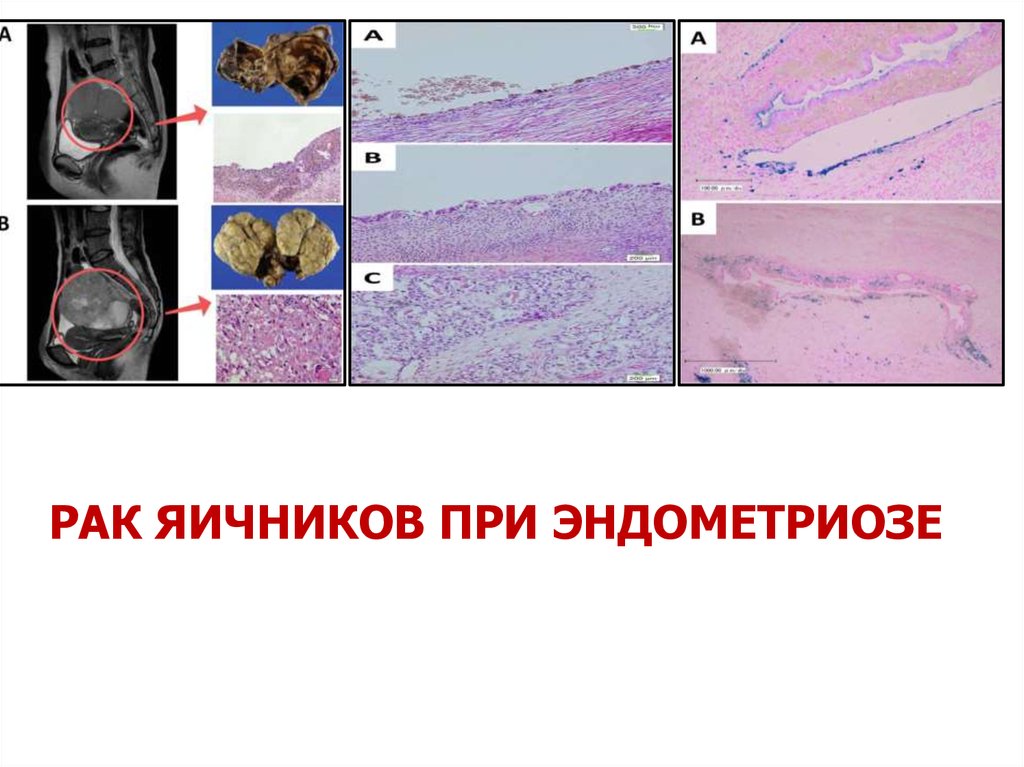
3.РЕЗУЛЬТАТЫГистологические исследования
Были собраны случаи злокачественных опухолей в яичном и вне
яичном эндометриозе. Среди 63% злокачественных образования в
яичном эндометриозе были светлые клетки или эндометриоидные
клетки. Из них 30% серозные пограничные линии. 52% раков из
эндометриозных кист были светлыми или эндометриоидными
клетками, а 20% были серозными карциномами.
Выводы: во 1ых эндометриоз со своей неопластической натурой,
существенно демонстрирует потенциал роста злокачественных
опухолей различных фенотипов
2) Среди раковых преобразований по неизвестным причинам светлые
клетки и эндометриоидные аденокарциномы доминируют
3) Гистологические процессы различаются между овариальными и вне
овариальными эндометриозами.
(3) Ссылка на источники
12
13. Биохимические исследования
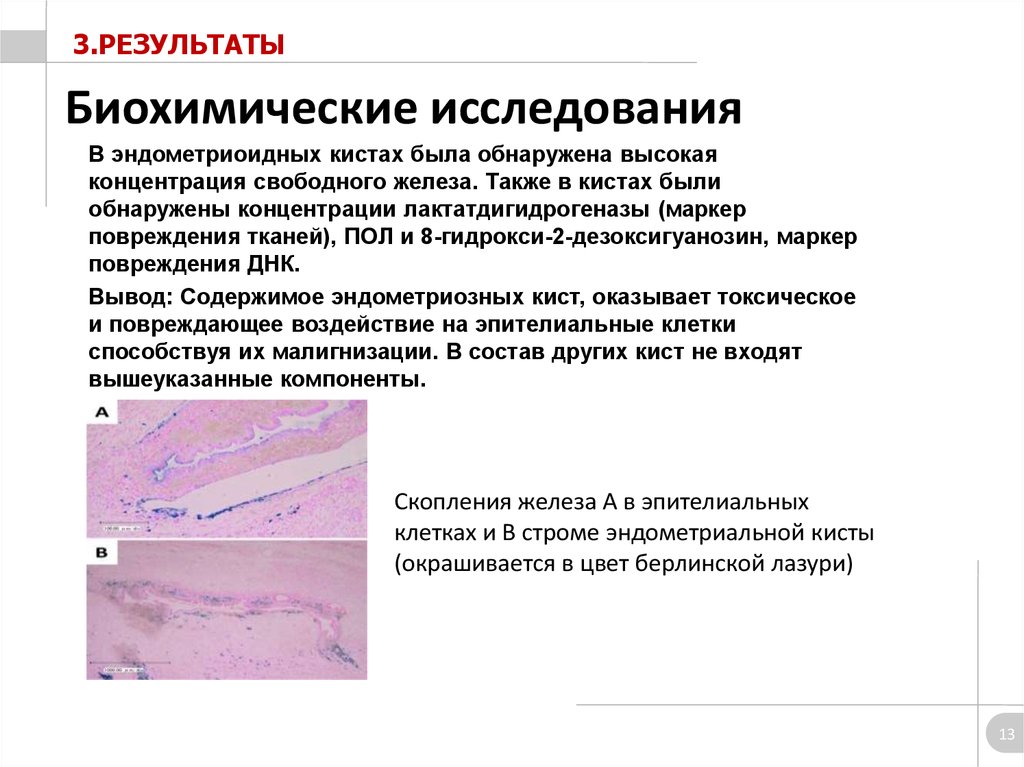
3.РЕЗУЛЬТАТЫБиохимические исследования
В эндометриоидных кистах была обнаружена высокая
концентрация свободного железа. Также в кистах были
обнаружены концентрации лактатдигидрогеназы (маркер
повреждения тканей), ПОЛ и 8-гидрокси-2-дезоксигуанозин, маркер
повреждения ДНК.
Вывод: Содержимое эндометриозных кист, оказывает токсическое
и повреждающее воздействие на эпителиальные клетки
способствуя их малигнизации. В состав других кист не входят
вышеуказанные компоненты.
Скопления железа А в эпителиальных
клетках и В строме эндометриальной кисты
(окрашивается в цвет берлинской лазури)
13
14. Выводы полностью соответствуют результатам исследования, учитывая ее сложность и новизну авторы указывали во время исследования
4. ОЦЕНКАВыводы полностью соответствуют результатам исследования,
учитывая ее сложность и новизну авторы указывали во
время исследования и указывают в выводах, что точные
молекулярные механизмы еще не выяснены
• Заключение: Работу в данном направлении следует продолжать,
учитывая, что недавно путем микроматричного анализа авторами,
было обнаружено, что ингибитор мультикиназы(сорафениб)
оказывает противоопухолевое действие у мышей
(Как по другому можно объяснить полученные результаты?)
Поскольку частота большинства результатов были далеки от 50%, то
есть большая вероятность того, что это результат малигнизации
покровного эпителия яичника который тоже недостаточно изучен с
параллельным течением эндометриоза или же есть еще какие либо
источники канцерогенеза яичников, которые нам еще не известны и
для их открытия необходимо продолжать исследования в области
генетики и молекулярной биологии.
14
15.
1516.
Литература (гистологического исследования)(3)Stern RC, Dash R, Bentley RC, et al. (2001) Malignancy in endometriosis: frequency and
comparison of ovarian and extraovarian
types. Int J Gynecol Pathol 20:133–139
Modesitt SC, Tortolero-Luna G, Robinson JB, et al. (2002) Ovarian
and extraovarian endometriosis-associated cancer. Obstet Gynecol
100:788–795
Rutgers JL, Scully RE (1988) Ovarian mullerian mucinous papillary cystadenomas of borderline
malignancy. A clinicopathologic
analysis. Cancer 61:340–348
Rutgers JL, Scully RE (1988) Ovarian mixed-epithelial papillary
cystadenomas of borderline malignancy of mullerian type. A clinicopathologic analysis. Cancer
61:546–554
.Lee KR, Nucci MR (2003) Ovarian mucinous and mixed epithelial
carcinomas of mullerian (endocervical-like) type: a clinicopathologic analysis of four cases of an
uncommon variant associated with
endometriosis. Int J Gynecol Pathol 22:42–51
Griffith LM, Carcangiu ML (1991) Sex cord tumor with annular
tubules associated with endometriosis of the fallopian tube. Am J
Clin Pathol 96:259–262
Manipadam MT, Munemane A, Emmanuel P, et al. (2008) McCluggage WG. Ovarian
adenosarcoma with extensive deciduoid morphology arising in endometriosis: a case report. Int J
Gynecol
16
17. Литература (молекулярно-генетический анализ)
(4) Martini M, Ciccarone M, Garganese G, et al. (2002) Possibleinvolvement of hMLH1, p16(INK4a) and PTEN in the malignant
transformation of endometriosis. Int J Cancer 102:398–406
Obata K, Hoshiai H (2000) Common genetic changes between
endometriosis and ovarian cancer. Gynecol Obstet Invest 50(Suppl
1):39–43
•Yagyu T, Tsuji Y, Haruta S, et al. (2006) Activation of mammalian
target of rapamycin in postmenopausal ovarian endometriosis. Int
J Gynecol Cancer 16:1545–1551
•Okuda T, Otsuka J, Sekizawa A, et al. (2003) p53 mutations and
overexpression affect prognosis of ovarian endometrioid cancer
but not clear cell cancer. Gynecol Oncol 88:318–325
• Amemiya S, Sekizawa A, Otsuka J, et al. (2004) Malignant
transformation of endometriosis and genetic alterations of
K-ras and microsatellite instability. Int J Gynaecol Obstet 86:
371–376
•Otsuka J, Okuda T, Sekizawa A, et al. (2004) K-ras mutation may
promote carcinogenesis of endometriosis leading to ovarian clear
cell carcinoma. Med Electron Microsc 37:188–192
17














 Медицина
Медицина