Похожие презентации:
Электролитическая диссоциация. Степень и константа диссоциации
1.
Образовательный центр«ПАРАМИТА»
Курс лекций по химии
2. Тема:
• Электролитическая диссоциация. Степень иконстанта диссоциации.
3. Растворы (расплавы)
Электролиты – проводятэлектрический ток:
• Соли
• Кислоты
• Основания
Ионные или ковалентные сильно
полярные хим. связи.
Неэлектролиты:
• Многие органич. в-ва
• Многие простые в-ва
Ковалентные неполярные или
малополярные хим. связи.
4.
2) В растворе или расплаве электролитов оны движутся хаотически.При пропускании через раствор или расплав электрического тока
положительно заряженные ионы движутся к отрицательно
заряженному электроду (катоду), а отрицательно заряженные ионы
к положительно заряженному электроду (аноду). Поэтому
положительно заряженные ионы называются КАТИОНАМИ, а
отрицательно заряженные ионы – АНИОНАМИ.
КАТИОНЫ:
АНИОНЫ:
5. Теория электролитической диссоциации Аррениуса (1887г.)
1) Молекулы электролитов при растворении или расплавлениираспадаются на ионы
Ионы – атомы или группы атомов, имеющие положительный или
отрицательй заряд.
6.
7.
3) Диссоциация процесс обратимый.8. Механизм электролитической диссоциации. Гидратация ионов.
1) Механизм диссоциации электролитов с ионнойсвязью
9.
2) Механизм диссоциации электролитов, которыесостоят из полярных молекул
10. Степень диссоциации
Степень диссоциации зависит:1)Природы растворяемого вещества
2) Концентрации раствора
3) Температуры
11. В зависимости от степени диссоциации:
Сильные электролиты – вводных растворах полностью
диссоциируют на ионы, т.е.
α=1 (100%):
• Соли
• Сильные кислоты
• Щелочи
Слабые электролиты – в
водных растворах не полностью
диссоциируют на ионы, т.е.
α <1 (100%):
• Слабые кислоты
• Слабые нерастворимые в воде
основания
• Гидроксид аммония
• Вода
12.
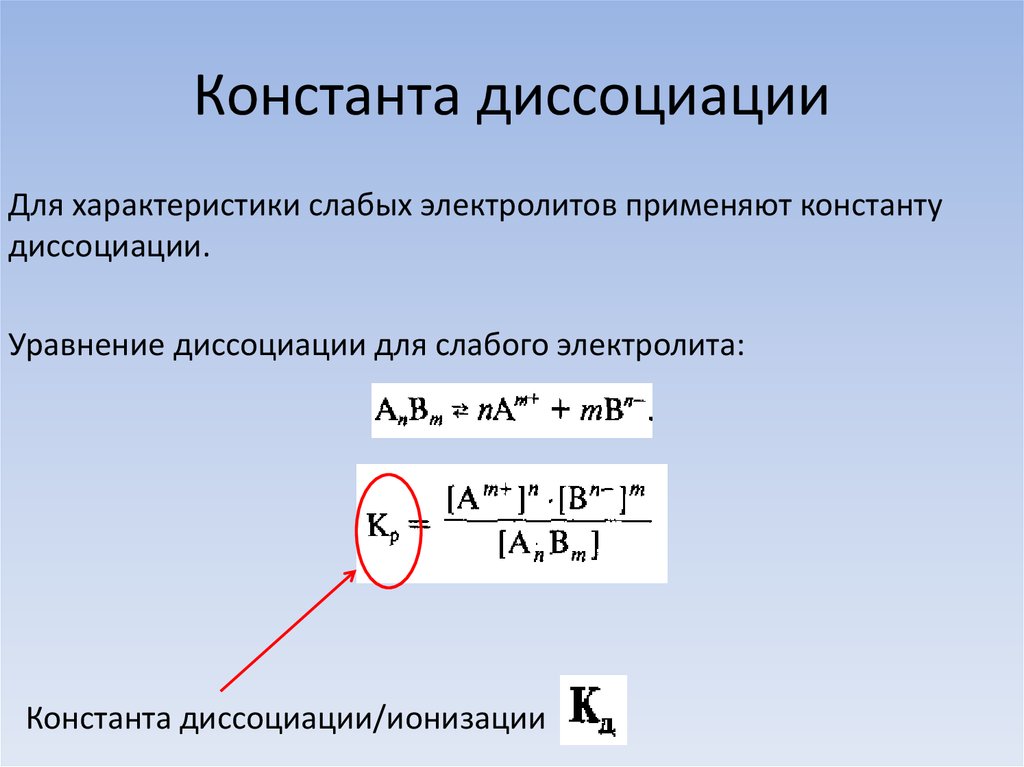
13. Константа диссоциации
Для характеристики слабых электролитов применяют константудиссоциации.
Уравнение диссоциации для слабого электролита:
Константа диссоциации/ионизации
14.
характеризует способность электролита диссоциировать наионы.
Чем больше
, тем легче электролит распадается на ионы, тем
больше его ионов в растворе, тем сильнее электролит.
ЗАВИСИТ: природы электролита и растворителя, температуры
НЕ ЗАВИСИТ: концентрации раствора
15. Диссоциация солей, оснований, амфотерных гидроксидов и солей в водных растворах
1) Сильные кислоты2) Слабые многоосновные кислоты диссоциируют ступенчато
(число ступеней диссоциации зависит от основности кислоты)
16.
17.
• Сильные однокислотные• Сильные двухкислотные
• Слабые многокислотные основания диссоциируют ступенчато



















 Химия
Химия








