Похожие презентации:
Основные типы связи
1.
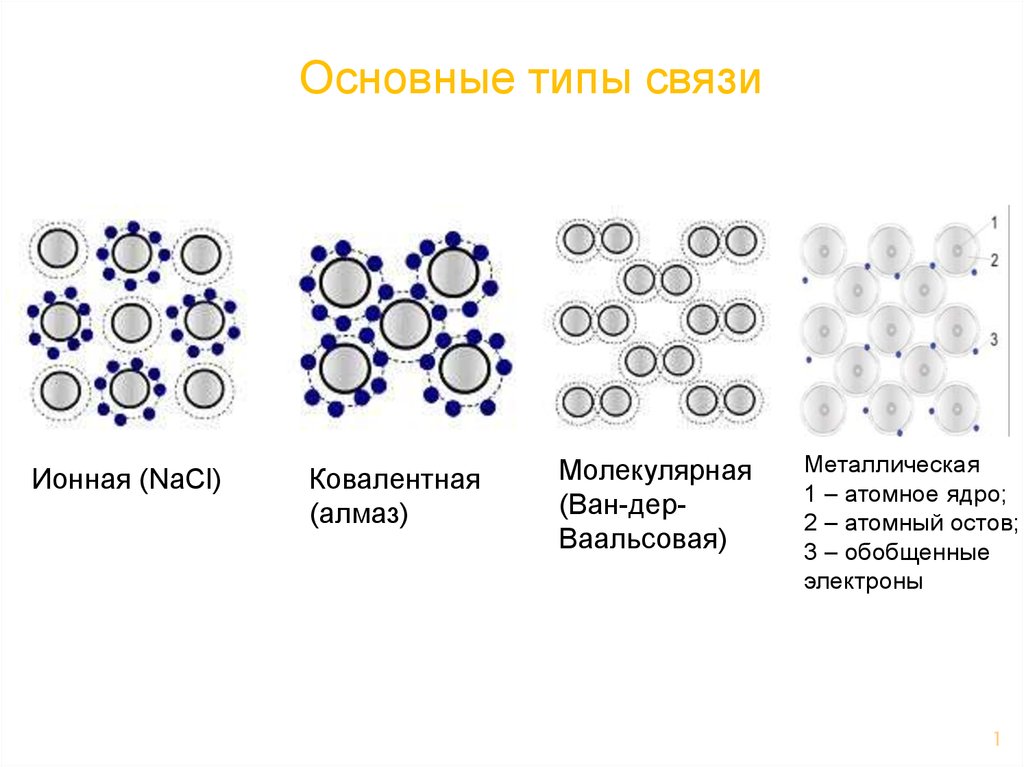
Основные типы связиИонная (NaCl)
Ковалентная
(алмаз)
Молекулярная
(Ван-дерВаальсовая)
Металлическая
1 – атомное ядро;
2 – атомный остов;
3 – обобщенные
электроны
1
2.
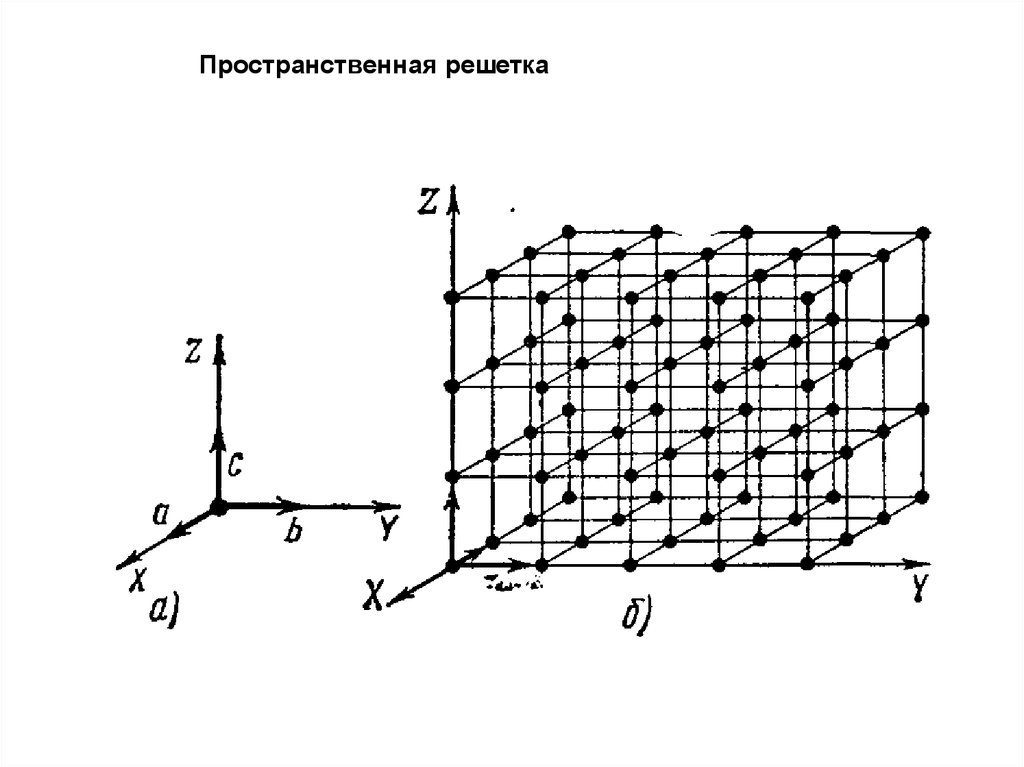
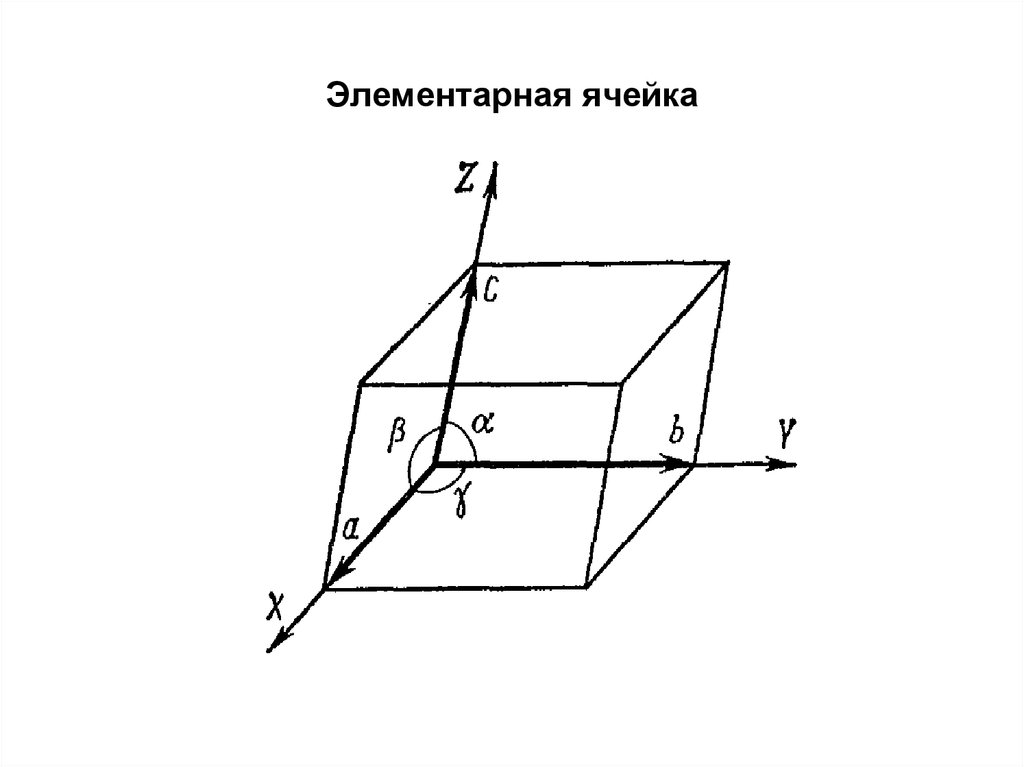
Пространственная решетка3. Элементарная ячейка
4.
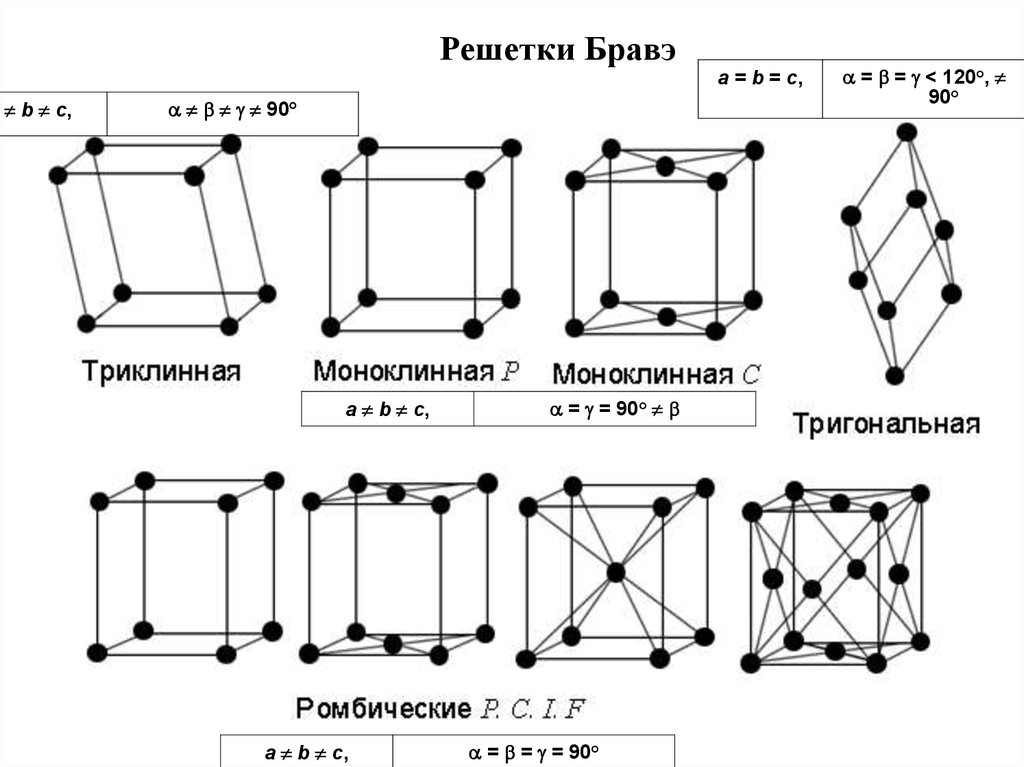
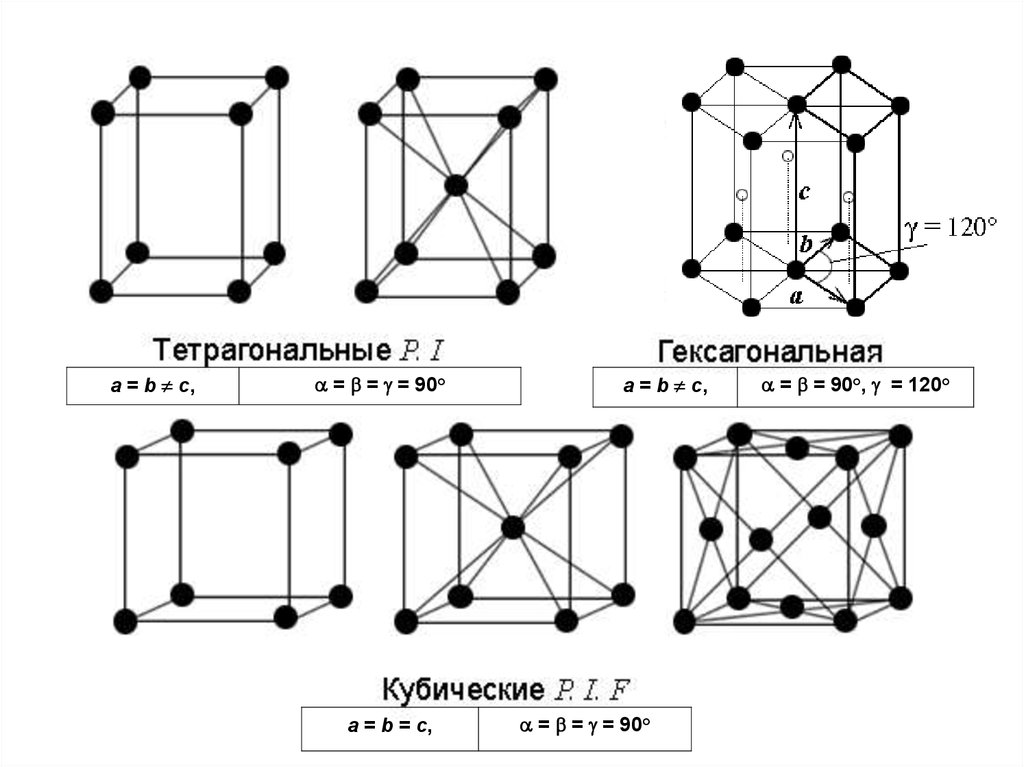
a b c,Решетки Бравэ
a = b = c,
90
a b c,
a b c,
= = 90°
= = = 90°
= = < 120°,
90°
5.
a = b c,= = = 90°
a = b = c,
a = b c,
= = = 90°
= = 90°, = 120°
6.
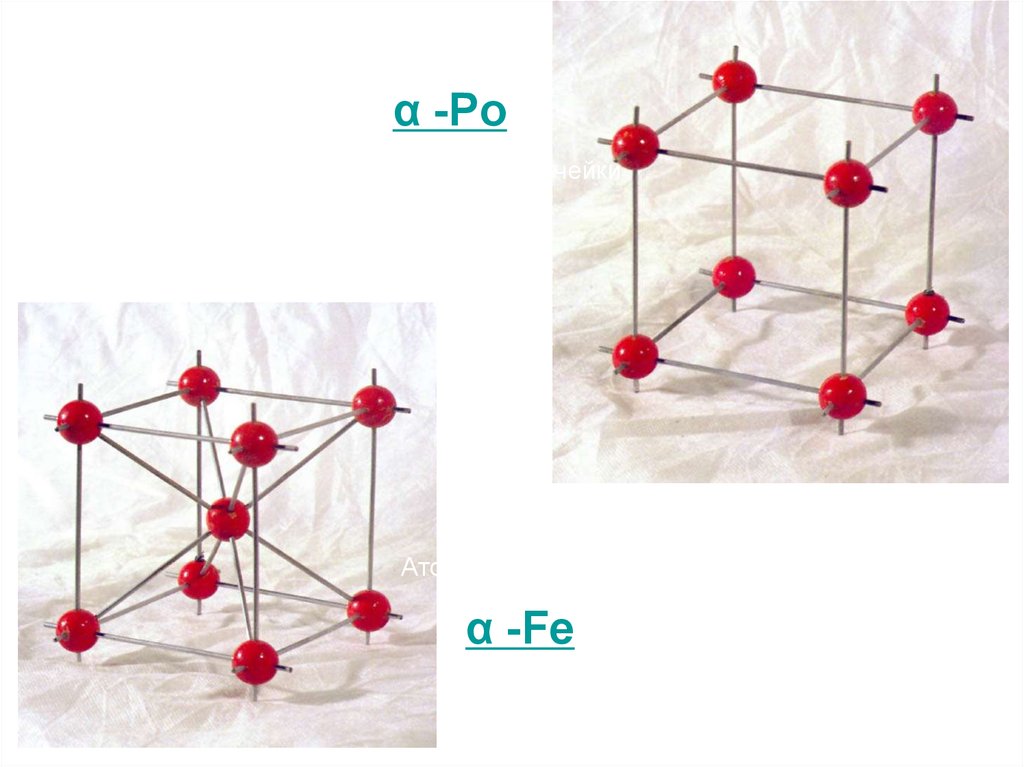
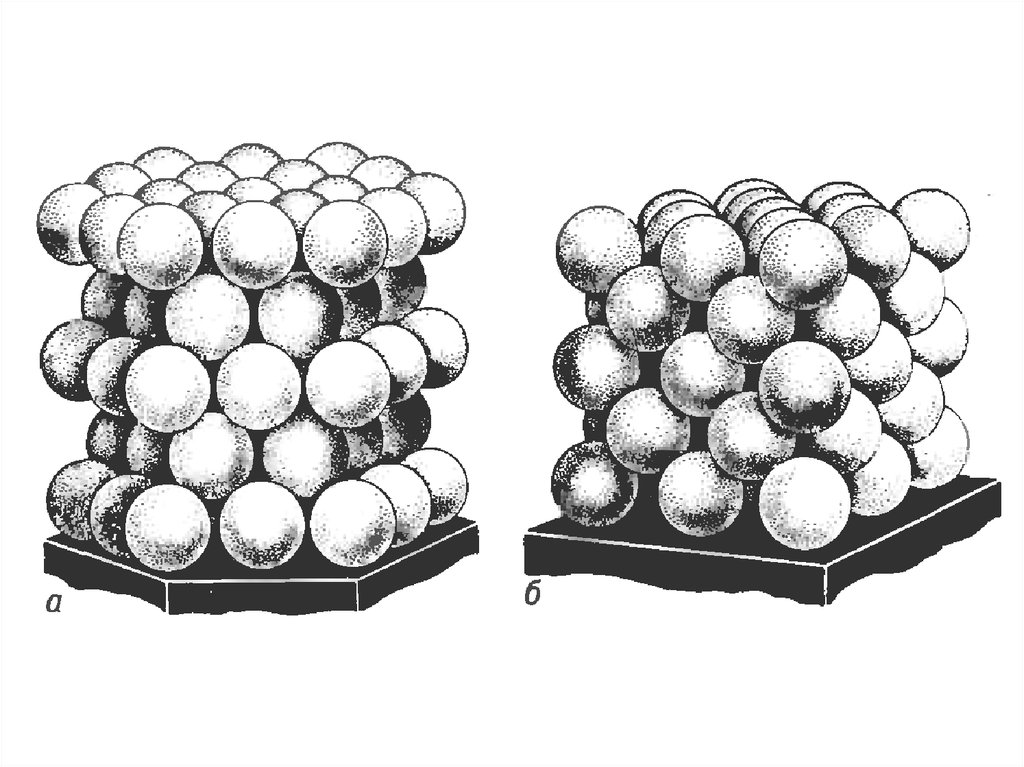
α -PoАтомы в вершинах кубической ячейки
Атомы в вершинах и в центре кубической ячейки
α -Fe
7.
α-графитАтомы C образуют слои, состоящие из
сопряженных правильных шестиугольников.
Слои налагаются по закону ...ABABAB...; слой
B сдвинут относительно слоя A на величину
вектора, равного связи C–C.
Отношение параметров c/a = 2,72.
Алмаз
8.
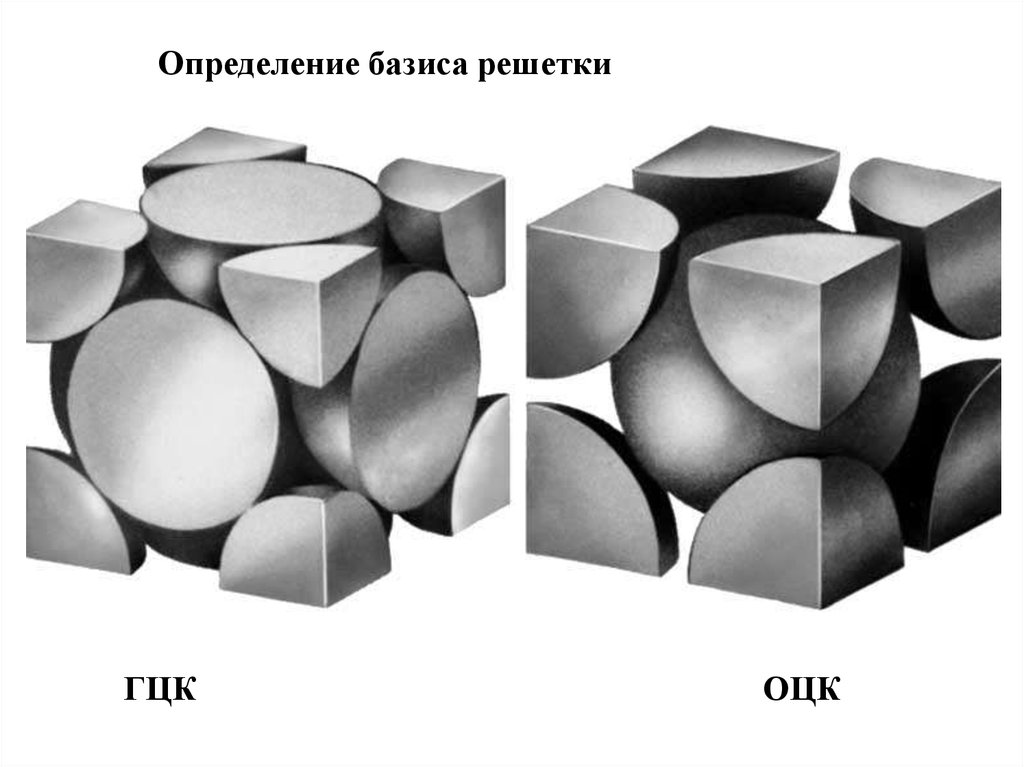
Определение базиса решеткиГЦК
ОЦК
9.
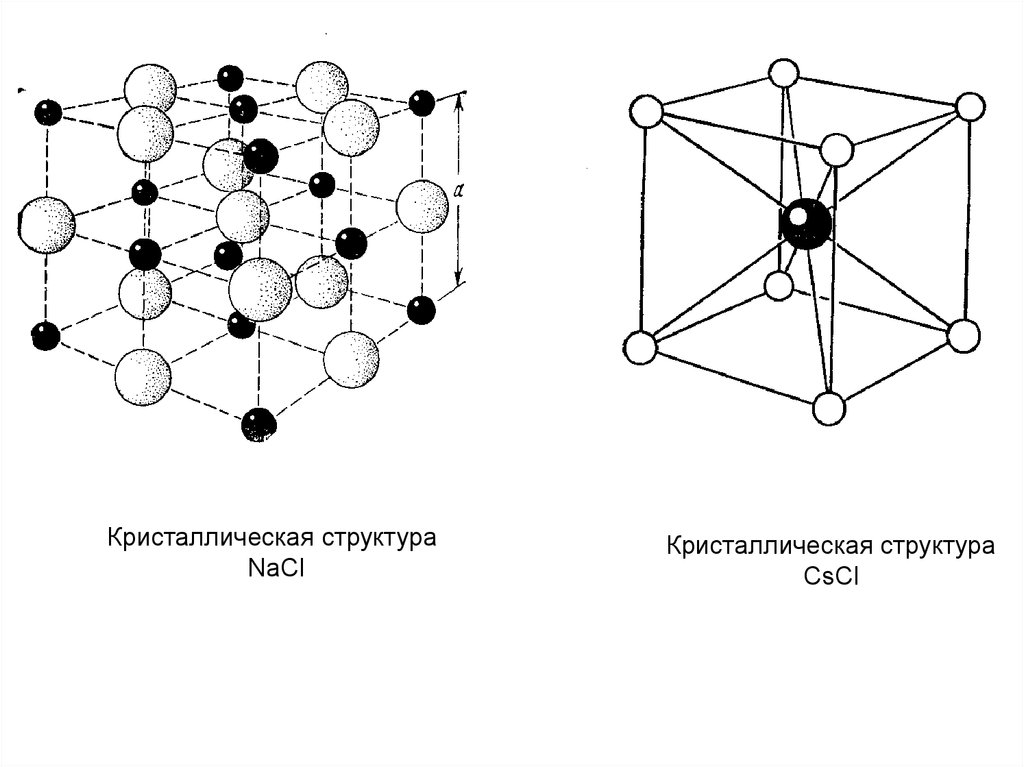
Кристаллическая структураNaCl
Кристаллическая структура
CsCl
10.
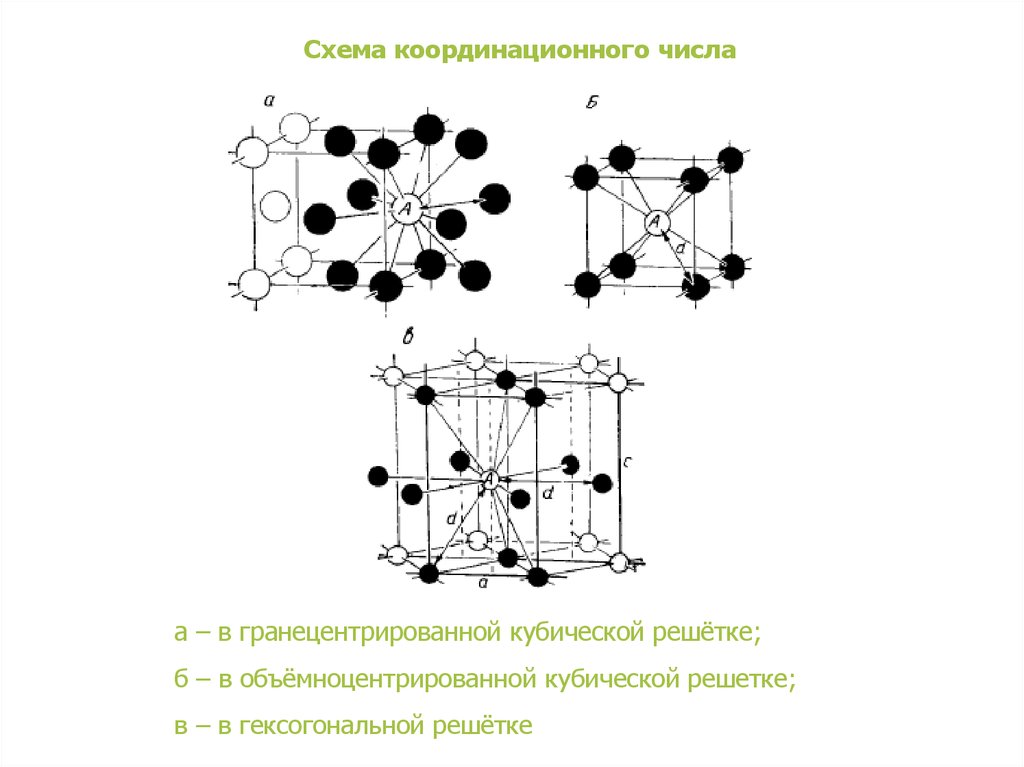
Схема координационного числаа – в гранецентрированной кубической решётке;
б – в объёмноцентрированной кубической решетке;
в – в гексогональной решётке
11.
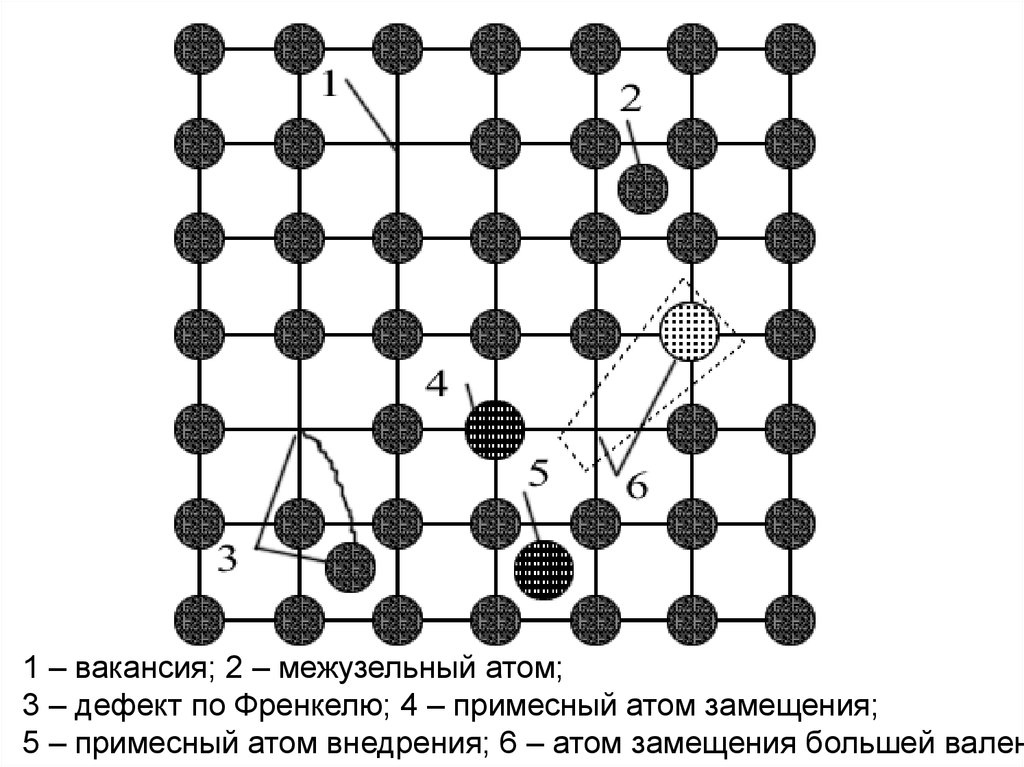
1 – вакансия; 2 – межузельный атом;3 – дефект по Френкелю; 4 – примесный атом замещения;
5 – примесный атом внедрения; 6 – атом замещения большей вален
12.
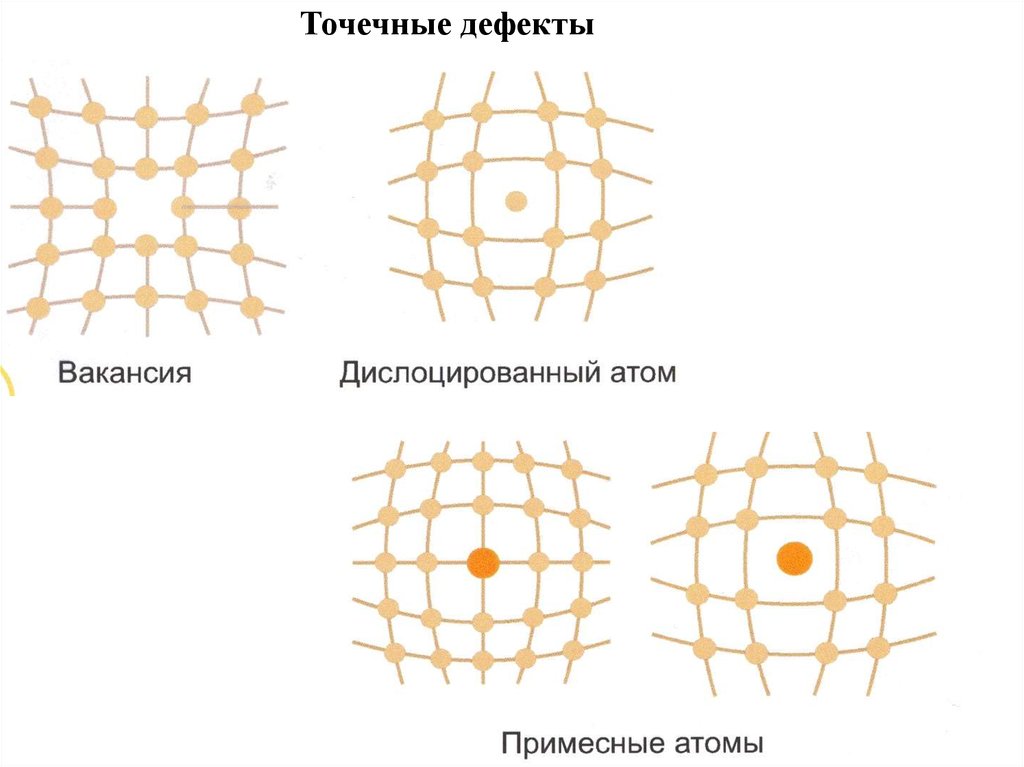
Точечные дефекты13.
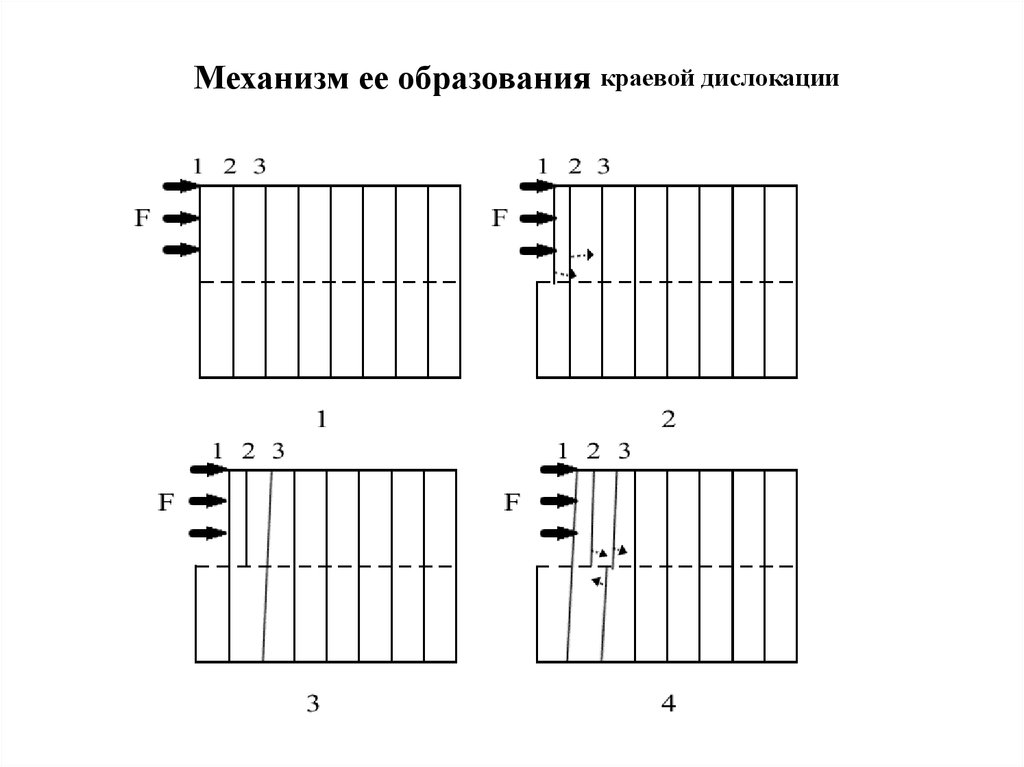
Механизм ее образования краевой дислокацииa
б
14.
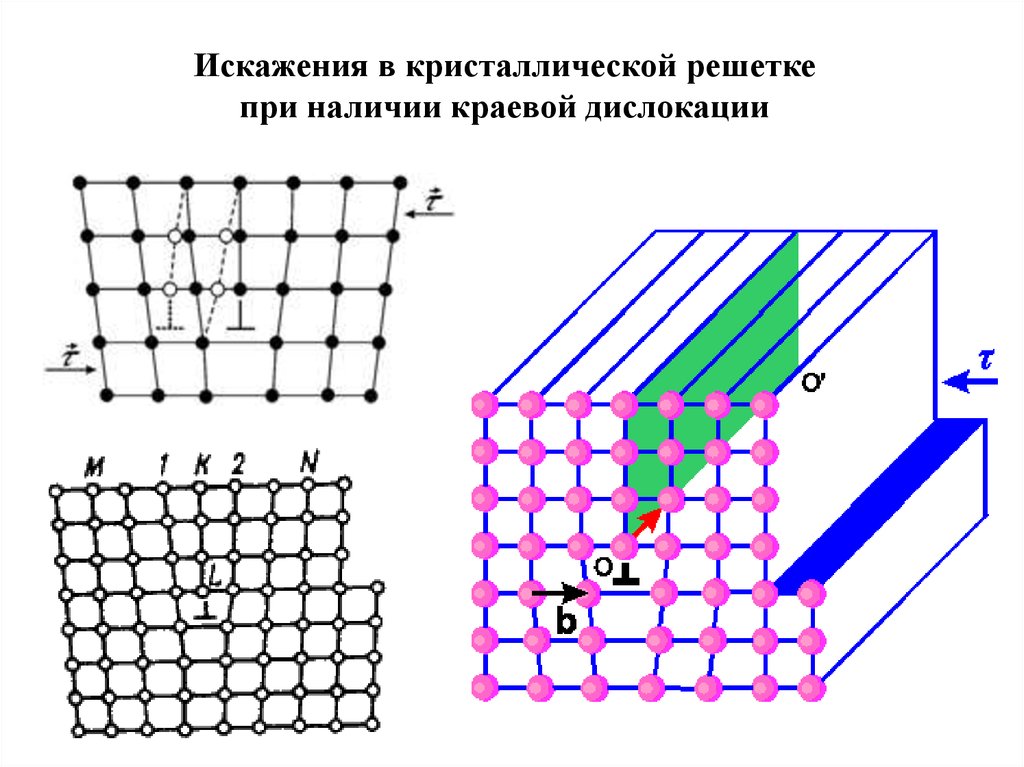
Искажения в кристаллической решеткепри наличии краевой дислокации
15.
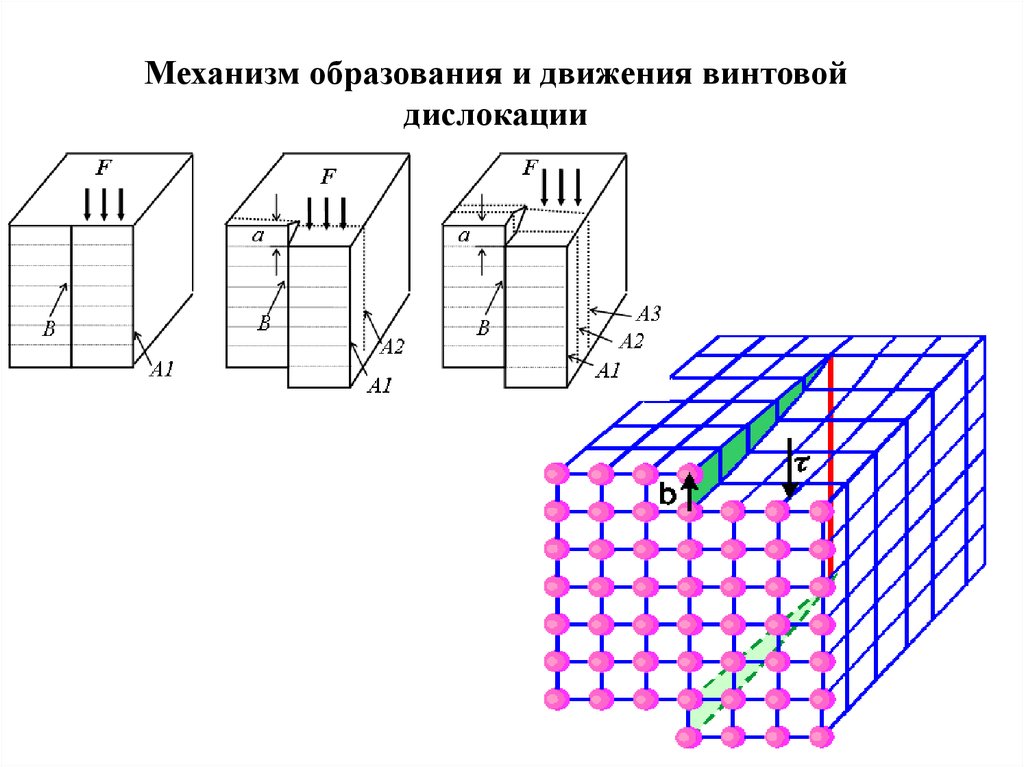
Механизм образования и движения винтовойдислокации
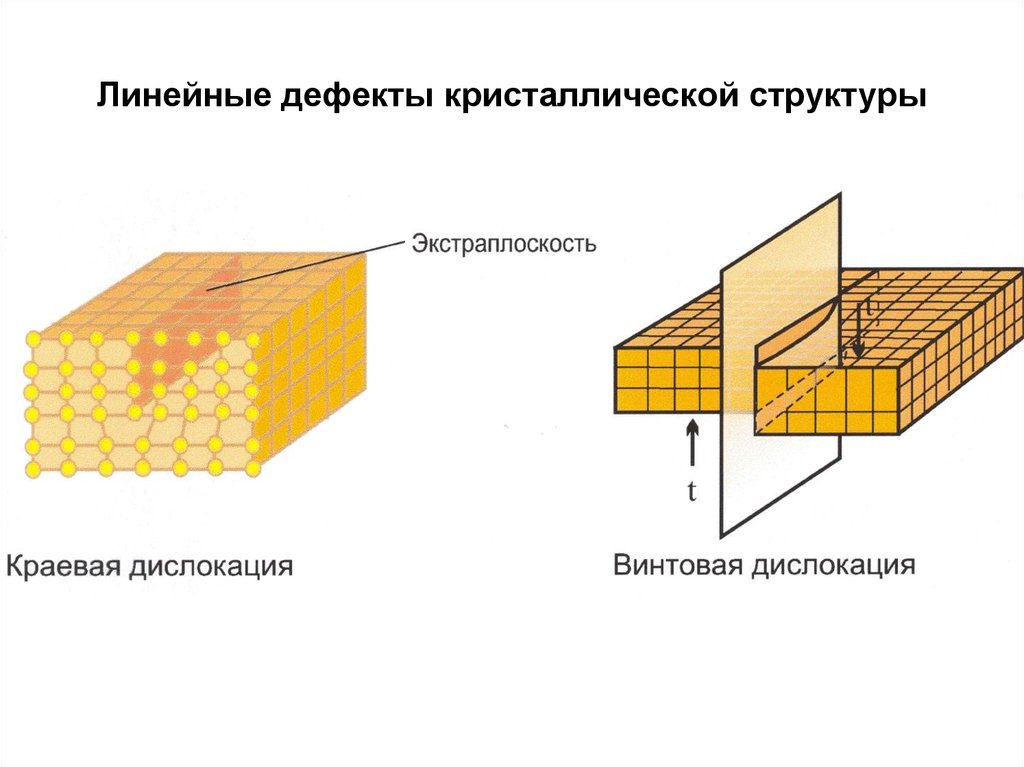
16. Линейные дефекты кристаллической структуры
17.
18.
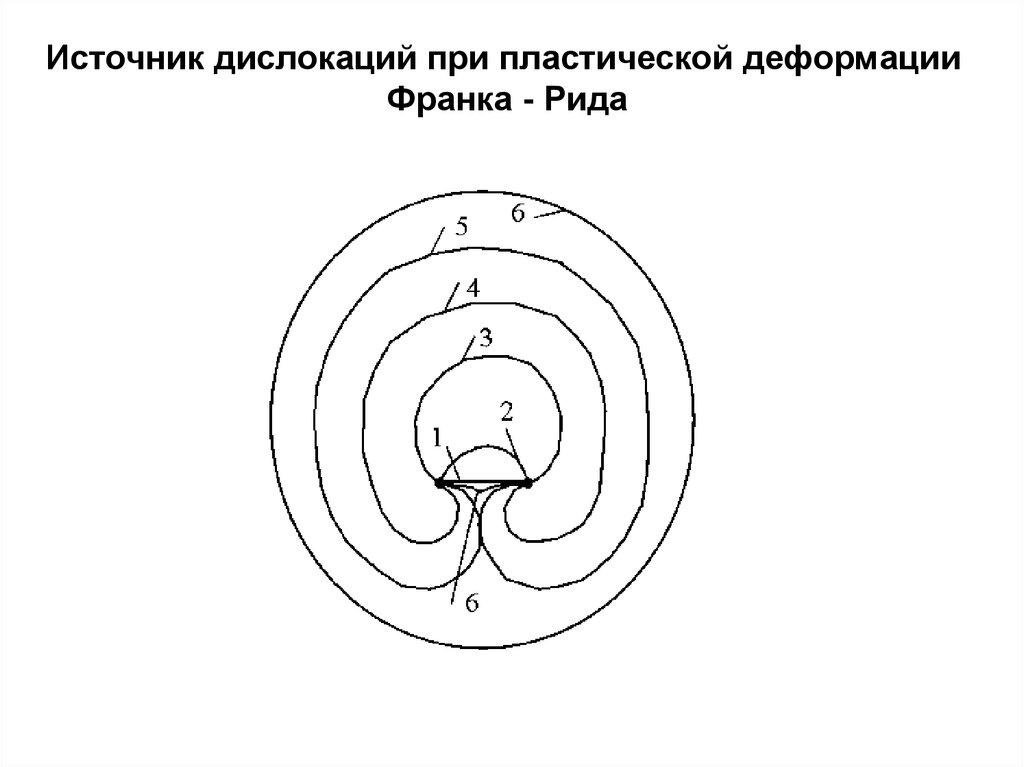
Источник дислокаций при пластической деформацииФранка - Рида
19.
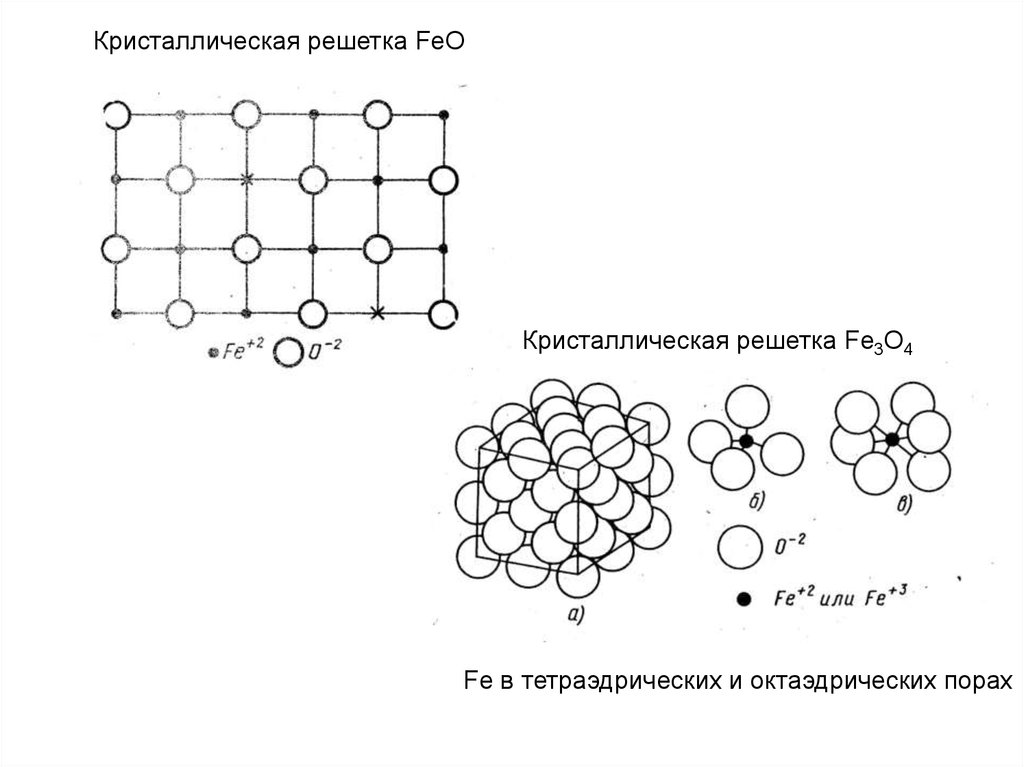
Кристаллическая решетка FeOКристаллическая решетка Fe3O4
Fe в тетраэдрических и октаэдрических порах
20.
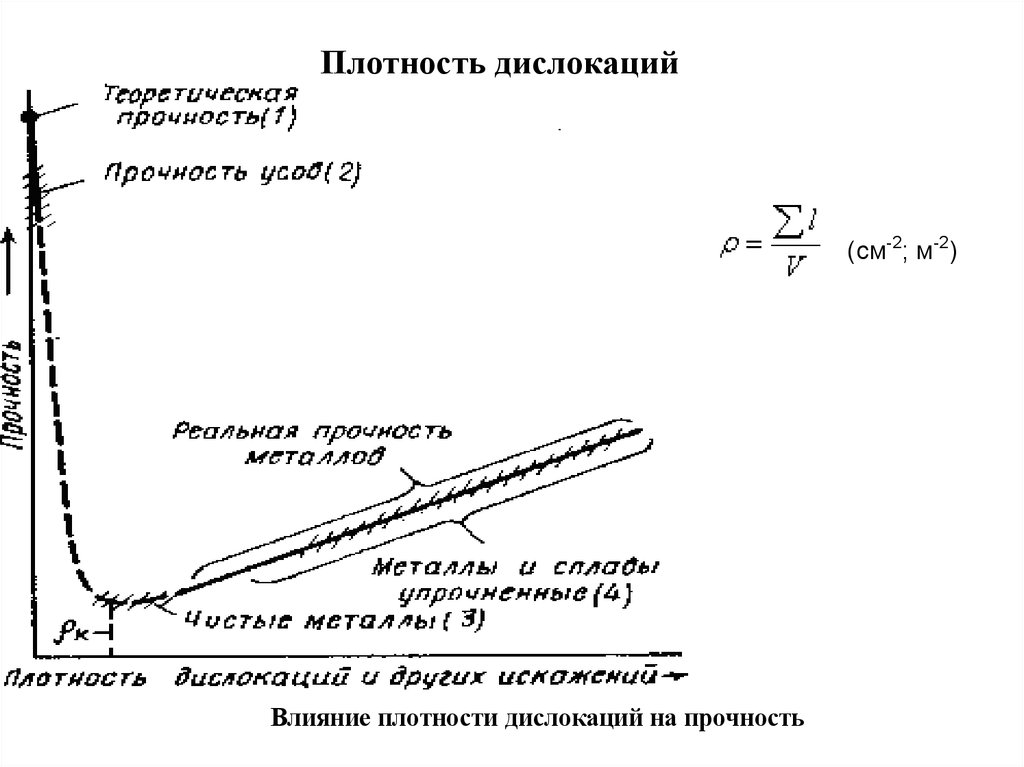
Плотность дислокаций(см-2; м-2)
Влияние плотности дислокаций на прочность
21.
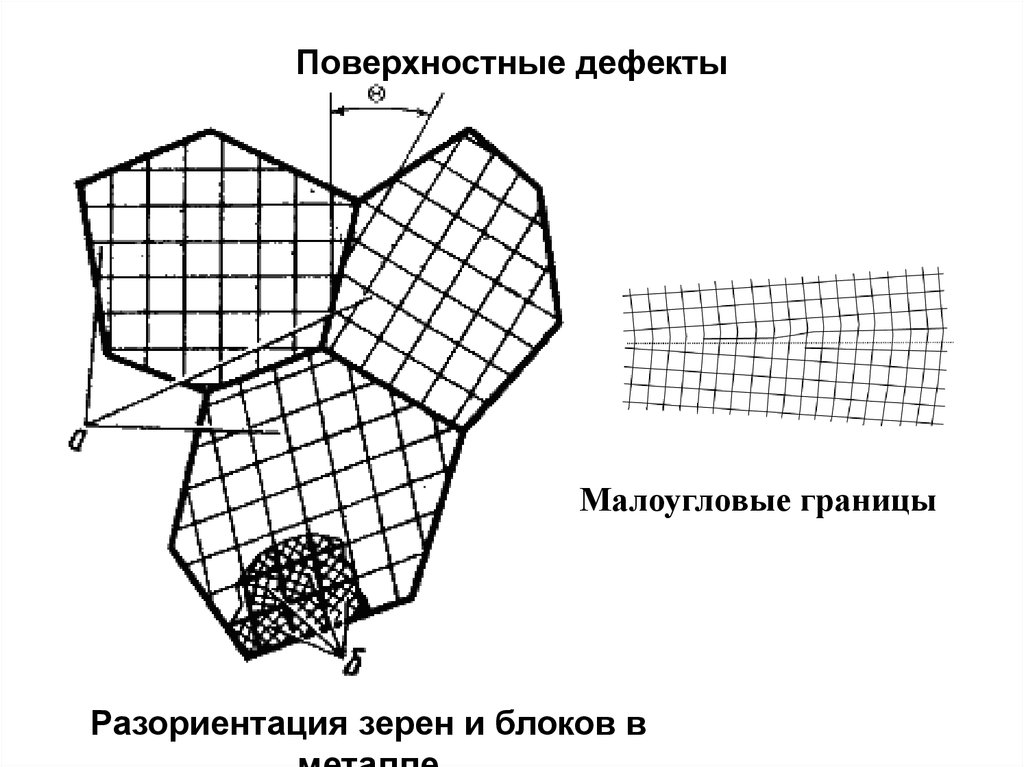
Поверхностные дефектыМалоугловые границы
Разориентация зерен и блоков в
22.
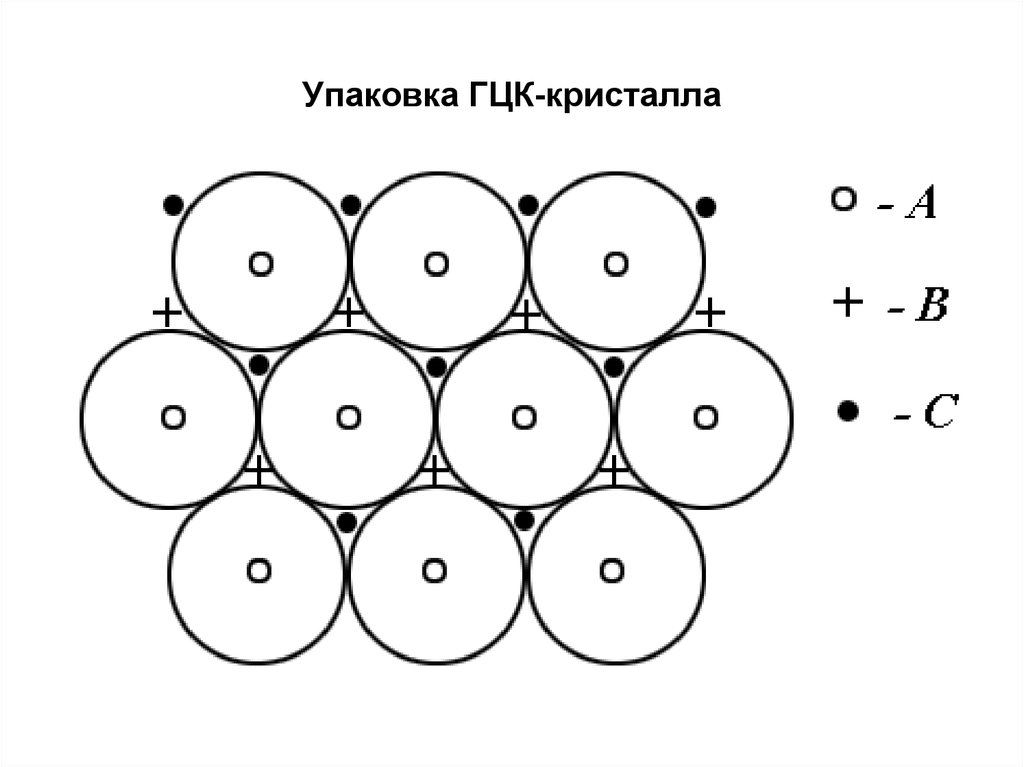
23. Упаковка ГЦК-кристалла
24.
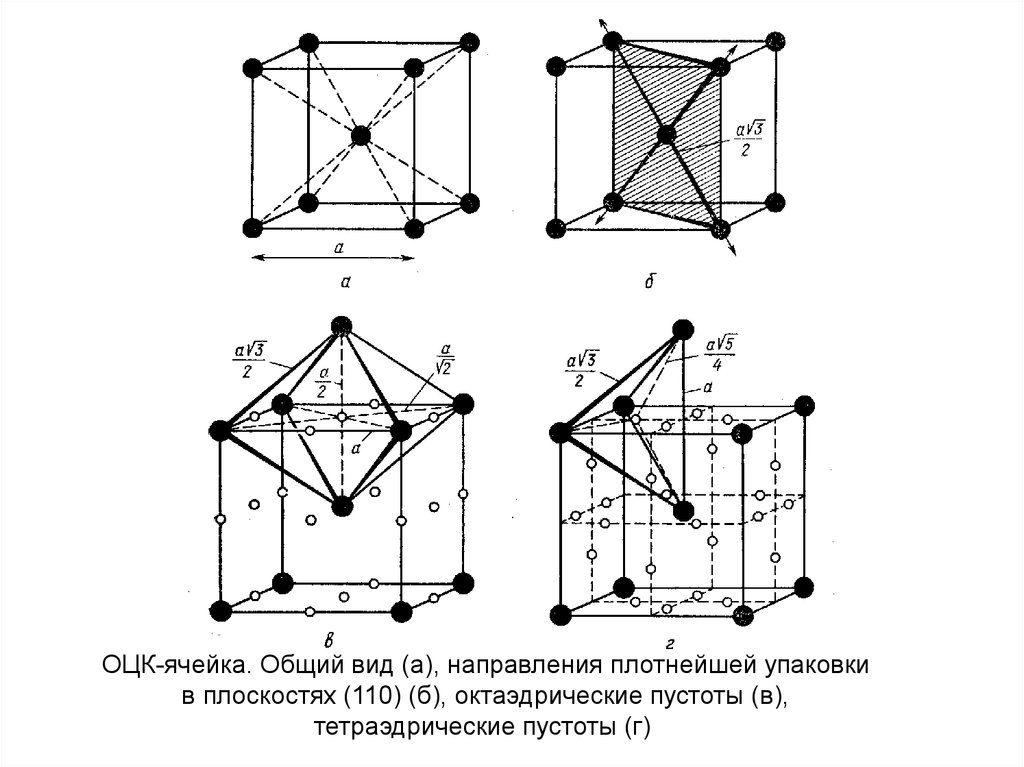
ОЦК-ячейка. Общий вид (а), направления плотнейшей упаковкив плоскостях (110) (б), октаэдрические пустоты (в),
тетраэдрические пустоты (г)
25.
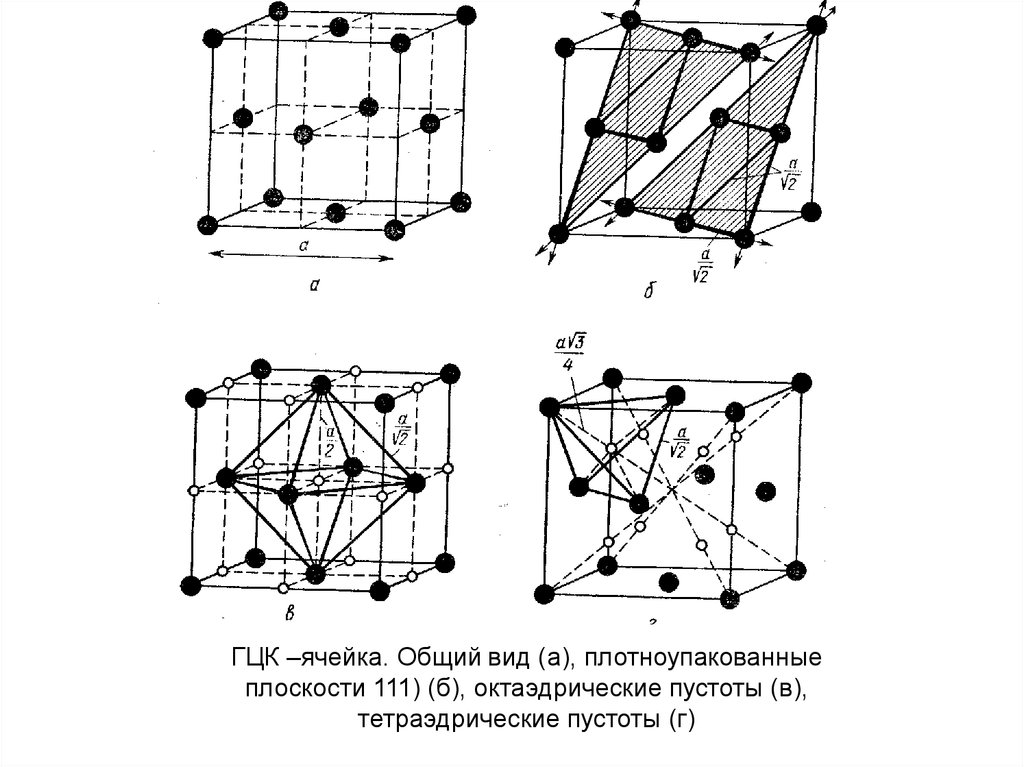
ГЦК –ячейка. Общий вид (а), плотноупакованныеплоскости 111) (б), октаэдрические пустоты (в),
тетраэдрические пустоты (г)
26.
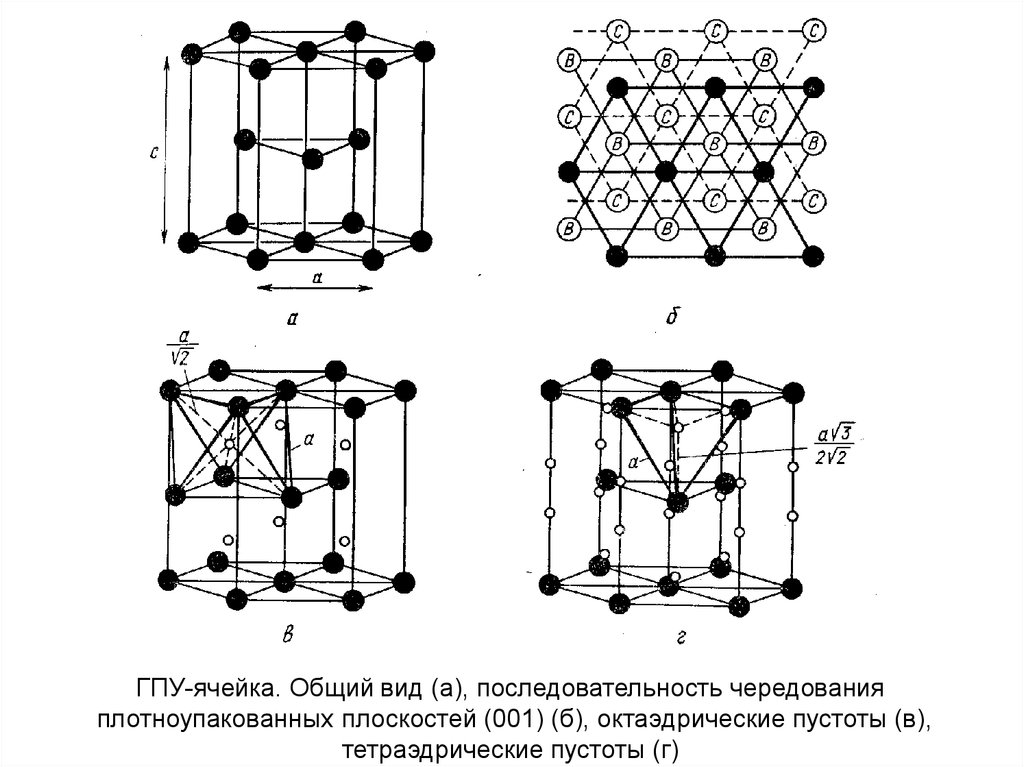
ГПУ-ячейка. Общий вид (а), последовательность чередованияплотноупакованных плоскостей (001) (б), октаэдрические пустоты (в),
тетраэдрические пустоты (г)
27.
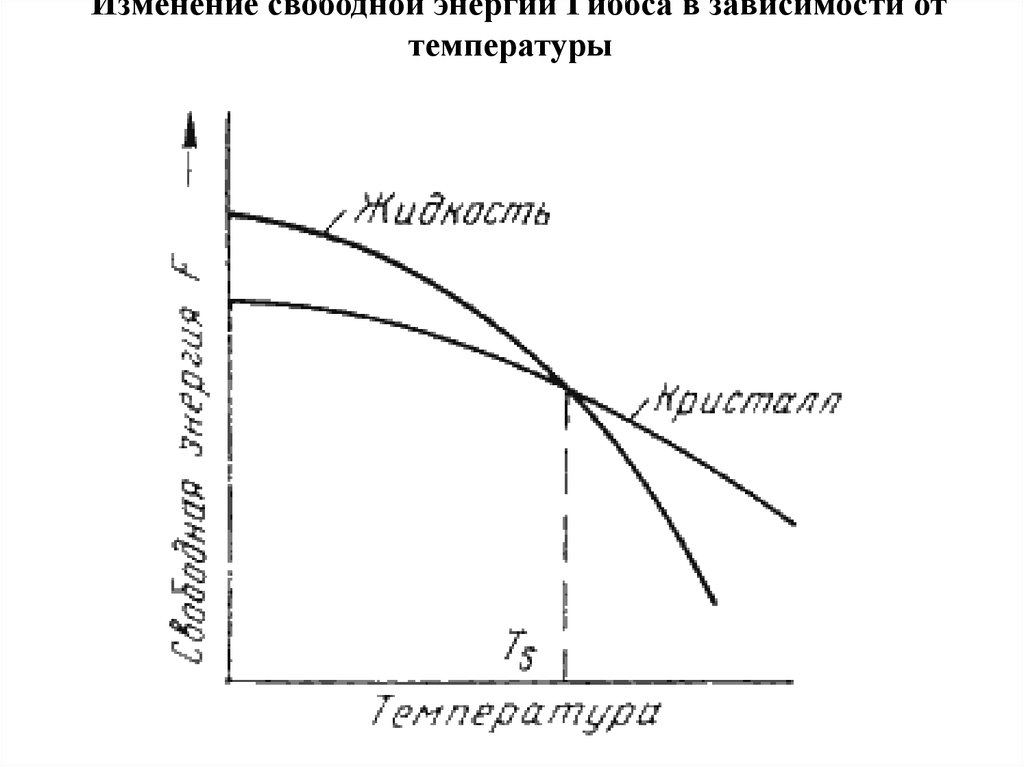
Изменение свободной энергии Гиббса в зависимости оттемпературы
28.
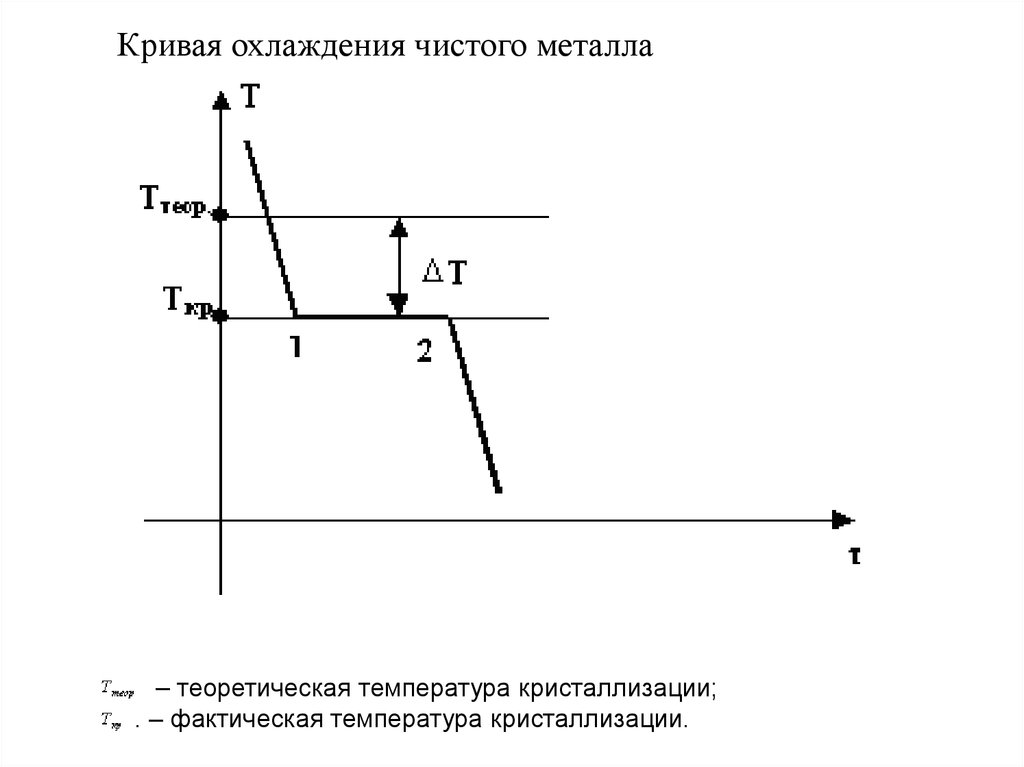
Кривая охлаждения чистого металла– теоретическая температура кристаллизации;
. – фактическая температура кристаллизации.
29.
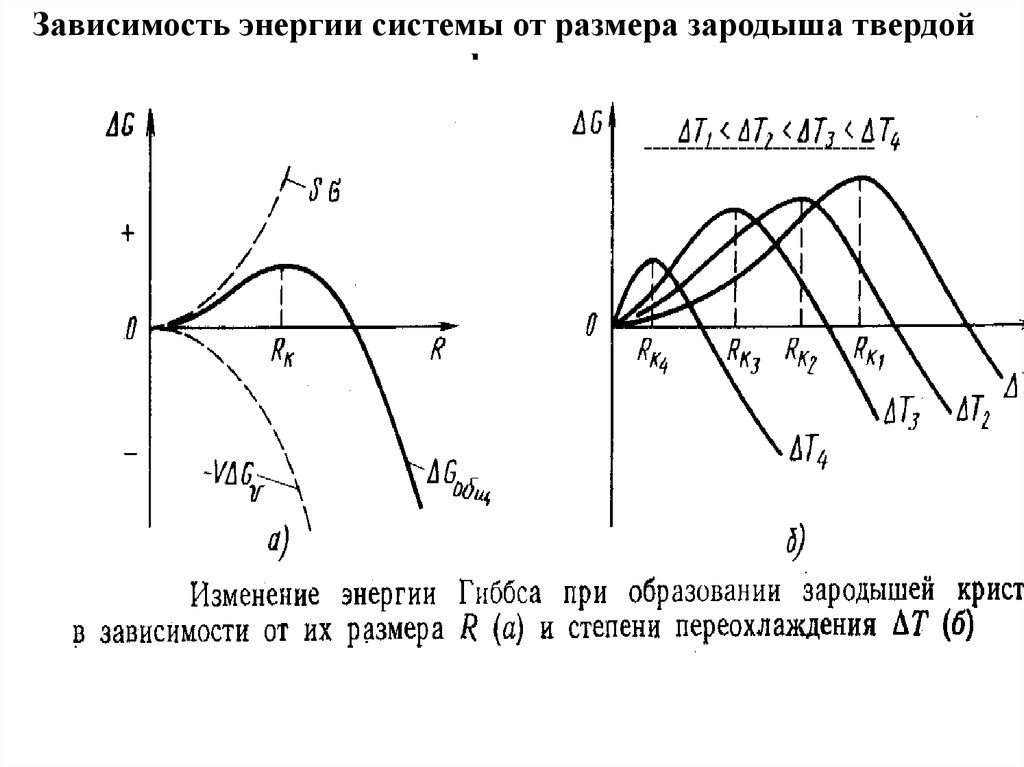
Зависимость энергии системы от размера зародыша твердойфазы
---------------------------
30.
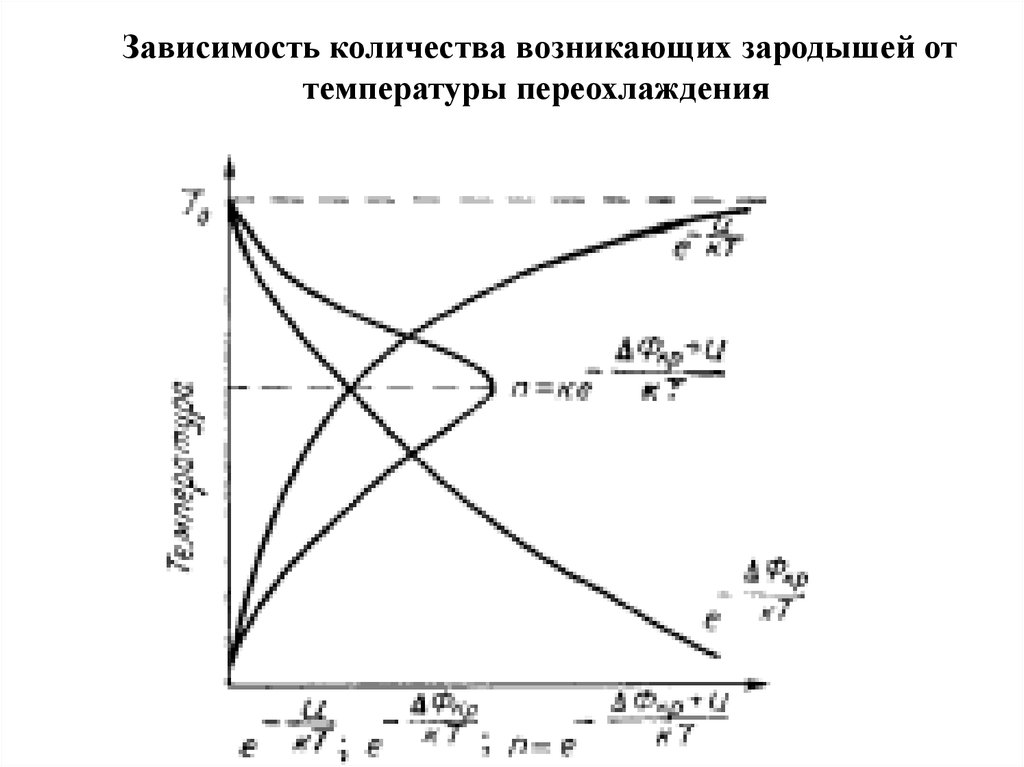
Зависимость количества возникающих зародышей оттемпературы переохлаждения
31.
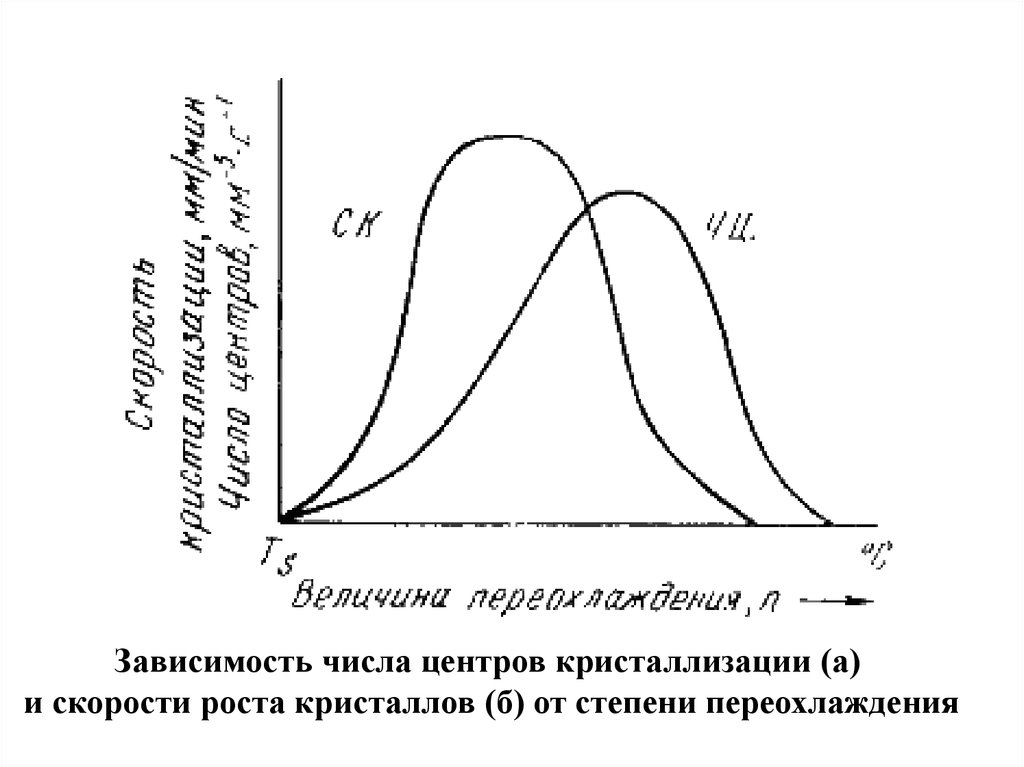
Зависимость числа центров кристаллизации (а)и скорости роста кристаллов (б) от степени переохлаждения
32.
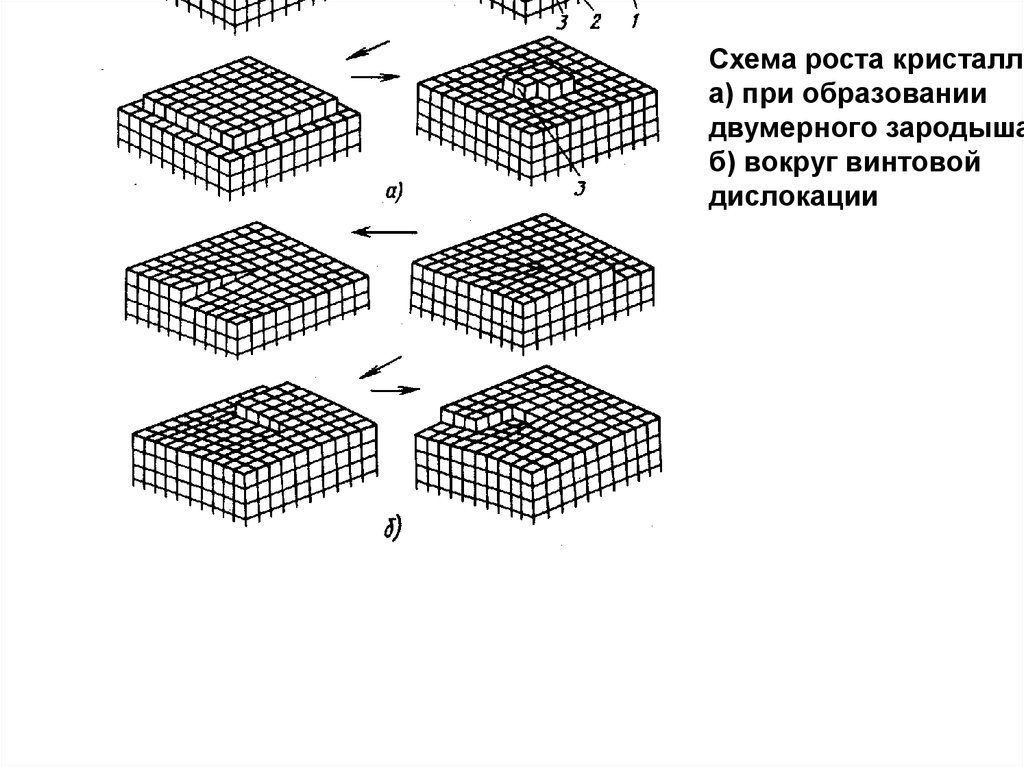
Схема роста кристаллаа) при образовании
двумерного зародыша
б) вокруг винтовой
дислокации
33.
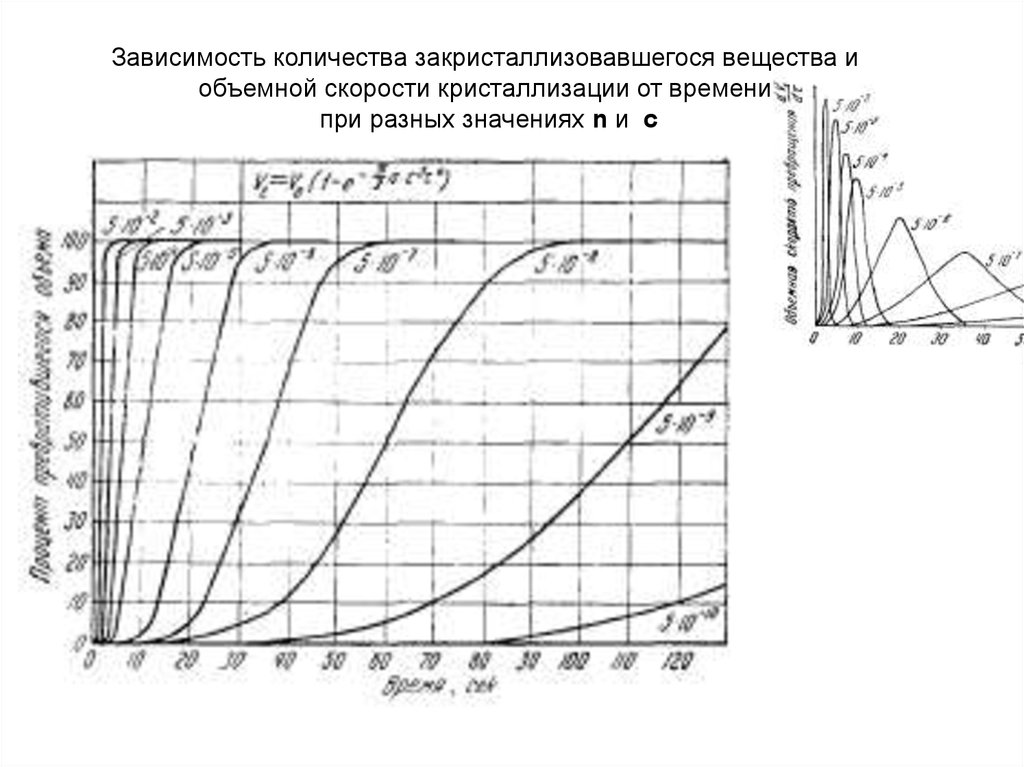
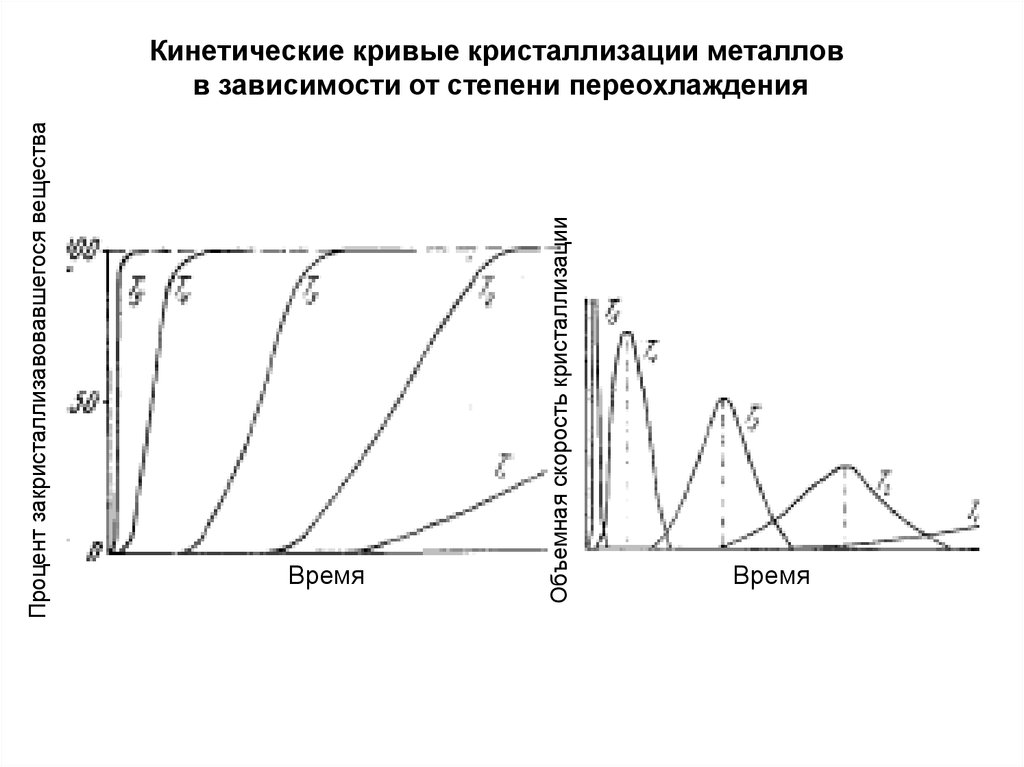
Зависимость количества закристаллизовавшегося вещества иобъемной скорости кристаллизации от времени
при разных значениях n и c
34.
ВремяОбъемная скорость кристаллизации
Процент закристаллизавовавшегося вещества
Кинетические кривые кристаллизации металлов
в зависимости от степени переохлаждения
Время
35.
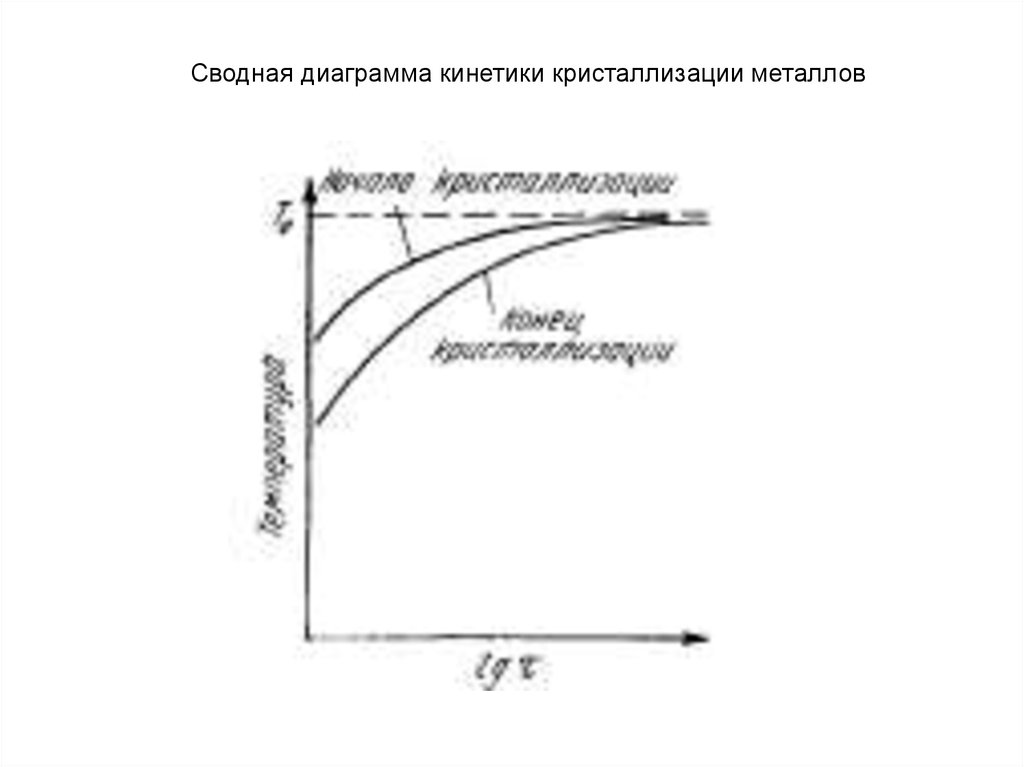
Сводная диаграмма кинетики кристаллизации металлов36.
37. Строение металлического слитка
Схема стального слитка, данная Черновым Д.К.,представлена на рис.3.7.
Слиток состоит из трех зон:
1. мелкокристаллическая корковая зона;
2. зона столбчатых кристаллов;
3. внутренняя зона крупных равноосных кристаллов.
Кристаллизация корковой зоны идет в условиях
максимального переохлаждения. Скорость кристаллизации
определяется большим числом центров кристаллизации.
Образуется мелкозернистая структура.
Жидкий металл под корковой зоной находится в условиях
меньшего переохлаждения. Число центров ограничено и
процесс кристаллизации реализуется за счет их интенсивного
роста до большого размера.



 Химия
Химия








