Похожие презентации:
Синтез высокооктановых компонентов топлива
1.
Превращения УВ в реакцияхполимеризации, алкилирования и изомеризации
(синтез высокооктановых компонентов топлива)
Требования к топливам для карбюраторных двигателей:
Октановое число 90-93
Можно получить за счет компаундирования –
добавление к базовым бензинам высокооктановых УВ и их смесе
УВ
Бутан
Изобутан
изооктан
бензол
ОЧ
92
98
100
107
2.
Способы получения высокооктановых изо-алканов1. Полимеризация олефинов,
с последующим гидрированием полимеров
2. Алкилирование изо-бутана олефинами
3. Изомеризация н-алканов либо легких фракций нефт
Способы получения ароматич соединений
для высокооктановых топлив
1. Алкилирование бензола олефинами
2. В процессе платформинга
3.
Синтез компонентов топлив( реакции алкилирования, полимеризации и изомеризаци
Проходят в присутствии кислых катализаторов
В жидкой или паровой вазе
Катализаторы:
1 сильные кислоты(серная, фосфорная, фтористоводородная)
– кислоты Бренстеда
2. Апротонные кислоты (хлорид алюминия, фторид бора)
– кислоты Льюиса
4.
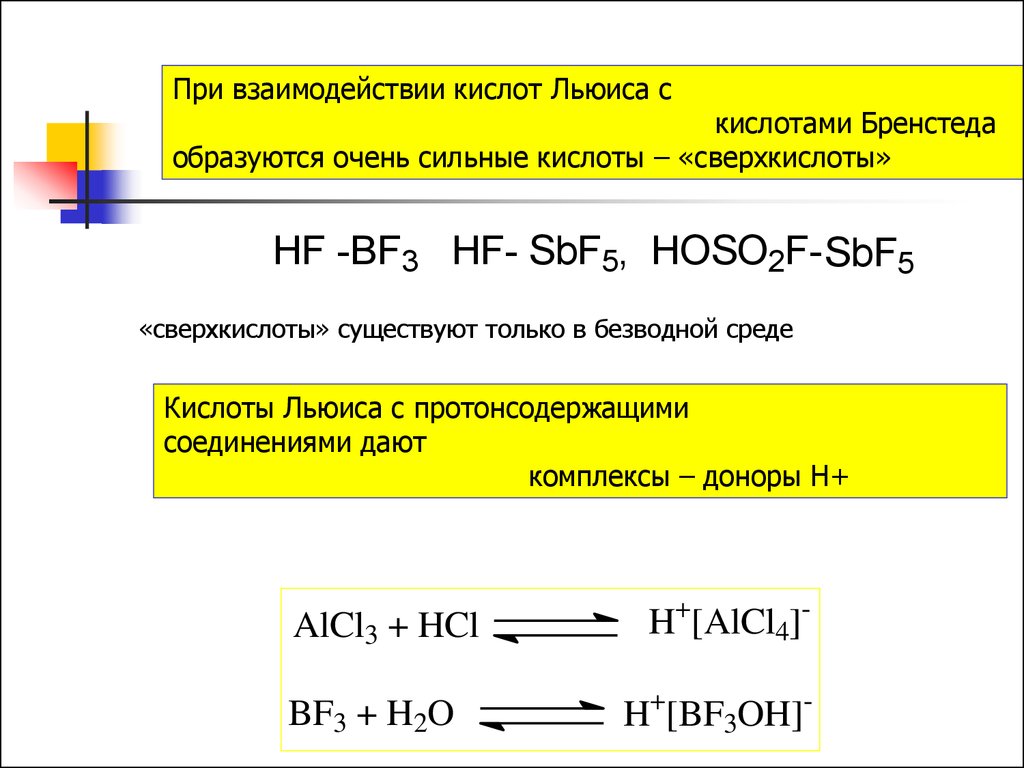
При взаимодействии кислот Льюиса скислотами Бренстеда
образуются очень сильные кислоты – «сверхкислоты»
HF -BF3 HF- SbF5, HOSO2F- SbF5
«сверхкислоты» существуют только в безводной среде
Кислоты Льюиса с протонсодержащими
соединениями дают
комплексы – доноры Н+
AlCl3 + HCl
BF3 + H2O
H+[AlCl4]H+[BF3OH]-
5.
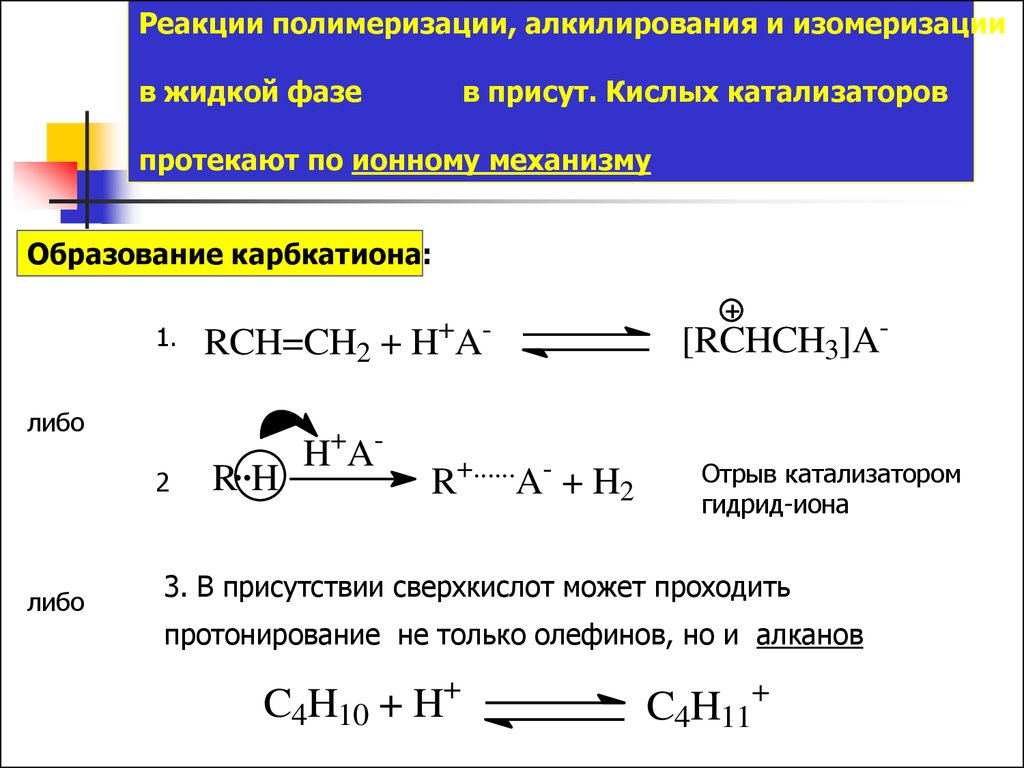
Реакции полимеризации, алкилирования и изомеризациив жидкой фазе
в присут. Кислых катализаторов
протекают по ионному механизму
Образование карбкатиона:
1.
+ -
RCH=CH2 + H A
либо
2
либо
RH
H+A-
R+......A- + H2
[RCHCH3]AОтрыв катализатором
гидрид-иона
3. В присутствии сверхкислот может проходить
протонирование не только олефинов, но и алканов
+
C4H10 + H
C4H11+
6.
Ступенчатая полимеризация олефиновПродукты: низкомолекулярные полимеры
Катализаторы в пром-ти: фосфорная кислота, цеолиты
Полимеризация
изо-бутилена
CH3
CH2
H2C=C-CH3 + C-CH3
CH3
CH3
H2C=C-CH2-C-CH3
CH3
CH3
Гидрированием смеси изо-октиленов можно получить изо-октан
7.
Механизм ступенчатой полимеризацииH2C=C-CH3 + H
CH3
CH3
CH3
CH3
H3C C + H2C=C-CH3
CH3
H3C-C-CH3
CH3
H3C-C-CH2-C-CH3
CH3
CH3
Может далее
присоединяться
к олефину
либо стабилизироваться
8.
Стабилизацияза счет отщепления протона
CH3
H3C-C-CH2-C=CH2
CH3
H3CCCH2CCH3
CH3 CH3
-H
CH3
(80%)
CH3
CH3
H3C-C-CH=C-CH3
CH3
CH3
(20%)
9.
ПРОЦЕССЫ АЛКИЛИРОВАНИЯАЛКИЛИРОВАНИЕМ называют процессы введения алкильных групп в
молекулы органических и некоторых неорганических веществ
C C C
10.
КЛАССИФИКАЦИЯ РЕАКЦИЙ АЛКИЛИРОВАНИЯ ПО ТИПУ СУБСТРАТА1. Алкилирование по атому углерода (С-алкилирование) состоит в замещении атома водорода,
находящегося при углеродном атоме на алкильную группу.
CnH2n+2
CmH2m
RCl
CmH2mHn+m+2
AlCl3
R
HCl
2. Алкилирование по атомам кислорода и серы (О- и S-алкилирование) – это реакция, в
результате которой алкильная группа связывается с атомами О или S
ArOH
RCl
NaSH
NaOH
RCl
NaCl
ArOR
RSH
H2O
NaCl
3. Алкилирование по атому азота (N-алкилирование) состоит в замещении атомов водорода
в аммиаке или аминах на алкильные группы
ROH
NH3
RNH2
H2O
RCl
NH3
RNH2
HCl
4. Алкилирование по атомам других элементов (Si-, Pb-, Al-алкилирование).
Алкильная группа связывается непосредственно с гетероатомом
2RCl
3C3H6
Al
Si
H2
R2SiCl2
(C3H8)3Al
11.
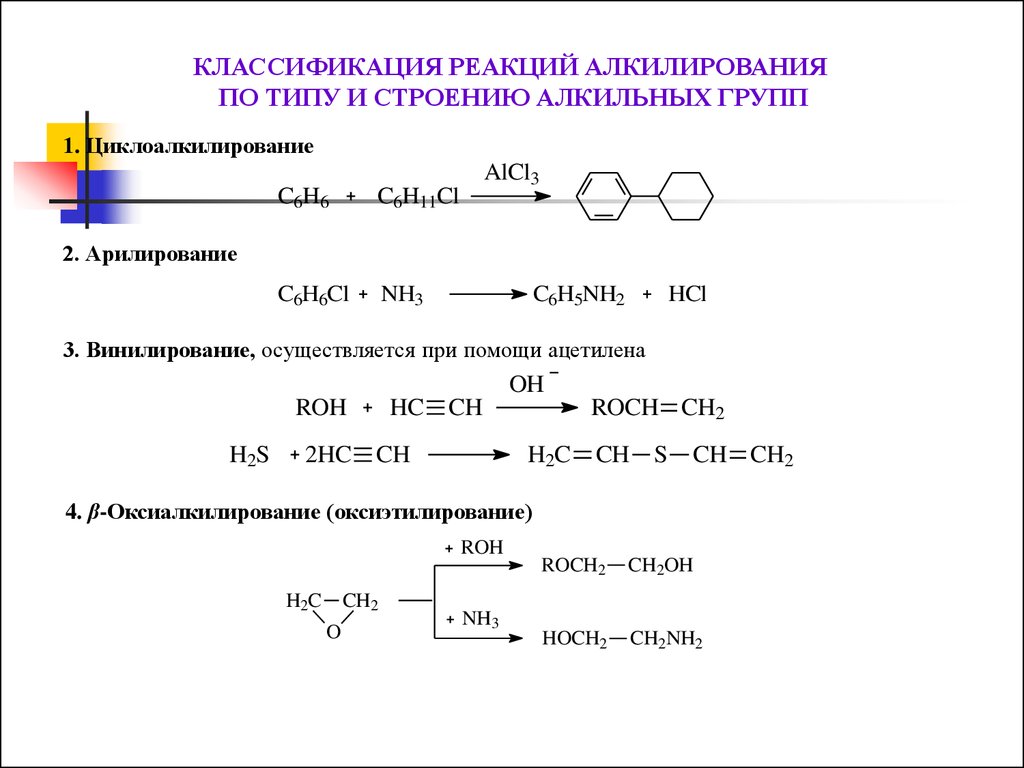
КЛАССИФИКАЦИЯ РЕАКЦИЙ АЛКИЛИРОВАНИЯПО ТИПУ И СТРОЕНИЮ АЛКИЛЬНЫХ ГРУПП
1. Циклоалкилирование
C6H6
C6H11Cl
C6H6Cl
NH3
AlCl3
2. Арилирование
C6H5NH2
HCl
3. Винилирование, осуществляется при помощи ацетилена
OH
ROH
H2S
2HC
HC
CH
CH
ROCH CH2
H2C
CH
S
CH CH2
4. β-Оксиалкилирование (оксиэтилирование)
ROH
H2C
CH2
O
NH3
ROCH2
CH2OH
HOCH2
CH2NH2
12.
КЛАССИФИКАЦИЯ АЛКИЛИРУЮЩИХ АГЕНТОВ ПО ТИПУ СВЯЗИ1. Ненасыщенные соединения (олефины и ацетилен). Применимы для С-алкилирования
парафинов и ароматических соединений. Алкилирование протекает по ионному механизму.
RCH CH2
H
RCH CH3
Реакционная способность олефинов определяется склонностью к образованию ионов карбония.
CH2 CH2 < CH3 CH CH2 < CH3 CH2 CH CH2 < (CH3)2C CH2
Под влиянием Т, hν и инициаторов алкилирование протекает по радикальному механизму
2. Хлорпроизводные соединения. Пригодны для С-, О-, S- и N-алкилирования.
а. Электрофильное замещение (характерно для С-алкилирования)
RCl AlCl3
R Cl AlCl3
R
AlCl4
б. Нуклеофильное замещение атома Cl
RCl
NH3
RNH3
Cl
RNH2
HCl
в. Свободнорадикальный механизм
4 PbNa
4 C2H5Cl
hv
4 Pb
4 NaCl
4 C2H5
4 NaCl
3. Спирты и простые эфиры. Пригодны для С-, О-, S- и N-алкилирования.
Для разрыва связи С-О требуются катализаторы кислотного типа
R OH
H
R OH2
R
H2O
Pb(C2H5)4 3Pb
13.
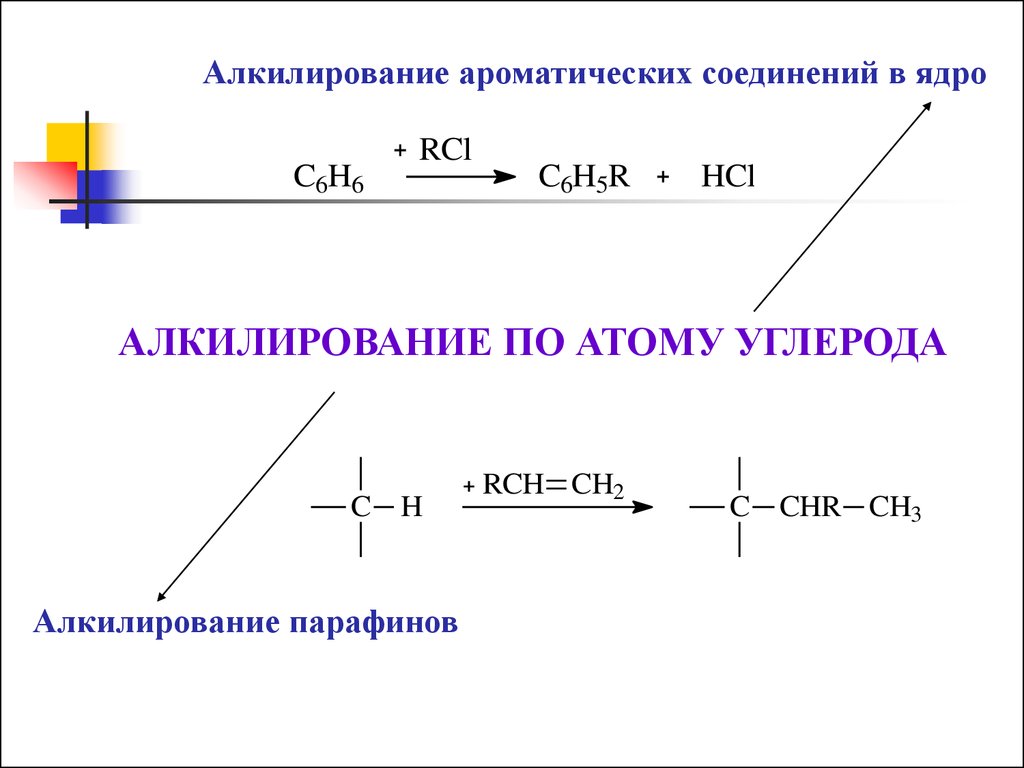
Алкилирование ароматических соединений в ядроC6H6
RCl
C6H5R
HCl
АЛКИЛИРОВАНИЕ ПО АТОМУ УГЛЕРОДА
C H
Алкилирование парафинов
RCH CH2
C CHR CH3
14.
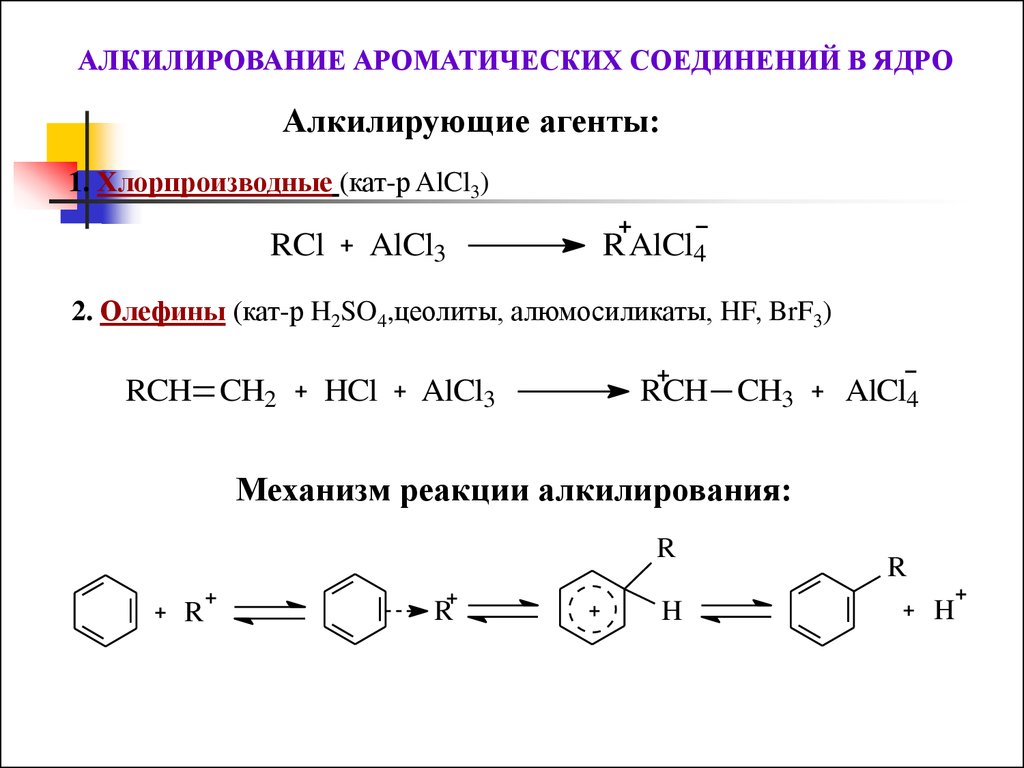
АЛКИЛИРОВАНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ В ЯДРОАлкилирующие агенты:
1. Хлорпроизводные (кат-р AlCl3)
RCl
AlCl3
RAlCl4
2. Олефины (кат-р H2SO4,цеолиты, алюмосиликаты, HF, BrF3)
RCH CH2
HCl
AlCl3
RCH CH3
AlCl4
Механизм реакции алкилирования:
R
R
R
H
R
H
15.
CH2CH3
CH2
CH CH2
H
H
CH3
CH3
CH2
PhH
Ph
CH CH3
PhH
CH2
CH3
CH3
H
CH CH3
H
Ph
(CH3)2C CH2
H
(CH3)2C CH3
PhH
(CH3)2
C CH3
Ph
H
16.
Реакции изомеризации в процессах алкилированияИзомеризация алкильной группы:
CH3
CH2
CH2
CH2
PhH
AlCl3
Cl
CH3
AlCl4
CH2
CH2
CH2
CH3
H
CH3
CH2
CH3
CH CH2
CH2
CH
CH3
PhH
CH2
CH3
CH2
CH2
CH2
CH
Ph
Изомеризация гомологов бензола:
R
R
R
R
R
R
R
R
R
R
R
R
R
R
R
R
R
R
Ph
CH3
17.
Алкилирование парафинов олефинамиПрименение: синтез высокооктановых моторных топлив
Химия процесса:
RH
CH2 CHR
RR CH CH3
T=1000C; при понижении температуры равновесие смещается вправо, а при
повышении идет крекинг
Сырье: изопарафины
Алкилирующие агенты: олефины (чаще н-бутилены)
H2SO4
(CH3)3CH н-C4H8
C8H18
компонент моторного топлива
Катализаторы: кислотного типа - H2SO4, AlCl3, HF (безводн.)
18.
Механизм реакции гетерогенный (электрофильное присоединение)осложнен реакцией изомеризации
H
CH2
CH3
CH CH2
CH CH2
CH3
CH3
(CH3)3CH
CH3
CH3
CH CH2
CH2
CH2
CH3
CH3 (CH3)3C
трет-бутилкатион
CH3
(CH3)3C
CH3
CH CH CH3
CH3
C CH CH CH3
CH3CH3
19.
CH3миграция
CH3
CH3
C CH CH
CH3
CH3
CH3
CH3
C CH CH
H
миграция
CH3CH3 CH3
CH3
CH3
C
CH3
CH3
CH3
CH3 CH3
CH3
CH3 CH3
C CH2
C
CH3
C
CH3
(CH3)3CH
CH3
(CH3)3C
CH3
трет-бутилкатион
Катионная полимеризация олефина:
H
C4H8
2C4H8
C8H16
C12H24
Подавление побочных процессов:
1. Избыток изо-парафина по отношению к олефину 4:1 – 6:1
2. Регулирование температуры H2SO4
HF
0-10 оС
20-30 оС
CH2
CH3
CH3 CH3
CH3
C CH CH
C CH CH
CH3
CH3 CH3
CH3
CH3
CH3
C CH2 CH
CH3
CH3
20.
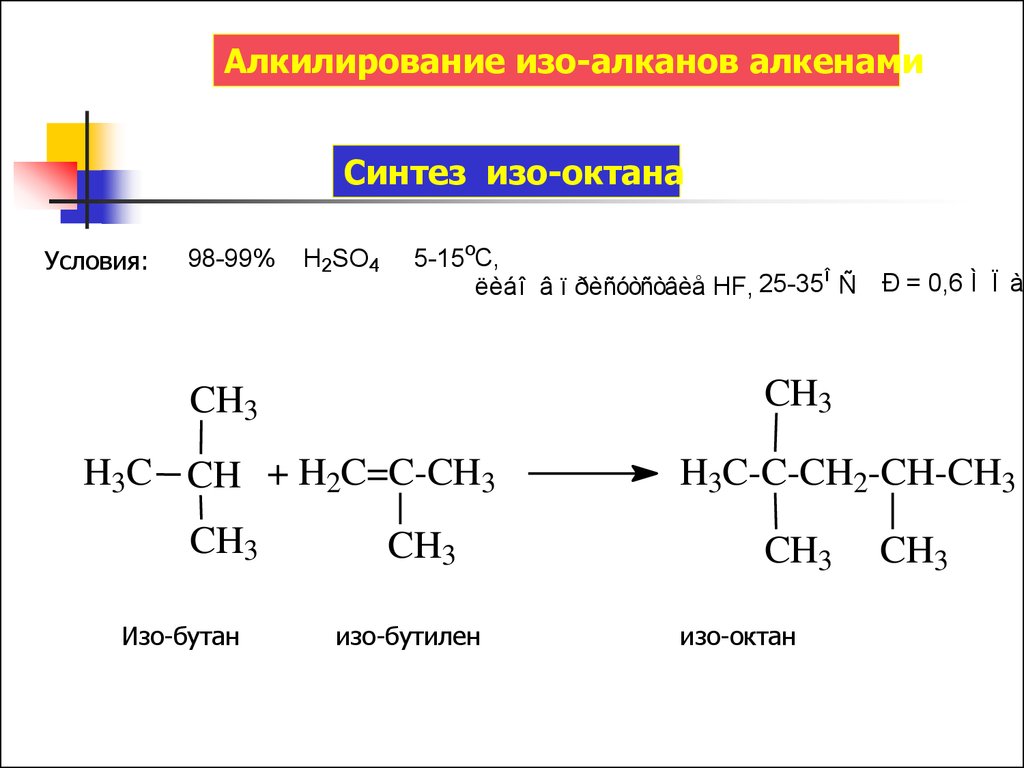
Алкилирование изо-алканов алкенамиСинтез изо-октана
Условия:
98-99%
H2SO4
5-15oC,
î
ëèáî â ï ðèñóòñòâèå HF, 25-35 Ñ Ð = 0,6 Ì Ï à
CH3
CH3
H3C CH + H2C=C-CH3
CH3
Изо-бутан
CH3
изо-бутилен
H3C-C-CH2-CH-CH3
CH3
изо-октан
CH3
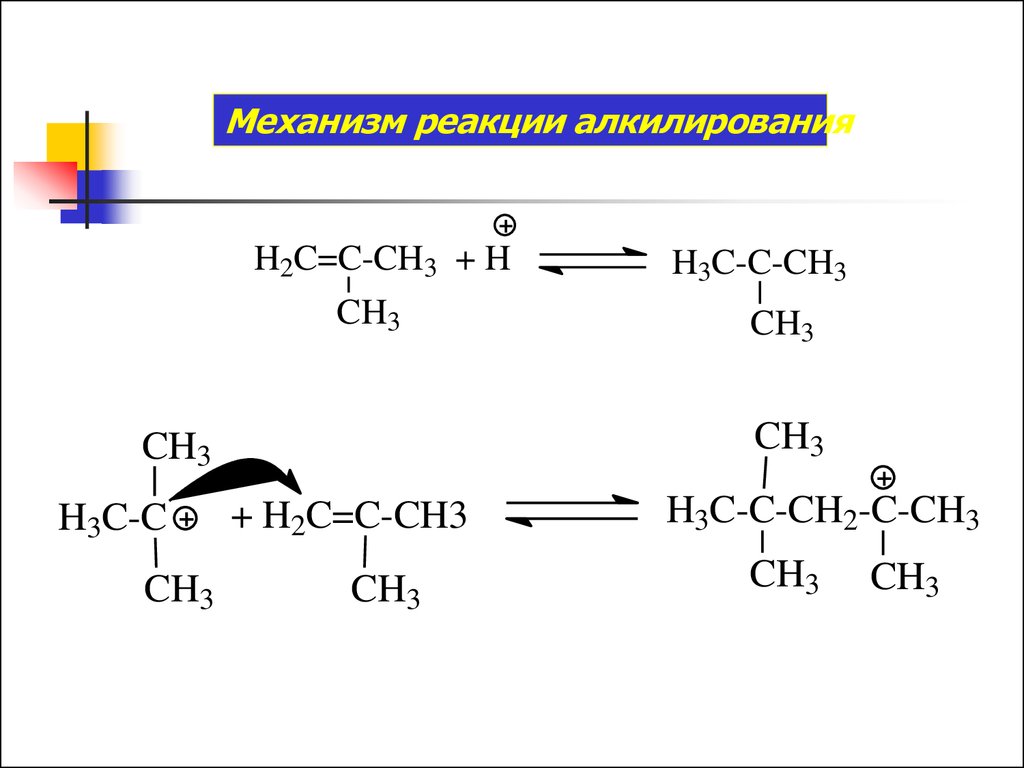
21.
Механизм реакции алкилированияH2C=C-CH3 + H
CH3
CH3
CH3
CH3
CH3
H3C-C
H3C-C-CH3
+ H2C=C-CH3
CH3
H3C-C-CH2-C-CH3
CH3
CH3
22.
CH3CH3
CH3
H3C-C-CH2-C-CH3 + H C-CH3
CH3
CH3
CH3
H3C-C-CH2-CH-CH3 + C-CH3
CH3
CH3
CH3
CH3
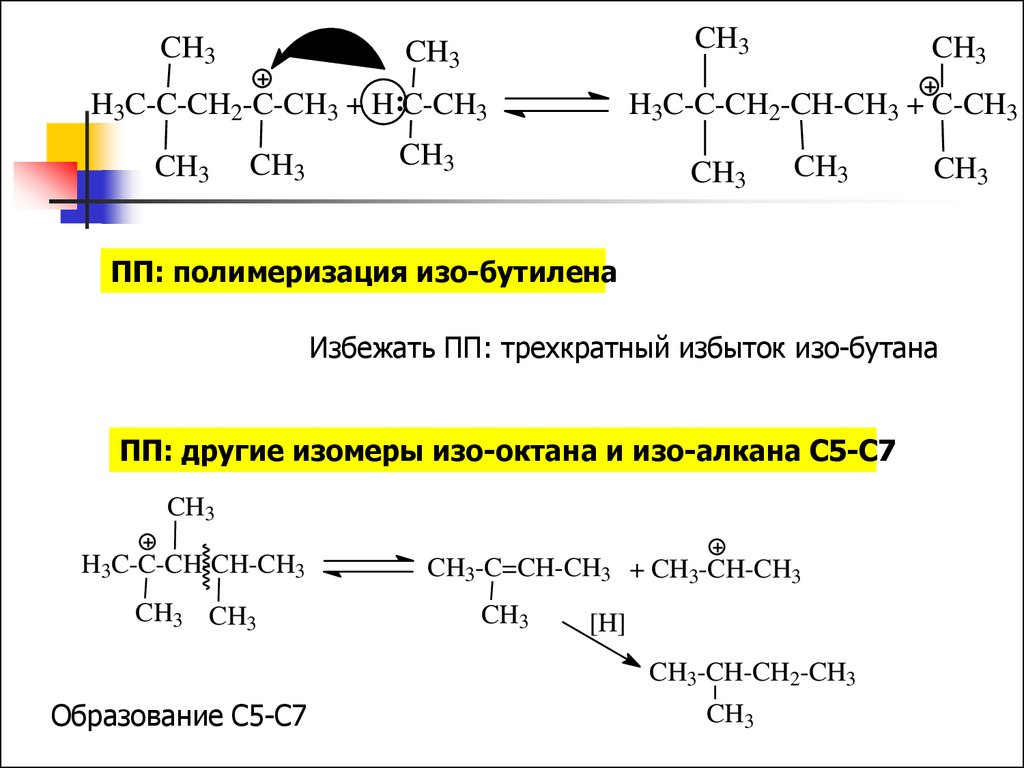
ПП: полимеризация изо-бутилена
Избежать ПП: трехкратный избыток изо-бутана
ПП: другие изомеры изо-октана и изо-алкана С5-С7
CH3
H3C-C-CH-CH-CH3
CH3 CH3
CH3-C=CH-CH3 + CH3-CH-CH3
CH3
[H]
CH3-CH-CH2-CH3
Образование С5-С7
CH3
23.
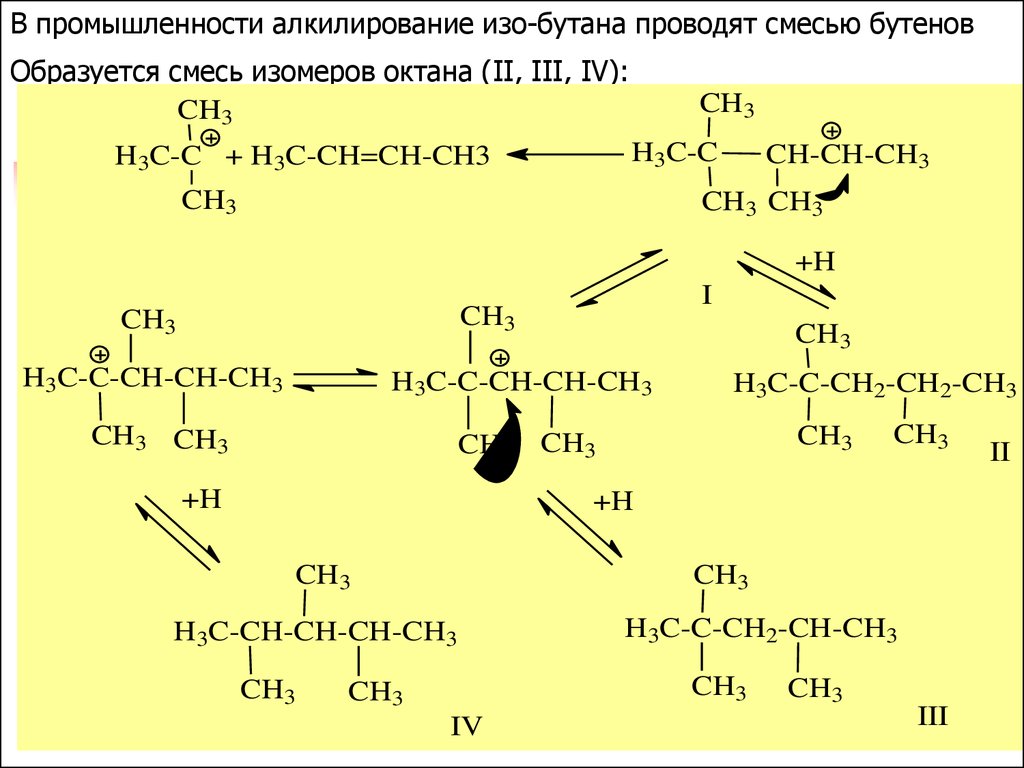
В промышленности алкилирование изо-бутана проводят смесью бутеновОбразуется смесь изомеров октана (II, III, IV):
CH3
CH3
H3C-C
H3C-C + H3C-CH=CH-CH3
CH3
CH-CH-CH3
CH3 CH3
+H
I
CH3
CH3
CH3
H3C-C-CH-CH-CH3
H3C-C-CH-CH-CH3
CH3 CH3
CH3 CH3
+H
H3C-C-CH2-CH2-CH3
CH3
CH3
+H
CH3
CH3
H3C-CH-CH-CH-CH3
CH3
H3C-C-CH2-CH-CH3
CH3
CH3
IV
CH3
III
II
24.
Синтез триптана, неогексана,2,3- диметилбутана
Триптан (изомер гептана) – образуется при каталитическом
алкилировании изобутана
пропиленом
HF, 10oC èçáû òî ê èçî -áóòàí à
H
H3C-C=CH2 + H
CH3
H3C-C H + CH3CHCH3
CH3
CH3-CH-CH3
CH3
H3C-C
+
CH3
CH3CH2CH3
25.
CH3CH3
+ H2C=CH-CH3
H3C C
H3C-C-CH2-CH-CH3
CH3
CH3
(CH3)3C H
H 3C
CH3
H3C-C-CH2-CH2-CH3 + (CH3)3C
H3C-C-CH-CH2-CH3
CH3
H3C
H 3C
CH3
H3C-CH-CH-CH2-CH3 + (CH3)3C
H3 C CH3
i-C4H10
H3C-C-CH-CH-CH3
2,2- и 2,3-диметилпентаны - основные продукты реакции
26.
Образование триптана объясняется схемой:CH3
CH3
H3C-C-CH2-CH-CH3
CH3
H3C-C-CH-CH2-CH3
CH3
H3C
CH3
H3C-C-CH-CH2
H3C-C-C-CH3
H3C CH3
H3C
CH3
H3C-C-C-CH3 + H C-CH3
H3C CH3
CH3
H3C CH3
H3C
CH3
H3C-C-CH-CH3 + H3C-C
H3C CH3
CH3
27.
Получение 2,3- диметилбутана каталитическим алкилированиемизо-бутана этиленом
CH3
CH3
H3C-CH + H2C=CH2
H3C-CH-CH-CH3
CH3
Механизм:
CH3
H3C-C
CH3
CH3
+ H2C=CH2
H3C-C-CH2-CH2
CH3
CH3
CH3
CH3
H3C-C-CH-CH3
H3C-C-CH-CH3
CH3
CH3
CH3
CH3
H3C-C-CH-CH3 + H . .C-CH3
CH3
CH3
CH3
H3C-C-CH-CH3 + (CH3)3C
H CH3
28.
Триптанможно получить
термическим алкилированием зо-бутана пропиленом:
CH3
H3C-CH + H2C=CH-CH3
CH3
Неогексан
t,P
CH3
H3C-C-CH-CH3
H3C CH3
можно получить
термическим алкилированием изо-бутана
CH3
H3C-CH + H2C=CH2
CH3
P,t
этиленом:
CH3
H3C-C-CH2-CH3
CH3
29.
Механизм термического алкилированияРадикальный
CH3
H3C-C . . H
CH3
CH3
H3C-C . + . H
CH3
CH3
H. . C-CH3
CH3
CH3
H3C-C
+ H2C=CH2
H3C-C-CH2-CH2
CH3
CH3
CH3
H3C-C-CH2-CH3 + C-CH3
CH3
CH3
30.
Изомеризация алкановВ промышленности цель изомеризации –
получение н.м. изо-алканов,
Либо низкозастывающих слаборазветвленных
высших алканов
Пути использования Н.м. изо-алканов
1. н.м. изо-алканы добавляют к авт. бензинам для повышения Ок
2. Сырье для получения изо-бутилена и изо-пропилена
Пути использования высших изо-алканов
1. Получают компоненты высококач. смазочных масел с высоким
индексом вязкости
2. Компоненты реактивных и дизельных топлив
3. Низкозастывающие дизельные топлива
31.
Условия изомеризацииКатализаторы изомеризации в промышленности:
AlCl3 или
Бифункциональные (Pt на цеолите или окиси Al
НСl и олефины применяют в качестве промоторов:
HCl + AlCl3
H+[AlCl4]-
Роль олефина как промотора - в образовании карбкатиона
Низкотемпературная изомеризация –
Термодинамически обеспечивается боле
и образование сильноразветвленных изо
32.
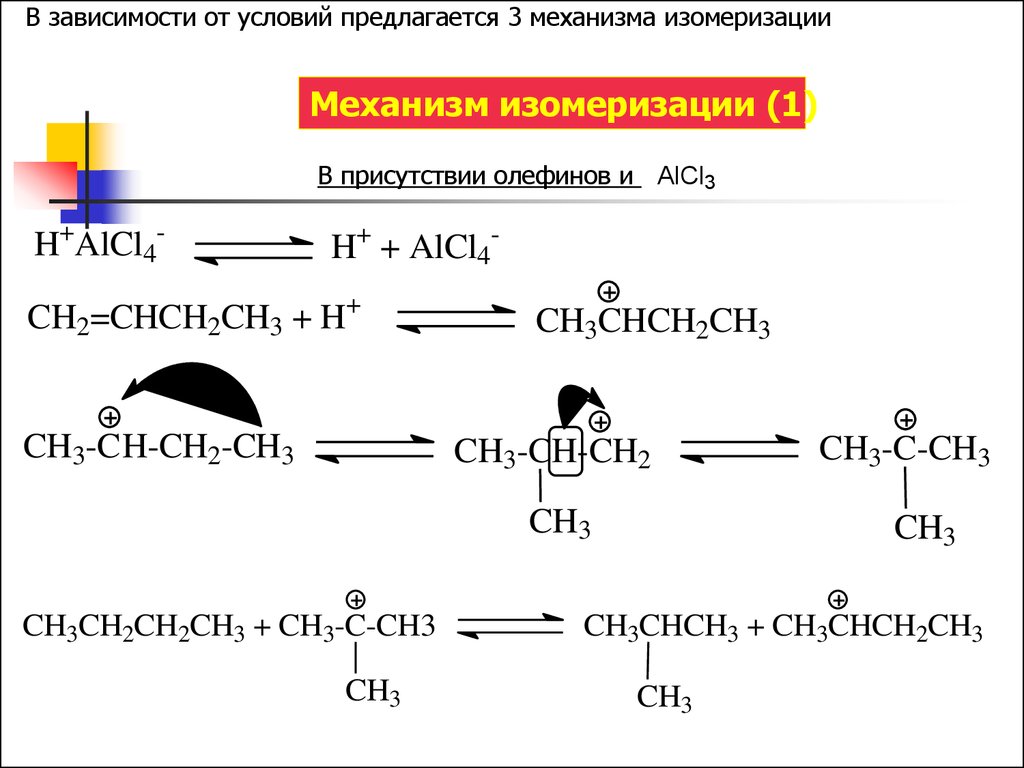
В зависимости от условий предлагается 3 механизма изомеризацииМеханизм изомеризации (1)
В присутствии олефинов и AlCl3
H+AlCl4-
H+ + AlCl4-
CH2=CHCH2CH3 + H+
CH3-CH-CH2-CH3
CH3CHCH2CH3
CH3-CH-CH2
CH3
CH3CH2CH2CH3 + CH3-C-CH3
CH3
CH3-C-CH3
CH3
CH3CHCH3 + CH3CHCH2CH3
CH3
33.
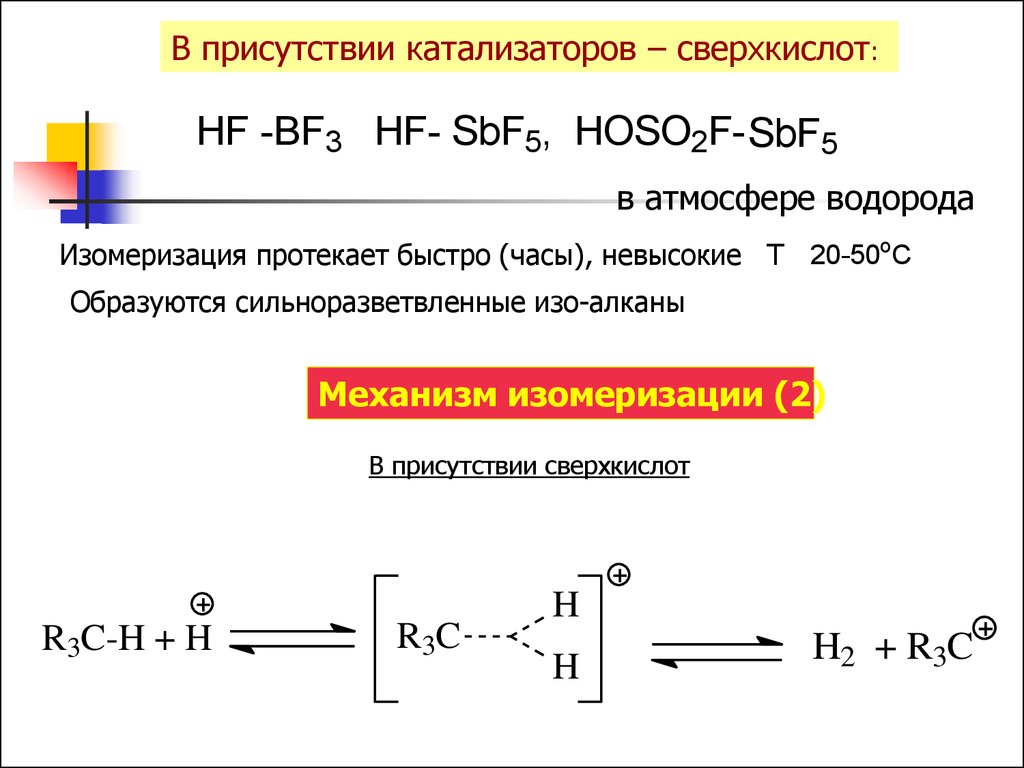
В присутствии катализаторов – сверхкислот:HF -BF3 HF- SbF5, HOSO2F- SbF5
в атмосфере водорода
Изомеризация протекает быстро (часы), невысокие Т 20-50oC
Образуются сильноразветвленные изо-алканы
Механизм изомеризации (2)
В присутствии сверхкислот
R3C-H + H
R3C
H
H
H2 + R3C
34.
Катион-радикальный механизм изомеризации (3)В присутствии цеолитов
e
CH3CH2CH2CH2CH3
kt
H3C-CH2CH2
H3CCH2CH2CH2CH3
CH2CH3
H
CH2CH3
H 3C
H 3C
CH2
CH2CH3
CHCH2CH3
H 3C
H 2C
H3C-CHCH2CH3
CH3
+e
35.
Изомеризация высших алкановГидроизомеризация
1. Получают компоненты высококач. смазочных масел с высоким
индексом вязкости
2. Компоненты реактивных и дизельных топлив
3. Низкозастывающие дизельные топлива
Сырье: парафины, гачи, петролатумы,
фракции прямой гонки высокопарафинистых нефтей
Условия: бифункциональные катализаторы
температура 350-470oC
Давление водорода 2-7 МПа
Наряду с изомеризацией протекает гидрирование аренов и гидроочистка
36.
Изомеризация высш.алканов на бифункциональных катализаторахпротекает с участием дегидрирующих (Pt)
и кислотных (носитель) центров
П.П. – реакция крекинга
протекает в результате распада карбкатионов
Отношение (Изомеризация / Крекинг) уменьшается с ростом М.М. алкана
Для подавления П.П. реакцию проводят при возможно низких Т
и повышенных давлениях водорода



























 Физика
Физика Химия
Химия








