Похожие презентации:
Окислительно- восстановительные реакции
1. Окислительно- ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
2.
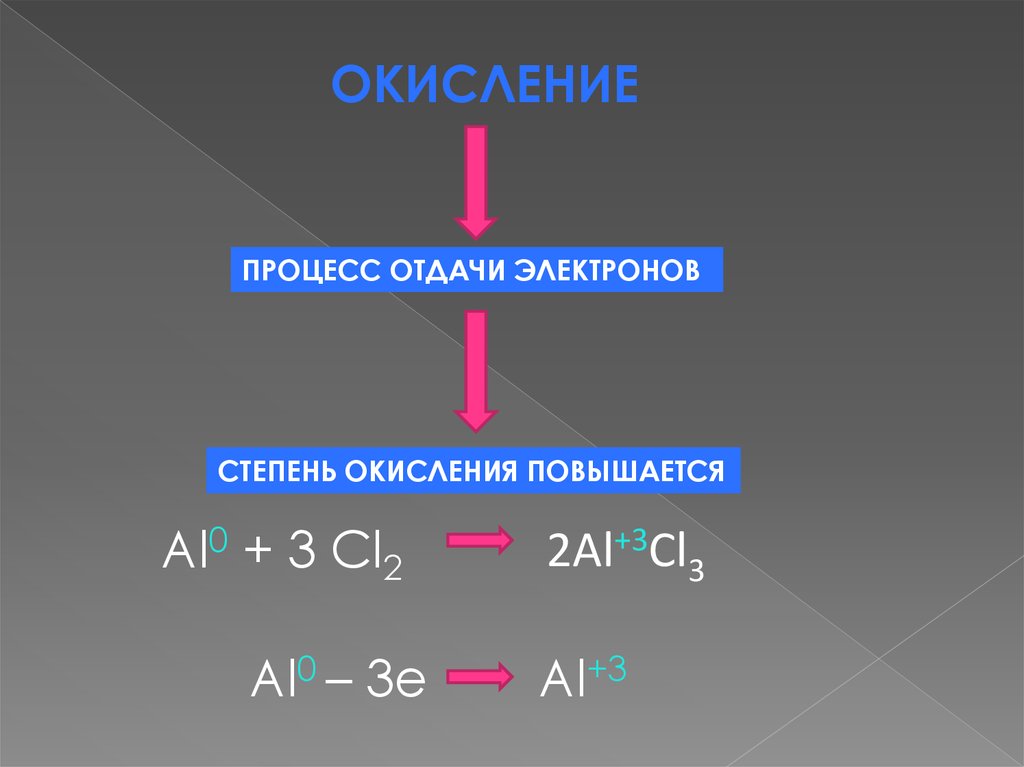
ОКИСЛЕНИЕПРОЦЕСС ОТДАЧИ ЭЛЕКТРОНОВ
СТЕПЕНЬ ОКИСЛЕНИЯ ПОВЫШАЕТСЯ
Al0 + 3 Cl2
Al0 – 3e
2Al+3Cl3
Al+3
3.
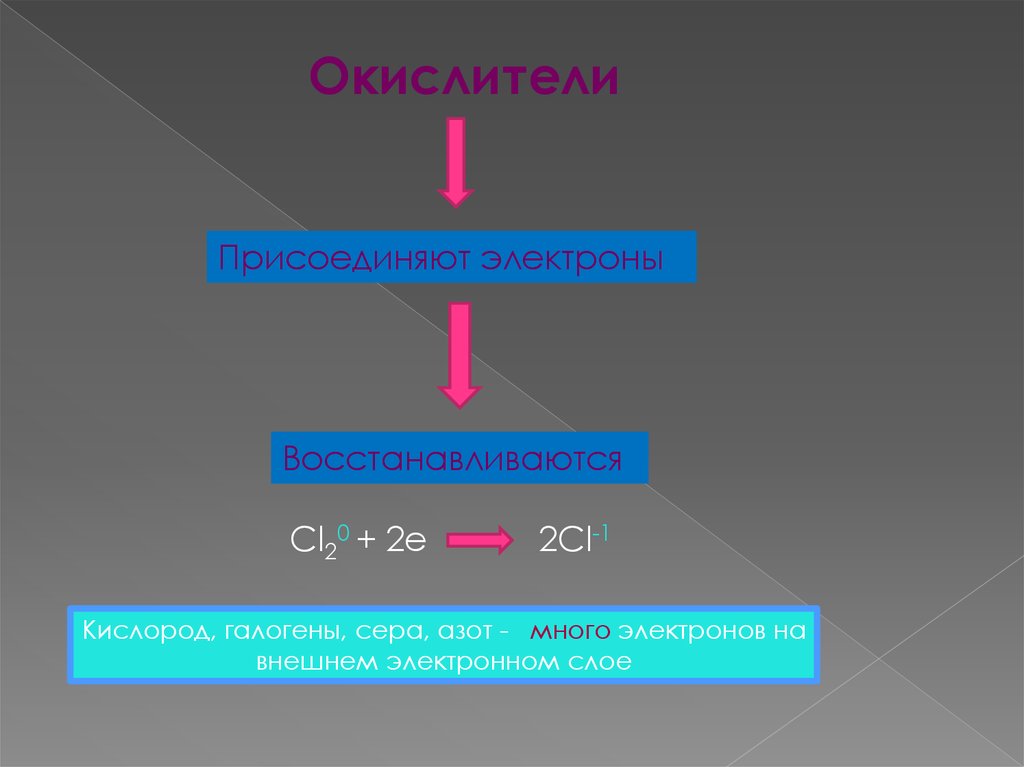
ОкислителиПрисоединяют электроны
Восстанавливаются
Cl20 + 2e
2Cl-1
Кислород, галогены, сера, азот - много электронов на
внешнем электронном слое
4.
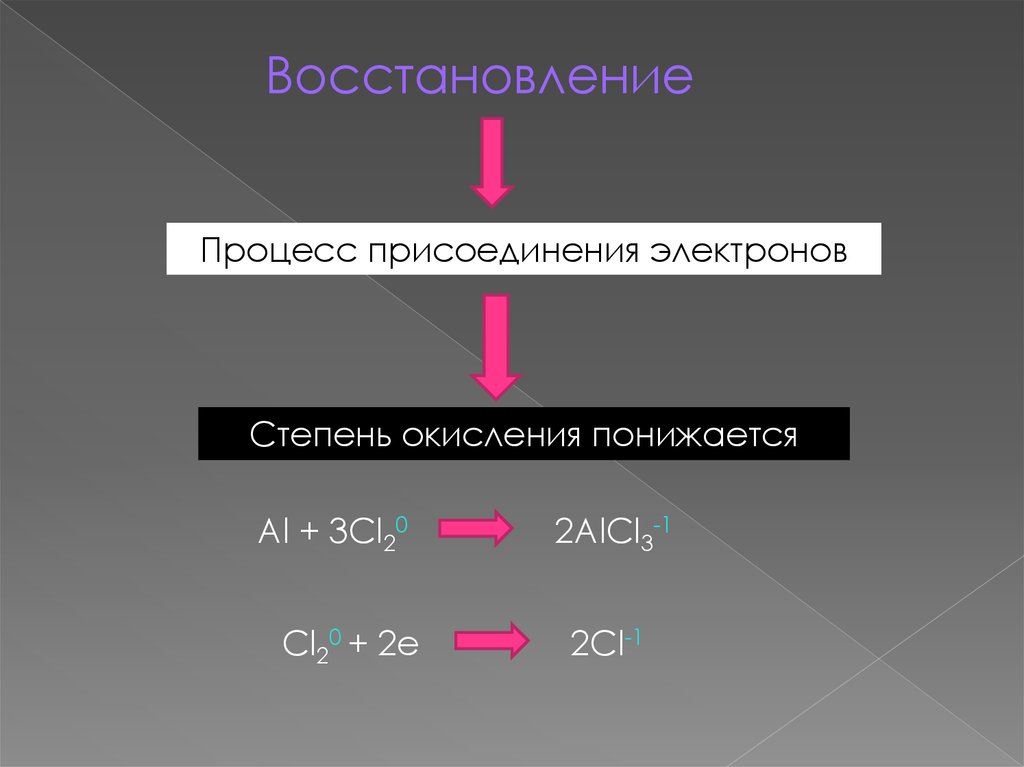
ВосстановлениеПроцесс присоединения электронов
Степень окисления понижается
Al + 3Cl20
Cl20 + 2e
2AlCl3-1
2Cl-1
5.
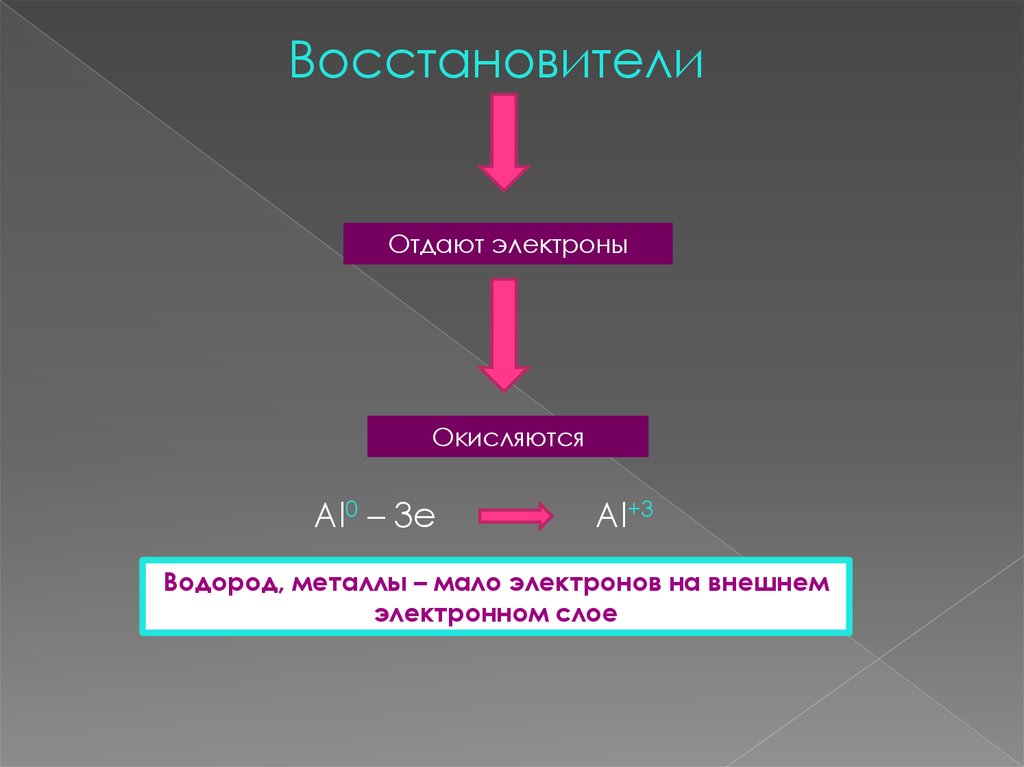
ВосстановителиОтдают электроны
Окисляются
Al0 – 3e
Al+3
Водород, металлы – мало электронов на внешнем
электронном слое
6. ОВР-окислительно-восстановительные реакции
Реакции в которых происходит изменениестепени окисления
Zn0+2H+1 Cl Zn+2 Cl2+H20
Zn0 -2e
Zn +2
Восстановитель,
окисляется , окисление
+1
0
2H + 2e
H
Окислитель
Восстанавливается
Восстановление
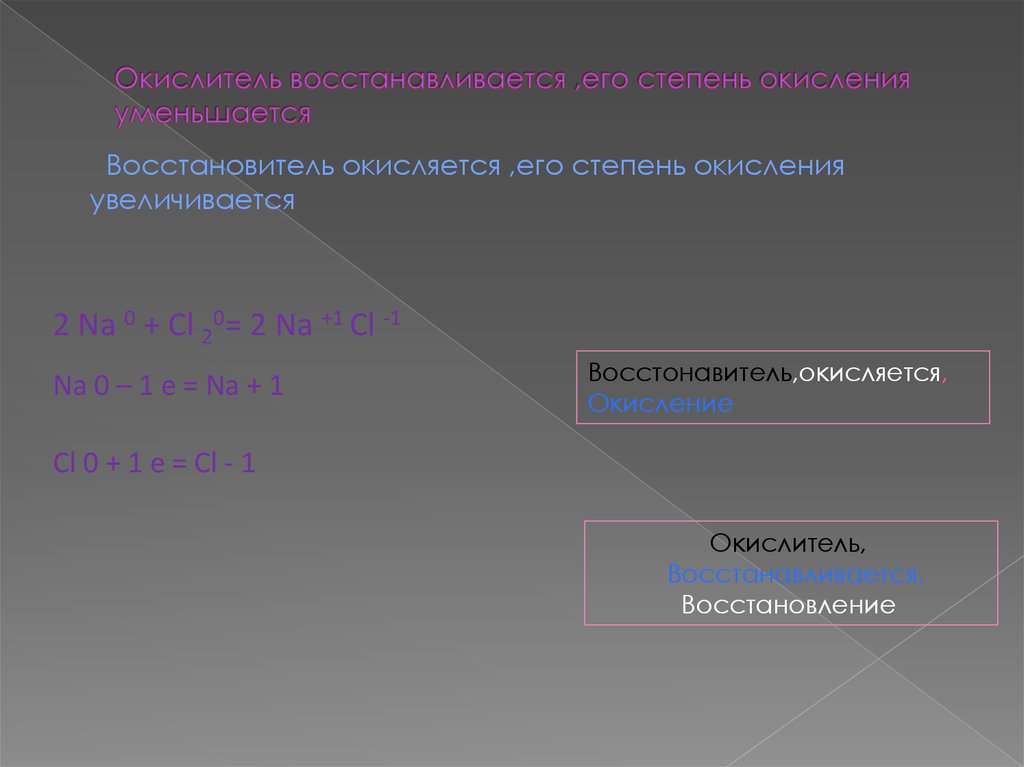
7. Окислитель восстанавливается ,его степень окисления уменьшается
Восстановитель окисляется ,его степень окисленияувеличивается
2 Nа 0 + Cl 20= 2 Nа +1 Cl -1
Na 0 – 1 e = Na + 1
Восстонавитель,окисляется,
Окисление
Cl 0 + 1 e = Cl - 1
Окислитель,
Восстанавливается,
Восстановление


 Химия
Химия








