Похожие презентации:
Свободные радикалы и болезни человека
1. Свободные радикалы и болезни человека
Биофизические основыпатологии клетки
Свободные радикалы и болезни человека
Ю.А. Владимиров, А.Н. Осипов
2018
2. Фосфолипазы
Фосфолипаза В работает как сумма фосфолипаз А1 и А2, т.е. гидролизуетобе сложноэфирные связи с жирнокислотными остатками R1 и R2.
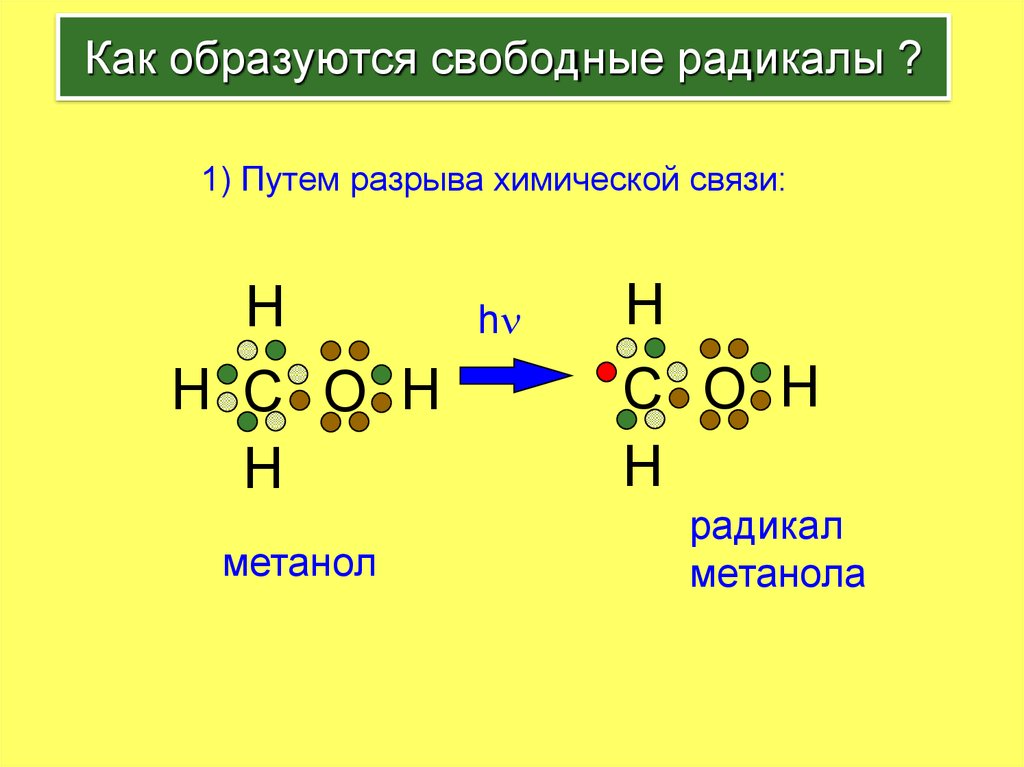
3. Как образуются свободные радикалы ?
1) Путем разрыва химической связи:H
H C O H
H
метанол
hn
H
C O H
H
радикал
метанола
4.
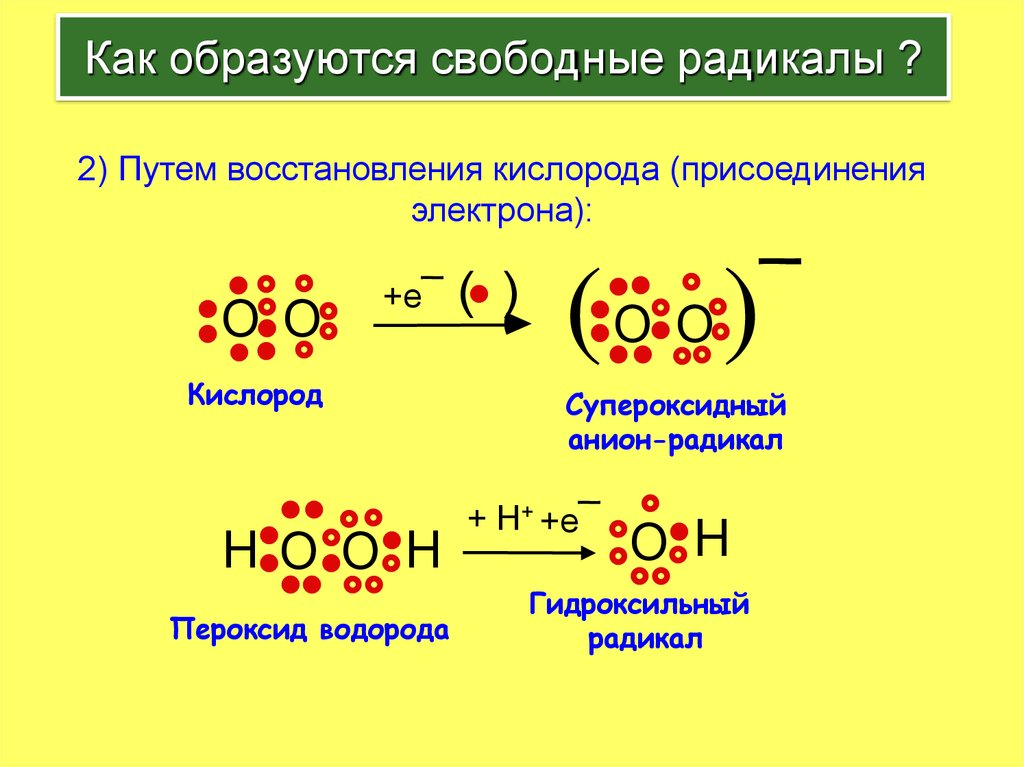
Как образуются свободные радикалы ?2) Путем восстановления кислорода (присоединения
электрона):
O O
+e¯
Кислород
HO O H
Пероксид водорода
( )
(
¯
O O
)
Супероксидный
анион-радикал
+ H+ +e¯
O H
Гидроксильный
радикал
5. Классификация свободных радикалов
Свободные радикалыПервичные
Третичные
Вторичные
Семихинонные
Супероксид
Гидроксил
Нитроксид
Радикалы
антиоксидантов
Радикалы
липидов
6. Активные формы кислорода (Reactive oxygen species, ROS)
7. Стадии последовательного одноэлектронного восстановления кислорода
O2+e-
1
O 2
H
O
2
2
+2H
+e-
+e-
+
2
3
OH- + OH
H2O
+H
+e-
+
4
8. Какие частицы относят к активным формам кислорода?
1. ●O2─супероксидный радикал
2. H2O2
пероксид водорода
3. ●OH
гидроксильный радикал
4. 1O2
синглетный кислород
5. ClO─
гипохлорит
6. ONOO─
пероксинитрит
7. NO
оксид азота
8. Радикалы липидов:
LO● (алкоксильный),
LOO● (пероксильный)
9. Метаболизм супероксидного радикала и пероксида водорода в водной среде
NADPH – оксидаза:O2 + e¯ ·O2¯
Супероксиддисмутаза (СОД): ·O2¯ + ·O2¯ + 2H+ O2 + H2O2
Глутатионпероксидаза: 2H2O2 + 2GSH 2H2O + O2 + GSSG
Каталаза: 2H2O2 2H2O + O2
Миелопероксидаза: H2O2 + Cl¯ H2O + ClO¯/HOCl
Реакция Фентона: H2O2 + Fe2+ Fe3+ + HO¯ + ·OH
Реакция c HOCl: HOCl + Fe2+ Fe3+ + Cl¯ + ·OH
10. Супероксидный радикал
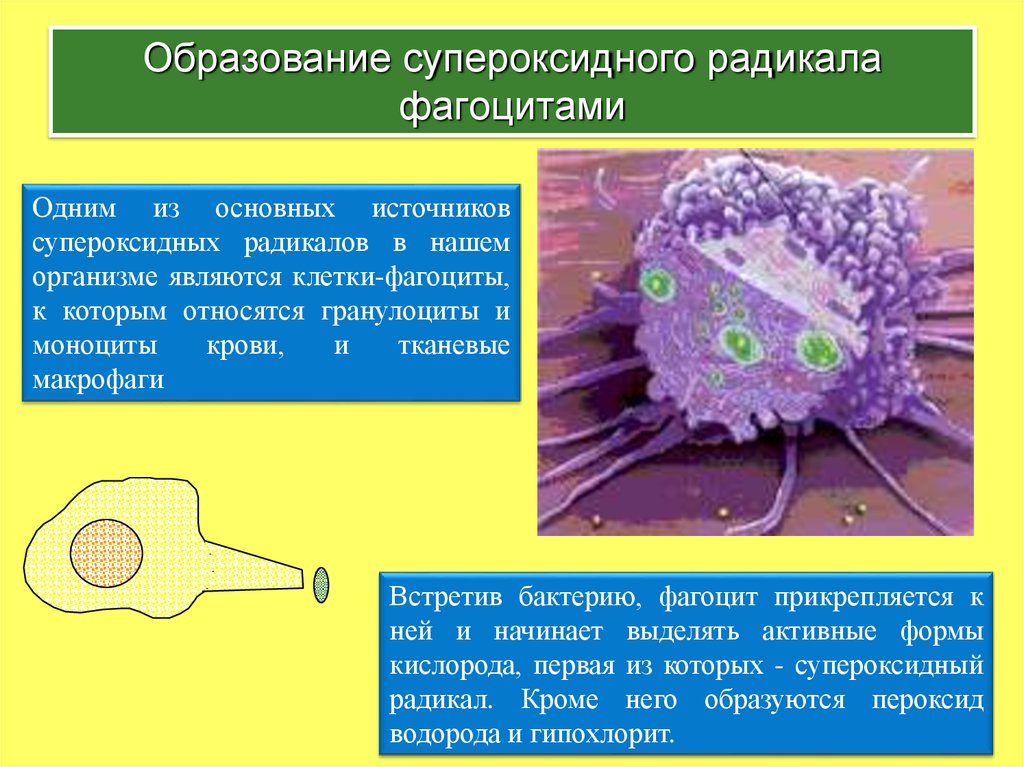
11. Образование супероксидного радикала фагоцитами
Одним из основных источниковсупероксидных радикалов в нашем
организме являются клетки-фагоциты,
к которым относятся гранулоциты и
моноциты
крови,
и
тканевые
макрофаги
Встретив бактерию, фагоцит прикрепляется к
ней и начинает выделять активные формы
кислорода, первая из которых - супероксидный
радикал. Кроме него образуются пероксид
водорода и гипохлорит.
12.
Активация фагоцита внешним стимулома
а—схематическое изображение клетки фагоцита;
1 — захват клеткой чужеродной частицы
(фагоцитоз);
2 — активация клетки химическим веществом,
например хематтрактантом;
б
б—участок клеточной мембраны;
НАДФН, образующийся при окислении глюкозы
(гексозомонофосфатный шунт), окисляется
ферментным комплексом цитоплазматической
мембраны (НАДФН-оксидазой) с образованием
супероксидных радикалов. В присутствии люминола
наблюдается интенсивная хемилюминесценция.
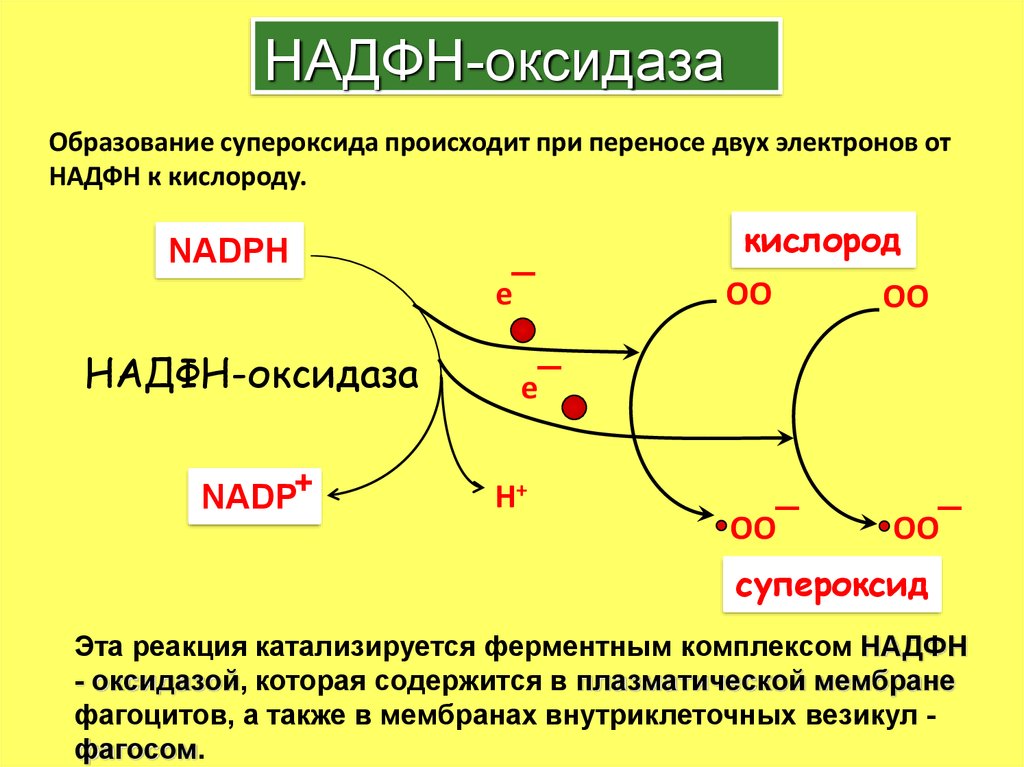
13. НАДФН-оксидаза
Образование супероксида происходит при переносе двух электронов отНАДФН к кислороду.
кислород
NADPH
e¯
НАДФН-оксидаза
NADP+
OO
OO
OO¯
OO¯
e¯
H+
супероксид
Эта реакция катализируется ферментным комплексом НАДФН
- оксидазой, которая содержится в плазматической мембране
фагоцитов, а также в мембранах внутриклеточных везикул фагосом.
14.
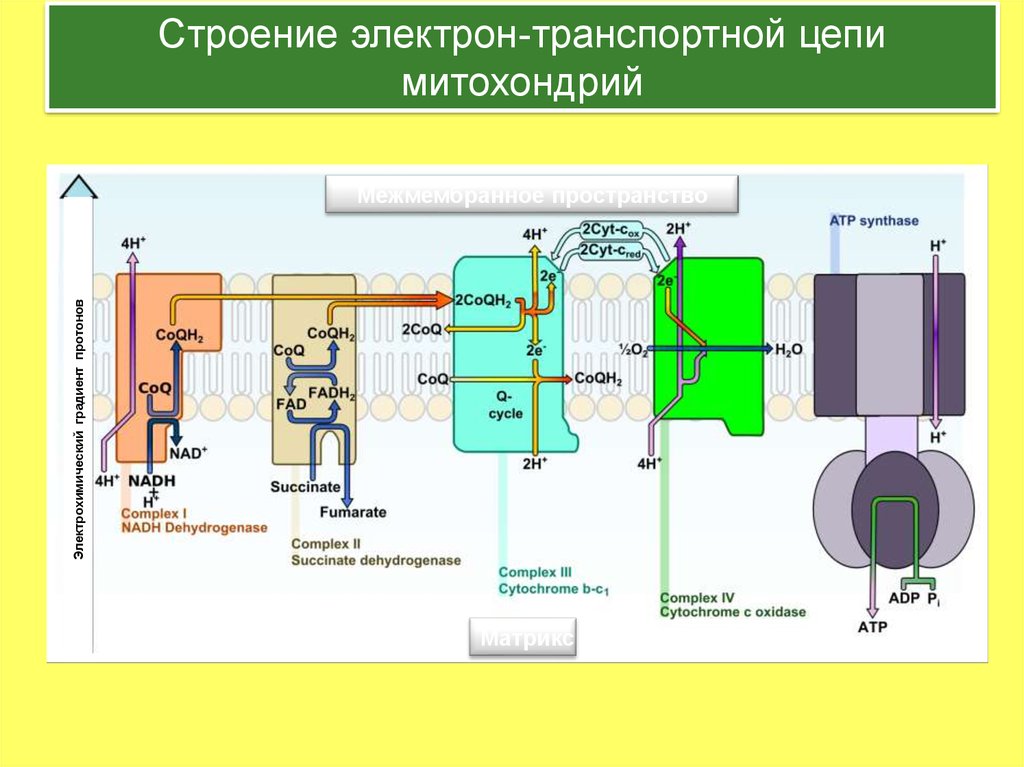
Строение электрон-транспортной цепимитохондрий
Электрохимический градиент протонов
Межмембранное пространство
Матрикс
15. Дыхательные комплексы митохондрий в норме
Образование супероксидныхрадикалов в митохондриях
Дыхательные комплексы митохондрий в норме
NAD+ + H+
Матрикс
NADH
4H+
2H2O
2e¯
IV
III
I
Q
NADH-дегидрогеназа
QH2
Цитохром c
оксидаза
Цитохром b-c1
II
e¯
C(Fe+3)
e¯
C(Fe+2)
O2
Внутренняя мембрана митохондрий
C(Fe+3)
Межмембранное пространство
Римскими цифрами обозначены дыхательные комплексы. Строчными буквами обозначены цитохромы. Комплекс II (сукцинат
дегидрогеназа) на рисунке не показан.
16. Дыхательные комплексы митохондрий при гипоксии
Образование супероксидныхрадикалов в митохондриях
NAD+ + H+
NADH
Дыхательные комплексы митохондрий при гипоксии
4H+
2e¯
I
Q
QH2
IV
III
II
e¯
C(Fe+3)
C(Fe+3)
e¯
C(Fe+2)
O2
2H2O
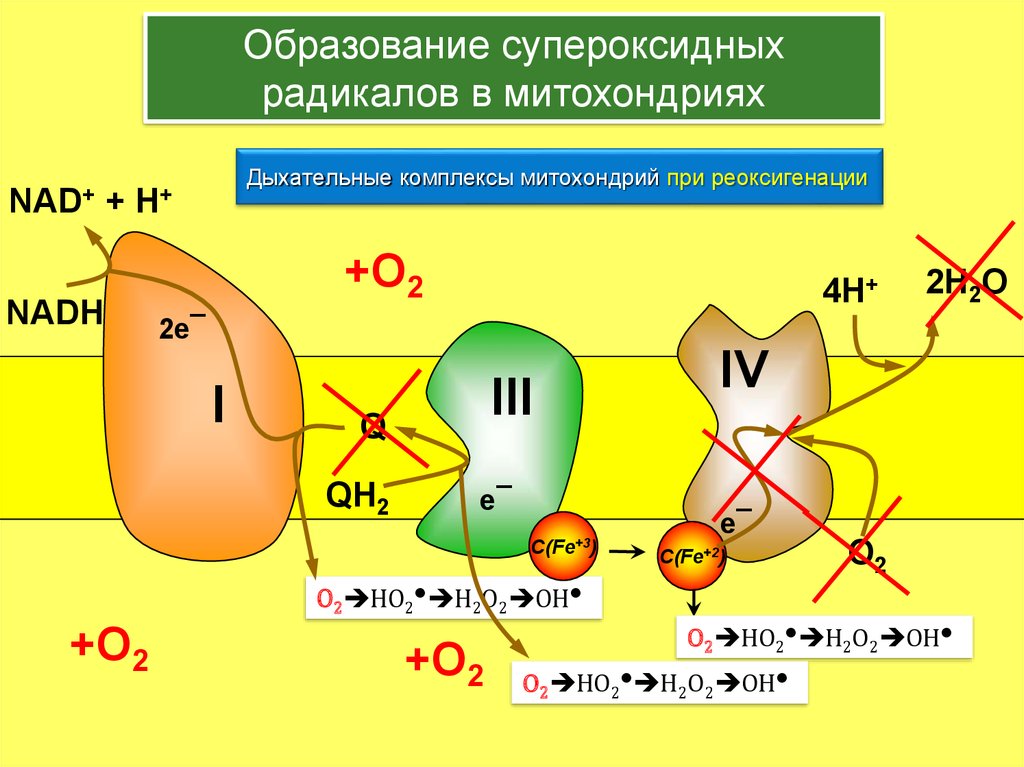
17. Дыхательные комплексы митохондрий при реоксигенации
Образование супероксидныхрадикалов в митохондриях
NAD+
+
Дыхательные комплексы митохондрий при реоксигенации
H+
NADH
+О2
4H+
2H2O
2e¯
I
III
II
Q
QH2
IV
e¯
C(Fe+3)
e¯
C(Fe+2)
O2
О2 НО2 Н2О2 ОН
+О2
+О2
О2 НО2 Н2О2 ОН
О2 НО2 Н2О2 ОН
18. Факторы, способствующие образованию супероксида митохондриями
1. Гипоксия и последующая реоксигенация2. Отравление дыхательной цепи (например цианидом)
3. Ингибирование цитохромоксидазы (например, нитроксидом)
4. Выход цитохрома c из митохондрий через мегапоры при
апоптозе
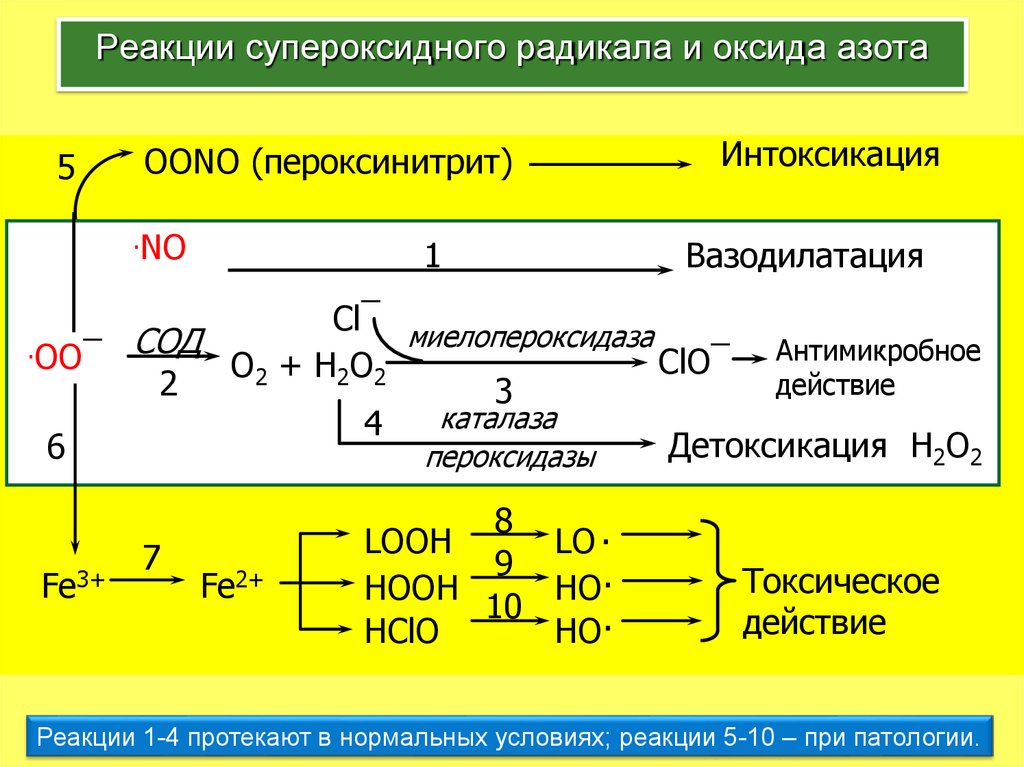
19. Реакции супероксидного радикала и оксида азота
5OONO (пероксинитрит)
.NO
1
Интоксикация
Вазодилатация
Cl¯ миелопероксидаза
.OO¯ СОД
ClO¯ Антимикробное
O2 + H2O2
действие
2
3
каталаза
4
Детоксикация H2O2
6
пероксидазы
Fe3+
7
Fe2+
8
LOOH
LO .
9
HOOH
HO.
10
HClO
HO.
Токсическое
действие
Реакции 1-4 протекают в нормальных условиях; реакции 5-10 – при патологии.
20. Синглетный кислород
1О2
21. Синглетный кислород: строение электронных оболочек
атомнаяорбиталь 1
атома
кислорода
молекулярная
орбиталь
атомная
орбиталь 2
атома
кислорода
2p-орбиталь
2p-орбиталь
2s-орбиталь
2s-орбиталь
символ
символ
триплетный кислород (основной)
синглетный кислород (химически активный)
22. Синглетный кислород: строение электронных оболочек
1О2
– является возбужденным состоянием обычного 3О2
Обычно образуется при фотохимических реакциях в присутствии
фотосенсибилизаторов
Используется при фотодинамической терапии опухолей (обычно
поверхностных, кожных).
Полифенолы (флавоноиды) и каротеноиды могут защищать клетки
от повреждающего действия 1О2.
23.
Препараты, используемые для фотодинамической терапии:Аласенс, Аминолевулиновая кислота, Гелеофор, Димегин, Радахлорин,
Фотосенс, Хлорин Е6, Фотолон, Фотогем
24.
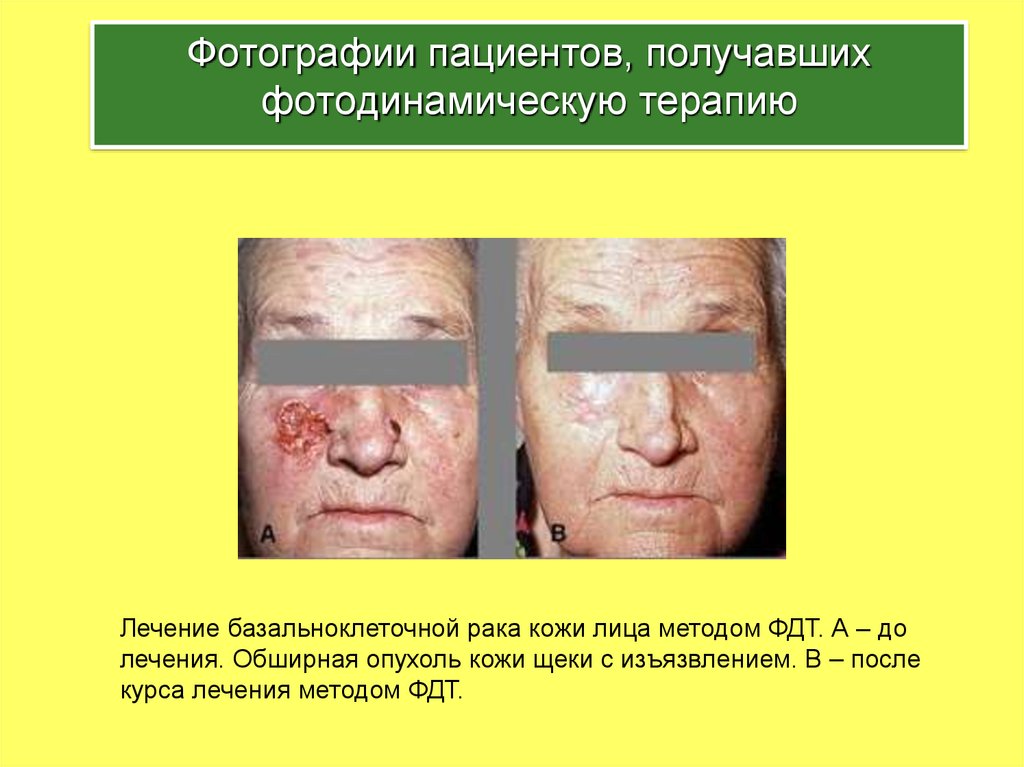
Фотографии пациентов, получавшихфотодинамическую терапию
Лечение базальноклеточной рака кожи лица методом ФДТ. А – до
лечения. Обширная опухоль кожи щеки с изъязвлением. В – после
курса лечения методом ФДТ.
25. Гипохлорит
OCl-/HOCl26. Гипохлорит
Образуется миелопероксидазой нейтрофилов из H2O2 и ClH2O2 + Cl- OCl-/HOClpK (OCl-/HOCl) = 7.5
Это означает, что при нормальном рН концентрации
OCl- и HOCl почти равны
Обладает хлорирующим действием и таким образом
разрушает бактерии и вирусы в очаге воспаления
Может образовывать ОН радикалы в реакции с ионами железа:
HOCl + Fe2+ Cl- + OH + Fe3+
27. Пероксинитрит
ONOO-28. Пероксинитрит: химические свойства
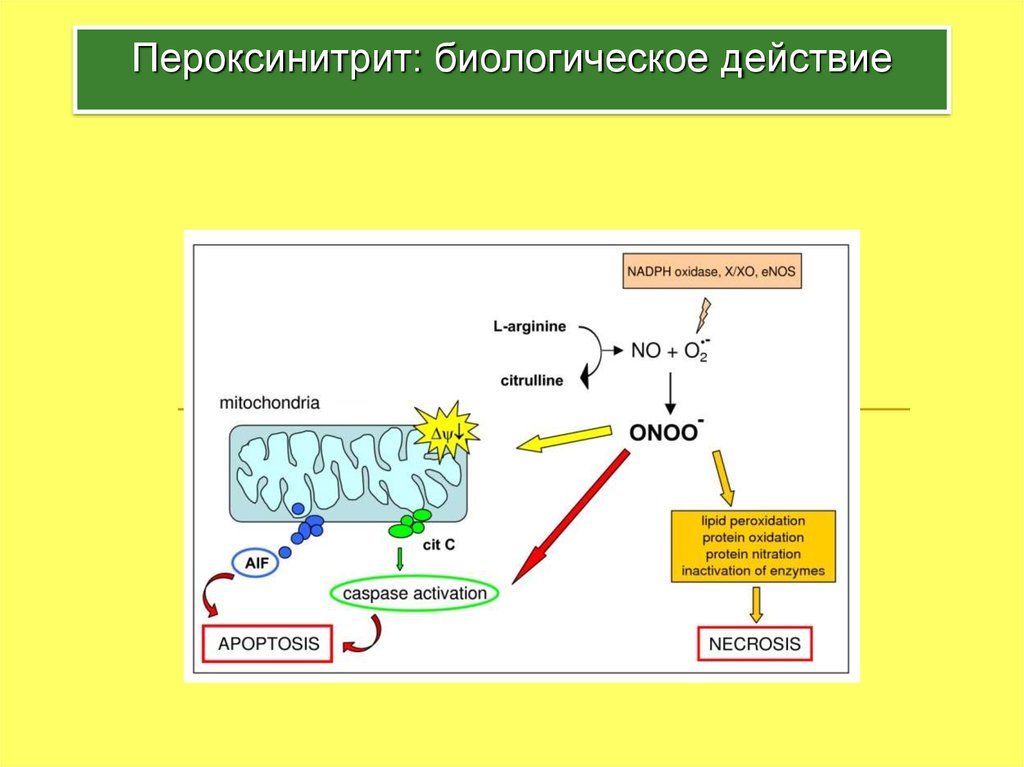
Образуется в реакции оксида азота и супероксидного радикала:NO + O2- ONOO-/ONOOH
Является сильным окислителем, может
взаимодействовать с липидами, белками и нуклеиновыми
кислотами.
ONOOH OH + NO2
ONOOH HNO3/NO3-
29. Пероксинитрит: биологическое действие
30. Оксид азота
31.
Химические свойства NON O
•участвует в процессе внутриклеточной передачи сигналов у
млекопитающих, включая человека. Он играет ключевую роль в
неврологии, физиологии и иммунологии.
•как свободный радикал - обладает высокой химической активностью. Он
легко взаимодействует с кислородом и озоном, превращаясь в двуокись
азота ( NO2) или с супероксидом, превращаясь в пероксинитрит (ONOO-).
В 1992 году Американское химическое общество присвоило
оксиду азота титул – «молекула года»
32. Химические свойства NO
1. Реакция с кислородом:2NO + O2 2NO2
2. Реакция с супероксидным радикалом:
NO + O2 - ОNOО3. Реакция с тиолами:
NO + RSH RSNO
4. Реакция с металлопротеинами:
NO + Hb(Fe3+) Hb(Fe2+)NO
33. В каких формах NO существует в организме?
Нитрозотиолы (RSNO):нитрозоцистеин (CysNO),
нитрозоглутатион (GSNO),
нитрозоальбумин (AlbNO) и др.
Нитрозометаллопротеины (Hb(Fe2+)NO):
нитрозогемоглобин (HbNO),
нитрозомиоглобин (MbNO),
нитрозоцитохром (CytNO) и др.
34. Образование NO в организме
Оксид азота синтезируется в организме из L-аргининаферментом NO-синтазой.
В организме есть 3 типа NO-синтаз (NOS):
1.
eNOS – эндотелиальная (эндотелий),
2.
nNOS – нейрональная (глиальные клетки) и
3.
iNOS – индуцибельная (тканевые макрофаги)
eNOS и nNOS активируются ионами Ca2+, в то время как
активация iNOS происходит в макрофагах в присутствии
ФНО или интерферона-g.
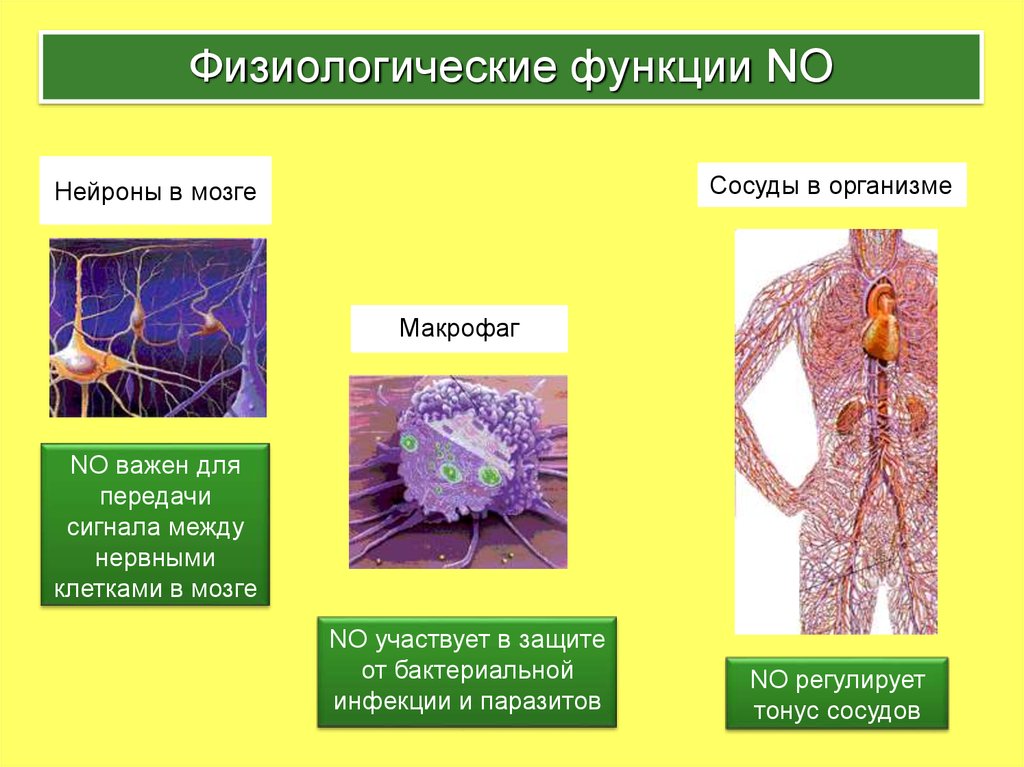
35. Физиологические функции NO
Сосуды в организмеНейроны в мозге
Макрофаг
NO важен для
передачи
сигнала между
нервными
клетками в мозге
NO участвует в защите
от бактериальной
инфекции и паразитов
NО регулирует
тонус сосудов
36.
Физиологические функции NOКроме того:
•тормозит агрегацию тромбоцитов и адгезию лейкоцитов к
эндотелию.
•может вызывать повреждения при гипокии-реперфузии: при
гипоксии синтезируется много оксида азота, а при
реперфузии появляется супероксид, который реагируя с
оксидом азота, образует токсичный пероксинитрит
37.
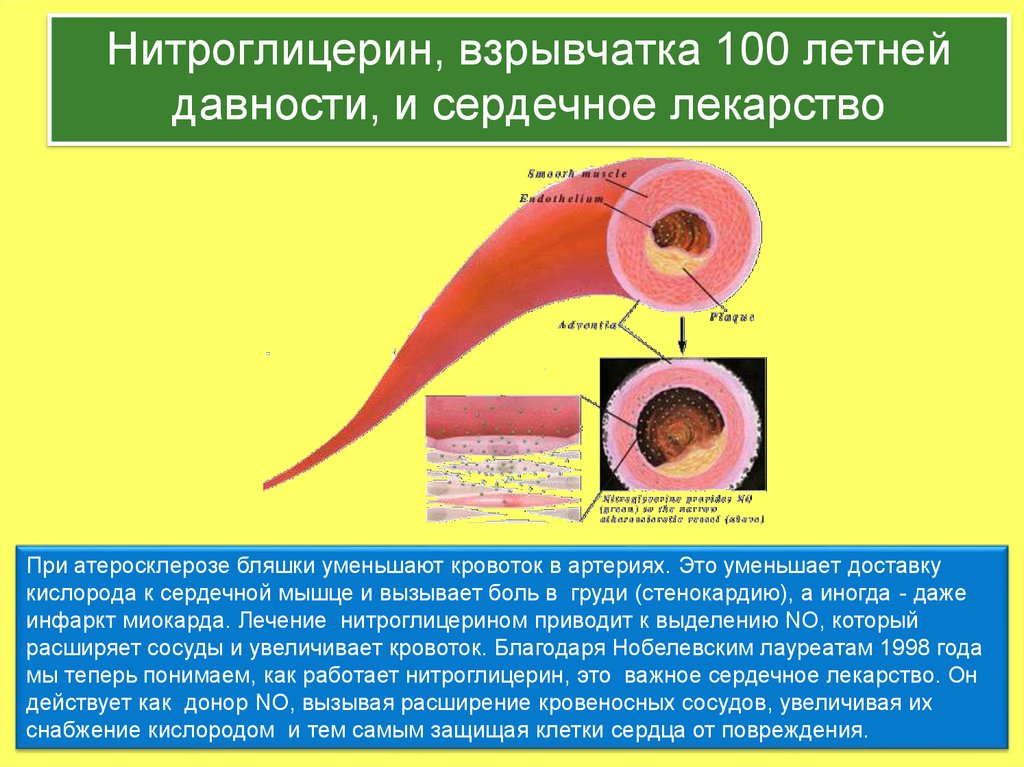
Схема образования NO в сосудах и тканях38. Нитроглицерин, взрывчатка 100 летней давности, и сердечное лекарство
При атеросклерозе бляшки уменьшают кровоток в артериях. Это уменьшает доставкукислорода к сердечной мышце и вызывает боль в груди (стенокардию), а иногда - даже
инфаркт миокарда. Лечение нитроглицерином приводит к выделению NO, который
расширяет сосуды и увеличивает кровоток. Благодаря Нобелевским лауреатам 1998 года
мы теперь понимаем, как работает нитроглицерин, это важное сердечное лекарство. Он
действует как донор NO, вызывая расширение кровеносных сосудов, увеличивая их
снабжение кислородом и тем самым защищая клетки сердца от повреждения.
39. Нобелевская Премия по Физиологии и Медицине 1998
"за открытие касающееся окиси азота как сигнальной молекулы в сердечно-сосудистой системе"Роберт Фуршготт,
Родился в 1916. Работает в Отд.
Фармакологии,
SUNY Health Science Center
New York
Луис Иньяро, Родился
в 1941.
Работает в Отд. Молекулярной
фармакологии, UCLA School of
Medicine, Los Angeles
Ферид Мурад,
Родился в 1936. Работает в
Отд. Интегративной биологии,
фармакологии и физиологии,
University of Texas Medical
School, Houston
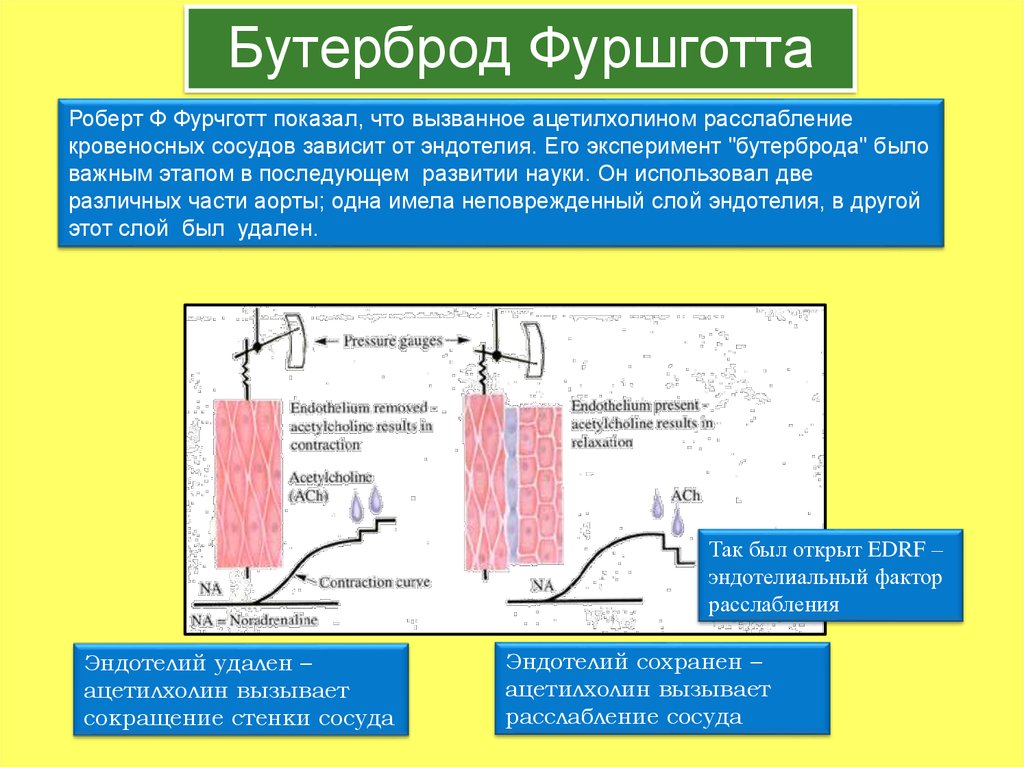
40. Бутерброд Фуршготта
Роберт Ф Фурчготт показал, что вызванное ацетилхолином расслаблениекровеносных сосудов зависит от эндотелия. Его эксперимент "бутерброда" было
важным этапом в последующем развитии науки. Он использовал две
различных части аорты; одна имела неповрежденный слой эндотелия, в другой
этот слой был удален.
Так был открыт EDRF –
эндотелиальный фактор
расслабления
Эндотелий удален –
ацетилхолин вызывает
сокращение стенки сосуда
Эндотелий сохранен –
ацетилхолин вызывает
расслабление сосуда
41. Спектральный анализ Иньярро
Луи Иньярро сообщил, что EDRF расслабляет кровеносные сосуды. Он такжеидентифицировал EDRF как молекулу, используя спектральный анализ
гемоглобина. Когда гемоглобин был подвергнут действию EDRF, максимум
поглощения света сдвигался; такое же изменение спектра наблюдали при
действии на гемоглобин окиси азота. Так был открыт новый принцип
передачи сигналов между клетками человеческого организма.
Спектрофотометр
Гемоглобин (желтый) при
взаимодействии с клетками
эндотелия давал сдвиг спектра,
точно такой же, как при действии на
гемоглобин окиси азота (зеленый).
42. Активация гуанилат-циклазы (по данным Мюрада)
Ферид Мюрад знал, что нитроглицерин вызывает расслабление клеток гладкоймышцы. Фермент, гуанилатциклаза, был активирован, и это вызвало рост концентрации
циклического ГМФ, что привело к расслаблению мышцы. Нитроглицерин действовал
через образование оксида азота? Мюрад барботировал NO-газ через ткань,
содержащую фермент; циклический GMP увеличивался. Так был обнаружен новый
способ действия лекарственного средства!
43. Расслабление стенок сосудов благодаря передаче сигнала между клетками
NO индуцирует синтез ц-ГМФ путем активации гуанилат-циклазы. Этоприводит к релаксации миозина гладких мышц
Ацетилхолин стимулирует синтез
оксида азота, в клетках эндотелия.
Затем NO проникает в
гладкомышечные клетки и вызывает их
расслабление.
44. Расслабление стенок сосудов благодаря передаче сигнала между клетками
Ацетилхолин стимулирует синтез оксидаазота, в клетках эндотелия. Затем NO
проникает в гладкомышечные клетки и
вызывает их расслабление.
NO индуцирует синтез цГМФ путем
активации гуанилат-циклазы.
































 Медицина
Медицина Химия
Химия








