Похожие презентации:
Проантоцианидины. Антиоксидантные и антирадикальные свойства
1. Проантоцианидины
Министерство образования и науки Российской ФедерацииМосковский технологический университет
Институт тонких химических технологий
Кафедра химии и технологии
высокомолекулярных соединений
имени Медведева С.С.
Проантоцианидины
Студентка группы ХЕМО-01-17
Пономарева Е.К.
Москва 2018
2. Проантоцианидины-
ПроантоцианидиныКонденсированные таннины, представляющие собойполимерные формы флавоноидов из группы
катехинов.
Одни из самых интересных и важных для человека
представителей растительных полифенольных
соединений.
флаванон
2
3.
проантоцианидины3
4. Строение и структура
R1OH
Базовая структура проантоцианидинов: R1,R2=H
(пропеларгонидины);
R1=H,R2=OH(процианидины);
HO
R1,R2=OH(продельфинидины)
B
O
8
A
C
R2
2
3
6
4
OH
HO
Структуры некоторых проантоцианидиновдимеров и тримеров типа А,В,С.
4
1-В1: R1 =OH; R2 =H; R3 =H; R4 =OH;
В2: R1 =OH; R2 =H; R3 =OH; R4 =H;
В3: R1 =H; R2 =OH; R3 =H; R4 =OH;
В4: R1 =H; R2 =OH; R3 =OH; R4 =H;
2 – B5: R1 =OH; R2 =H; R3 =H; R4 =OH;
B6: R1 =H; R2 =OH; R3 =OH; R4 =H;
B7: R1 =H; R2 =OH; R3 =H; R4 =OH;
B8: R1 =H; R2 =OH; R3 =H; R4 =OH;
3 – C1: R1 =OH; R2 =H; C2: R1 =H; R2 =OH;
4 – A2
5. Получение проантоцианидина
5Ступенчатая схема ферментативного биосинтеза проантоцианидина;
F3H- флаванон-3- гидроксилаза; DFR-дигидрофлаванол редуктаза;
ANS-синтез антоцианидинов; ANR- антоцианидина редуктаза ; LARлейкоантоцианидин редуктаза; GT-антоцианидин
гликозилтрансфераза.
Cхема образования карбкатионных
дополнительных единиц для биосинтеза
проантоцианидина . LAR- лейкоантоцианидин
редуктаза; ANR – антоцианидин редуктаза, PPOполифенол оксидаза.
6. Взаимодействие с белками
Образованиетаннин-белковые связи
Сродство к белкам зависит от:
природы белка
природы молекулы проантоцианидина
молекулярного веса проантоцианидина
степени галлоизации
степени гидроксилирования
ингибитор
ксантиноксидаза
гиалуронидаза
коллагеназа
6
ксантиноксидаза
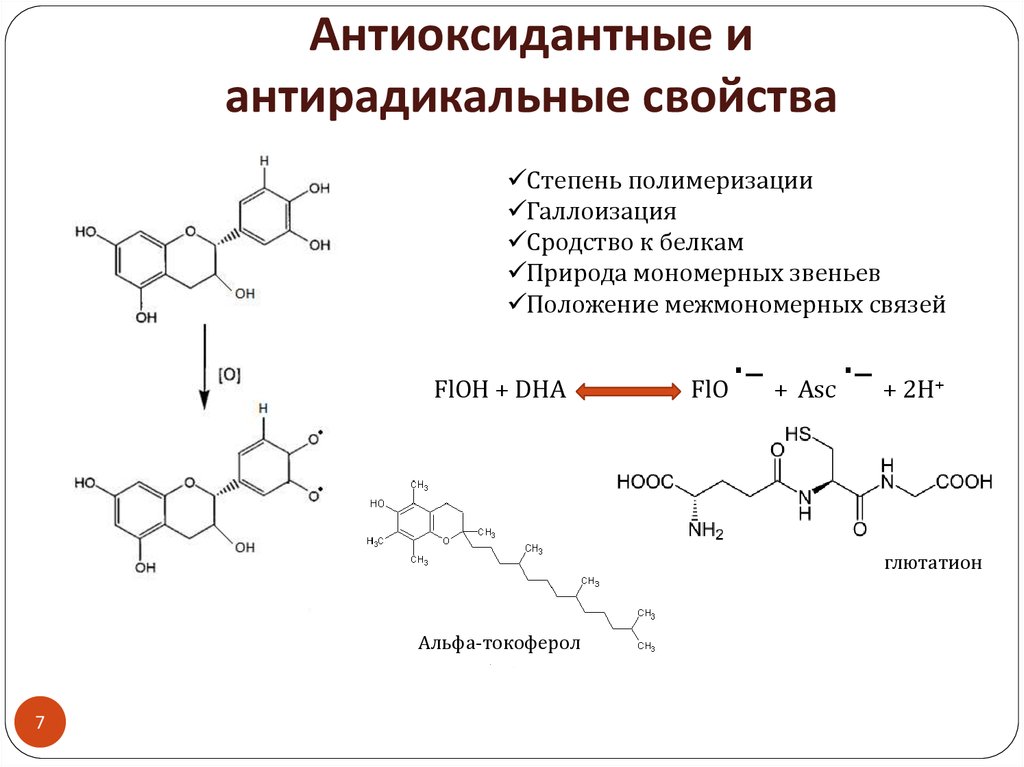
7. Антиоксидантные и антирадикальные свойства
Степень полимеризацииГаллоизация
Сродство к белкам
Природа мономерных звеньев
Положение межмономерных связей
FlOH + DHA
FlO
·– + Asc ·– + 2H+
глютатион
Альфа-токоферол
7
8. Образование комплексов с металлами
(1) Ме (n+1)+ —флав+О2(2) Ме n+ —флав+О2
·–
Ме n+ —флав+О2
·– +2H+
Ме (n+1)+ —флав+H2O2
Где Ме- металлы переменной валентности: Fe (n=2); Cu(n=1) и др.
H
O
Fe
O
HO
O
OH
8
HO
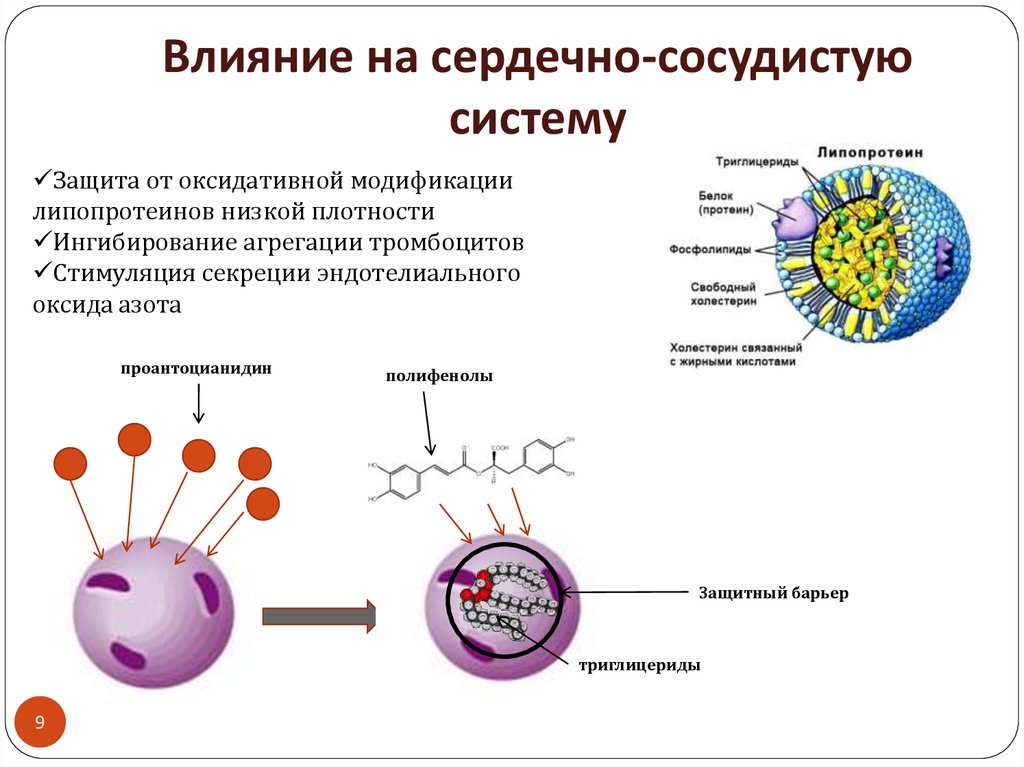
9. Влияние на сердечно-сосудистую систему
Защита от оксидативной модификациилипопротеинов низкой плотности
Ингибирование агрегации тромбоцитов
Стимуляция секреции эндотелиального
оксида азота
проантоцианидин
полифенолы
Защитный барьер
триглицериды
9
10.
проантоцианидин10









 Химия
Химия








