Похожие презентации:
Антибактериальная терапия жизнеугрожающих инфекций – возможности и ограничения
1. Антибактериальная терапия жизнеугрожающих инфекций – возможности и ограничения
Российский Сепсис ФорумИнститут хирургии им. А.В. Вишневского
Антибактериальная терапия
жизнеугрожающих инфекций –
возможности и ограничения
Кулабухов В.В.
Краснодар
27-28 февраля 2018 года
2. Принципы терапии сепсиса
Клиническийфармаколог
Клинический
микробиолог
УСТРАНЕНИЕ ОЧАГА
ИНФЕКЦИИ
АДЕКВАТНАЯ
АНТИМИКРОБНАЯ
ТЕРАПИЯ
Клинический
эпидемиолог
КОРРЕКЦИЯ НАРУШЕНИЙ
ОРГАНОВ И СИСТЕМ
3.
4.
Кулабухов В.В.01.04.201
8
5.
«Антибиотики надоназначать, только если
речь идет о жизни и
смерти.
Они не должны
продаваться в аптеках, как
аспирин»
Howard Florey
6.
• July 27 2012• WAAR (World Alliance against Antibiotic
Resistance): Safeguarding Antibiotics
• Jean Carlet, Claude Rambaud, Céline Pulcini, on
behalf of the WAAR, international section of the
Alliance Contre le développement des Bactéries
Multi-résistantes (AC-de-BMR)
7. 12 бактерий, для борьбы с которыми необходимо разработать новые антибиотики
Срочность 1: критическая
Срочность
1: критическая
• Acinetobacter baumannii, устойчивая к карбапенемам
• Pseudomonas aeruginosa, устойчивая к карбапенемам
• Acinetobacter
baumannii, устойчивая к карбапенемам
• Enterobacteriaceae, устойчивая к карбапенемам, продуценты БЛРС
Срочность 2: высокая
• Pseudomonas
aeruginosa, устойчивая к карбапенемам
• Enterococcus faecium, ванкомицин-резистентная
• Staphylococcus aureus, метициллин-резистентная,
ванкомицин-резистентная
• Enterobacteriaceae,
устойчивая
к карбапенемам, продуценты
БЛРС
• Helicobacter pylori, кларитромицин-резистентная
• Campylobacter spp., устойчивая к фторхинолонам
• Neisseria gonorrhoeae, цефалоспорин-резистентная, устойчивая к фторхинолонам
Срочность
высокая
• Salmonellae,2:
устойчивая
к фторхинолонам
• Enterococcus
faecium, ванкомицин-резистентная
Срочность 3: средняя
• Streptococcus pneumoniae, не восприимчива к пенициллину
• Staphylococcus
aureus, метициллин-резистентная, ванкомицин
• Haemophilus influenzae, ампициллин-резистентная
резистентная
• Shigella spp., устойчиваяя к фторхинолонам
8. Антибактериальная терапия
• Начать внутривенное введение антимикробных препаратов как можнораньше в течение первого часа после выявления септического шока
(1В) и тяжелого сепсиса
(1С).
• Начальная эмпирическая антимикробная терапия включает один или
несколько препаратов, которые активны в отношении всех наиболее
вероятных возбудителей (бактерий, грибов, вирусов) и создают
адекватные концентрации в тканях, явившихся причиной сепсиса
(1В).
• Режим антимикробной терапии должен переоцениваться ежедневно с
целью оптимизации активности препаратов для предотвращения
развития резистентности, снижения токсичности и стоимости
(1С).
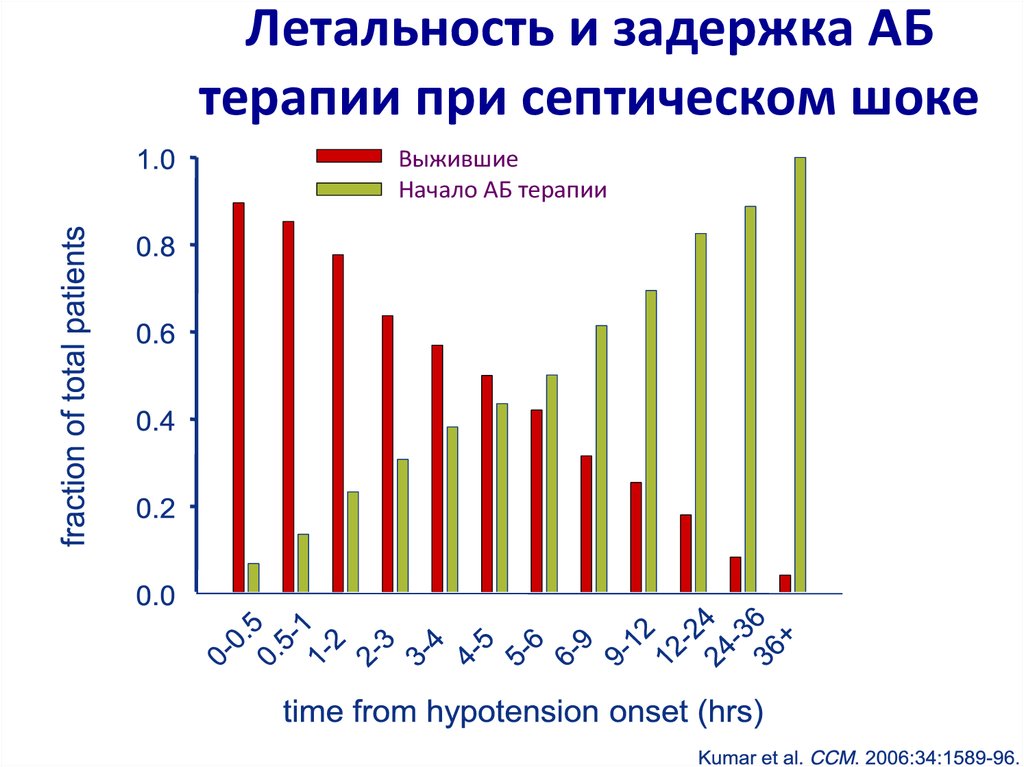
9. Летальность и задержка АБ терапии при септическом шоке
ВыжившиеНачало АБ терапии
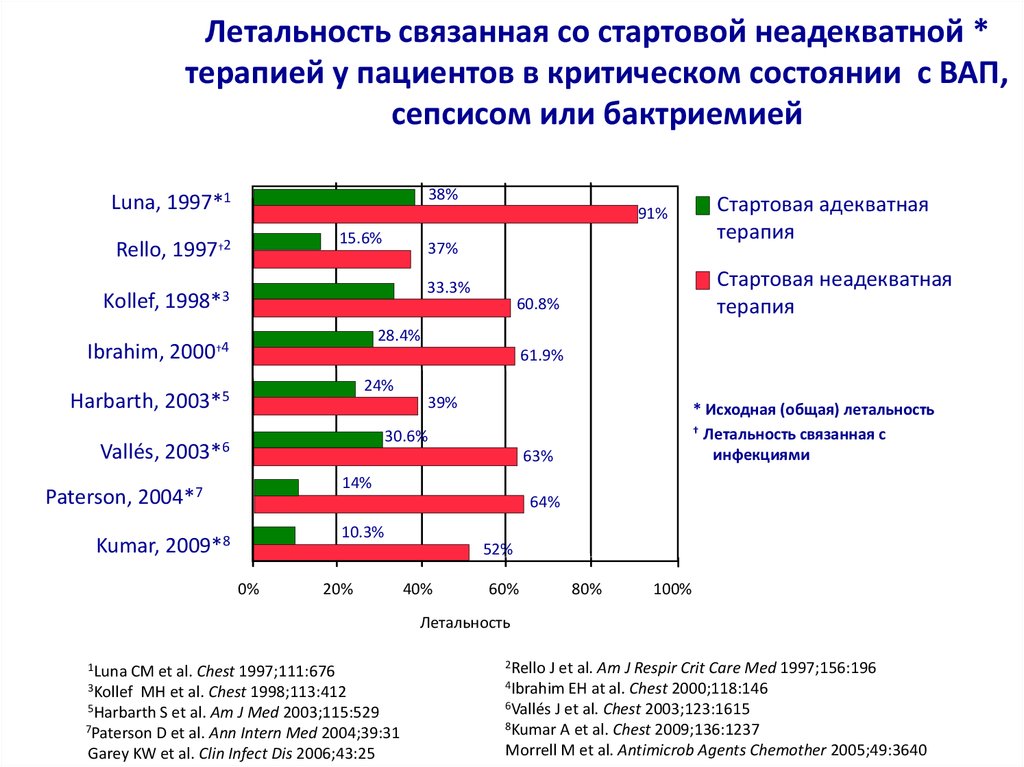
10. Летальность связанная со стартовой неадекватной * терапией у пациентов в критическом состоянии с ВАП, сепсисом или бактриемией
Летальность связанная со стартовой неадекватной *терапией у пациентов в критическом состоянии с ВАП,
сепсисом или бактриемией
38%
Luna, 1997*1
91%
15.6%
Rello, 1997†2
Kollef,
37%
33.3%
1998*3
Стартовая адекватная
терапия
Стартовая неадекватная
терапия
60.8%
28.4%
Ibrahim, 2000†4
61.9%
24%
Harbarth, 2003*5
39%
* Исходная (общая) летальность
† Летальность связанная с
инфекциями
30.6%
Vallés, 2003*6
63%
14%
Paterson, 2004*7
64%
10.3%
Kumar, 2009*8
0%
20%
52%
40%
60%
80%
100%
Летальность
1Luna
CM et al. Chest 1997;111:676
3Kollef MH et al. Chest 1998;113:412
5Harbarth S et al. Am J Med 2003;115:529
7Paterson D et al. Ann Intern Med 2004;39:31
Garey KW et al. Clin Infect Dis 2006;43:25
2Rello
J et al. Am J Respir Crit Care Med 1997;156:196
EH at al. Chest 2000;118:146
6Vallés J et al. Chest 2003;123:1615
8Kumar A et al. Chest 2009;136:1237
Morrell M et al. Antimicrob Agents Chemother 2005;49:3640
4Ibrahim
11. Проблемы АБ терапии
• Глобальное нарастание уровня резистентной флоры• Появление карбапенем- резистентных штаммов
• Появление MDR штаммов во внешней среде
• Отсутствие новых классов АБ препаратов в ближайшие годы
• Широкая доступность для населения
• Неудовлетворительная лабораторная диагностика
• Неадекватная антибиотикопрофилактика
• Низкий уровень образования практикующих врачей
12.
Диагностика инфекцииЭмпирическая АБ терапия
Антибактериальная терапия
Целенаправленная АБ терапия
Прекращение АБ терапии
13. Кто живёт в стационарах?
no ESKAPEEnterococcus faecium
Staphylococcus aureus
Klebsiella
pneumoniae
Clostridium
difficile
Acinetobacter Baumannii
Pseudomonas aeruginosa
Klebsiella
pneumoniae
Enterobacter spp
Escherichia coli
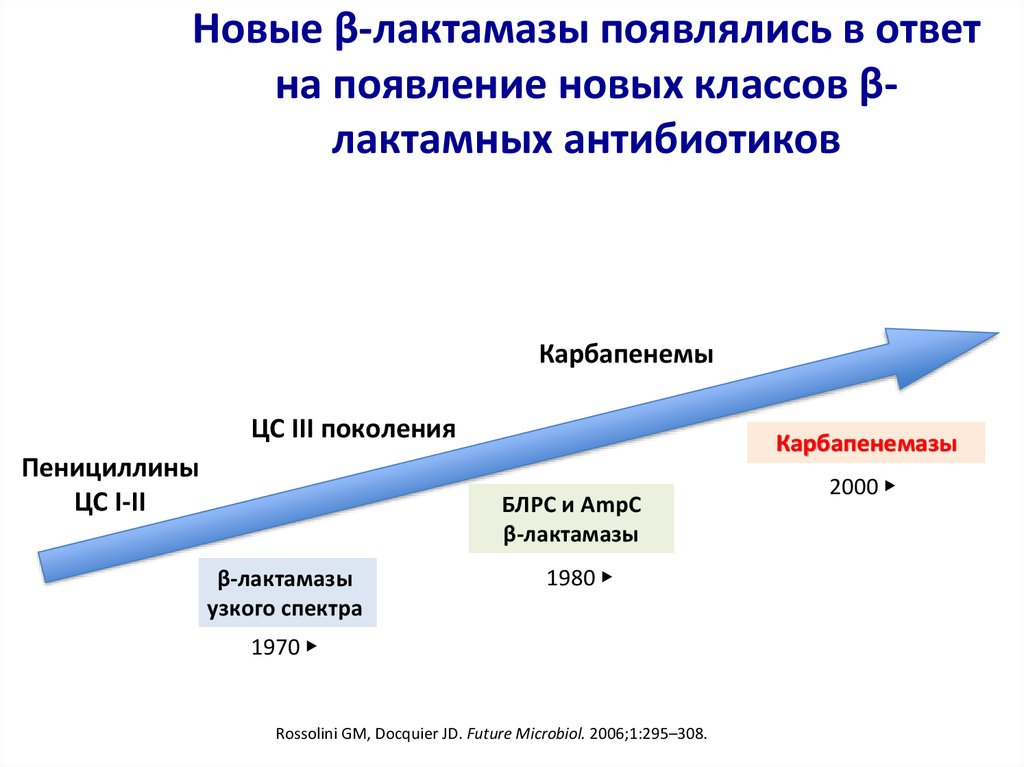
14. Новые β-лактамазы появлялись в ответ на появление новых классов β-лактамных антибиотиков
Новые β-лактамазы появлялись в ответна появление новых классов βлактамных антибиотиков
Карбапенемы
ЦС III поколения
Пенициллины
ЦС I-II
Карбапенемазы
БЛРС и AmpC
β-лактамазы
β-лактамазы
узкого спектра
1980 ▶
1970 ▶
Rossolini GM, Docquier JD. Future Microbiol. 2006;1:295–308.
2000 ▶
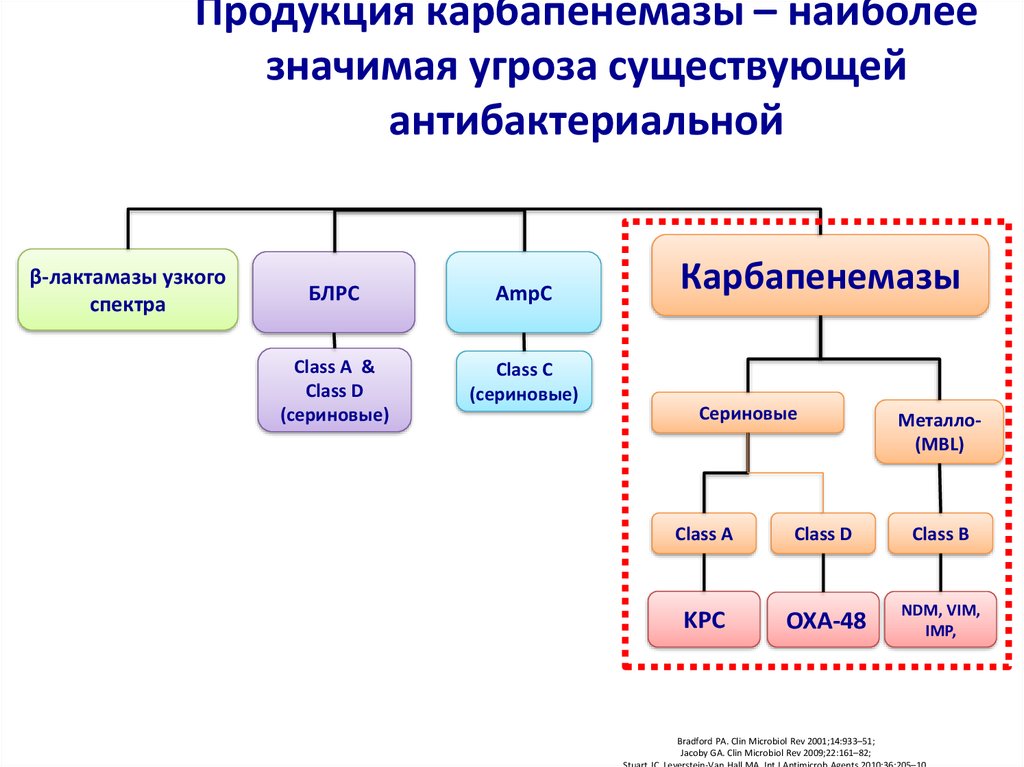
15. Продукция карбапенемазы – наиболее значимая угроза существующей антибактериальной
Продукция карбапенемазы – наиболеезначимая угроза существующей
антибактериальной
β-лактамазы узкого
спектра
БЛРС
AmpC
Class A &
Class D
(сериновые)
Class C
(сериновые)
Карбапенемазы
Сериновые
Металло(MBL)
Class A
Class D
Class B
KPC
OXA-48
NDM, VIM,
IMP,
Bradford PA. Clin Microbiol Rev 2001;14:933–51;
Jacoby GA. Clin Microbiol Rev 2009;22:161–82;
Stuart JC, Leverstein-Van Hall MA. Int J Antimicrob Agents 2010;36:205–10.
16.
17.
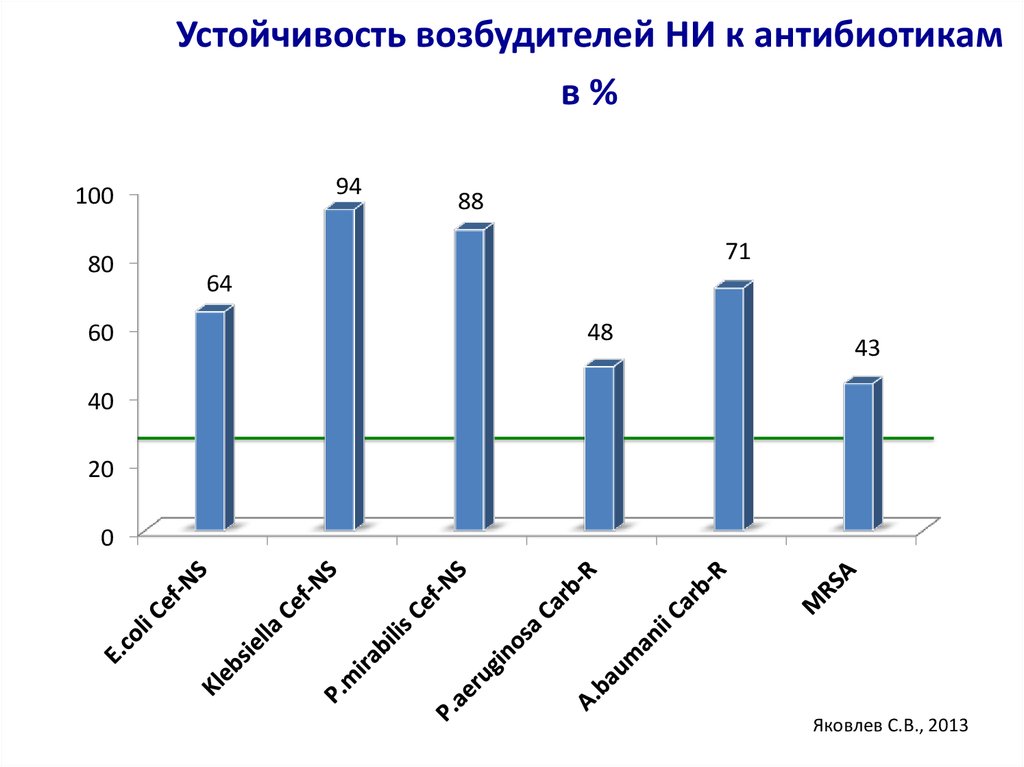
Устойчивость возбудителей НИ к антибиотикамв%
94
100
80
60
88
71
64
48
43
40
20
0
Яковлев С.В., 2013
18.
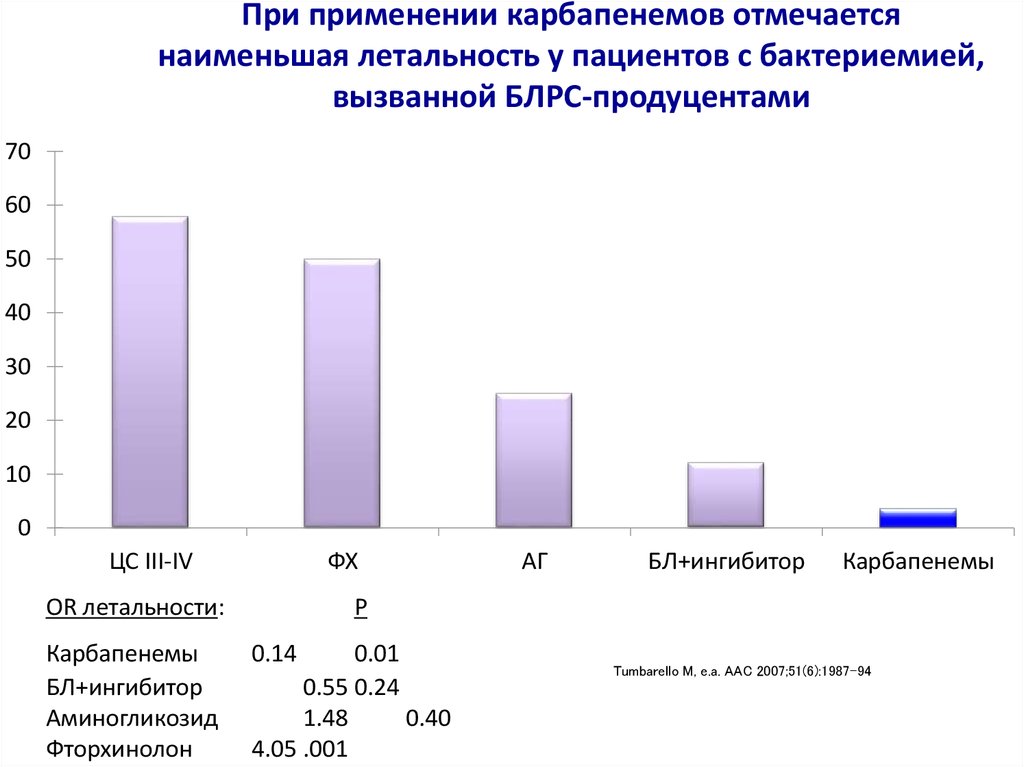
При применении карбапенемов отмечаетсянаименьшая летальность у пациентов с бактериемией,
вызванной БЛРС-продуцентами
70
60
50
40
30
20
10
0
ЦС III-IV
ФХ
OR летальности:
Карбапенемы
БЛ+ингибитор
Аминогликозид
Фторхинолон
АГ
БЛ+ингибитор
Карбапенемы
Р
0.14
0.01
0.55 0.24
1.48
0.40
4.05 .001
Tumbarello M, e.a. AAC 2007;51(6):1987-94
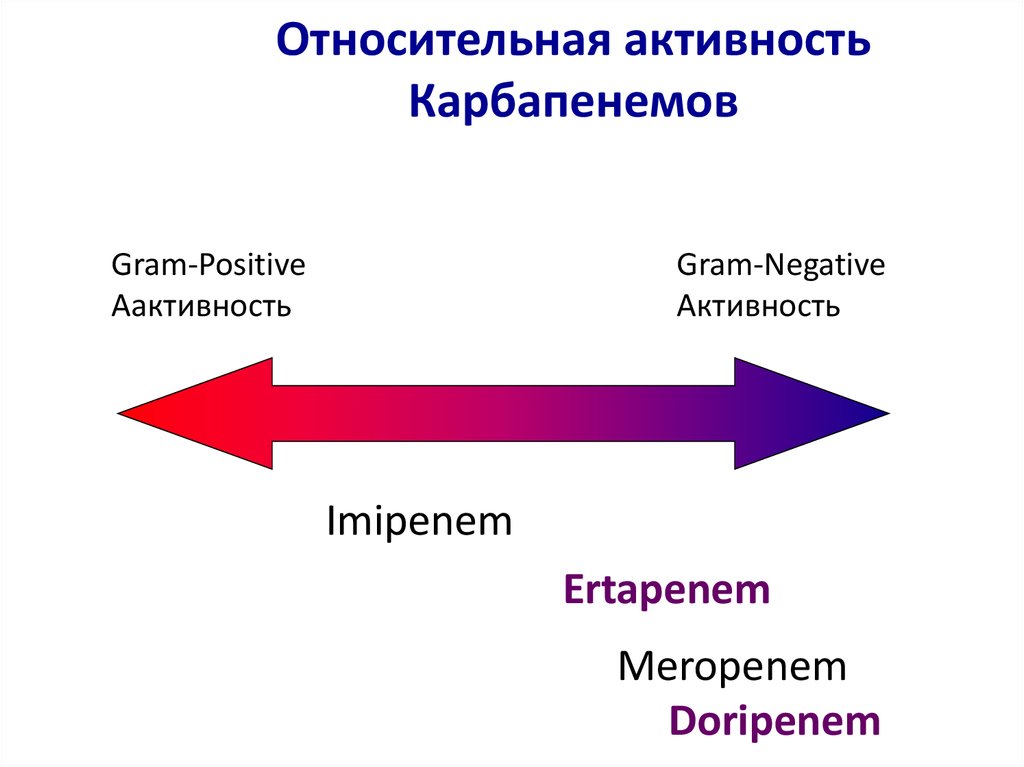
19. Относительная активность Карбапенемов
Gram-PositiveAактивность
Gram-Negative
Активность
Imipenem
Ertapenem
Meropenem
Doripenem
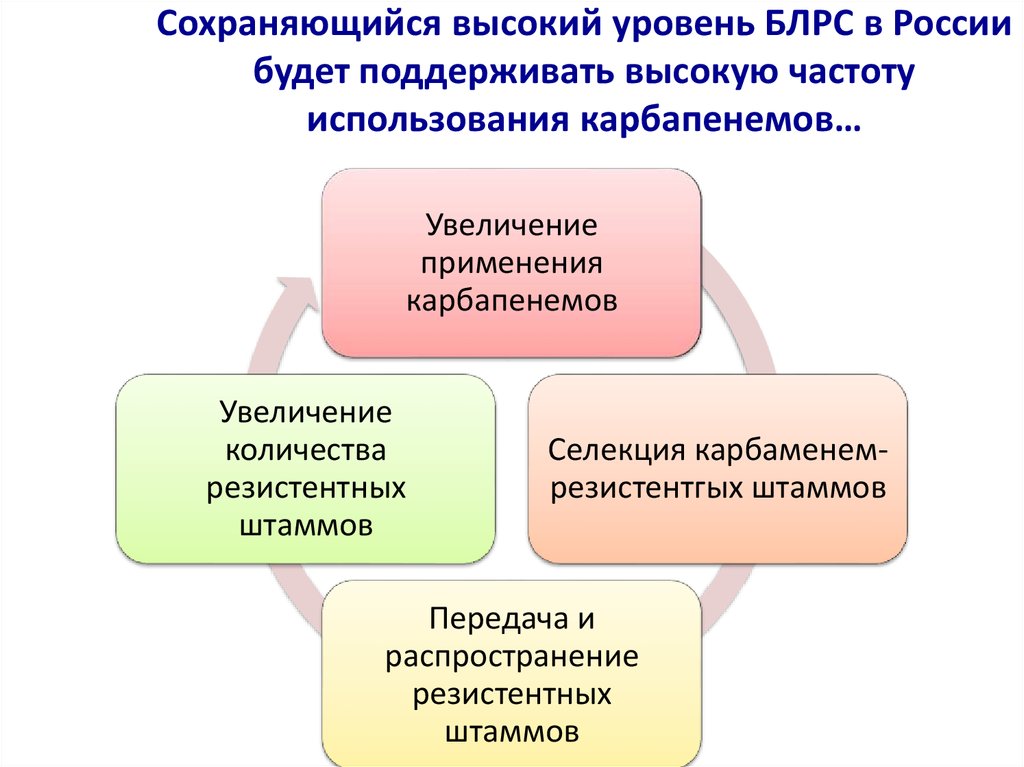
20. Сохраняющийся высокий уровень БЛРС в России будет поддерживать высокую частоту использования карбапенемов…
Сохраняющийся высокий уровень БЛРС в Россиибудет поддерживать высокую частоту
использования карбапенемов…
Увеличение
применения
карбапенемов
Увеличение
количества
резистентных
штаммов
Селекция карбаменемрезистентгых штаммов
Передача и
распространение
резистентных
штаммов
21.
22. Факторы риска наличия полирезистентных возбудителей
Неадекватный инфекционный контрольОбъём работы персонала
Контаминация оборудования
Инвазивные манипуляции
Эндотрахеальная интубация
ЦВК
Уретральный катетер
Длительное пребывание в стационаре
Горизонтальная передача инфекции
Рост колонизации эндогенной флорой
Перевод пациента из другого стационара;
Пребывание в домах длительного ухода (домах престарелых и
др.)
Госпитализация в течение 2-х и более дней в предшествующие
3 – 6 месяцев;
23. Факторы риска наличия полирезистентных возбудителей
ИВЛ > 7 днейПредшествующая АБТ цефалоспоринами 3-го
поколения, фторхинолонами, карбапенемами (< 1 мес)
Неадекватный выбор антибиотика
Неадекватное дозирование
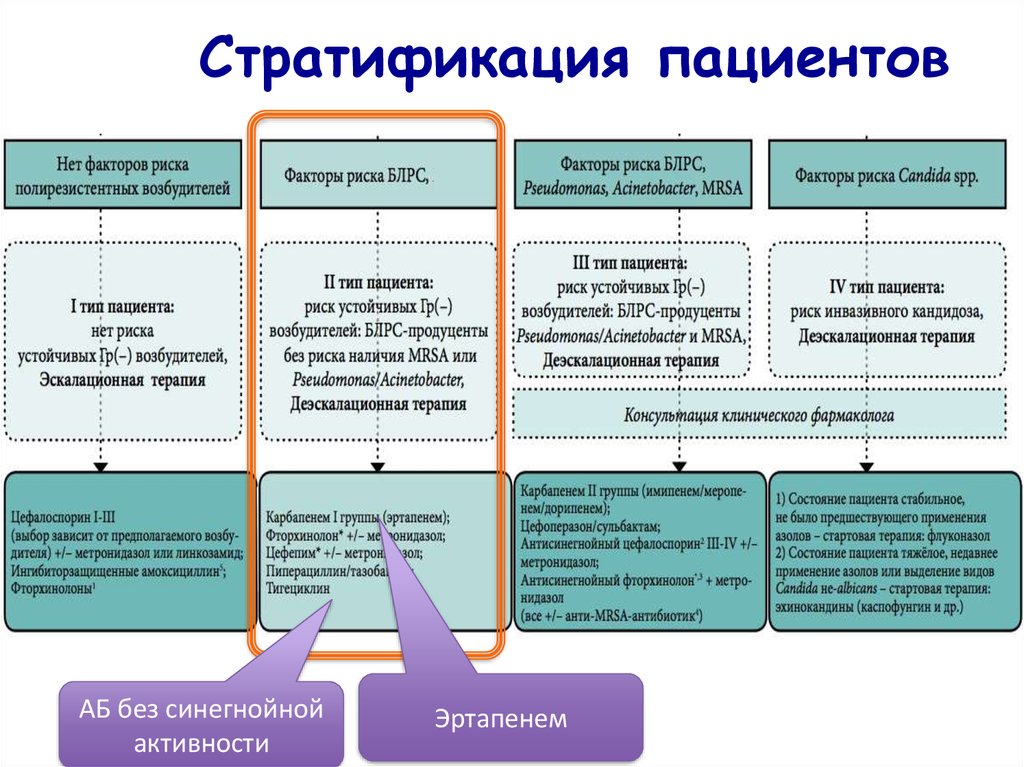
24. Стратификация пациентов
АБ без синегнойнойактивности
Эртапенем
25.
EnterobacteriaceaePseudomonas aeruginosa
Acinetobacter spp.
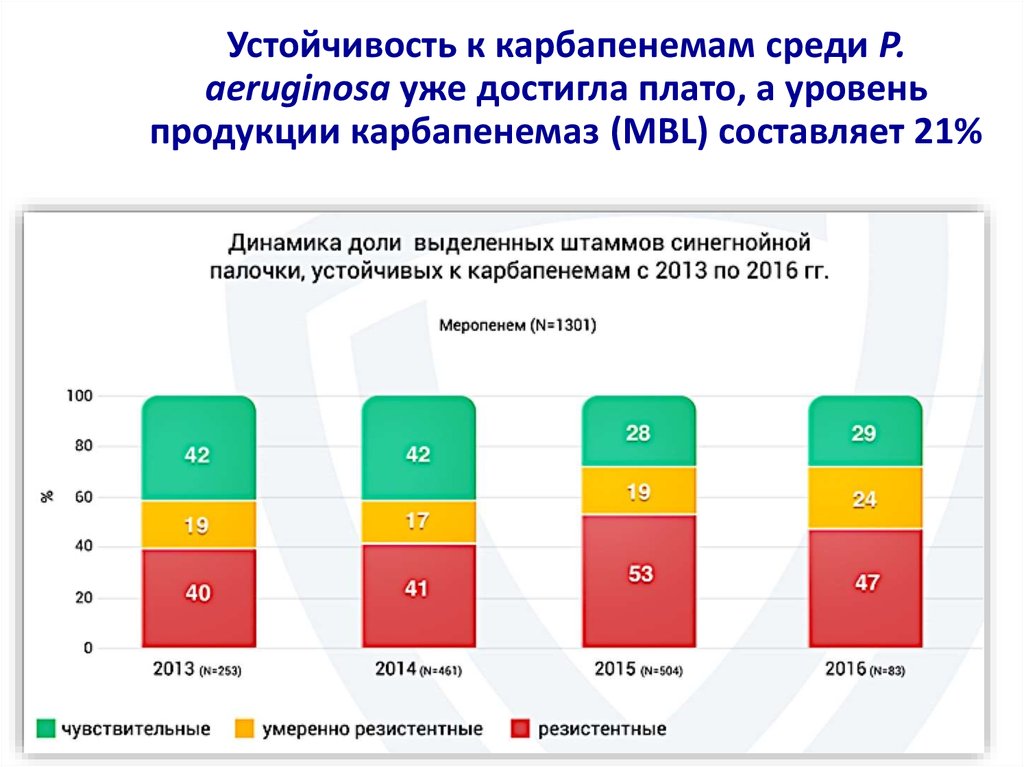
26. Устойчивость к карбапенемам среди P. aeruginosa уже достигла плато, а уровень продукции карбапенемаз (MBL) составляет 21%
Устойчивость к карбапенемам среди P.aeruginosa уже достигла плато, а уровень
продукции карбапенемаз (MBL) составляет 21%
http://map.antibiotic.ru/
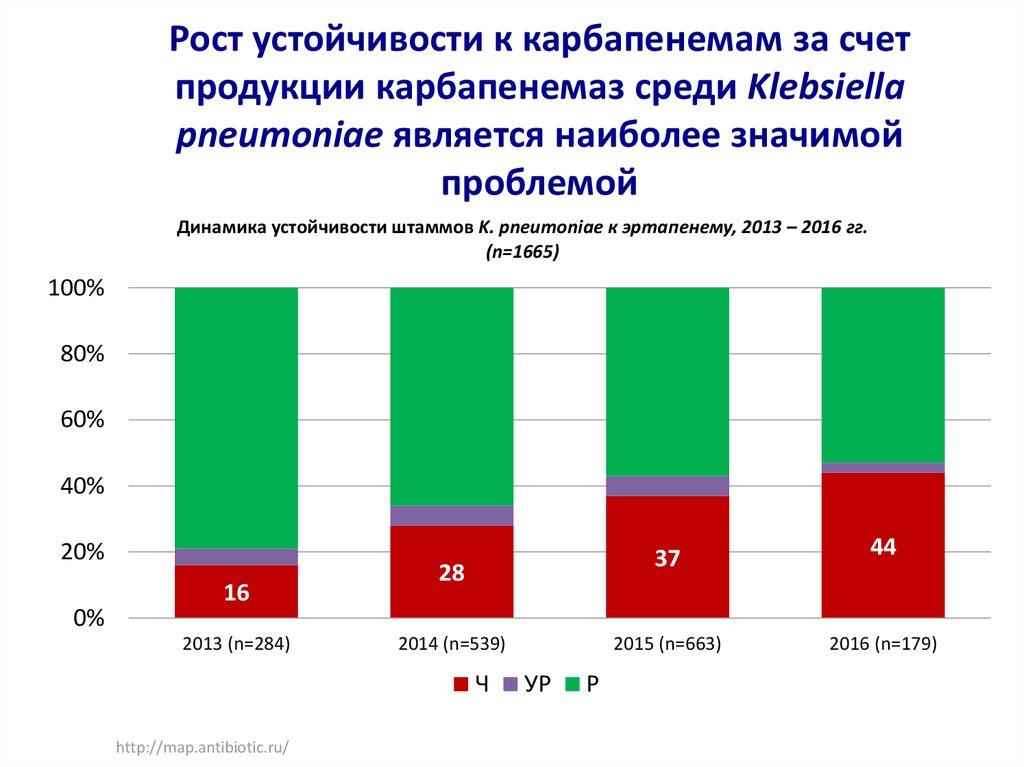
27. Рост устойчивости к карбапенемам за счет продукции карбапенемаз среди Klebsiella pneumoniae является наиболее значимой
Рост устойчивости к карбапенемам за счетпродукции карбапенемаз среди Klebsiella
pneumoniae является наиболее значимой
проблемой
Динамика устойчивости штаммов K. pneumoniae к эртапенему, 2013 – 2016 гг.
(n=1665)
100%
80%
60%
40%
20%
0%
16
2013 (n=284)
37
28
2014 (n=539)
Ч
http://map.antibiotic.ru/
2015 (n=663)
УР
Р
44
2016 (n=179)
28.
Антимикробные препараты, которые могут сохранятьактивость в отношении карбапенем-резистентных
грам(-) бактерий
«Старые» препараты
Тигециклин
Полимиксины (колистин и полимиксин В)
Фосфомицин
Сульбактам
Амикацин
Перспектива
Новые β-лактамы
Неогликозиды
Новые глицилциклины
Пептиды
Ингибиторы ДНК-топоизомераз
………
29. Комбинированная терапия продуцентов КарбапенемR
Колистин – Тигециклин
Тигециклин – Фосфомицин
Полимиксин– Фосфомицин
Эртапенем- Карбапенем II
Полимиксин- Рифампицин
Карбапенем – Полимиксин
Карбапенем – Тигециклин
Тигециклин – Амикацин
Тигециклин – Полимиксин– Карбапенем
Тигециклин – Гентамицин – Карбапенем
Колистин – Гентамицин – Карбапенем
Карбапенем – Полимиксин– Тигециклин - Амикацин
Falagas, ME. et al., 2014
30.
Цефтазидим/авибактамЗарегистрированные в России показания:
Осложненные интра-абдоминальные инфекции
(в комбинации с метронидазолом)
Осложненные инфекции мочевых путей
Нозокомиальная пневмония (ВАП)
Все жизнеугрожающие инфекции, вызванные
чувствительными патогенами
активность в отношении штаммов энтеробактерий, продуцирующих KPC и
OXA карбапенемазы
31.
Цефтолозан/тазобактамЗарегистрированные в США показания:
Осложненные интра-абдоминальные инфекции
Осложненные инфекции мочевых путей
высокая среди всех β-лактамов активность в Pseudomonas aeruginosa, в том
числе в отношении многих штаммов, устойчивых к цефтазидиму и
карбапенемов
32. Антимикробные агенты доступные в настоящее время для лечения MRSA инфекции
• Внутривенные антибактериальные средства длямонотерапии MRSA инфекции
1.
2.
3.
4.
5.
6.
7.
Ванкомицин
Даптомицин
Линезолид
Тедизолид
Тигециклин
Телаванцин
Цефтаролин
33. Ванкомицин-золотой стандарт…
Ванкомицин-золотой стандарт…• Ванкомицин в нашей стране остается
антибиотиком первой линии терапии серьезных
инфекций, вызванных MRSA, в том числе
инфекции кожи и мягких тканей, пневмонии,
инфекции кровотока.
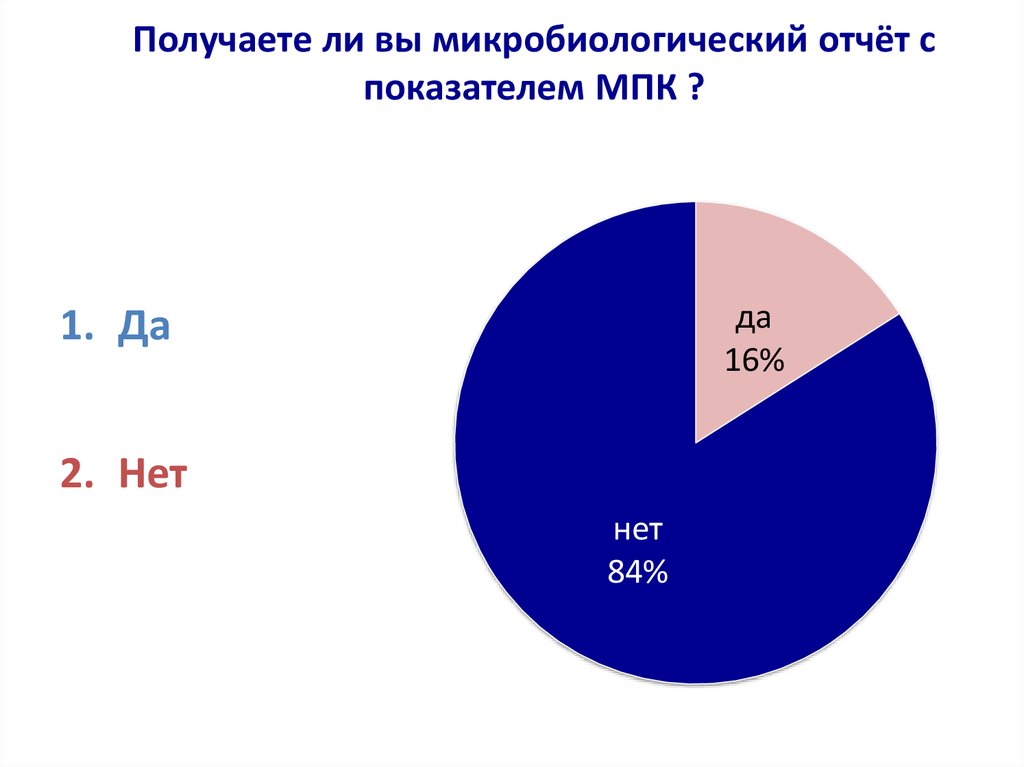
34. Получаете ли вы микробиологический отчёт с показателем МПК ?
Получаете ли вы микробиологический отчёт споказателем МПК ?
да
16%
1. Да
2. Нет
нет
84%
35.
Распределение МПК ванкомицина штаммов MRSA,выделенных в Европе
диско-диффузионный метод не выявляет
штаммы MRSA со сниженной
чувствительностью к ванкомицину
[Sader H, AAC2006;50:2330-6]
www.escmid.org
2012
36. Проблемы Ванкомицина
- Медленныйбактерицидный эффект.
Длительное время
эрадикации МRSA
- Появление R- штаммов
S.aureus (VRSA, VISA, hVISA)
- Неэффективность терапии с
повышением МПК
- Тканевая пенетрация зависит
от степени воспаления
- Недостаточно высокая
концентрация в лёгких
- Для оптимального эффекта
необходимо AUC\MIC >400,
что труднодостижимо при
целевой концентрации в
крови -15-20 мг/л
- Повышение риска
нефротоксичности
ассоциирует с
длительностью
применения
37. Линезолид
• Линезолид первый бактериостатический антибиотик оксазолидинон• Одобрен FDA для лечения внутрибольничной пневмонии
• Обладает превосходной биодоступностью и пенетрацией в
лёгочную ткань
• Линезолид препарат выбора внебольничной MRSA -пневмонии,
т.к. он подавляет лейкоцидин Пантон Валентина (PVL),
продуцируемый S. аureus, вызывающий некротическую пневмонию
• Побочные эффекты линезолида включают миелосупрессию (при
длительности терапии более 2-х недель), периферическую
нейропатию и усиление токсических эффектов серотонина
Kisgen JJ, Mansour H, Unger NR, Childs LM. Am J Health Syst Pharm. 2014;71(8):621-633.
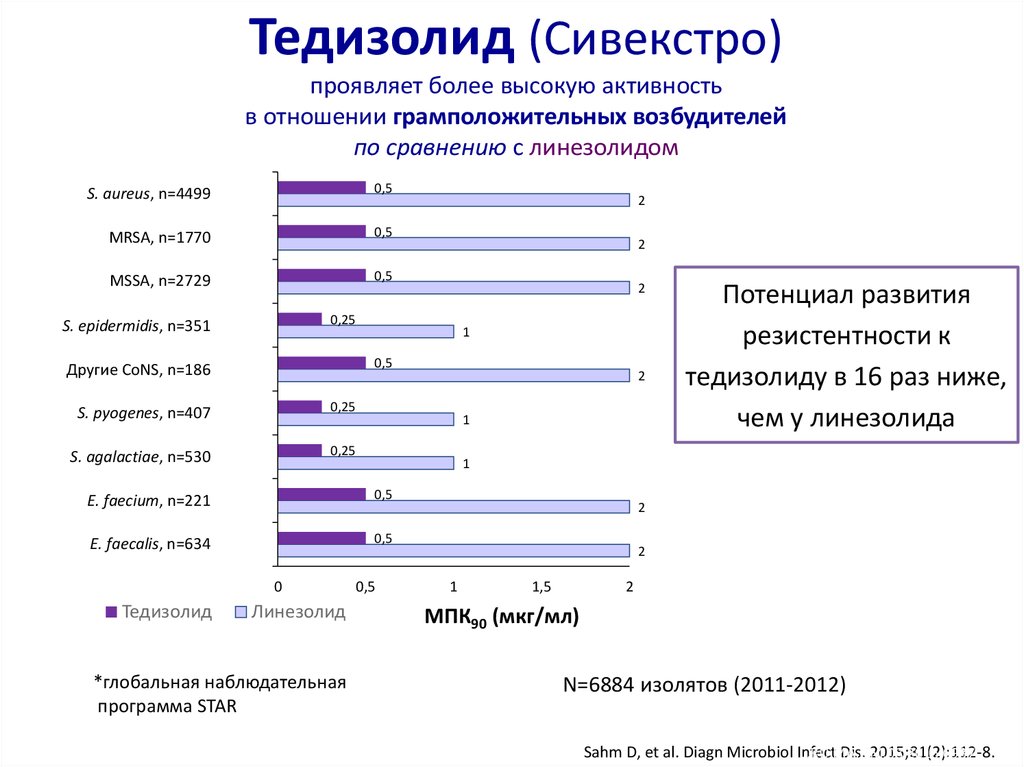
38. Тедизолид (Сивекстро) проявляет более высокую активность в отношении грамположительных возбудителей по сравнению с линезолидом
Тедизолид (Сивекстро)проявляет более высокую активность
в отношении грамположительных возбудителей
по сравнению с линезолидом
S. aureus, n=4499
0,5
MRSA, n=1770
0,5
MSSA, n=2729
0,5
2
2
0,25
S. epidermidis, n=351
1
0,5
Другие CoNS, n=186
S. pyogenes, n=407
0,25
S. agalactiae, n=530
0,25
E. faecalis, n=634
0,5
Линезолид
*глобальная наблюдательная
программа STAR
Потенциал развития
резистентности к
тедизолиду в 16 раз ниже,
чем у линезолида
1
0,5
0
2
1
E. faecium, n=221
Тедизолид
2
0,5
2
2
1
1,5
2
МПК90 (мкг/мл)
N=6884 изолятов (2011-2012)
Sahm D, et al. Diagn Microbiol Infect
Dis. 2015;81(2):112-8.
L.RU.MA.GM.08.2016.0937
39. Преимущества
• Более высокая, по сравнению с линезолидом, активность в отношенииMRSA (штаммы дикого типа и мутантные)
• Сохраняет активность в отношении штаммов с геном cfr+
• Линейная фармакокинетика, минимальная кумуляция и высокая
биодоступность при пероральном введении обеспечивают сопоставимую
концентрацию и действие между внутривенной и пероральной формами
• Период полувыведения (~ 10-11 часов) позволяет принимать препарат
один раз в сутки
• Высокая концентрация в подкожно-жировой клетчатке и мышечной ткани
• Не требует коррекции дозы при использовании у особых групп пациентов
• Достаточен 6- ти девный курс терапии
• Возможен переход на таблетированные формы
L.RU.MA.GM.08.2016.0937
40. Даптомицин (Кубицин)
• Циклический липопептид• Осложненные инфекции кожи и мягких тканей
(взрослые)
• Бактериемия St. aureus, включая эндокардит
• Не должен использоваться для лечения MRSA
нозокомиальной пневмонии, так как инактвируется
лёгочным сурфактантом.
Silverman JA, Mortin LI, Vanpraagh AD, Li T, Alder J.
J Infect Dis. 2005;191(12):2149-2152
41. MRSA-бактериемия (МПК>1мкг/мл)
MRSA-бактериемия(МПК>1мкг/мл)
Даптомицин vs ванкомицин
Клинические неудачи
17% vs 31% (p=0,08)
Летальность
9% vs 20% (р=0,04)
СL Moor CID 2012; 54:51
42. Тигециклин
• Тигециклин является бактериостатическим глициклином.• Выбор второго или третьего ряда в программе лечения MRSA
из-за его недостаточной плазменной концентрации.
• В 2010 году FDA заявило о повышенном риске смертности,
связанной с использованием тигециклина по сравнению с
другими средствами.
• Не рекомендован FDA для терапии госпитальной пневмонии
Rodvold KA, Gotfried MH, Cwik M, Korth-Bradley JM, Dukart G, Ellis-Grosse
EJ.. J Antimicrob Chemother. 2006;58(6):1221-1229.
43. Цефтаролин
• Представитель пятого поколенияцефалоспоринов,
• Одобрен FDA для лечения инфекции кожи и
мягких тканей и внебольничной
пневмонии.
Sakoulas G, Moise PA, Casapao AM, et al. Clin Ther. 2014;36(10):1317-1333.
44. Телаванцин (Вибатив)
новый класс препаратов
липогликопептид
два механизма действия
бактерицидный
нозокомиальная пневмония
инфекции кожи и мягких тканей
биопленки
отечественный препарат
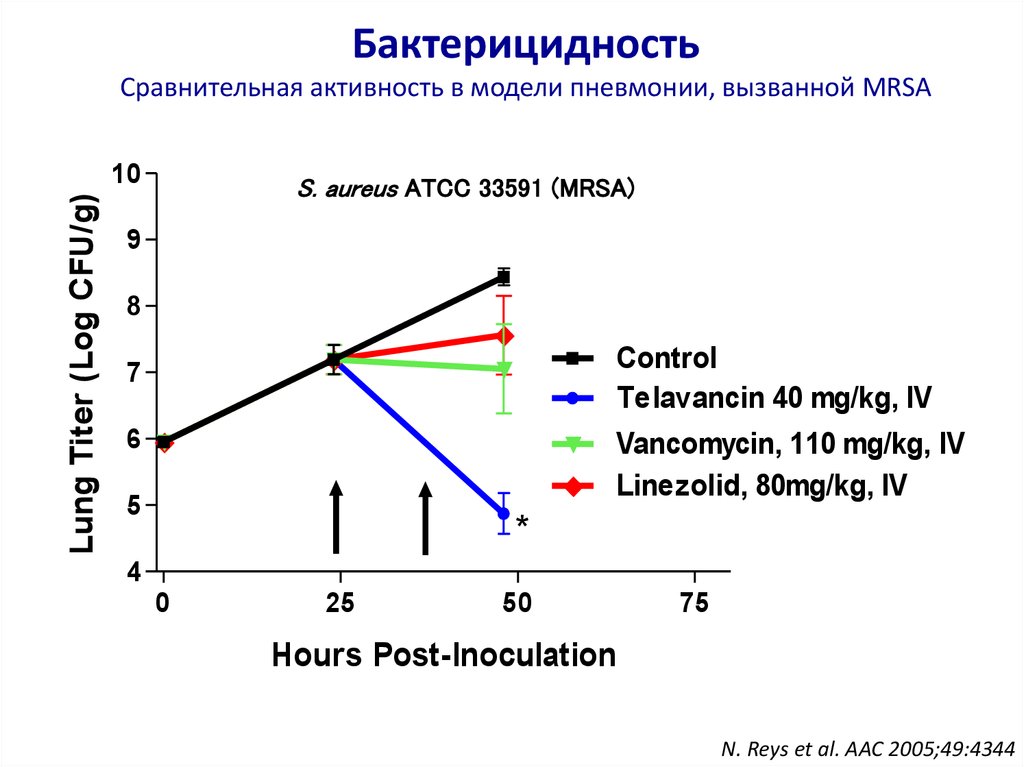
45. Бактерицидность Сравнительная активность в модели пневмонии, вызванной MRSA
Lung Titer (Log CFU/g)10
S. aureus ATCC 33591 (MRSA)
9
8
Control
Telavancin 40 mg/kg, IV
7
6
Vancomycin, 110 mg/kg, IV
Linezolid, 80mg/kg, IV
5
*
4
0
25
50
75
Hours Post-Inoculation
N. Reys et al. AAC 2005;49:4344
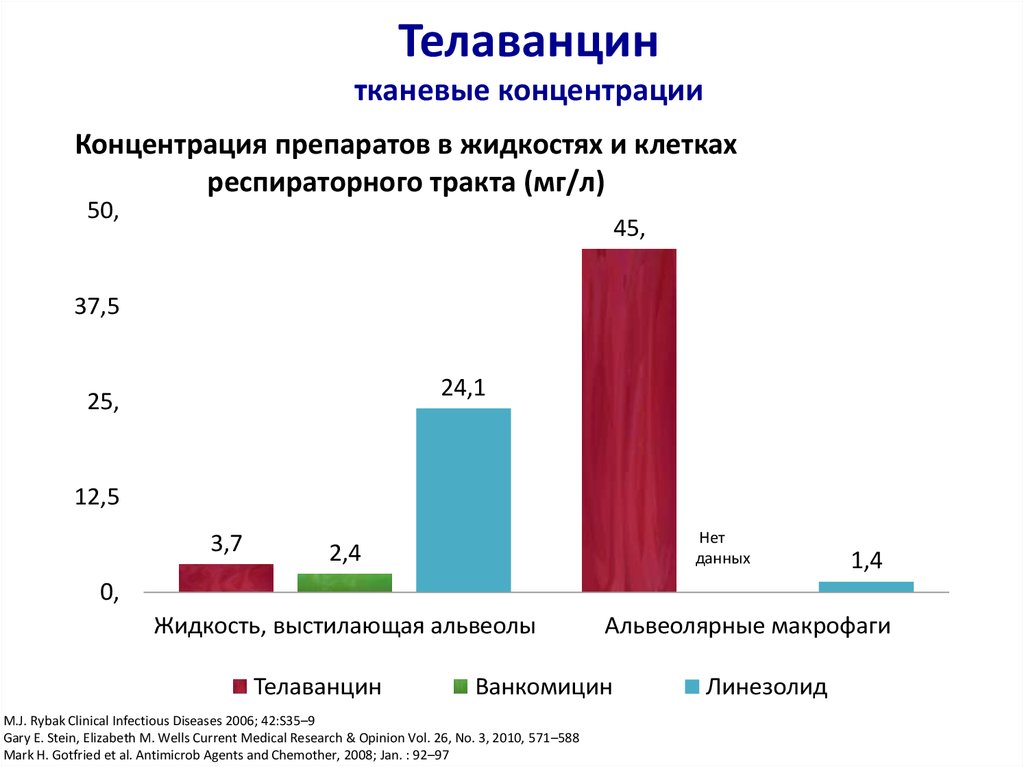
46. Телаванцин тканевые концентрации
Концентрация препаратов в жидкостях и клеткахреспираторного тракта (мг/л)
50,
45,
37,5
24,1
25,
12,5
3,7
Нет
данных
2,4
1,4
0,
Жидкость, выстилающая альвеолы
Телаванцин
Альвеолярные макрофаги
Ванкомицин
M.J. Rybak Clinical Infectious Diseases 2006; 42:S35–9
Gary E. Stein, Elizabeth M. Wells Current Medical Research & Opinion Vol. 26, No. 3, 2010, 571–588
Mark H. Gotfried et al. Antimicrob Agents and Chemother, 2008; Jan. : 92–97
Линезолид
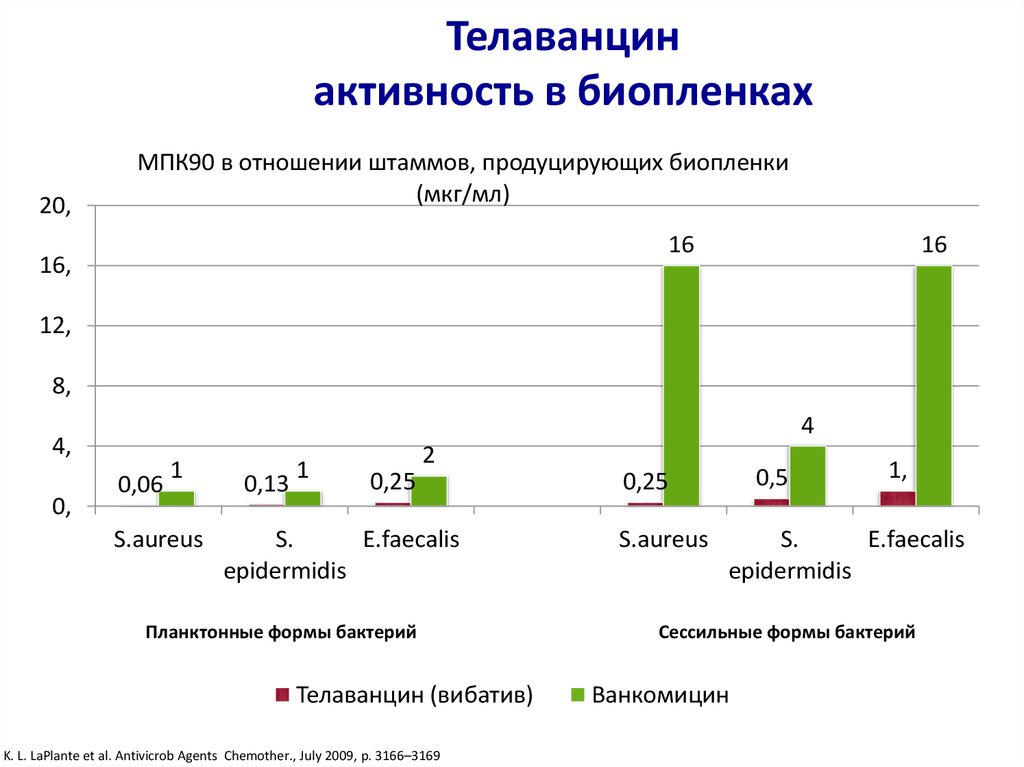
47. Телаванцин активность в биопленках
20,МПК90 в отношении штаммов, продуцирующих биопленки
(мкг/мл)
16
16,
16
12,
8,
4
4,
0,
0,06
1
S.aureus
0,13
1
2
0,25
S.
E.faecalis
epidermidis
Планктонные формы бактерий
Телаванцин (вибатив)
K. L. LaPlante et al. Antivicrob Agents Chemother., July 2009, p. 3166–3169
0,5
0,25
S.aureus
1,
S.
E.faecalis
epidermidis
Сессильные формы бактерий
Ванкомицин
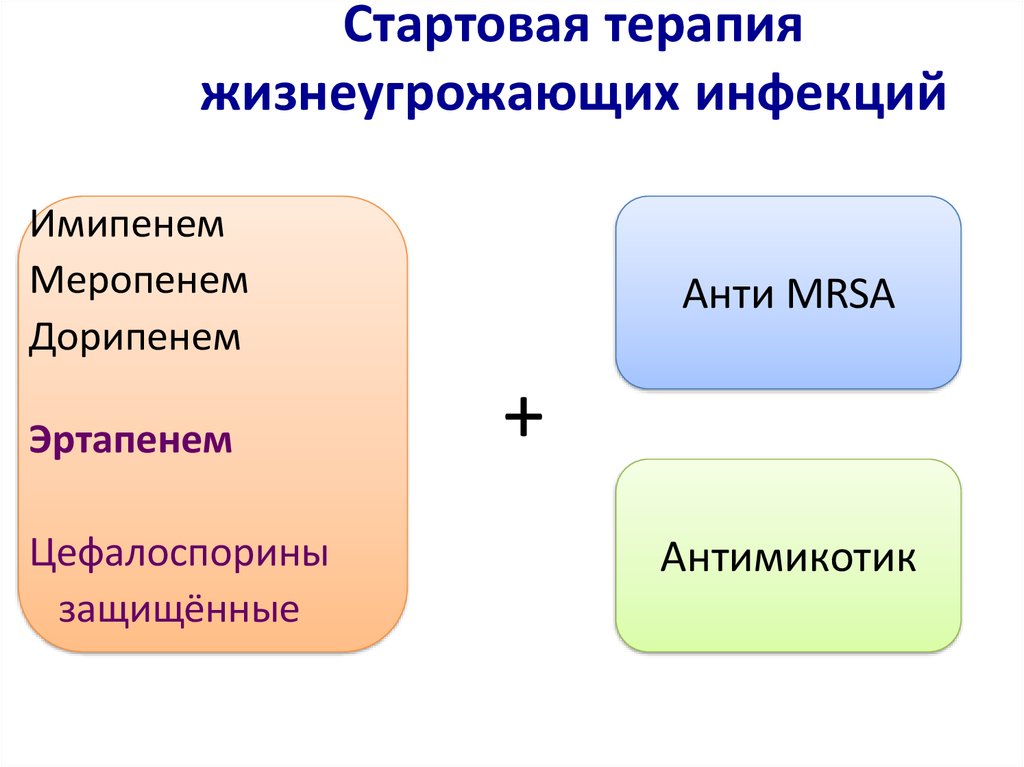
48. Стартовая терапия жизнеугрожающих инфекций
Стартовая терапияжизнеугрожающих инфекций
Имипенем
Меропенем
Дорипенем
Эртапенем
Цефалоспорины
защищённые
Анти MRSA
+
Антимикотик
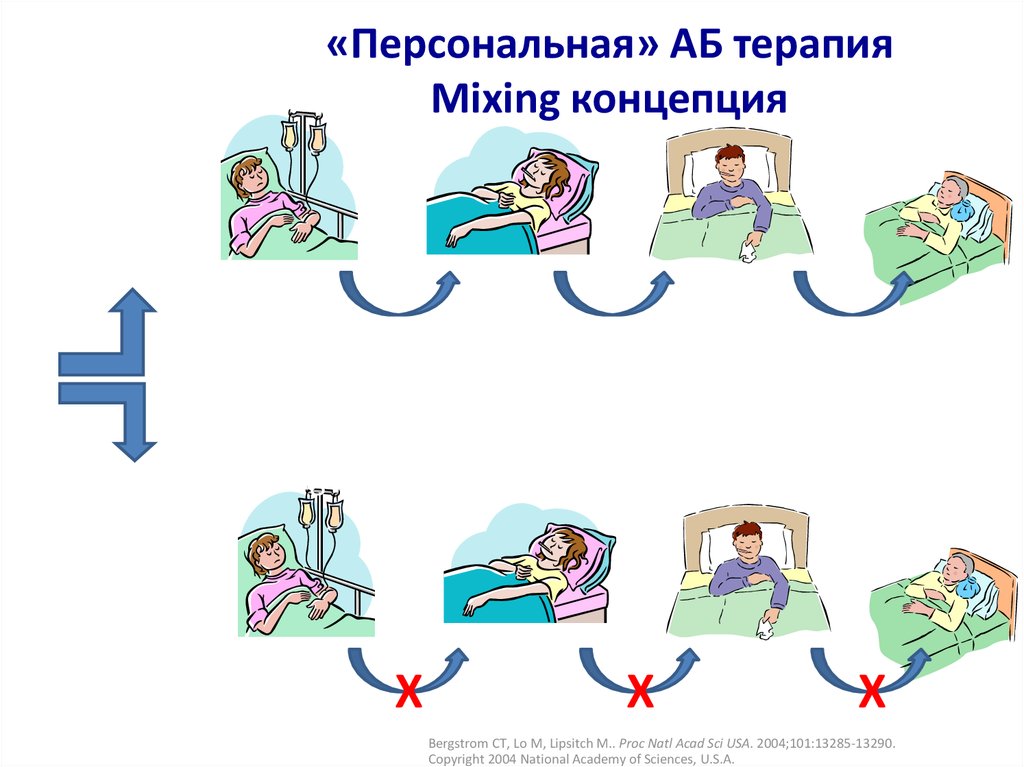
49.
«Персональная» АБ терапияDrug A
Mixing
Drug A концепция
Drug A
Drug A
Drug A
Drug B
Drug C
Drug D
X
X
X
Bergstrom CT, Lo M, Lipsitch M.. Proc Natl Acad Sci USA. 2004;101:13285-13290.
Copyright 2004 National Academy of Sciences, U.S.A.
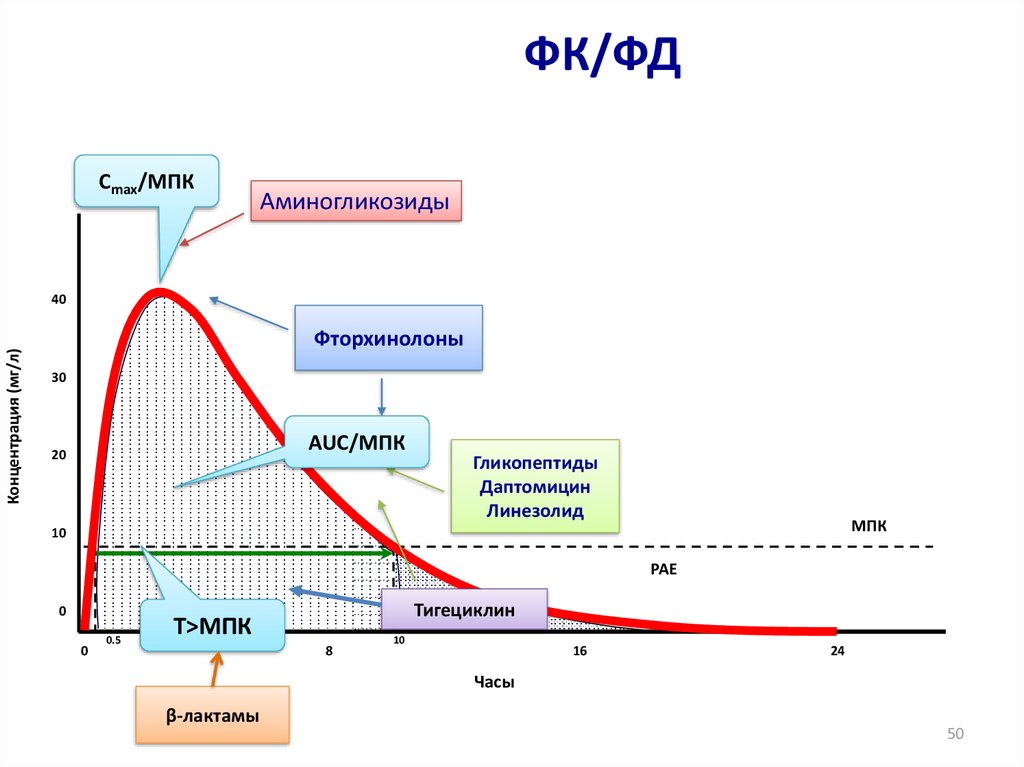
50.
ФК/ФДСmax/МПК
Аминогликозиды
Концентрация (мг/л)
40
Фторхинолоны
30
AUC/МПК
20
Гликопептиды
Даптомицин
Линезолид
МПК
10
PAE
0
0
0.5
Тигециклин
Т>МПК
8
10
16
24
Часы
β-лактамы
50
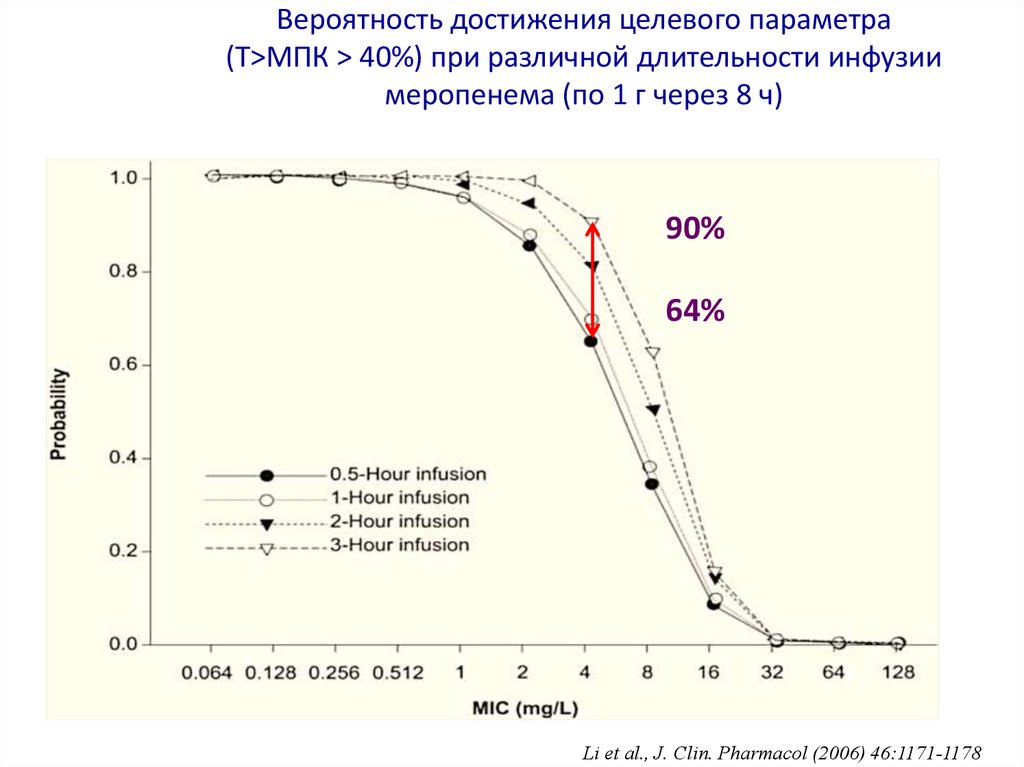
51. Вероятность достижения целевого параметра (Т>МПК > 40%) при различной длительности инфузии меропенема (по 1 г через 8 ч)
Вероятность достижения целевого параметра(Т>МПК > 40%) при различной длительности инфузии
меропенема (по 1 г через 8 ч)
90%
64%
Li et al., J. Clin. Pharmacol (2006) 46:1171-1178
52. Исследование DALI (Defining Antibiotic Levels in Intensive care unit patients) Оценка ФК/ФД антимикробных препаратов N=500, 70
ОРИТДозировка антибиотиков у больных ОРИТ должна отличаться
от стандартной в силу проведения инфузионной терапии,
наличия полиорганной недостаточности (ОССН, ОППН),
увеличения объёма распределения и не может быть
идентичной рекомендуемой, так как ФК/ФД на начальном
этапе изучается у здоровых добровольцев. Изучение
концентрации антибиотиков у больных в ОРИТ
демонстрирует, что для достижения эффекта дозу
необходимо увеличивать на 74% от рекомендуемой
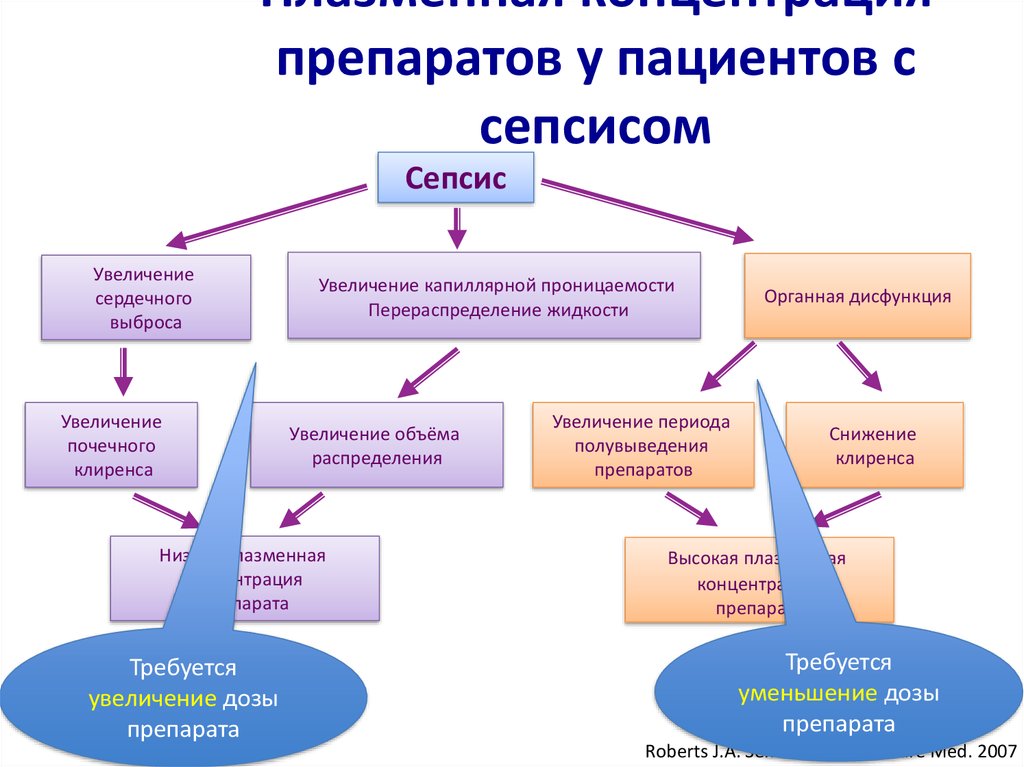
53. Плазменная концентрация препаратов у пациентов с сепсисом
СепсисУвеличение
сердечного
выброса
Увеличение
почечного
клиренса
Увеличение капиллярной проницаемости
Перераспределение жидкости
Увеличение объёма
распределения
Низкая плазменная
концентрация
препарата
Требуется
увеличение дозы
препарата
Увеличение периода
полувыведения
препаратов
Органная дисфункция
Снижение
клиренса
Высокая плазменная
концентрация
препарата
Требуется
уменьшение дозы
препарата
53
Roberts J.A. Semin Respir Crit Care Med. 2007
54.
Torres J. A., Tafur J. D., Briceno D. F., Viollegas M. V. GenericAntibiotics are a Risk Factor for Mortality in Acinetobacter
baumannii Infections in Colombian Intensive Care Units
(ICUs).
49th ICAAC, San Francisco, California, USA, September 12–15, 2009.
Poster# K–312.
Conclusions: In Colombia,
patients with NIAb tend to be
severely ill and have prolonged
hospitalizations as described
elsewhere. Many strains are
multi-drug resistant. The use of
generics appears to be a risk
factor for mortality.
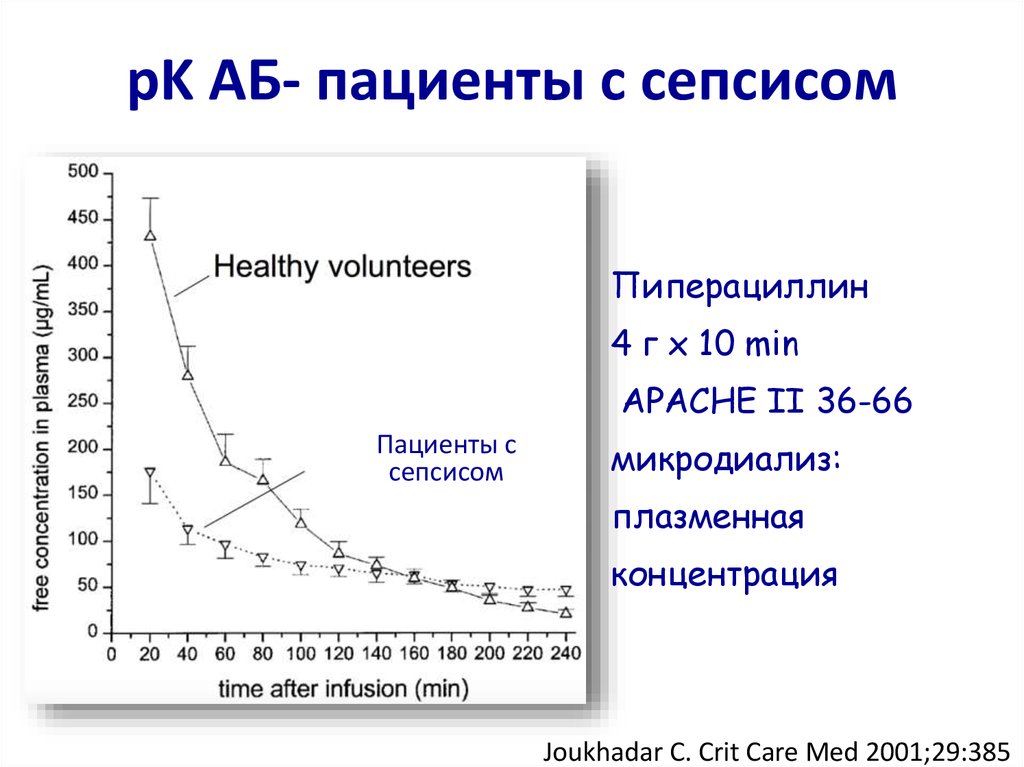
55. pK АБ- пациенты с сепсисом
Пиперациллин4 г х 10 min
APACHE II 36-66
Пациенты с
сепсисом
микродиализ:
плазменная
концентрация
Joukhadar C. Crit Care Med 2001;29:385
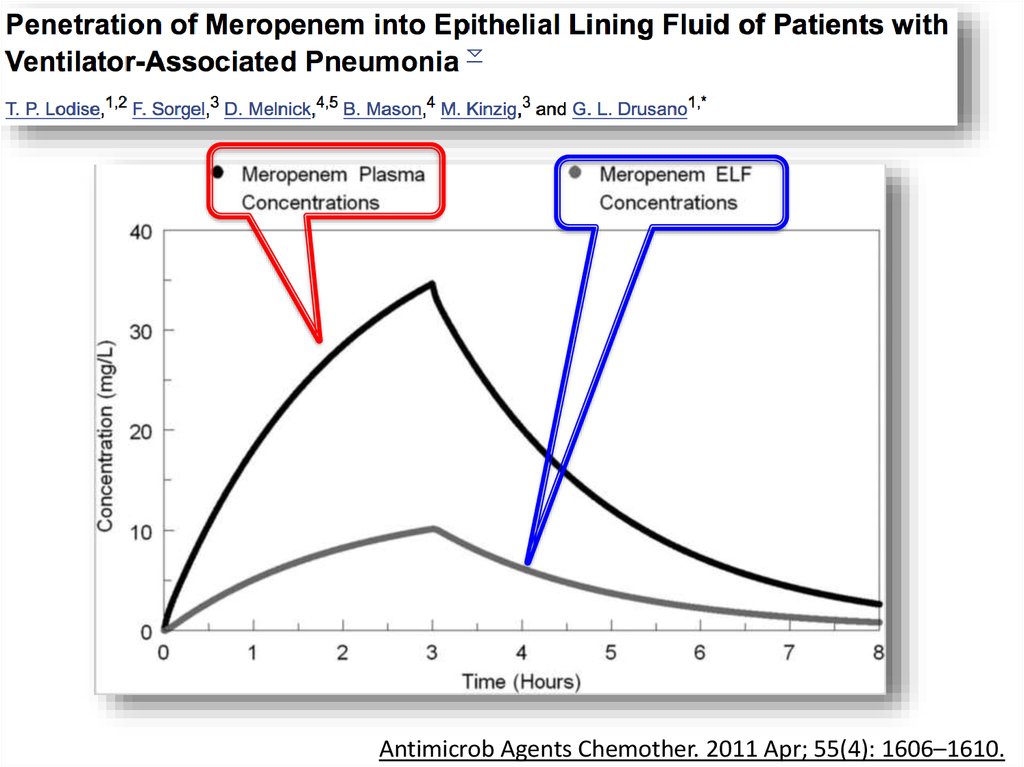
56.
Antimicrob Agents Chemother. 2011 Apr; 55(4): 1606–1610.57. Терапия кандидемии
Эхинокандины• Микафунгин, Анидулафунгин, Каспофунгин,
AI
Азолы
Вориконазол
Флуконазол
Итраконазол
Позаконазол
BI
CI
D II
D III
Полиены
AmB деоксихолат
AmB липосомальный
AmB липидный комплекс C II
AmB коллоидно- дисперсионный
DI
BI
D II
58.
Мы пришли к заключению, что у взрослых пациентовв критическом состоянии без нейтропении с
доказанным или подозреваемым ИК системная
антифунгальная терапия течение 5 дней с
последующим переходом на флуконазол была связана
с уменьшением потребления препаратов без
очевидного вредного эффекта и 28- дневной
летальности.
59.
w w w. s e p s i s f o r u m . r u59


































 Медицина
Медицина








