Похожие презентации:
Катаболизм аминокислот и обезвреживание аммиака
1.
КАТАБОЛИЗМ АМИНОКИСЛОТИ
ОБЕЗВРЕЖИВАНИЕ АММИАКА
2.
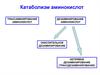
Источники и пути утилизации аминокислотисточники
аминокислот
источники
аминогрупп
Нет
специфических
форм
депонирования
аминокислот
источник
углеродной
части молекул
аминокислот
ЦТК
глюкогенные
и кетогенные
аминокислоты
3.
Пути образования аммиакаДезаминирование
аминокислот
Дезаминирование
биогенных аминов
Дезаминирование
нуклеотидов
Микрофлора
кишечника
(гниение белков)
АММИАК (NH3)
В норме концентрация NH3 в крови: 25 – 40 мкмоль/л.
Избыток NH3 токсичен.
В плазме крови и цитоплазме клеток аммиак превращается в ион аммония:
NH3 + H+ NH4+ (доля NH3 около 1%)
4.
Токсическое действие избытка аммиака1. В крови избыток NH3 приводит к алкалозу (сдвиг рН в щелочную сторону). Ухудшается сродство Hb к кислороду гипоксия
тканей, накопление СО2 и замедление синтеза АТФ (дефицит
свободной энергии). Более всех страдают клетки ЦНС.
2. В клетках ЦНС избыток NH3 стимулирует образование
глутамина:
глутамат + NH3 + АТФ глутамин + АТФ + Фн
Накопление глутамина в цитоплазме – повышение осмотического давления и далее - отёк мозга.
3. NH3 легко диффундирует через клеточные и митохондриальные мембраны. Усиливается синтез глутамата, что вызывает
дефицит a-кетоглутаровой кислоты:
a-кетоглутарат + НАДН + NH3 глутамат + НАД+
5.
Дефицит a-кетоглутарата вызывает:• замедление трансаминирования и, как следствие, угнетается
синтез нейромедиаторов (дофамин, ацетилхолин и др.);
• торможение работы ЦТК (a-кетоглутарат – важнейший интермедиат цикла) дефицит энергии.
4. Ион NH4+, в отличие от NH3, не диффундирует через биомембраны. Избыток NH4+ нарушает трансмембранный транспорт Na+ и
K+ (конкуренция за ионные каналы). Одно из негативных последствий этого – нарушение проведения импульсов по отросткам
нервных клеток.
6.
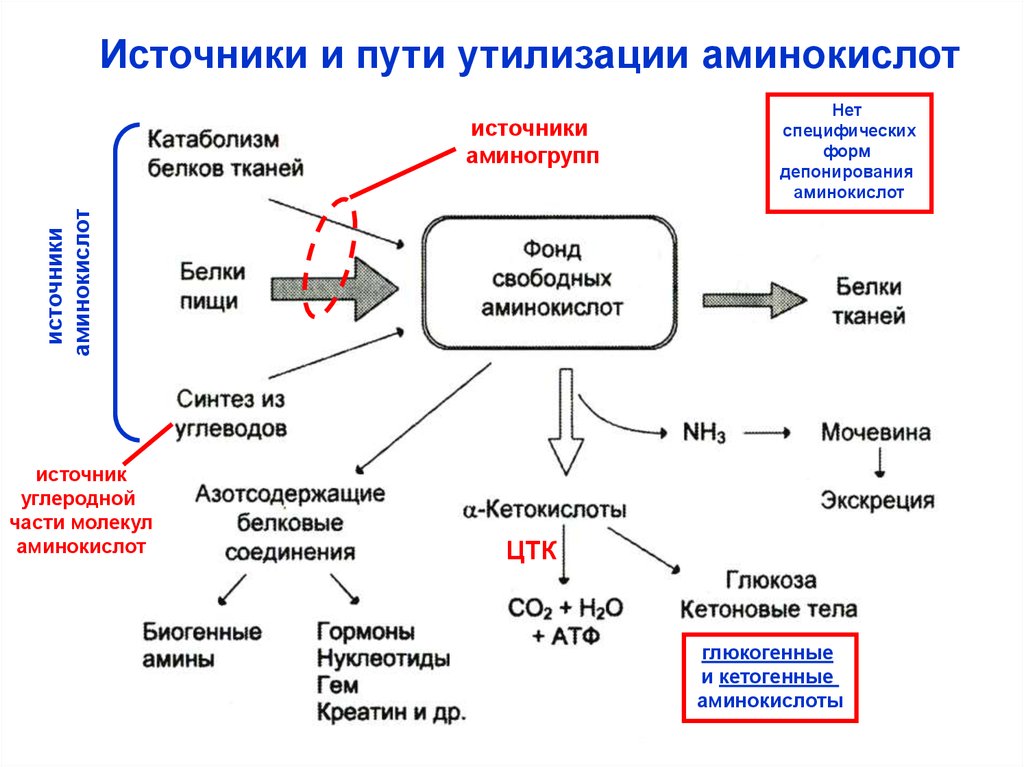
Обезвреживание аммиакаВысокая активность реакций
дезаминирования аминокислот
в тканях
В норме образуется
до 20 г аммиака / сутки
Низкая [NH3] в крови
(N: 25 – 40 мкмоль/л)
Увеличение в крови [NH3]
до 0,6 ммоль/л – судороги и
далее кома.
Высокая активность связывания
NH3 c образованием нетоксичных
продуктов и их выведение из
организма с мочой.
7.
Реакции связывания NH31. Основная реакция связывания аммиака происходит в митохондриях всех тканей (наиболее активно в мышцах, печени и
мозге):
глутаминсинтетаза
глутамат + NH3 + АТФ
глутамин + АДФ + Фн
Mg2+
Синтезированный глутамин выходит из клеток путём облегченной диффузии и поступает в кровь. С током крови глутамин
доставляется в энтероциты и почки.
Энтероциты:
глутаминаза
(большая
глутамин
глутамат + NH3 часть выводится почками)
трансаминирование
глутамат + пируват
a-кетоглутарат + аланин
(через v. portae доставляется в печень)
8.
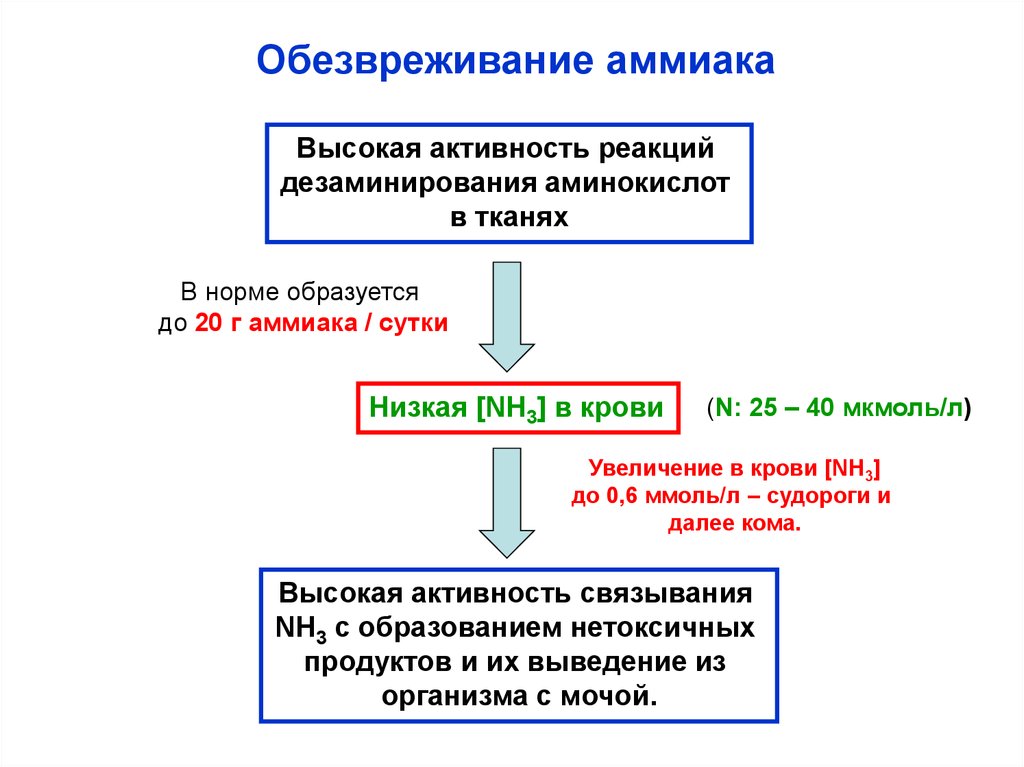
СО - NH2I
(CH2)2
I
HC - NH2
I
COOH
глутамин
+H2O
глутаминаза
СОOH
I
(CH2)2
I
HC - NH2
I
COOH
глутамат
+ NH3
аммиак
9.
Почки:С участием почечной глутаминазы (аналогично с энтероцитами) происходит гидролиз глутамина с освобождением NH3.
Аммиак нейтрализует кислые продукты обмена, превращается в
соли аммония (NH3 + H+ NH4+) и экскретируется с мочой.
В норме в почках образуется и выводится ок. 0,5 г солей
аммония в сутки.
В условиях ацидоза происходит индукция синтеза почечной
глутаминазы, что важно для восстановления нарушенного
кислотно-щелочного гомеостаза организма и предотвращения
потери значительной части Na+ и K+.
В условиях алкалоза количество глутаминазы почек уменьшается.
10.
2. Обезвреживание аммиака путем синтеза аспарагина:+ NH3 + ATP
аспартат
аспарагин + AMP + PPi
аспарагинсинтетаза
(глутаминзависимая)
3. Восстановительное аминирование a-кетоглутарата:
a-кетоглутарат
+ NH3 + НАДН
глутамат-ДГ
глутамат
+ NH3 + ATP
глутамин
глутаматсинтетаза
Реакция способствует связыванию 2 молекул аммиака (NH3).
Мышечная масса в организме сравнительно велика;
Мышцы интенсивно окисляют глюкозу и аминокислоты (источники энергии);
Активность мышечной глутамат-ДГ сравнительно мала, а
непрямое дезаминирование аминокислот малоэффективно;
Мышцы выделяют много аланина, в составе которого выводится избыток аммиака.
11.
Цикл глюкоза - аланин6
5
1
3
4
2
1 – Образование аланина при окислении аминокислот в гликолизе
2 – Выход аланина в кровь
3 – Непрямое дезаминирование аланина в печени
4 – Обезвреживание аммиака в орнитиновом цикле
5 – Включение пирувата в глюконеогенез
6 – Глюкоза поступает из крови в мышцы, где вновь окисляется до пирувата
12.
Основная масса аммиака обезвреживается в печени путёмсинтеза водорастворимого соединения – мочевины – в орнитиновом цикле.
NH2
I
C=O
I
NH2
Мочевина – полный амид угольной кислоты; С-атом происходит из СО2, только один атом азота - из аммиака.
Мочевина – основной конечный продукт азотистого обмена
(90% всего выводимого азота). В норме ежесуточно выделяется
ок. 25 г мочевины.
И.П. Павлов установил, что мочевина образуется исключительно в печени.
В 40-х годах ХХ в. Кребс и Гензеляйт показали, что синтез
мочевины – циклический метаболический процесс. Ключевой
метаболит, замыкающий цикл – орнитин.
Позже цикл синтеза мочевины получил название «орнитиновый цикл» или «цикл Кребса – Гензеляйта».
13.
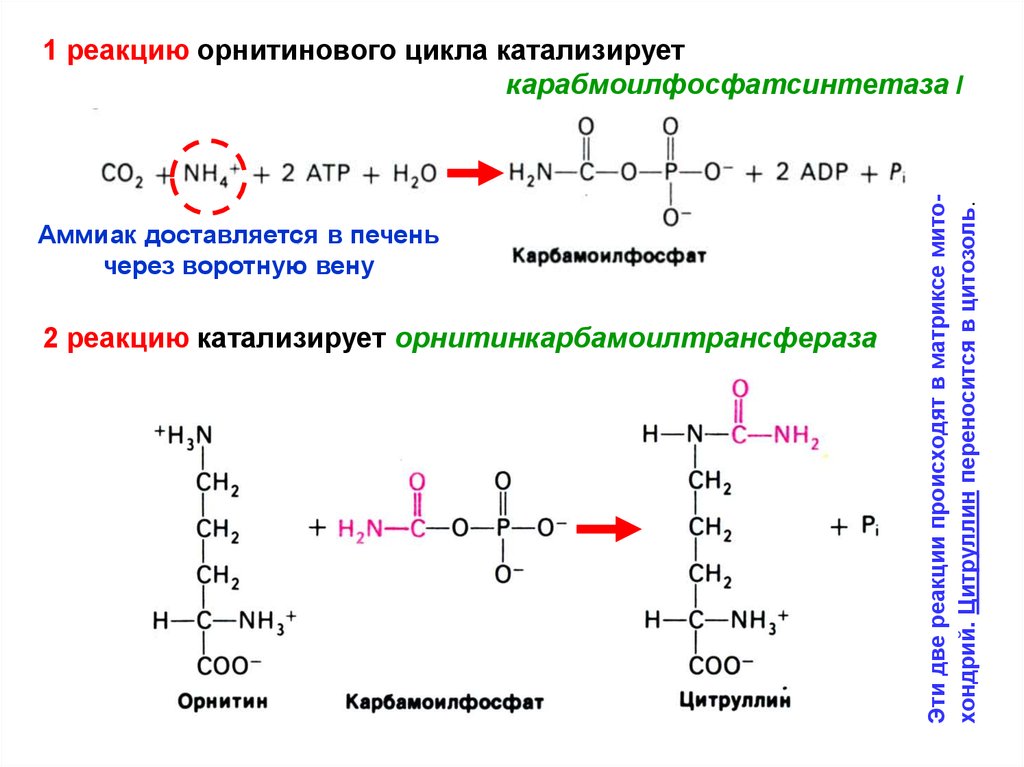
Аммиак доставляется в печеньчерез воротную вену
2 реакцию катализирует орнитинкарбамоилтрансфераза
Эти две реакции происходят в матриксе митохондрий. Цитруллин переносится в цитозоль.
1 реакцию орнитинового цикла катализирует
карабмоилфосфатсинтетаза I
14.
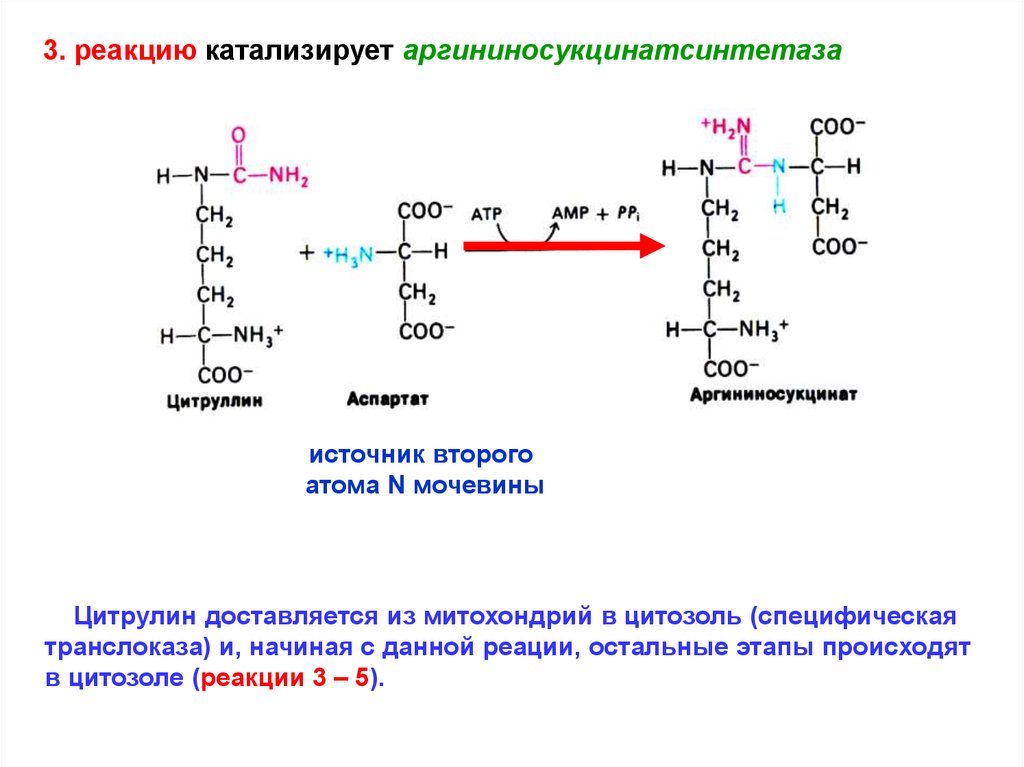
3. реакцию катализирует аргининосукцинатсинтетазаисточник второго
атома N мочевины
Цитрулин доставляется из митохондрий в цитозоль (специфическая
транслоказа) и, начиная с данной реации, остальные этапы происходят
в цитозоле (реакции 3 – 5).
15.
4. реакцию катализирует аргининосукцинатлиазаамингруппа аспартата
оказывается в составе
аргинина
16.
5. реакцию катализирует аргиназаОбразовавшийся орнитин возвращается в матрикс митохондрий
(специфическая транслоказа), где он снова взаимодействует с новой
молекулой карбамоилфосфата и цикл замыкается.
17.
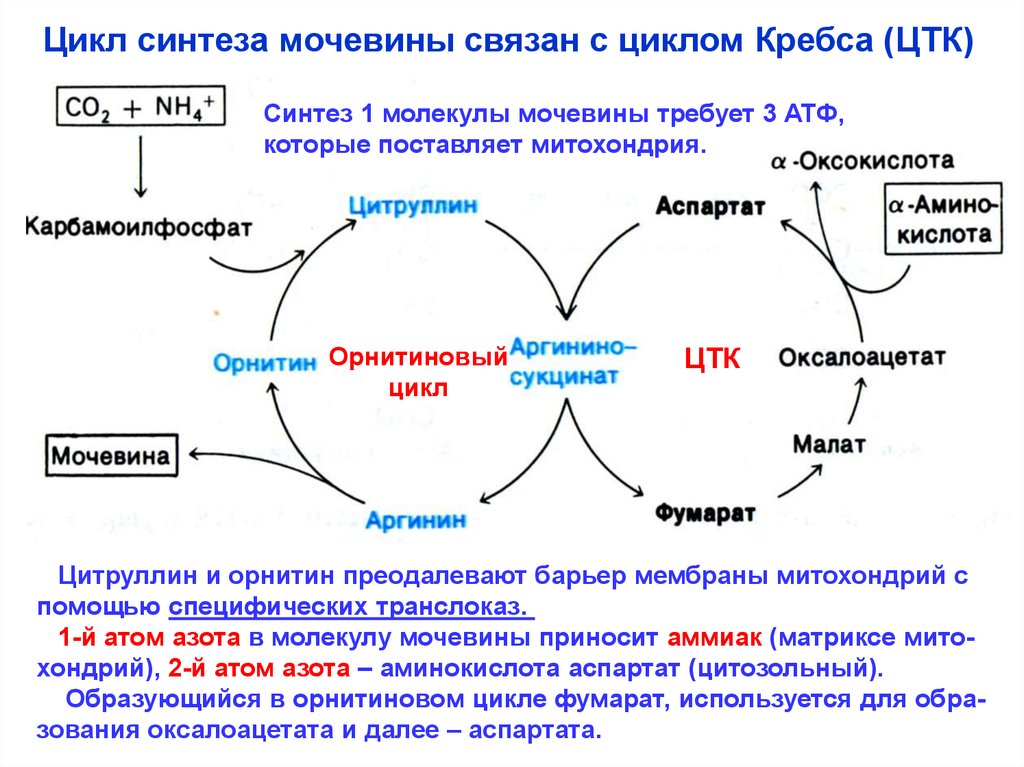
Цикл синтеза мочевины связан с циклом Кребса (ЦТК)Синтез 1 молекулы мочевины требует 3 АТФ,
которые поставляет митохондрия.
Орнитиновый
цикл
ЦТК
Цитруллин и орнитин преодалевают барьер мембраны митохондрий с
помощью специфических транслоказ.
1-й атом азота в молекулу мочевины приносит аммиак (матриксе митохондрий), 2-й атом азота – аминокислота аспартат (цитозольный).
Образующийся в орнитиновом цикле фумарат, используется для образования оксалоацетата и далее – аспартата.











 Биология
Биология