Похожие презентации:
Современное состояние и пути совершенствования стандартизации лекарственных средств
1. СОВРЕМЕННОЕ СОСТОЯНИЕ И ПУТИ СОВЕРШЕНСТВОВАНИЯ СТАНДАРТИЗАЦИИ ЛЕКАРСТВЕННЫХ СРЕДСТВ
СОВРЕМЕННЫЕ МЕТОДЫФАРМАЦЕВТИЧЕСКОГО
АНАЛИЗА
2. СОВРЕМЕННЫЕ МЕТОДЫ ФАРМАЦЕВТИЧЕСКОГО АНАЛИЗА
АНТРОПОВА Г.А.,доцент кафедры
фармации
3.
ФАРМАЦЕВТИЧЕСКИЙ АНАЛИЗЭто наука о химической характеристике и
измерении биологически активных веществ на
всех этапах производства: от контроля сырья
до оценки качества полученного ЛВ, изучения
его стабильности, установления сроков
годности и стандартизации готовой
лекарственной формы.
4. КРИТЕРИИ ФАРМ. АНАЛИЗА
1. ИЗБИРАТЕЛЬНОСТЬ МЕТОДА2. ТОЧНОСТЬ
ВОСПРОИЗВОДИМОСТЬ
ПРАВИЛЬНОСТЬ
3. ЧУВСТВИТЕЛЬНОСТЬ
ПРЕДЕЛ ОБНАРУЖЕНИЯ
4. ФАКТОР ВРЕМЕНИ
5.
ФОРМЫ (ИЛИ ВИДЫ) ФАРМ. АНАЛИЗА1. ФАРМАКОПЕЙНЫЙ АНАЛИЗ
2. ПОСТАДИЙНЫЙ КОНТРОЛЬ
ПРОИЗВОДСТВА ЛЕК. СРЕДСТВ
3. АНАЛИЗ ЛЕК. ФОРМ ИНДИВИДУАЛЬНОГО
ИЗГОТОВЛЕНИЯ
4. ЭКСПРЕСС-АНАЛИЗ
5. БИОФАРМАЦЕВТИЧЕСКИЙ АНАЛИЗ
6.
Отбор проб (выборок) лекарственных средствНа федеральном уровне определены следующие
цели отбора проб (выборок) ЛС:
1) экспертиза качества ЛС при государственной регистрации
ЛС;
2) проверка качества, проведение испытаний образцов ЛС при
осуществлении государственного контроля (надзора) в сфере
обращения ЛС;
3) проведение испытаний ЛС, зарегистрированных и
внесенных в Государственный Реестр, в аккредитованных
испытательных лабораториях для подтверждения
соответствия в форме принятия декларации о соответствии.
7.
Стандартом, устанавливающим отбор проб вРФ, является ОФС «Отбор проб (выборок) ЛС»,
включенная в ГФХI издания.
Статья регламентирует общие правила,
особенности отбора проб ЛС в расфасовке «ангро»
и отбора проб готовых ЛС (штучной продукции) с
целью проведения анализа выборки и выдачи
заключения о качестве ЛС. Методы отбора проб
лекарственного растительного сырья установлены
ОФС 42-0013-03 «Правила приемки лекарственного
растительного сырья и методы отбора проб».
8.
ПОРЯДОК ОТБОРА ПРОБЫУКАЗАН В ФС, ИЛИ В ОФС (ГФ XI, т. 2, с. 15)
Отбор пробы производят только из
неповрежденных, укупоренных и упакованных
согласно НТД упаковочных единиц.
При отборе проб (выборок) необходимо
принимать меры предосторожности, учитывая
токсичность, взрывоопасность, огнеопасность,
гигроскопичность и другие свойства ЛС,
а также предохранять их от загрязнений.
9.
МНОГОСТУПЕНЧАТЫЙ ОТБОР ПРОБ:I ступень: отбор единиц упаковочной тары (ящиков,
коробок, мешков…)
II ступень: отбор упаковочных единиц, находящихся
в упаковочной таре (коробок, флаконов, банок…)
III ступень: отбор продукции в первичной упаковке
(ампул, флаконов, туб, контурных упаковок…)
10.
Из отобранных напоследней ступени
упаковочных единиц после
контроля по внешнему виду
берут пробу (выборку) для
исследования препарата на
соответствие требованиям
НТД в количестве,
необходимом для 4 полных
физико-химических
анализов
(для контролирующих
организаций — на 6
полных физико-химических
анализов).
11.
Из расфасовки «ангро» берут точечные пробы,взятые примерно в равных количествах из верхнего,
среднего и нижнего слоев каждой упаковочной единицы.
После установления однородности все эти пробы
смешивают.
При отборе проб сыпучих и вязких ЛС точечные
пробы отбирают пробоотборником, изготовленным из
инертного материала.
Одноразовый пробоотборник
Зональные пробоотборники
12.
Жидкие ЛС сначала тщательно перемешивают. Вслучае, если перемешивание жидкости затруднено
(большие емкости), точечные пробы отбирают без
перемешивания из разных слоев.
Отбор выборок готовых ЛС (штучной продукции)
проводят из ненарушенных заводских упаковочных
единиц.
Отбор выборок готовых ЛС для инъекций на
отсутствие в них механических включений должен
производиться согласно действующей инструкции.
13.
СВЕРХЧИСТЫЙ ПРОБООТБОР ЖИДКОСТЕЙ14.
На всех фармацевтических предприятиях производится постоянныйконтроль качества используемой воды. Объектами контроля являются:
вода питьевая как материал для получения воды очищенной. В
основном проверяется сторонними организациями, например, водоканалом.
вода очищенная – вода, полученная дистилляцией, обратным
осмосом, деионизацией, ультрафильтрацией или комбинацией методов, используемая
в нестерильном фармацевтическом производстве.
вода для инъекций, полученная дистилляцией в несколько этапов
и предназначенная для растворения ЛВ перед фильтрацией и для последнего
ополаскивания первичной тары фарм. продукции, приготовляемой асептически.
Отбор проб проводится в определенных точках:
Пробы должны отбирать обученные работники, метод отбора проб должен
быть задокументирован
Пробы воды для проведения микробиологических анализов должны
помещаться в стерильную тару
Пробы воды в тот же день должны быть проанализированы в
микробиологической лаборатории
Пробы для определения эндотоксинов должны отбираться в специальную
апирогенную тару
Порядок пробоотбора – микробиология, эндотоксины, химический разбор,
остальные анализы
15.
Изучение имеющегося международного опыта подокументам ВОЗ, Европейского Союза, Таможенного Союза,
ведущих зарубежных фармакопей показало, что наибольший
объём информации содержит «Руководство ВОЗ по отбору
проб фармацевтических продуктов и связанных с ними
материалов» (WHO guidelines for sampling of pharmaceutical
products and related materials. Annex 4. WHO Technical Report
Series. No 929.2005).
Руководство ВОЗ предназначено как для органов надзора,
лабораторий контроля качества, таможенных и полицейских служб, так и
для производителей, оптовых и розничных звеньев обращения ЛС и может
быть применено к различным классам и типам фармацевтических
продуктов и связанных с ними материалов. В Руководстве ВОЗ уделено
внимание выбору надлежащего плана отбора проб, действиям при
выполнении процедуры отбора проб различных объектов, приведены
рекомендации по выбору оборудования для отбора проб (требования к
пробоотборникам), обращается внимание на практический аспект проверки
однородности отобранных проб и др.
16. ЭТАПЫ ФАРМ. АНАЛИЗА
1.2.
3.
4.
5.
6.
ХАРАКТЕРИСТИКА ВНЕШНЕГО ВИДА.
ОПИСАНИЕ. РАСТВОРИМОСТЬ.
ПОДЛИННОСТЬ.
ИСПЫТАНИЕ НА ЧИСТОТУ.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ.
ЗАКЛЮЧЕНИЕ О СООТВЕТСТВИИ ЛС
ТРЕБОВАНИЯМ НД.
17. ОБЩИЕ ПРИНЦИПЫ ИСПЫТАНИЙ ПОДЛИННОСТИ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ
I. ФИЗИЧЕСКИЕ МЕТОДЫ УСТАНОВЛЕНИЯПОДЛИННОСТИ
А. АГРЕГАТНОЕ СОСТОЯНИЕ
Б. ОКРАСКА, ЗАПАХ
В. ФОРМА КРИСТАЛЛОВ, ИЛИ ВИД
АМОРФНОГО ВЕЩЕСТВА
Г. ГИГРОСКОПИЧНОСТЬ ИЛИ СТЕПЕНЬ
ВЫВЕТРИВАЕМОСТИ НА ВОЗДУХЕ
Д. УСТОЙЧИВОСТЬ К ВОЗДЕЙСТВИЮ СВЕТА,
КИСЛОРОДА ВОЗДУХА
Е. ЛЕТУЧЕСТЬ, ПОДВИЖНОСТЬ,
ВОСПЛАМЕНЯЕМОСТЬ ЖИДКОСТЕЙ
18.
1. ОПРЕДЕЛЕНИЕ СТЕПЕНИ БЕЛИЗНЫПОРОШКООБРАЗНЫХ ЛС
ГФ XI, Т. 1, с. 47
СТЕПЕНЬ БЕЛИЗНЫ ОЦЕНИВАЮТ ИНСТРУМЕНТАЛЬНЫМИ
МЕТОДАМИ НА ОСНОВЕ СПЕКТРАЛЬНОЙ ХАРАКТЕРИСТИКИ
СВЕТА, ОТРАЖЕННОГО ОТ ОБРАЗЦА.
ИЗМЕРЯЮТ КОЭФФИЦИЕНТЫ
ОТРАЖЕНИЯ (r) – ЭТО
ОТНОШЕНИЕ ВЕЛИЧИНЫ
ОТРАЖЕННОГО СВЕТОВОГО
ПОТОКА К ВЕЛИЧИНЕ
ПАДАЮЩЕГО СВЕТОВОГО
ПОТОКА
19.
2. ТЕМПЕРАТУРА ПЛАВЛЕНИЯГФ XI, Т. 1, с. 16
ЭТО ТЕМПЕРАТУРА, ПРИ
КОТОРОЙ ТВЕРДОЕ ТЕЛО
НАХОДИТСЯ В РАВНОВЕСИИ
С ЖИДКОЙ ФАЗОЙ ПРИ
НАСЫЩЕННОЙ ФАЗЕ ПАРА
КАПИЛЛЯРНЫЙ МЕТОД
Прибор для определения температуры
плавления: 1 - колба; 2 - пробирка; 3 термометр; 4 - капилляр.
20.
Для веществ, неустойчивыхпри нагревании, определяют
температуру разложения.
Температурой разложения
называют температуру, при которой
происходит резкое изменение
физического состояния вещества
(вспенивание) при нагревании.
21.
Приборы серии МР свысокой точностью
определяют температуру
или интервал плавления.
Кроме этого, MP
оснащены микровидеокамерой и мощным
ПО, позволяющим
наблюдать за процессом
плавления, изменением
цвета и фазовыми
превращениями на экране
прибора, а также делать
видеозапись
происходящих процессов.
22.
3. ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУРЫЗАТВЕРДЕВАНИЯ
ГФ XI, Т. 1, с. 20
Температурой
затвердевания называют
температуру, при
которой вещество
переходит из жидкого
состояния в твердое при
охлаждении.
1 - толстостенная пробирка; 2 - термометр; 3 - мешалка;
4 - пробирка (воздушная баня); 5 - стакан; 6 - термометр.
23.
4. ТЕМПЕРАТУРНЫЕ ПРЕДЕЛЫПЕРЕГОНКИ И ТОЧКА КИПЕНИЯ
Под температурными пределами перегонки
подразумевают интервал между начальной и конечной
температурой кипения при нормальном давлении 101,3
кПа (760 мм рт. ст.).
Точка кипения —
скорректированная
температура, при
которой давление пара
жидкости достигает
101,3 кПа.
ГФXII, с. 36
24.
5. ПЛОТНОСТЬГФXII, с. 36
Плотность - масса единицы объема
вещества
Метод 1
Применяют для определения плотности
жидкостей с точностью до ± 0,001 г/см3 с
помощью пикнометра.
Метод 2
Применяют для определения плотности твердых
жиров и воска. Проводят все операции с
дистиллированной водой и высушивают
пикнометр, как описано в методе 1.
25.
ПИКНОМЕТРЫдля жидкостей
для газов
для твердых и
сыпучих материалов
26.
Метод 3Применяют для определения плотности
жидкостей с точностью до ± 0,01 г/см3 с
помощью ареометра.
Метод 4
Применяют для определения плотности
жидкостей и газов в малом объеме (1-2 мл) с
точностью до ± 0,0001 г/см3 с помощью
плотномера.
Принцип измерения плотности
плотномером основан на определении
периода колебаний U-образной
измерительной трубки определенного
объема, вызываемых электромагнитным
генератором. При заполнении трубки
испытуемым веществом частота колебаний
трубки меняется в зависимости от массы
(плотности) вещества (ИЗМЕРЯЕТСЯ
ДАТЧИКОМ).
27.
6. ВЯЗКОСТЬГФ XI, Т. 1, с. 87
Вязкость (внутреннее трение) - свойство текучих
тел оказывать сопротивление перемещению
одной их части относительно другой.
Различают динамическую,
кинематическую, относительную,
удельную, приведенную и
характеристическую вязкости.
вязкость одной жидкости
относительно другой —
относительная вязкость
28.
Динамическая вязкость или коэффициентвязкости (η). ВЫРАЖАЮТ в паскальсекундах (Па*c)- система СИ. Динамическую
вязкость (η) обычно выражают в пуазах (пз)
или сантипуазах (1 спз = 0,01 пз).
Жидкость имеет вязкость 1 пз, если
напряжение сдвига
1 дин/см2 создает скорость сдвига 1 с1.
29.
ВЯЗКОСТЬКинематическую вязкость (v), получают делением величины
динамической вязкости η на плотность жидкости р,
выраженную в килограммах на метр кубический (кгхм3),
измеренную при той же температуре
КИНЕМАТИЧЕСКУЮ ВЯЗКОСТЬ обычно выражают в
стоксах (ст) или сантистоксах (1 сст = 0,01 ст),
в системе СИ - в метрах квадратных на секунду (м2хс _1)
Для измерения кинематической вязкости применяются
капиллярные вискозиметры типа Оствальда и Уббелоде с
различными модификациями.
30.
Вискозиметр спадающим
шариком
1 - калибровочные
отметки; 2 — шарик
Вискозиметр стеклянный
капиллярный ВПЖ
Вискозиметр состоит из
капилляра с радиусом R и
длиной L, через который под
действием силы тяжести
протекает жидкость объема V.
31.
Вискозиметр спадающим
шариком
Thermo Electron «Haake тип С»
Вискозиметр с падающим
шариком проводит
измерение вязкости
прозрачных ньютоновских
жидкостей (образцов).
Результаты измерения
даются в единицах
динамической вязкости.
32.
7. РАСТВОРИМОСТЬПОНЯТИЕ РАСТВОРИМОСТИ
приводится в качестве
характеристики
приблизительной
растворимости
лекарственного вещества при
температуре от 15 до 25 °С.
ГФ XI, Т. 1, с. 176
ГФ XII, с. 92
Колба
Эрленмейера
33.
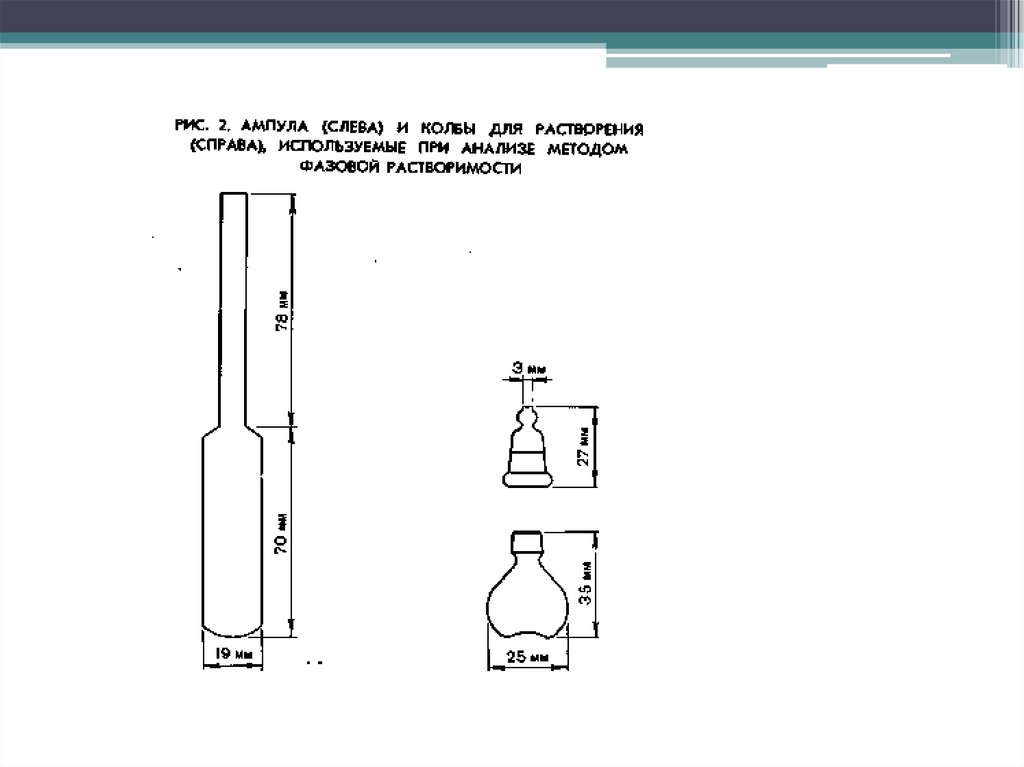
8. МЕТОД ФАЗОВОЙ РАСТВОРИМОСТИГФ XI, т. 1, с. 149
ЭТО КОЛИЧЕСТВЕННАЯ ОЦЕНКА СТЕПЕНИ ЧИСТОТЫ
ЛВ ПУТЕМ ТОЧНЫХ ИЗМЕРЕНИЙ ЗНАЧЕНИЙ
РАСТВОРИМОСТИ.
МЕТОД ОСНОВАН НА ПРАВИЛЕ ФАЗ ГИББСА
(УСТАНАВЛИВАЕТ ЗАВИСИМОСТЬ МЕЖДУ ЧИСЛОМ
ФАЗ И ЧИСЛОМ КОМПОНЕНТОВ В УСЛОВИЯХ
РАВНОВЕСИЯ).
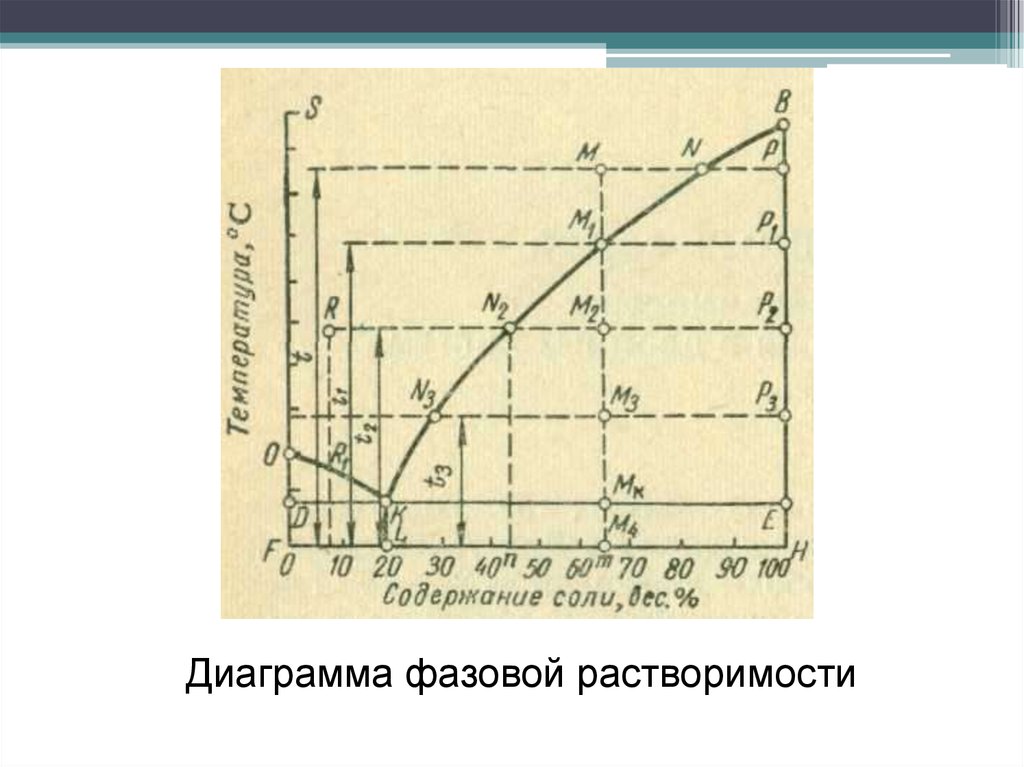
ПО ДИАГРАММЕ ФАЗОВОЙ РАСТВОРИМОСТИ
ОПРЕДЕЛЯЮТ СОДЕРЖАНИЕ РАСТВОРЕННОГО ЛВ, т.е.
УСТАНАВЛИВАЮТ, ЯВЛЯЕТСЯ ЛИ ИСПЫТУЕМЫЙ
ПРЕПАРАТ ИНДИВИДУАЛЬНЫМ ВЕЩЕСТВОМ ИЛИ
СМЕСЬЮ.
34.
35.
Диаграмма фазовой растворимости36.
II. ХИМИЧЕСКИЕ МЕТОДЫУСТАНОВЛЕНИЯ ПОДЛИННОСТИ
ДЛЯ ОПРЕДЕЛЕНИЯ ПОДЛИННОСТИ ИСПОЛЬЗУЮТ
СОЧЕТАНИЕ ГРУППОВЫХ И СПЕЦИФИЧЕСКИХ
ХИМИЧЕСКИХ РЕАКЦИЙ
СОЗДАНЫ
УНИФИЦИРОВАННЫЕ
МЕТОДИКИ ДЛЯ
ИДЕНТИФИКАЦИИ,
ОБЪЕДИНЕНЫ В ОФС
«ОБЩИЕ РЕАКЦИИ НА
ПОДЛИННОСТЬ»
ГФ XI, Т. 1, с. 159
37.
1. УСТАНОВЛЕНИЕ ПОДЛИННОСТИНЕОРГАНИЧЕСКИХ ЛВ
А) РЕАКЦИИ ОСАЖДЕНИЯ
Б) ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ
РЕАКЦИИ
В) РЕАКЦИИ НЕЙТРАЛИЗАЦИИ И
РАЗЛОЖЕНИЯ АНИОНОВ
Г) ИЗМЕНЕНИЕ ОКРАСКИ БЕСЦВЕТНОГО
ПЛАМЕНИ
Д) ИЗМЕНЕНИЯ, ПРОИСХОДЯЩИЕ ПРИ
НАГРЕВАНИИ И ПРОКАЛИВАНИИ
ПРЕПАРАТОВ
38.
2. ИДЕНТИФИКАЦИЯЭЛЕМЕНТООРГАНИЧЕСКИХ ЛВ
3. СПОСОБЫ ИСПЫТАНИЙ
ПОДЛИННОСТИ ОРГАНИЧЕСКИХ ЛВ
А) ОБЩИЕ ХИМИЧЕСКИЕ РЕАКЦИИ
ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Б) РЕАКЦИИ ОБРАЗОВАНИЯ СОЛЕЙ И
КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
В) ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ
ОСНОВАНИЙ И ИХ СОЛЕЙ
39.
III. ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫГазовая
хроматография
Высокоэффективная
жидкостная
хроматография
ИКспектроскопия
40. ИСПЫТАНИЯ НА ЧИСТОТУ
ЧИСТОТА ЛЮБОГО ВЕЩЕСТВАРЕГУЛИРУЕТСЯ ЧЕРЕЗ НОРМИРОВАНИЕ В
НЕМ ПРИМЕСЕЙ И ЯВЛЯЕТСЯ НАИБОЛЕЕ
СЛОЖНЫМ ВОПРОСОМ КАЧЕСТВА
41.
ПРИМЕСЬ – ЭТО ЛЮБОЙ КОМПОНЕНТСУБСТАНЦИИ, КОТОРЫЙ НЕ ЯВЛЯЕТСЯ
ХИМИЧЕСКИМ ОБЪЕКТОМ,
ОПРЕДЕЛЯЕМЫМ КАК ИССЛЕДУЕМАЯ
СУБСТАНЦИЯ.
ПРИМЕСЬ - ЛЮБОЙ НЕЖЕЛАТЕЛЬНЫЙ
КОМПОНЕНТ ПРОМЕЖУТОЧНОГО
СОЕДИНЕНИЯ ИЛИ АКТИВНОГО
ИНГРЕДИЕНТА.
42.
РАЗЛИЧНЫЕ ВИДЫ ПРИМЕСЕЙ1. ЧУЖЕРОДНЫЕ ВЕЩЕСТВА
(foreign substances)
2. ТОКСИЧНЫЕ ПРИМЕСИ
(toxic impurities)
3. СОПУТСТВУЮЩИЕ ВЕЩЕСТВА
(concomitant components)
ко-эффекторы (co-effectors)
4. СИГНАЛЬНЫЕ ПРИМЕСИ
(signal impurities)
43.
5. ОБЫЧНЫЕ ПРИМЕСИ(ordinary impurities)
6. РОДСТВЕННЫЕ ВЕЩЕСТВА
(related substances)
7. ПРОИЗВОДСТВЕННЫЕ
ЗАГРЯЗНЯЮЩИЕ ВЕЩЕСТВА
(process contaminants)
44.
ПО ИСТОЧНИКУ ПОЛУЧЕНИЯИЛИ ПО СПОСОБУ ПОПАДАНИЯ:
1.ПРОДУКТ ДЕГРАДАЦИИ (ПРИОБРЕТЕННЫЕ)
2.ПРОИЗВОДСТВЕННОЕ ЗАГРЯЗНЯЮЩЕЕ
ВЕЩЕСТВО
(ПРИМЕСИ ТЕХНОЛОГИЧЕСКИЕ)
ОСНОВНОЙ КРИТЕРИЙ
ДОБРОКАЧЕСТВЕННОСТИ:
наличие допустимых пределов
физиологически неактивных
примесей и отсутствие токсичных
45.
ПО ПРИРОДЕ ПРИМЕСИ ДЕЛЯТСЯ:1. ХИМИЧЕСКИЕ
А) ОСТАТОЧНЫЕ РАСТВОРИТЕЛИ
Б) ОРГАНИЧЕСКИЕ ПРИМЕСИ
(ИДЕНТИФИЦИРОВАННЫЕ,
НЕИДЕНТИФИЦИРОВАННЫЕ,
ПОТЕНЦИАЛЬНЫЕ ПРИМЕСИ)
В) НЕОРГАНИЧЕСКИЕ ПРИМЕСИ
2. СТРУКТУРНЫЕ (СТЕРЕОИЗОМЕРЫ)
3. ФИЗИЧЕСКИЕ (ПОЛИМОРФНЫЕ)
4. БИОЛОГИЧЕСКИЕ
5. БИОХИМИЧЕСКИЕ
46. СПОСОБЫ ИСПЫТАНИЙ НА ЧИСТОТУ
ВСЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВАНЕЗАВИСИМО ОТ СПОСОБА
ПОЛУЧЕНИЯ ИСПЫТЫВАЮТ НА
ЧИСТОТУ
47.
1. ИСПЫТАНИЯ НА ЧИСТОТУ ИДОПУСТИМЫЕ ПРЕДЕЛЫ ПРИМЕСЕЙ:
ОФС ГФ XI, т. 1, с. 165
ОБЩИЕ ИСПЫТАНИЯ НА ПРИМЕСИ
НЕОРГАНИЧЕСКИХ ИОНОВ
ПУТИ ОПРЕДЕЛЕНИЯ
МАКСИМАЛЬНОГО
СОДЕРЖАНИЯ ПРИМЕСЕЙ
1.
2.
СРАВНЕНИЕ С ЭТАЛОНОМ (СТАНДАРТОМ)
ПО ОТСУТСТВИЮ ПОЛОЖИТЕЛЬНОЙ
РЕАКЦИИ
48.
2. ОПРЕДЕЛЕНИЕ ЛЕТУЧИХВЕЩЕСТВ И ВОДЫ
Вода в веществе может содержаться в виде
капиллярной, абсорбционной связанной, химически
связанной (гидратной и кристаллогидратной) или
свободной.
Влажность обычно характеризуется
количеством воды в веществе, выраженным в
процентах (%) от первоначальной массы влажного
вещества (массовая влажность) или её объёма
(объёмная влажность).
49.
КАЧЕСТВЕННЫЕ МЕТОДЫ ОБНАРУЖЕНИЯ ВЛАГИА) С ПОМОЩЬЮ ОРГАНИЧЕСКИХ
РАСТВОРИТЕЛЕЙ
Проба на содержание влаги в органических
растворителях алифатического ряда. Определение
основано на том, что в присутствии следов воды взаимная
растворимость алифатических (например, ацетон) и
ароматических (бензол, толуол) растворителей понижается
(помутнение раствора).
С повышением температуры взаимная
растворимость повышается и муть исчезает. Проба очень
чувствительна и дает возможность определить следы
влаги.
50.
Б) ПРОБА С БЕЗВОДНЫМ CuSO4В присутствии влаги безводный сульфат меди
переходит в кристаллогидрат, вследствие чего
окраска соли меняется - становится голубой.
В) ОХЛАЖДЕНИЕ
По помутнению при охлаждении до ОºС
Г) ПРИ ПОМОЩИ ПИКРИНОВОЙ
КИСЛОТЫ
Сравнивая окраску с эталонным раствором
51.
Д) ПРОБА НА СОДЕРЖАНИЕ ВЛАГИ,ОСНОВАННАЯ НА ГИДРОЛИЗЕ ЭТИЛАТА
АЛЮМИНИЯ
Проба заключается в том, что при смешении
толуольного раствора этилата алюминия с испытуемым
веществом при наличии влаги в нем в зависимости от
ее содержания образуется слабая муть (осадок гидрата
окиси алюминия):
Аl(С2Н5O)3 + 3Н2О→Аl(ОН)3↓+ 3С2Н5ОН
Реакция дает положительный результат при
содержании влаги в веществе 0,05% и более.
52.
КОЛИЧЕСТВЕННЫЕ МЕТОДЫОПРЕДЕЛЕНИЯ ВЛАГИ
А) МЕТОД ВЫСУШИВАНИЯ
ГФ XI, т. 1, с. 176
X=
(m-m1 )×100
m
Х – влажность
вещества, %
m – масса вещества до высушивания, г
m1 – масса вещества после высушивания, г
53.
Б) ОПРЕДЕЛЕНИЕ ВОДЫ МЕТОДОМДИСТИЛЛЯЦИИ ГФ XI, т. 1, с. 177
Метод основан на физическом свойстве паров двух
несмешивающихся жидкостей (воды и органического
растворителя) – перегоняться при более низкой
температуре, чем каждая из этих жидкостей
V ∙ 100
X = --------m
Х – содержание воды, %
V – объем воды, отсчитываемый по градуированной
пробирке, мл
m – масса ЛВ, взятая для анализа, г
54.
В) МЕТОД ТИТРОВАНИЯ РЕАКТИВОМК.ФИШЕРА
ГФ XI, т. 1, с. 177
Реактив К. Фишера: раствор диоксида серы, йода и
пиридина в метиловом спирте.
I2 + SO2 + H2O + 3 C5H5N →
→ 2C6H5N • HI + C5H5NSO3
C5H5NSO3 + CH3OH →
→ C6H5N • HSO4CH3
55.
Объёмометрический титратор870KF Titrino plus фирмы
Metrohm предназначен для
определения влаги
по Карлу Фишеру в диапазоне
100 ppm... 100%.
KF Титратор для повседневных
анализов. Отображение кривой
объем/время на ЖК дисплее в
режиме реального времени.
56.
Г) МЕТОД ГЖХ;ОТРАЖАТЕЛЬНАЯ СПЕКТРОФОТОМЕТРИЯ
Автоматический анализатор
влагосодержания
«AND MX-50»
Принцип действия
анализаторов основан на
высушивании образца с
одновременным
автоматическим
взвешиванием на электронных
весах.
57.
3.УСТАНОВЛЕНИЕ рН средыКИСЛОТНОСТЬ ИЛИ ЩЕЛОЧНОСТЬ
рН
ГФ XI, т. 1, с. 113
колориметрический способ
потенциометрический способ
58.
4. Определение прозрачности и степенимутности жидкостей
Эталонами для
определения степени мутности служат взвеси из
гидразина сульфата (1%) и гексаметилентетрамина
(10%).
ОФС 42-0051-07 ГФ XII, с. 98
Испытуемую жидкость считают прозрачной, если
она по прозрачности не отличается от воды или
растворителя, используемого при приготовлении
испытуемой жидкости, или выдерживает сравнение с
эталоном I, т.е. ее опалесценция (мутность) не превышает
опалесценцию (мутность) эталона I при просмотре в
описанных выше условиях.
59.
60.
61.
62.
5. Определение окраски жидкостейОФС ГФ XI, т. 1, с. 194
Исходные растворы: CoCl2, K2Cr2O7, CuSO4, FeCl3 и
H2SO4 0,1 моль/л
ОФС 42-0050-07 ГФ XII, с. 93
Окраску жидкостей определяют визуально одним из
методов, приведенных в ОФС, путем сравнения с
соответствующими эталонами.
Прозрачность раствора, Цветность раствора.
Данные испытания обязательно вводят для субстанций,
используемых для приготовления парентеральных,
глазных, назальных и ушных ЛС. Концентрация
испытуемых растворов должна быть приближена к
концентрации изготавливаемой из этой субстанции ЛФ.
Определение цветности раствора особенно важно для
оценки качества белых, почти белых или белых с оттенком
субстанций.
63.
Окраску жидкостей определяют визуально путем сравнения ссоответствующими эталонами цветности.
эталон
ЛС
Исследуемые жидкости и эталоны берут для сравнения в равных
количествах.
Сравнение производят в пробирках одинакового стекла и диаметра
при дневном отраженном свете на матово - белом фоне.
Окраска исследуемого образца должна быть вполне идентична эталону
или только приближаться к отмеченной окраске, не превышая ее по
интенсивности, но несколько отличаясь от нее по тону.
64.
• Жидкость, которая должна бытьбесцветной, рассматривают сверху через
весь слой жидкости на матово - белом
фоне.
• ГЛУТАМИНОВАЯ КИСЛОТА
Раствор, 1 г субстанции в 10 мл
1 М раствора хлороводородной кислоты
должен быть бесцветным или выдерживать
сравнение с эталоном В9
40 мм
Бесцветными считают жидкости, которые по
цвету не отличаются от воды, а в случае
растворов - от соответствующего растворителя
или выдерживают сравнение с эталоном В9, т.е.
должны быть окрашены не более интенсивно,
чем эталон В9 .
65.
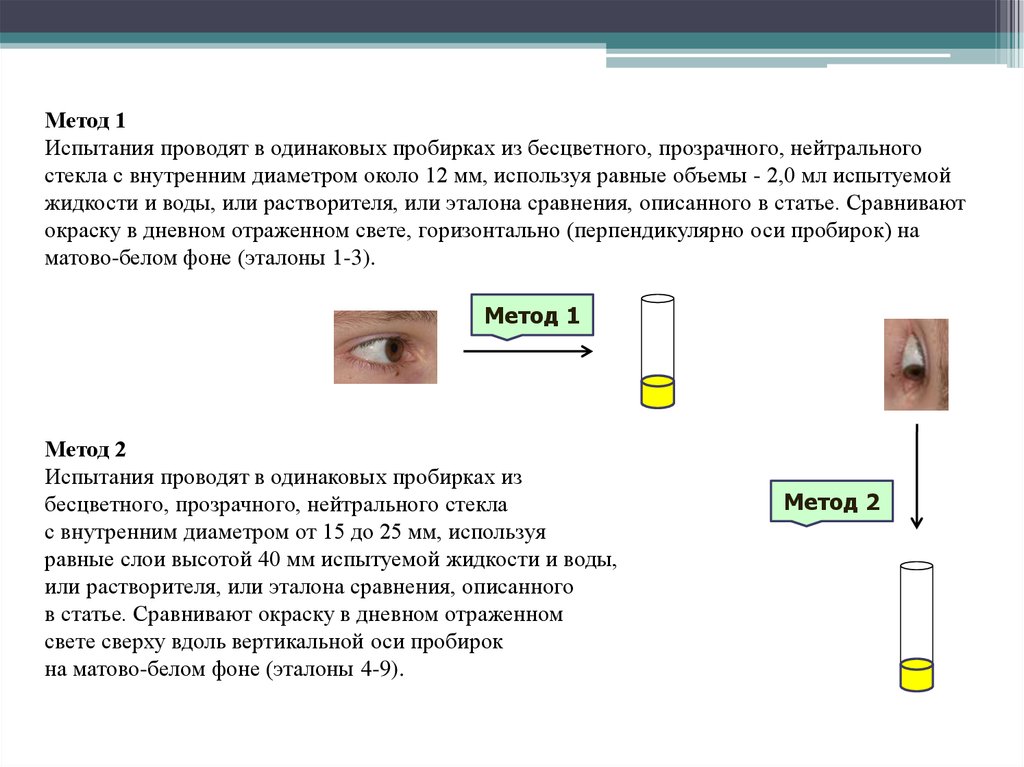
Метод 1Испытания проводят в одинаковых пробирках из бесцветного, прозрачного, нейтрального
стекла с внутренним диаметром около 12 мм, используя равные объемы - 2,0 мл испытуемой
жидкости и воды, или растворителя, или эталона сравнения, описанного в статье. Сравнивают
окраску в дневном отраженном свете, горизонтально (перпендикулярно оси пробирок) на
матово-белом фоне (эталоны 1-3).
Метод 1
Метод 2
Испытания проводят в одинаковых пробирках из
бесцветного, прозрачного, нейтрального стекла
с внутренним диаметром от 15 до 25 мм, используя
равные слои высотой 40 мм испытуемой жидкости и воды,
или растворителя, или эталона сравнения, описанного
в статье. Сравнивают окраску в дневном отраженном
свете сверху вдоль вертикальной оси пробирок
на матово-белом фоне (эталоны 4-9).
Метод 2
66.
Приготовление исходных растворовЖелтый раствор... FeCl3 χ 6 Н20
растворяют в смеси, приготовленной из 25 мл концентрированной
хлористоводородной кислоты и 975 мл воды
Красный раствор. СоС12 х 6 Н2O
Голубой раствор. CuSO4 x 5 Н2O
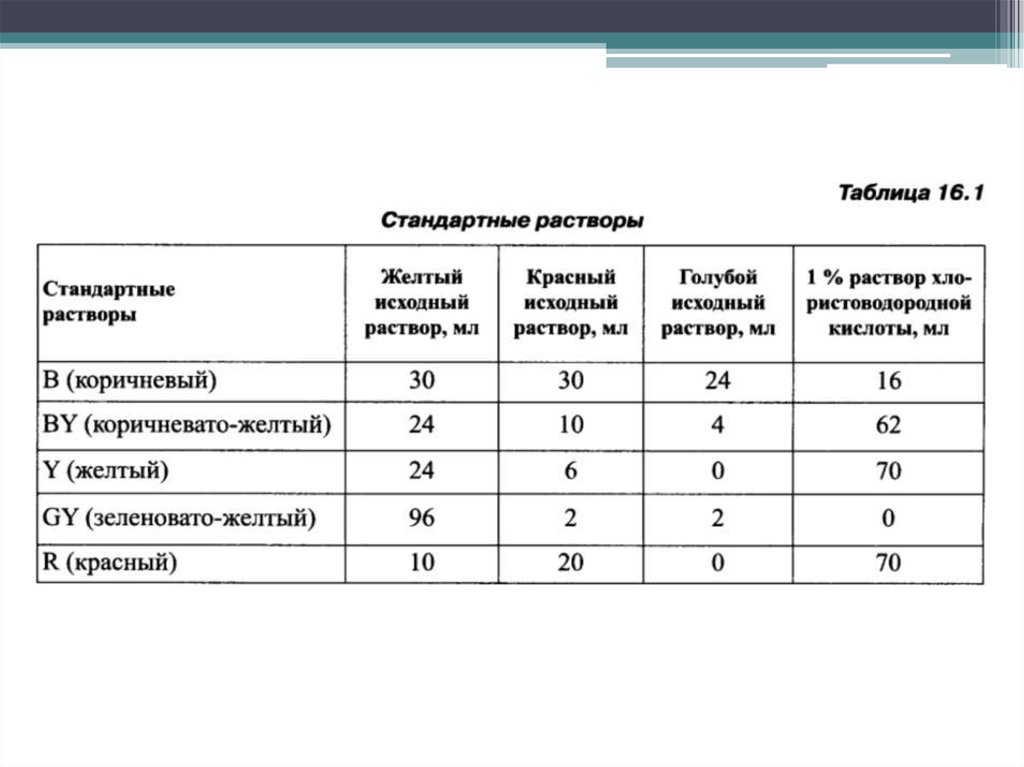
Приготовление стандартных растворов
Стандартные растворы, получаемые смешением
исходных растворов железа хлорида, кобальта
хлорида и меди сульфата с 1 % раствором
хлористоводородной кислоты, представлены в
табл. 16.1.
67.
68.
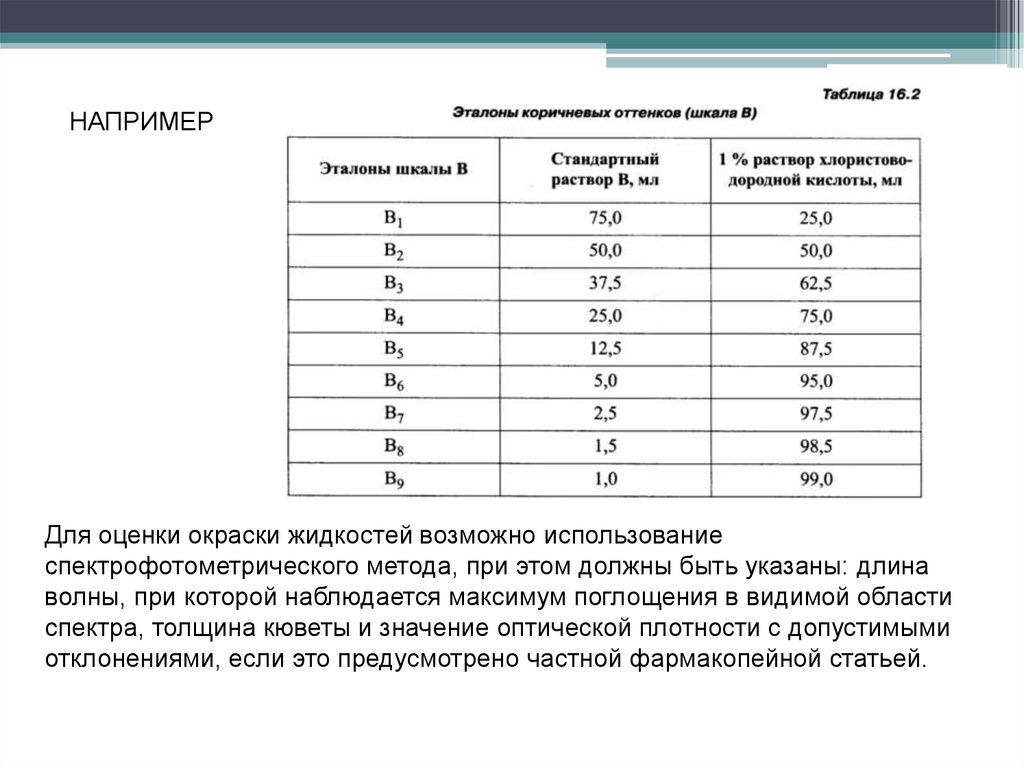
Приготовление эталоновЭталоны готовят из пяти стандартных растворов
путем разбавления их 1 % раствором
хлористоводородной кислоты.
Количества компонентов для приготовления эталонов
цветности приведены в табл. 16.2-16.6.
Сравнение степени окраски жидкости с эталонами (В, BY, Υ, GY, R)1-3
обычно проводят по методу I; в случае использования эталонов В4.9, (BY, Υ,
GY, R)4-7 применяют метод II.
Степень окраски испытуемого раствора не должна превышать
степень окраски соответствующего эталона. Цвет испытуемого образца
должен быть максимально приближен к цвету соответствующего эталона.
69.
НАПРИМЕРДля оценки окраски жидкостей возможно использование
спектрофотометрического метода, при этом должны быть указаны: длина
волны, при которой наблюдается максимум поглощения в видимой области
спектра, толщина кюветы и значение оптической плотности с допустимыми
отклонениями, если это предусмотрено частной фармакопейной статьей.
70.
6. Примеси органических веществ7. ОПРЕДЕЛЕНИЕ ЗОЛЫ
ОФС ГФ XI, т. 2, с. 24
Определение общей золы
Прокаливание навески препарата в тигле
(m посл. взвеш. - m тигля, г) • 100
X =--------------------------------------------m лек. вещества
71.
Определение золы, нерастворимой вхлороводородной кислоте
К остатку в тигле + 15 мл 10% HCl
накрывают
стеклом и нагревают 10 минут, затем фильтруют, переносят в
тигель, высушивают, сжигают, прокаливают, взвешивают.
Определение сульфатной золы
Получают после нагревания и прокаливания навески
препарата, обработанной концентрированной серной
кислотой.
72.
8. ОПРЕДЕЛЕНИЕ ПОКАЗАТЕЛЕЙКАЧЕСТВА ЖИРНЫХ И ЭФИРНЫХ МАСЕЛ
В состав готовых ЛФ часто входят
различные жиры. Жиры представляют собой
сложные эфиры глицерина и высших
органических предельных и непредельных кислот
(в основном С10-C18).
Для аналитической характеристики жиров
применяются специфические показатели кислотное число, число омыления, йодное число,
эфирное число.
73.
А) КИСЛОТНОЕ ЧИСЛОПриродные жиры нейтральны. Однако при
хранении или переработке могут частично
произойти процессы омыления или окисления,
вследствие чего образуется примесь свободных
жирных кислот. Количество этих кислот может быть
охарактеризовано кислотным числом.
ОФС ГФ XI, т. 1, с. 191
Кислотное число – количество мг калия
гидроксида, необходимого для нейтрализации
свободных кислот, содержащихся в 1 г
исследуемого вещества
74.
Б) ЧИСЛО ОМЫЛЕНИЯ(ОФС ГФ XI, т. 1, с. 192) –
количество мг калия гидроксида,
необходимое для нейтрализации
свободных кислот и кислот,
образующихся при полном гидролизе
сложных эфиров, содержащихся в 1 г
исследуемого вещества.
Число омыления для большинства жиров обычно колеблется в
пределах от 150 до 195. Малые числа омыления указывают на присутствие
высокомолекулярных кислот или неомыленных веществ. Высокое число
омыления свидетельствует о повышенном содержании кислот относительно
низкомолекулярных.
75.
В) ЭФИРНОЕ ЧИСЛО(ОФС ГФ XI, т. 1, с. 193) –
количество мг калия гидроксида,
необходимое для нейтрализации кислот,
образующихся при полном гидролизе
сложных эфиров, содержащихся в 1 г
исследуемого вещества.
Эфирное число определяют по разности
между числом омыления и кислотным
числом.
76.
Г) ЙОДНОЕ ЧИСЛО(ОФС ГФ XI, т. 1, с. 193) –
количество г йода, связываемое 100 г
исследуемого вещества.
Для определения йодного числа применяют
растворы хлорида йода - ICl, бромида йода - IBr или
йода в растворе сулемы, которые обладают большей
реакционной способностью, чем растворы йода в
спирте или других растворителях. Йодное число
является мерой ненасыщенности кислот жиров. Оно
особенно важно для оценки качества высыхающих
масел.
77.
Д) ГИДРОКСИЛЬНОЕ ЧИСЛО– количество мг КОН, необходимое
для нейтрализации кислоты,
выделяющейся при ацетилировании 1 г
исследуемого вещества.
Определяют по реакции с уксусным
ангидридом и последующем титровании спиртовым
раствором КОН.
78.
Е) ПЕРЕКИСНОЕ ЧИСЛО–количество перекиси, выраженное в
миллиэквивалентах активного
кислорода, содержащееся в 1000 г
испытуемого вещества.
Определяют по реакции с калия йодидом в
смеси уксусной кислоты и хлороформа, затем
выделившийся йод оттитровывают натрия
тиосульфатом.
79.
Ж) АНИЗИДИНОВОЕ ЧИСЛО- при перекисном окислении жиров и
липидов образуются сопряженные диеновые
гидроперекиси, и величина оптической
активности характеризует степень
окисленности испытуемого вещества.
80.
9. ВОССТАНАВЛИВАЮЩИЕВЕЩЕСТВА
КРАСЯЩИЕ ВЕЩЕСТВА
10. СПЕЦИФИЧЕСКИЕ ПРИМЕСИ
81.
КОЛИЧЕСТВЕННОЕОПРЕДЕЛЕНИЕ ЛЕК. СРЕДСТВ
1. ХИМИЧЕСКИЕ
2. ФИЗИЧЕСКИЕ
3. ФИЗИКОХИМИЧЕСКИЕ
4. БИОЛОГИЧЕСКИЕ
82.
СПАСИБО ЗАВНИМАНИЕ!













































































 Химия
Химия








