Похожие презентации:
Уравнения Михаэлиса – Ментен и Моно, кинетические модели различных ферментаций, соотношения для кинетических параметров роста
1.
ФГБОУ ВПО «Вятский государственный университет»Биологический факультет
Кафедра микробиологии
Дисциплина
«Основы физиологии роста и культивирования микроорганизмов»
«Уравнения Михаэлиса – Ментен и Моно, кинетические модели
различных ферментаций, соотношения для кинетических параметров
роста »
Выполнила магистрант Куликова Л.Е. БМм-11
Проверил: д.т.н., профессор Лещенко А.А.
1
2. Модели описания кинетики ферментативных реакций
1. Фермент и субстрат образуют фермент-субстратный комплекс за счет силфизической природы. В дальнейшем при распаде фермент-субстратного
комплекса высвобождается фермент и продукт.
(1)
где ,Е - фермент, Р- продукт, S - субстрат, ES - фермент— субстратный
комплекс, реакция образования которого обратима и характеризуется
константами К1– константа скорости прямой реакции, К-1 – константа
скорости обратной реакции, K+2 - константа скорости реакции
2. Концентрация субстрата выше концентрации фермента, поэтому при
[Р = 0], [ES] – const
V = K+2[ES]
(2)
где,V – скорость образования продукта
2
3. 3. Определение константы диссоциации фермент-субстратного комплекса Ks = (3) где, Ks - константа диссоциации (равновесия)
[E0]= [E] + [ES] или [E] = [E0] – [ES](4)
где, [E0]- общая концентрация фермента, [E] – концентрация свободного фермента
[ES] – фермент связанный в комплекс
из уравнения (3)
подставляем значения
[ES] =
[E] = [E0] – [ES]
из (4), получаем
[ES] Ks =[E0] [S] - [ES] [S] или
подставляем выражение (5) в V = K+2[ES] (2),
V=
[ES] =
(5)
получаем
(6)
где, K+2 [E0] – максимальная скорость достигаемая когда весь фермент
связан в комплекс
3
4. V = (7) или, принимая Ks = Km при k+2 ‹ k+1
V=или, принимая Ks = Km
V=
при
(7)
k+2 ‹ k+1
=
(8)
Уравнение Михаэлис-Ментен
где, Km = Ks - мера сродства фермента к субстрату
Km константа Михаэлиса-Ментен
4
5.
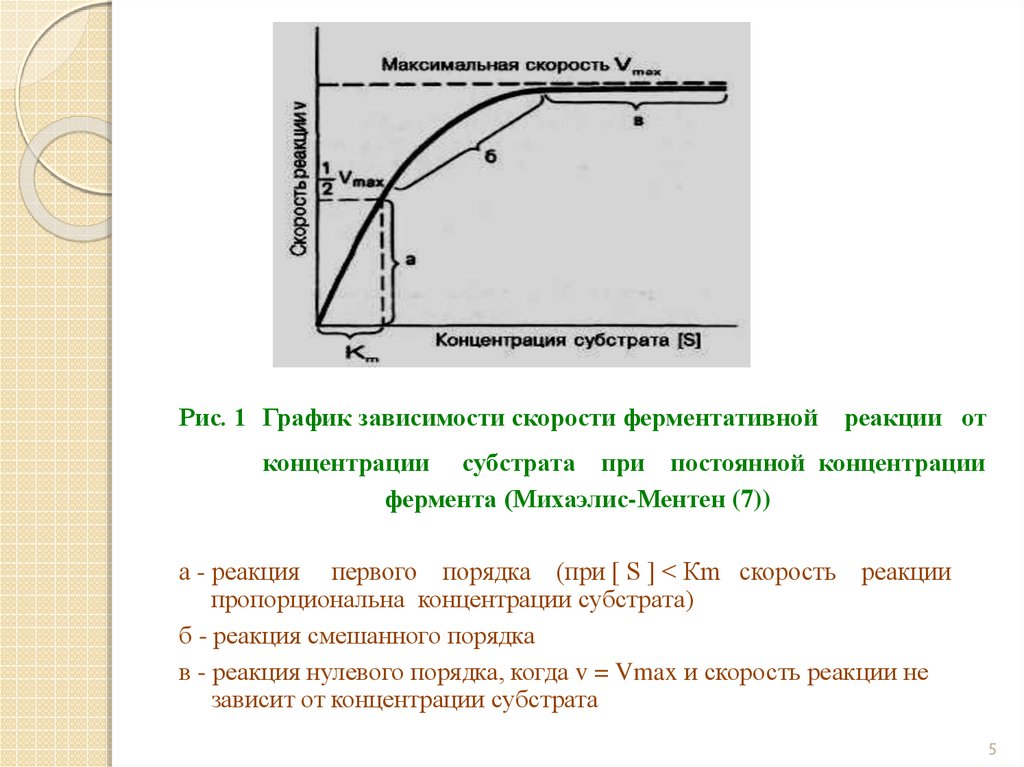
Рис. 1 График зависимости скорости ферментативнойреакции от
концентрации субстрата при постоянной концентрации
фермента (Михаэлис-Ментен (7))
а - реакция первого порядка (при [ S ] < Кm скорость реакции
пропорциональна концентрации субстрата)
б - реакция смешанного порядка
в - реакция нулевого порядка, когда v = Vmax и скорость реакции не
зависит от концентрации субстрата
5
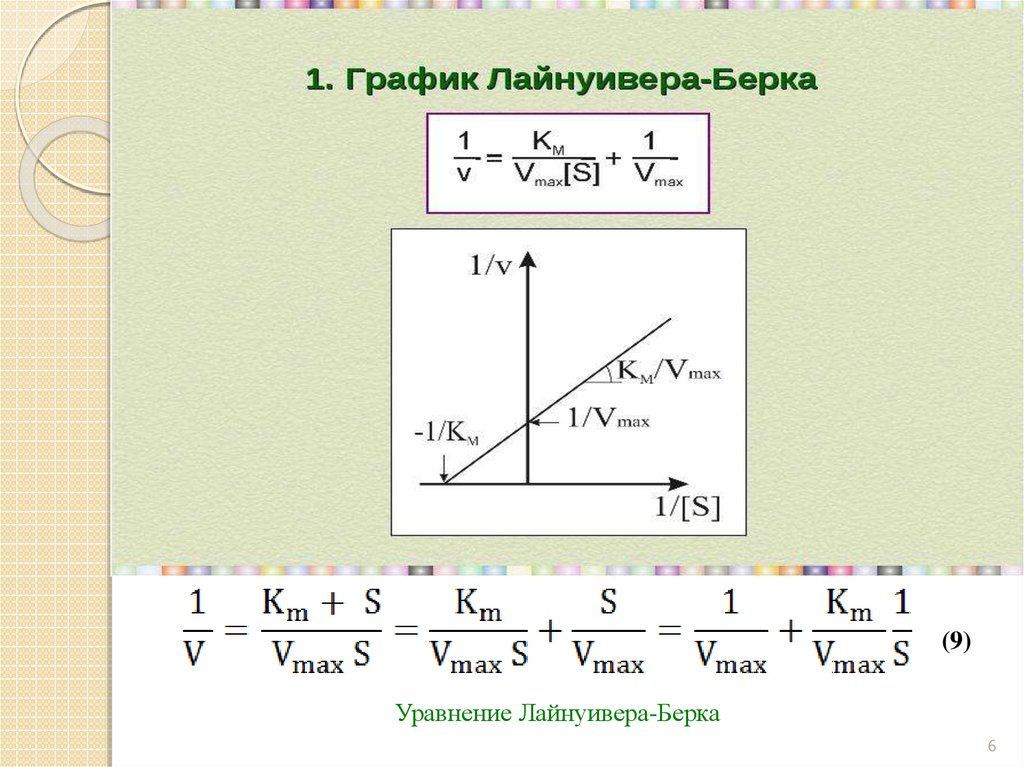
6.
(9)Уравнение Лайнуивера-Берка
6
7.
УравнениеМоно
описывает зависимость скорости роста
микроорганизмов от концентрации субстрата и идентично уравнению
Михаэлис-Ментен
(8)
(10)
(11)
Уравнение Моно
где, µ - удельная скорость роста; µm - максимальная величина удельной
скорости роста; Ks – концентрация субстрата, при которой удельная
скорость роста равна ½ максимальной (константа насыщения).
Рис. 3. Зависимость удельной скорости роста от концентрации субстрата по
модели Моно
7
8. Кинетические показатели параметров роста клетки
1. Общая скорость роста клетки(12)
2. Удельная скорость роста клетки
(13)
где µ = const
lnX = lnX0 + µt
(14)
(15)
где X0 – концентрация биомассы при t = 0
(16)
X = X0eµt
(17)
Выражение (17) экспоненциального роста
8
9. (18) Уравнение экспоненциального роста
■ удельная скорость роста (µ)связана со временем удвоения массы клеток
td соотношением
X = 2X0
тогда:
известно,
и
t = td
(19)
td = ln 2/µ = 0,693/µ
dX/dt = µX
Из уравнения (10) Моно получаем выражение для случая роста клетки
(20)
9
10. Кинетические модели различных ферментаций
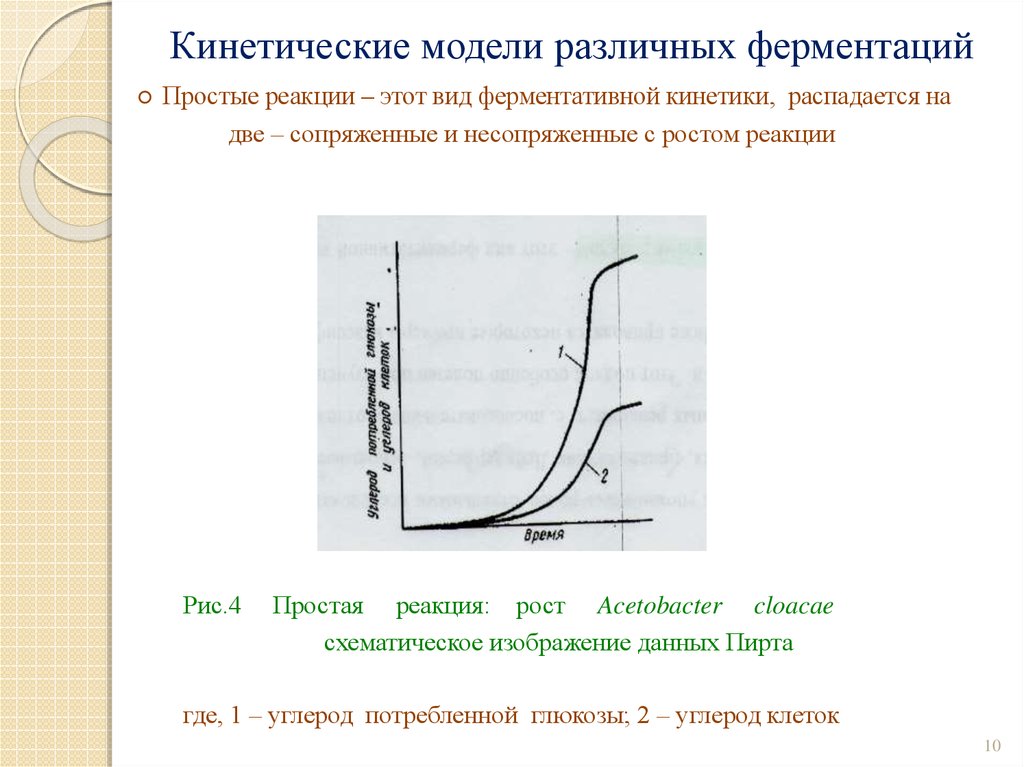
○ Простые реакции – этот вид ферментативной кинетики, распадается надве – сопряженные и несопряженные с ростом реакции
Рис.4
Простая реакция: рост Acetobacter cloacae
схематическое изображение данных Пирта
где, 1 – углерод потребленной глюкозы; 2 – углерод клеток
10
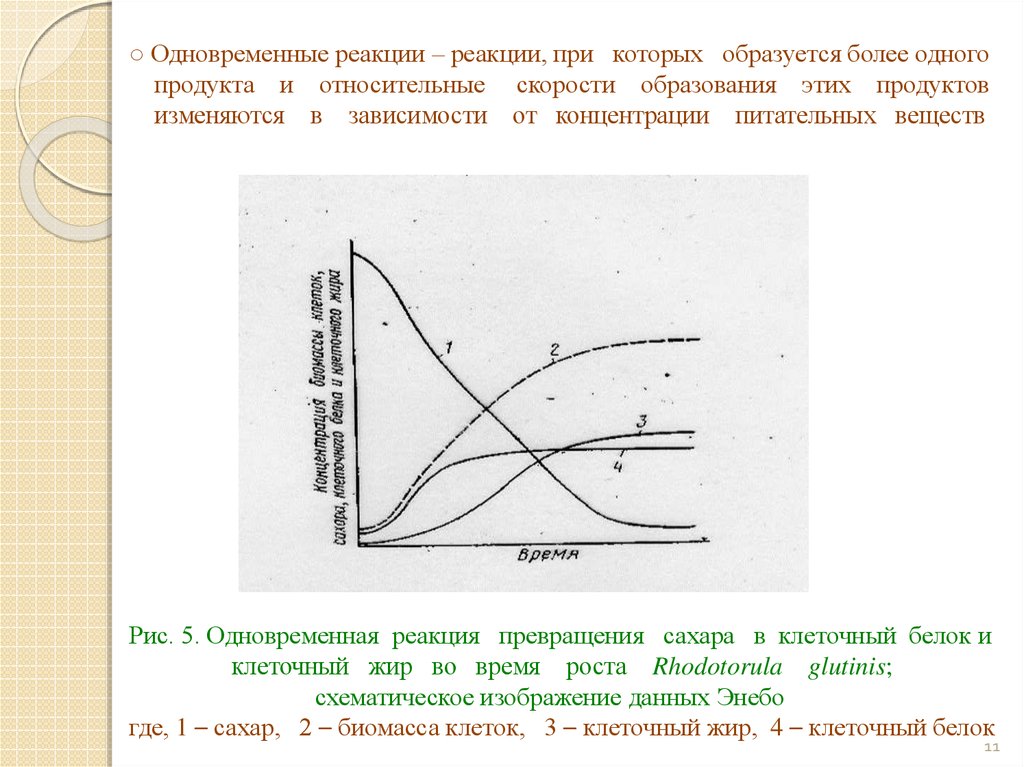
11. ○ Одновременные реакции – реакции, при которых образуется более одного продукта и относительные скорости образования этих
продуктовизменяются в зависимости от концентрации питательных веществ
Рис. 5. Одновременная реакция превращения сахара в клеточный белок и
клеточный жир во время роста Rhodotorula glutinis;
схематическое изображение данных Энебо
где, 1 – сахар, 2 – биомасса клеток, 3 – клеточный жир, 4 – клеточный белок
11
12. ○ Последовательные реакции – это реакции, в которых отдельный промежуточный продукт накапливается в каком-либо количестве перед
тем как образуется конечный продуктРис. 5. Последовательная реакция превращения глюкозы в глюконовую
кислоту Pseudomonas ovalis схематическое изображение данных
Рейли и Хемфри
где, 1 – глюкоза, 2 - глюконовая кислота, 3 – глюконолактон
12
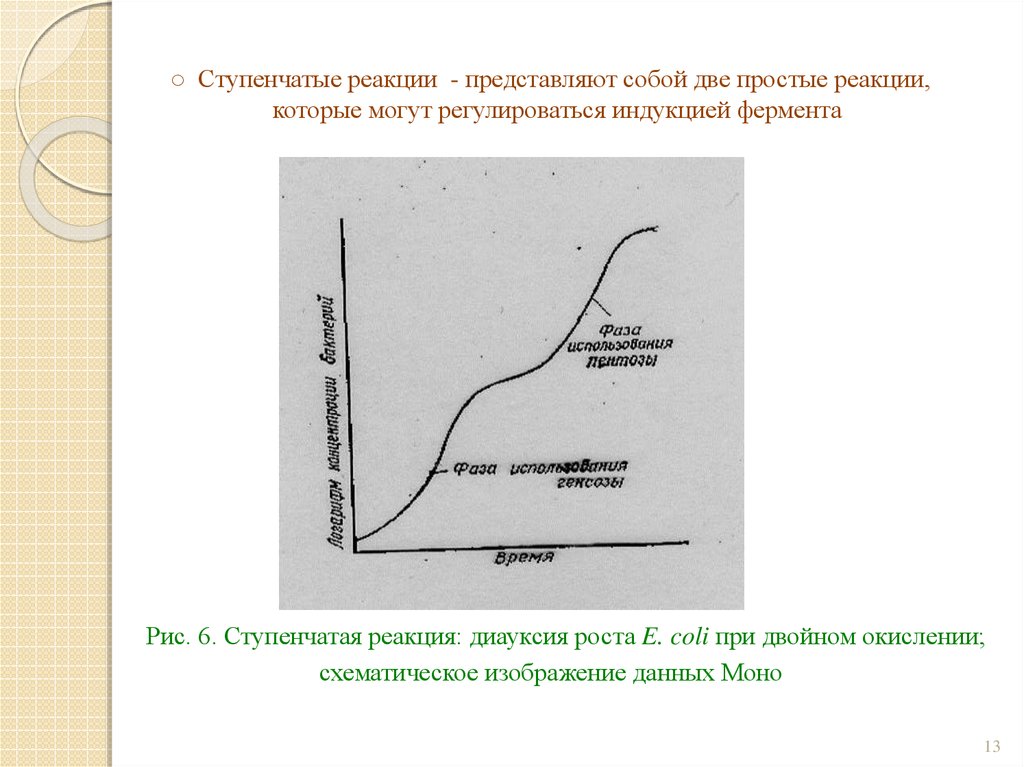
13. ○ Ступенчатые реакции - представляют собой две простые реакции, которые могут регулироваться индукцией фермента
Рис. 6. Ступенчатая реакция: диауксия роста E. coli при двойном окислении;схематическое изображение данных Моно
13
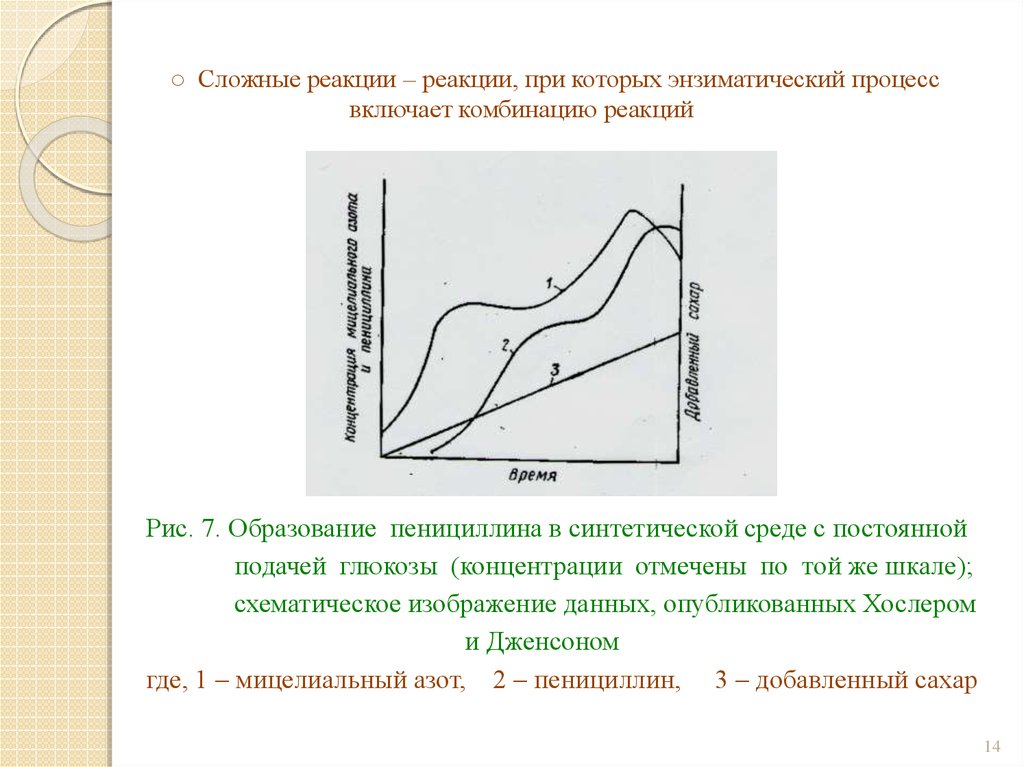
14. ○ Сложные реакции – реакции, при которых энзиматический процесс включает комбинацию реакций
Рис. 7. Образование пенициллина в синтетической среде с постояннойподачей глюкозы (концентрации отмечены по той же шкале);
схематическое изображение данных, опубликованных Хослером
и Дженсоном
где, 1 – мицелиальный азот, 2 – пенициллин, 3 – добавленный сахар
14









 Биология
Биология








