Похожие презентации:
Классификация химических методов
1. Лекция 8
2.
Химические методы получениянаноматериалов
3. Классификация химических методов
Чисто химические способы:• золь-гель синтез,
• синтез в мицеллах,
• химическое осаждение,
• удаление одного из компонентов гетерогенной системы.
4.
Особое место занимают методы, где наночастицы образуются врезультате различных «физических» воздействий, например,
ультразвука или микроволн.
С одной стороны, микроструктура получаемых в ходе воздействия
наноматериалов во многом определяется параметрами
физического воздействия: частотой, интенсивностью и так далее.
Однако это воздействие в первую очередь инициирует
прохождение в реакционной смеси различных процессов, в
первую очередь, химических реакций, что и приводит к
формированию материала с особенной микроструктурой, фазовым
составом, уникальными функциональными свойствами.
Следует отметить, что зачастую получить материал, обладающий
такими свойствами, не используя соответствующее «физическое»
воздействие, невозможно.
5.
Физико-химическая группа методов• с ультразвуком
• с микроволнами
• сольвотермальный синтез,
• синтез в сверхкритических растворителях,
• пиролиз аэрозолей
• большинство методов роста наночастиц или пленок из газовой
фазы
• химическое осаждение из газовой фазы (CVD),
• рост наноструктур по механизму пар-жидкость-кристалл.
6. Классификация химических методов
• методы, где наноматериал получают по той или иной химическойреакции, в которых участвуют определённые классы веществ;
• различные варианты электрохимических реакций.
• плазмохимический синтез
• криохимический синтез;
• пиролиз
7.
Методы синтеза наносред с помощью химических реакций весьмаразнообразны. Делят на три группы.
• К первой относятся методы, в которых диспергирование
происходит в ходе химического превращения (химические
реакции)
• Во вторую включены методы, основанные на различных
вариантах электрохимических реакций.
• К третьей группе относятся методы, в определенной степени
сочетающие химические и физические превращения.
8. Получение наноматериалов с использованием химических реакций
Метод осажденияМетод осаждения заключается в осаждении гидроксидов
металлов из растворов их солей с помощью осадителей. В
качестве последних используются щелочные растворы, например,
NH4OH, NaOH, КОН и др.
В общем виде процесс соответствует следующей реакции:
• Мех(А)y + (К)ОН —> Меx(ОН)y + КА,
• где А — анионы: NO3-, Cl- , SO42• К — катионы: Na+, NH+, К+;
• х, у — коэффициенты.
9.
Путем регулирования pH и температуры раствора возможносоздание оптимальных условий осаждения для получения
наноматериалов, при которых достигаются большие скорости
кристаллизации и, соответственно, образуется высокодисперсный
гидроксид. Полученный осадок промывают, сушат, прокаливают и,
при необходимости, восстанавливают.
Нанопорошки металлов, полученные данным методом, имеют
размер частиц от 10 до 150 нм. Варьируя параметры процесса
осаждения, можно изменять размер, а также получать порошки
сферической, игольчатой, чешуйчатой, неправильной формы.
10. Способ соосаждения
Синтез сложных гидроксидных соединений металловВ этом случае в реакционный сосуд одновременно из различных
емкостей подают осадитель и смешанный раствор солей металлов.
При постоянном перемешивании, а при необходимости, и нагреве,
протекает химическая реакция:
Ме'а (A)b + Me’’c(A)d + (К)ОН -> (Me', Ме'')x(ОН)y + КА,
где А — анионы; Me', Me” — катионы разных металлов и щелочи,
соответственно; a, b, с, d — коэффициенты.
11.
Далее, аналогично методу осаждения, порошок тщательноотмывают от растворенных анионов, сушат, а затем подвергают
термическому разложению и (или) восстановлению.
Данный метод позволяет получать сложные кислородсодержащие
соединения с заданным соотношением катионов, что приводит к
повышенной растворимости металлов друг в друге в конечном
продукте.
12. Осаждение в эмульсиях
Осаждение в эмульсиях получается в создаваемыхнесмешивающихся растворах. Таким образом можно получать
наночастицы, покрытые слом органических молекул.
Например, для синтеза наночастиц α-Fe203 с оболочкой
использовался водный раствор FeCl2 концентрацией 0,01 моль/л,
додецилбензол сульфанат натрия и бензол. Эмульсия получалась
при интенсивном перемешивании жидкостей.
Для осаждения в органической среде соединений железа
добавлялся NaOH. Средний размер частиц α-Fe203, покрытых слоем
органических молекул, по данным просвечивающей электронной
микроскопии составлял 2,1 нм.
13. Осаждение и соосаждение в наносостоянии
Можно получать оксидные, металлические и металлооксидныепорошки, композиции на их основе, ферриты и соли (например,
ВаТiO3) с частицами разной формы, химического и фазового
составов, дисперсностью, распределением по размерам.
Кроме того, материалы, синтезированные этими методами,
характеризуются высокой химической однородностью и
реакционной способностью.
14. Метод гетерофазного взаимодействия
Основан на замещении катионов или анионов твердой фазы наионы окружающей жидкой среды.
Метод используется для получения композиционных частиц, в
частности, наночастиц одного материала, покрытых слоем
другого.
Например, наночастицы CdS, покрытые слоем PbS, получали при
частичном замещении ионов кадмия на ионы свинца. Для этого
стабилизированные поливинилпирролидоном наночастицы CdS
помещали в раствор, содержащих катионы Рb2+. В зависимости от
концентрации Рb2+ и времени взаимодействия можно заместить
часть или весь кадмий на свинец.
Для наночастиц CdS размером 6 нм процесс их полного
превращения в PbS заканчивался за 2 часа.
15.
Метод позволяет также получать различные металлическиепорошки с размером частиц 10-100 нм, если осуществлять
взаимодействие твердой соли металлов с раствором щелочи.
Например, размер частиц нанопорошка Ni, полученного таким
образом, составил 20 нм. Форма конечных наночастиц металлов
определяется в данном методе морфологией кристаллов исходных
твердых солей.
16. Золь-гельный метод
Первоначально золь-гельный метод был разработан дляполучения порошка железа. Способ заключается в осаждении из
водных растворов нерастворимых металлических соединений в
виде геля и последующем их восстановлении.
Как показывает практика, в ходе процесса осуществляется
химическая очистка продукта. Например, содержание Fe в
конечном порошке составляет 98,5-99,5%.
В качестве исходных веществ используются соли железа, а также
отходы металлургического производства: лом металлов или
отработанный травильный раствор. Использование вторичного
сырья предоставляет возможность производства чистого и
относительно дешевого нанопорошка железа.
Данным методом можно получать и другие классы материалов в
наносостоянии: оксидную керамику, сплавы, соли металлов.
17.
В золь-гель методе сначала получают золь, а после сушки — гель,который может использоваться непосредственно для получения
пленок или монолитных изделий.
Весьма эффективно применение геля в качестве связки в
технологиях производства керамики, что не только облегчает
формование, но и снижает температуру обжига. Но чаще этим
методом из геля получают нанопорошки.
18.
Золь можно получить гидролизом солей слабых оснований (SiCl4,ТiCl4). Например, нанопорошок оксида титана был получен
гидролизом титанил-сульфата. С целью сдерживания процессов
взаимодействия наночастиц с окружающей средой воду можно
заменить на органическую среду.
19.
Первая стадия золь-гель метода получения наночастицзаключается в образовании лиозоля — растворителя, в котором
распределены коллоидные частицы диаметром 3 - 4 нм.
Чаще всего коллоидные частицы получают путем гидролиза
силикатов или органических производных кремния — силоксанов,
метокси-, этокси- или пропоксисиланов.
Важными параметрами при этом являются значение рН среды,
соотношение воды и кремния, наличие и природа катализатора.
Высокие значения рН и большой избыток воды способствуют
образованию коллоидных частиц, а низкие величины рН —
появлению линейных полимеров кремния.
Механизм протекающих химических реакций часто весьма сложен
и может включать катализ кислотами и основаниями.
20.
Вторая стадия — гелирование, при котором отдельные частицысцепляются и образуют пространственную сетку, а система
приобретает определенную форму. Эта стадия также может
протекать при высоких или низких значениях рН, что определяет
структуру образующегося после сушки материала.
Третья стадия — старение геля. В это время происходит
уплотнение пространственной сетки, сближение первоначальных
частиц, уменьшение ячеек сетчатой структуры, усадка
сформованного материала.
21.
Четвертая стадия — сушка — сопровождается образованиемматериала с пористостью 30-80 % и довольно крупными порами.
Эта стадия является весьма критичной, поскольку удаление
растворителя может привести к нарушению монолитности геля и
образованию из-за возникающих напряжений трещин.
Пятая стадия состоит в термическом уплотнении геля, снижении
пористости и среднего размера оставшихся пор.
22.
Шестая стадия — стеклование геля. Число и размер порзначительно сокращаются, а изделие приобретает свойства
обычного твердого стеклянного тела.
Для устранения образования трещин при сушке используют
добавки специальных веществ — химических регуляторов сушки
(ХРС). Эти добавки замедляют гидролиз, способствуют
образованию более разветвленной, но менее плотной
пространственной сетки Si02 с порами большего размера и более
однородными по размеру.
Повышение размера и однородности пор под действием кислых
ХРС приводит к более равномерному удалению растворителя из
пор и устранению трещин, возникающих вблизи крупных пор.
Щелочные реагенты действуют в обратном направлении:
увеличивают размер частиц и уменьшают размер пор.
23.
Сушку можно проводить не при обычных условиях, а всверхкритических, при повышенном давлении, что предотвращает
усадку и приводит к образованию ксерогеля с пористостью до 98 %.
При получении порошков и тонких покрытий усадка и
растрескивание при сушке меньше, чем при получении массивных
изделий. Для получения порошков и микросфер используют
диспергирование концентрированных гидрозолей и проведение
гелирования с помощью водоотнимающего органического реагента.
24.
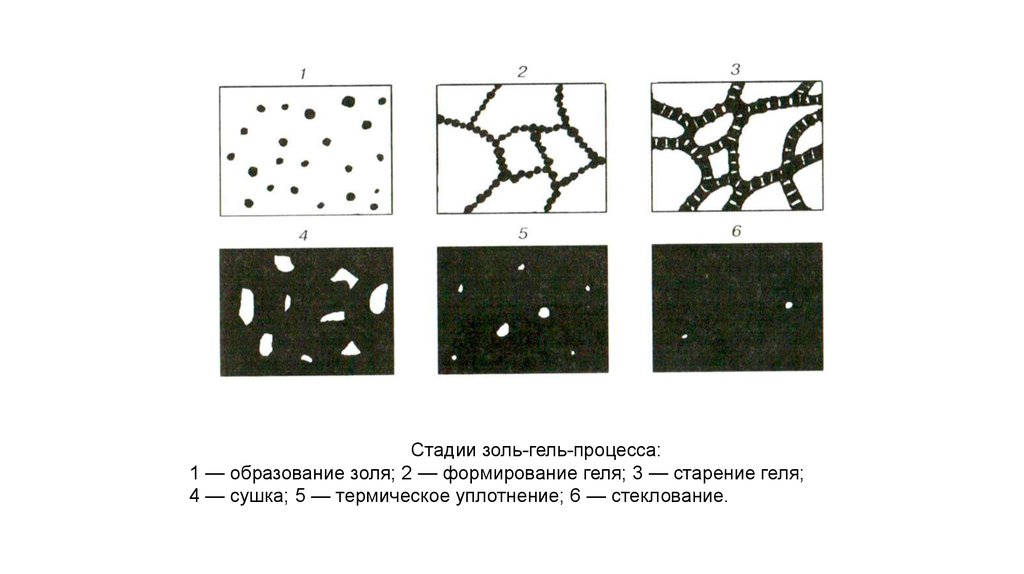
Стадии золь-гель-процесса:1 — образование золя; 2 — формирование геля; 3 — старение геля;
4 — сушка; 5 — термическое уплотнение; 6 — стеклование.
25.
Преимущества методов осаждения :• простоту аппаратурного оформления, экономичность;
• возможность регулирования свойств конечных порошков в ходе
их получения;
• возможность получения двойных и тройных композиций с
равномерным распределением компонентов;
• высокую чистоту конечного продукта.
Недостатки методов осаждения :
• многостадийность процесса;
• потеря части продукта в гелевом осадке;
• как правило, невысокая производительность.
Наиболее сложной и длительной стадией методов осаждения
является процедура промывки и фильтрации осадка.
26. Сверхкритическая сушка
Схема лабораторнойустановки для
сверхкритической сушки:
1 – автоклав;
2 – сосуд с гелем;
3 – термостатируемая
емкость;
4 – перистальтический
насос;
5 – баллон с жидким СО2;
6 – насос.
Распределение пор по
размерам для
гидрофильного и
гидрофобного аэрогеля,
плотность которых
составляет 0.155 г/см3
Микрофотографии образцов аэрогеля
после процесса кристаллизации
лекарственного вещества:
а,б – образование крупных кристаллов;
в – образование нанокристаллов;
г – растрескивание аэрогеля при резком
сбросе давления
Курс Н.В. Меньшутиной «Введение в наноинженерию»
27. Способы испарения растворителя
Суть этих процессов заключается в распылении раствора в виденебольших капель и удалении с высокой скоростью из них растворителя.
При понижении температуры охлаждающей среды размер получаемых
частиц уменьшается, но не монотонно. В интервале 233-243 К
наблюдается скачкообразное уменьшение размера до некоторого
предела (около 100 нм), который при дальнейшем понижении
температуры изменяется незначительно. При этом скорость
замораживания составляет 5-8 мм/с.
С увеличением скорости охлаждения распределение частиц по
размерам становится все более узким. Монодисперсной система
становится при достижении скорости охлаждения 30-59 К/с. Согласно
теории, криохимическим методом можно получать наночастицы
размером 0,5-5 нм.
28. Криогенная технология
Способ заключается в том, что готовится раствор необходимого состава,который распыляется в камеру с криогенной средой, например, жидким
азотом и быстро замораживается.
На следующем этапе давление газовой среды уменьшается до значений
ниже тройной точки равновесия диспергируемой системы, а
температура повышается для возгонки растворителя.
В результате получается продукт, состоящий из тончайших пористых
гранул. Дальнейшая их обработка зависит от назначения конечного
порошка.
Путем прокаливания гранул на воздухе можно получить оксиды,
восстановлением — порошки металлов, например Си, W и их сплавы;
селективным восстановлением — смесь оксидов и металлов, например
Cu-Th02.
29. Сублимационная сушка
Суть способа заключается в распылении водного раствора солиметалла в органическую жидкость, в которой поддерживается
низкая температура. При этом осуществляется мгновенное
замораживание. Затем из осадка в условиях низких температур и
пониженного давления возгонкой удаляется вода. Конечный
продукт получается после термического разложения.
В результате данного процесса формируется высокая площадь
поверхности наноматериалов. Этим способом получен, например,
нанооксид никеля, легированный литием, который используется в
топливных элементах
30. Вакуумная сублимационная сушилка
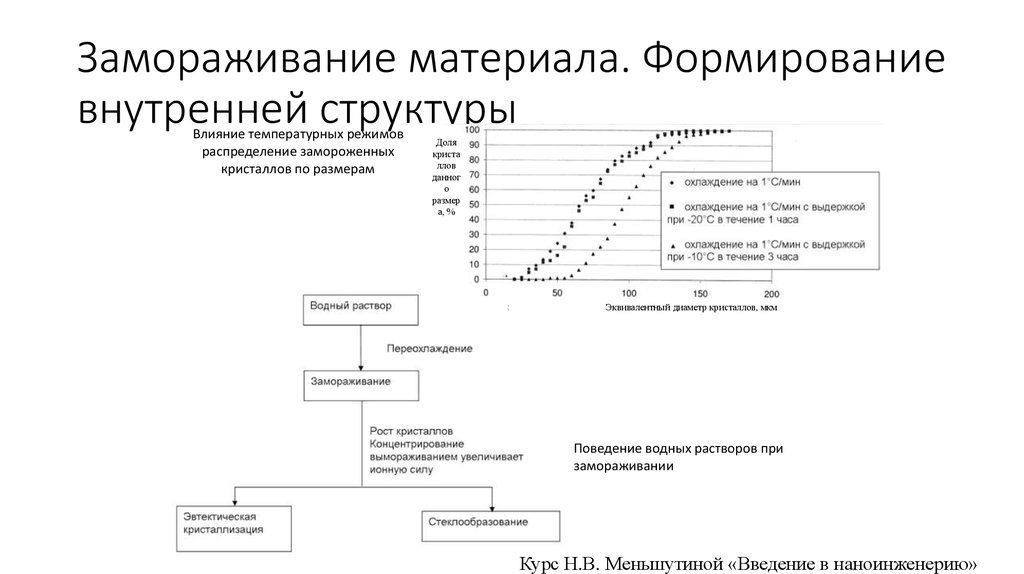
Cублимационная установка FD-531. Замораживание материала. Формирование внутренней структуры
Влияние температурных режимовраспределение замороженных
кристаллов по размерам
Доля
криста
ллов
данног
о
размер
а, %
Эквивалентный диаметр кристаллов, мкм
Поведение водных растворов при
замораживании
Курс Н.В. Меньшутиной «Введение в наноинженерию»
32. Структура замороженных кристаллов в вертикальном поперечном сечении (10%-го маннитола)
А - верхнее положение, зародышиобразовались при –2.04 °С;
Б - нижнее положение, зародыши
образовались при –2.04 °С;
В - верхнее положение, зародыши
образовались при –8.17 °С;
Г - нижнее положение, зародыши
образовались при –8.17 °С.
Курс Н.В. Меньшутиной «Введение в наноинженерию»
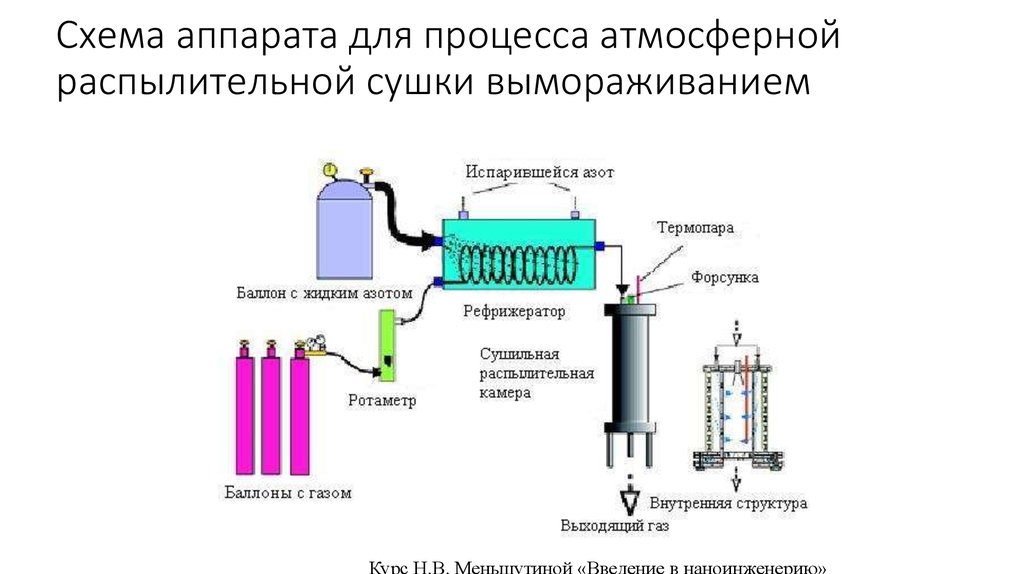
33. Схема аппарата для процесса атмосферной распылительной сушки вымораживанием
Курс Н.В. Меньшутиной «Введение в наноинженерию»34. Примеры использования
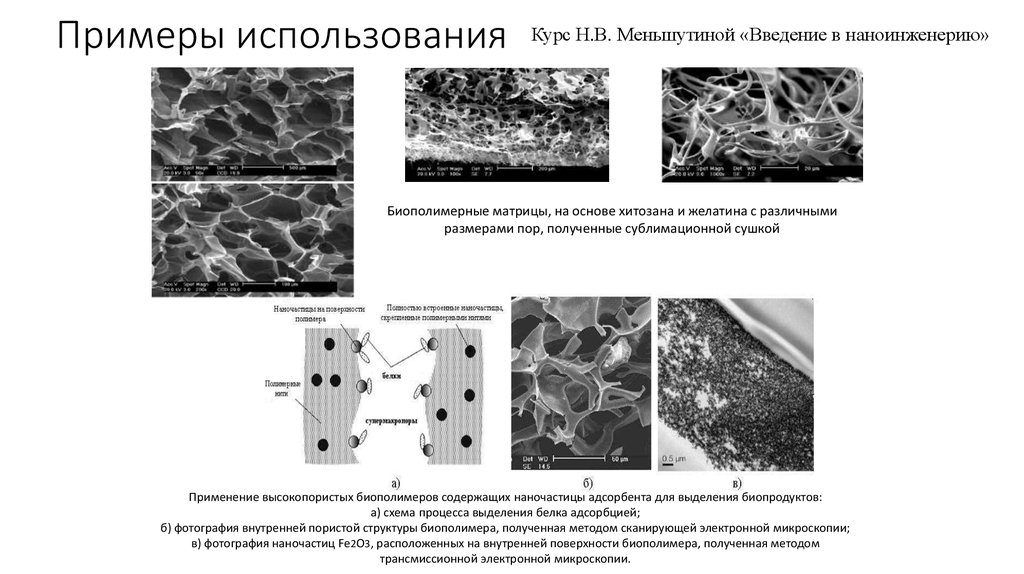
Курс Н.В. Меньшутиной «Введение в наноинженерию»Биополимерные матрицы, на основе хитозана и желатина с различными
размерами пор, полученные сублимационной сушкой
Применение высокопористых биополимеров содержащих наночастицы адсорбента для выделения биопродуктов:
а) схема процесса выделения белка адсорбцией;
б) фотография внутренней пористой структуры биополимера, полученная методом сканирующей электронной микроскопии;
в) фотография наночастиц Fe2O3, расположенных на внутренней поверхности биополимера, полученная методом
трансмиссионной электронной микроскопии.
35. Способ испарительного терморазложения
Раствор соли металла распыляется в окружающую атмосферу,нагретую до высокой температуры. В результате этого процесса
происходит испарение растворителя и термическое разложение
соли металла.
С целью использования теплоты, выделяющейся при сгорании, в
качестве растворителя применяют горючие вещества, например
спирты.
Способ позволяет получать в одну стадию нанопорошки ферритов
и оксидов сложного состава, которые в дальнейшем используются
для производства высококачественной керамики.
35
36.
Способы испарения растворителя позволяют получатьнанопорошки металлов и различных соединений с очень
маленьким размером частиц и высокой удельной поверхностью.
Однако их общим недостатком является необходимость сложного
оборудования и специального подбора сред.
36
































 Физика
Физика








