Похожие презентации:
Процессы ацилирования
1. ПРОЦЕССЫ АЦИЛИРОВАНИЯ
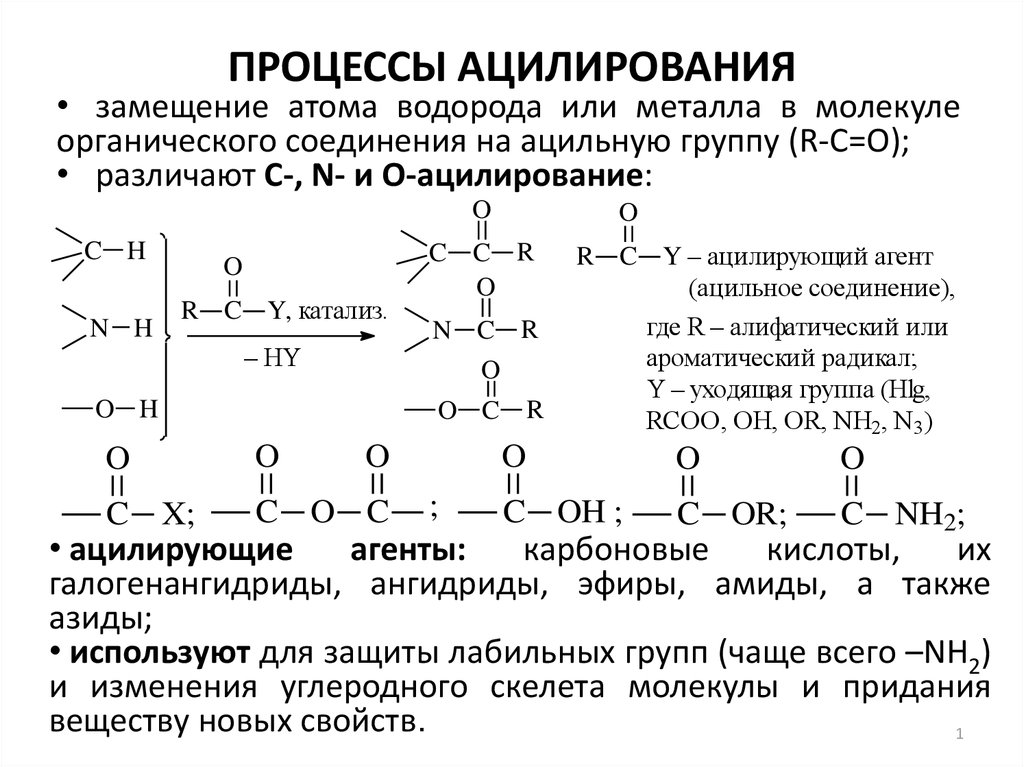
• замещение атома водорода или металла в молекулеорганического соединения на ацильную группу (R-C=O);
• различают С-, N- и О-ацилирование:
O
C H
N H
O
R C Y, катализ.
– HY
O H
C C R
O
N C R
O
O C
O
O
C X;
C O C
O
O
;
R
R C Y – ацилирующий агент
(ацильное соединение),
где R – алифатический или
ароматический радикал;
Y – уходящая группа (Hlg,
RCOO, OH, OR, NH2, N3)
O
O
O
C OH ;
C OR;
C NH2;
• ацилирующие
агенты:
карбоновые
кислоты,
их
галогенангидриды, ангидриды, эфиры, амиды, а также
азиды;
• используют для защиты лабильных групп (чаще всего –NH2)
и изменения углеродного скелета молекулы и придания
веществу новых свойств.
1
2. C-ацилирование аренов по Фриделю-Крафтсу (синтез ароматических кетонов)
C-ацилирование аренов по ФриделюКрафтсу (синтез ароматических кетонов)O
_
ArH + Y C–(Ar)R
катализатор
O
Ar–C–R(Ar) + HY
• Ацилирующие агенты: в основном,
кислоты, их ангидриды и хлорангидриды.
O
O
O
C OH <
C O C
карбоновые
O
<
C Cl;
•Реакция родственна алкилированию по ФриделюКрафтсу.
•Субстраты – активированные арены.
•Механизм SE, но в отличие от алкилирования реакция
ацилирования необратимая;
•Катализаторы — те же вещества, что и при
алкилировании: протонные и апротонные кислоты,
оксид алюминия, силикагель и др.;
2
3. Отличие реакций ацилирования и алкилирования аренов по Фриделю-Крафтсу
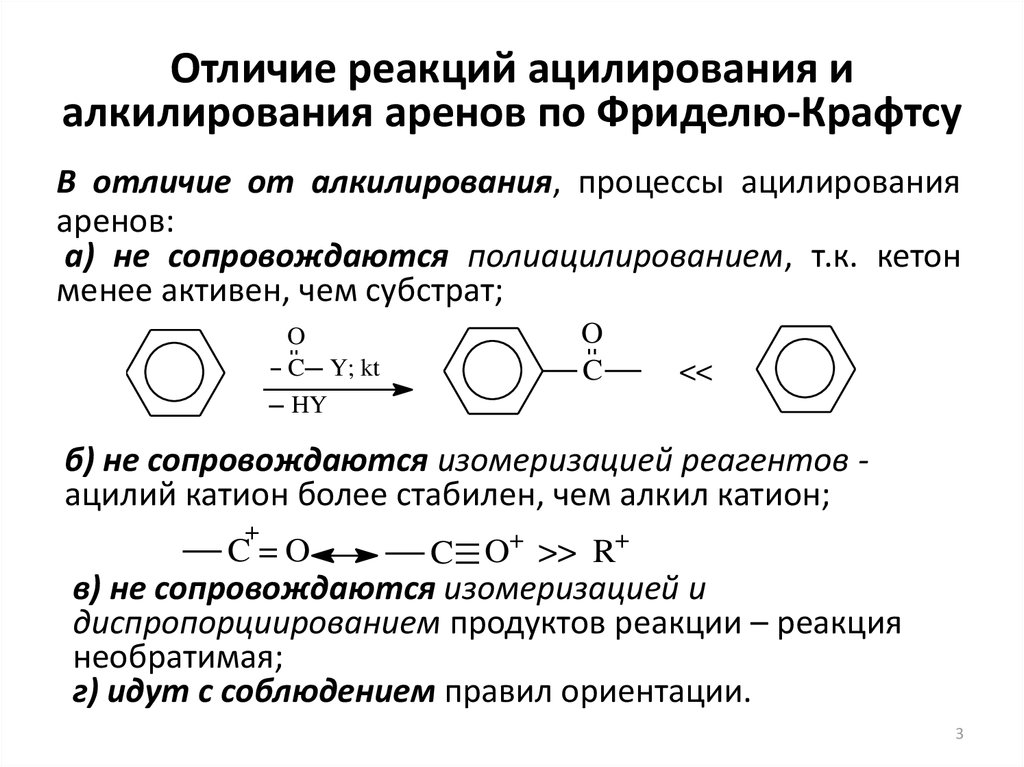
В отличие от алкилирования, процессы ацилированияаренов:
а) не сопровождаются полиацилированием, т.к. кетон
менее активен, чем субстрат;
O
C
Y; kt
O
C
<<
HY
б) не сопровождаются изомеризацией реагентов ацилий катион более стабилен, чем алкил катион;
+
C=O
C O+ >> R+
в) не сопровождаются изомеризацией и
диспропорциированием продуктов реакции – реакция
необратимая;
г) идут с соблюдением правил ориентации.
3
4. Механизм образования электрофильных частиц
OC Y
+
O AlCl3
O AlCl3
+
C Y
O H
C Y
O H
AlCl3
+
H
C Y
+
+
C Y
+
–
C O + AlCl3Y
+
C O + HY
• В результате взаимодействия ацилирующих агентов с
катализатором образуются электрофильные частицы:
- во-первых, биполярный ион, который является более
слабым, но более вероятным реагентом, чем
свободный ацилий-катион;
- во-вторых, катионы ацилия [RC+=O ↔ RC≡O+], которые
значительно активнее комплекса и стабильнее, чем
алкилкатионы (за счет более равномерного
распределения электронного облака по частице и
образования оксониевого катиона). Чаще всего ацилий
катионы образуются при использовании ацилхлорида.
4
5. Количество кислоты Льюиса
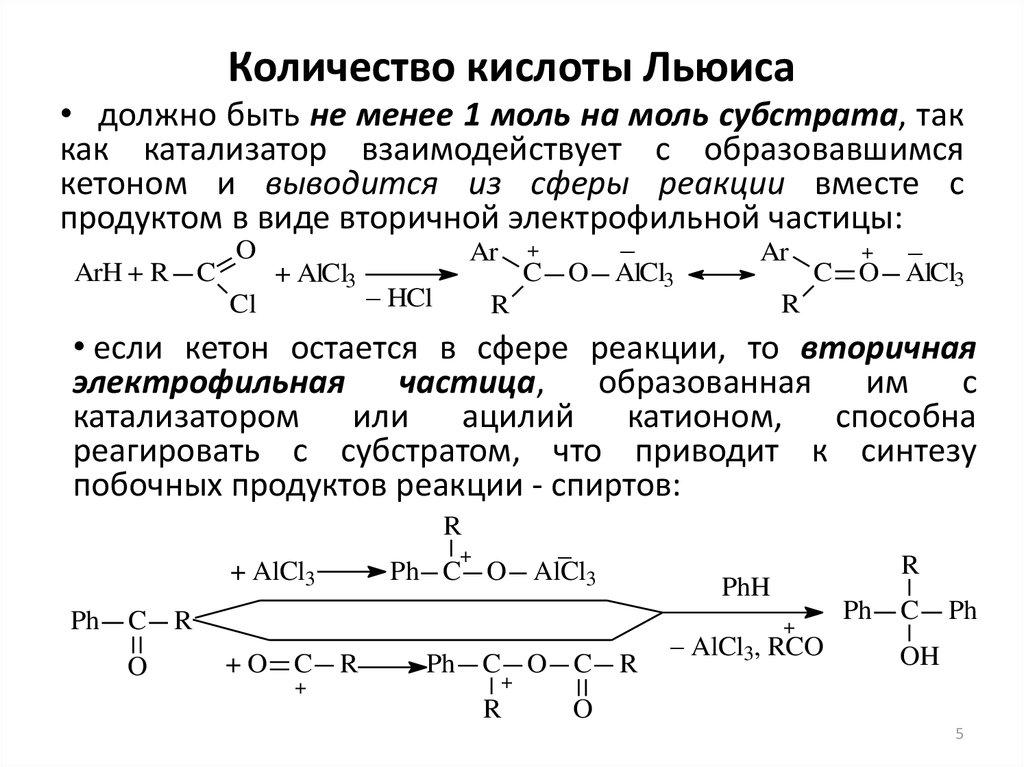
• должно быть не менее 1 моль на моль субстрата, таккак катализатор взаимодействует с образовавшимся
кетоном и выводится из сферы реакции вместе с
продуктом в виде вторичной электрофильной частицы:
ArH + R
C
O
+ AlCl3
Cl
–
C O AlCl3
Ar
– HCl
+
Ar
–
C O AlCl3
+
R
R
• если кетон остается в сфере реакции, то вторичная
электрофильная
частица,
образованная
им с
катализатором или ацилий катионом, способна
реагировать с субстратом, что приводит к синтезу
побочных продуктов реакции - спиртов:
R
+
–
Ph C O AlCl3
+ AlCl3
Ph
C
O
R
PhH
R
+
+O C
+
R
Ph C O C
+
R
R
– AlCl3, RCO
Ph
C
Ph
OH
O
5
6. С-ацилирование аренов хлорангидридами кислот
• Хлорангидридыкислот
—
самые
активные
ацилирующие
агенты,
но
малодоступные,
нестабильные, дорогие (легко разлагаются влагой
воздуха, трудно сохранить, поэтому их синтезируют
перед использованием) и самые токсичные и
агрессивные (выделяется HCl).
• Условия реакции (температура, время, катализатор)
зависят от активности субстрата и хлорангидрида.
• Чаще всего синтез кетонов осуществляют в присутствии
активного катализатора хлорида алюминия при низких
температурах. При использовании хлорида цинка
реакция идет в более жестких условиях.
• Мало
активированные
арены,
содержащие
карбонильные, нитро-, циано-, сульфо-, карбоксильные
и другие электроноакцепторные группы, а также
пиридины и аналогичные циклы в реакцию не
вступают.
6
7. С-ацилирование аренов ангидридами кислот
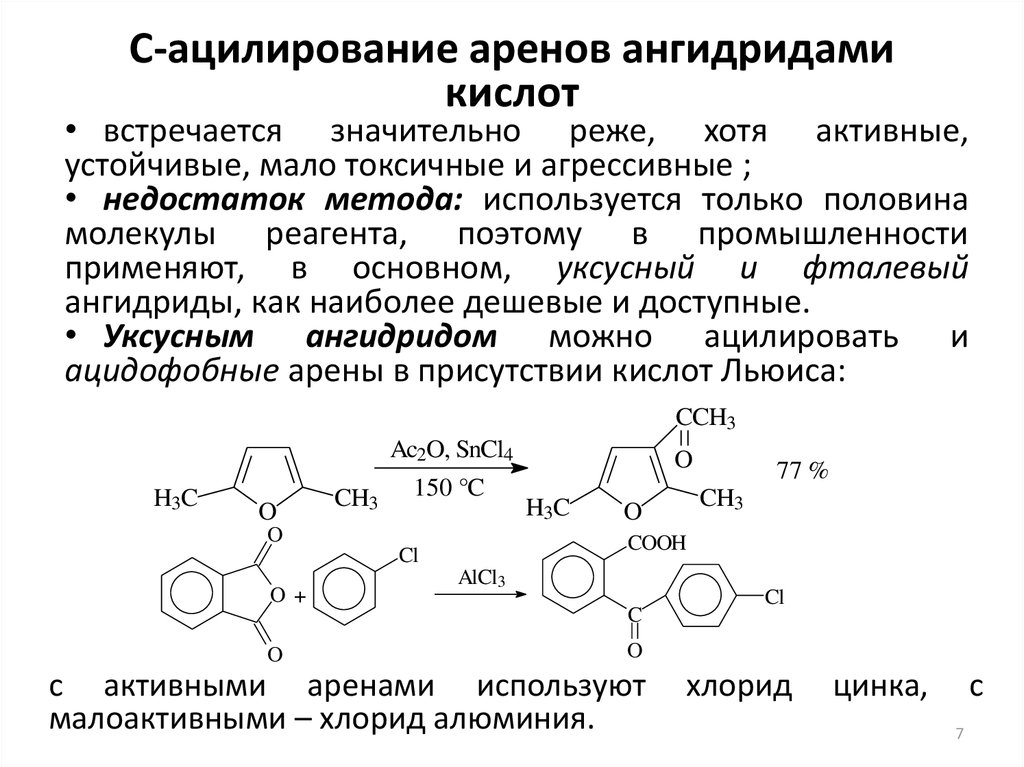
• встречается значительно реже, хотя активные,устойчивые, мало токсичные и агрессивные ;
• недостаток метода: используется только половина
молекулы реагента, поэтому в промышленности
применяют, в основном, уксусный и фталевый
ангидриды, как наиболее дешевые и доступные.
• Уксусным ангидридом можно ацилировать и
ацидофобные арены в присутствии кислот Льюиса:
CCH3
Ac2O, SnCl4
H3C
O
CH3
150 °C
O
O
H3C
77 %
CH3
O
COOH
Cl
O+
O
AlCl3
C
Cl
O
с активными аренами используют
малоактивными – хлорид алюминия.
хлорид
цинка,
с
7
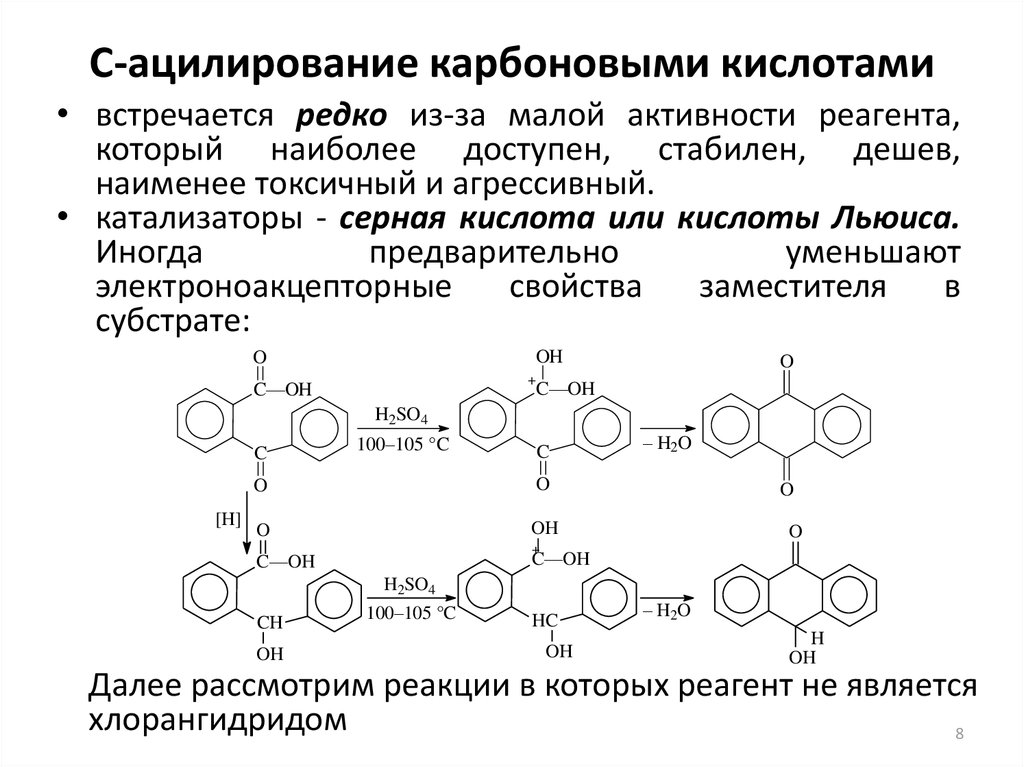
8. С-ацилирование карбоновыми кислотами
• встречается редко из-за малой активности реагента,который наиболее доступен, стабилен, дешев,
наименее токсичный и агрессивный.
• катализаторы - серная кислота или кислоты Льюиса.
Иногда
предварительно
уменьшают
электроноакцепторные
свойства
заместителя
в
субстрате:
OH
O
+
C—OH
O
C—OH
H2SO4
C
[H]
100–105 °C
C
O
O
O
OH
– H2O
O
O
+
C—OH
C—OH
H2SO4
CH
OH
100–105 °C
HC
OH
– H2O
H
OH
Далее рассмотрим реакции в которых реагент не является
хлорангидридом
8
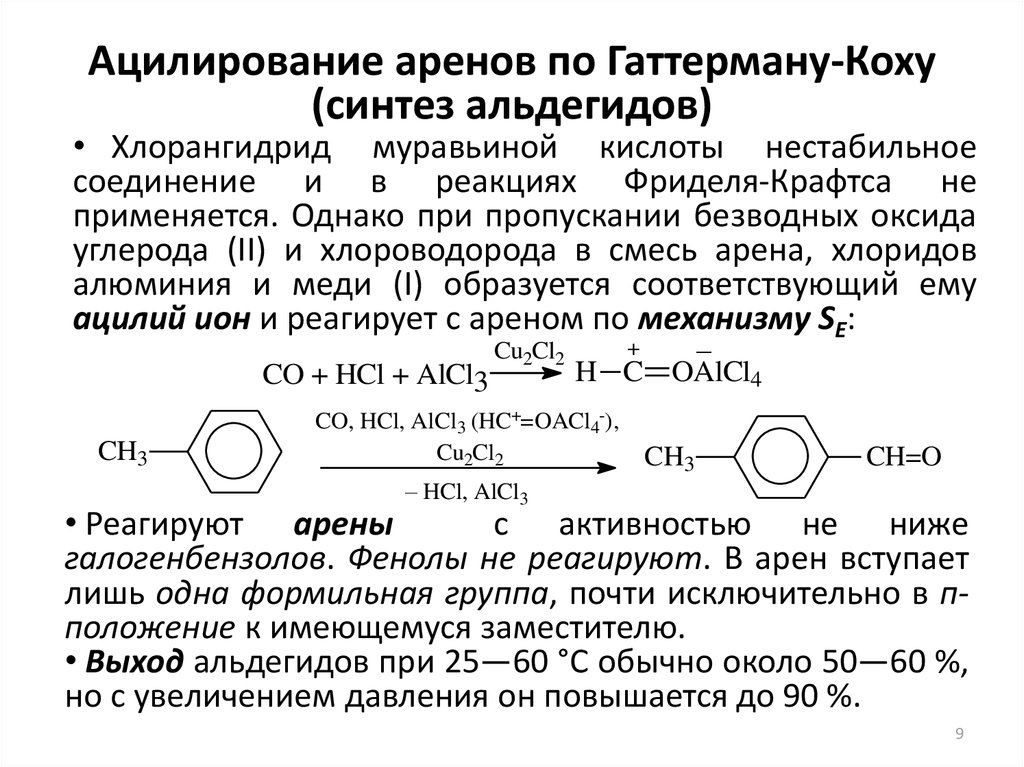
9. Ацилирование аренов по Гаттерману-Коху (синтез альдегидов)
• Хлорангидрид муравьиной кислоты нестабильноесоединение и в реакциях Фриделя-Крафтса не
применяется. Однако при пропускании безводных оксида
углерода (II) и хлороводорода в смесь арена, хлоридов
алюминия и меди (I) образуется соответствующий ему
ацилий ион и реагирует с ареном по механизму SE:
CO + HCl + AlCl3
CH3
Cu2Cl2
–
H C OAlCl4
CO, HCl, AlCl3 (HC+=OACl4-),
Cu2Cl2
+
CH3
CH=O
– HCl, AlCl3
• Реагируют арены
с активностью не ниже
галогенбензолов. Фенолы не реагируют. В арен вступает
лишь одна формильная группа, почти исключительно в пположение к имеющемуся заместителю.
• Выход альдегидов при 25—60 °С обычно около 50—60 %,
но с увеличением давления он повышается до 90 %.
9
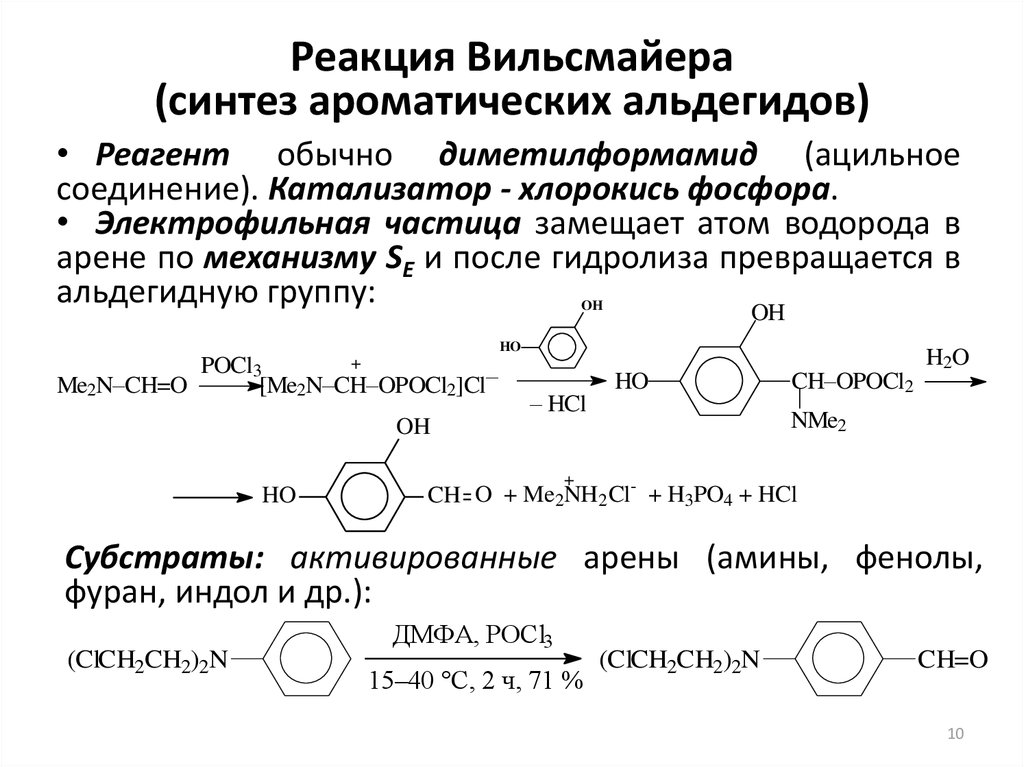
10. Реакция Вильсмайера (синтез ароматических альдегидов)
• Реагент обычно диметилформамид (ацильноесоединение). Катализатор - хлорокись фосфора.
• Электрофильная частица замещает атом водорода в
арене по механизму SE и после гидролиза превращается в
альдегидную группу:
OH
OH
HO
H2O
+
POCl3
Me2N–CH=O
[Me2N–CH–OPOCl2]Cl–
– HCl
HO
NMe2
OH
HO
CH–OPOCl2
+
CH O + Me2NH2 Cl- + H3PO4 + HCl
Субстраты: активированные арены (амины, фенолы,
фуран, индол и др.):
(ClCH2CH2)2N
ДМФА, POCl3
15–40 °C, 2 ч, 71 %
(ClCH2CH2)2N
CH=O
10
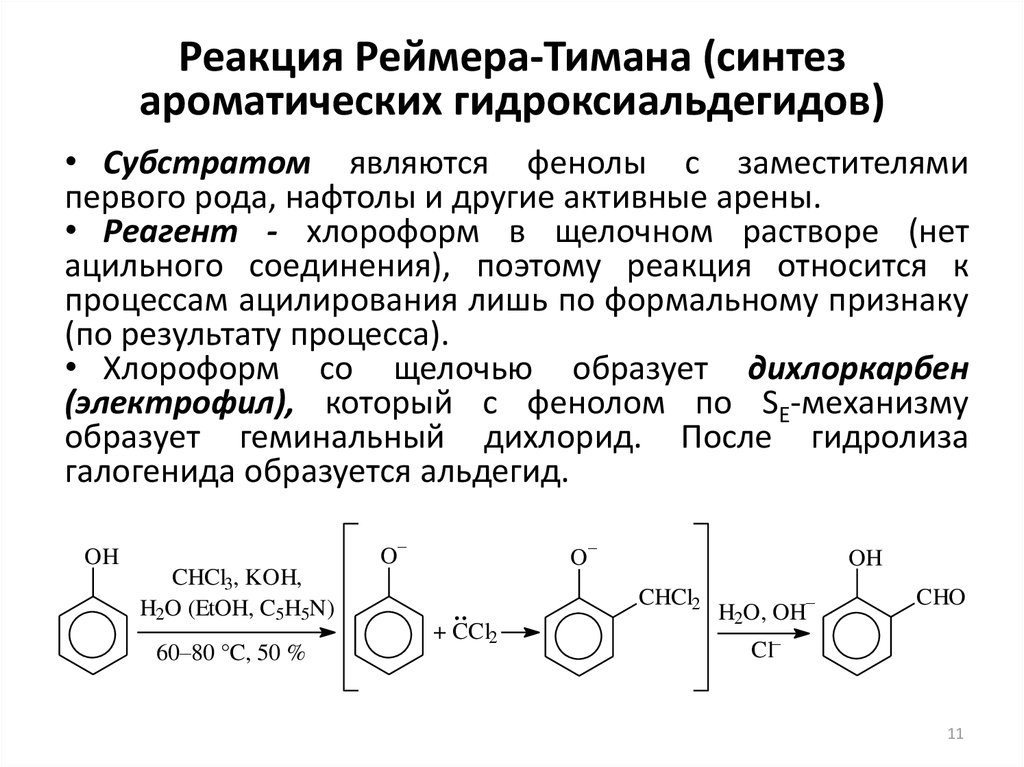
11. Реакция Реймера-Тимана (синтез ароматических гидроксиальдегидов)
• Субстратом являются фенолы с заместителямипервого рода, нафтолы и другие активные арены.
• Реагент - хлороформ в щелочном растворе (нет
ацильного соединения), поэтому реакция относится к
процессам ацилирования лишь по формальному признаку
(по результату процесса).
• Хлороформ со щелочью образует дихлоркарбен
(электрофил), который с фенолом по SE-механизму
образует геминальный дихлорид. После гидролиза
галогенида образуется альдегид.
OH
O–
CHCl3, KOH,
H2O (EtOH, C5H5N)
60–80 °C, 50 %
O
–
OH
CHCl2
+ CCl2
–
H2O, OH
CHO
Cl–
11
12. Реакция Кольбе-Шмидта (синтез ароматических гидроксикислот)
• Субстратом являются фенолы и аминофенолы.• Ацилирующий агент – ангидрид угольной кислоты.
• Синтез ароматических гидроксикислот ведут в
автоклаве при 180оС.
• В настоящее время считают, что реакция проходит через
стадию образования -комплекса по SE-механизму.
O
H
+
-
C
O C O
Na
O
+
O Na
COONa
O
+
Na
OH
O
ONa
OH
COONa
CO2
NH2
–
NH2
12
13. N-ацилирование (синтез амидов кислот)
OO
R–NH2 + Y–C–R'
– HY
RNH–C–R'
• применяется как для получения нового соединения,
так и для защиты аминогруппы;
• ацилирующие агенты: все ацильные производные
карбоновых кислот;
• обычно реакцию рассматривают как нуклеофильное
замещение уходящей группы в ацильных соединениях в
два этапа: присоединение — отщепление (SNAE):
O
–
O
–
C Y + Nu
+
(AN)
–
C Y
O
–
(E)
C Nu + Y
Nu
• скорость реакции ацилирования и условия ее проведения
в значительной мере зависят от строения ацилирующего
агента и субстрата.
13
14. Реакционная способность ацильных соединений
–O
–
–
R +C Y + Nu
(AN)
O
O
C Y
C Nu + Y
–
(E)
Nu
• Определяется величиной положительного заряда на
атоме углерода карбонильной группы и способностью
уходящей группы уходить.
• Величина положительного заряда С +=О - группы и,
следовательно, активность реагента увеличивается с
повышением электроноакцепторных свойств радикала
(R). От этого фактора зависит и сила кислоты, поэтому
сравнивая константы диссоциации кислот можно
оценить и их ацилирующую активность. Так, сила кислот
и ацилирующая активность увеличивается в ряду:
CH3CH2COOH < CH3COOH < HCOOH < ClCH2COOH
pKa = 4,88
4,76
3,77
2,86
14
15. Влияние уходящей группы на d+ ацильной группы
Влияние уходящей группы на + ацильнойгруппы
• В ацильных соединениях одной и той же кислоты,
величина + - результат взаимодействия электронных
облаков карбонильной и уходящей групп:
+
O
–
C
+
–
C
Cl
O
–I1
+C1
O
~
<<
+
O
–
C
+
O
–
C
O H
O R
+
O
–
C
NH2
C
+
O –I2
+C2
>
–I3
>
<
+C3
<
+
Величина уменьшается
–I4
+C4
>
<<
–I5
+C5
• Величина
+
увеличивается
при
возрастании
отрицательного индукционного эффекта и уменьшении
положительного эффекта сопряжения.
15
16. Способность группы Y уходить
–O
O
C Y
C Nu + Y
–
(E)
Nu
• чем более сильным основанием является Y , тем хуже
уходит. При определении силы основания обычно
используют константу диссоциации сопряженной с ним
кислоты: чем сильнее кислота, тем слабее сопряженное с
ней основание:
Сила оснований возрастает, способность уходяющих групп уходить уменьшается
–
Cl
–COO
–
HO
–
RO
–
–
NH2
Сила кислот уменьшается (для сравнения приведены примерные величины ионизации)
HCl
–COOH
~1
10
–5
HOH
–14
10
ROH
–16
10
NH3
–25
менее 10
• В связи с величиной заряда и способности группы Y
уходить ацилирующая активность уменьшается от
хлорангидрида кислоты к амиду.
16
17. Хлорангидриды карбоновых кислот
• (+) самые активные ацилирующие агенты; реакциинеобратимые;
реагенты
можно
брать
в
стехиометрических соотношениях.
• (-) наиболее дорогие, малоустойчивые, токсичные и
агрессивные агенты, что усложняет технологический
процесс; как правило, используют только тогда, когда
другие агенты не дают хороших результатов.
• Выделяющийся хлороводород образует соли с
аминами что препятствует реакции ацилирования. Для его
связывания обычно используют основания (карбонаты,
щелочь), например в синтезе фолиевой кислоты –
гидрокарбонат натрия:
O
COOH
CH–NH2
CH2
CH2COOH
Cl
C
NO 2
COONa
CH NH C
NaHCO3
– NaCl, CO2, H2O
CH2
NO2
O
CH2COONa
17
18. Ангидриды карбоновых кислот
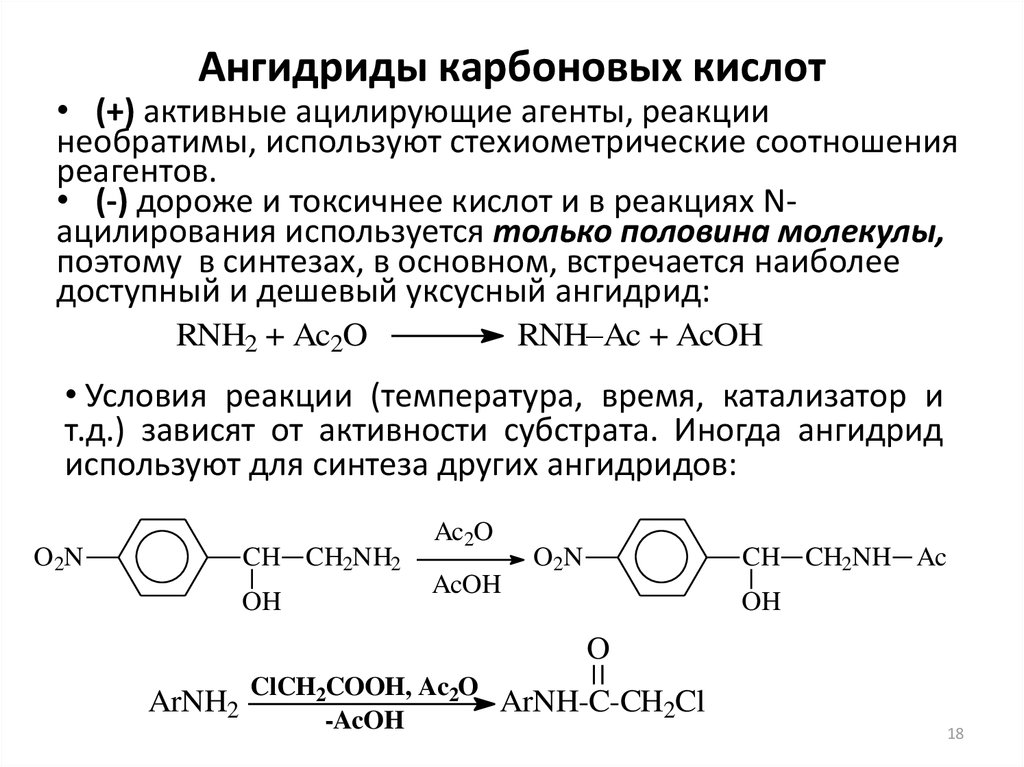
• (+) активные ацилирующие агенты, реакциинеобратимы, используют стехиометрические соотношения
реагентов.
• (-) дороже и токсичнее кислот и в реакциях Nацилирования используется только половина молекулы,
поэтому в синтезах, в основном, встречается наиболее
доступный и дешевый уксусный ангидрид:
RNH2 + Ac2O
RNH–Ac + AcOH
• Условия реакции (температура, время, катализатор и
т.д.) зависят от активности субстрата. Иногда ангидрид
используют для синтеза других ангидридов:
O2N
CH CH2NH2
OH
Ac2O
AcOH
O2N
CH CH2NH Ac
OH
O
ArNH2
ClCH2COOH, Ac2O
-AcOH
ArNH-C-CH2Cl
18
19. Карбоновые кислоты
• (+) наиболее дешевые и доступные;• (-) значительно менее активные реагенты, чем их
ангидриды, образуют с аминами соли, которые не
ацилируются, реакция обратимая.
• Для разрушения солей реакционную массу нагревают
до образования достаточного количества исходного амина
и кислоты:
–
–
O
O
RNH2 + R C OH
O
+
R C NH2R
OH
RNH2
O
O
R C NHR
R C NHR
–
RN H3
– OH
OH
+
RNH3+ + R C O–
• Для смещения равновесия в сторону целевого продукта
применяют избыток наиболее дешевого реагента (кислоты
или амина) и/или выводят образующуюся воду из сферы
реакции
(отгоняют
или
связывают
средствами,
поглощающими воду). Для ускорения реакции используют
минеральную кислоту в качестве катализатора.
19
20. Формилирование и ацетилирование аминов
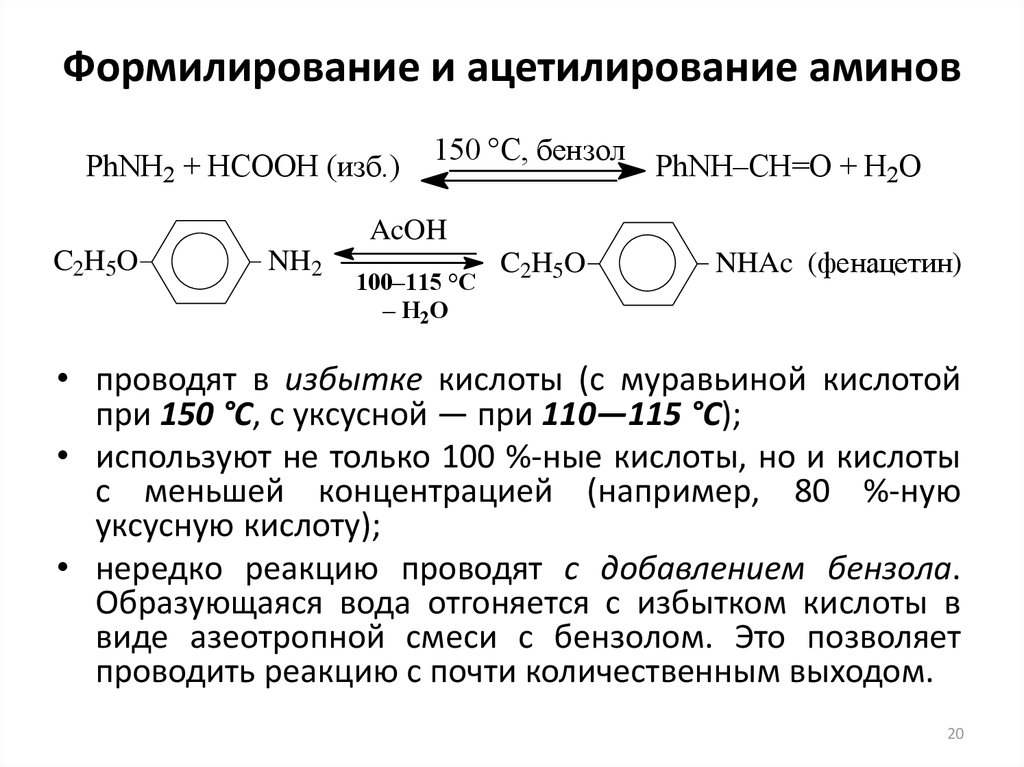
PhNH2 + HCOOH (изб.)150 °C, бензол
PhNH–CH=O + H2O
AcOH
C2H5O
NH2
100–115 °C
– H2O
C2H5O
NHAc (фенацетин)
• проводят в избытке кислоты (с муравьиной кислотой
при 150 °С, с уксусной — при 110—115 °С);
• используют не только 100 %-ные кислоты, но и кислоты
с меньшей концентрацией (например, 80 %-ную
уксусную кислоту);
• нередко реакцию проводят с добавлением бензола.
Образующаяся вода отгоняется с избытком кислоты в
виде азеотропной смеси с бензолом. Это позволяет
проводить реакцию с почти количественным выходом.
20
21. Сложные эфиры карбоновых кислот
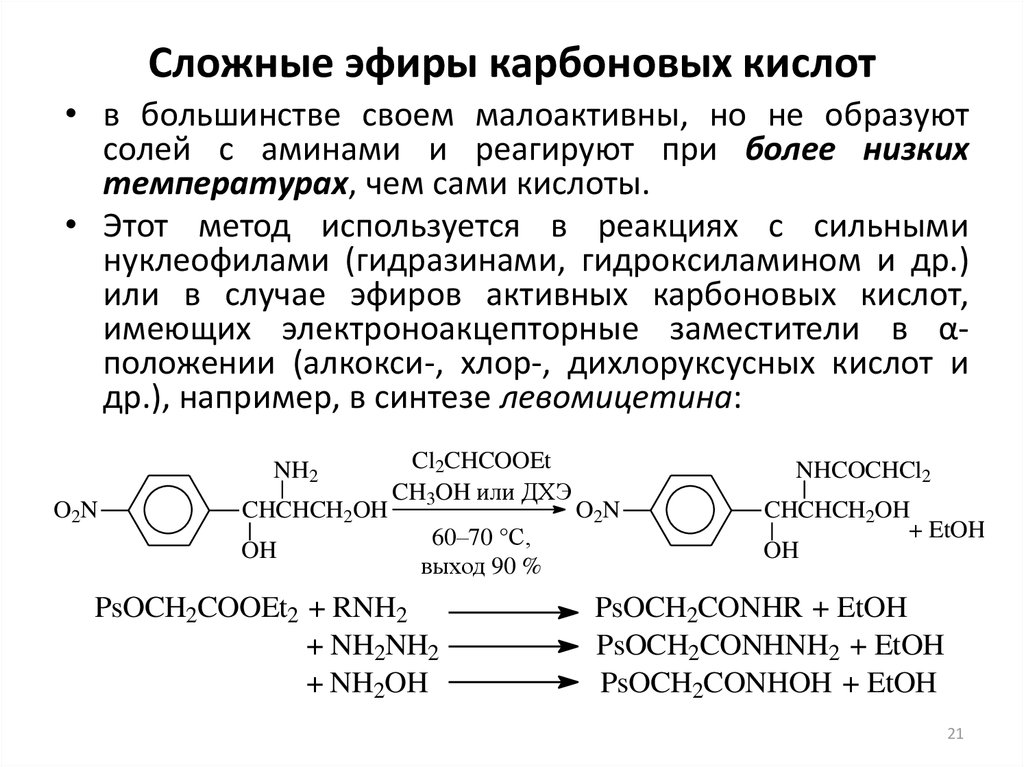
• в большинстве своем малоактивны, но не образуютсолей с аминами и реагируют при более низких
температурах, чем сами кислоты.
• Этот метод используется в реакциях с сильными
нуклеофилами (гидразинами, гидроксиламином и др.)
или в случае эфиров активных карбоновых кислот,
имеющих электроноакцепторные заместители в αположении (алкокси-, хлор-, дихлоруксусных кислот и
др.), например, в синтезе левомицетина:
NH2
O2N
CHCHCH2OH
OH
Cl2CHCOOEt
CH3OH или ДХЭ
60–70 °С,
выход 90 %
PsOCH2COOEt2 + RNH2
+ NH2NH2
+ NH2OH
NHCOCHCl2
O2N
CHCHCH2OH
+ EtOH
OH
PsOCH2CONHR + EtOH
PsOCH2CONHNH2 + EtOH
PsOCH2CONHOH + EtOH
21
22. N-ацилирование амидами карбоновых кислот
• применяют очень редко из-за малой активностиреагента. Тем не менее, известны реакции, где
применение амидов в качестве ацилирующих агентов
технологически и экономически оправдано.
• Амид муравьиной кислоты, который получают из
окиси углерода и аммиака, применяется для
формилирования аминов:
RNH2 + HCONH2
-NH3
O
O
NH2–C–NH2 + RNH2
O
R–C–NHOH
RNH CH O
NH2OH
NH3
NH2–C–NHR + NH3
O
R–C–NH2
NH2NH2
NH3
O
R–C–NHNH2
22
23. О-Ацилирование (синтез сложных эфиров)
OO
R(Ph)-OH + - C-Y
R(Ph)-O-C- + HY
• проводится реже, чем аминогрупп и идет менее
энергично.
• Механизмы О- и N-ацилирования, обычно, одинаковые
SNAE, поэтому активность ацильных соединений
изменяется
– также, как при N-ацилировании.
O
O
–
C Y + Nu
+
(AN)
–
O
–
C Y
C Nu + Y
(E)
Nu
• Условия реакции зависят от строения субстрата и
реагента.
–
+
O
C
–
+
O
C
Cl
O
C
+
O -
–
+
O
C
O H
–
+
O
C
–
+
C
O R
Ацилирующая способность уменьшается
O
NH2
23
24. О-Ацилирование хлорангидридами кислот
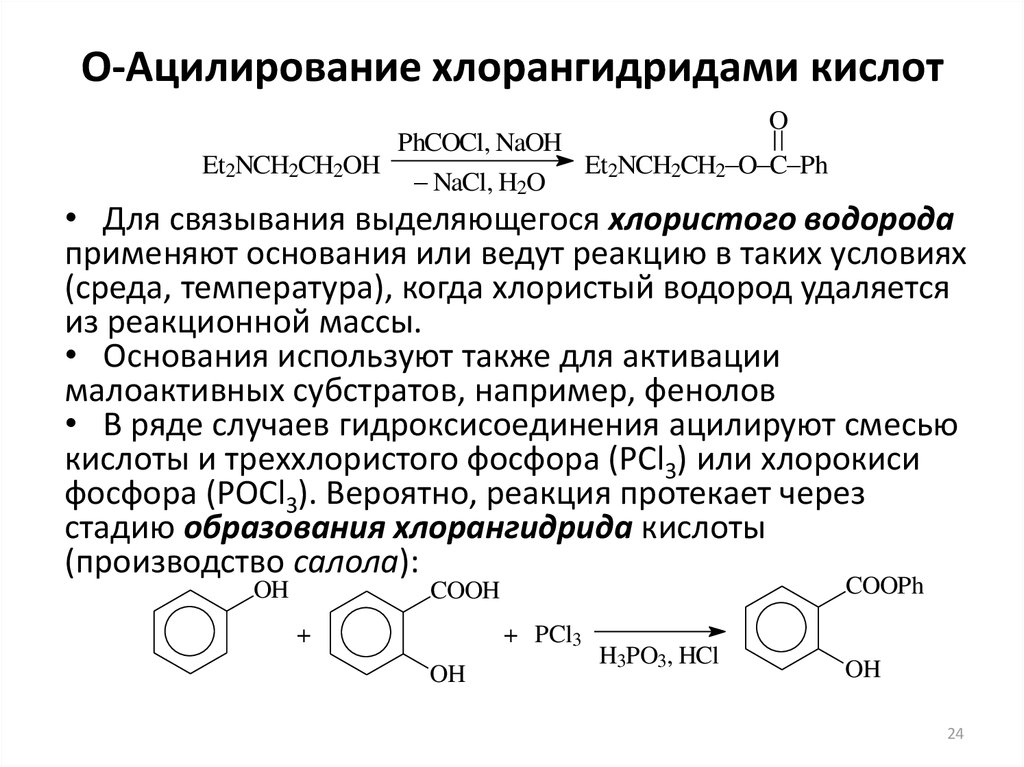
Et2NCH2CH2OHPhCOCl, NaOH
– NaCl, H2O
O
Et2NCH2CH2–O–C–Ph
• Для связывания выделяющегося хлористого водорода
применяют основания или ведут реакцию в таких условиях
(среда, температура), когда хлористый водород удаляется
из реакционной массы.
• Основания используют также для активации
малоактивных субстратов, например, фенолов
• В ряде случаев гидроксисоединения ацилируют смесью
кислоты и треххлористого фосфора (PCl3) или хлорокиси
фосфора (POCl3). Вероятно, реакция протекает через
стадию образования хлорангидрида кислоты
(производство салола):
OH
COOPh
COOH
+
+ PCl3
OH
H3PO3, HCl
OH
24
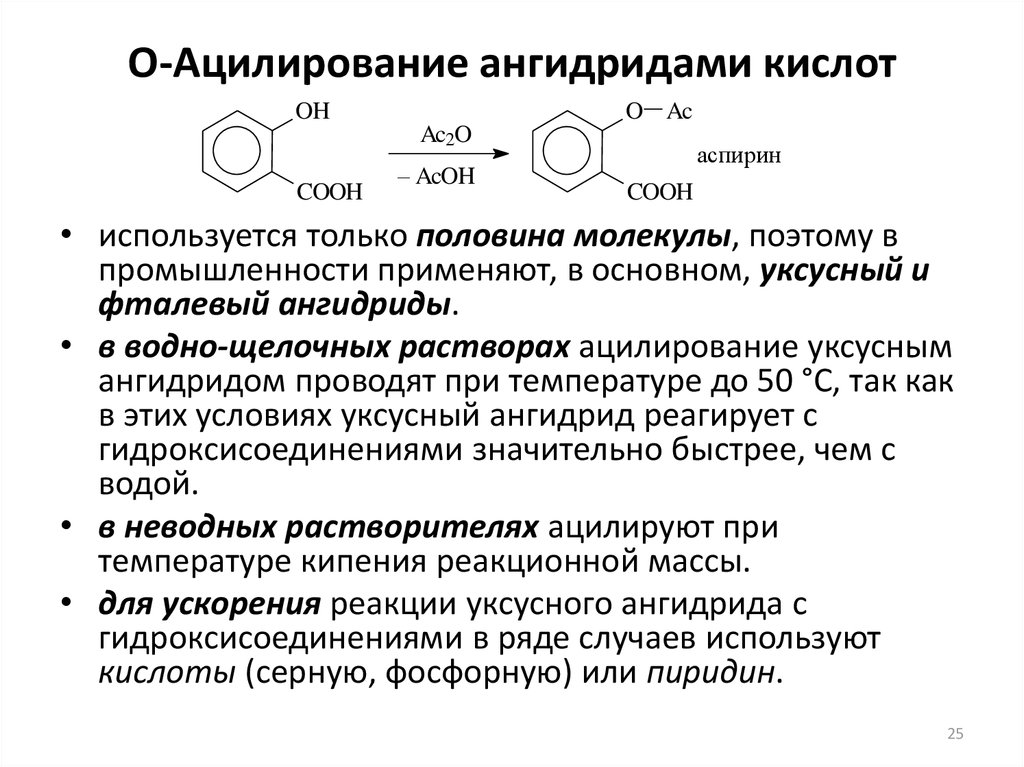
25. О-Ацилирование ангидридами кислот
OHO Ac
Ac2O
COOH
– AcOH
аспирин
COOH
• используется только половина молекулы, поэтому в
промышленности применяют, в основном, уксусный и
фталевый ангидриды.
• в водно-щелочных растворах ацилирование уксусным
ангидридом проводят при температуре до 50 °С, так как
в этих условиях уксусный ангидрид реагирует с
гидроксисоединениями значительно быстрее, чем с
водой.
• в неводных растворителях ацилируют при
температуре кипения реакционной массы.
• для ускорения реакции уксусного ангидрида с
гидроксисоединениями в ряде случаев используют
кислоты (серную, фосфорную) или пиридин.
25
26. О-Ацилирование карбоновыми кислотами
CH3CH—CH—COOHCH3 NH2
EtOH, HCl
эфир
CH3CH—CH—COOEt
–
– H2O
CH3 NH3+Cl
• наиболее дешевый и доступный реагент
• но значительно менее активный, чем ангидриды, не
взаимодействует с фенолами,
• реакции со спиртами обратимые,
• Реакцию этерификации обычно ведут в присутствии
минеральных кислот (серной, соляной, фосфорной), с
азеотропной отгонкой воды, в избытке одного из
реагентов.
COOH
CH
CH2
O
NH—C—Ph
S
CH2COOH
CH3OH, H2SO4
– H2O
COOCH3
CH
CH2
O
NH—C—Ph
S
CH2COOCH3
26
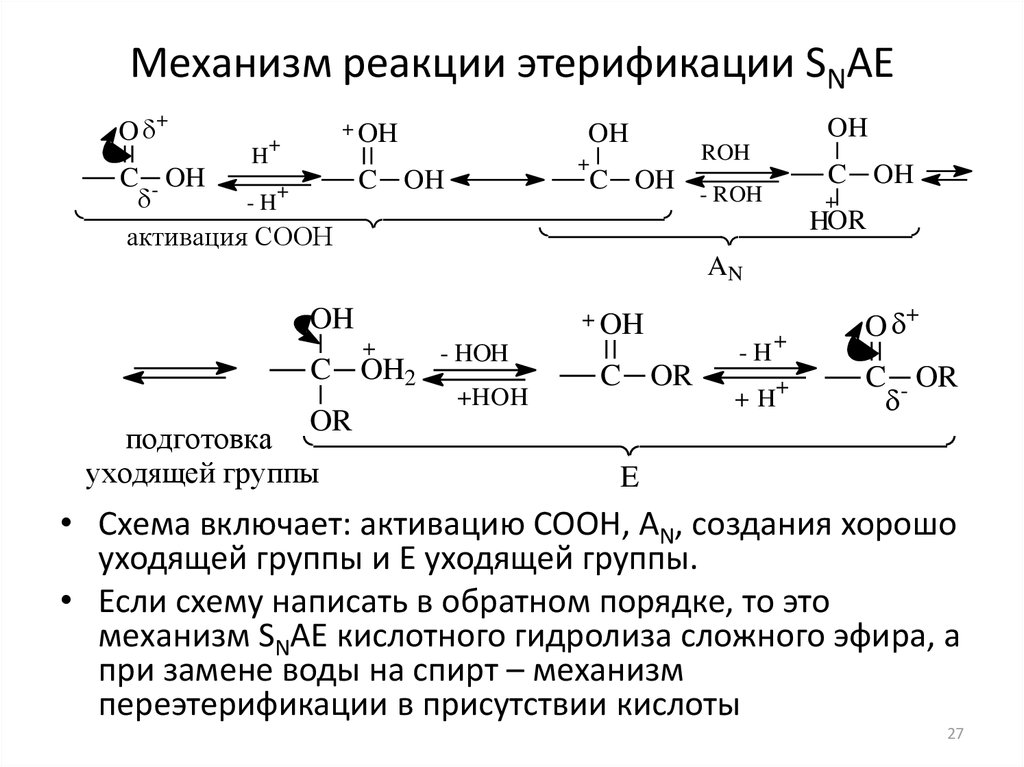
27. Механизм реакции этерификации SNAE
O ++
H
+ OH
OH
+
C - OH
C OH
+
-H
активация СООН
OH
ROH
C OH
C OH - ROH
+
HOR
AN
OH
+
C OH2
OR
подготовка
уходящей группы
+ OH
- HOH
+HOH
C OR
-H
+
+H
+
O +
C - OR
E
• Схема включает: активацию СООН, AN, создания хорошо
уходящей группы и E уходящей группы.
• Если схему написать в обратном порядке, то это
механизм SNAE кислотного гидролиза сложного эфира, а
при замене воды на спирт – механизм
переэтерификации в присутствии кислоты
27
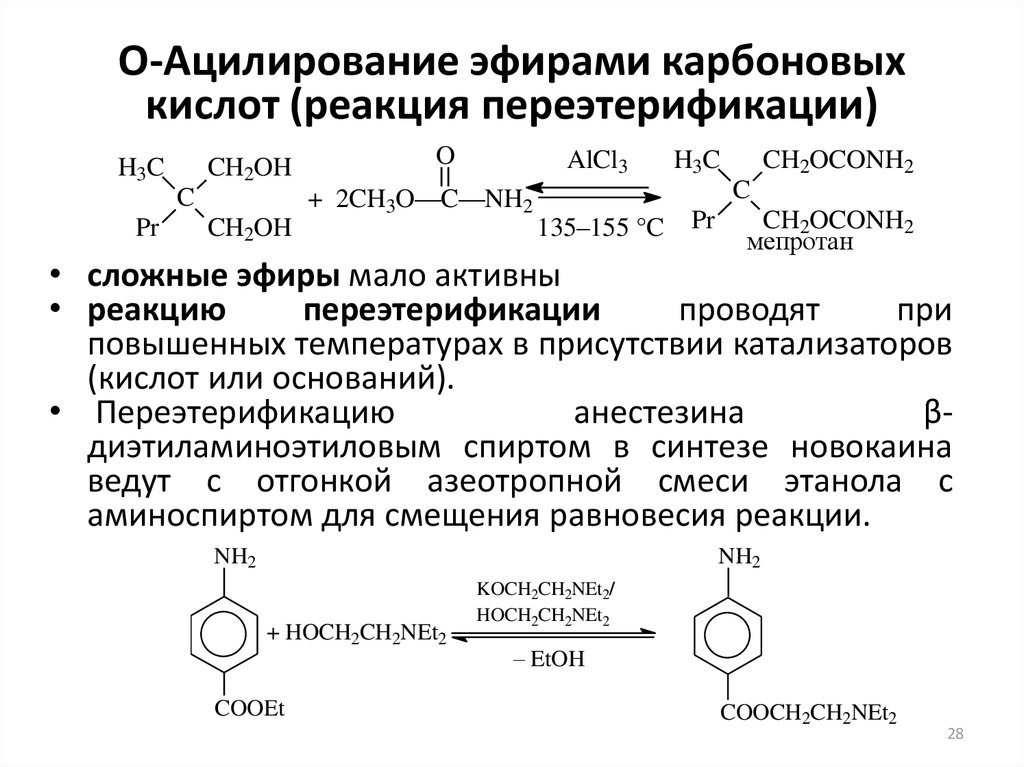
28. О-Ацилирование эфирами карбоновых кислот (реакция переэтерификации)
H3CCH2OH
C
Pr
O
AlCl3
CH2OCONH2
C
+ 2CH3O—C—NH2
CH2OH
H3C
135–155 °C
Pr
CH2OCONH2
мепротан
• сложные эфиры мало активны
• реакцию
переэтерификации
проводят
при
повышенных температурах в присутствии катализаторов
(кислот или оснований).
• Переэтерификацию
анестезина
βдиэтиламиноэтиловым спиртом в синтезе новокаина
ведут с отгонкой азеотропной смеси этанола с
аминоспиртом для смещения равновесия реакции.
NH2
NH2
+ HOCH2CH2NEt2
COOEt
KOCH2CH2NEt2/
HOCH2CH2NEt2
– EtOH
COOCH2CH2NEt2
28













 Химия
Химия








