Похожие презентации:
Болезнь Альцгеймера
1.
Подготовила студентка 6 курсаКолесникова М.В.
2.
Болезнь Альцгеймерпредставляет
собой
прогрессирующее
нейродегенеративное
заболевание с характерными
клиническими
и
патоморфологическими
чертами,
индивидуальными
особенностями
течения
и
выраженности симптомов, а
также
множественными
этиопатогенетическими
механизмами.
Заболевание получило свое
название благодаря трудам
известного немецкого патолога
и
патоморфолога
Алоиза
Альцгеймера.
3.
*В 1906 году на съезде психиатров
в
Тюбингеме
А.
Альцгеймер
сообщил об открытой им новой
болезни – особом виде старческого
слабоумия,
начинавшегося
значительно раньше, чем обычное
сенильное слабоумие.
* Вскрытие его пациентки Августы,
произведенное Альцгеймером в 1906
г. после ее смерти, подтвердило, что
причиной ее интеллектуальной
деградации было неизвестное науке
заболевание, поражающее мозг.
Под микроскопом в клетках мозга
были
обнаружены
беловые
образования
—
своеобразные
клубочки. Кроме того, Альцгеймер
отмечает отложения «величиной с
просяное зёрнышко» (сегодня их
называют амилоидными бляшками).
4.
Статистика.В наше время по данным американских патологов на
долю болезни Альцгеймера приходится до 60% всех
случаев деменции в странах Европы и Северной
Америки. Частота встречаемости деменции возрастает
по мере увеличения возраста: от 2–3% в популяции до
65 лет и до 20–30% в возрасте 80 лет и старше.
Заболевание вдвое чаще встречается у женщин, чем у
мужчин, что скорее всего связано с большей
продолжительностью жизни женщин.
Согласно данным Организации Объединенных Наций в
2010 г. 35,6 млн чел. в мире страдали от деменции, в
России – 1,2 млн чел. По прогнозам Всемирной
организации здравоохранения (ВОЗ), общее число
людей с деменцией будет удваиваться каждые 20 лет
и составит 65,7 млн в 2030 г. и 115,4 млн в 2050 г.
5.
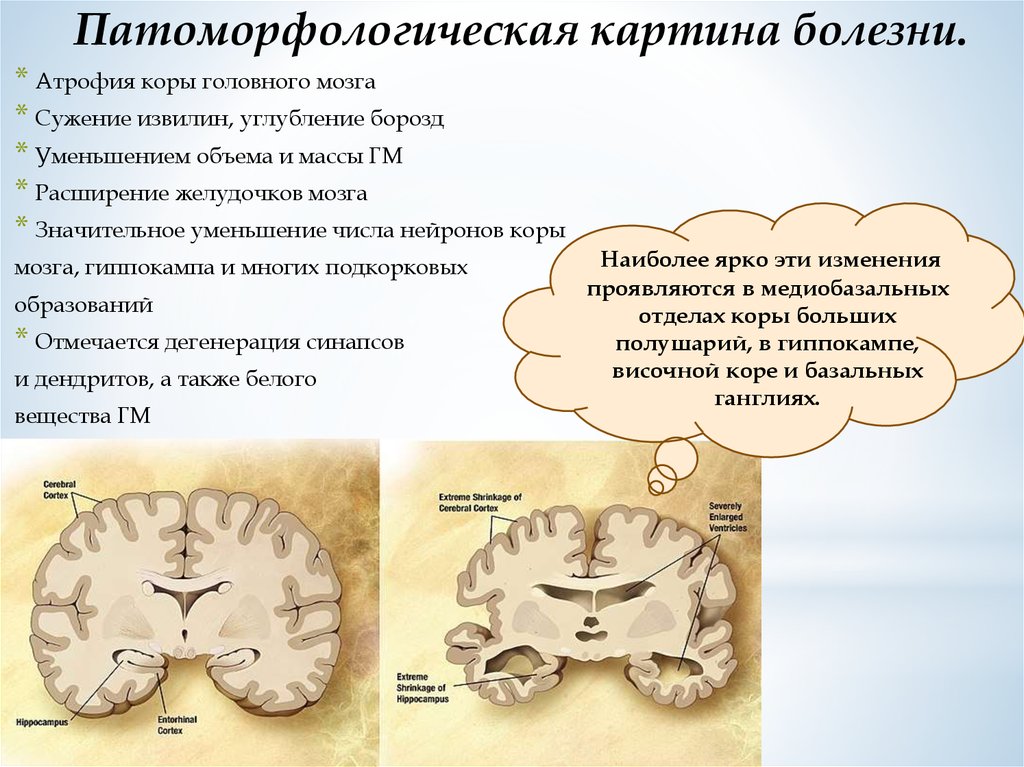
Патоморфологическая картина болезни.* Атрофия коры головного мозга
* Сужение извилин, углубление борозд
* Уменьшением объема и массы ГМ
* Расширение желудочков мозга
* Значительное уменьшение числа нейронов коры
мозга, гиппокампа и многих подкорковых
образований
* Отмечается дегенерация синапсов
и дендритов, а также белого
вещества ГМ
Наиболее ярко эти изменения
проявляются в медиобазальных
отделах коры больших
полушарий, в гиппокампе,
височной коре и базальных
ганглиях.
6.
Характерными патоморфологическими изменениями головногомозга
при
болезни
Альцгеймера
являются
диффузно
распространенные ≪сенильные амилоидные бляшки≫ и
≪нейрофибриллярные клубки≫. При этом амилоидные бляшки
располагаются экстрацеллюляроно, а нейрофибриллярные клубки
образуются в цитоплазме нейронов.
7.
*Патогенетические механизмы, лежащие в основе
болезни Альцгеймер.
В настоящее время идентифицированы три гена, мутации
которых
приводят
к
возникновению
наследственных
(аутосомно-доминантных)
форм
болезни
Альцгеймера,
характеризующихся ранним развитием этого заболевания:
* Ген белка-предшественника бета-амилоида (АРР – Amyloid
Precursor Protein), расположенный на 21 хромосоме и
ответственный за 3 – 5% всех ранних (пресенильных) форм
болезни Альцгеймера.
* Гены, расположенные на 14 и 1 хромосомах, обеспечивающие
синтез мембранных белков – пресенелинов (PS1, пресенелин 1 и
PS2, пресенелин 2). В нейронах головного мозга эти белки
экспрессированы в эндоплазматическом ретикулуме тел
нейронов и дендритов. При этом мутации гена PS1
обуславливают большинство (60 – 70%) всех ранних
(≪семейных≫) форм болезни Альцгеймера, а мутации гена
PS2, напротив, встречаются достаточно редко.
8.
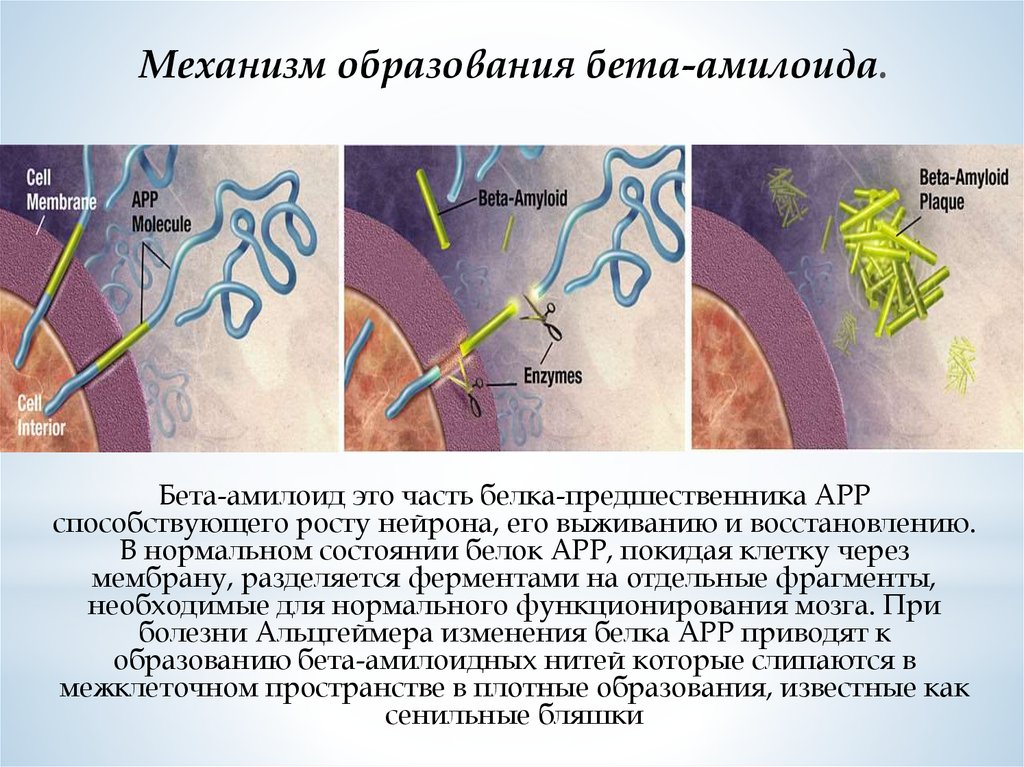
Механизм образования бета-амилоида.Бета-амилоид это часть белка-предшественника АРР
способствующего росту нейрона, его выживанию и восстановлению.
В нормальном состоянии белок АРР, покидая клетку через
мембрану, разделяется ферментами на отдельные фрагменты,
необходимые для нормального функционирования мозга. При
болезни Альцгеймера изменения белка АРР приводят к
образованию бета-амилоидных нитей которые слипаются в
межклеточном пространстве в плотные образования, известные как
сенильные бляшки
9.
НормаКаждый нейрон имеет внутри себя цитоскелет, в
состав
которого
входят
микротрубочки.
Микротрубочки являются рельсами, по которым
питательные
вещества
транспортируются
к
различным частям нейрона. Тау-белок скрепляет эти
микротрубочки стабилизируя их структуру.
Тау-белок
Патология
1) Изменённый
Патология тау-белок
покидает микротрубочки,
нити его объединяется в
клубки внутри нейрона.
2)
Микротрубочки
распадаются,
транспортная
система
клетки разрушается
3) Передача ионного кода
от
клетки
к
клетке
нарушается.
4)
Нейрон
перестаёт
выполнять свои функции
5)
Запускается
предназначенная
для
этого случая программа
апоптоза,
нейрон
разрушается.
10.
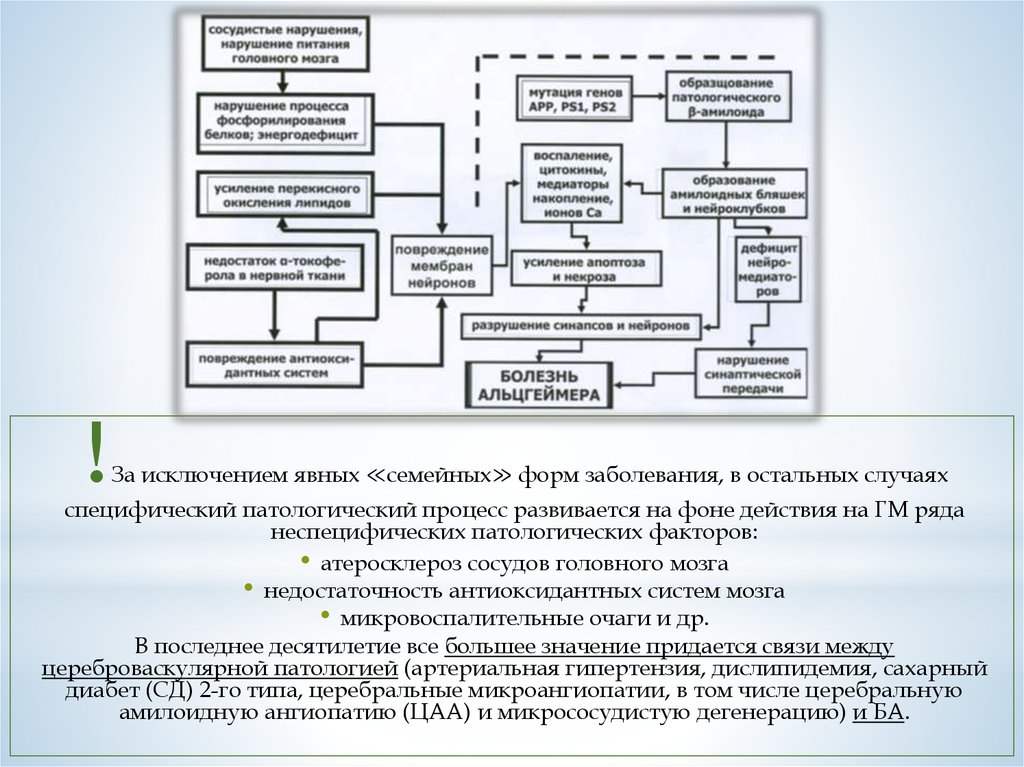
!За исключением явных ≪семейных≫ форм заболевания, в остальных случаях
специфический патологический процесс развивается на фоне действия на ГМ ряда
неспецифических патологических факторов:
• атеросклероз сосудов головного мозга
• недостаточность антиоксидантных систем мозга
• микровоспалительные очаги и др.
В последнее десятилетие все большее значение придается связи между
цереброваскулярной патологией (артериальная гипертензия, дислипидемия, сахарный
диабет (СД) 2-го типа, церебральные микроангиопатии, в том числе церебральную
амилоидную ангиопатию (ЦAA) и микрососудистую дегенерацию) и БА.
11.
Клиническая картина заболевания.БА в зависимости от возраста дебюта делится:
* с поздним началом (у пациентов старше 85 лет)
* типичным дебютом (65–80 лет)
* ранним дебютом (60 лет и менее)
Рассматривают также несколько клинических вариантов
течения БА:
* амнестический
* афазический
* апраксический,
* с визуально-пространственными
нарушениями
* поведенческий
12.
* Прогрессирующее нарушение памяти, попринципу ≪от настоящего к прошлому≫
* Нарушение внимания (больные становятся
неспособными сосредоточится на какой либо
проблеме)
* Неуклонное нарастание симптомов прогрессирующей
деменции постепенно приводит к нарушению
процессов мышления и способности к обучению
* Дезориентация во времени и пространстве
* Затруднения при подборе слов, трудности в общении,
изменения личности.
* Со временем больные полностью утрачивает
способность к самообслуживанию, становятся
беспомощными, требуют постоянного наблюдения со
стороны родственников или медицинских работников.
13.
Диагностика заболеванияДиагностические критерии деменции типа Альцгеймера Американской психиатрической
ассоциации (APA, 2000)
- Развивается множественный дефицит познавательных функций, который проявляется
одновременно, по крайней мере, в двух:
* нарушением памяти (способности запоминать новую или воспроизводить ранее
запомненную информацию);
* одним или несколькими нарушениями других когнитивных функций:
* афазией;
* апраксией;
* агнозией;
* нарушением исполнительных функций.
- Когнитивный дефицит влечет за собой существенное нарушение социальной адаптации или
способности к трудовой деятельности
- Течение болезни характеризуется постепенным началом и прогрессированием когнитивного
снижения.
- Нарушение когнитивных функций не зависит от:
* других заболеваний центральной нервной системы (ЦНС), которые сопровождаются
прогрессирующим снижением памяти и других когнитивных функций;
* общих заболеваний, которые могут приводить к деменции;
* состояний, связанных с влиянием различных веществ.
- Когнитивный дефицит отмечается не только в делириозном состоянии.
- Следует отличать нарушения когнитивных функций, связанные с другими психиатрическими
расстройствами, например с депрессивным расстройством или шизофренией).
14.
Критерии синдрома слабоумия.Слабоумие – это снижение памяти и других
познавательных функций по сравнению с предыдущим
состоянием пациента, что определяется по упадку
деятельности и по отклонениям, отмеченным при
проведении
клинического
обследования
и
нейропсихологических тестов.
Диагноз слабоумия не ставится, если у пациента
наблюдается нарушение сознания, либо когда наличие
других клинических нарушений препятствует адекватной
оценке психического состояния.
Диагноз слабоумия ставится на основе поведения
пациента и не может быть подтвержден МРТ/КТ, ЭЭГ или
другими инструментальными исследованиями, хотя с их
помощью
можно
выявить
определенные
причины
слабоумия.
15.
Критерии диагноза определенной БА включаютклинические
критерии
вероятной
БА
и
гистопатологическое подтверждение, полученное при
биопсии или аутопсии.
В пользу диагноза вероятной БА свидетельствуют:
• прогрессирующее снижение специфических познавательных функций в виде развития
афазии, апраксии и агнозии;
• нарушение способности осуществлять повседневную деятельность и изменение стереотипов
поведения;
• наличие в семье аналогичных заболеваний, особенно подтвержденных нейропатологически;
• нормальный характер или неспецифические изменения на ЭЭГ (увеличение удельного веса
медленной активности);
• признаки атрофии головного мозга, зафиксированные при КТ или МРТ;
• признаки, не противоречащие диагнозу вероятной БА (после исключения других заболеваний
ЦНС);
• наличие стадий «плато» при прогрессирующем течении заболевания;
• присоединение симптомов депрессии, бессонницы, раздражительности, делирия, иллюзий,
бреда, пароксизмов вербальных, эмоциональных и физических нарушений, сексуальных
расстройств и потери массы тела;
• другие неврологические нарушения, особенно на поздних стадиях болезни, такие как
нарушения в двигательной сфере – повышение мышечного тонуса, миоклонии или нарушения
походки;
• судорожные приступы (на поздних стадиях болезни);
• нормальные для данного возраста результаты КТ или МРТ головного мозга.
16.
Оценку функции внимания и концентрации, памяти нанедавние и отдаленные события, речи, праксиса,
исполнительных и зрительно-пространственных функций.
для определения состояния пациента.
17.
Полное неврологическое обследование для определенияпризнаков других заболеваний, которые могут быть причиной
деменции (мультиинфарктных процессов, болезни Паркинсона и
др.)
Диффернциальный диагноз следует проводить с афазией,
кортико-базальной дегенерацией, деменцией с тельцами Леви,
фронто-темпоральной
деменцией,
болезнью
Лима,
нейросифилисом, болезнью Паркинсона, прионовыми болезнями,
заболеваниями щитовидной железы, болезнью Вилсона и др.
Могут быть проведены следующие лабораторные тесты:
o оценка показателей клеток крови и кобаламина
o исследование уровня печеночных энзимов
o анализ уровня тиреоидного стимулирующего гормона (TSH)
o тесты для исключения сифилиса
o уровень витамина D (существует возможная связь между
недостатком витамина D и когнитивным снижением)
Люмбарная пункция проводится для измерения тау и амилоида в
цеброспинальной жидкости (уровень тау и фосфорилированного
тау часто повышается, а уровень амилоида обычно низкий)
Генетическое тестирование мутаций АРР и пресенилинов
18.
МРТ-или КТ-сканирования ГМ при БА могут
свидетельствовать о наличии диффузной кортикальной
и/или
церебральной
атрофии.
В
клинических
исследованиях было показано, что атрофия гиппокампа
может рассматриваться как валидный биомаркер
нейропатологии альцгеймеровского типа.
19.
20.
Лечение.Медикаментозное
Немедикаментозное
21.
Лекарственная терапияВыбор препарата на стадии деменции
должен удовлетворять всем принципам базисной
терапии.
В настоящее время этим требованиям
удовлетворяют две группы препаратов:
ингибиторы ацетилхолинэстеразы (ИАХЭ) и
обратимый ингибитор NMDA-рецепторов
22.
ИАХЭ.В настоящее время в России для лечения БА применяются
три препарата ИАХЭ:
На фоне приема ИАХЭ отмечается уменьшение
выраженности когнитивных расстройств, в частности
нарушений памяти, дисрегуляторных расстройств. Особенно
хорошо эта группа препаратов зарекомендовала себя при
наличии у пациентов психотических нарушений.
Побочные эффекты ИАХЭ проявляются желудочнокишечными расстройствами и проходят при отмене
препарата или уменьшении его дозы.
23.
Блокатор NMDA-глутаматных рецепторов.Тормозит глутаматергическую нейротрансмиссию и
прогрессирование
нейродегенеративных
процессов,
оказывает нейромодулирующее действие.
Способствует нормализации психической активности
(улучшает память и способность к концентрации внимания,
уменьшает утомляемость, симптомы депрессии и пр.) и
коррекции двигательных нарушений.
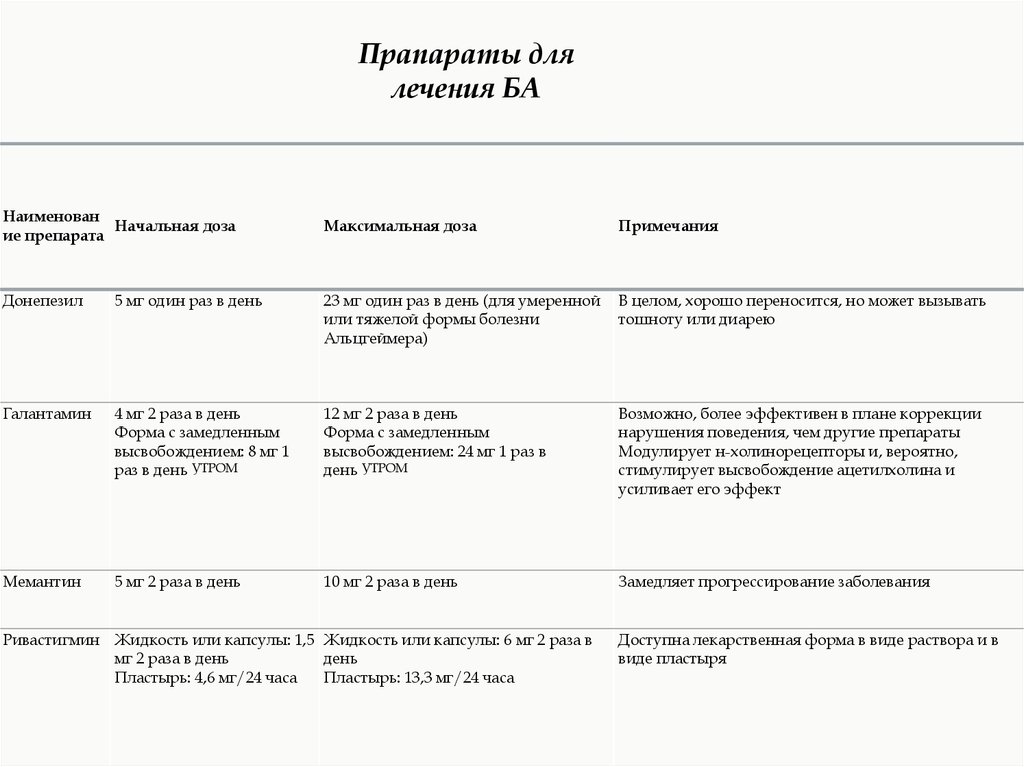
24.
Прапараты длялечения БА
Наименован
Начальная доза
ие препарата
Максимальная доза
Примечания
Донепезил
5 мг один раз в день
23 мг один раз в день (для умеренной
или тяжелой формы болезни
Альцгеймера)
В целом, хорошо переносится, но может вызывать
тошноту или диарею
Галантамин
4 мг 2 раза в день
Форма с замедленным
высвобождением: 8 мг 1
раз в день УТРОМ
12 мг 2 раза в день
Форма с замедленным
высвобождением: 24 мг 1 раз в
день УТРОМ
Возможно, более эффективен в плане коррекции
нарушения поведения, чем другие препараты
Модулирует н-холинорецепторы и, вероятно,
стимулирует высвобождение ацетилхолина и
усиливает его эффект
Мемантин
5 мг 2 раза в день
10 мг 2 раза в день
Замедляет прогрессирование заболевания
Ривастигмин Жидкость или капсулы: 1,5 Жидкость или капсулы: 6 мг 2 раза в
мг 2 раза в день
день
Пластырь: 4,6 мг/24 часа
Пластырь: 13,3 мг/24 часа
Доступна лекарственная форма в виде раствора и в
виде пластыря
25.
«Если вы – больная «Альцгеймером» мышка, товам повезло, мы вас вылечим. Но если вы
человек – увы.»
26.
Новые данные.VTV Therapeutics – это небольшая компания в
штате
Северная
Королина
(США),
которая
испытывает
препарат
Азелирагонпрепарат,
ингибирующий рецептор RAGE, помогая людям с
умеренным снижением когнитивной сферы при БА.
Ожидается, что 3 фаза завершится в 2018 г.
Адукамумаб, препарат компании Biogen –
ингибитор BACE (бета-секретазы). Ожидается, что
результаты будут получены в 2019 г. или в начале
2020 г.
Ланабецестат (BACE-ингибитор) – готовится к
выходу в 2019 г.
У Genentech имеется 2 препарата на поздних
стадиях разработки : Кренезумаб и Гантенерумаб.
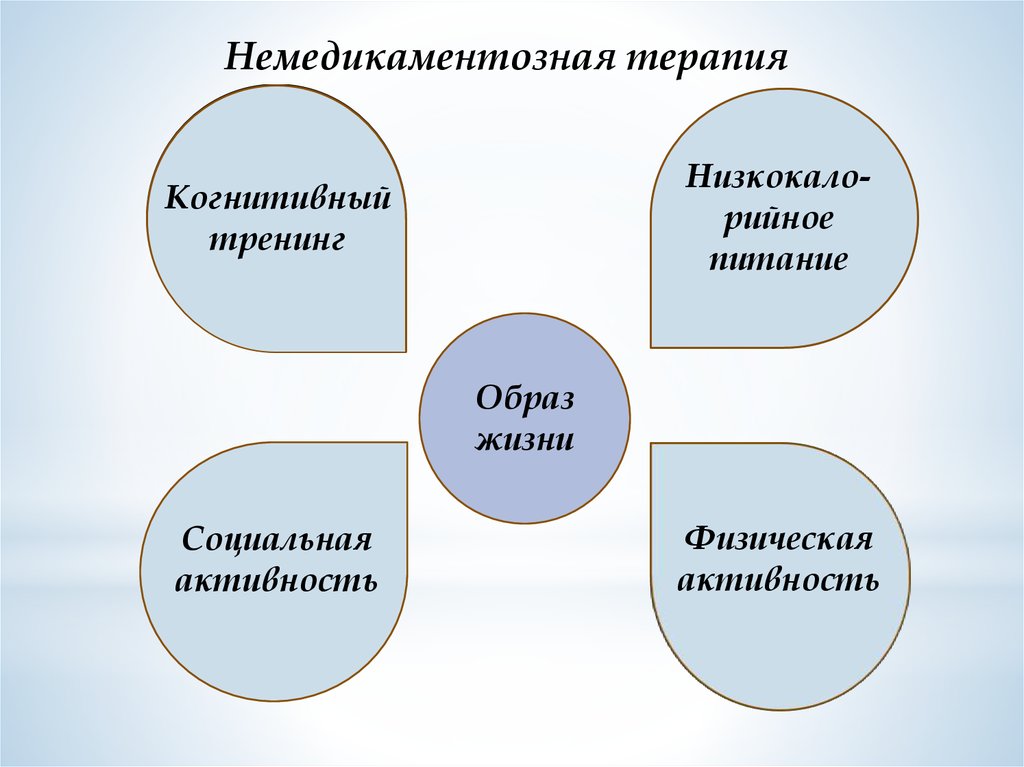
27.
Немедикаментозная терапияНизкокалорийное
питание
Когнитивный
тренинг
Образ
жизни
Социальная
активность
Физическая
активность





















 Медицина
Медицина








