Похожие презентации:
Катализ. Факторы, влияющие на скорость реакции
1.
Катализ.Факторы влияющие
на скорость реакции
2.
Катализ – это явлениеизменения
скорости
реакции под влиянием
веществ, называемых
катализаторами.
3.
Катализаторы–
это вещества, изменяющие
скорость химической реакции,
но не изменяющиеся в ходе
процесса ни качественно, ни
количественно. Они не входят в
состав продуктов реакции.
4.
Небольшиеколичества
катализаторов способны
существенно
изменить
скорость взаимодействия
большого
количества
реагирующих веществ.
5.
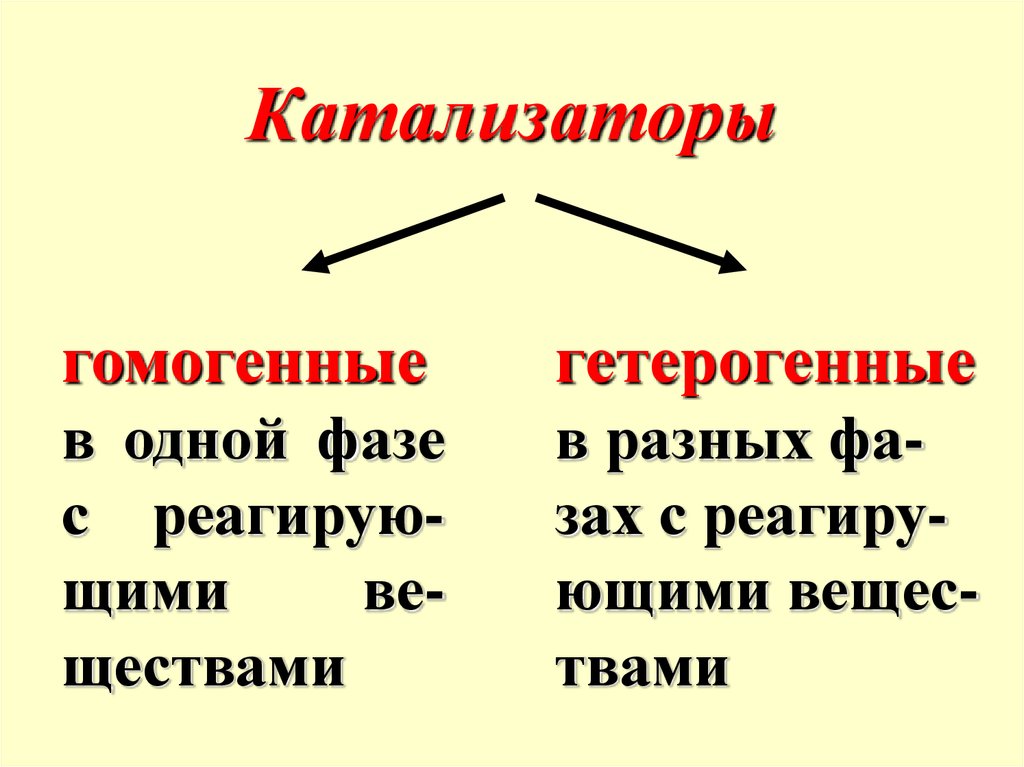
Катализаторыгомогенные
гетерогенные
в одной фазе
с реагирующими
веществами
в разных фазах с реагирующими веществами
6.
Пример гетерогенногокатализа
.... N + 3H
2
2
Pt
2NH3
7.
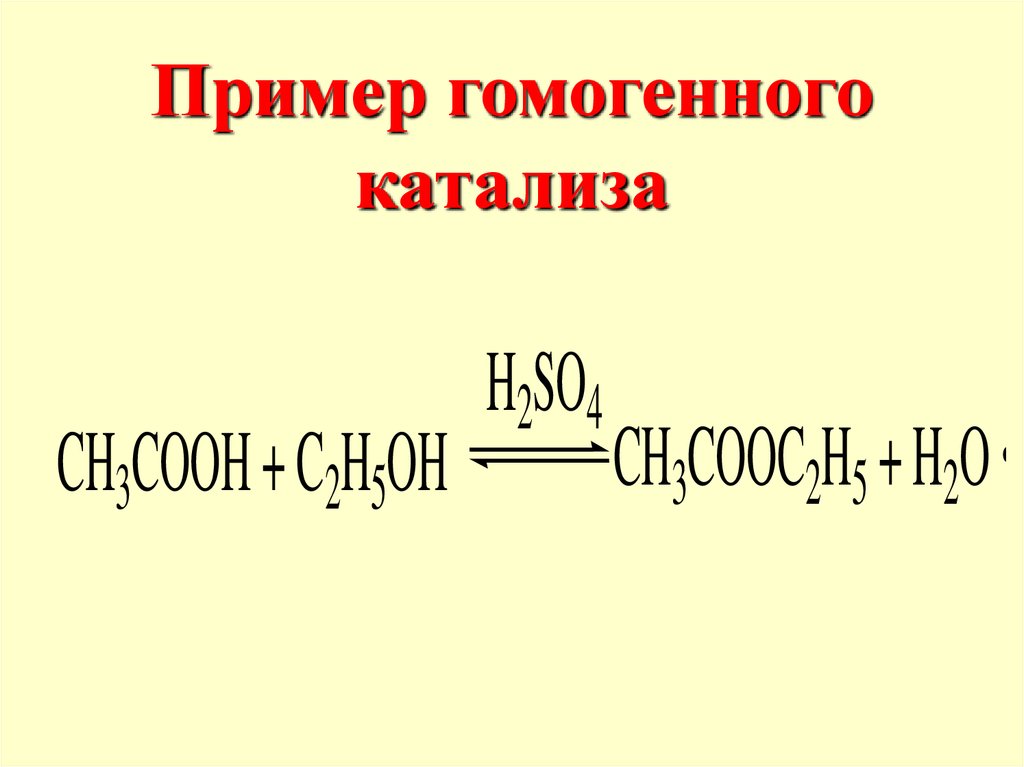
Пример гомогенногокатализа
CH3COOH + C2H5OH
H2SO4
...
CH3COOC2H5 + H2O
8.
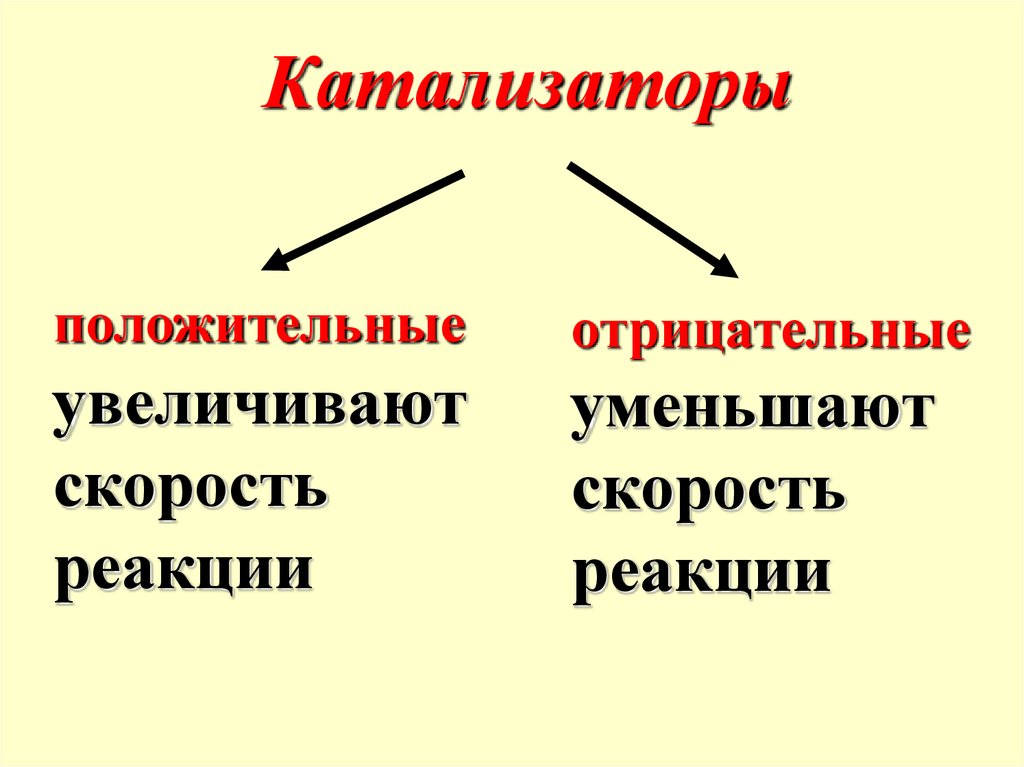
Катализаторыположительные
отрицательные
увеличивают
скорость
реакции
уменьшают
скорость
реакции
9.
Ингибиторы–
вещества,
уменьшающие скорость реакции, но расходующиеся при этом сами.
10.
С точки зрения теорииактивного
комплекса
механизм
действия
катализаторов в том, что
они изменяют высоту
энергетического барьера
химической реакции.
11.
Без катализатора:А + В ↔ А...В → АВ
В присутствии
затора:
катали-
А + В + К↔ А...К...В →
→ АВ + К
12.
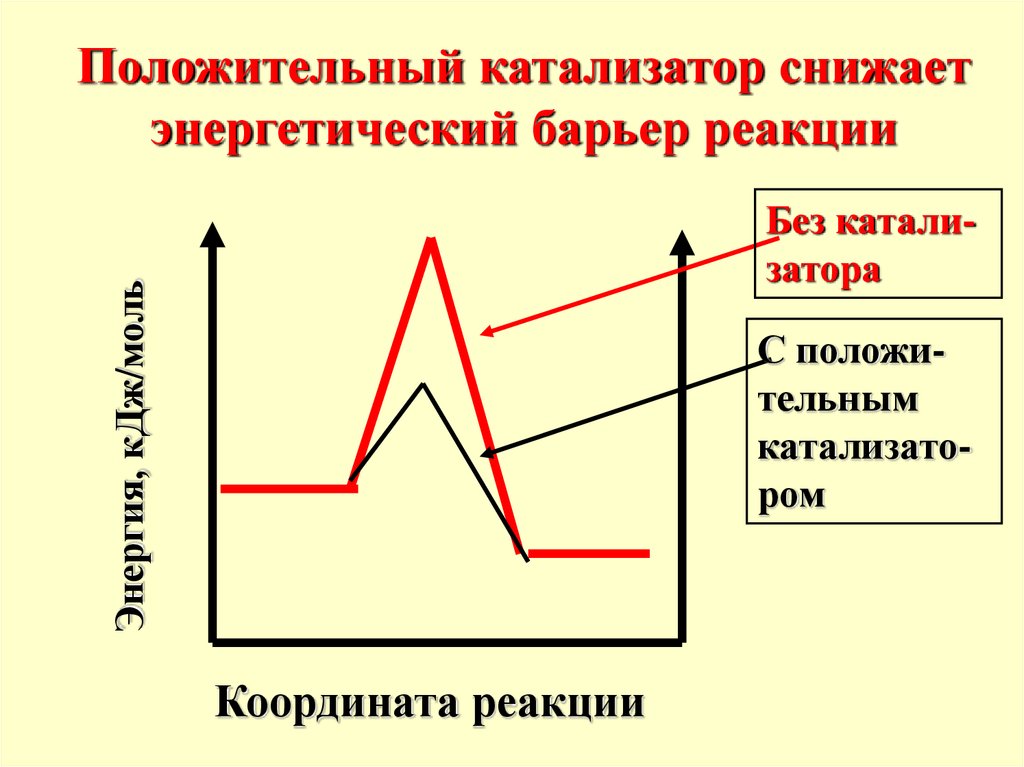
Положительный катализатор снижаетэнергетический барьер реакции
Энергия, кДж/моль
Без катализатора
С положительным
катализатором
Координата реакции
13.
Под воздействием положительного катализаторав реакционной смеси
возрастает доля активных молекул при данной
температуре.
Скорость
реакции увеличивается.
14.
Под воздействием отрицательного катализаторав реакционной смеси
снижается доля активных молекул при данной
температуре.
Скорость
реакции уменьшается.
15.
Разрушениеслоя Земли
озонового
– пример
гомогенного
катализа,
протекающего в атмосфере
под воздействием фреонов.
16.
Фреоны– это фторохлороуглеводороды (СF2Cl2),
применяемые как хладагенты. При обычных условиях
они отличаются высокой
устойчивостью к разложению.
17.
Ватмосфере
происходит
разложение
фреонов
под
воздействием
ультрафиолетового излучения солнца:
CF2Cl2
CF2Cl
+
Cl
Cl - катализатор
разложения озона
18.
Без катализаторапроцесс протекает по
схеме:
O3 + O 2 O2
Eак = 17,1 кДж/моль
19.
В присутствии катализатора:O3 + Cl ClO + O2
Eак= 2,1 кДж/моль
ClO + O Cl + O2
Eак = 0,4 кДж/моль
O3 + O 2 O2
Cl
20.
Вещества,усиливающие действие катализаторов, называются промоторами, а ослабляющие - каталитическими
ядами.
21.
Практически всебиохимические реакции
являются ферментативными.
Ферменты (биокатализаторы) –
это
вещества
белковой
природы,
активированные
катионами металлов.
22.
Известно около 2000различных ферментов,
~150 из них выделены,
причем
некоторые
используются в качестве
лекарственных
препаратов.
23.
Трипсин и химотрипсин– лечение бронхитов и пневмонии;
пепсин – лечение гастрита;
плазмин – лечение инфаркта;
панкреатин – лечение поджелудочной железы.
24.
Ферменты отличаются отобычных катализаторов:
а)
более
высокой
каталитической
активностью;
б)
высокой
специфичностью, т.е. избирательностью действия.




















 Химия
Химия








