Похожие презентации:
Химические реакции полимеров. Классификация
1.
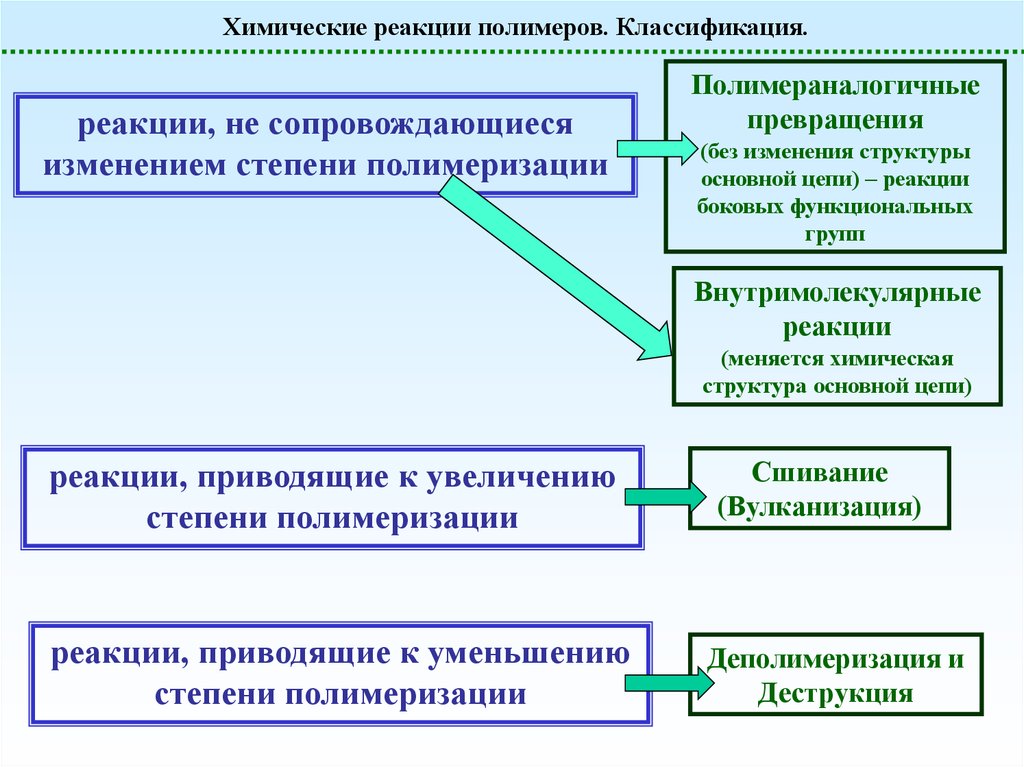
Химические реакции полимеров. Классификация.реакции, не сопровождающиеся
изменением степени полимеризации
Полимераналогичные
превращения
(без изменения структуры
основной цепи) – реакции
боковых функциональных
групп
Внутримолекулярные
реакции
(меняется химическая
структура основной цепи)
реакции, приводящие к увеличению
степени полимеризации
реакции, приводящие к уменьшению
степени полимеризации
Сшивание
(Вулканизация)
Деполимеризация и
Деструкция
2.
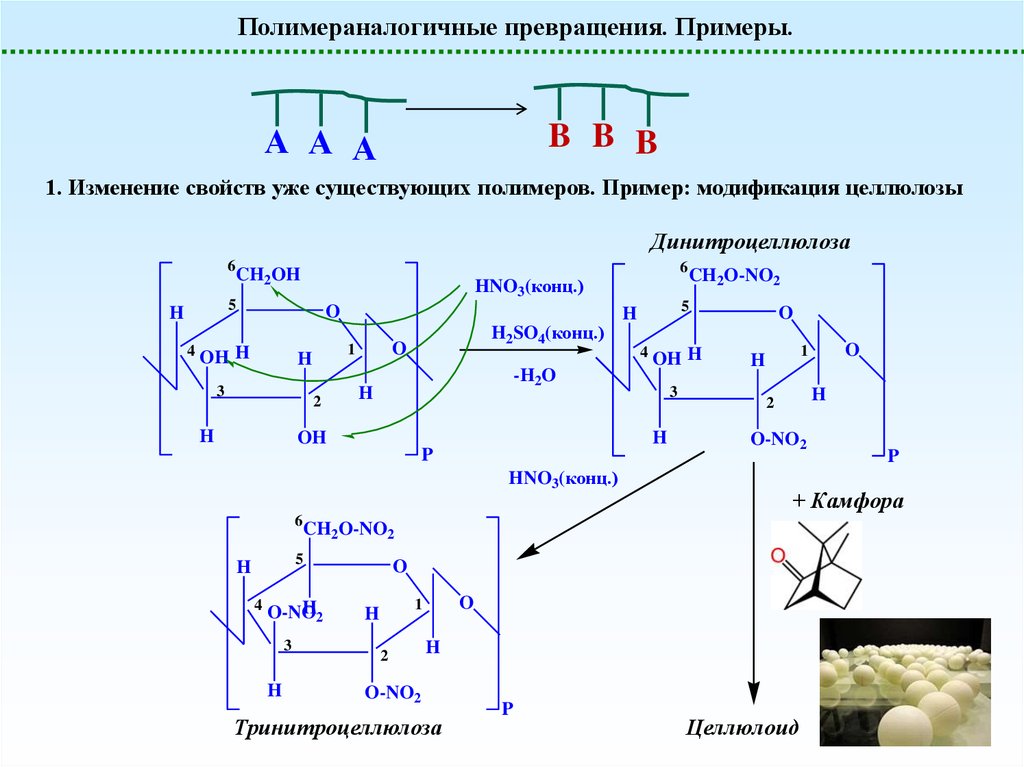
Полимераналогичные превращения. Примеры.А А А
B B B
1. Изменение свойств уже существующих полимеров. Пример: модификация целлюлозы
Динитроцеллюлоза
6
6
CH2OH
HNO3(конц.)
5
H
O
4 OH H
3
2
H
O
1
H
-H2O
H
P
HNO3(конц.)
2
H
H
2
O-NO2
2
H
O-NO2
Тринитроцеллюлоза
P
P
+ Камфора
O
1
H
O
1
H
O
4 O-NO
H
3
3
O
CH2O-NO2
5
H
4 OH H
H
OH
6
5
H
H2SO4(конц.)
CH2O-NO2
Целлюлоид
3.
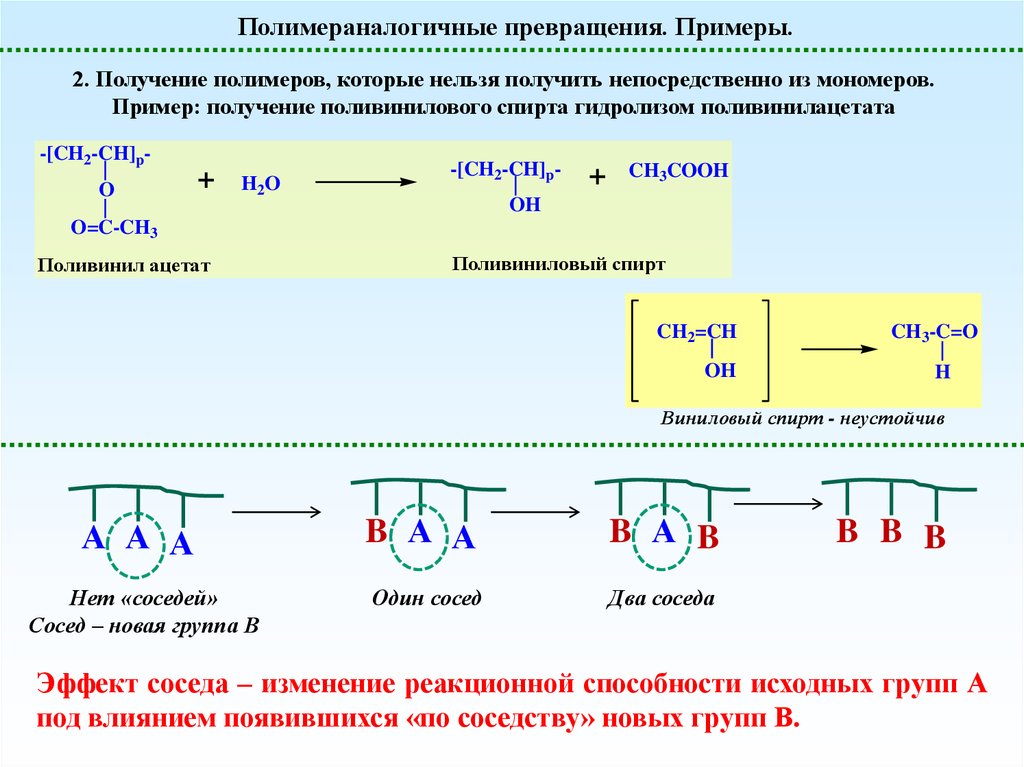
Полимераналогичные превращения. Примеры.2. Получение полимеров, которые нельзя получить непосредственно из мономеров.
Пример: получение поливинилового спирта гидролизом поливинилацетата
-[CH2-CH]pO
+
H2O
-[CH2-CH]p-
+
CH3COOH
OH
O=C-CH3
Поливинил ацетат
Поливиниловый спирт
CH2=CH
OH
CH3-C=O
H
Виниловый спирт - неустойчив
А А А
B А А
B А B
Нет «соседей»
Сосед – новая группа В
Один сосед
Два соседа
B B B
Эффект соседа – изменение реакционной способности исходных групп А
под влиянием появившихся «по соседству» новых групп В.
4.
Полимераналогичные превращения. Эффект соседа.-А
-В
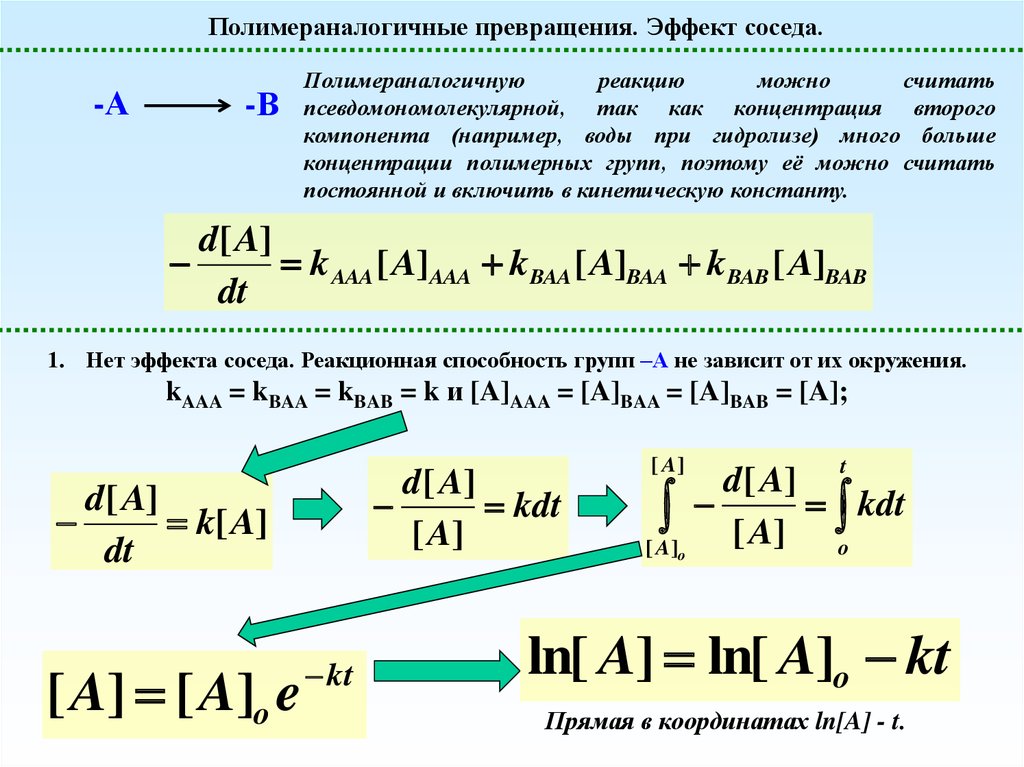
Полимераналогичную
реакцию
можно
считать
псевдомономолекулярной, так как концентрация второго
компонента (например, воды при гидролизе) много больше
концентрации полимерных групп, поэтому её можно считать
постоянной и включить в кинетическую константу.
d[ A]
k AAA [ A]AAA k BAA [ A]BAA k BAB [ A]BAB
dt
1. Нет эффекта соседа. Реакционная способность групп –А не зависит от их окружения.
kAAA = kBAA = kBAB = k и [A]AAA = [A]BAA = [A]BAB = [A];
d [ A]
kdt
[ A]
d[ A]
k[ A]
dt
[ A] [ A]o e
kt
[ A]
t
d [ A]
kdt
[ A] o
[ A ]o
ln[ A] ln[ A]o kt
Прямая в координатах ln[A] - t.
5.
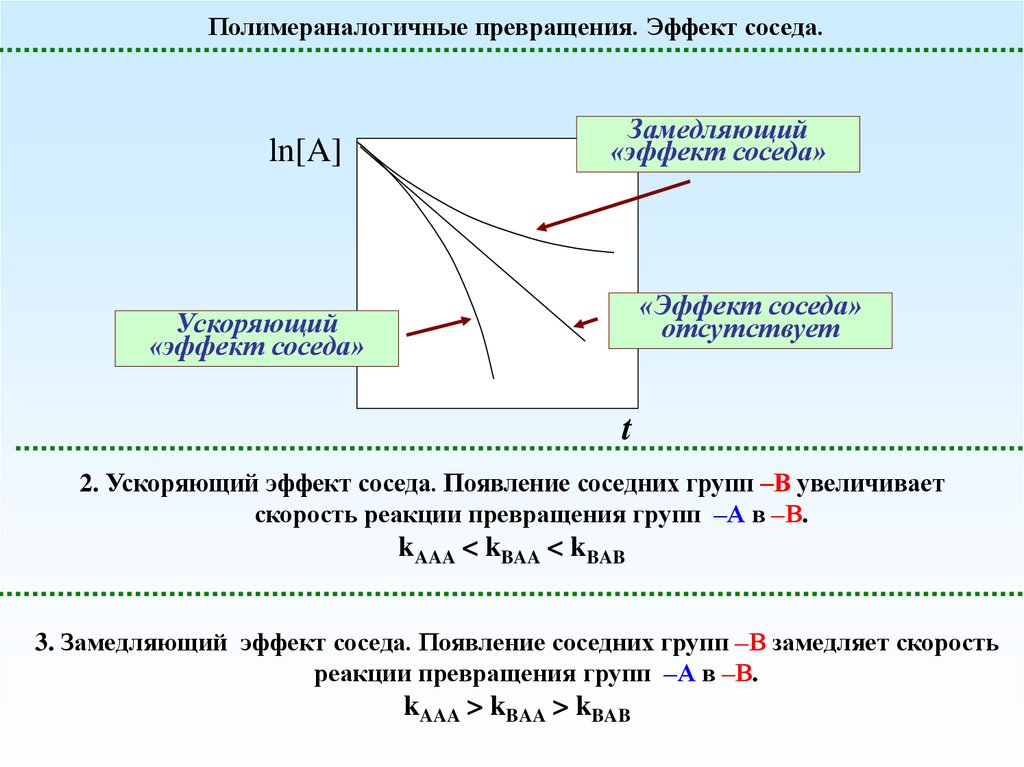
Полимераналогичные превращения. Эффект соседа.ln[A]
Замедляющий
«эффект соседа»
«Эффект соседа»
отсутствует
Ускоряющий
«эффект соседа»
t
2. Ускоряющий эффект соседа. Появление соседних групп –В увеличивает
скорость реакции превращения групп –А в –В.
kAAA < kBAA < kBAB
3. Замедляющий эффект соседа. Появление соседних групп –В замедляет скорость
реакции превращения групп –А в –В.
kAAA > kBAA > kBAB
6.
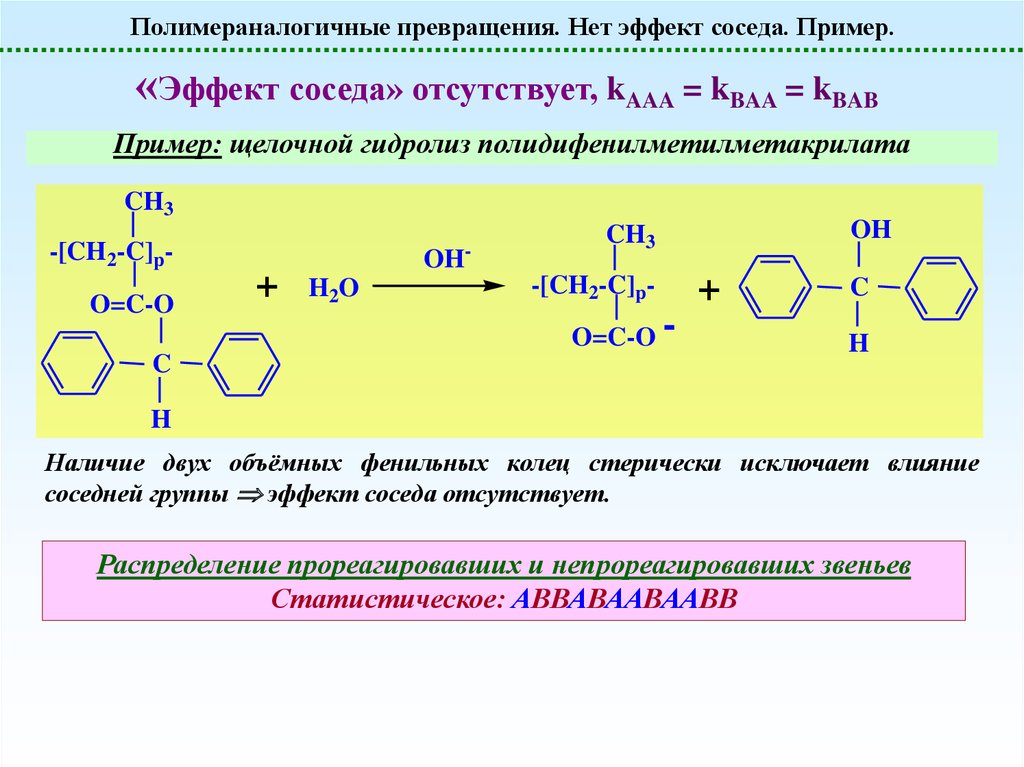
Полимераналогичные превращения. Нет эффект соседа. Пример.«Эффект соседа» отсутствует, kAAA = kBAA = kBAB
Пример: щелочной гидролиз полидифенилметилметакрилата
CH3
-[CH2-C]pO=C-O
C
+
OHH 2O
OH
CH3
-[CH2-C]pO=C-O -
+
C
H
H
Наличие двух объёмных фенильных колец стерически исключает влияние
соседней группы эффект соседа отсутствует.
Распределение прореагировавших и непрореагировавших звеньев
Статистическое: АВВАВААВААВВ
7.
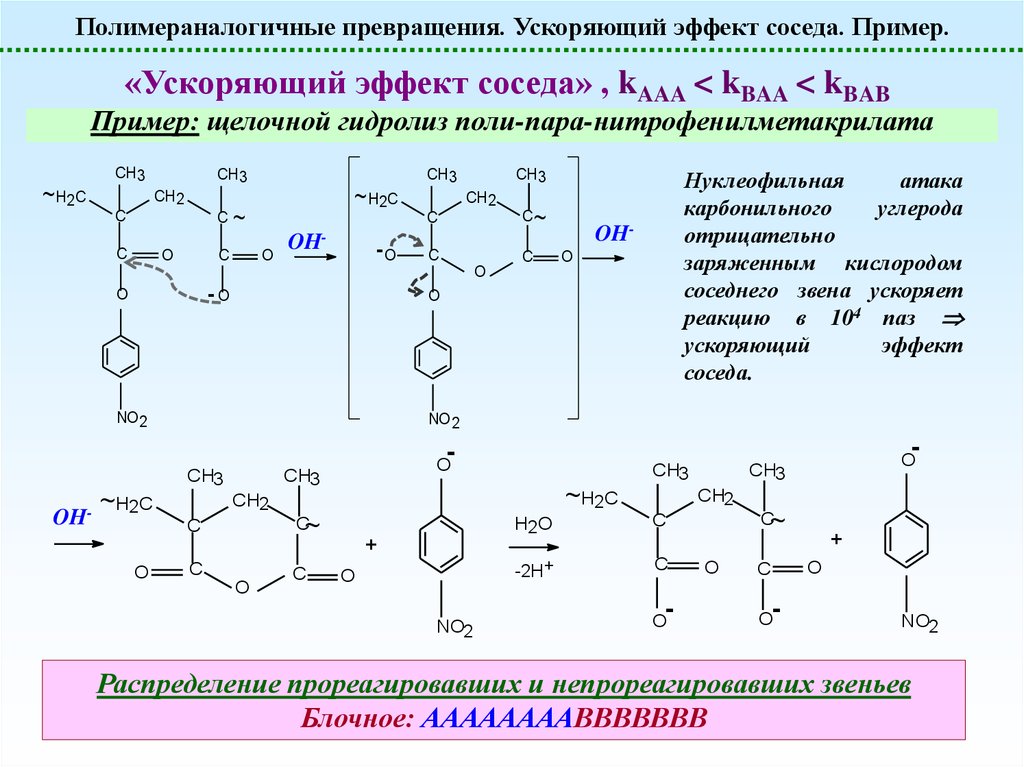
Полимераналогичные превращения. Ускоряющий эффект соседа. Пример.«Ускоряющий эффект соседа» , kAAA < kBAA < kBAB
Пример: щелочной гидролиз поли-пара-нитрофенилметакрилата
CH 3
~H2C
CH 3
CH 3
~H2C
CH 2
C
C
C
O
~
C
CH 2
C~
C
O
OH-
-O
Нуклеофильная
атака
карбонильного
углерода
отрицательно
заряженным кислородом
соседнего звена ускоряет
реакцию в 104 паз
ускоряющий
эффект
соседа.
CH 3
C
C
OHO
O
-O
O
O
NO 2
NO 2
-
-
CH3
OH-
~H2C
CH3
CH3
~H2C
CH2
C~
C
O
O
C
O
C
+
O
NO2
O
CH3
CH2
H2O
C
-2H+
C
-
O
C~
O
C
O-
+
O
NO2
Распределение прореагировавших и непрореагировавших звеньев
Блочное: ААААААААВВВВВВВ
8.
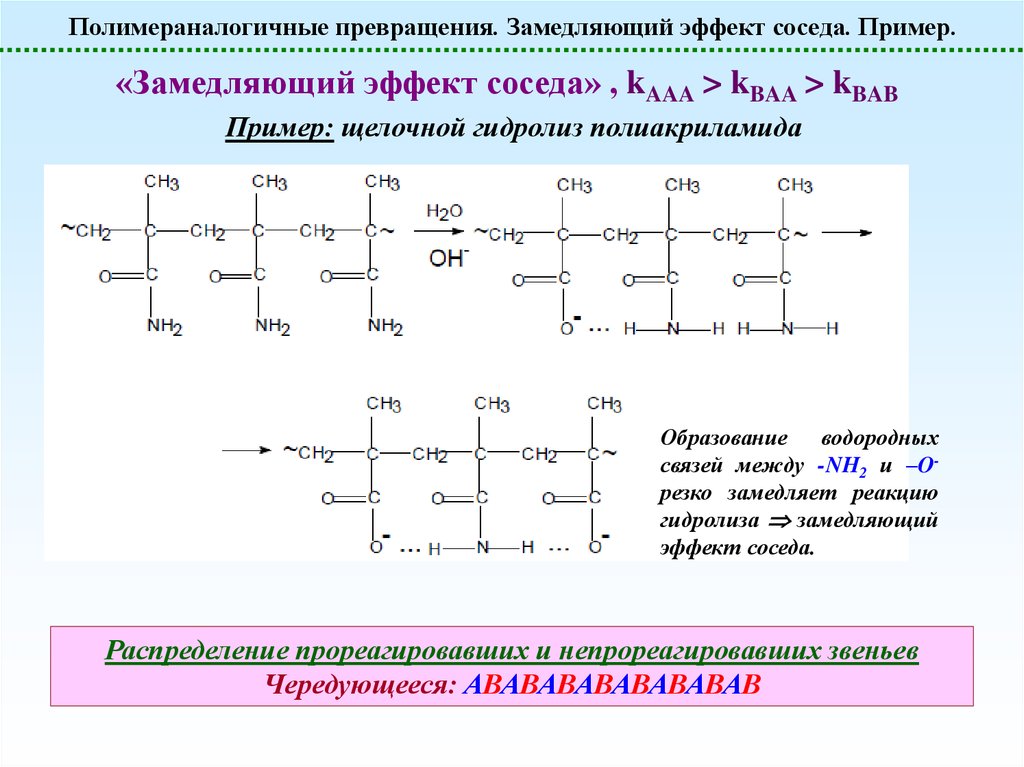
Полимераналогичные превращения. Замедляющий эффект соседа. Пример.«Замедляющий эффект соседа» , kAAA > kBAA > kBAB
Пример: щелочной гидролиз полиакриламида
Образование водородных
связей между -NH2 и –Oрезко замедляет реакцию
гидролиза замедляющий
эффект соседа.
Распределение прореагировавших и непрореагировавших звеньев
Чередующееся: АВАВАВАВАВАВАВАВ
9.
Полимераналогичные превращения. Другие полимерные эффектыНа скорость полимераналогичных превращений могут оказывать
другие полимерные эффекты:
•Конформационный
эффект
фепментативный катализ);
(гидролиз
поливиниацетата,
•Конфигурационный эффект (различие в реакционной способности изои синдио- изомеров);
•Надмолекулярный эффект (гидратированная и негидратированная
целлюлоза), аморфные и кристаллические области полимеров и др.
•Другие (концентрационный, электростатический)
10.
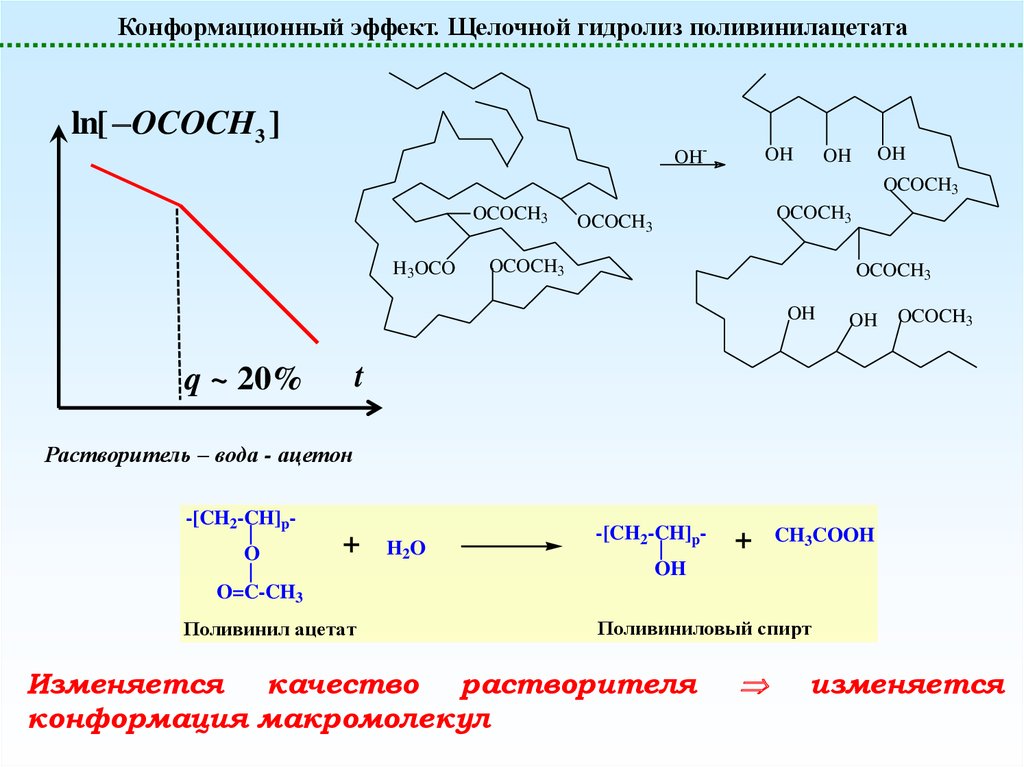
Конформационный эффект. Щелочной гидролиз поливинилацетатаln[ OCOCH3 ]
OH-
OH
OH
OH
OCOCH3
OCOCH3
H3OCO
OCOCH3
OCOCH3
OCOCH3
OCOCH3
OH
OH
OCOCH3
t
q ~ 20%
Растворитель – вода - ацетон
-[CH2-CH]pO
+
H2O
-[CH2-CH]p-
+
CH3COOH
OH
O=C-CH3
Поливинил ацетат
Поливиниловый спирт
Изменяется качество растворителя
конформация макромолекул
изменяется
11.
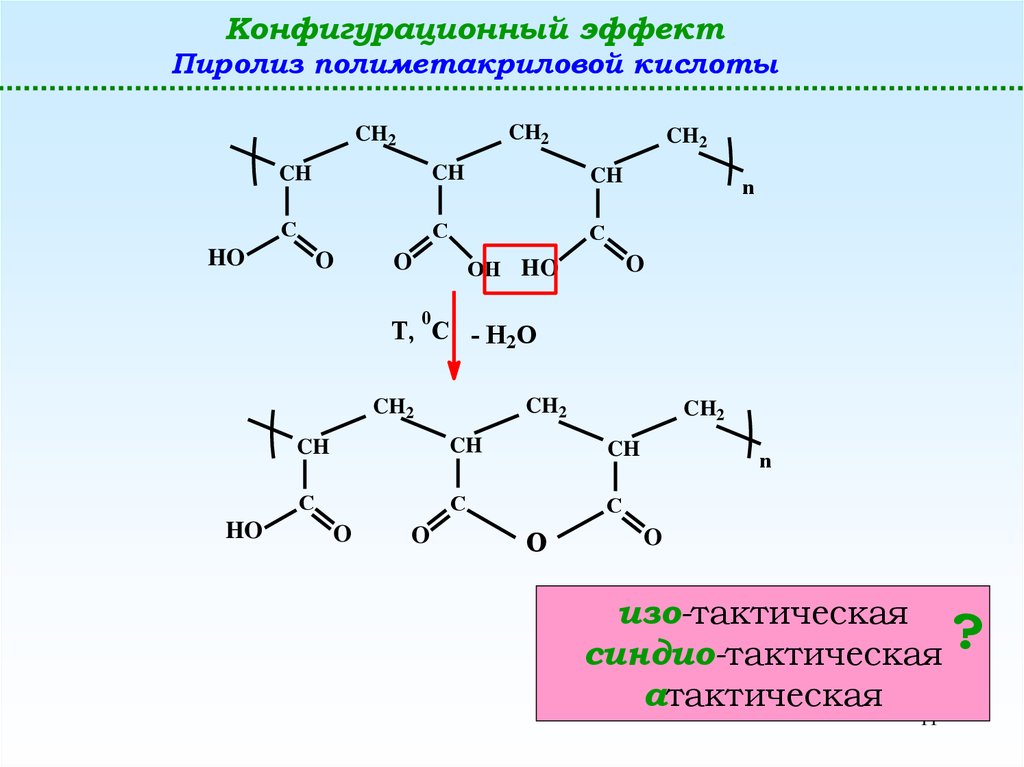
Конфигурационный эффектПиролиз полиметакриловой кислоты
CH2
CH2
CH2
CH
CH
CH
C
C
C
HO
O
O
n
O
OH HO
0
T, C - H2O
CH2
CH2
HO
CH2
CH
CH
CH
C
C
C
O
O
O
n
O
изо-тактическая
синдио-тактическая ?
атактическая
11
12.
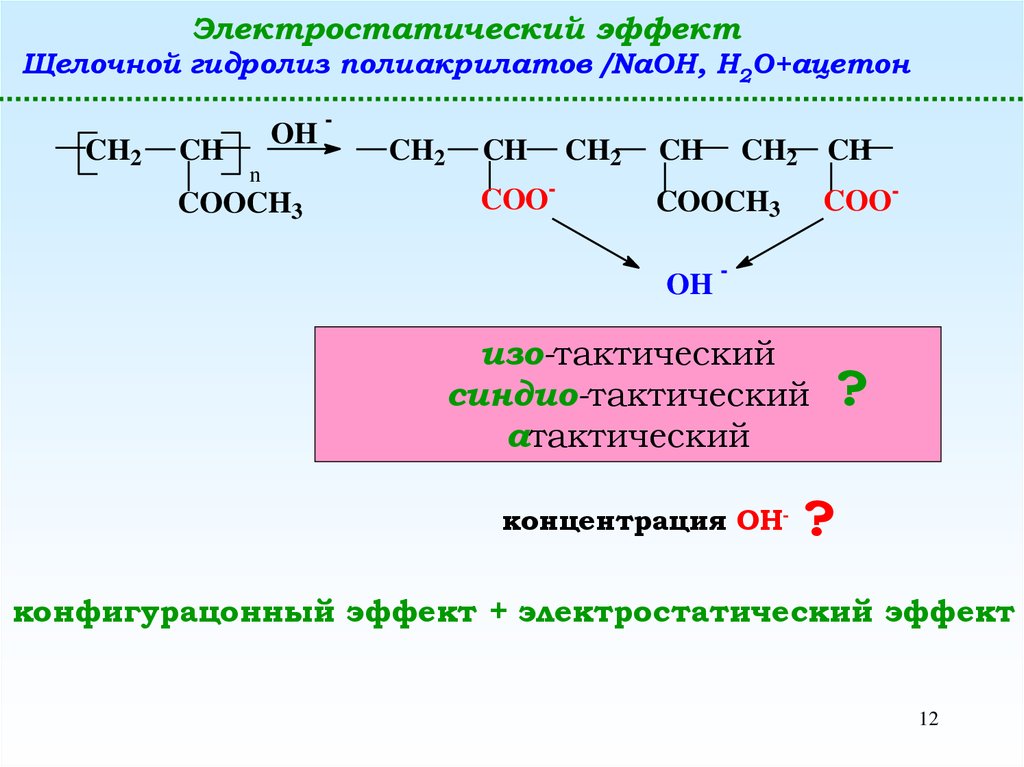
Электростатический эффектЩелочной гидролиз полиакрилатов /NaOH, H2O+ацетон
CH2
OH
CH
n
COOCH3
-
CH2
CH
COO-
CH2
CH2 CH
CH
COO-
COOCH3
OH
-
изо-тактический
синдио-тактический
атактический
концентрация ОН-
?
?
конфигурацонный эффект + электростатический эффект
12
13.
Надмолекулярный эффектХлорирование полиэтилена в твердой фазе
Скорость реакции в аморфных участках выше, чем
в кристаллических
Окисление полипропилена
Скорость уменьшается
ориентации полимера
при
предварительной
Результатом надмолекулярного эффекта является
композиционная
неоднородность
продуктов
полимераналогичных превращений
13
14.
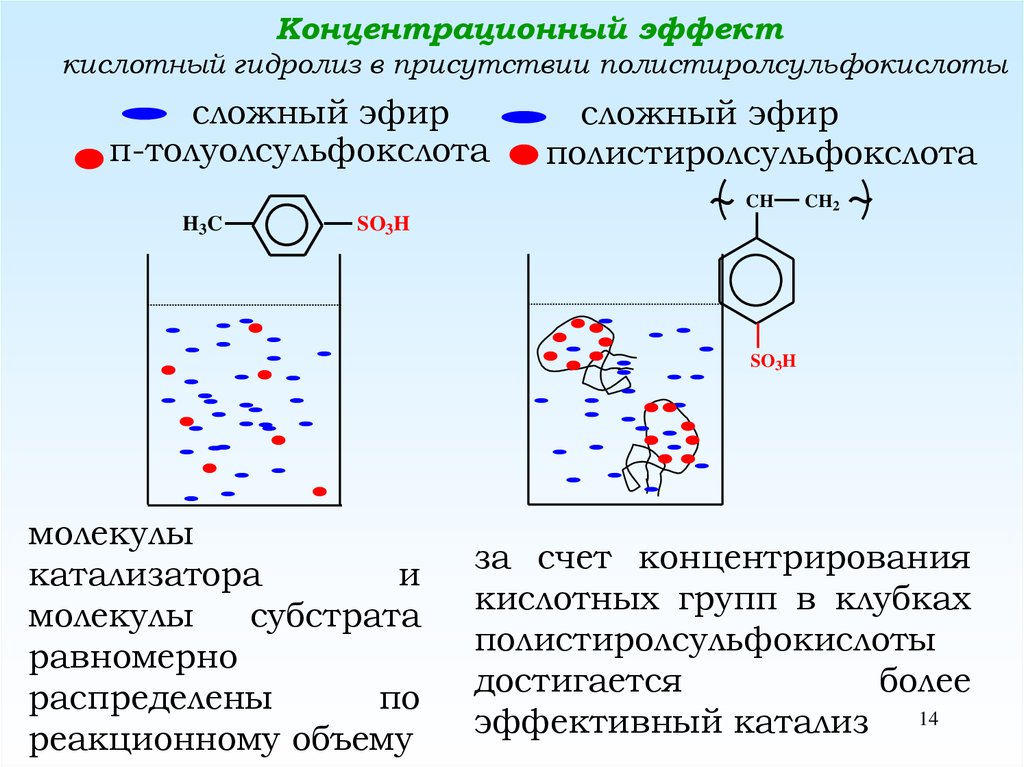
Концентрационный эффекткислотный гидролиз в присутствии полистиролсульфокислоты
сложный эфир
п-толуолсульфокслота
H3C
SO3H
сложный эфир
полистиролсульфокслота
~
CH
CH2
~
SO3H
молекулы
катализатора
и
молекулы
субстрата
равномерно
распределены
по
реакционному объему
за счет концентрирования
кислотных групп в клубках
полистиролсульфокислоты
достигается
более
эффективный катализ 14
15.
Внутримолекулярные реакции. Примеры.Внутримолекулярные реакции – реакции, приводящие к изменению структуры (скелета)
основной цепи без изменения степени полимеризации.
Пример 1: пиролиз поливинилового спирта
Нагревание
Поливиниловый спирт
2. Синтез полиацетилена (поливинилена)
CH2
CH
CH2
CH
n
OH
CH2
CH
OH
CH2
CH
n
OAc
OAc
CH2
CH
CH2
Cl
- CH3COOH
- HCl
CH
n
Cl
- H2O
CH2
CH
CH2
CH
n
16.
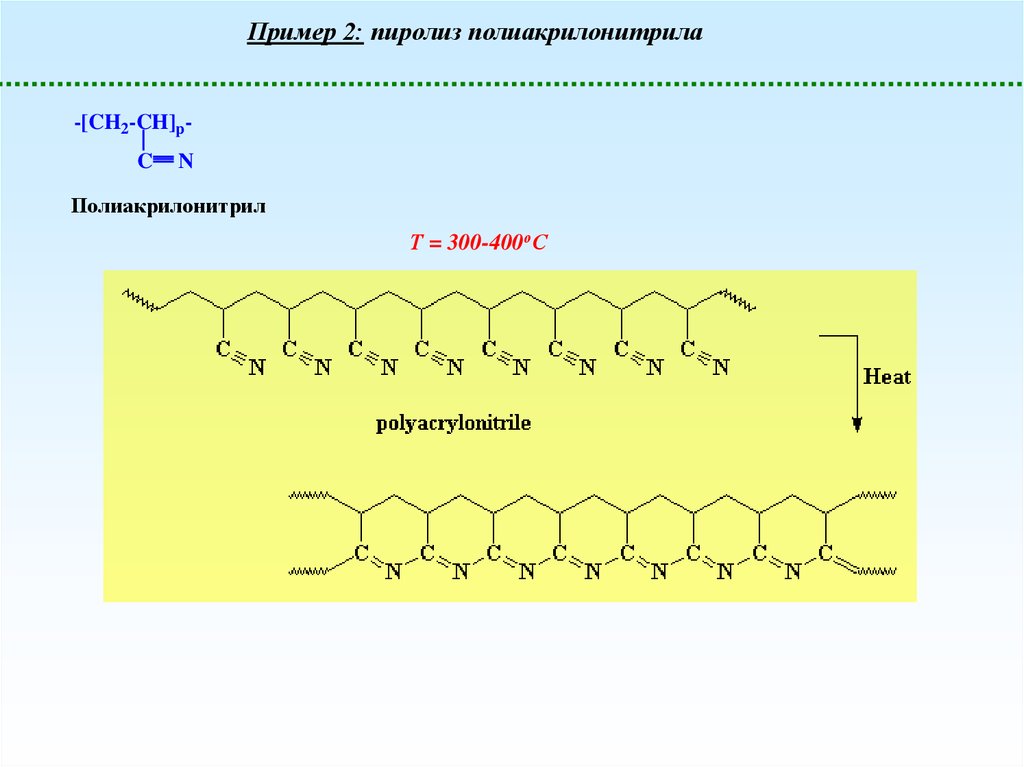
Пример 2: пиролиз полиакрилонитрила-[CH2-CH]pC
N
Полиакрилонитрил
Т = 300-400оС
17.
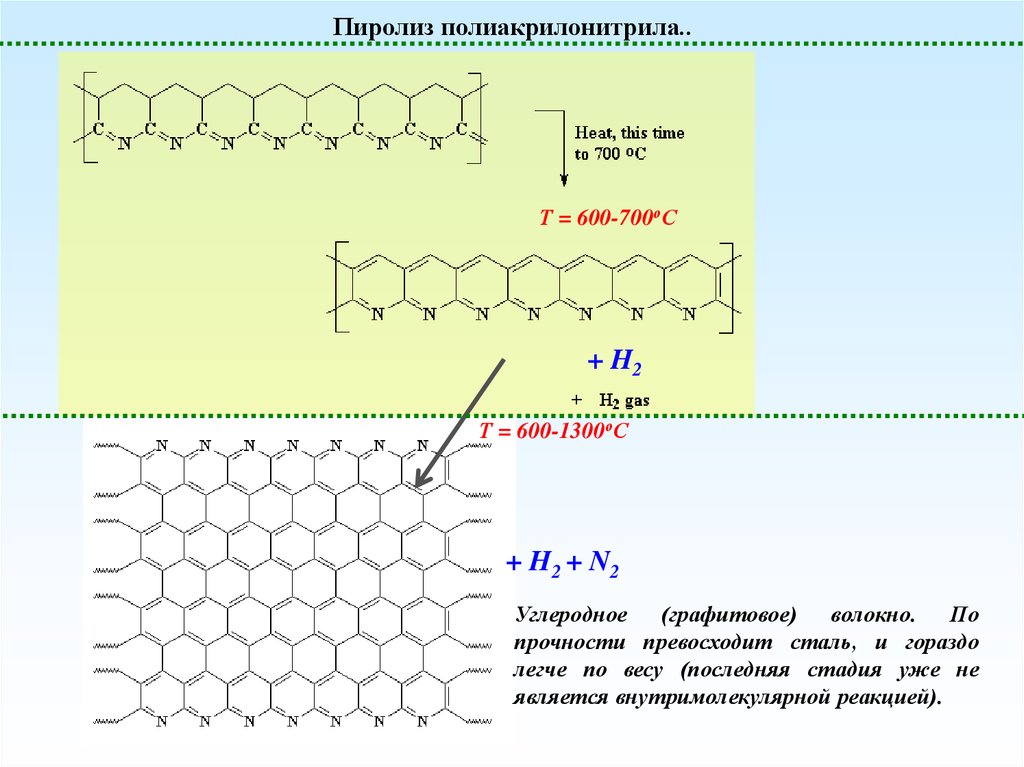
Пиролиз полиакрилонитрила..Т = 600-700оС
+ H2
Т = 600-1300оС
+ H2 + N 2
Углеродное (графитовое) волокно. По
прочности превосходит сталь, и гораздо
легче по весу (последняя стадия уже не
является внутримолекулярной реакцией).
18.
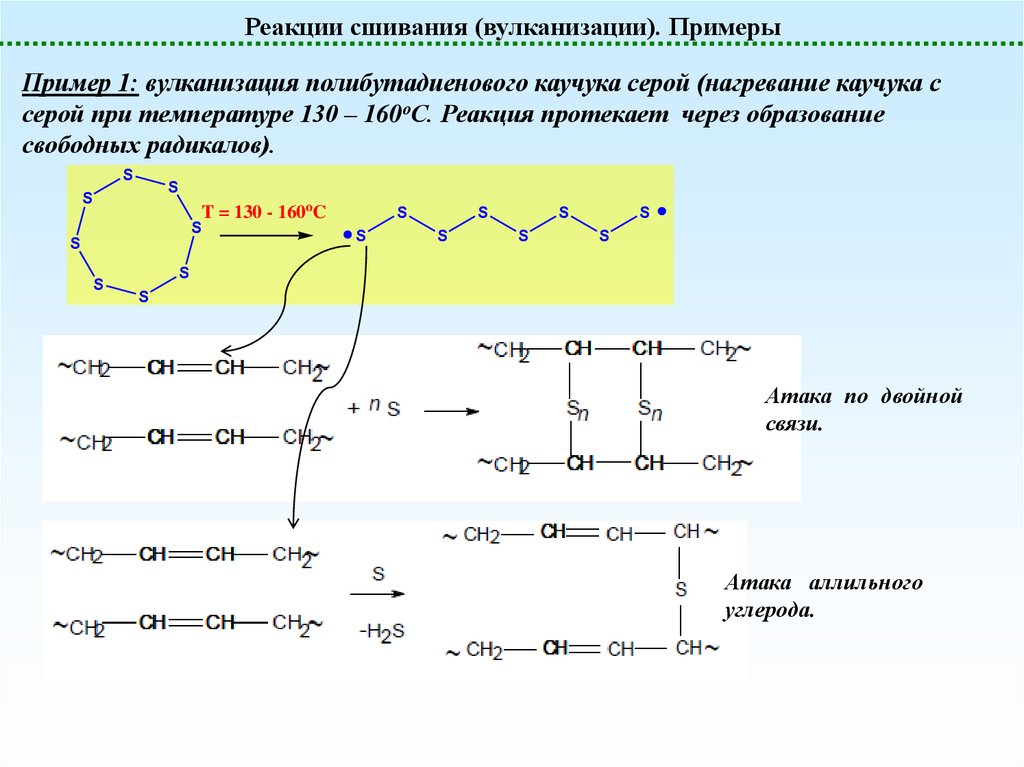
Реакции сшивания (вулканизации). ПримерыПример 1: вулканизация полибутадиенового каучука серой (нагревание каучука с
серой при температуре 130 – 160оС. Реакция протекает через образование
свободных радикалов).
S
S
S
T = 130 - 160oC
S
S
S
S
S
S
S
S
S
S
S
S
S
Атака по двойной
связи.
Атака аллильного
углерода.
19.
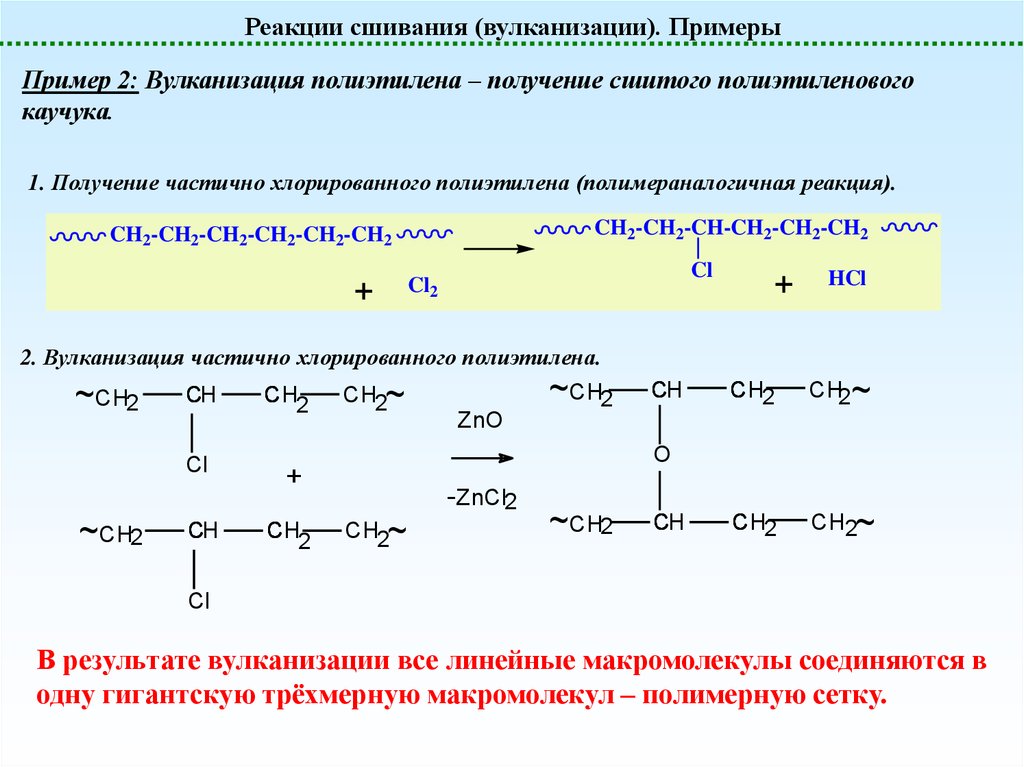
Реакции сшивания (вулканизации). ПримерыПример 2: Вулканизация полиэтилена – получение сшитого полиэтиленового
каучука.
1. Получение частично хлорированного полиэтилена (полимераналогичная реакция).
CH2-CH2-CH-CH2-CH2-CH2
CH2-CH2-CH2-CH2-CH2-CH2
+
Cl
Cl2
+
HCl
2. Вулканизация частично хлорированного полиэтилена.
~CH2
CH
Cl
~CH2
CH
CH2
CH2~
CH
CH2
CH2~
CH2
CH2~
ZnO
O
+
CH2
~CH2
-ZnCl2
CH2~
~CH2
CH
Cl
В результате вулканизации все линейные макромолекулы соединяются в
одну гигантскую трёхмерную макромолекул – полимерную сетку.
20.
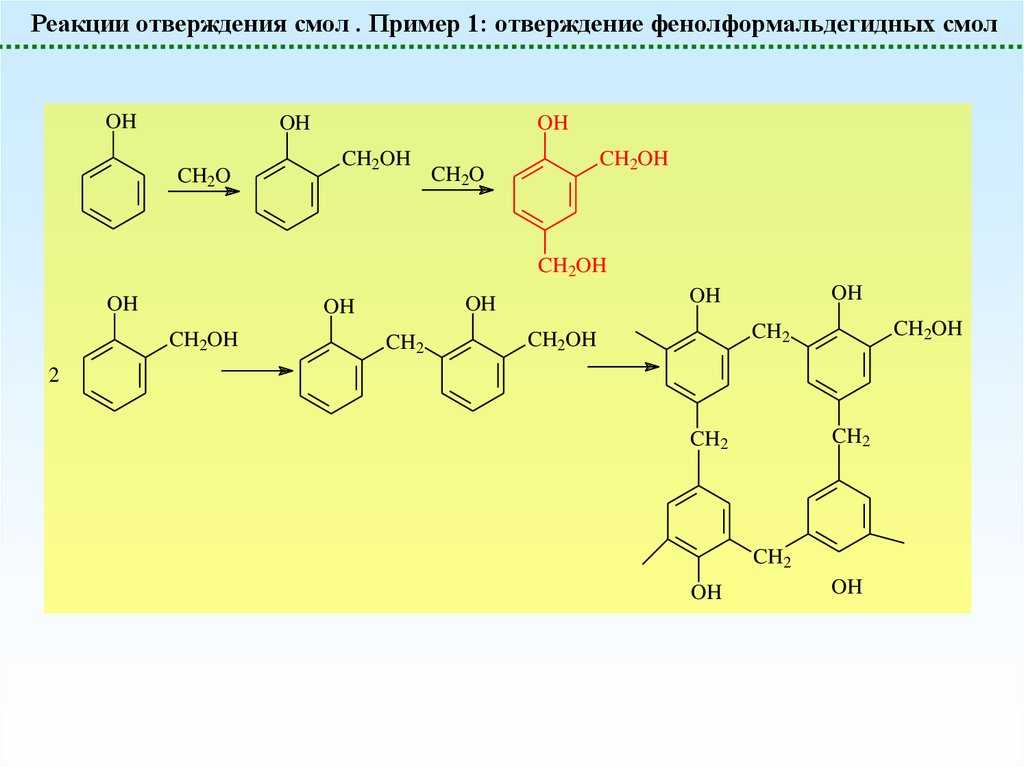
Реакции отверждения смол . Пример 1: отверждение фенолформальдегидных смолOH
OH
CH2O
OH
CH2OH
CH2OH
CH2O
CH2OH
OH
CH2OH
CH2
OH
OH
OH
OH
CH2OH
CH2
CH2OH
2
CH2
CH2
CH2
OH
OH
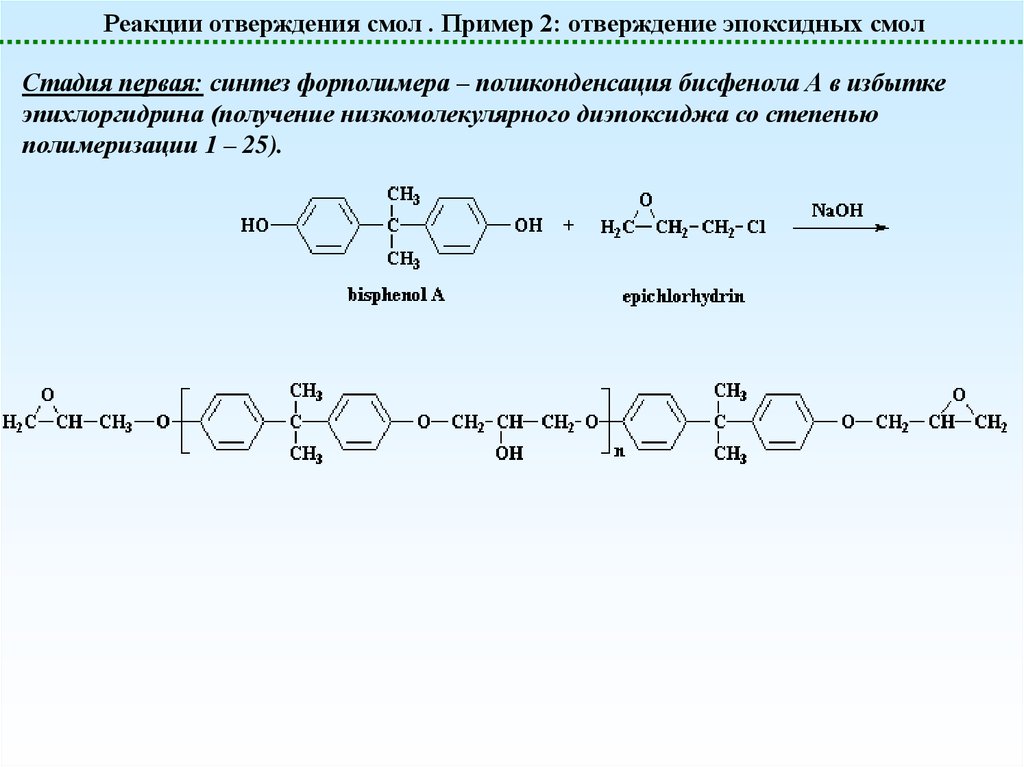
21.
Реакции отверждения смол . Пример 2: отверждение эпоксидных смолСтадия первая: синтез форполимера – поликонденсация бисфенола А в избытке
эпихлоргидрина (получение низкомолекулярного диэпоксиджа со степенью
полимеризации 1 – 25).
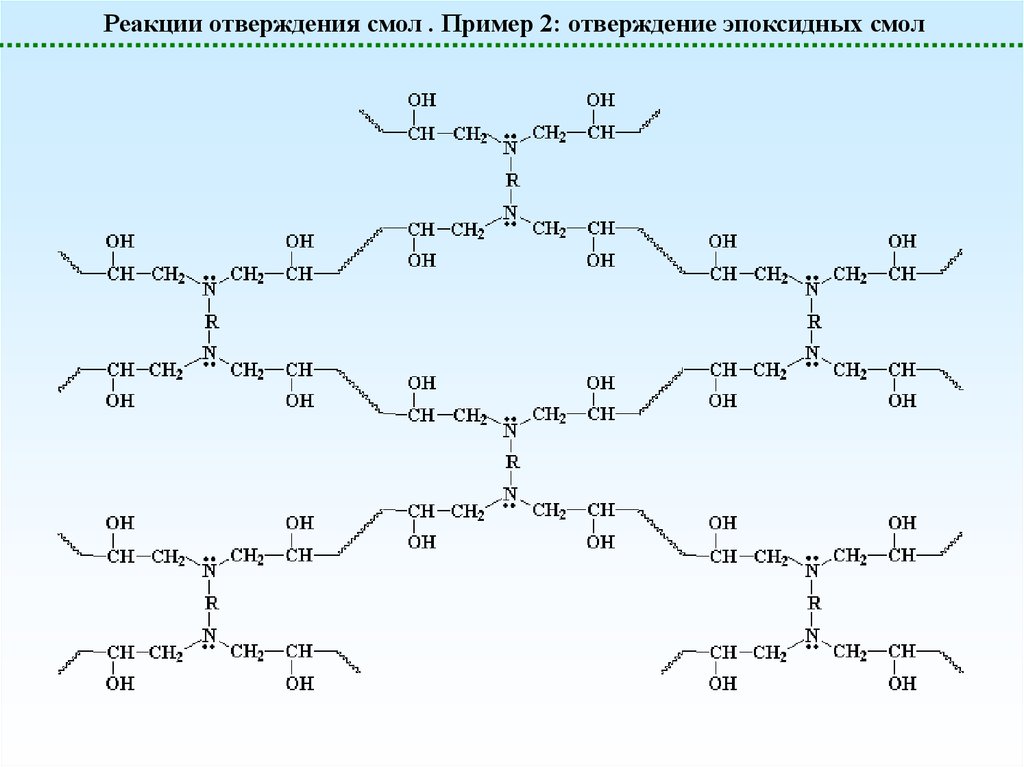
22.
Реакции отверждения смол . Пример 2: отверждение эпоксидных смолСтадия вторая: сшивание молекул форполимера диаминами.
23.
Реакции отверждения смол . Пример 2: отверждение эпоксидных смол24.
ДЕСТРУКЦИЯ (случайная)ХИМИЧЕСКАЯ (гетероцепных
полимеров)
+
NH
*CH
C
R
O
NH
CH2OH
H
R
O
H
O
H
H
H
C
n
H
_
(OH )
O
H
OH
H
глюкоза
CH2OH
CH2OH
H
O
H
OH
OH
H
(CH2)4
~O
H
+
H
H
~
+
H
OH
O
COOH
R
O
H
OH
*CH
NH2
CH2OH
O
H
OH
H или ОН
*CH
O
H
OH
H
H
H
C
O
O
(CH2)4
OH
+
~
OH
H
H
OH
OH
C
O
H
OH
O
H
OH
OH
O
CH2OH
H
OH
HOCH2CH2OH
HOCH2CH2O
C
O
C
O
~
24
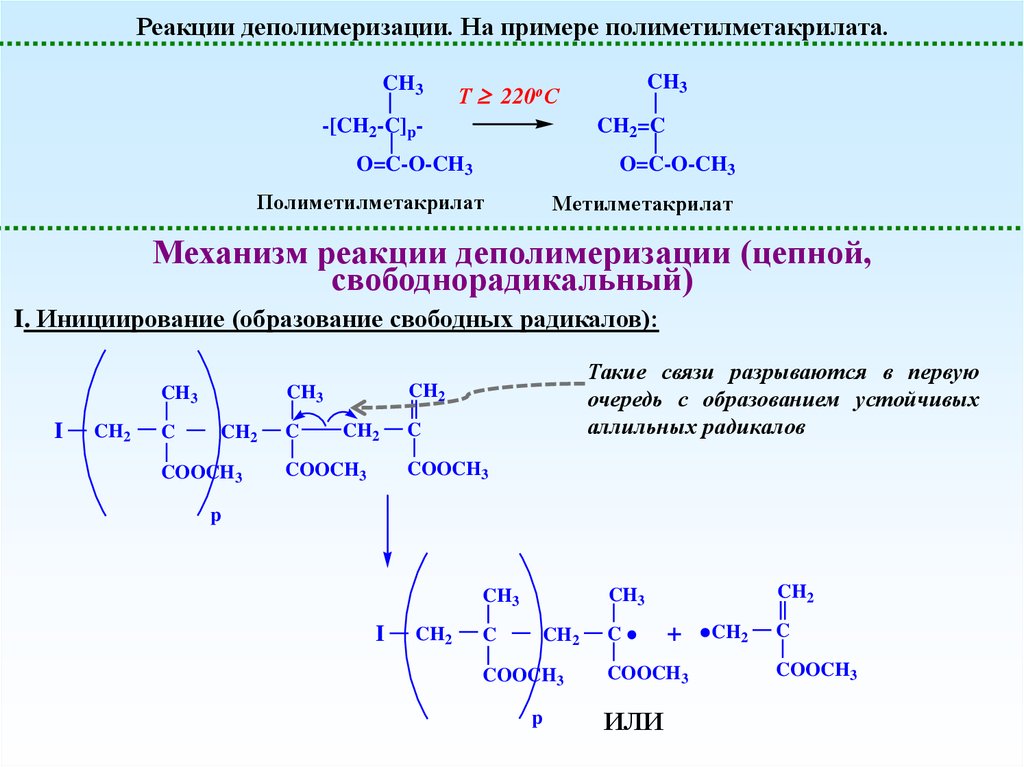
25.
Реакции деполимеризации. На примере полиметилметакрилата.CH3
CH3
Т 220оС
-[CH2-C]p-
CH2=C
O=C-O-CH3
O=C-O-CH3
Полиметилметакрилат
Метилметакрилат
Механизм реакции деполимеризации (цепной,
свободнорадикальный)
I. Инициирование (образование свободных радикалов):
CH3
CH3
I
CH2
C
CH2
COOCH3
C
Такие связи разрываются в первую
очередь с образованием устойчивых
аллильных радикалов
CH2
CH2
C
COOCH3
COOCH3
p
I
CH2
C
CH2
CH3
CH3
CH2
COOCH3
p
C
+
COOCH3
ИЛИ
CH2
C
COOCH3
26.
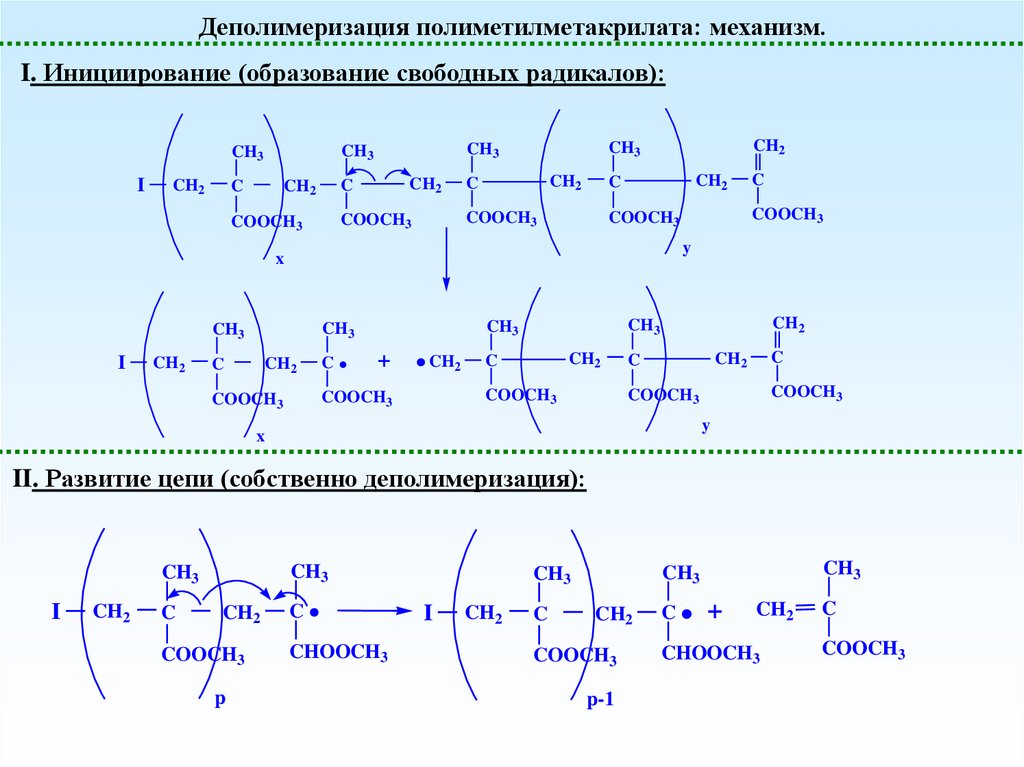
Деполимеризация полиметилметакрилата: механизм.I. Инициирование (образование свободных радикалов):
I
CH2
CH2
C
CH2
C
CH2
C
CH2
C
COOCH3
COOCH3
COOCH3
CH2
CH3
CH3
CH3
CH3
y
CH2
C
C
+
CH2
CH2
C
COOCH3
COOCH3
COOCH3
CH2
CH3
CH3
CH3
CH3
CH2
COOCH3
COOCH3
x
I
C
C
CH2
C
COOCH3
COOCH3
y
x
II. Развитие цепи (собственно деполимеризация):
CH3
CH3
I
CH2
C
CH2
COOCH3
p
C
CHOOCH3
I
CH2
C
CH3
CH3
CH3
CH2
COOCH3
p-1
C
+
CH2
CHOOCH3
C
COOCH3
27.
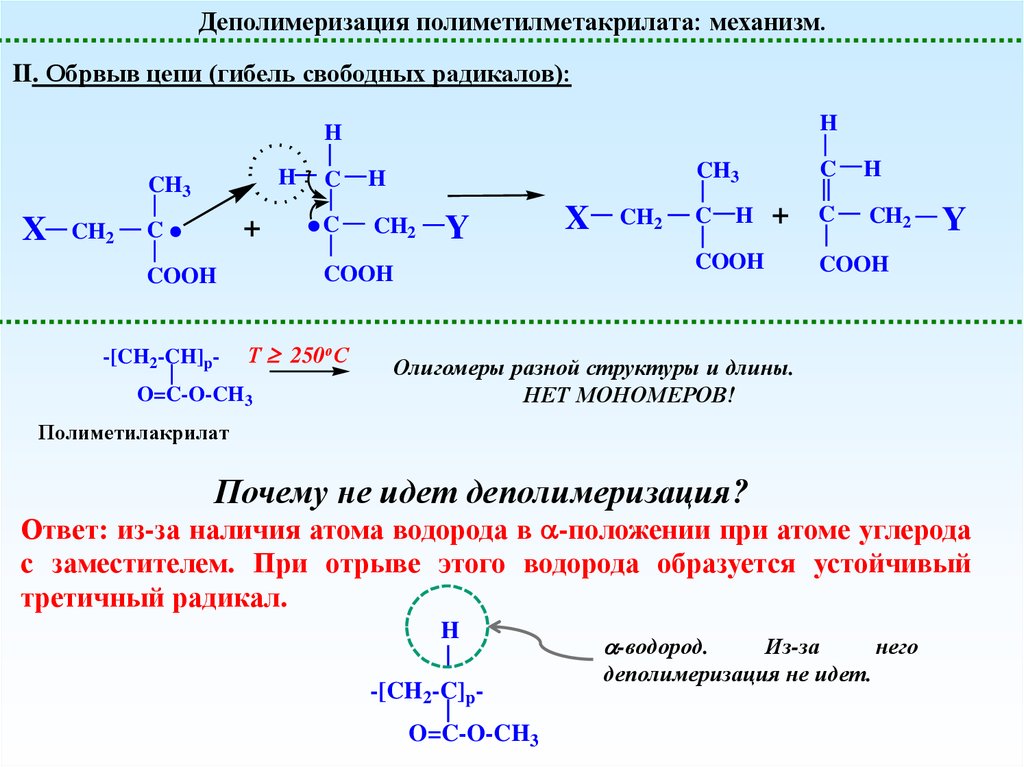
Деполимеризация полиметилметакрилата: механизм.II. Обрвыв цепи (гибель свободных радикалов):
H
H
H
CH3
X
CH2
+
C
H
C
CH2
Y
Т 250оС
O=C-O-CH3
X
CH2
C
H
+
COOH
COOH
COOH
-[CH2-CH]p-
CH3
C
C
H
C
CH2
Y
COOH
Олигомеры разной структуры и длины.
НЕТ МОНОМЕРОВ!
Полиметилакрилат
Почему не идет деполимеризация?
Ответ: из-за наличия атома водорода в -положении при атоме углерода
с заместителем. При отрыве этого водорода образуется устойчивый
третичный радикал.
H
-[CH2-C]pO=C-O-CH3
-водород.
Из-за
него
деполимеризация не идет.
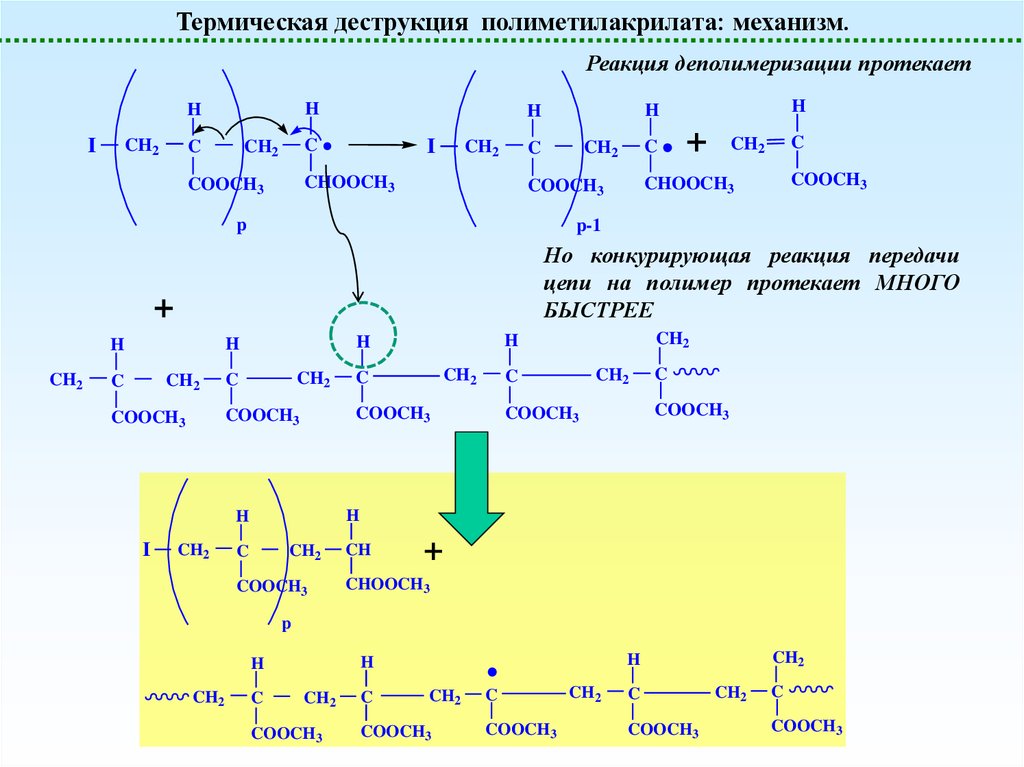
28.
Термическая деструкция полиметилакрилата: механизм.Реакция деполимеризации протекает
H
H
I
CH2
I
C
CH2
C
CH2
COOCH3
Но конкурирующая реакция передачи
цепи на полимер протекает МНОГО
БЫСТРЕЕ
CH2
CH2
C
CH2
C
C
COOCH3
COOCH3
H
H
CH2
CH2
C
COOCH3
COOCH3
COOCH3
CH2
H
H
H
H
I
C
CH2
p-1
+
C
+
CHOOCH3
COOCH3
p
CH2
C
CH2
C
CHOOCH3
COOCH3
H
H
H
CH2
C
COOCH3
CH
+
CHOOCH3
p
CH2
C
CH2
COOCH3
C
CH2
H
H
H
CH2
COOCH3
C
COOCH3
CH2
C
COOCH3
CH2
C
COOCH3
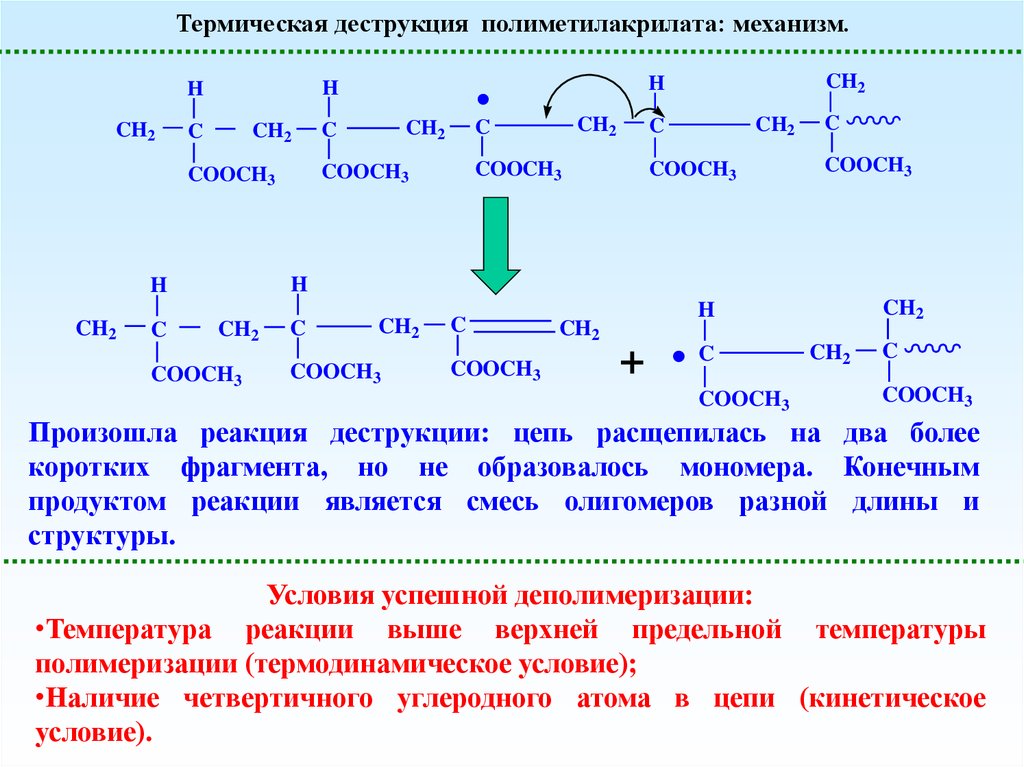
29.
Термическая деструкция полиметилакрилата: механизм.CH2
CH2
C
CH2
H
H
C
C
CH2
COOCH3
CH2
COOCH3
CH2
C
CH2
C
C
COOCH3
CH2
C
COOCH3
COOCH3
COOCH3
CH2
H
H
H
COOCH3
C
COOCH3
CH2
H
CH2
+
C
COOCH3
CH2
C
COOCH3
Произошла реакция деструкции: цепь расщепилась на два более
коротких фрагмента, но не образовалось мономера. Конечным
продуктом реакции является смесь олигомеров разной длины и
структуры.
Условия успешной деполимеризации:
•Температура реакции выше верхней предельной температуры
полимеризации (термодинамическое условие);
•Наличие четвертичного углеродного атома в цепи (кинетическое
условие).
30.
Термолиз различных полимеров и выход мономераНазвание полимера
Выход продуктов термического
разложения
CH3
Полиметилметакрилат
-[CH2-C]p-
Мономер > 90%
O=C-O-CH3
Полиметилакрилат
O=C-O-CH3
CH3
-[CH2-C]p-
Мономер ~ 1%, олигомеры
-[CH2-CH]p-
Поли- -метилстирол
Мономер > 90 %
-[CH2-CH]p-
Полистирол
Мономер ~ 45%
CH3
-[CH2-C]pC
Полиметакрилонитрил
Мономер ~ 85%
N
Полиакрилонитрил
-[CH2-CH]pC
Политетрафторэтилен
Полиэтилен
Мономер ~ 1%, олигомеры
N
-[CF2-CF2]p-
-[CH2-CH2]p-
Мономер ~ 90%
Мономер < 1%, олигомеры
31.
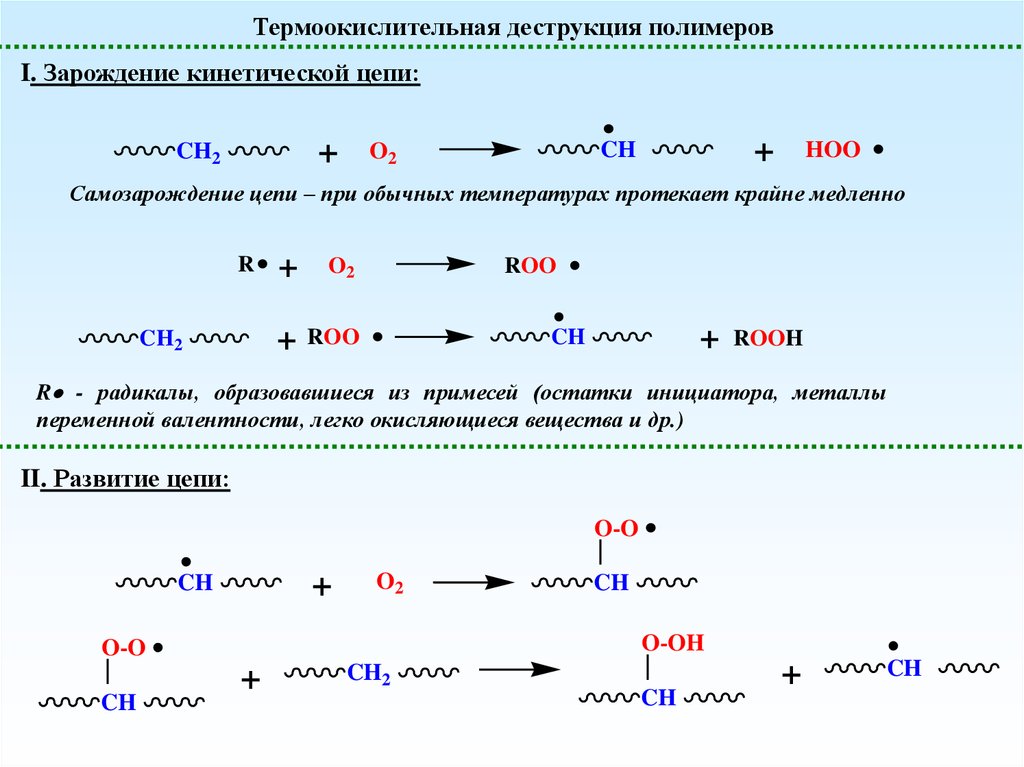
Термоокислительная деструкция полимеровI. Зарождение кинетической цепи:
+
CH2
+
CH
O2
HOO
Самозарождение цепи – при обычных температурах протекает крайне медленно
R
CH2
+
O2
+
ROO
ROO
+
CH
ROOH
R - радикалы, образовавшиеся из примесей (остатки инициатора, металлы
переменной валентности, легко окисляющиеся вещества и др.)
II. Развитие цепи:
O-O
+
CH
O2
O-OH
O-O
CH
CH
+
CH2
CH
+
CH
32.
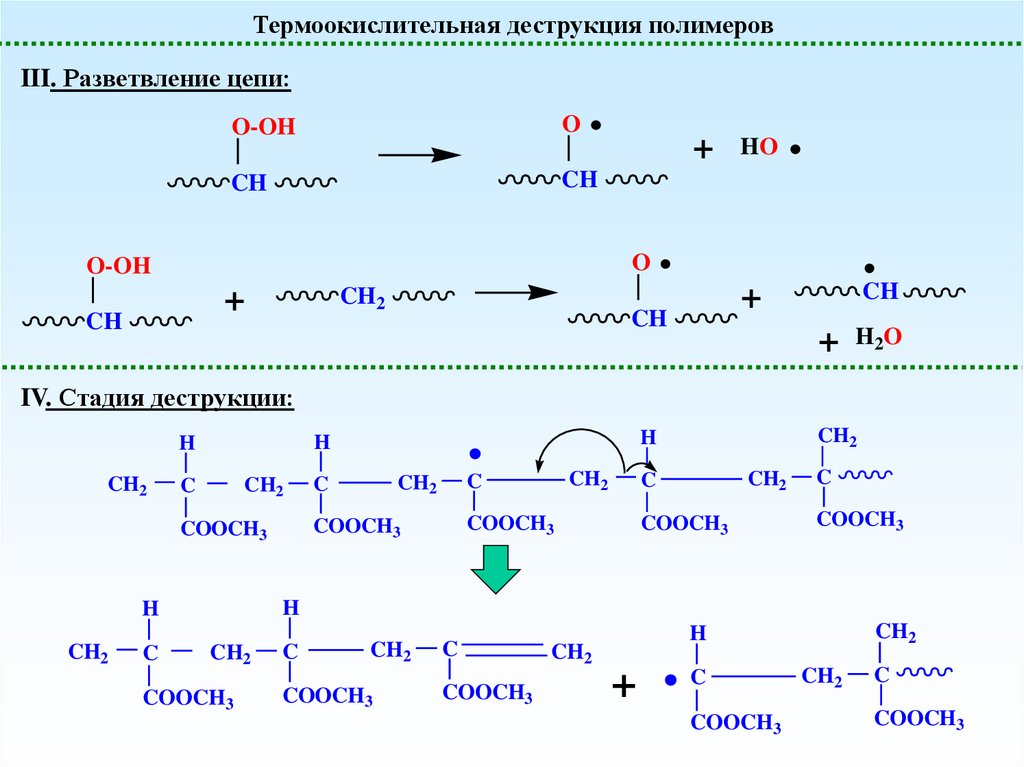
Термоокислительная деструкция полимеровIII. Разветвление цепи:
O-OH
O
CH
CH
+
HO
O
O-OH
+
CH
CH2
CH
+
CH
+
H2O
IV. Стадия деструкции:
CH2
CH2
C
C
CH2
C
COOCH3
COOCH3
C
COOCH3
H
H
CH2
CH2
C
CH2
C
COOCH3
COOCH3
CH2
H
H
H
CH2
COOCH3
C
CH2
COOCH3
C
COOCH3
CH2
H
CH2
+
C
COOCH3
CH2
C
COOCH3
33.
Термоокислительная деструкция полимеровCH2
CH2
C
C
CH2
CH4
COOCH3
CH2
COOCH3
C
CH2
C
O
CH2
COOCH3
C
COOCH3
CH2
+
C
COOCH3
C
COOCH3
COOCH3
H
H
CH2
CH2
C
COOCH3
COOCH3
CH2
O
H
H
CH2
CH2
C
COOCH3
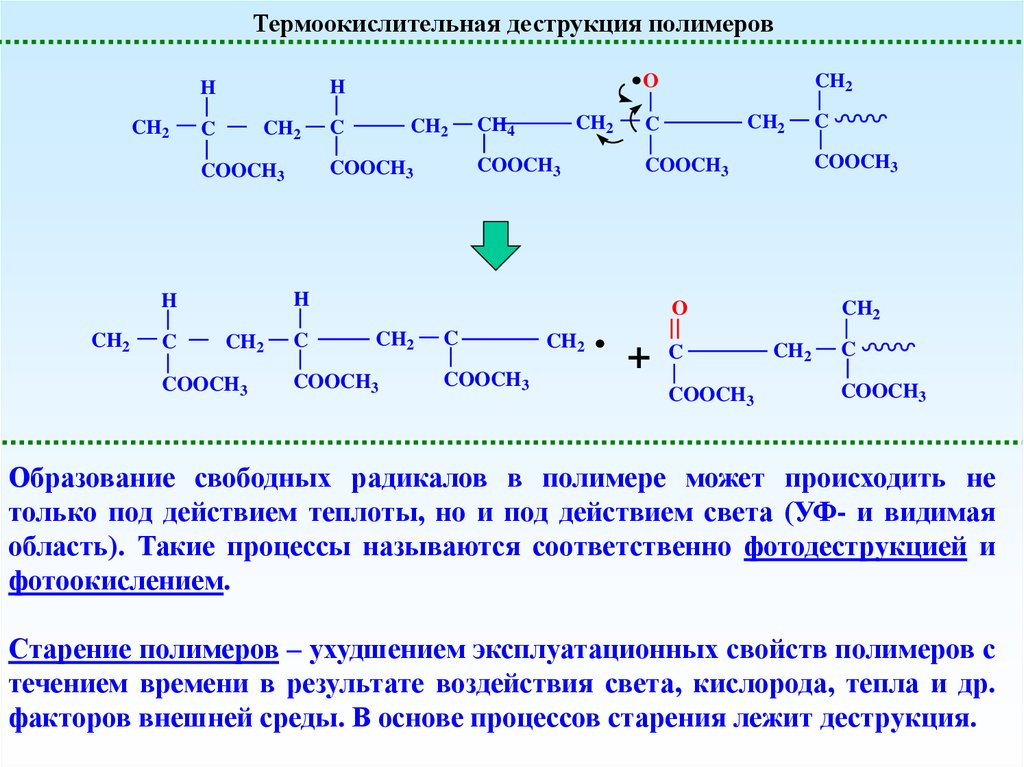
Образование свободных радикалов в полимере может происходить не
только под действием теплоты, но и под действием света (УФ- и видимая
область). Такие процессы называются соответственно фотодеструкцией и
фотоокислением.
Старение полимеров – ухудшением эксплуатационных свойств полимеров с
течением времени в результате воздействия света, кислорода, тепла и др.
факторов внешней среды. В основе процессов старения лежит деструкция.
34.
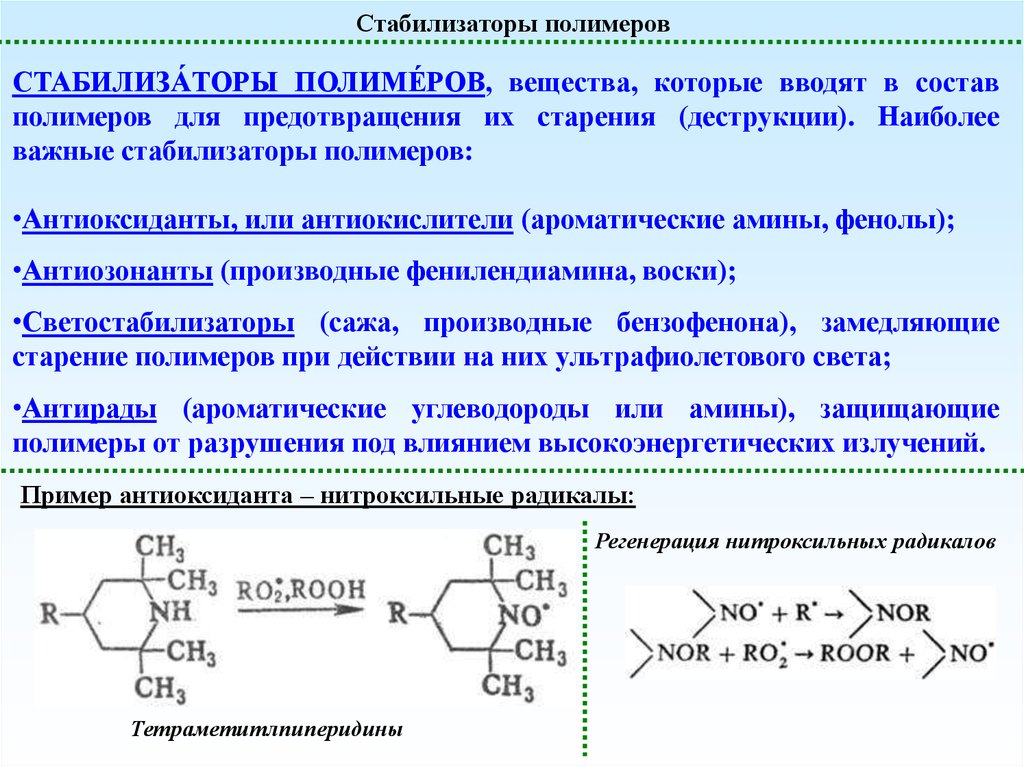
Стабилизаторы полимеровСТАБИЛИЗА́ТОРЫ ПОЛИМЕ́ РОВ, вещества, которые вводят в состав
полимеров для предотвращения их старения (деструкции). Наиболее
важные стабилизаторы полимеров:
•Антиоксиданты, или антиокислители (ароматические амины, фенолы);
•Антиозонанты (производные фенилендиамина, воски);
•Светостабилизаторы (сажа, производные бензофенона), замедляющие
старение полимеров при действии на них ультрафиолетового света;
•Антирады (ароматические углеводороды или амины), защищающие
полимеры от разрушения под влиянием высокоэнергетических излучений.
Пример антиоксиданта – нитроксильные радикалы:
Регенерация нитроксильных радикалов
Тетраметитлпиперидины






 Химия
Химия








