Похожие презентации:
Стратегия перевода технологий в Россию. Биофармацевтическая промышленность
1. Стратегия перевода технологий в Россию: экономическая целесообразность, масштабированиe и соответствие cGMP
Клюшниченко Вадим ЕвгеньевичProcess Development,
Altus Biologics Inc.
Cambridge, MA,
USA
2. Предпосылки для перевода технологий за пределы США
Устаревшие патенты и необходимость снижения цен
Высокие цены на сырье и рабочую силу
Высокая конкуренция среди производителей дженериков, особенно в
третьих странах
Почему в Россию?
Новый рынок с неизбалованным покупателем и отсутствием
отечественного производсва
Быстрое развитие экономической и правовой системы
Стремление России войти в ВТО и другие международные
организации, требующие сертификации производства
Хорошее теоретическое образование и концентрация технических
специалистов в крупных городах
Биофармацевтическая промышленность является одной из наиболее
прибыльных и быстрорастущих отраслей мировой экономики
3. Типы диабета
• Тип I возникает в детстве в связи сгенетическими изменениями
(~10% больных)
• Тип II развивается в зрелом и
преклонном возрасте (90% больных)
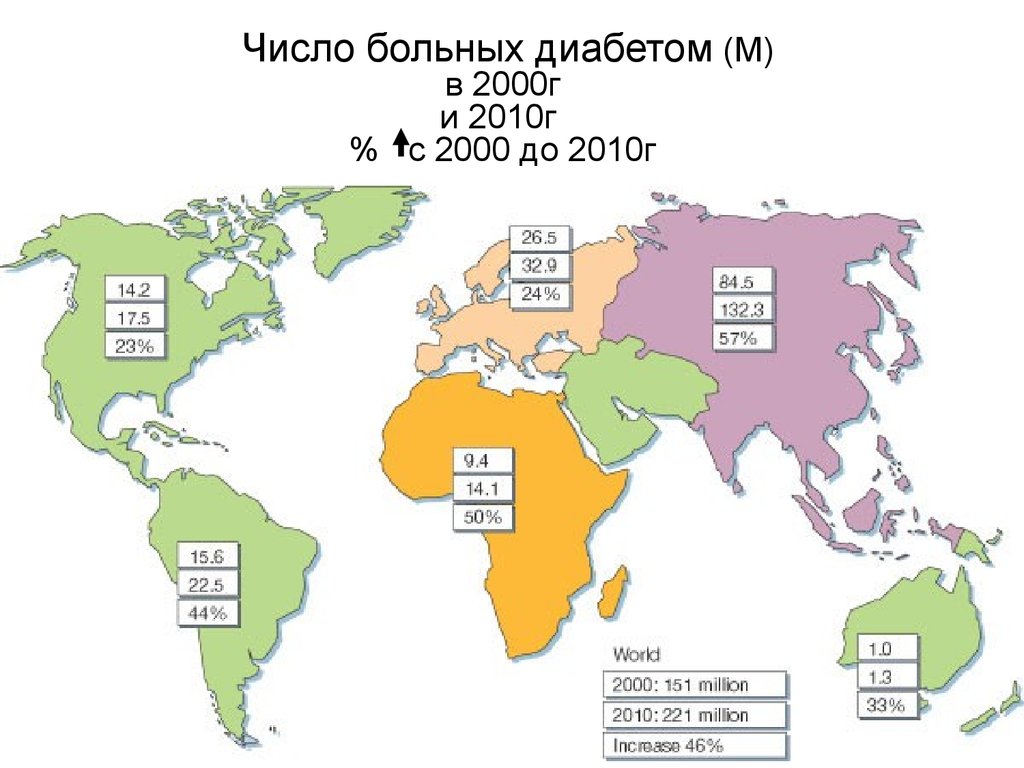
4. Число больных диабетом (М) в 2000г и 2010г % с 2000 до 2010г
5. Статистика больных диабетом в России
Тип I (рост 0.2% в год)
– 270,261 зарегистрированных больных по оценкам Минздрава на 1
января 2002
– 1,125,000 по соотношению больных в США к общему
населению
• Тип II (рост 4.2 % в год)
– 1,912,147 зарегистрированных больных по оценкам Минздрава на
1 января 2002
– 4-6 миллионов по предварительным оценкам:
• ~ 50% от соотношения больных в США к общему населению
• 3-5% населения России страдают от диабета неопубликованные
данные
Дополнитеньные пациенты
– Постоперационные
– Пожилого возраста
– Принимающие инсулин в комбинации с другими лекарствами
Итого - 2.5 миллиона пациентов, принимающих инсулин
6. Потребность в инсулине в России и странах СНГ
35E/день
28.6 дней/ампулу (1000E/ ампулу or 40 mg инсулина ампулу)
12.8 ампулгод
21 U$ / ампулу (цена в аптеках Москвы)
268 $/год на покупку инсулина/пациента
2.5 M инсулин-зависимых пациентов в России и 3.5 M в СНГ
671 $M/г инсулиновый рынок в России и 940 $M/г в СНГ
1300 kg/г потребность в инсулине в России и 1800 kg/г в СНГ
7. Производство и импортные поставки инсулина в России
• Фереин• Национальные биотехнологии
• Другие российские проекты
• Еli Lilly, Novo Nordisk, Aventis
• Восточно-Европейские, Латино-Американские,
Азиатские страны
• Животный инсулин
• Соотношение цены, качества и производственных
ресурсов ?
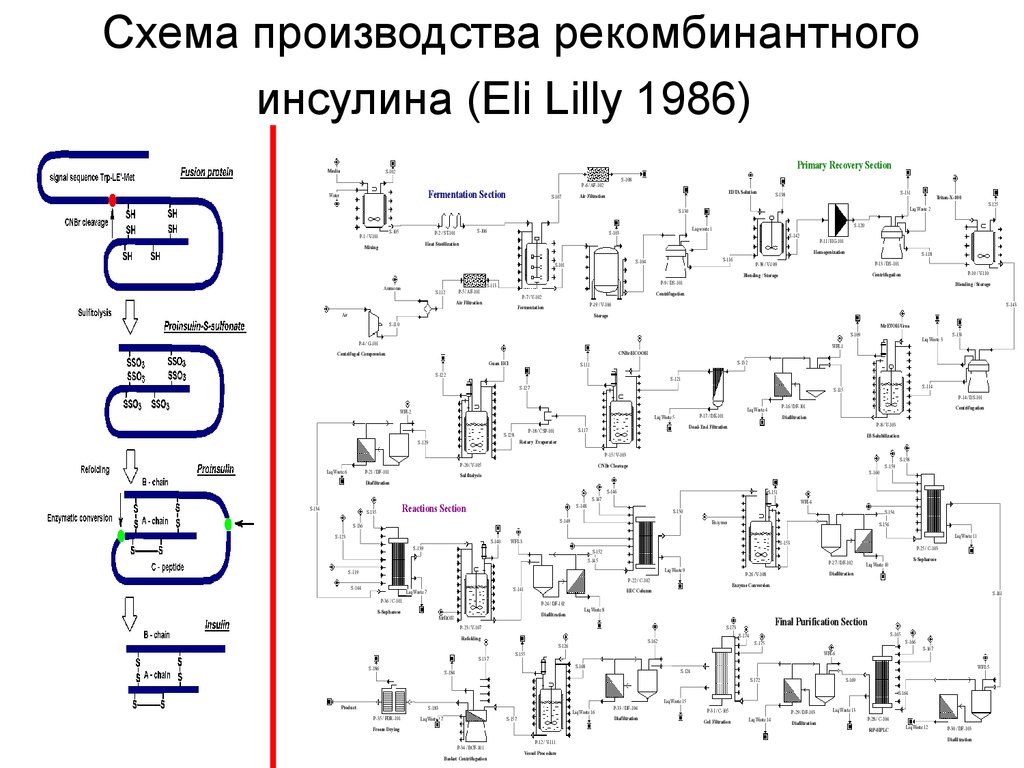
8. Схема производства рекомбинантного инсулина (Eli Lilly 1986)
MediaPrimary Recovery Section
S-102
Fermentation Section
Water
S-108
P-6 / AF-102
S-107
EDTA Solution
Air Filtration
S-131
S-138
S-105
P-1 / V-101
S-106
P-2 / ST-101
Liq waste 1
S-103
S-142
P-11 / HG-101
Homogenization
S-116
S-104
S-101
S-118
P-13 / DS-101
P-38 / V-109
S-112
P-5 / AF-101
P-10 / V-110
Centrifugation
Blending / Storage
Ammonia
P-9 / DS-101
S-113
Blending / Storage
Centrifugation
P-7 / V-102
Air Filtration
S-125
S-120
Heat Sterilization
Mixing
Triton-X-100
Liq Waste 2
S-130
S-143
P-19 / V-106
Fermentation
Air
Storage
S-110
MrETOH/Urea
S-109
P-4 / G-101
Liq Waste 3
S-133
WFI-1
CNBr/HCOOH
Centrifugal Compression
Guan HCl
S-132
S-111
S-122
S-121
S-127
S-114
S-115
P-14 / DS-101
P-16 / DF-101
Liq Waste 4
WFI-2
P-17 / DE-101
Liq Waste 5
P-8 / V-103
Dead-End Filtration
S-117
P-18 / CSP-101
S-128
Centrifugation
Diafiltration
IB Solubilization
Rotary Evaporator
S-129
P-15 / V-103
P-20 / V-105
Liq Waste 6
P-21 / DF-101
S-158
CNBr Cleavage
S-160
Sulfitolysis
S-159
Diafiltration
S-146
S-134
Reactions Section
S-135
S-151
S-147
WFI-4
S-148
S-150
S-149
S-136
S-123
S-140
S-154
Enzymes
S-156
Liq Waste 11
WFI-3
S-153
S-139
P-25 / C-103
S-152
S-145
P-27 / DF-102
Liq Waste 9
S-119
P-22 / C-102
S-144
S-141
Liq Waste 7
P-24 / DF-102
S-Sepharose
Enzyme Conversion
HIC Column
P-36 / C-101
Diafiltration
MrEtOH
S-161
Liq Waste 8
P-23 / V-107
S-165
S-174
S-162
S-126
S-186
Final Purification Section
S-173
Refolding
S-137
S-Sepharose
Liq Waste 10
Diafiltration
P-26 / V-108
S-166
S-175
S-167
WFI-6
S-155
S-168
S-184
WFI-5
S-124
S-169
S-172
S-164
Liq Waste 15
Product
S-183
P-35 / FDR-101
Liq Waste 16
Liq Waste 17
S-157
Freeze Drying
P-33 / DF-104
P-31 / C-105
Diafiltration
Gel Filtration
P-29 / DF-103
Liq Waste 14
Diafiltration
Liq Waste 13
P-28 / C-104
RP-HPLC
P-34 / BCF-101
Basket Centrifugation
P-12 / V-111
Vessel Procedure
Liq Waste 12
P-30 / DF-103
Diafiltration
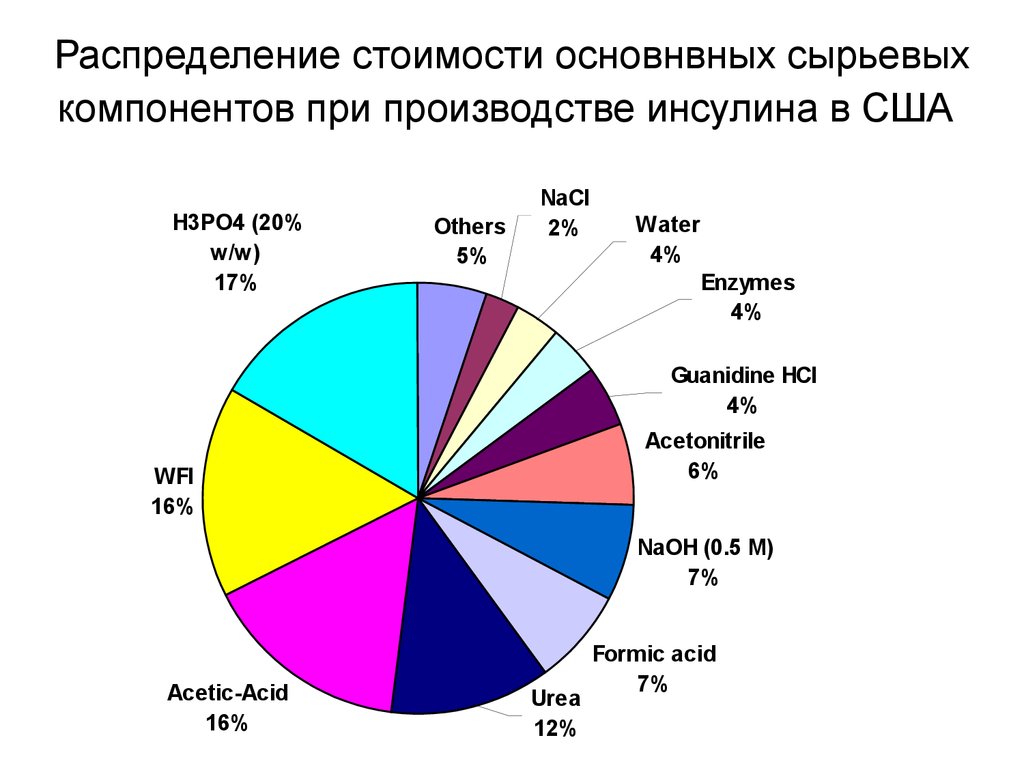
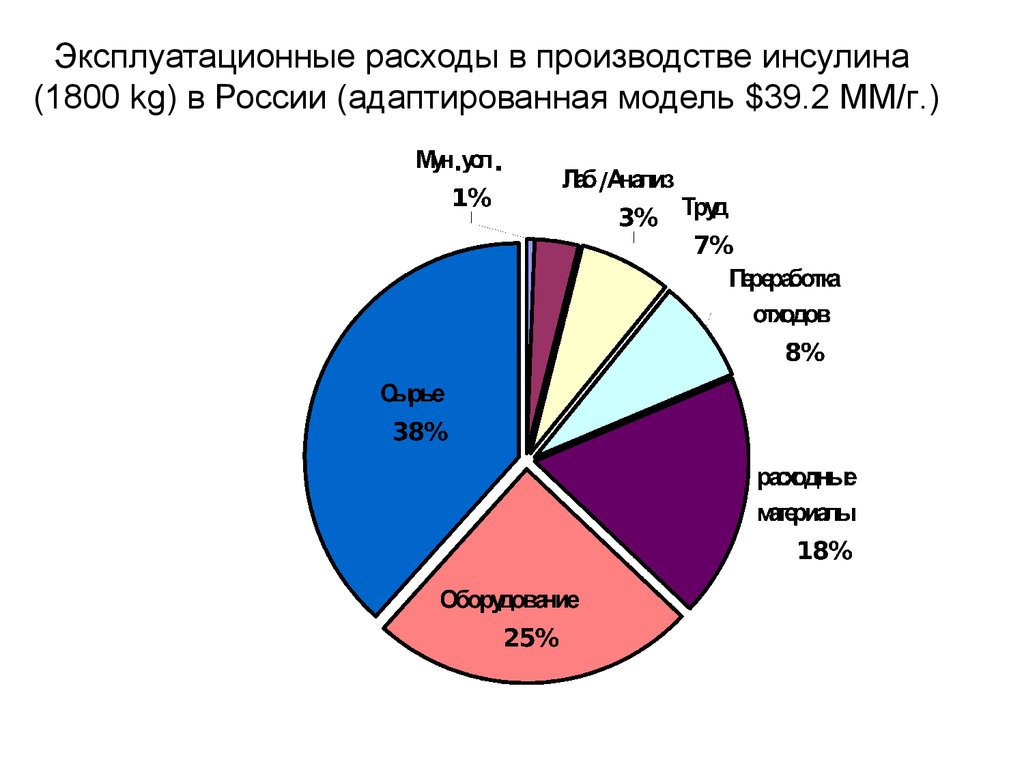
9. Распределение стоимости основнвных сырьевых компонентов при производстве инсулина в США
H3PO4 (20%w/w)
17%
Others
5%
NaCl
2%
Water
4%
Enzymes
4%
Guanidine HCl
4%
Acetonitrile
6%
WFI
16%
NaOH (0.5 M)
7%
Acetic-Acid
16%
Urea
12%
Formic acid
7%
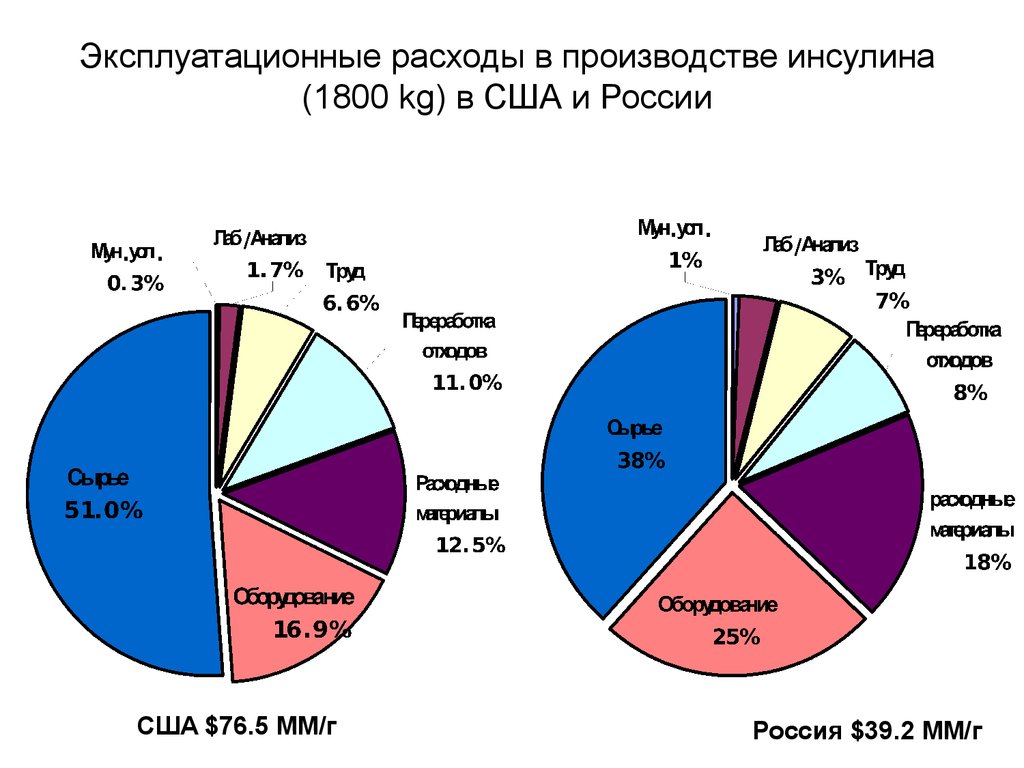
10. Эксплуатационные расходы в производстве инсулина (1800 kg) в США и России
США $76.5 МM/гРоссия $39.2 MМ/г
11. Эксплуатационные расходы в производстве инсулина (1800 kg) в России (адаптированная модель $39.2 MМ/г.)
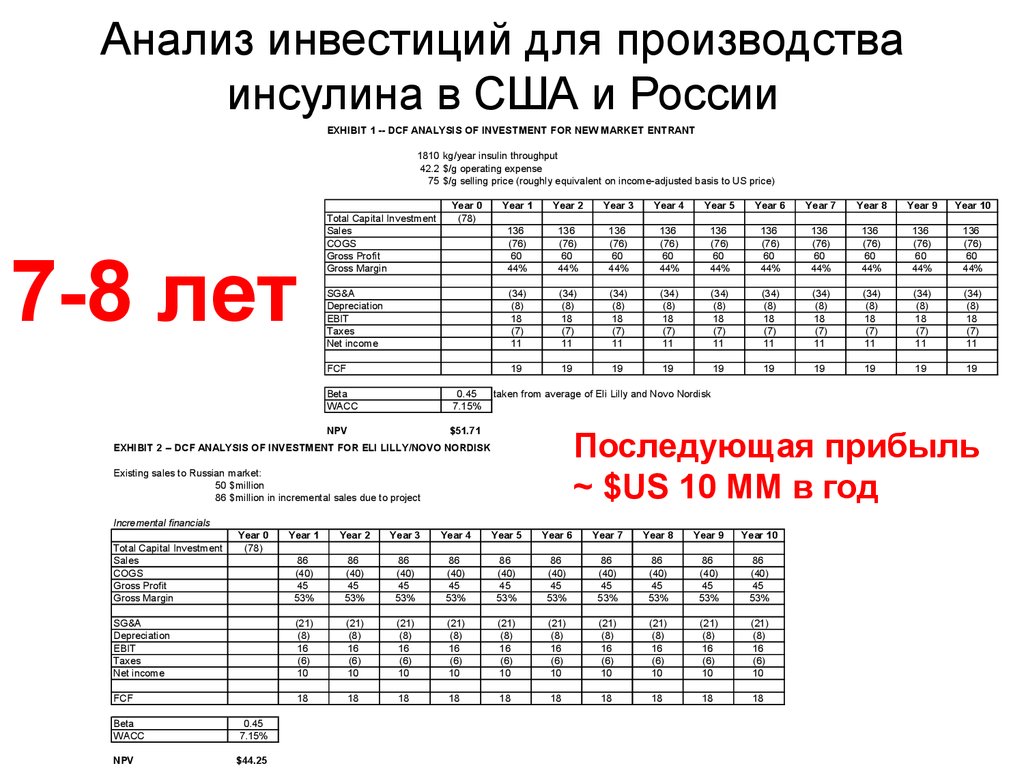
12. Анализ инвестиций для производства инсулина в США и России
EXHIBIT 1 -- DCF ANALYSIS OF INVESTMENT FOR NEW MARKET ENTRANT1810 kg/year insulin throughput
42.2 $/g operating expense
75 $/g selling price (roughly equivalent on income-adjusted basis to US price)
7-8 лет
Year 1
Year 2
Year 3
Year 4
Year 5
Year 6
Year 7
Year 8
Year 9
Year 10
136
(76)
60
44%
136
(76)
60
44%
136
(76)
60
44%
136
(76)
60
44%
136
(76)
60
44%
136
(76)
60
44%
136
(76)
60
44%
136
(76)
60
44%
136
(76)
60
44%
136
(76)
60
44%
SG&A
Depreciation
EBIT
Taxes
Net income
(34)
(8)
18
(7)
11
(34)
(8)
18
(7)
11
(34)
(8)
18
(7)
11
(34)
(8)
18
(7)
11
(34)
(8)
18
(7)
11
(34)
(8)
18
(7)
11
(34)
(8)
18
(7)
11
(34)
(8)
18
(7)
11
(34)
(8)
18
(7)
11
(34)
(8)
18
(7)
11
FCF
19
19
19
19
19
19
19
19
19
19
Total Capital Investment
Sales
COGS
Gross Profit
Gross Margin
Year 0
(78)
Beta
WACC
0.45
7.15%
NPV
$51.71
taken from average of Eli Lilly and Novo Nordisk
Последующая прибыль
~ $US 10 ММ в год
EXHIBIT 2 -- DCF ANALYSIS OF INVESTMENT FOR ELI LILLY/NOVO NORDISK
Existing sales to Russian market:
50 $million
86 $million in incremental sales due to project
Incremental financials
Year 1
Year 2
Year 3
Year 4
Year 5
Year 6
Year 7
Year 8
Year 9
Year 10
86
(40)
45
53%
86
(40)
45
53%
86
(40)
45
53%
86
(40)
45
53%
86
(40)
45
53%
86
(40)
45
53%
86
(40)
45
53%
86
(40)
45
53%
86
(40)
45
53%
86
(40)
45
53%
SG&A
Depreciation
EBIT
Taxes
Net income
(21)
(8)
16
(6)
10
(21)
(8)
16
(6)
10
(21)
(8)
16
(6)
10
(21)
(8)
16
(6)
10
(21)
(8)
16
(6)
10
(21)
(8)
16
(6)
10
(21)
(8)
16
(6)
10
(21)
(8)
16
(6)
10
(21)
(8)
16
(6)
10
(21)
(8)
16
(6)
10
FCF
18
18
18
18
18
18
18
18
18
18
Total Capital Investment
Sales
COGS
Gross Profit
Gross Margin
Year 0
(78)
Beta
WACC
0.45
7.15%
NPV
$44.25
13. Ключевые моменты при разработке и передаче GMP технологий
Биохимия процесса (лаб. масштаб)
Аналитика
Дизайн экспериментов (DOE)
Масштабирование
Характеризация процессов
Валидация процессов
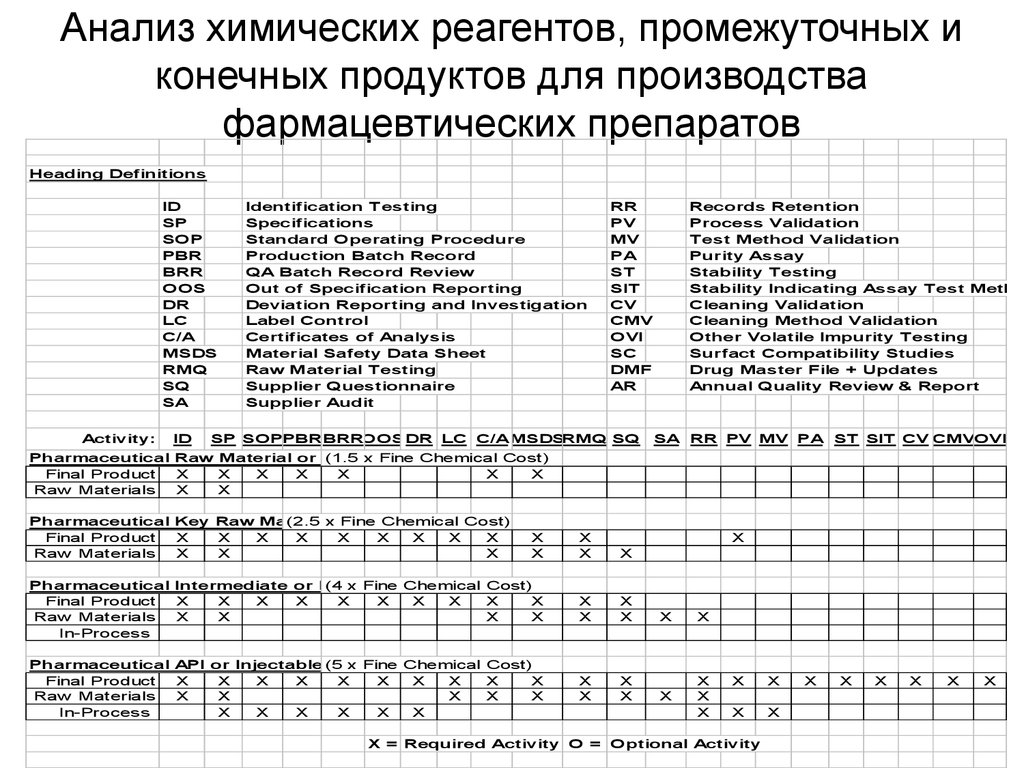
14. Анализ химических реагентов, промежуточных и конечных продуктов для производства фармацевтических препаратов
Heading DefinitionsID
SP
SOP
PBR
BRR
OOS
DR
LC
C/A
MSDS
RMQ
SQ
SA
Activity:
ID
Identification Testing
Specifications
Standard Operating Procedure
Production Batch Record
QA Batch Record Review
Out of Specification Reporting
Deviation Reporting and Investigation
Label Control
Certificates of Analysis
Material Safety Data Sheet
Raw Material Testing
Supplier Questionnaire
Supplier Audit
RR
PV
MV
PA
ST
SIT
CV
CMV
OVI
SC
DMF
AR
SP SOPPBRBRROOSDR LC C/AMSDSRMQ SQ
Records Retention
Process Validation
Test Method Validation
Purity Assay
Stability Testing
Stability Indicating Assay Test Metho
Cleaning Validation
Cleaning Method Validation
Other Volatile Impurity Testing
Surfact Compatibility Studies
Drug Master File + Updates
Annual Quality Review & Report
SA RR PV MV PA ST SIT CV CMVOVI
Pharmaceutical Raw Material or Food
(1.5 x cGMP
Fine Chemical Cost)
Final Product
X
X
X
X
X
X
X
Raw Materials
X
X
Pharmaceutical Key Raw Material
(2.5 x Fine Chemical Cost)
Final Product
X
X
X
X
X
X
X
X
X
Raw Materials
X
X
X
X
X
X
X
X
X
Pharmaceutical Intermediate or Excipient
(4 x Fine Chemical Cost)
Final Product
X
X
X
X
X
X
X
X
X
X
Raw Materials
X
X
X
X
In-Process
X
X
X
X
X
X
Pharmaceutical API or Injectable (5
Ingredient
x Fine Chemical Cost)
Final Product
X
X
X
X
X
X
X
X
X
X
Raw Materials
X
X
X
X
X
In-Process
X
X
X
X
X
X
X
X
X
X
X
X
X
X
X
X
X
X
X = Required Activity O = Optional Activity
X
X
X
X
X
X
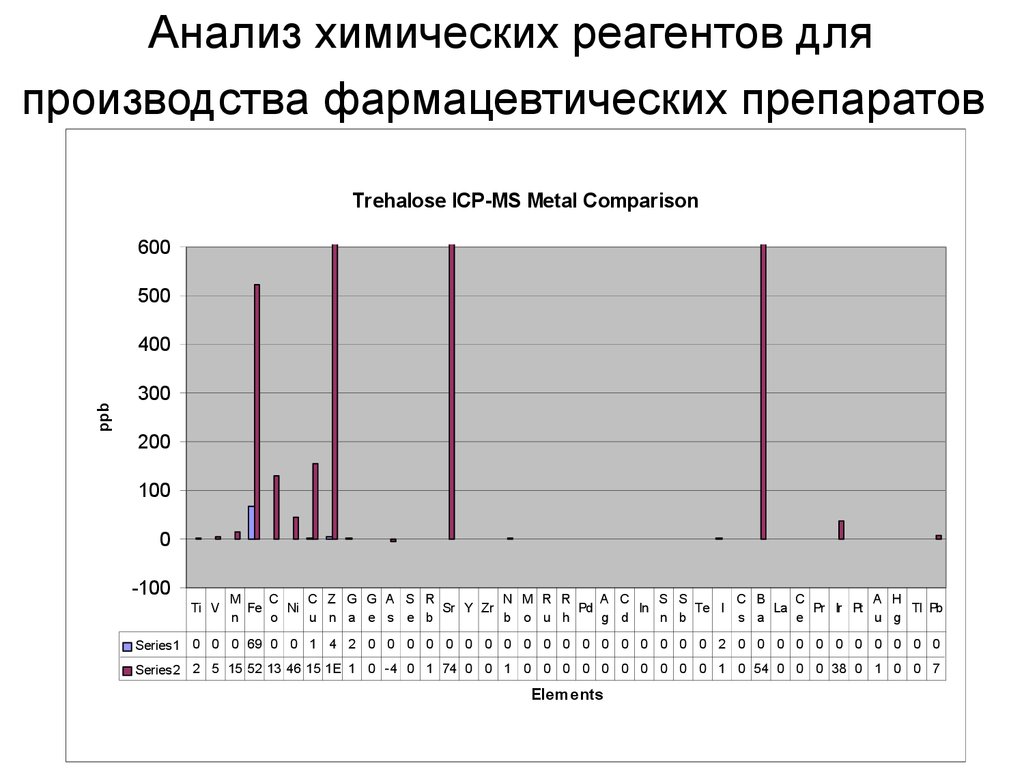
15. Анализ химических реагентов для производства фармацевтических препаратов
Trehalose ICP-MS Metal Comparison600
500
ppb
400
300
200
100
0
-100
Ti V
M
C
C Z G G A S R
N M R R
A C
S S
C B
C
A H
Fe
Ni
Sr Y Zr
Pd
In
Te I
La
Pr Ir Pt
Tl Pb
n
o
u n a e s e b
b o u h
g d
n b
s a
e
u g
Series1 0 0 0 69 0 0 1 4 2 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 2 0 0 0 0 0 0 0 0 0 0 0
Series2 2 5 15 52 13 46 15 1E 1 0 -4 0 1 74 0 0 1 0 0 0 0 0 0 0 0 0 0 1 0 54 0 0 0 38 0 1 0 0 7
Elements
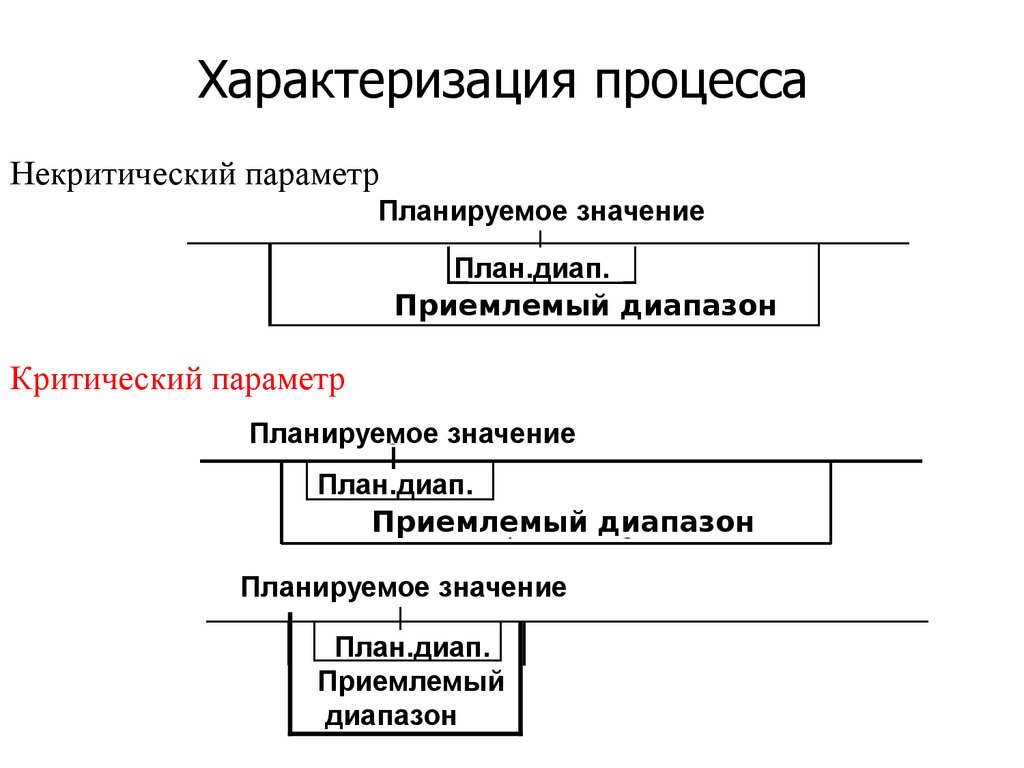
16.
Характеризация процессаНекритический параметр
Планируемое значение
План.диап.
Приемлемый диапазон
Критический параметр
Планируемое значение
План.диап.
Приемлемый диапазон
Планируемое значение
План.диап.
Приемлемый
диапазон
17.
Некритические параметры процессаDr.Greg Blank, Genentech
18.
Критические параметры процессаDr.Greg Blank, Genentech
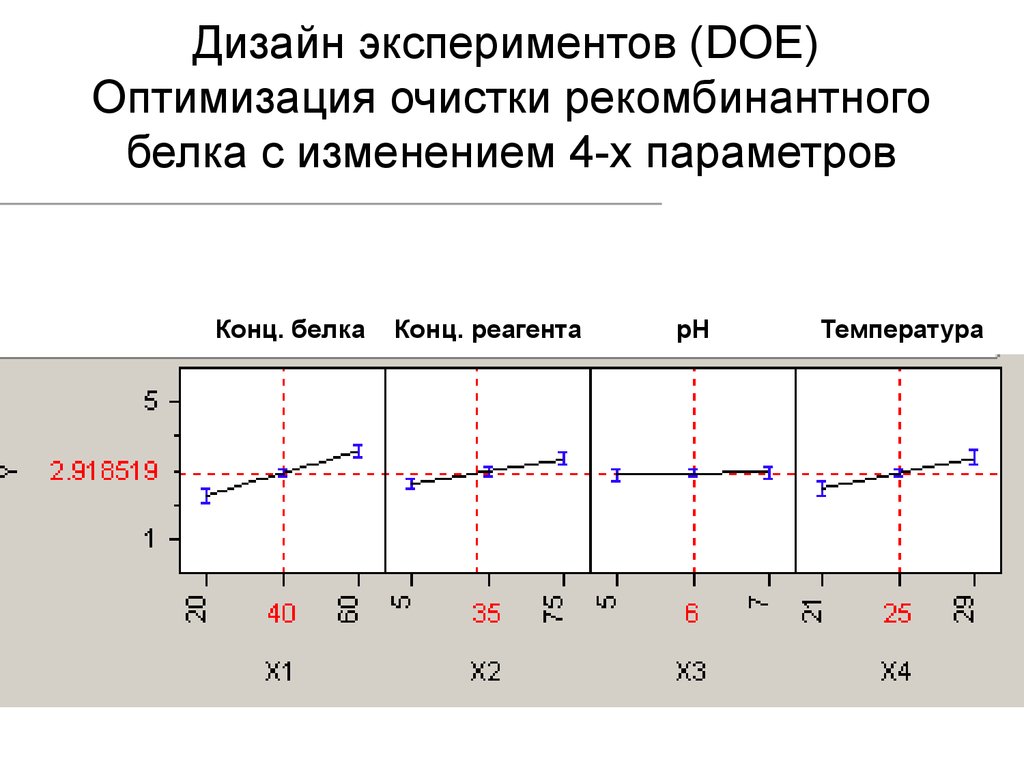
19. Дизайн экспериментов (DOE) Оптимизация очистки рекомбинантного белка с изменением 4-х параметров
Конц. белкаКонц. реагента
рН
Температура
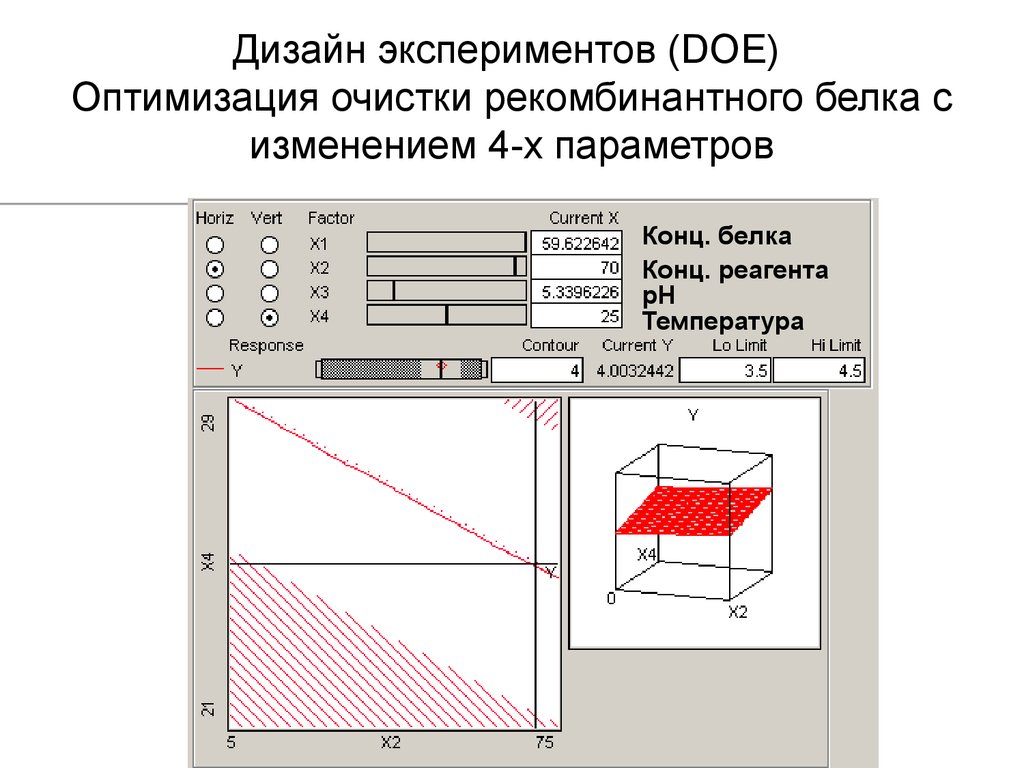
20. Дизайн экспериментов (DOE) Оптимизация очистки рекомбинантного белка с изменением 4-х параметров
Конц. белкаКонц. реагента
рН
Температура
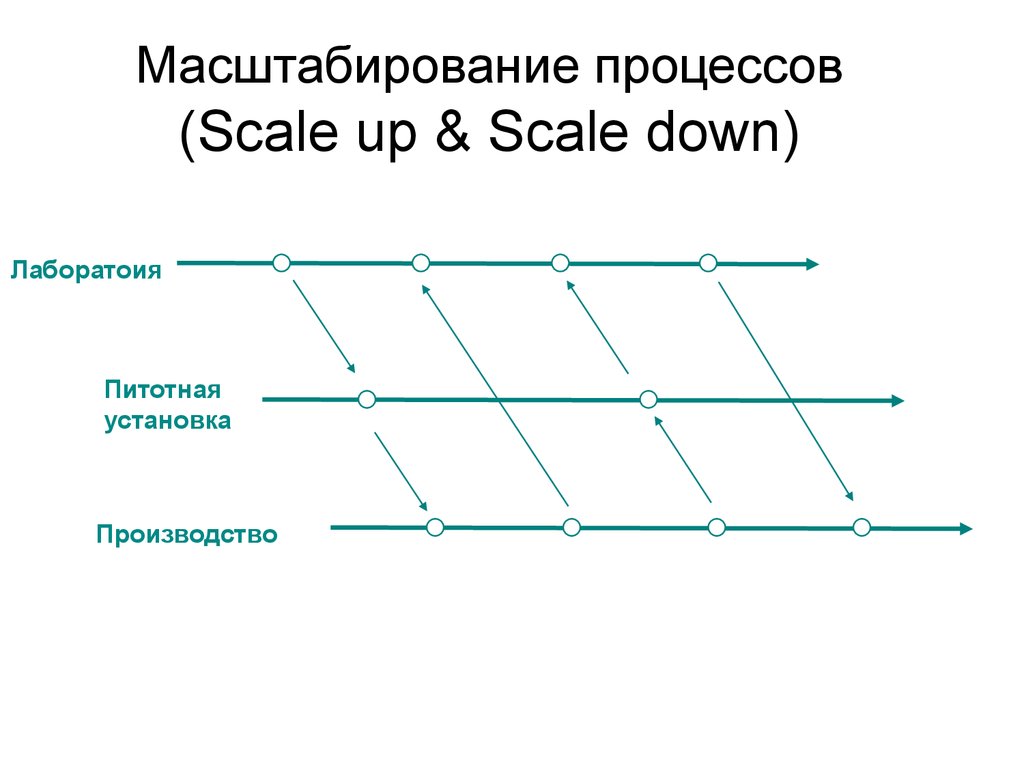
21. Mасштабированиe процессов (Scale up & Scale down)
Mасштабированиe процессов(Scale up & Scale down)
Лаборатоия
Питотная
установка
Производство
22.
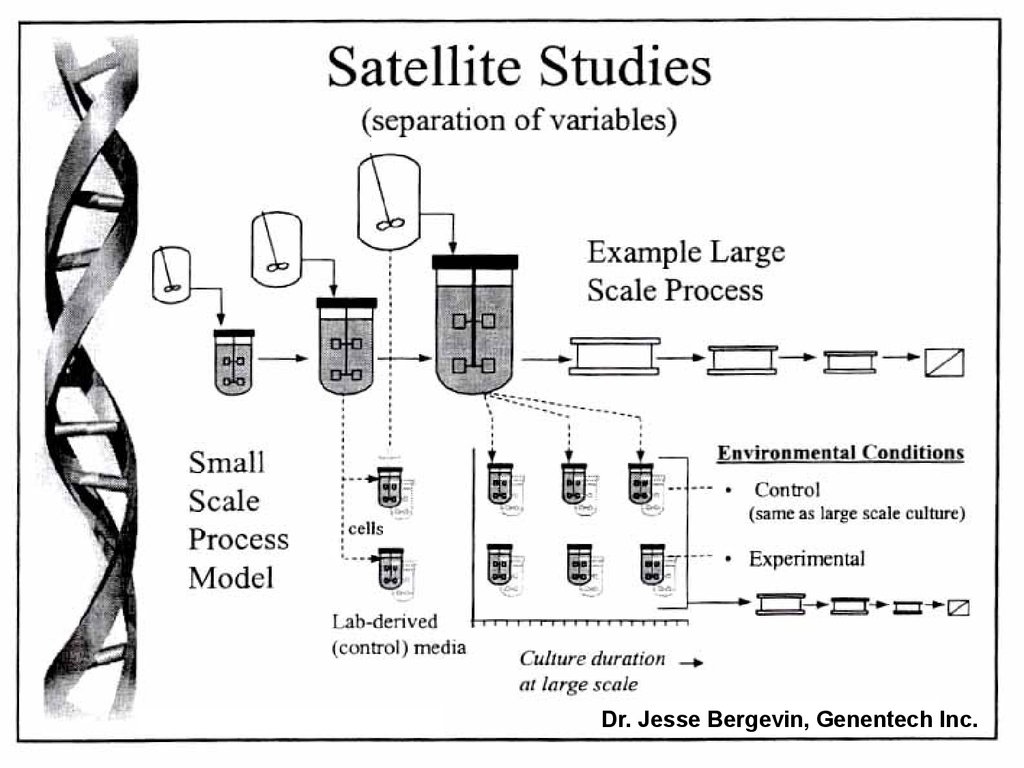
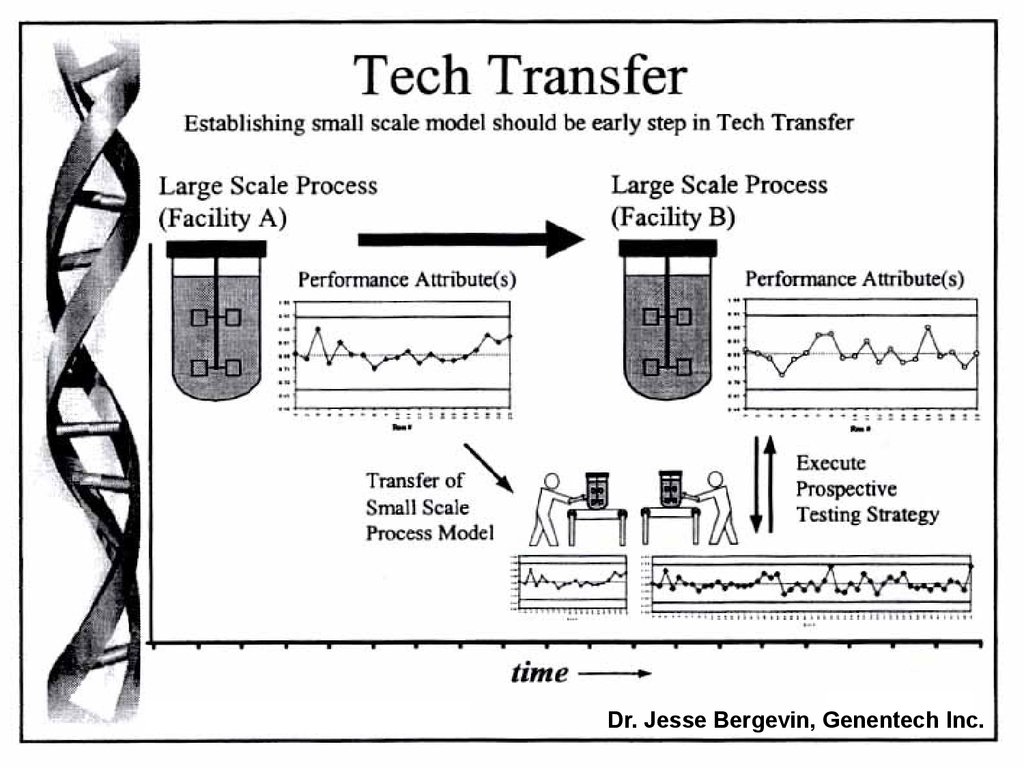
Dr. Jesse Bergevin, Genentech Inc.23.
Dr. Jesse Bergevin, Genentech Inc.24.
25. Выводы
• Перевод технологий производсва биофармацевтическихпрепаратов в Россию может быть успешным и прибыльным
при
– Развитии внутренней сырьевой инфраструктуры для фарм производства
(включая транспортировку хранение и переработку)
– Анализе локального фармацевтического рынка
– Анализе инвестиций стоимости производства
– Расположении производства и обучения специалистов
– Взаимосвязью с правительством
– Защите интеллектуальной собственности
– Развитии страховой медицинской системы
Со временем эти компании смогут обеспечить всю потребность
фармацевтического рынка пльзуясь преимуществом низких цен и
неизбалованостью потребителя
• При правильной корпоративной стратегии развивающиеся
российские компании смогут занять эту нишу без
доминирования иностранных фармацевтических компаний
26. Благодарности:
• Robert Bruch, Sloan School of Management, MIT,Cambridge, MA
• Alexey Bulychev, Alantos Pharmaceuticals Inc., Cambridge,
MA
• Andre Ditsch & Lakshman Pernenkil
Department of Chemical Engineering, MIT, Cambridge, MA
• Florence Tao, Harvard School of Public Health, Harvard
University, Cambridge, MA
• Kurt Bronson & Steve Kozlovski
Center for Biologics Evaluation and Research, FDA
27. Вопросы?
Ответы :info@biorus.com
vadim@biorus.com
www.biorus.com
Professional Association
of Russian-Speaking Bioscientists













 Экономика
Экономика Медицина
Медицина








