Похожие презентации:
Схема газохроматографического анализа
1.
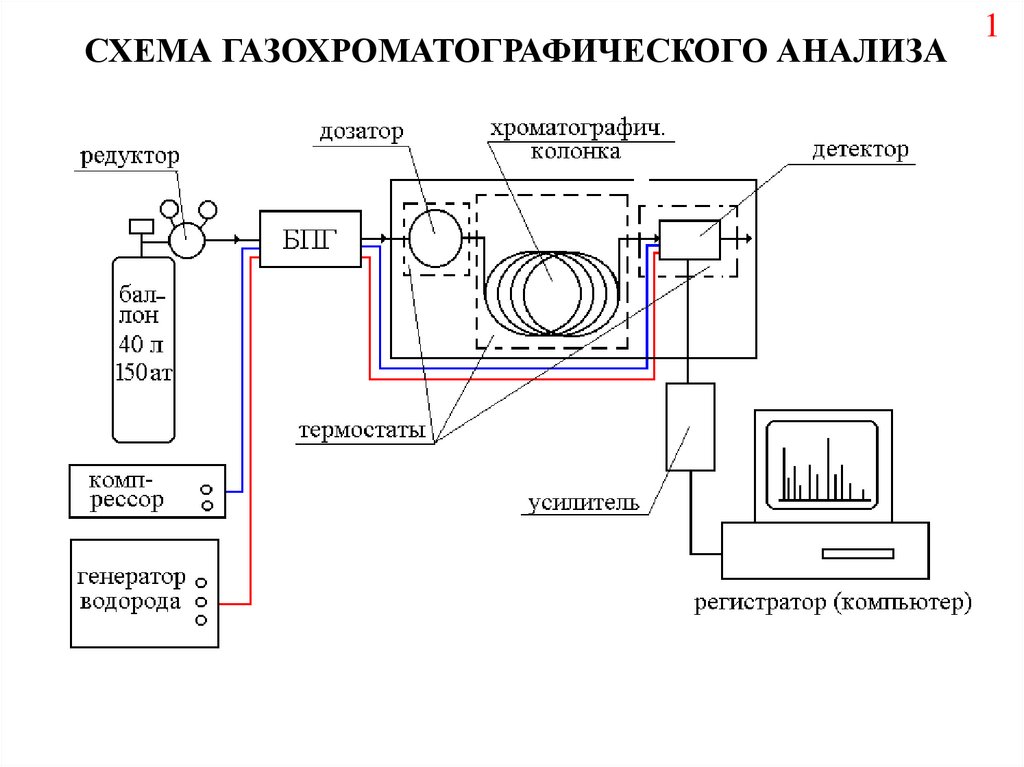
СХЕМА ГАЗОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА1
2.
ТРЕБОВАНИЯ К ГАЗУ-НОСИТЕЛЮ2
1) Химическая инертность
2) Подходящие для детектирования физ.-химические свойства
3) Доступность
Зависимость ВЭТТ от газа-носителя для насадочных колонок
3.
ТРЕБОВАНИЯ К СИСТЕМАМ ДОЗИРОВАНИЯ1. Максимальная воспроизводимость дозирования.
2. Минимальный вклад в размывание пиков
3. Постоянство состава пробы до и после дозирования
3
4.
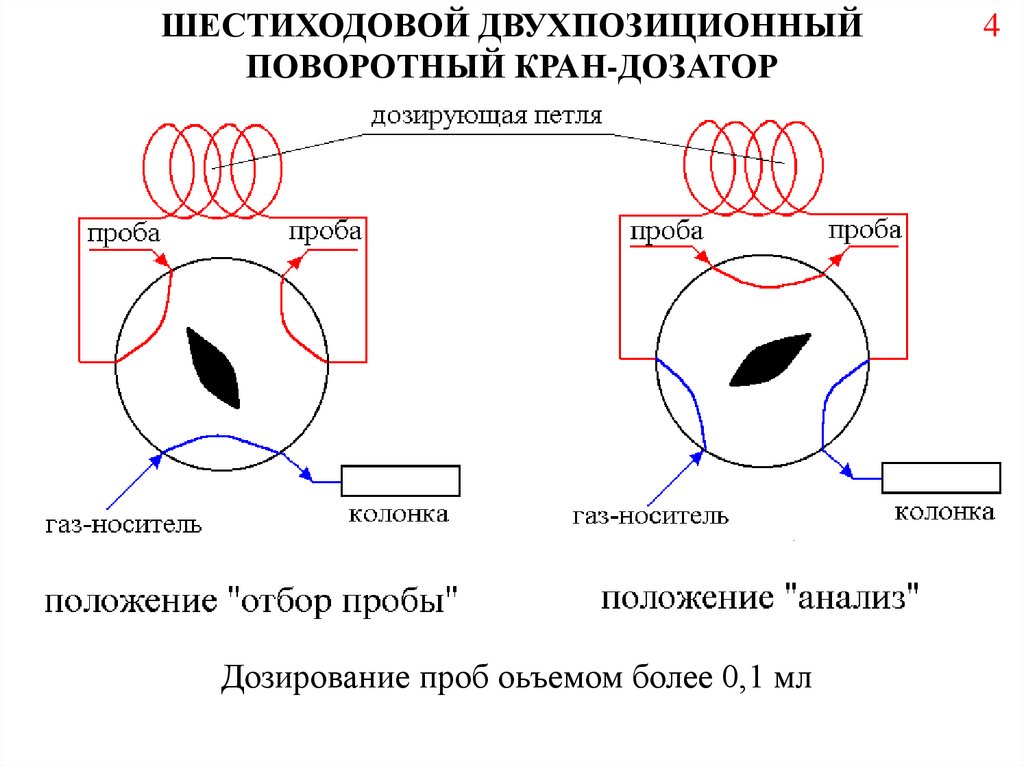
ШЕСТИХОДОВОЙ ДВУХПОЗИЦИОННЫЙПОВОРОТНЫЙ КРАН-ДОЗАТОР
Дозирование проб оьъемом более 0,1 мл
4
5.
ЧЕТЫРЕХХОДОВОЙ ДВУХПОЗИЦИОННЫЙПОВОРОТНЫЙ КРАН-ДОЗАТОР
Дозирование проб объемом менее 0,1 мл
5
6.
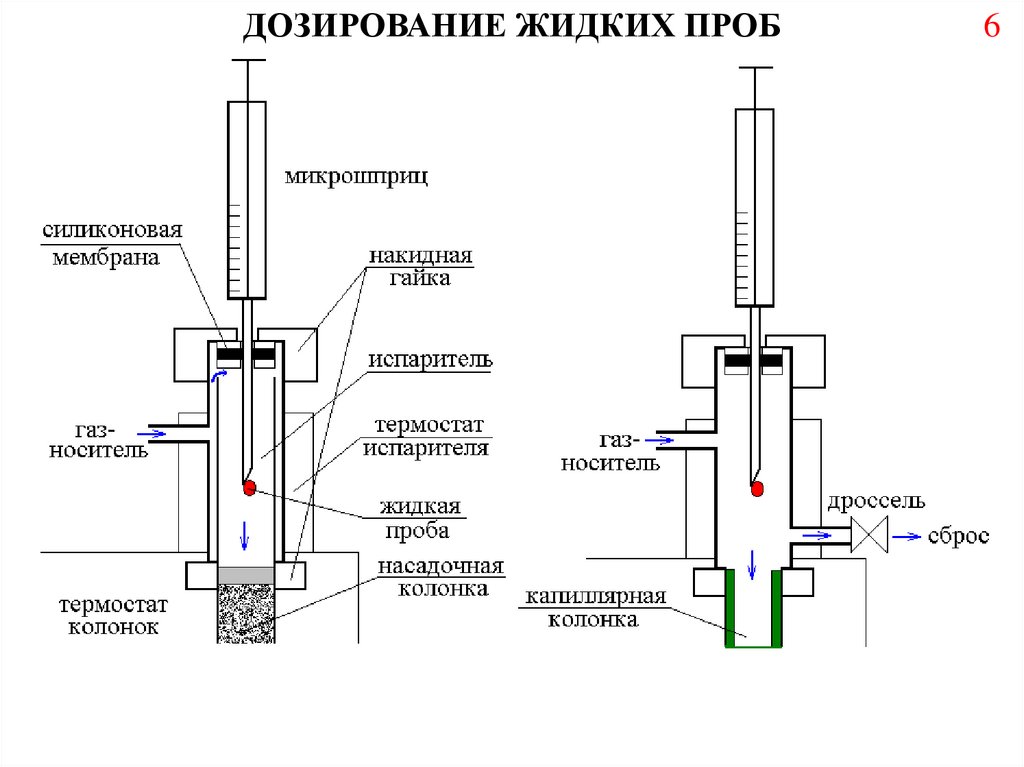
ДОЗИРОВАНИЕ ЖИДКИХ ПРОБ6
7.
7КРИТЕРИИ ВЫБОРА СТАЦИОНАРНОЙ ФАЗЫ В ГАЗОВОЙ
ХРОМАТОГРАФИИ
1. Достаточно высокая селективность фазы
2. Обратимость процесса и линейность изотермы
межфазного распределения
3. Величина шума детектора
4. Стабильность параметров удерживания и
долговечность фазы
8.
СЕЛЕКТИВНОСТЬ СТАЦИОНАРНОЙ ФАЗЫK1
K2
e
Q1 Q2
RT
Q S
RT
R
K e
e
Q
RT
Q E
- коэффициент селективности стационарной фазы;
K – коэффициент межфазного распределения компонента;
Q – молярная теплота межфазного перехода компонента
(адсорбции или растворения);
T – температура, K; R – универсальная газовая постоянная;
S – изменение энтропии в результате межфазного перехода;
E – энергия межмолекулярного взаимодействия между компонентом
и стационарной фазой.
8
9.
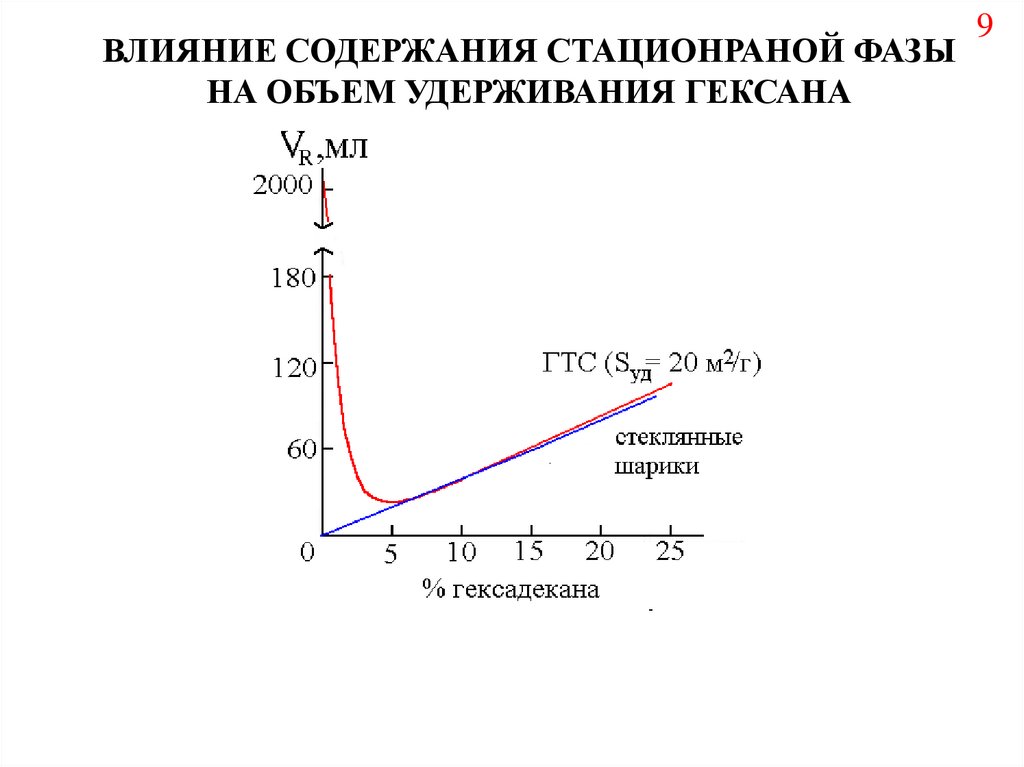
ВЛИЯНИЕ СОДЕРЖАНИЯ СТАЦИОНРАНОЙ ФАЗЫНА ОБЪЕМ УДЕРЖИВАНИЯ ГЕКСАНА
9
10.
10ТИПЫ СЕЛЕКТИВНОСТИ СТАЦИОНАРНОЙ ФАЗЫ
1. Селективность по отношению к разделению гомологов;
2. Селективность по отношению к разделению изомеров;
гом
изом
3. Селективность по отношению к разделению компонентов с
одинаковой температурой кипения. пол
11.
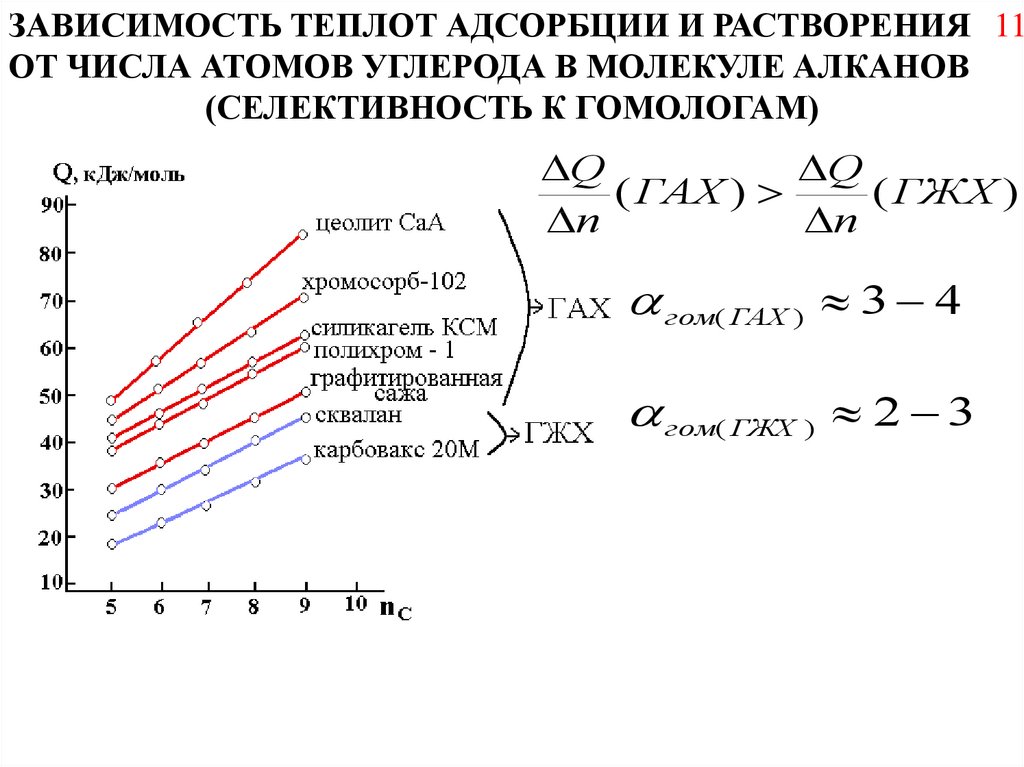
ЗАВИСИМОСТЬ ТЕПЛОТ АДСОРБЦИИ И РАСТВОРЕНИЯ 11ОТ ЧИСЛА АТОМОВ УГЛЕРОДА В МОЛЕКУЛЕ АЛКАНОВ
(СЕЛЕКТИВНОСТЬ К ГОМОЛОГАМ)
Q
Q
( ГАХ )
( ГЖХ )
n
n
гом( ГАХ ) 3 4
гом( ГЖХ ) 2 3
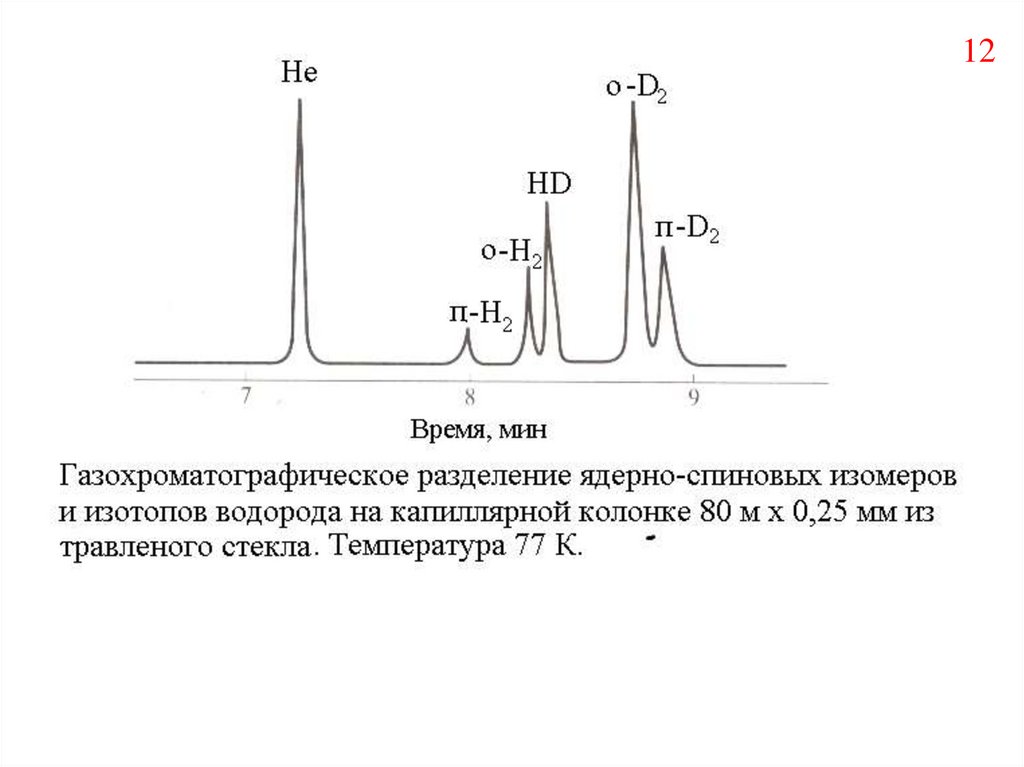
12.
1213.
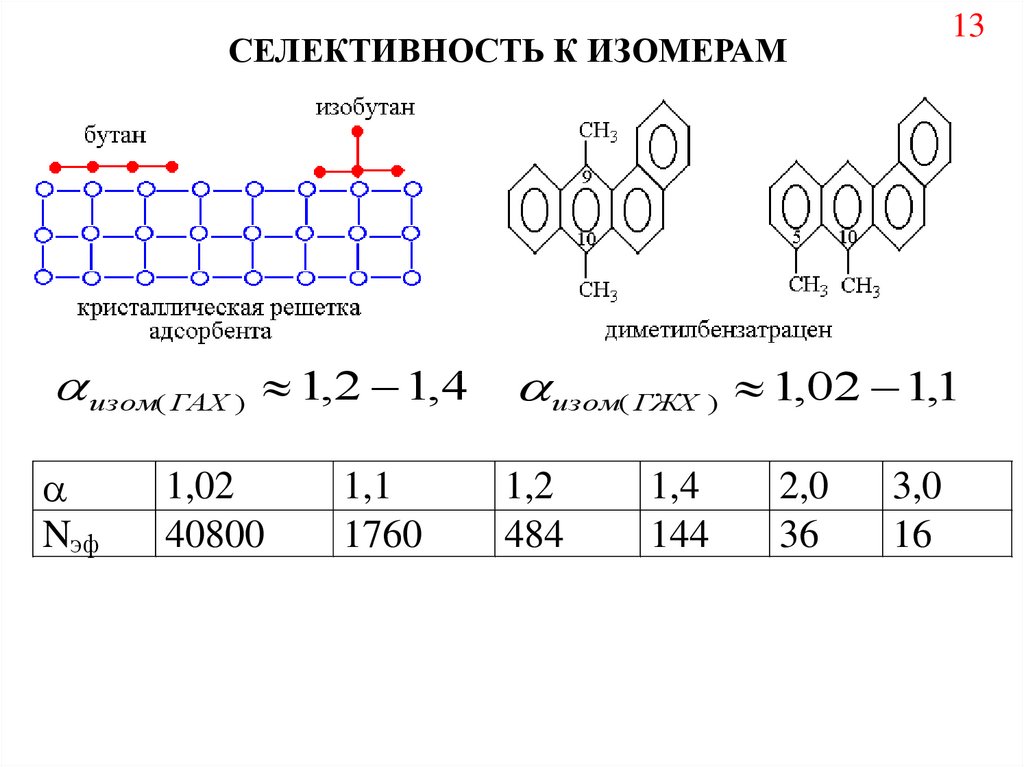
13СЕЛЕКТИВНОСТЬ К ИЗОМЕРАМ
изом( ГАХ ) 1,2 1,4
изом( ГЖХ ) 1,02 1,1
Nэф
1,2
484
1,02
40800
1,1
1760
1,4
144
2,0
36
3,0
16
14.
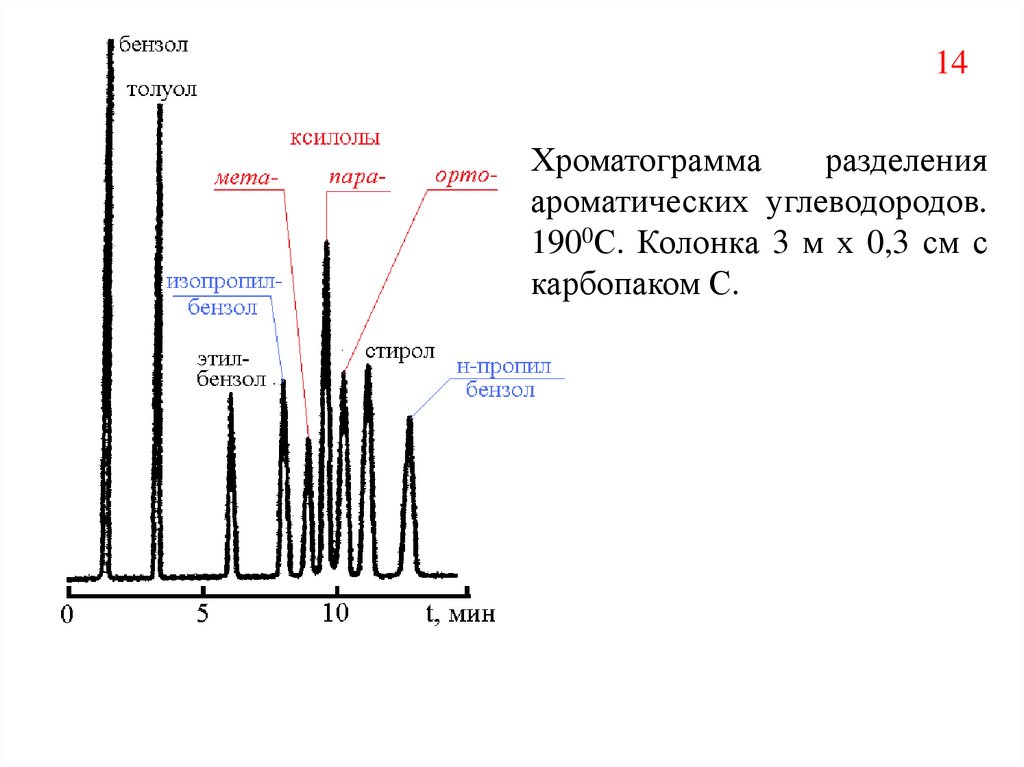
14Хроматограмма
разделения
ароматических углеводородов.
1900С. Колонка 3 м х 0,3 см с
карбопаком С.
15.
15СЕЛЕКТИВНОСТЬ ПО ОТНОШЕНИЮ К ВЕЩЕСТВАМ
С БЛИЗКИМИ ТЕМПЕРАТУРАМИ КИПЕНИЯ
PG = nLP0 - закон Рауля для идеальных растворов
P – парциальное давление компонента в газовой фазе над раствором;
nL – его молярная доля в растворе;
P0– давление насыщенного пара компонента
CL~ nL ; CG ~PG ; K = CL/CG ~ nL/(nLP0) ~ 1/P0
СG и СL – концентрация компонента в газовой и жидкой фазах
= K1/K2 = P02/P01
PG = nLP0 - Закон для неидеальных растворов
- коэффициент активности компонента в растворе;
= K1/K2 = 2P02/ 1P01
Если давления насыщенного пара двух веществ равны
= 2/ 1
16.
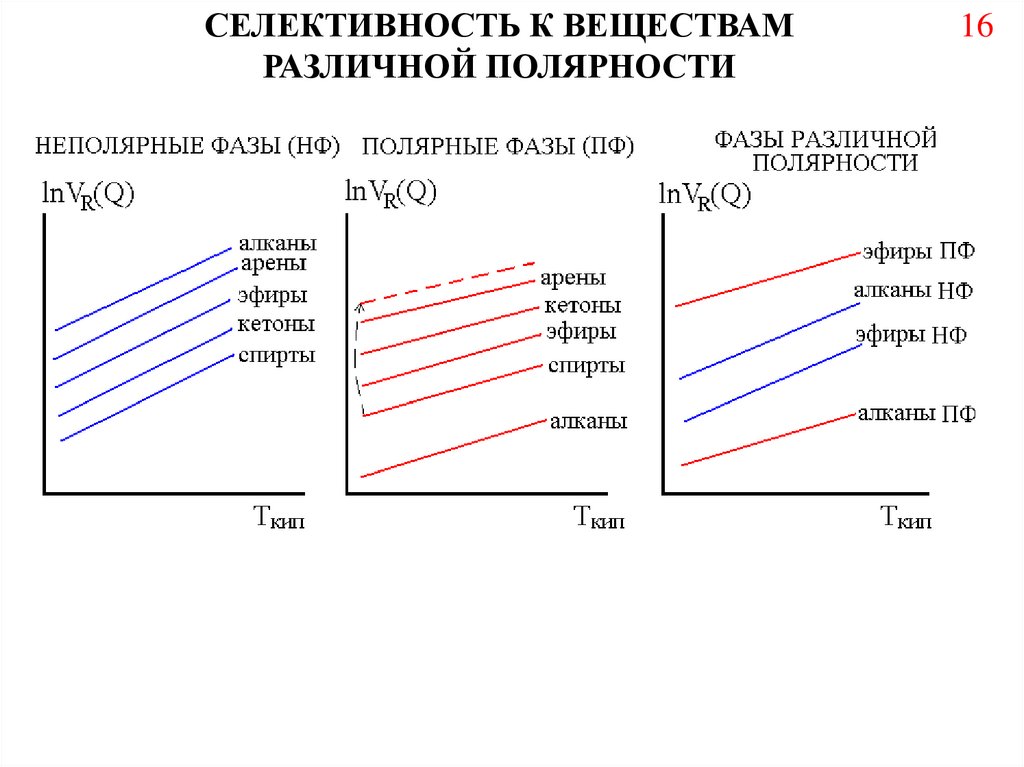
СЕЛЕКТИВНОСТЬ К ВЕЩЕСТВАМРАЗЛИЧНОЙ ПОЛЯРНОСТИ
16
17.
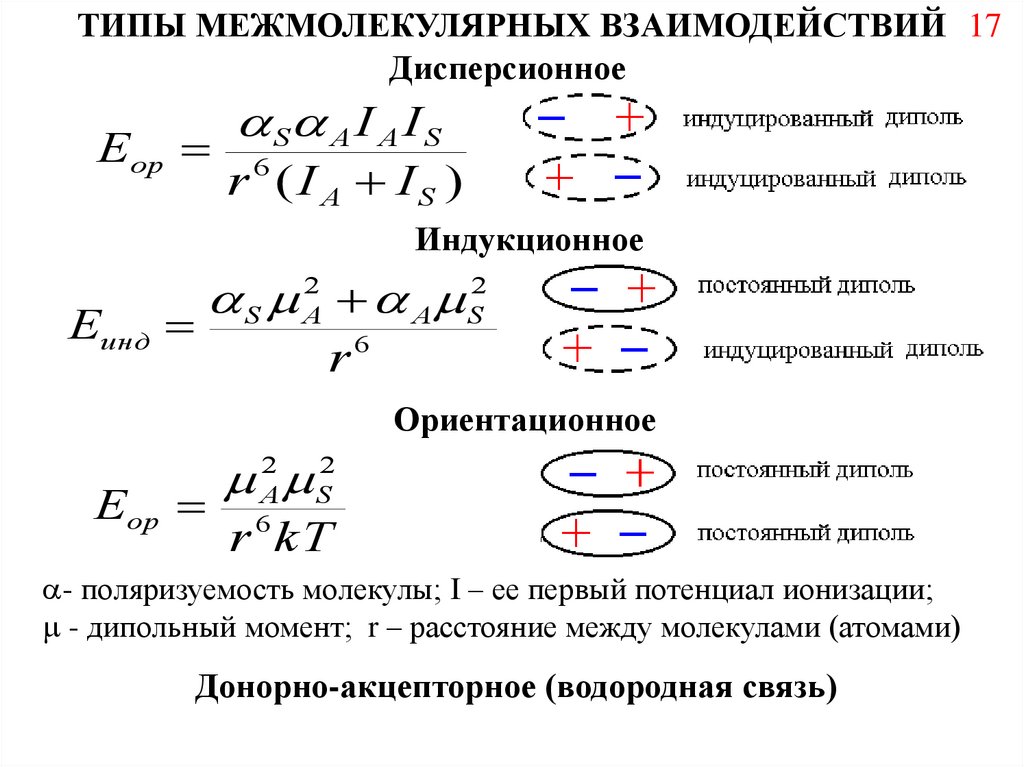
ТИПЫ МЕЖМОЛЕКУЛЯРНЫХ ВЗАИМОДЕЙСТВИЙ 17Дисперсионное
Eор
S A I A I S
r 6 (I A I S )
Индукционное
Eинд
S A
2
A
2
S
r6
Ориентационное
Eор
A2 S2
r 6 kT
- поляризуемость молекулы; I – ее первый потенциал ионизации;
- дипольный момент; r – расстояние между молекулами (атомами)
Донорно-акцепторное (водородная связь)
18.
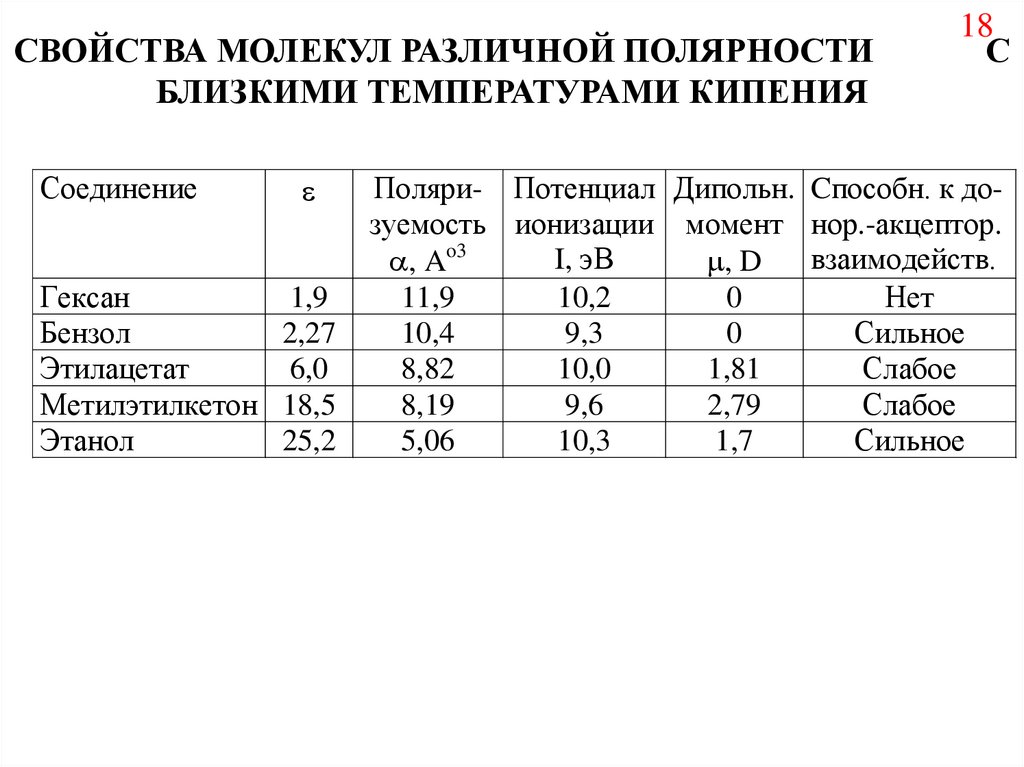
СВОЙСТВА МОЛЕКУЛ РАЗЛИЧНОЙ ПОЛЯРНОСТИБЛИЗКИМИ ТЕМПЕРАТУРАМИ КИПЕНИЯ
Соединение
Гексан
1,9
Бензол
2,27
Этилацетат
6,0
Метилэтилкетон 18,5
Этанол
25,2
18
С
Поляри- Потенциал Дипольн. Cпособн. к дозуемость ионизации момент нор.-акцептор.
I, эВ
взаимодейств.
, Ao3
, D
11,9
10,2
0
Нет
10,4
9,3
0
Сильное
8,82
10,0
1,81
Слабое
8,19
9,6
2,79
Слабое
5,06
10,3
1,7
Сильное
19.
19ПОЛЯРНОСТЬ СТАЦИОНАРНЫХ ФАЗ ПО РОРШНАЙДЕРУ
q1 qx
P 100 1
q1 q2
VR ( бутадиен 1,3)
q lg
V
R ( бутан)
1 – оксидипропионитрил N C – (CH2)2 – O – (CH2)2 – C N
2 – сквалан С30H62 – гексаметилтетракозан
P – (0 5) % – неполярная фаза
P – (5 15) % – слабополярная фаза
P – (15 35) % – среднеполярная фаза
P – (35 50) % – полярная фаза
P – (50 100) % – сильнополярная фаза
20.
СЕЛЕКТИВНОСТЬ СТАЦИОНАРНЫХ ФАЗПО МАК-РЕЙНОЛЬДСУ
I = Ii – Iсквалан
I – логарифмические индекс удерживания Ковача при 120 0С
x = Iбензол – характеризует селективность фазы к
ароматическим и ненасыщенным унлеводородам;
y = Iбутанол – характеризует селективность фазы к спиртам,
кислотам, аминам и алкилгалогенидам;
z = Iметилпропилкетон – характеризует селективность фазы к
карбонильным соединениям (альдегидам, кетонам, сложным
эфирам);
s = Iнитропропан – характеризует селективность фазы к
нитропроизводным;
u = Iпиридин – характеризует селективность фазы к
гетероциклическим соединениям.
20
21.
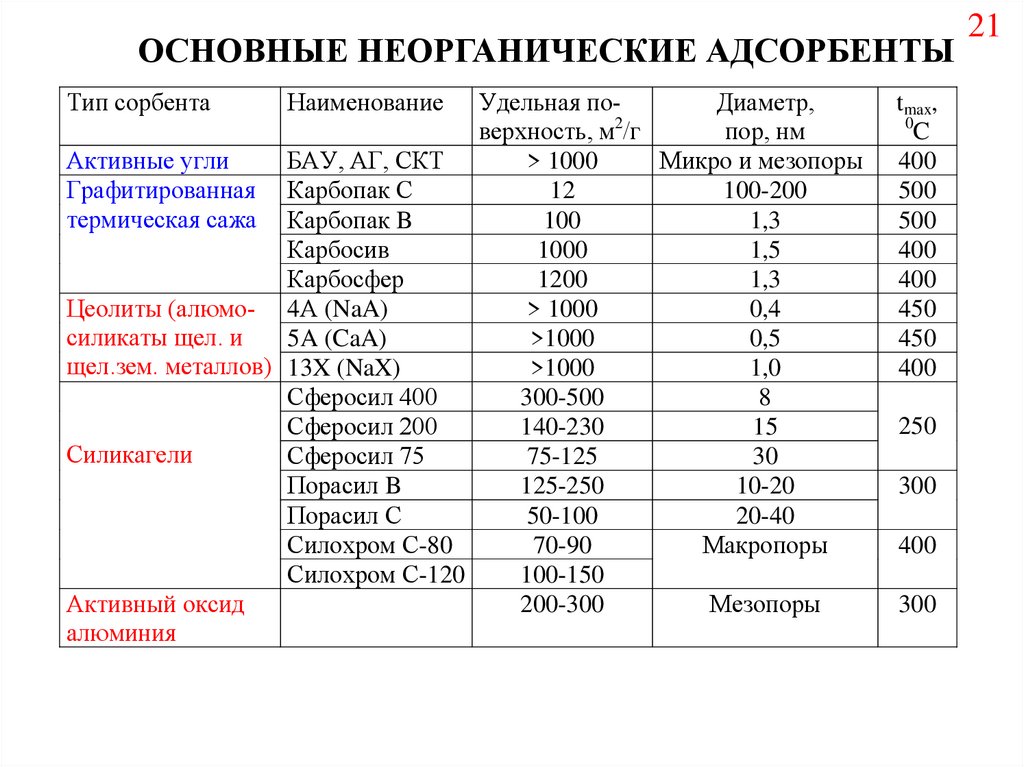
ОСНОВНЫЕ НЕОРГАНИЧЕСКИЕ АДСОРБЕНТЫТип сорбента
Наименование
Удельная поДиаметр,
2
верхность, м /г
пор, нм
Активные угли
БАУ, АГ, СКТ
> 1000
Микро и мезопоры
Графитированная Карбопак С
12
100-200
термическая сажа Карбопак B
100
1,3
Карбосив
1000
1,5
Карбосфер
1200
1,3
Цеолиты (алюмо- 4А (NaA)
> 1000
0,4
силикаты щел. и
5A (CaA)
>1000
0,5
щел.зем. металлов) 13X (NaX)
>1000
1,0
Сферосил 400
300-500
8
Сферосил 200
140-230
15
Силикагели
Сферосил 75
75-125
30
Порасил B
125-250
10-20
Порасил С
50-100
20-40
Силохром С-80
70-90
Макропоры
Силохром С-120
100-150
Активный оксид
200-300
Мезопоры
алюминия
tmax,
0
C
400
500
500
400
400
450
450
400
250
300
400
300
21
22.
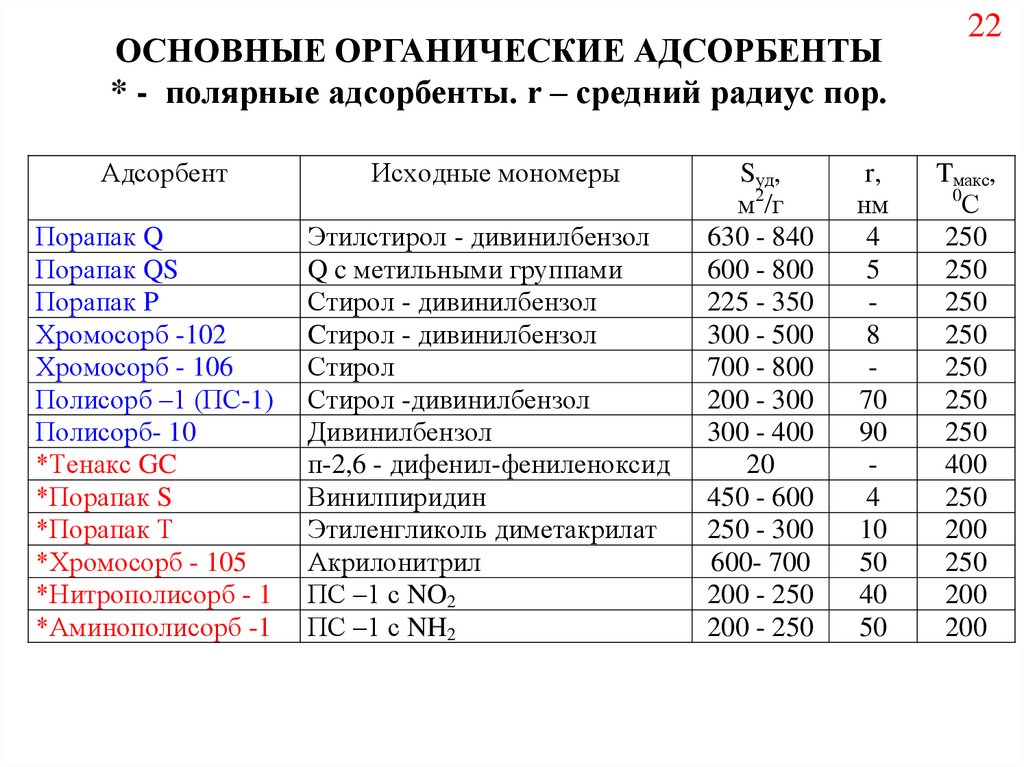
ОСНОВНЫЕ ОРГАНИЧЕСКИЕ АДСОРБЕНТЫ* - полярные адсорбенты. r – средний радиус пор.
Адсорбент
Порапак Q
Порапак QS
Порапак P
Хромосорб -102
Хромосорб - 106
Полисорб –1 (ПС-1)
Полисорб- 10
*Тенакс GC
*Порапак S
*Порапак Т
*Хромосорб - 105
*Нитрополисорб - 1
*Аминополисорб -1
Исходные мономеры
Этилстирол - дивинилбензол
Q c метильными группами
Стирол - дивинилбензол
Cтирол - дивинилбензол
Стирол
Стирол -дивинилбензол
Дивинилбензол
п-2,6 - дифенил-фениленоксид
Винилпиридин
Этиленгликоль диметакрилат
Акрилонитрил
ПС –1 с NO2
ПС –1 с NH2
Sуд,
м2/г
630 - 840
600 - 800
225 - 350
300 - 500
700 - 800
200 - 300
300 - 400
20
450 - 600
250 - 300
600- 700
200 - 250
200 - 250
r,
нм
4
5
8
70
90
4
10
50
40
50
22
Tмакс,
0
С
250
250
250
250
250
250
250
400
250
200
250
200
200
23.
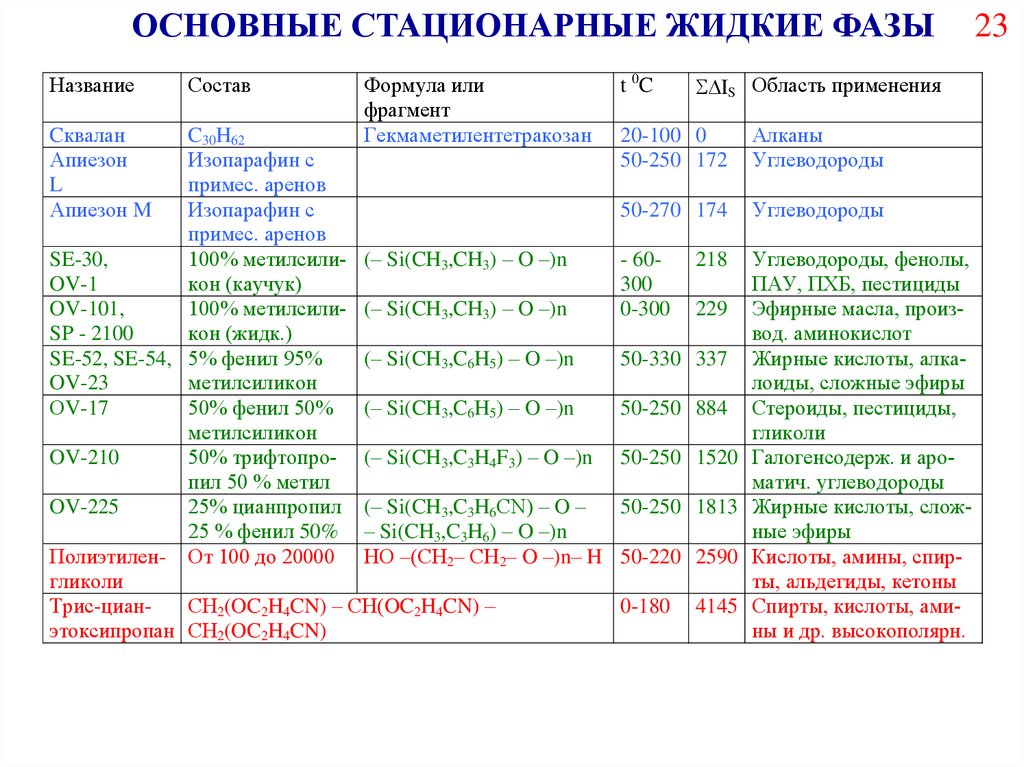
ОСНОВНЫЕ СТАЦИОНАРНЫЕ ЖИДКИЕ ФАЗЫНазвание
Cквалан
Апиезон
L
Апиезон M
Состав
Формула или
фрагмент
Гекмаметилентетракозан
C30H62
Изопарафин с
примес. аренов
Изопарафин с
примес. аренов
SE-30,
100% метилсили- (– Si(CH3,CH3) – O –)n
OV-1
кон (каучук)
OV-101,
100% метилсили- (– Si(CH3,CH3) – O –)n
SP - 2100
кон (жидк.)
SE-52, SE-54, 5% фенил 95%
(– Si(CH3,C6H5) – O –)n
OV-23
метилсиликон
ОV-17
50% фенил 50% (– Si(CH3,C6H5) – O –)n
метилсиликон
OV-210
50% трифтопро- (– Si(CH3,C3H4F3) – O –)n
пил 50 % метил
OV-225
25% цианпропил (– Si(CH3,C3H6СN) – O –
25 % фенил 50% – Si(CH3,C3H6) – O –)n
Полиэтилен- От 100 до 20000 НО –(СН2– СН2– O –)n– H
гликоли
Трис-цианСН2(OC2H4CN) – СН(OC2H4CN) –
этоксипропан СН2(OC2H4CN)
t 0C
IS Область применения
20-100 0
50-250 172
Алканы
Углеводороды
50-270 174
Углеводороды
- 60300
0-300
Углеводороды, фенолы,
ПАУ, ПХБ, пестициды
Эфирные масла, производ. аминокислот
Жирные кислоты, алкалоиды, сложные эфиры
Стероиды, пестициды,
гликоли
Галогенсодерж. и ароматич. углеводороды
Жирные кислоты, сложные эфиры
Кислоты, амины, спирты, альдегиды, кетоны
Спирты, кислоты, амины и др. высокополярн.
218
229
50-330 337
50-250 884
50-250 1520
50-250 1813
50-220 2590
0-180
4145
23
24.
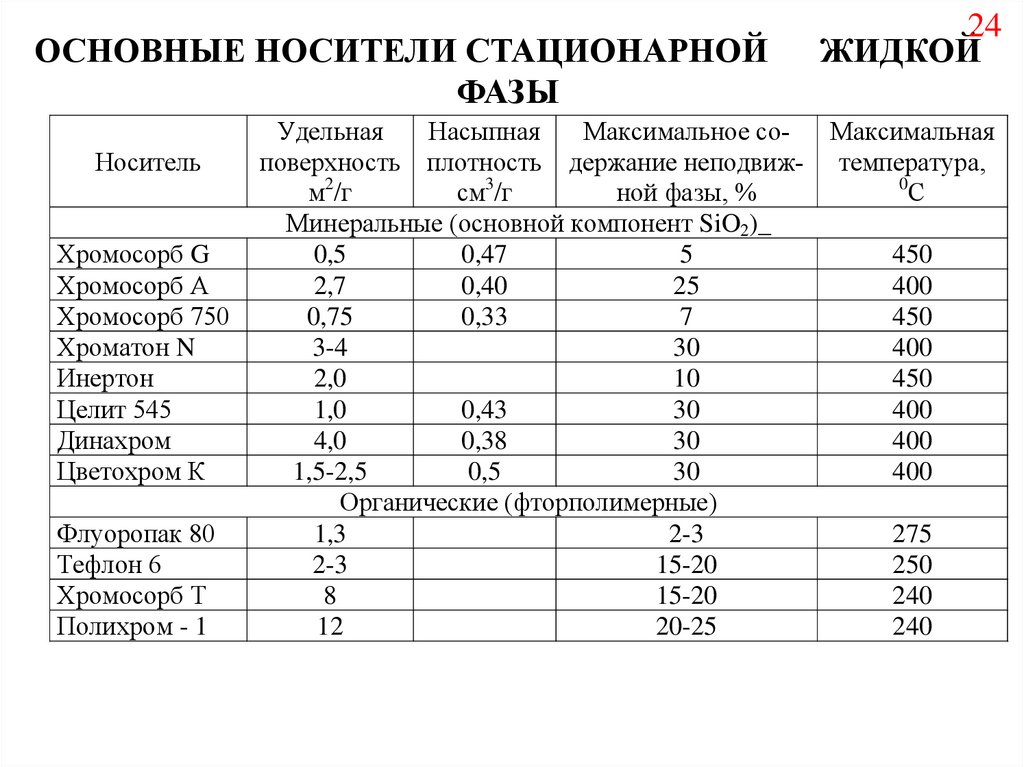
ОСНОВНЫЕ НОСИТЕЛИ СТАЦИОНАРНОЙФАЗЫ
Носитель
Хромосорб G
Хромосорб А
Хромосорб 750
Хроматон N
Инертон
Целит 545
Динахром
Цветохром К
Флуоропак 80
Тефлон 6
Хромосорб Т
Полихром - 1
24
ЖИДКОЙ
Удельная
Насыпная
Максимальное соМаксимальная
поверхность плотность держание неподвиж- температура,
0
м2/г
см3/г
ной фазы, %
С
Минеральные (основной компонент SiO2)_
0,5
0,47
5
450
2,7
0,40
25
400
0,75
0,33
7
450
3-4
30
400
2,0
10
450
1,0
0,43
30
400
4,0
0,38
30
400
1,5-2,5
0,5
30
400
Органические (фторполимерные)
1,3
2-3
275
2-3
15-20
250
8
15-20
240
12
20-25
240
25.
25СПОСОБЫ ОБРАБОТКИ НОСИТЕЛЕЙ
Маркировка
носителей
NAW
AW
BW
ABW
DMCS
HMDS
Способы обработки
Без обработки
Промытый кислотой (разбавленная HCl)
Промытый основанием (спиртовый раствор
КОН)
Последовательное сочетание двух способов
обработки
Гидрофобизированный диметилдихлорсиланом
(10 % раствор в толуоле)
Гидрофобизированный гексаметилдисилазаном
26.
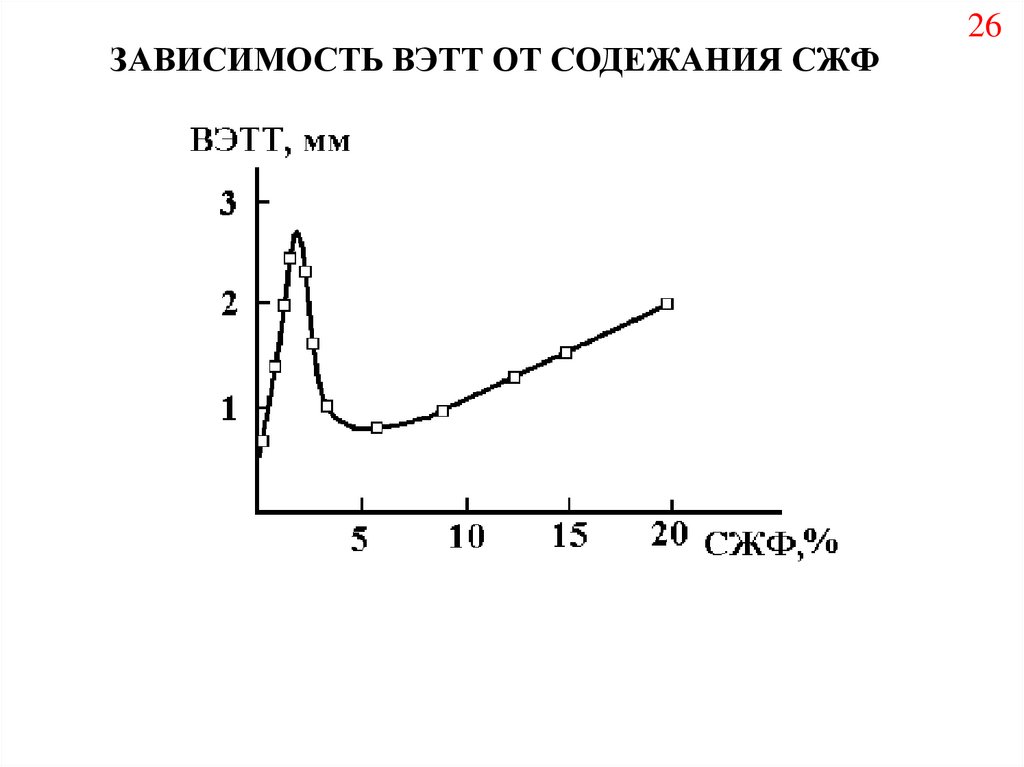
ЗАВИСИМОСТЬ ВЭТТ ОТ СОДЕЖАНИЯ СЖФ26
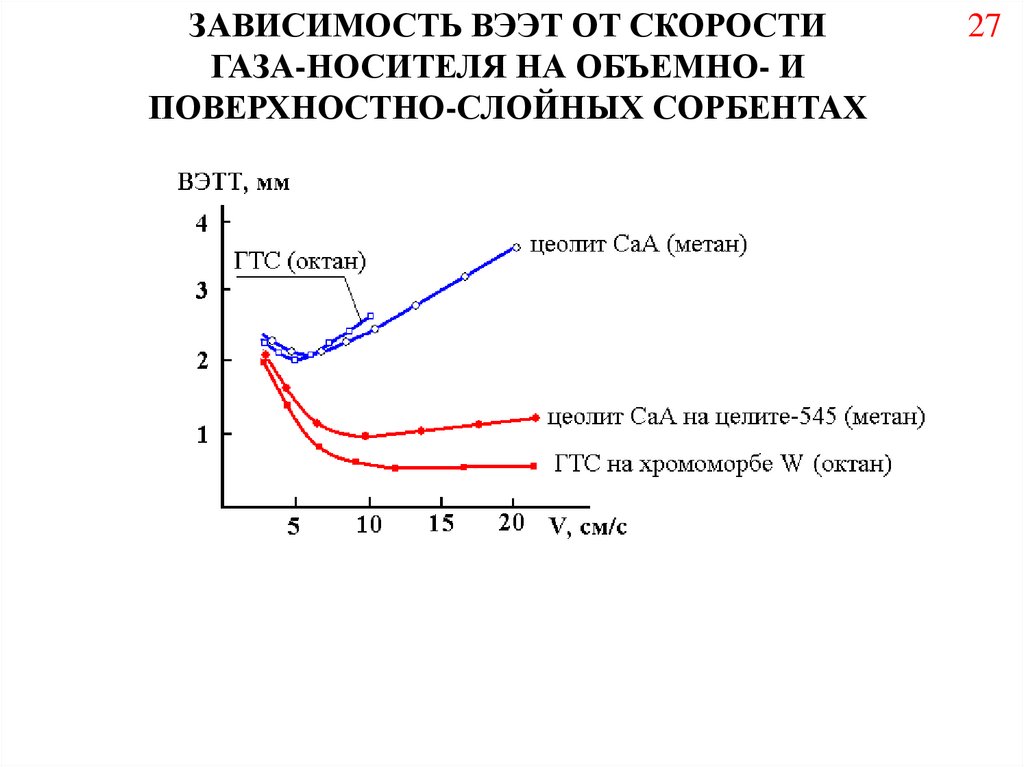
27.
ЗАВИСИМОСТЬ ВЭЭТ ОТ СКОРОСТИГАЗА-НОСИТЕЛЯ НА ОБЪЕМНО- И
ПОВЕРХНОСТНО-СЛОЙНЫХ СОРБЕНТАХ
27
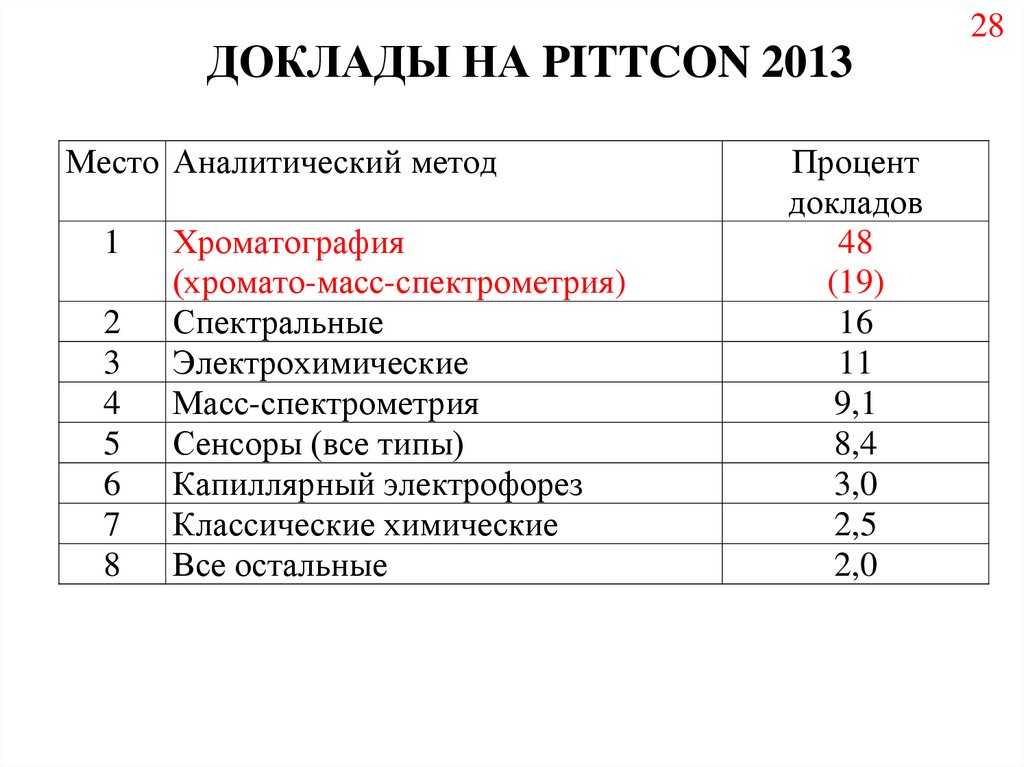
28.
ДОКЛАДЫ НА PITTCON 2013Место Аналитический метод
1
2
3
4
5
6
7
8
Хроматография
(хромато-масс-спектрометрия)
Спектральные
Электрохимические
Масс-спектрометрия
Сенсоры (все типы)
Капиллярный электрофорез
Классические химические
Все остальные
Процент
докладов
48
(19)
16
11
9,1
8,4
3,0
2,5
2,0
28
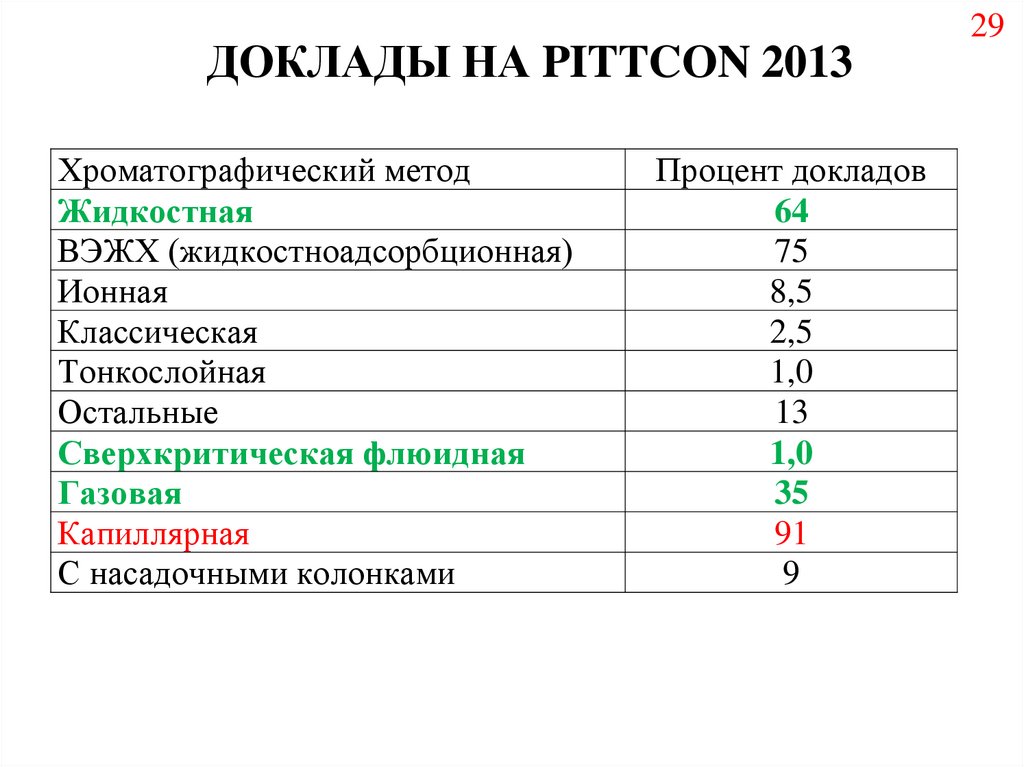
29.
ДОКЛАДЫ НА PITTCON 2013Хроматографический метод
Жидкостная
ВЭЖХ (жидкостноадсорбционная)
Ионная
Классическая
Тонкослойная
Остальные
Сверхкритическая флюидная
Газовая
Капиллярная
С насадочными колонками
Процент докладов
64
75
8,5
2,5
1,0
13
1,0
35
91
9
29
30.
ДОСТОНИНСТВА КАПИЛЛЯРНОЙГАЗОВОЙ ХРОМАТОГРАФИИ
1.
2.
3.
4.
5.
6.
Высокая эффективность
Высокая разделительная способность
Экспрессность
Высокая информативность
Легкость идентификации
Малый объем пробы
НЕДОСТАТКИ
1. Относительно высокая стоимость материалов
2. Меньшая долговечность и надёжность
3. Относительно невысокая чувствительность
30
31.
ОСНОВНЫЕ ОБЛАСТИ ПРИМЕНЕНИЯКАПИЛЛЯРНОЙ ГАЗОВОЙ ХРОМАТОГРАФИИ
• определение компонентов с близкими свойствами
31
• анализ сложных смесей с большим числом разнообразных веществ
В частности, КГХ применяется для анализа и определения:
• изотопов и изомеров газообразных веществ
• изомеров положения и цис- транс-изомеров
• газовых конденсатов, бензиновых фракций и сырой нефти
• воздуха загрязненных городов
• примесей в питьевой и природных водах
• безалкогольных и алкогольных напитков
• биологических жидкостей
•ароматов пищевых продуктов
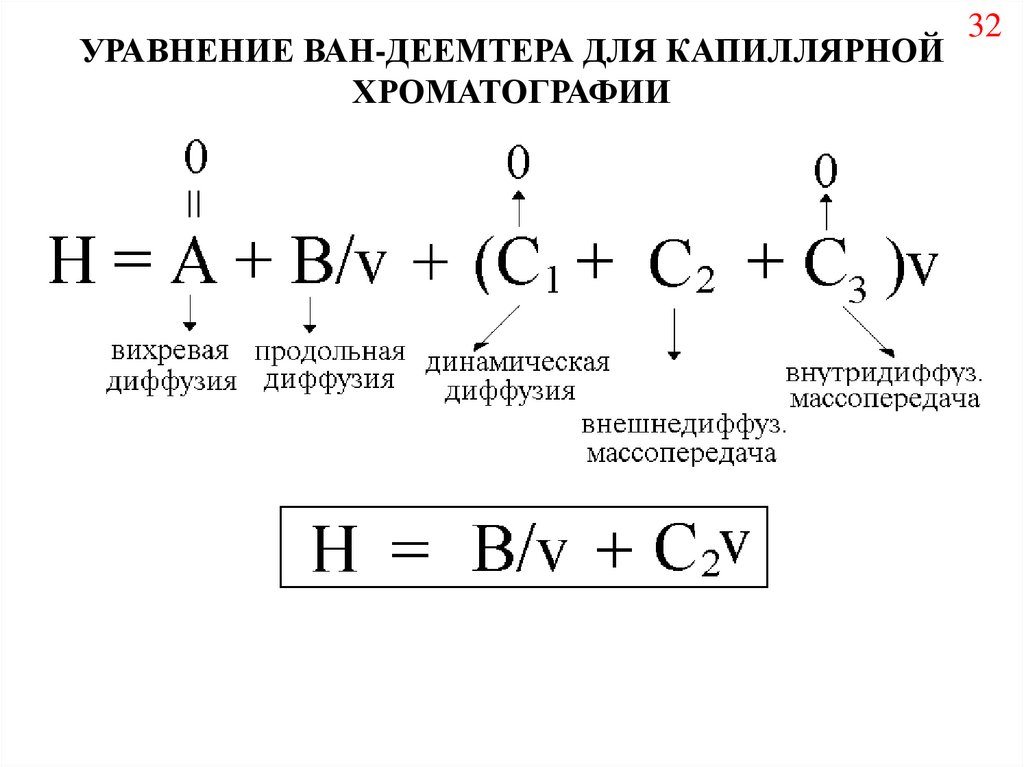
32.
УРАВНЕНИЕ ВАН-ДЕЕМТЕРА ДЛЯ КАПИЛЛЯРНОЙХРОМАТОГРАФИИ
32
33.
2 DMr (1 6k 11k )
H
[
]v
2
v
DM
24(1 k )
2
2
DM – коэффициент диффузии в подвижной газовой фазе;
r – радиус капиллярной колонки ;
k – фактор удерживания (коэфф. емкости) k = K(VS/VM)
33
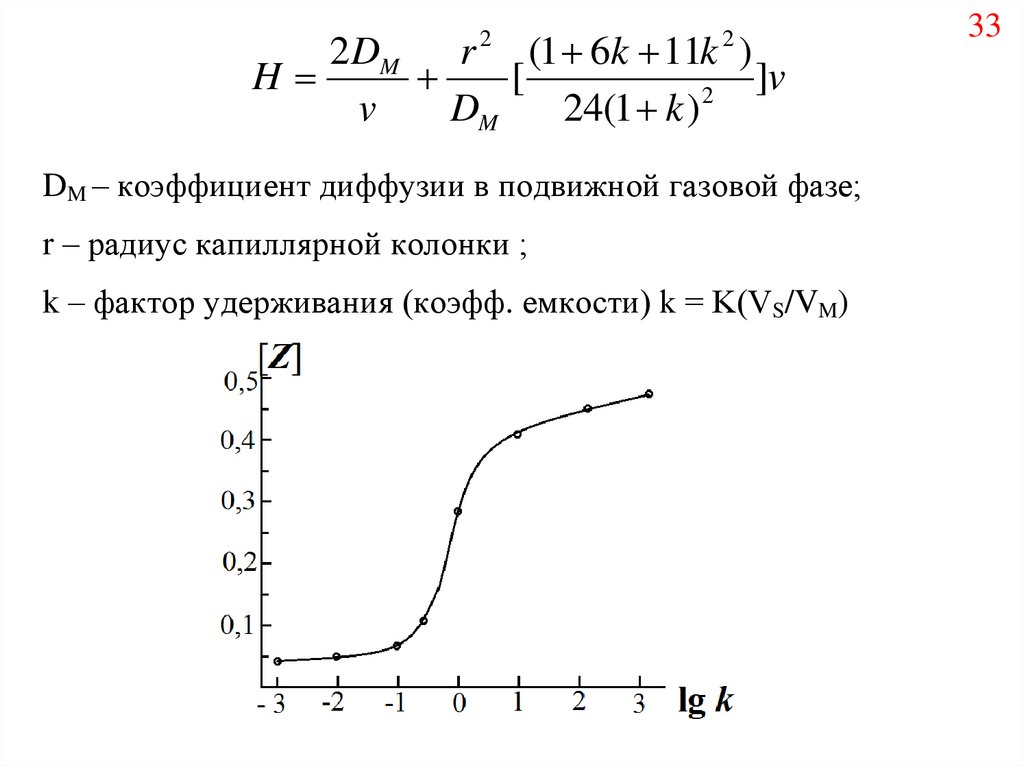
34.
34hmin
k
Z
1 6k 11k
r
2
3(1 k )
2
0
0,01
0,1
1
10
100
∞
0,58
0,59
0,70
1,22
1,78
1,90
1,91
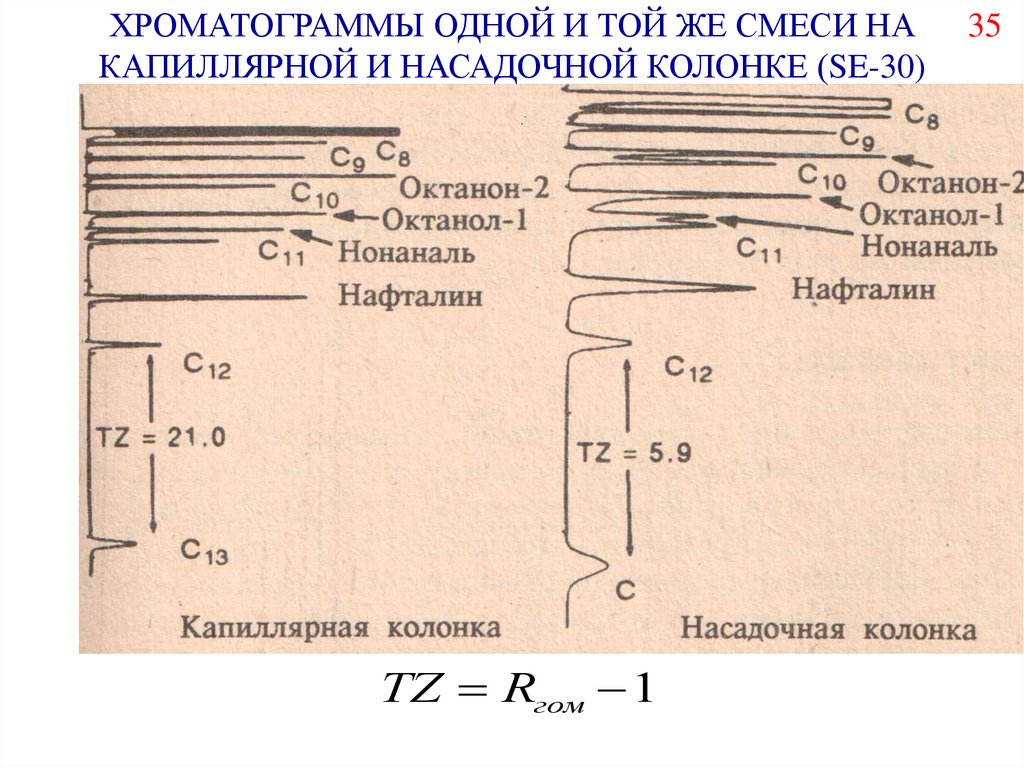
35.
ХРОМАТОГРАММЫ ОДНОЙ И ТОЙ ЖЕ СМЕСИ НАКАПИЛЛЯРНОЙ И НАСАДОЧНОЙ КОЛОНКЕ (SE-30)
TZ Rгом 1
35
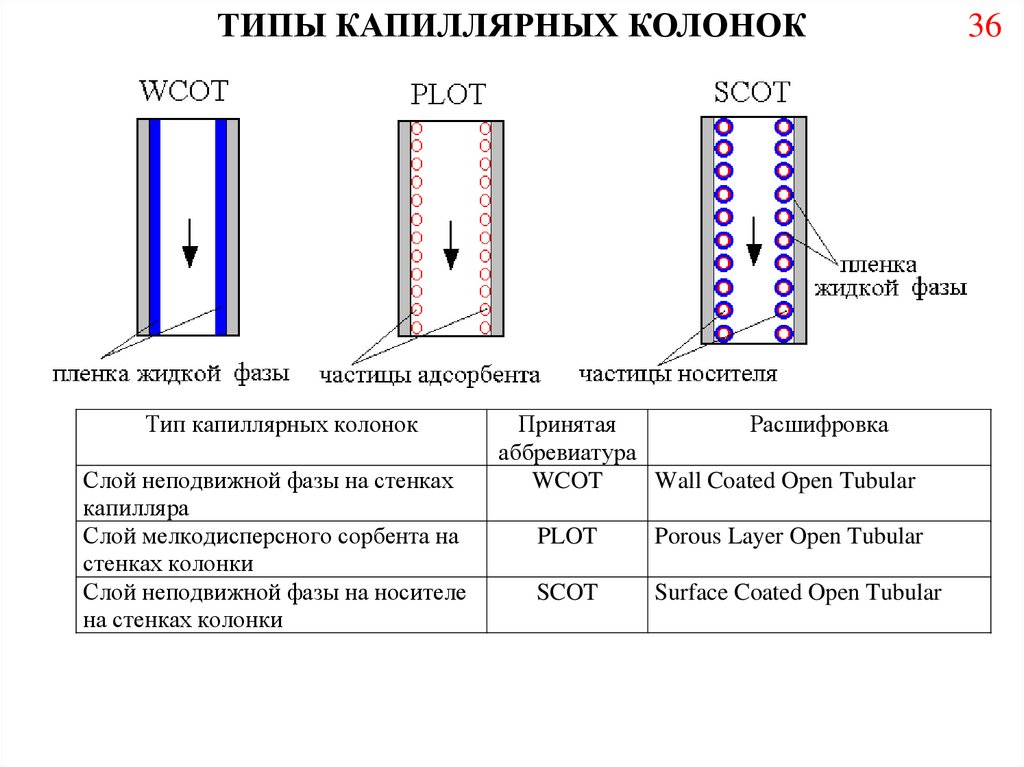
36.
ТИПЫ КАПИЛЛЯРНЫХ КОЛОНОКТип капиллярных колонок
Слой неподвижной фазы на стенках
капилляра
Слой мелкодисперсного сорбента на
стенках колонки
Слой неподвижной фазы на носителе
на стенках колонки
Принятая
Расшифровка
аббревиатура
WCOT
Wall Coated Open Tubular
PLOT
Porous Layer Open Tubular
SCOT
Surface Coated Open Tubular
36
37.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА РАЗДЕЛЕНИЕ ВКАПИЛЛЯРНОЙ ГАЗОВОЙ ХРОМАТОГРАФИИ
• природа
и скорость газа-носителя
• длина и радиус хроматографической колонки
•толщина пленки и размер частиц
стационарной фазы
•природа стационарной фазы
• температура
37
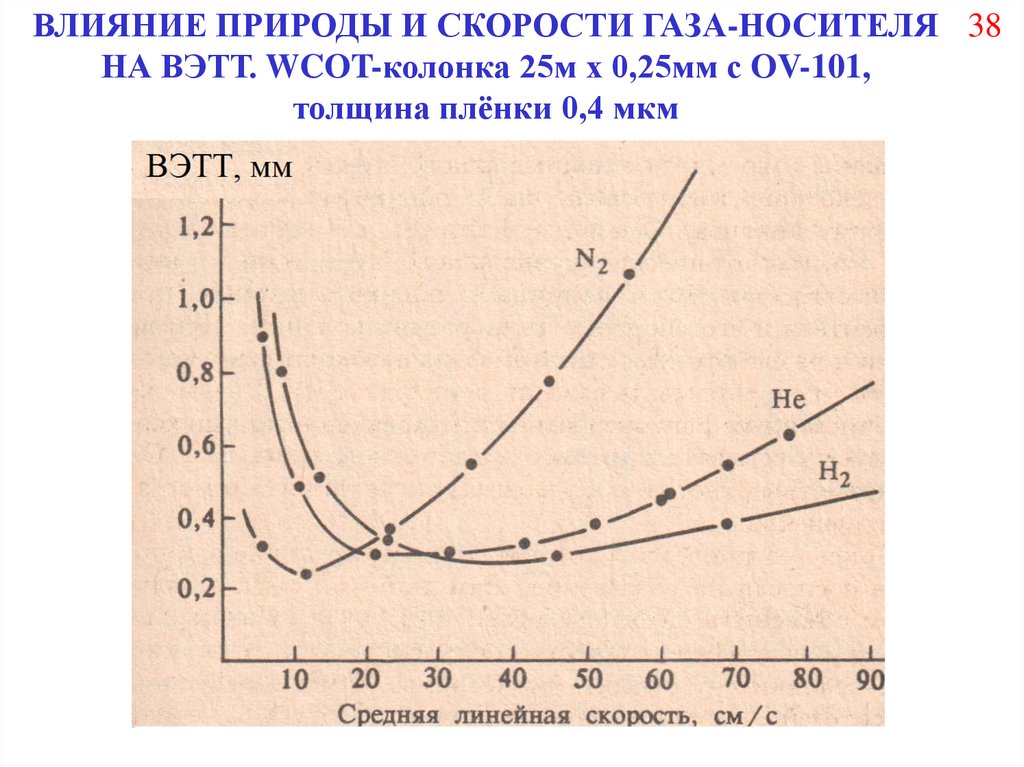
38.
ВЛИЯНИЕ ПРИРОДЫ И СКОРОСТИ ГАЗА-НОСИТЕЛЯ 38НА ВЭТТ. WCOT-колонка 25м х 0,25мм с OV-101,
толщина плёнки 0,4 мкм
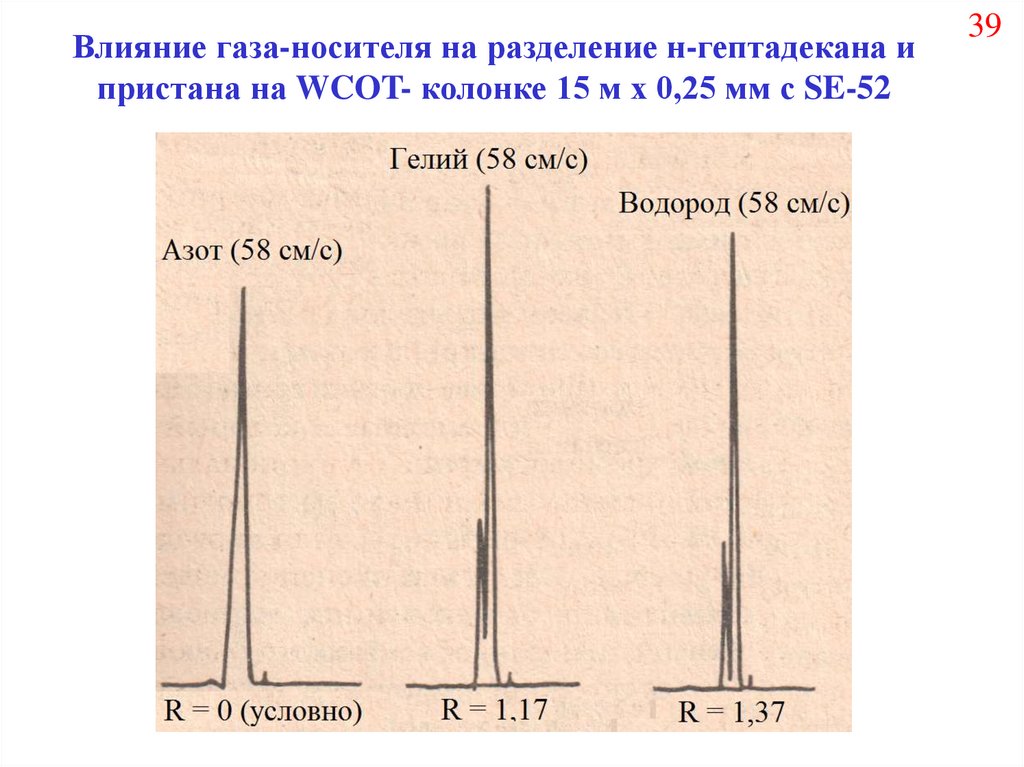
39.
Влияние газа-носителя на разделение н-гептадекана ипристана на WCOT- колонке 15 м х 0,25 мм с SE-52
39
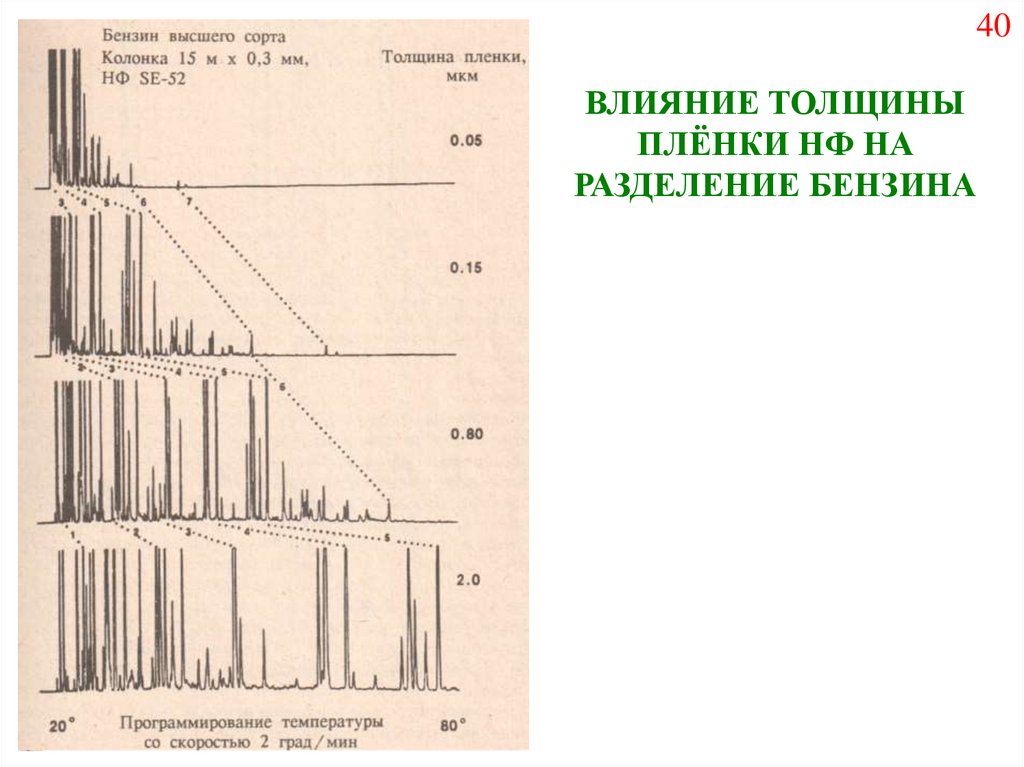
40.
40ВЛИЯНИЕ ТОЛЩИНЫ
ПЛЁНКИ НФ НА
РАЗДЕЛЕНИЕ БЕНЗИНА
41.
ВЛИЯНИЕ РАЗЛИЧНЫХ ФАКТОРОВ НА РАЗДЕЛЕНИЕ 41'
K
1
ср
N эф
R разр 0,5
'
1 K ср 1
L
L
N эф
R разд 0,212 K сел
H эф
H
= K2/K1 = VR(2) / VR(1) - коэффициент селективности стационарной фазы;
Kcр - среднее значение факторов удерживания разделяемых компонентов;
L – длина хроматографической колонки;
Hэф – высота, эквивалентная эффективной теоретической тарелки;
K cел = 2(VR(2)-VR(1))/(VR(2) + VR(1)) – селективность хроматограф. колонки.
d 2f
2k 2
H (C 3 )
v
2
Ds 4(1 k )
df – толщина плёнки стационарной фазы,
DS – коэффициент диффузии в этой фазе;
K – фактор удерживания
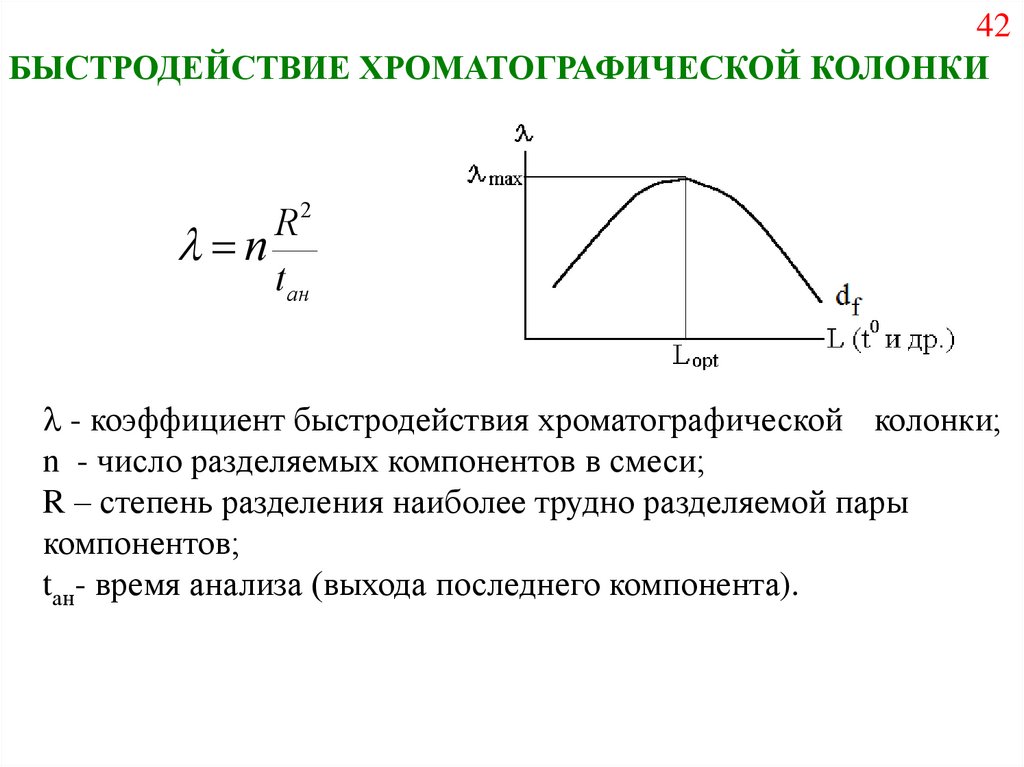
42.
42БЫСТРОДЕЙСТВИЕ ХРОМАТОГРАФИЧЕСКОЙ КОЛОНКИ
R2
n
tан
- коэффициент быстродействия хроматографической колонки;
n - число разделяемых компонентов в смеси;
R – степень разделения наиболее трудно разделяемой пары
компонентов;
tан- время анализа (выхода последнего компонента).
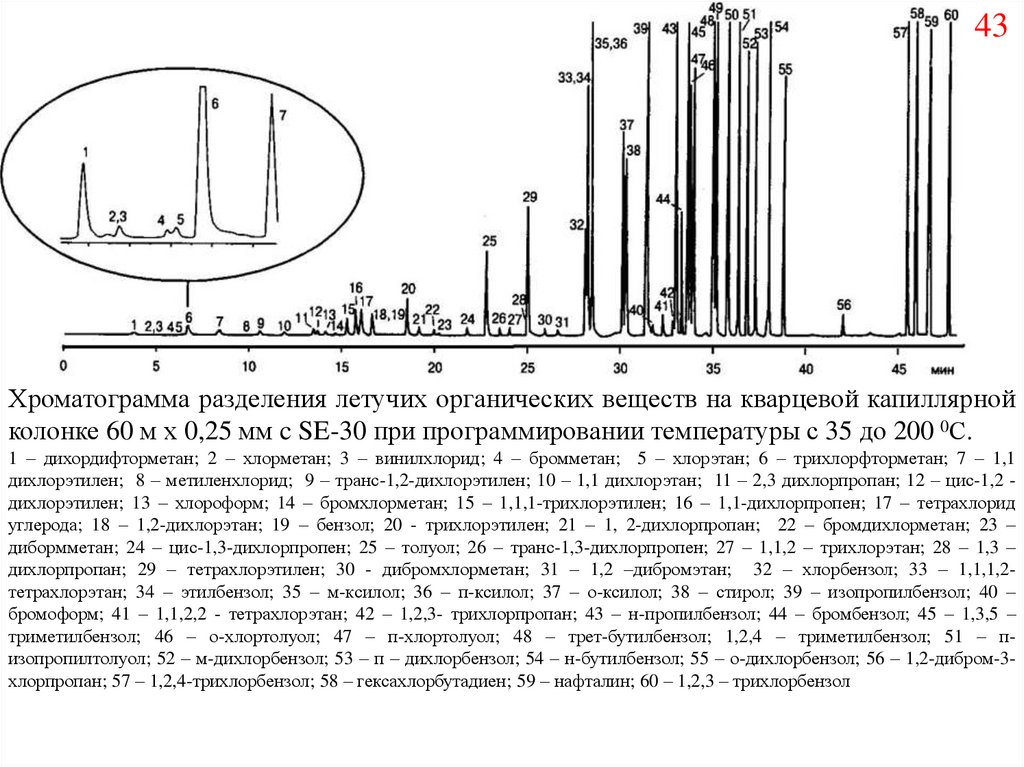
43.
43Хроматограмма разделения летучих органических веществ на кварцевой капиллярной
колонке 60 м х 0,25 мм c SE-30 при программировании температуры с 35 до 200 0С.
1 – дихордифторметан; 2 – хлорметан; 3 – винилхлорид; 4 – бромметан; 5 – хлорэтан; 6 – трихлорфторметан; 7 – 1,1
дихлорэтилен; 8 – метиленхлорид; 9 – транс-1,2-дихлорэтилен; 10 – 1,1 дихлорэтан; 11 – 2,3 дихлорпропан; 12 – цис-1,2 дихлорэтилен; 13 – хлороформ; 14 – бромхлорметан; 15 – 1,1,1-трихлорэтилен; 16 – 1,1-дихлорпропен; 17 – тетрахлорид
углерода; 18 – 1,2-дихлорэтан; 19 – бензол; 20 - трихлорэтилен; 21 – 1, 2-дихлорпропан; 22 – бромдихлорметан; 23 –
дибормметан; 24 – цис-1,3-дихлорпропен; 25 – толуол; 26 – транс-1,3-дихлорпропен; 27 – 1,1,2 – трихлорэтан; 28 – 1,3 –
дихлорпропан; 29 – тетрахлорэтилен; 30 - дибромхлорметан; 31 – 1,2 –дибромэтан; 32 – хлорбензол; 33 – 1,1,1,2тетрахлорэтан; 34 – этилбензол; 35 – м-ксилол; 36 – п-ксилол; 37 – о-ксилол; 38 – стирол; 39 – изопропилбензол; 40 –
бромоформ; 41 – 1,1,2,2 - тетрахлорэтан; 42 – 1,2,3- трихлорпропан; 43 – н-пропилбензол; 44 – бромбензол; 45 – 1,3,5 –
триметилбензол; 46 – о-хлортолуол; 47 – п-хлортолуол; 48 – трет-бутилбензол; 1,2,4 – триметилбензол; 51 – пизопропилтолуол; 52 – м-дихлорбензол; 53 – п – дихлорбензол; 54 – н-бутилбензол; 55 – о-дихлорбензол; 56 – 1,2-дибром-3хлорпропан; 57 – 1,2,4-трихлорбензол; 58 – гексахлорбутадиен; 59 – нафталин; 60 – 1,2,3 – трихлорбензол
44.
НЕДОСТАТКИ ТРАДИЦИОННОЙ КАПИЛЛЯРНОЙГАЗОВОЙ ХРОМАТОГРАФИИ
1. Необходимость дозирования очень малых объемов пробы
(менее 0,1 мкл жидкости)
2. Более низкая чувствительность анализа
3. Меньшая долговечность и меньшая воспроизводимость
параметров удерживания
44
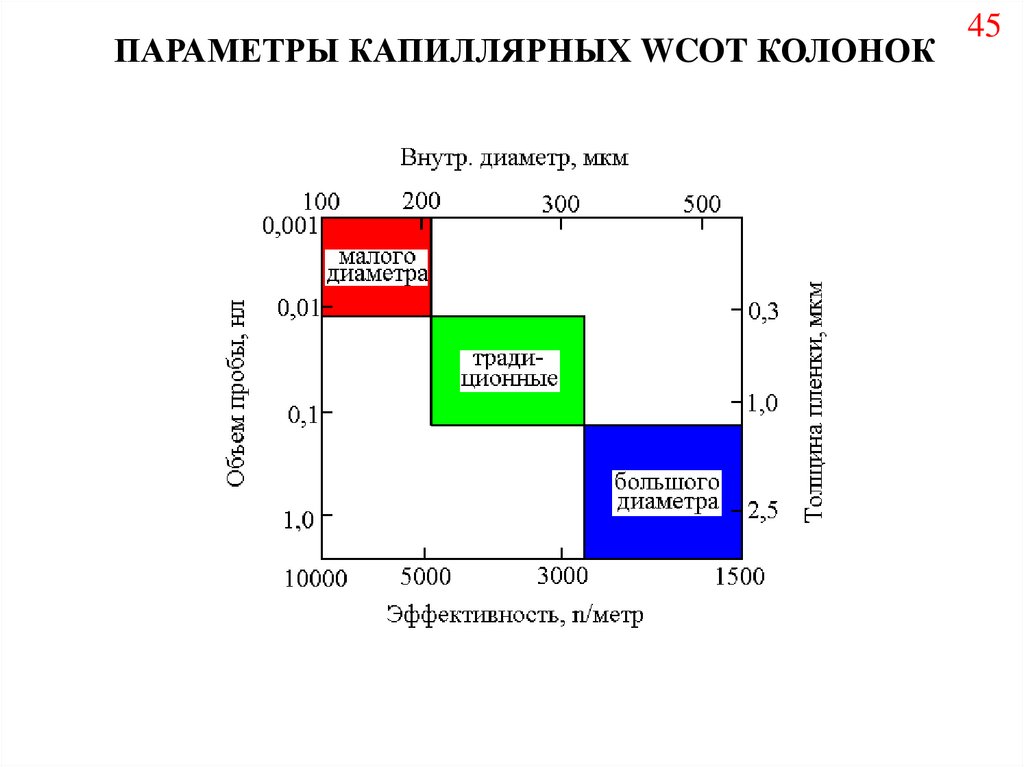
45.
ПАРАМЕТРЫ КАПИЛЛЯРНЫХ WCOT КОЛОНОК45
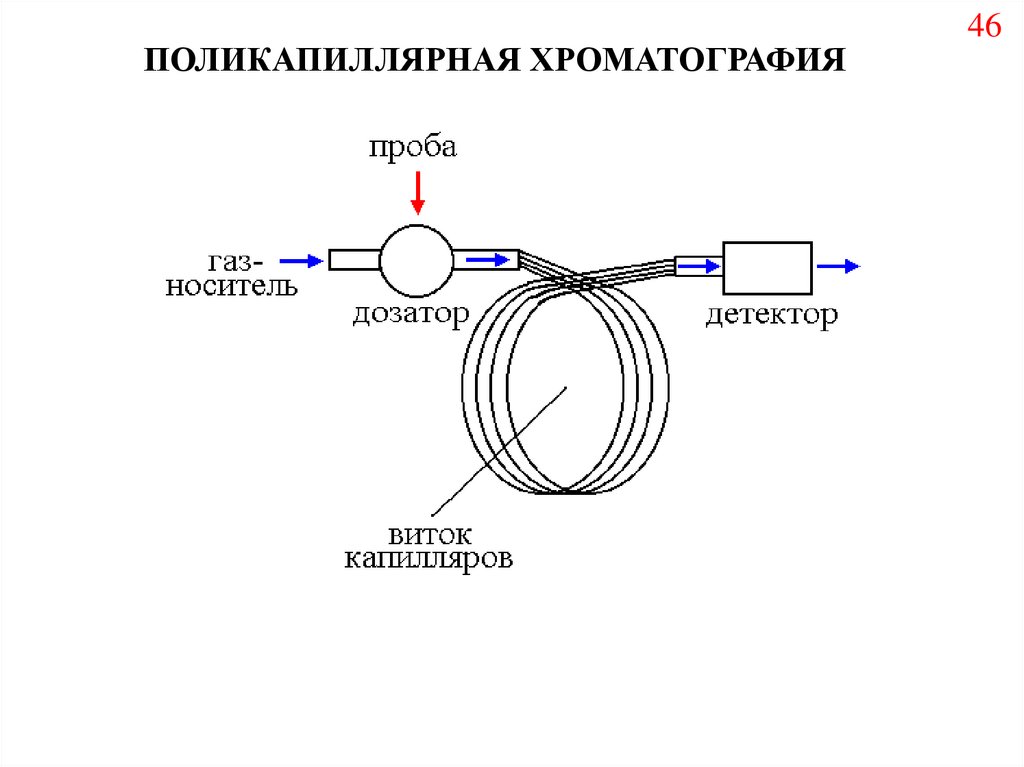
46.
ПОЛИКАПИЛЛЯРНАЯ ХРОМАТОГРАФИЯ46
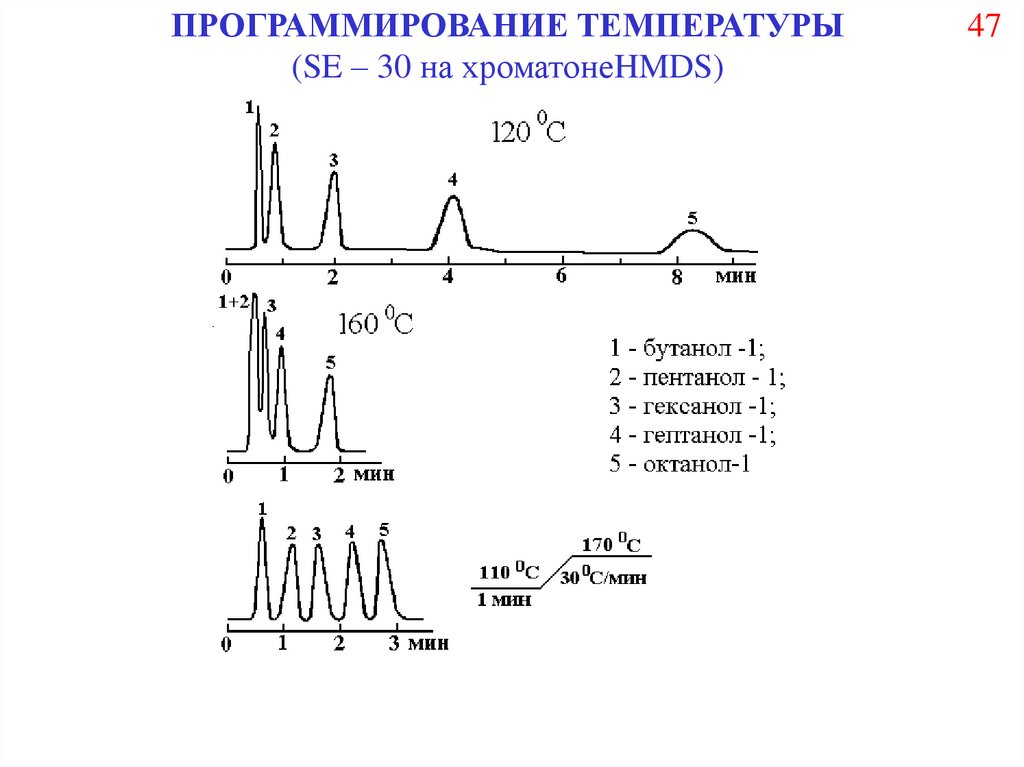
47.
ПРОГРАММИРОВАНИЕ ТЕМПЕРАТУРЫ(SE – 30 на хроматонеHMDS)
47
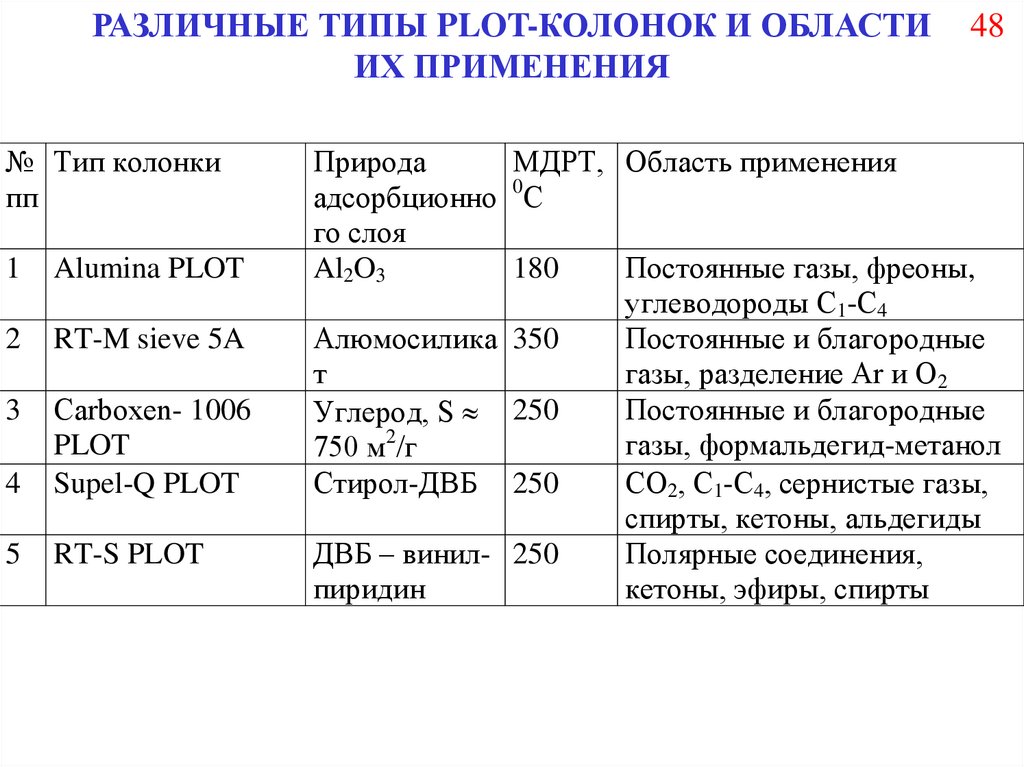
48.
РАЗЛИЧНЫЕ ТИПЫ PLOT-КОЛОНОК И ОБЛАСТИИХ ПРИМЕНЕНИЯ
№ Тип колонки
пп
1
Alumina PLOT
2
RT-M sieve 5A
3
4
Сarboxen- 1006
PLOT
Supel-Q PLOT
5
RT-S PLOT
48
Природа
МДРТ, Область применения
адсорбционно 0С
го слоя
Al2O3
180
Постоянные газы, фреоны,
углеводороды С1-С4
Алюмосилика 350
Постоянные и благородные
т
газы, разделение Ar и О2
Постоянные и благородные
Углерод, S 250
газы, формальдегид-метанол
750 м2/г
Cтирол-ДВБ 250
СО2, С1-С4, сернистые газы,
спирты, кетоны, альдегиды
ДВБ – винил- 250
Полярные соединения,
пиридин
кетоны, эфиры, спирты
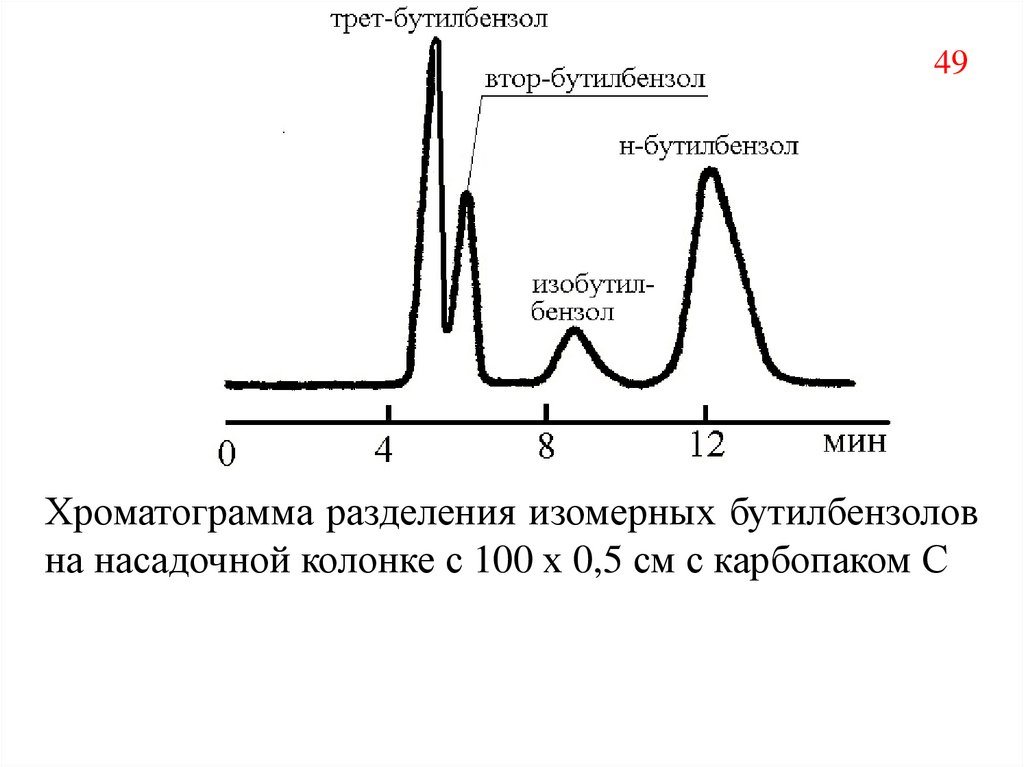
49.
49Хроматограмма разделения изомерных бутилбензолов
на насадочной колонке с 100 х 0,5 см с карбопаком С
50.
ХРОМАТОГРАММЫ МЕТИЛОВЫХ ЭФИРОВКИСЛОТ
ЖИРНЫХ
50
Традиционная хроматография
30 м х 0,25 мм х 0,2 мкм
v = 30 см/c
Быстрая хроматография
10 м х 0,1 мм х 0,1 мкм
v = 40 см/c
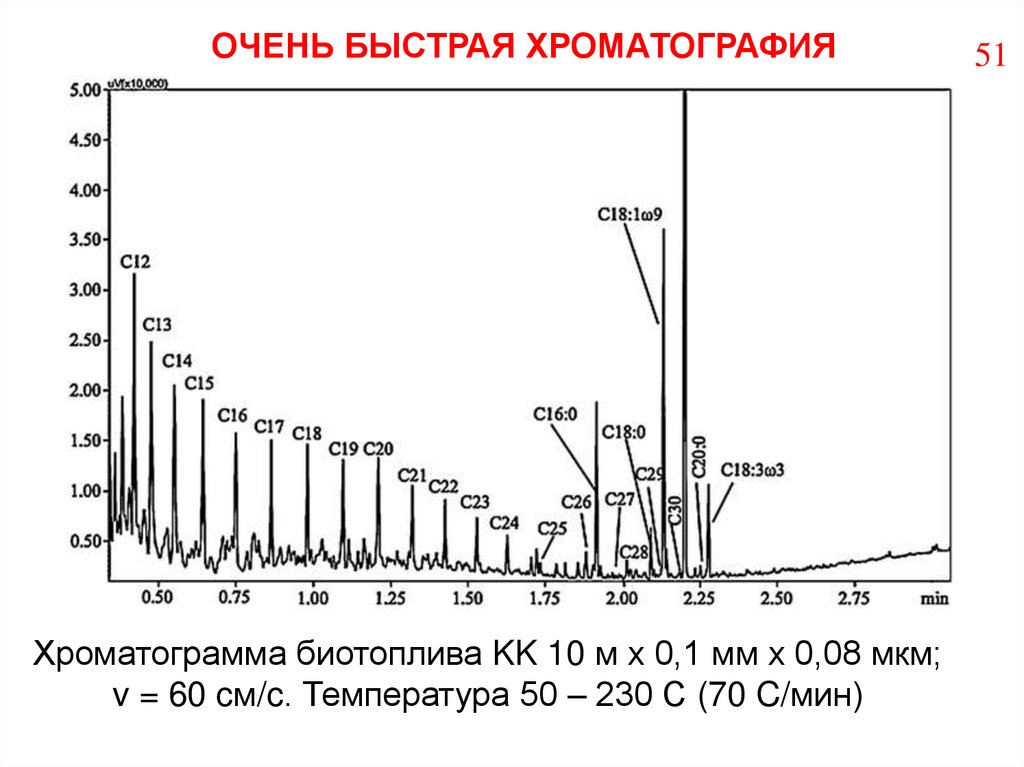
51.
ОЧЕНЬ БЫСТРАЯ ХРОМАТОГРАФИЯХроматограмма биотоплива KK 10 м х 0,1 мм х 0,08 мкм;
v = 60 cм/c. Температура 50 – 230 С (70 C/мин)
51
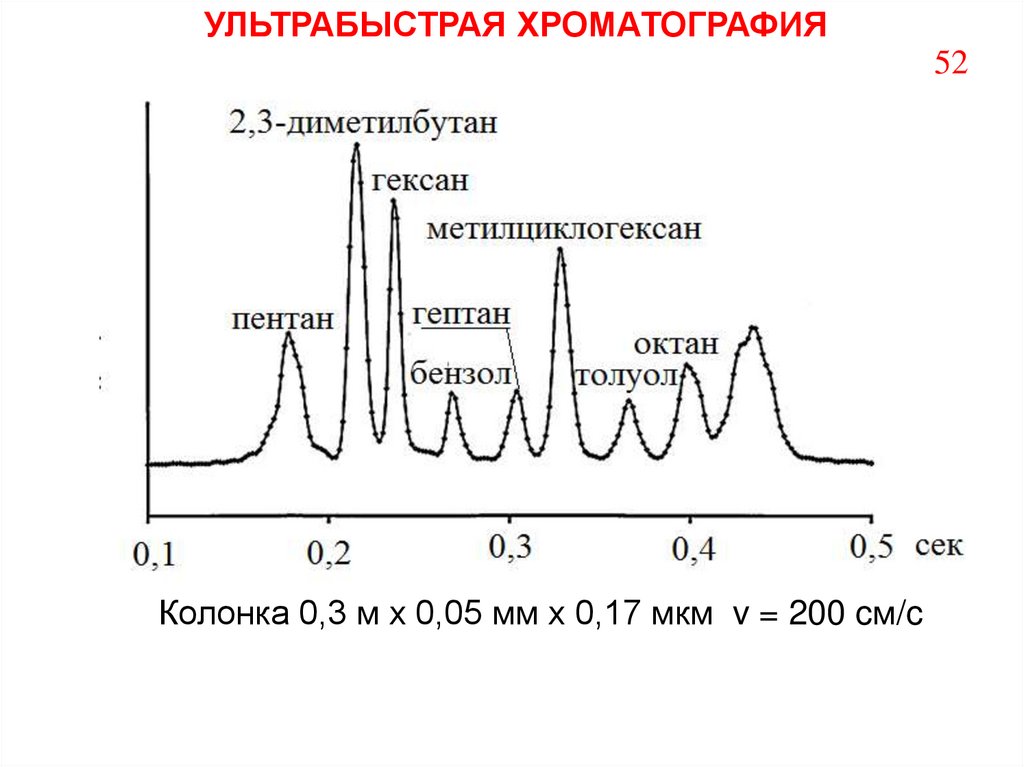
52.
УЛЬТРАБЫСТРАЯ ХРОМАТОГРАФИЯ52
Колонка 0,3 м х 0,05 мм х 0,17 мкм v = 200 cм/c
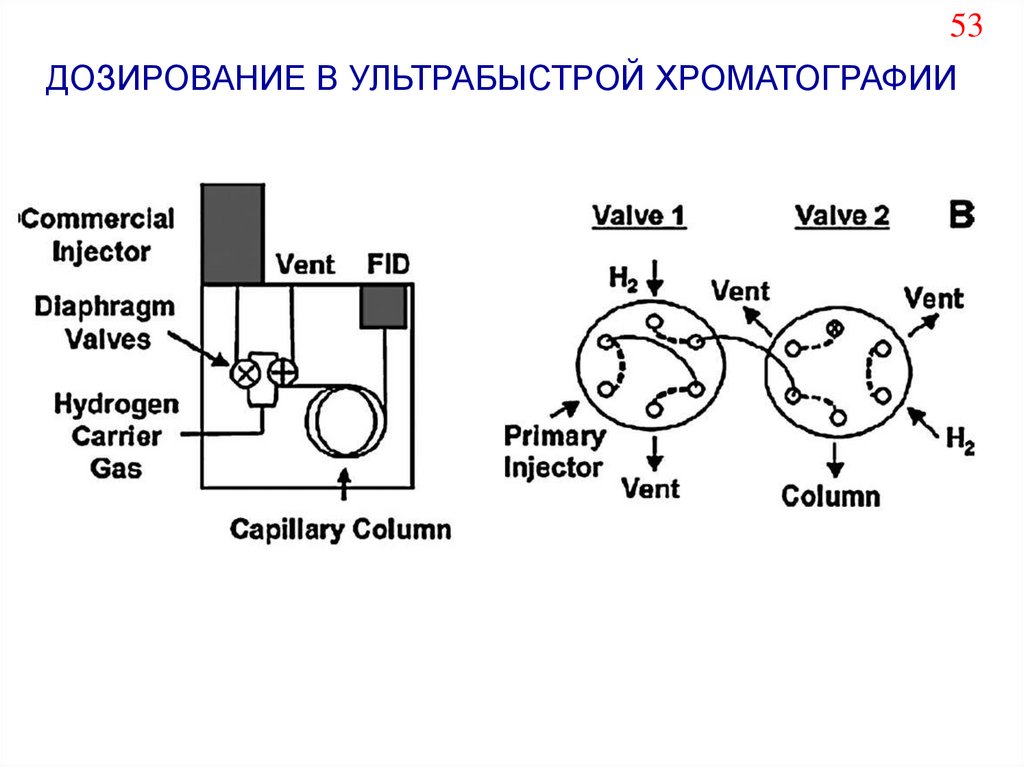
53.
53ДОЗИРОВАНИЕ В УЛЬТРАБЫСТРОЙ ХРОМАТОГРАФИИ
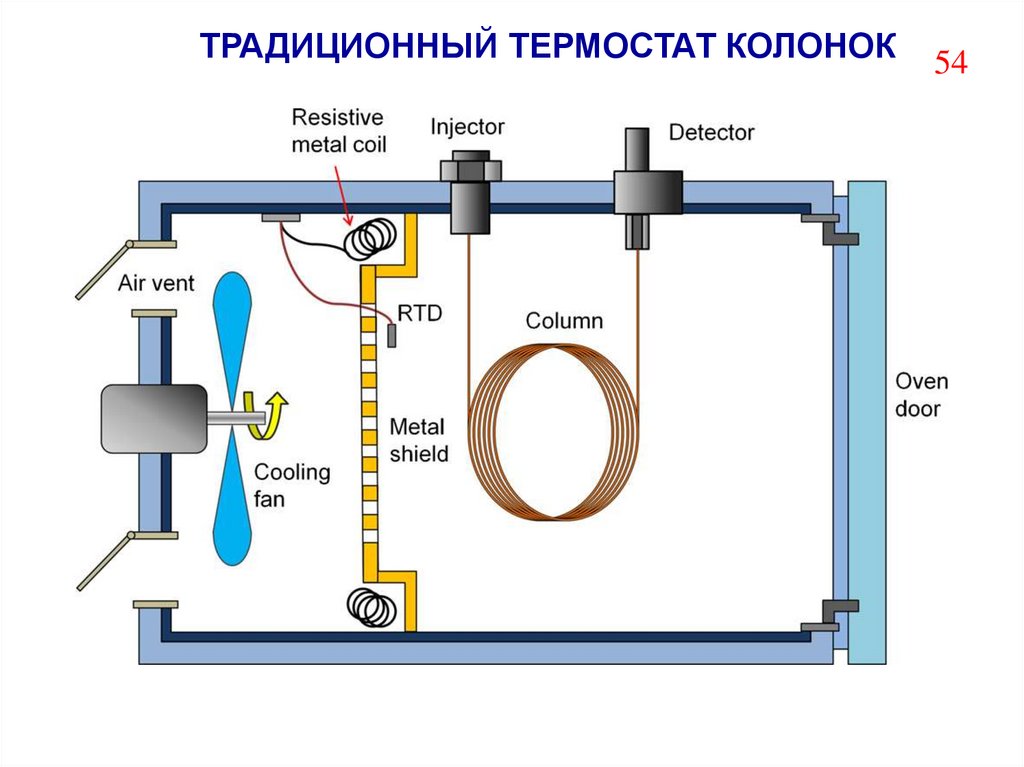
54.
ТРАДИЦИОННЫЙ ТЕРМОСТАТ КОЛОНОК54
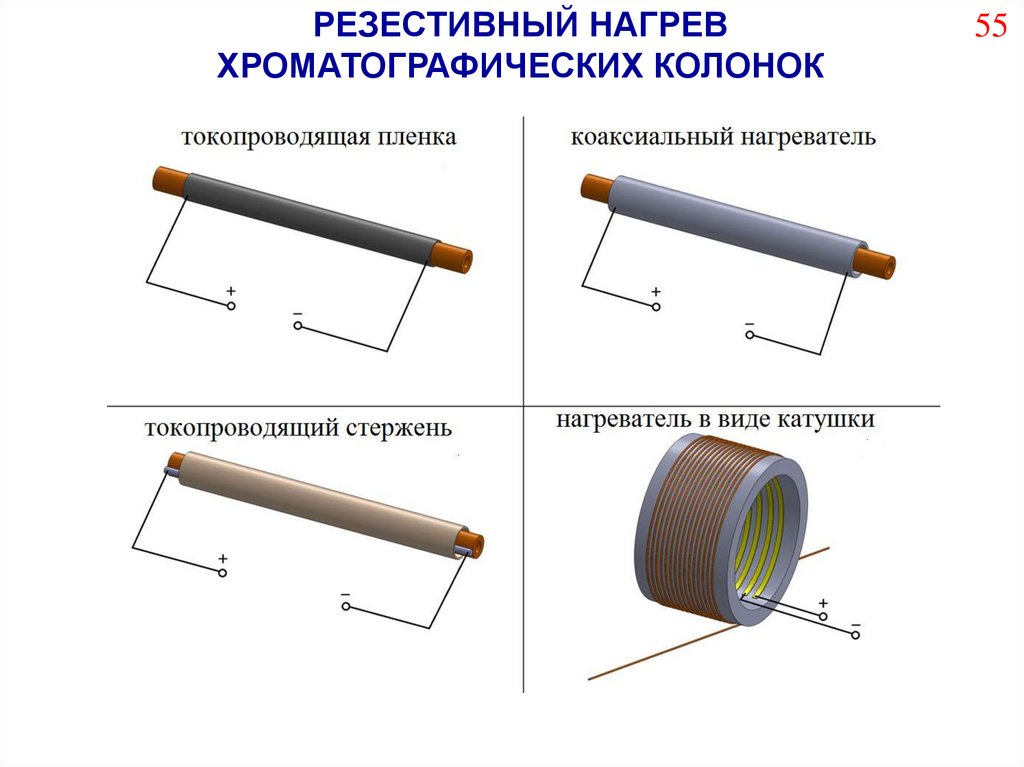
55.
РЕЗЕСТИВНЫЙ НАГРЕВХРОМАТОГРАФИЧЕСКИХ КОЛОНОК
55
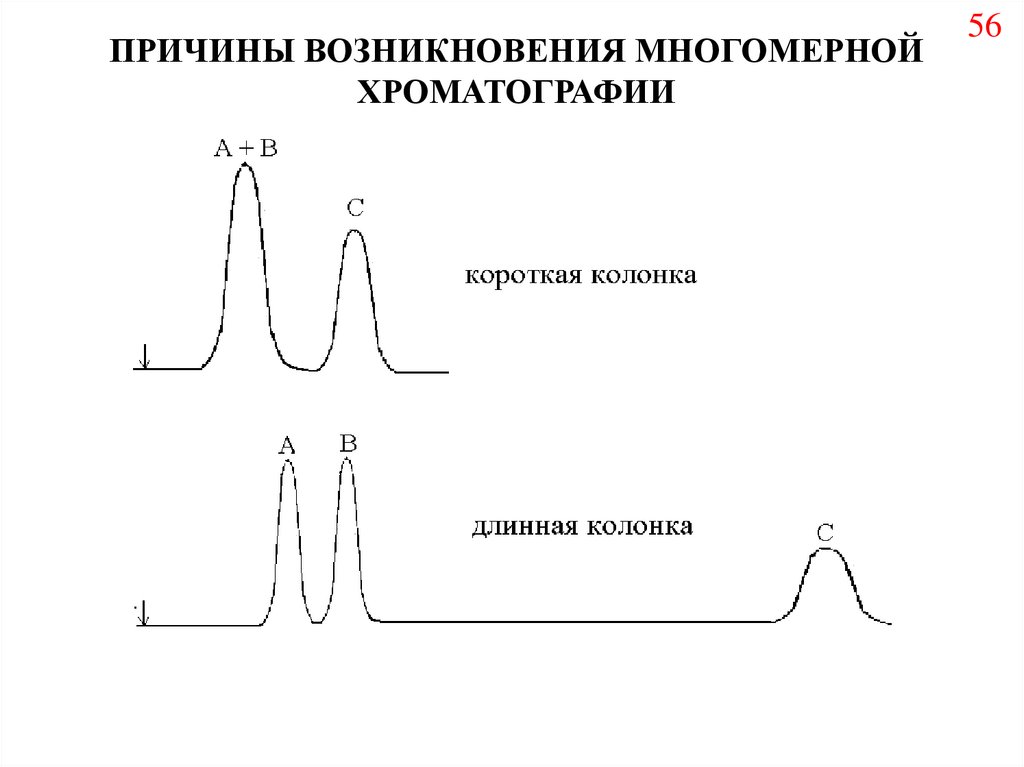
56.
ПРИЧИНЫ ВОЗНИКНОВЕНИЯ МНОГОМЕРНОЙХРОМАТОГРАФИИ
56
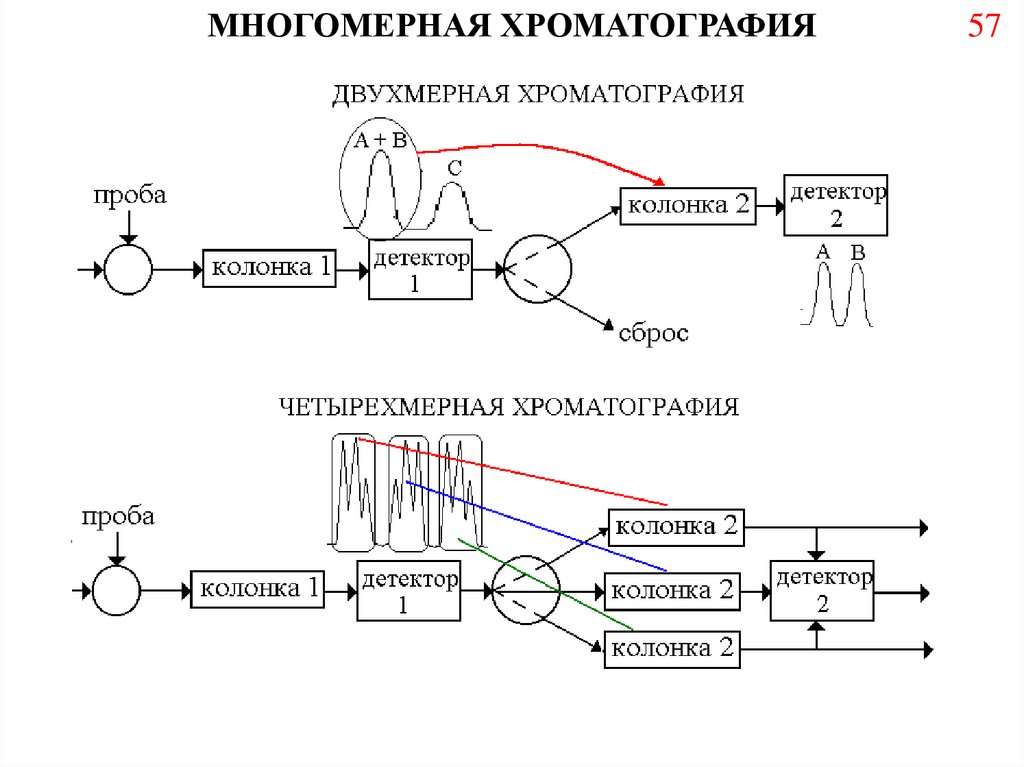
57.
МНОГОМЕРНАЯ ХРОМАТОГРАФИЯ57
58.
ПИРОЛИЗНАЯ ГАЗОВАЯ ХРОМАТОГРАФИЯ58
Пиролизная (пиролитиенчская) хроматография – гибридный метод анализа,
включающий термическое разложение пробы без доступа воздуха и
последующее газохроматографическое определение получаемых продуктов
Основные объекты анализа
полимеры; лаки, краски, тяжелые нефтепродукты, типа
гудронов, фармацевтические продукты и микроорганизмы
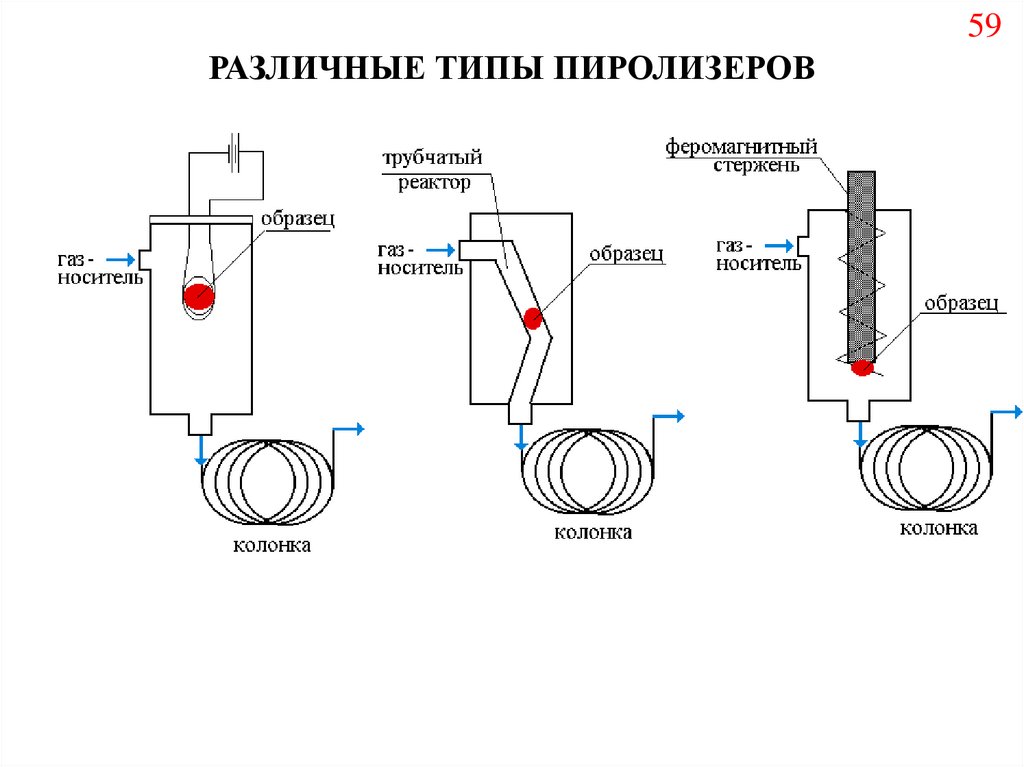
Требования, предъявляемые к пиролизерам
1) Точная установка и поддержание заданной температуры;
2) Полное удаление остатков предыдущей пробы;
3) Высокая герметичность, исключение попадание воздуха;
4) Непрерывный поток газа-носителя через пиролизер
59.
59РАЗЛИЧНЫЕ ТИПЫ ПИРОЛИЗЕРОВ
60.
ТЕМПЕРАТУРНЫЕ РЕЖИМЫ ПИРОЛИЗАТемпература
Название
процесса
200 – 400 0С Термическое
разложение
400 – 500 0С Мягкий пиролиз
60
Характеристика
Образующиеся продукты по молярной
массе не сильно отлучаются от исходных
Чаще всего используется для анализа
биологических объектов: аминокислот,
белков, крахмала, бактерий
500 – 800 0С Средний пи- Анализ полимеров. Определение струкролиз
туры химически инертных полимеров.
Образуется до 20-50 компонентов.
800 – 1100 Жесткий пи- Происходит разрыв связей углерод – уг0
С
ролиз
лерод.Образуется более 100 компонентов.
Сложность интерпретации.
61.
ОБРАЩЕННАЯ ГАЗОВАЯ ХРОМАТОГРАФИЯ61
62.
62ОБЛАСТИ ПРИМЕНЕНИЯ ОБРАЩЕННОЙ ГХ
1) Определение температур стеклования и плавления полимеров
2) Определение степени кристалличности полимеров и изучение
кинетики их кристаллизации
3) Определение коэффициентов активности и
термодинамических параметров (свободной энергии,
энтальпии и энтропии) взаимодействия полимер растворитель
А.Е. Нестеров Обращенная газовая хроматография. Киев. Наукова
думка. 1988. 184 с.





















 Физика
Физика








