Похожие презентации:
Фотометрия. Клинический спектрофотометр
1.
2.
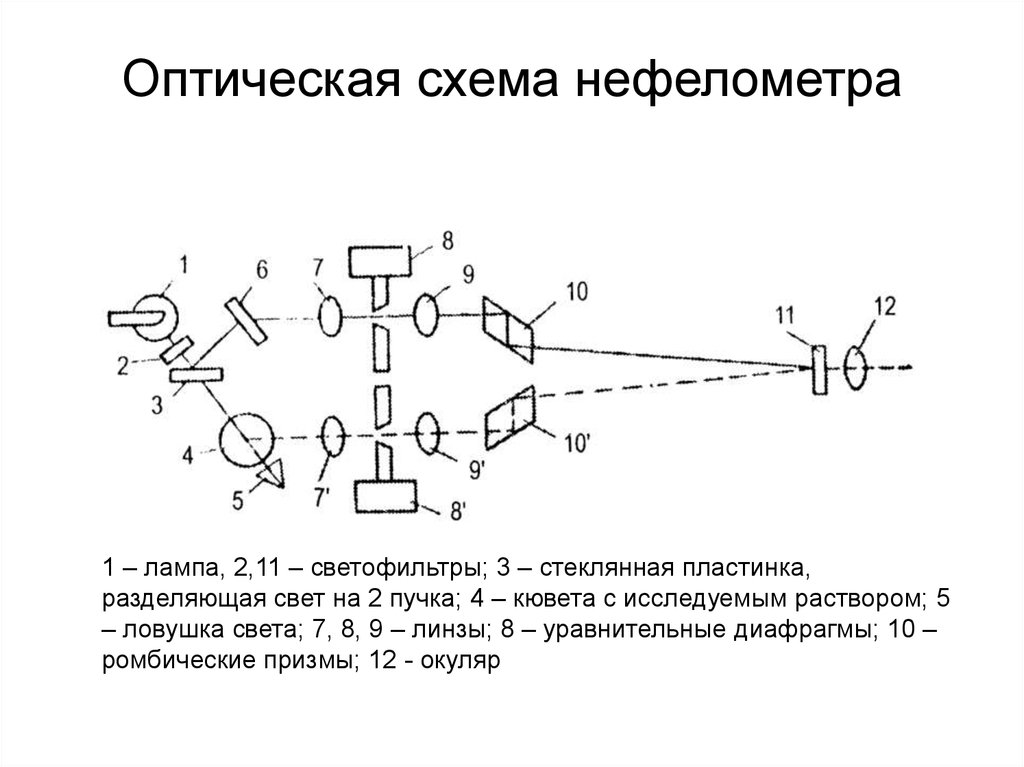
3. Оптическая схема нефелометра
1 – лампа, 2,11 – светофильтры; 3 – стеклянная пластинка,разделяющая свет на 2 пучка; 4 – кювета с исследуемым раствором; 5
– ловушка света; 7, 8, 9 – линзы; 8 – уравнительные диафрагмы; 10 –
ромбические призмы; 12 - окуляр
4. Схема пламенного фотометра
1 – цилиндры с топливом и воздухом; 2 – клапаны регуляции давления иустройства для измерения расхода газов; распылительная камера; 6 –
устройство для осушения распылительной камеры, 7 – фокусирующая линза;
входная щель монохроматора; 9 – призма, разделяющая свет по длине волны;
10 – выходая щель монохроматора; 11 - фотодетектор
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
15. КЛИНИЧЕСКИЙ СПЕКТРОФОТОМЕТР
16.
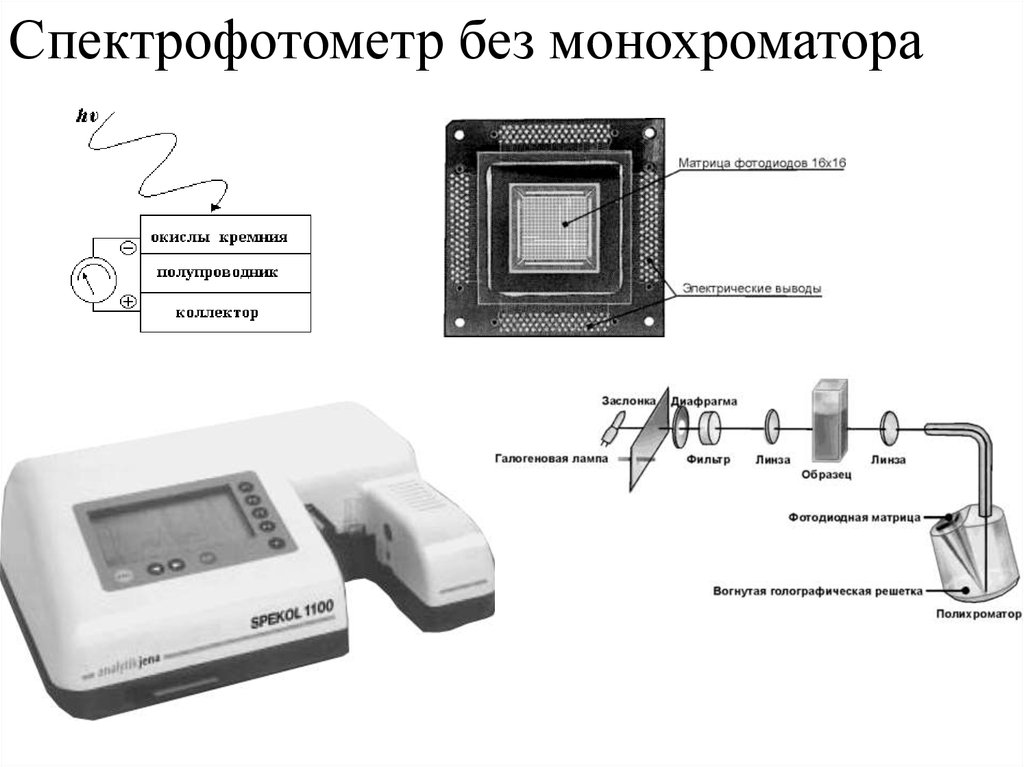
Спектрофотометр без монохроматора17. Кормей-мульти – программируемый фотометр с проточной кюветой
18.
АСпектры поглощения
НАД+ и НАД Н
длина волны
250
340
19. Сопряженные реакции
АЛТАланин + -КГ
Пируват + Глутамат
ЛДГ
Пируват + НАДН
КК
КФ + АДФ
КК
Лактат + НАД
Креатин + АТФ
гексокиназа
АТФ + глюкоза
Гл-6-Ф + НАДН
АДФ + Гл-6-Ф
Гл-6-ФДГ
6-ФГ + НАД
20. Фотометрические методы анализа
21.
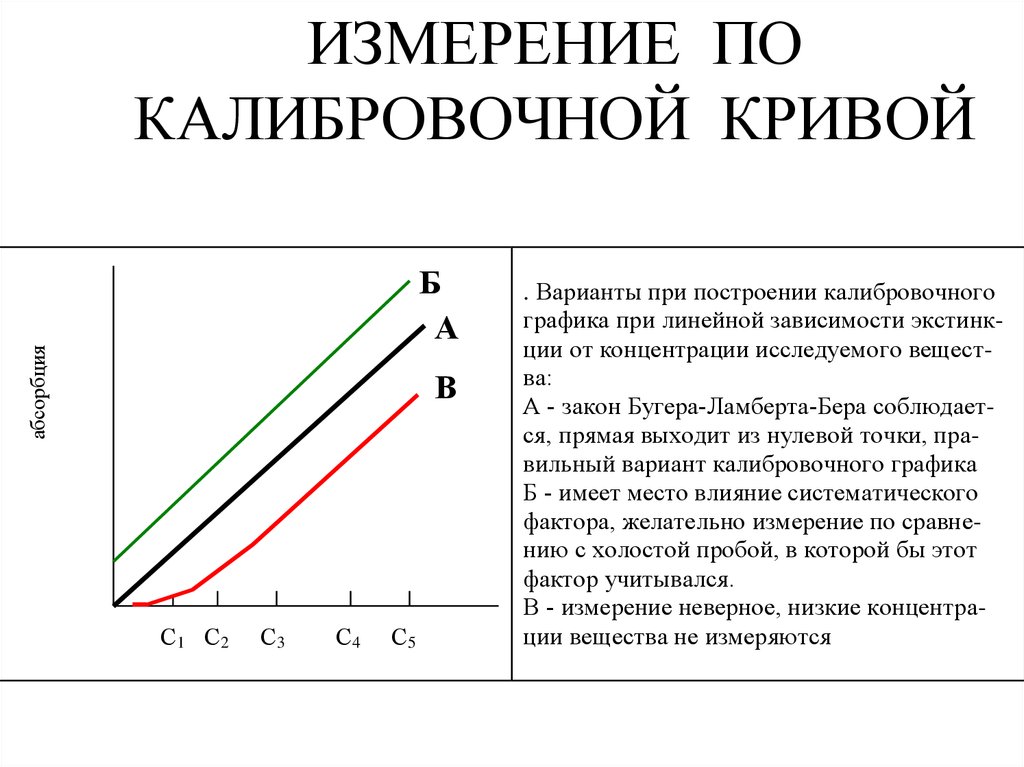
ИЗМЕРЕНИЕ ПОКАЛИБРОВОЧНОЙ КРИВОЙ
абсорбция
Б
А
В
С1 С2
С3
С4
С5
. Варианты при построении калибровочного
графика при линейной зависимости экстинкции от концентрации исследуемого вещества:
А - закон Бугера-Ламберта-Бера соблюдается, прямая выходит из нулевой точки, правильный вариант калибровочного графика
Б - имеет место влияние систематического
фактора, желательно измерение по сравнению с холостой пробой, в которой бы этот
фактор учитывался.
В - измерение неверное, низкие концентрации вещества не измеряются
22. Методы сравнения стандартного и опытного образца
• Анализируемая и стандартная пробаобрабатываются в одинаковых условиях
• При больших сериях – стандартную пробу
исследовать в начале серии и через каждые
20 проб
• Расчет ведут по ствндарту или по фактору
• Расчет по стандарту: Сi = Di х Cст/Dст
• Расчет по фактору: С = D х F
23. Методы определения без использования калибратора
• Фотометрические единицы (в случаеотсутствия калибратора – средние
молекулы, серомукоид) – оптическую
плотность умножают на 100
• (D = 0,3, ответ – 30 единиц)
24. Методы определения без использования калибратора
• Определение концентрации по молярномупоказателю поглощения – применение закона
Бургера
С = D/lхξ (концентрация определяется
делением измеренной оптической
плотности на известный для данного
вещества молярный показатель
поглощения при длине волны измерения: С =
D/ξ)
Учитывать разведение образца
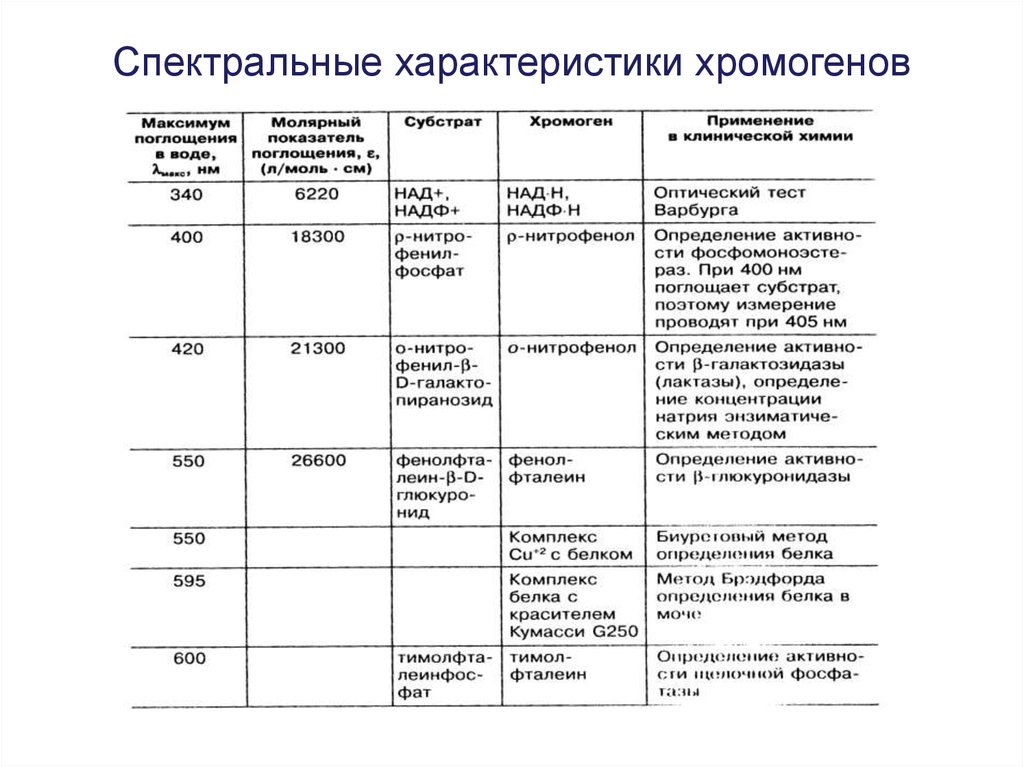
25. Спектральные характеристики хромогенов
26. Примеры:
Определение концентрации НАДН на основе определения
оптической плотности
Молярный показатель НАДН при 340 нм 6,22х10 3 лхмоль -1см-1. (ввести
верхний символ). Измерена оптическая плотность в 1 см кювете – 0,38
Концентрация НАДН определяется по соотношению
Определение содержания гемоглобина гемоглобинцианидным методом
Милимолярный коэффициент при 540 нм = 11
Молекулярная масса гемоглобина – 64458, состоит из 4 суъединицю
Эквивалентный вес Hb = 16114, т.е. 1 моль соответствует 16,114 Hb в крови
Кровь разводят трансформирующим раствором 1:251 (0,02 мл крови + 5,0 мл
трансформирующего раствора)
27.
28. Измерение по конечной точке
Конечная точкаАбсорбция
буфер
проба
реактив
А = Аобщ – Абланка
Бланк по рабочему
раствору
Бланк по кювете
время
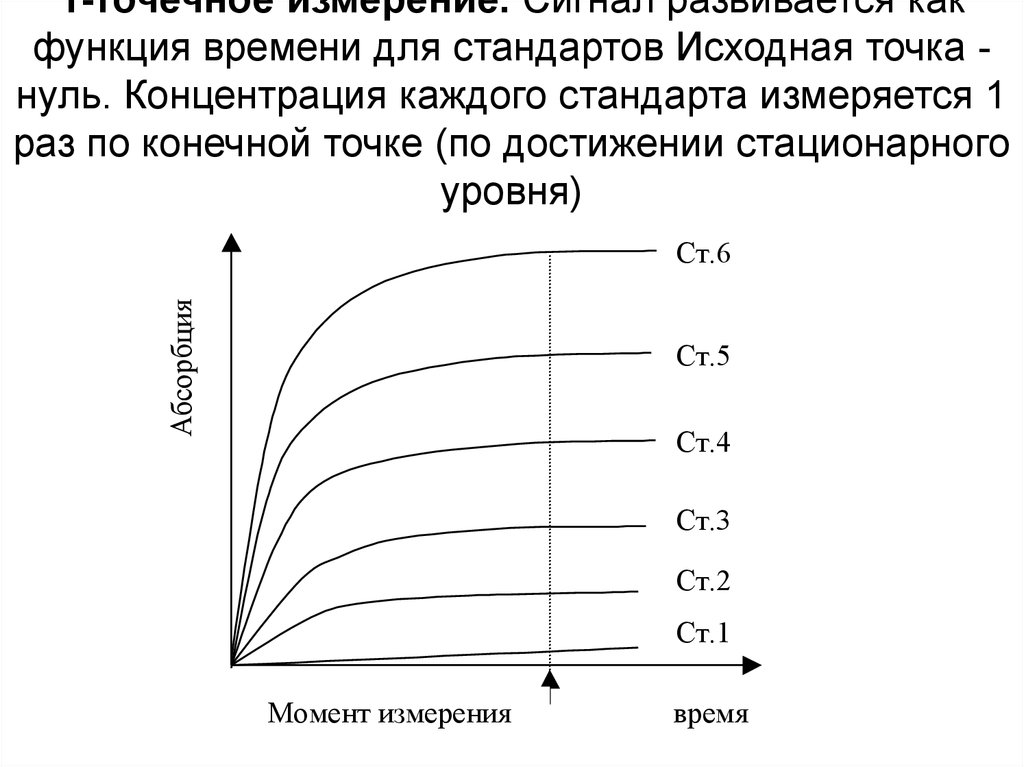
29. 1-точечное измерение. Сигнал развивается как функция времени для стандартов Исходная точка - нуль. Концентрация каждого
1-точечное измерение. Сигнал развивается какфункция времени для стандартов Исходная точка нуль. Концентрация каждого стандарта измеряется 1
раз по конечной точке (по достижении стационарного
уровня)
Абсорбция
Ст.6
Ст.5
Ст.4
Ст.3
Ст.2
Ст.1
Момент измерения
время
30. Измерение по кинетике
А - скорость постоянна, в любой период можно по скорости реакции оцениватьактивность фермента, Б - скорость реакции постоянно снижается, рекомендуется
активность фермента оценивать по начальной скорости, В - линейный участок, на
котором рекомендуется определять активность фермента, устанавливается в середине
периода инкубации
А
Б
В
абсорбция
Начальная
скорость
Lag
фаза
время
31.
Кинетическое измерение требуетобеспечения наряду с фотометрическим
адекватным обеспечением, также
точного поддержания температуры в
измерительной кювете и правильного
отсчета временных интервалов. Так,
общепринятым считается поддержание
температуры в измерительной ячейке в
пределах 0,1 оС
32. Волоконный световод минимизирует оптическую схему
33. Спектр поглощения производных гемоглобина
спектры поглощения производных гемоглобина: 1 – дезоксигемоглобина (HbH); 2 –карбоксигемоглобина (HbCO) 3 – оксигемоглобина (HbO2); 4 – метгемоглобина (MetHb).
34.
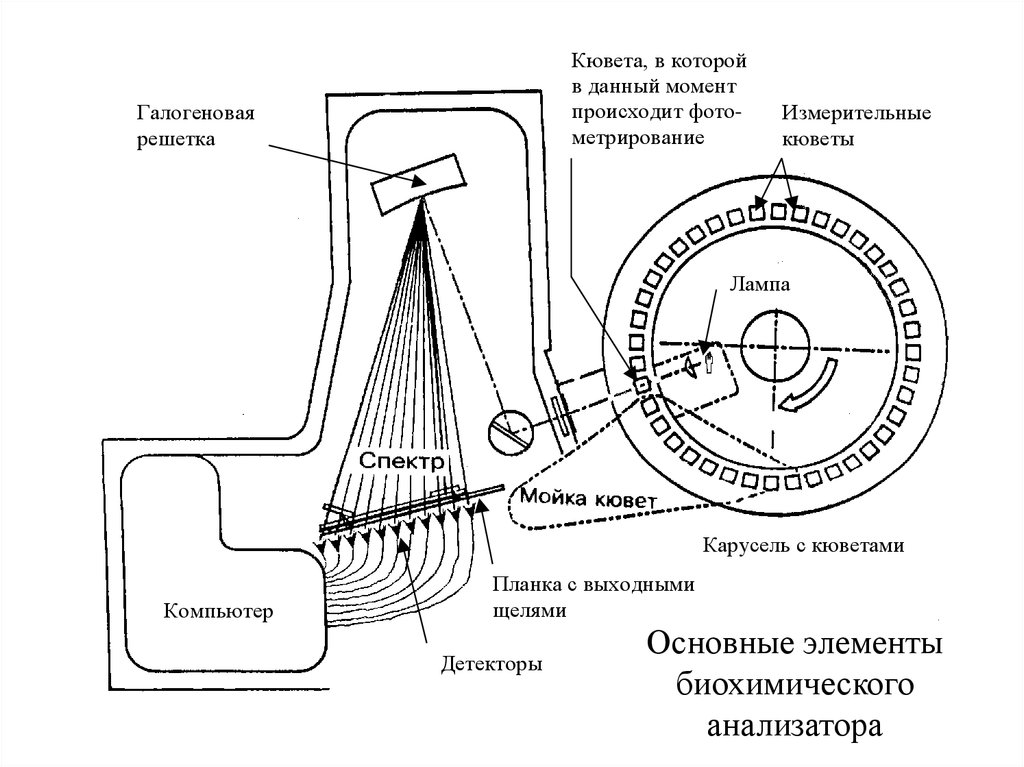
Кювета, в которойв данный момент
происходит фотометрирование
Галогеновая
решетка
Измерительные
кюветы
Лампа
Карусель с кюветами
Компьютер
Планка с выходными
щелями
Детекторы
Основные элементы
биохимического
анализатора
35.
Состоявшееся решение - укрепить оснащенность ЛПУоборудованием, в т.ч. лабораторным
А) создан табель оснащения КДЛ
Б) из Федерального Фонда выделены средства на
закупку оборудования
В) проведен тендер на закупку 4 комплектов
(ЛОТов) лабораторного оборудования
Г) на основании заявок с территорий составлен
реестр распределения оборудования






















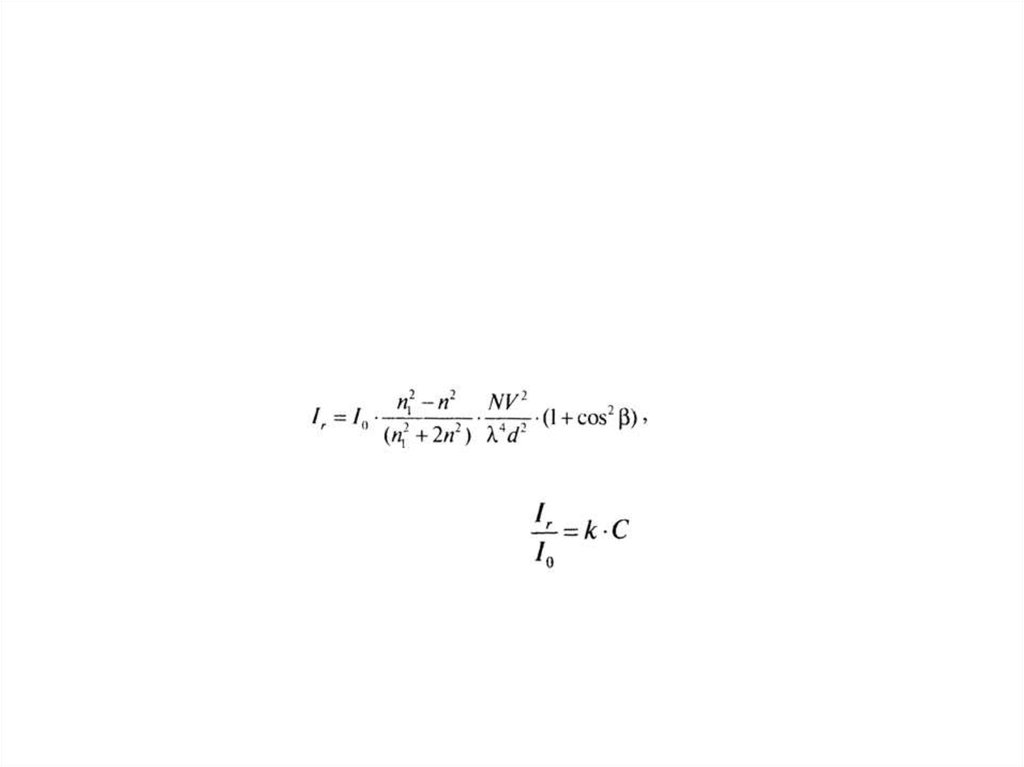






 Медицина
Медицина Физика
Физика








