Похожие презентации:
Анодное растворение mn5si3-электрода в сернокислом фторидсодержащем электролите
1. АНОДНОЕ РАСТВОРЕНИЕ Mn5Si3-ЭЛЕКТРОДА В СЕРНОКИСЛОМ ФТОРИДСОДЕРЖАЩЕМ ЭЛЕКТРОЛИТЕ
«Пермский государственный национальный исследовательский университет»Полковников Игорь Сергеевич
АНОДНОЕ РАСТВОРЕНИЕ Mn5Si3-ЭЛЕКТРОДА
В СЕРНОКИСЛОМ ФТОРИДСОДЕРЖАЩЕМ ЭЛЕКТРОЛИТЕ
Научный руководитель:
д.х.н., профессор
Шеин Анатолий Борисович
Пермь - 2017
2.
2Цель работы: установление кинетических закономерностей анодного
поведения
Mn5Si3-электрода
в
сернокислом
бесфторидном
и
фторидсодержащем электролитах, выяснение механизмов растворения и
пассивации силицида, определение роли металла и кремния в кинетике
анодных процессов
Задачи работы:
Исследовать анодное поведение силицида марганца в растворе серной кислоты методами
поляризационных и импедансных измерений. Установить кинетику и механизмы
процессов, протекающих на Mn5Si3 при потенциалах характерных участков его анодной
поляризационной кривой
Определить влияние фторида натрия на электрохимическое поведение силицида
марганца в сернокислой среде. Выяснить механизмы воздействия фтороводородной
кислоты на анодное поведение Mn5Si3 в зависимости от величины электродной
поляризации и концентрации фторида.
Изучить морфологию поверхности Mn5Si3 после анодного травления в растворе серной
кислоты и растворе, содержащем NaF
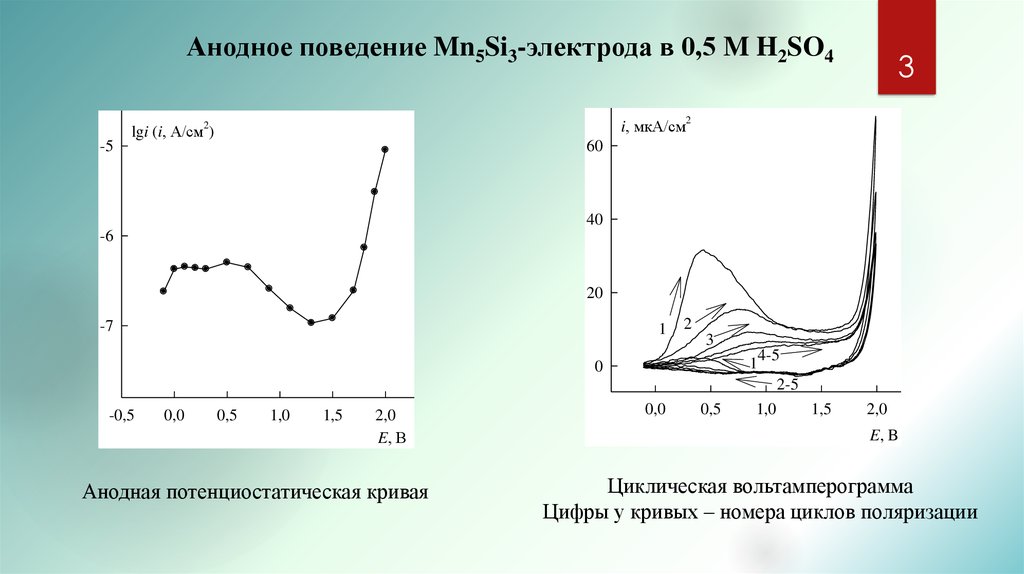
3. Анодное поведение Mn5Si3-электрода в 0,5 M H2SO4
i, мкА/см2
lgi (i, А/см )
3
2
60
-5
40
-6
20
-7
1
2
3
1
0
4-5
2-5
-0,5
0,0
0,5
1,0
1,5
2,0
E, В
Анодная потенциостатическая кривая
0,0
0,5
1,0
1,5
2,0
E, B
Циклическая вольтамперограмма
Цифры у кривых – номера циклов поляризации
4.
Потенциодинамические кривые Mn5Si3-электрода в 0,5 M H2SO4400
i, мкА/см2
200 мВ/с
iкp = k1ν+k2ν1/2
k1ν – поверхностные процессы
k2ν1/2 – диффузионные процессы
150 мВ/с
300
2
-3,5
lgiкр (iкр, А/см )
100 мВ/с
200
iкp = kνx
-4,0
50 мВ/с
30 мВ/с
20 мВ/с
10 мВ/с
5 мВ/с
100
0
0,0
0,5
1,0
1,5
2,0
Е, В
4
x = 0,84
-4,5
-2,0
-1,5
-1,0
lg ( , В/с)
5. Анодное поведение Mn5Si3-электрода в 0,5 M H2SO4
Электродные процессы:2
lgi (i, А/см )
А1-А3
-6
А1
А2
А1
А3
0,0
0,5
1,0
1,5
lgi
Si + 2H2O = SiO2 + 4H+ + 4e–
20
1
Mn(v) → Mn(s),
Mn(s) = Mn2+ + 2e–
K = -0,95
15
0
А2
-7
-0,5
i, мкА/см2
25
-5
5
2,0
E, В
Mn + H2O = MnO + 2H+ + 2e–
10
Mn2O3 + H2O = 2MnO2 + 2H+ + 2e–
А3 Mn2+ + 2H O = MnO + 4H+ + 2e–
2
2
2Mn2+ + 3H2O = Mn2O3 + 6H+ + 2e–
Анодная потенциостатическая кривая
5
-1
0
1
2
3 lgt
0
0
500
1000
1500
t, c
Хроноамперограмма при E = -0,1 В
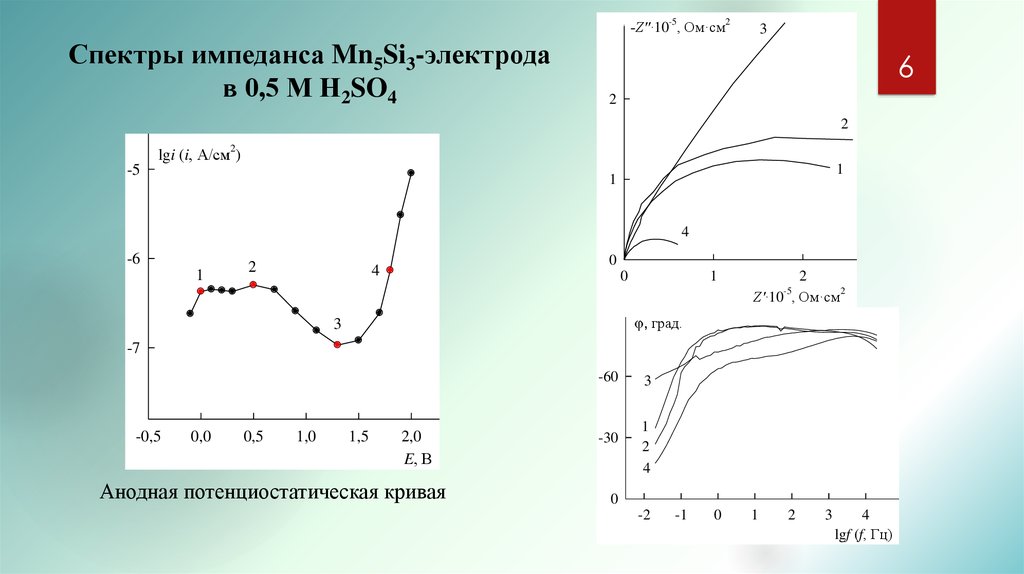
6. Спектры импеданса Mn5Si3-электрода в 0,5 М Н2SO4
3Спектры импеданса Mn5Si3-электрода
в 0,5 М Н2SO4
-5
-Z''·10 , Ом·см
2
3
6
2
2
2
lgi (i, А/см )
-5
1
1
4
-6
1
2
0
4
0
1
2
-5
2
Z'·10 , Ом·см
0
1
, град.
3
-7
-60
-0,5
0,0
0,5
1,0
1,5
2,0
E, В
Анодная потенциостатическая кривая
-30
3
1
2
4
0
-2
-1
2
3
4
lgf (f, Гц)
7. Зависимость толщины оксидной пленки на Mn5Si3-электроде от потенциала
Ki = dd/dE , нм/Вd, нм
1,0
K2 = 0,37 нм/В
0,8
K1 = 0,68 нм/В
0,6
0,0
0,5
1,0
1,5
2,0
E, В
KSi = (0,4 – 0,7) нм/В
7
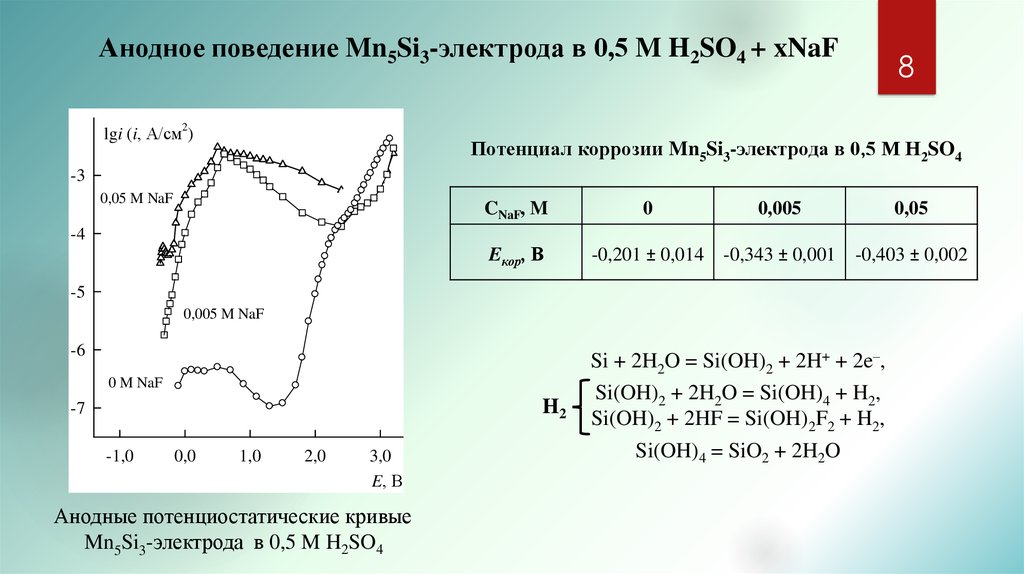
8. Анодное поведение Mn5Si3-электрода в 0,5 M H2SO4 + xNaF
82
lgi (i, А/см )
Потенциал коррозии Mn5Si3-электрода в 0,5 M H2SO4
-3
0,05 M NaF
CNaF, M
0
0,005
0,05
Eкор, В
-0,201 ± 0,014
-0,343 ± 0,001
-0,403 ± 0,002
-4
-5
0,005 M NaF
-6
0 M NaF
H2
-7
-1,0
0,0
1,0
2,0
3,0
E, В
Анодные потенциостатические кривые
Mn5Si3-электрода в 0,5 M H2SO4
Si + 2H2O = Si(OH)2 + 2H+ + 2e–,
Si(OH)2 + 2H2O = Si(OH)4 + H2,
Si(OH)2 + 2HF = Si(OH)2F2 + H2,
Si(OH)4 = SiO2 + 2H2O
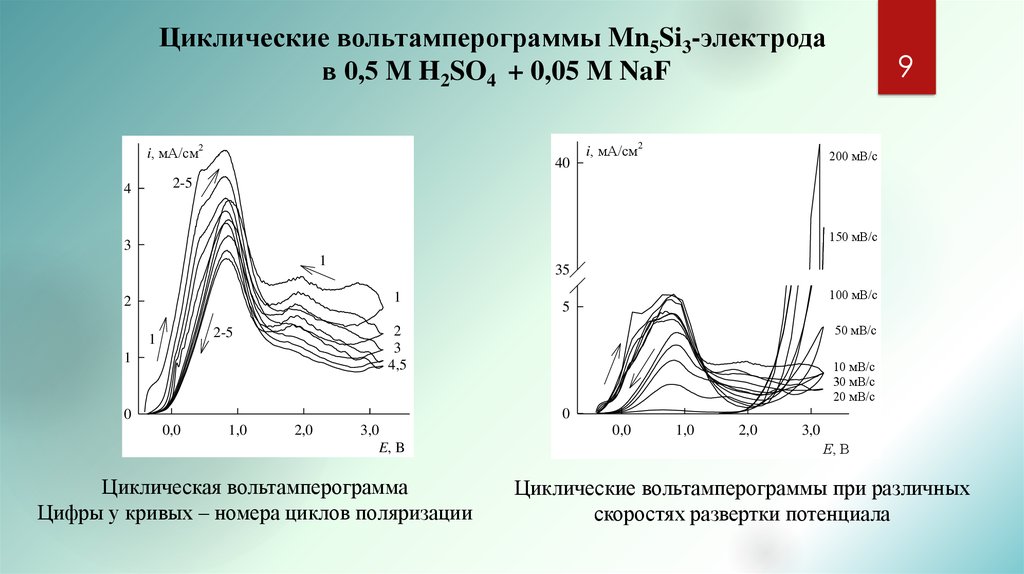
9. Циклические вольтамперограммы Mn5Si3-электрода в 0,5 M H2SO4 + 0,05 M NaF
i, мА/см2
40
i, мА/см2
9
200 мВ/с
2-5
4
150 мВ/с
3
1
35
1
2
50 мВ/с
2
3
4,5
2-5
1
100 мВ/с
5
1
10 мВ/с
30 мВ/с
20 мВ/с
0
0
0,0
1,0
2,0
3,0
E, B
Циклическая вольтамперограмма
Цифры у кривых – номера циклов поляризации
0,0
1,0
2,0
3,0
Е, В
Циклические вольтамперограммы при различных
скоростях развертки потенциала
10.
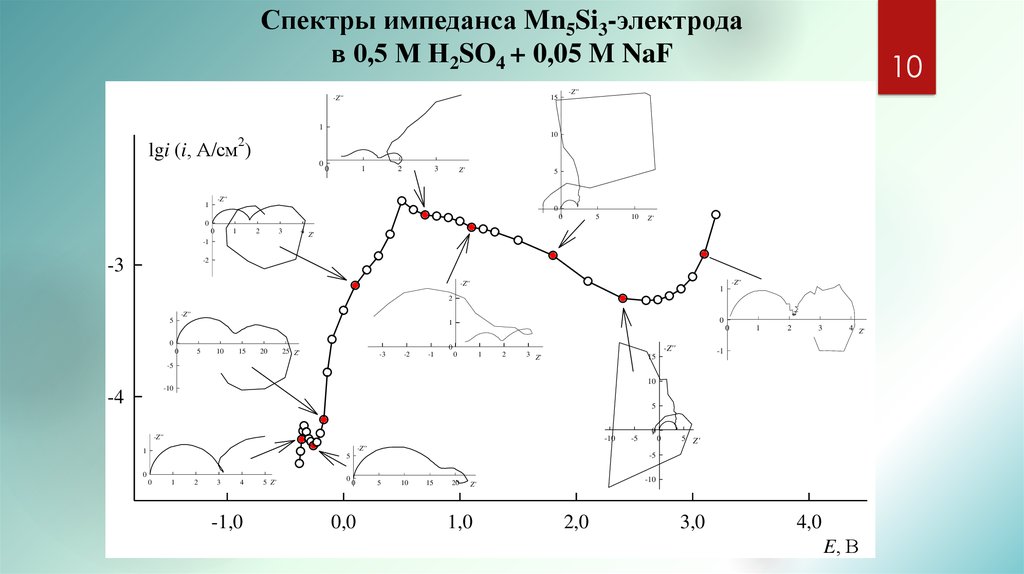
Спектры импеданса Mn5Si3-электродав 0,5 М Н2SO4 + 0,05 M NaF
-Z''
15
-Z''
10
1
10
2
lgi (i, А/см )
0
0
1
2
3
Z'
5
-Z''
1
0
0
5
10
0
0
1
2
3
4
Z'
Z'
5
-1
-2
-3
-Z''
-Z''
1
2
-Z''
5
0
1
0
0
5
10
15
20
0
0
25 Z'
-3
-2
-1
0
1
2
-Z''
3 Z'
1
2
3
4 Z'
-1
15
-5
10
-10
-4
5
0
-Z''
-10
-5
0
5 Z'
-Z''
1
-5
5
0
0
1
2
3
4
-1,0
5 Z'
0
0
0,0
5
10
15
20
-10
Z'
1,0
2,0
3,0
4,0
E, В
11.
Спектры импеданса Mn5Si3-электродав 0,5 М Н2SO4 + 0,05 M NaF
-Z''
15
-Z''
11
1
2
lgi (i, А/см )
10
0
0
1
2
3
Z'
5
-Z''
1
0
0
5
10
Z'
0
0
1
2
3
4
Z'
5
-1
-2
-3
-Z''
-Z''
1
2
-Z''
5
1
0
0
0
5
10
15
20
25 Z'
0
-3
-5
-2
-1
0
1
2
1
2
3
4 Z'
15
3 Z'
-1
10
-10
-4
0
-Z''
5
0
-10
-Z''
-Z''
1
0
1
2
3
4
-1,0
0
5 Z'
0,0
0
0
5 Z'
-5
5
0
-5
5
10
15
20
1,0
-10
Z'
2,0
3,0
4,0
E, В
12. Анодное поведение Mn5Si3-электрода в 0,5 M H2SO4 + xNaF
Электродные процессы:2
lgi (i, А/см )
-3
А3
А4
А2
А1
Mn = Mn2+ + 2e–
А2
Mn + H2O = MnO + 2H+ + 2e–
А3
MnO + 2H2O = Mn3O4 + 2H+ +2e –
2Mn3O4 + H2O = 3Mn2O3 + 2H+ + 2e –
Mn2O3 + H2O = 2MnO2 + 2H+ + 2e–
А4
-4
Mn2+ + 2H2O = MnO2 + 4H+ + 2e–
2Mn2+ + 3H2O = Mn2O3 + 6H+ + 2e–
А1
Si + 2H2O = SiO2 + 4H+ + 4e–
0,0
1,0
2,0
3,0
E, В
Анодная потенциостатическая кривая
Mn5Si3-электрода в 0,5 M H2SO4 + 0,05 M NaF
А1-А4
Si + 2HF = SiF2 + 2H+ + 2e–
2SiF2 = Si + SiF4
SiO2 + 6HF = H2 SiF6 + 2H2O
SiO(OH)2 + 2HF = SiF2(OH)2 + H2O
12
13.
Микрофотографии поверхности Mn5Si3-электродав области пассивации (×700)
Исходный образец
13
Анодное травление
0,5 М H2SO4
0,5 М H2SO4 + 0,005 М NaF
0,5 М H2SO4 + 0,05 М NaF
14. Выводы:
141. Анодное поведение силицида марганца (Mn5Si3) в растворе серной кислоты в области потенциалов от E коррозии до E
перепассивации включительно определяется поверхностной химически стойкой в кислых средах оксидной пленкой.
Основу пленки составляет SiO2 с небольшим содержанием оксидов марганца (MnO, Mn2O3, MnO2).
2. Формирование пассивной пленки на Mn5Si3 в растворе серной кислоты осуществляется по линейному закону:
константы анодирования составляют 0,68 и 0,37 нм/В для интервалов потенциалов (-0,1 – 0,3) В и (0,5 – 0,9) В
соответственно. Толщина оксидной пленки на силициде при этих значениях E варьирует в диапазоне (0,5 – 1,2) нм.
3. Перепассивация Mn5Si3 в растворе серной кислоты обусловлена окислением металлического компонента сплава,
сопровождаемого частичным разрушением оксидной пленки, возрастанием дефектности, ослаблением ее изоляционных
свойств.
4. Влияние фторида натрия, вызывающего активацию анодного растворения Mn5Si3 в растворе серной кислоты, связано с
ослаблением пассивирующего действия кислородсодержащих соединений кремния и оксидов марганца. С ростом
концентрации фторида роль металла и продуктов его окисления в кинетике анодных процессов на силициде значительно
возрастает. Тем не менее, роль кремния в пассивации Mn5Si3 даже в присутствии фторида остается высокой.
5. Активное анодное растворение Mn5Si3 во фторидсодержащем электролите обусловлено процессами ионизации металла
и окисления кремния; реакция окисления кремния, по-видимому, включает электрохимические и химическую стадии,
сопровождается выделением водорода. Пассивное состояние Mn5Si3 во фторидсодержащем определяется поверхностной
оксидной пленкой, основу которой составляют оксиды металла с небольшим содержанием диоксида кремния. Процесс
выделения кислорода на силициде в присутствии фторида характеризуется значительным перенапряжением.
15. Спасибо за внимание!
15Спасибо за внимание!










 Химия
Химия








