Похожие презентации:
Кристалічна ґрадка. Встановити взаємозв’язок між будовою речовин та їх фізичними властивостями
1.
Кристалічні ґратки.Залежність
фізичних
властивостей
речовини від типів
кристалічних ґраток
2.
Цілі: встановити взаємозв’язокміж
будовою речовин та їх фізичними
властивостями на підставі знань про
типи хімічних зв’язків у неорганічних
речовинах; ознайомитися з типами
кристалічних ґраток (атомною,
молекулярною, йонною, металевою).
3.
«Одного разу, під час бенкетуКлеопатра заявила, що вип'є десять
мільйонів сестерцій(93 млн.гр.)
- Який напій випила
Клеопатра?
- Що сталося з
перлиною?
Вона вийняла з вуха сергу з
перлиною, рівної якої не було в усьому
світі, і кинула її в чашу, де та вмить
розчинилася. На очах здивованої
публіки красуня залпом випила це
питво».
4.
Будова твердих речовинАморфна
Структурні частинки
речовини
розміщуються
безладно
Приклад:
глина
Кристалічна
Структурні
частинки
речовини
розміщуються
впорядковано
Приклад: кухонна
сіль
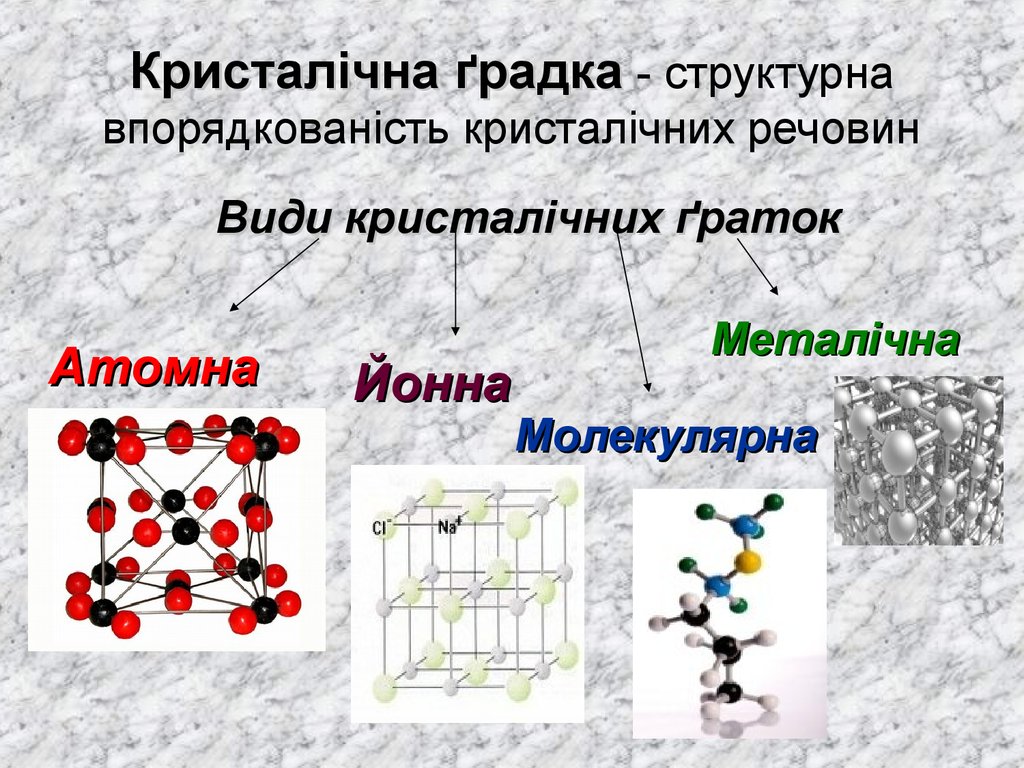
5. Кристалічна ґрадка - структурна впорядкованість кристалічних речовин
Види кристалічних ґратокАтомна
Йонна
Металічна
Молекулярна
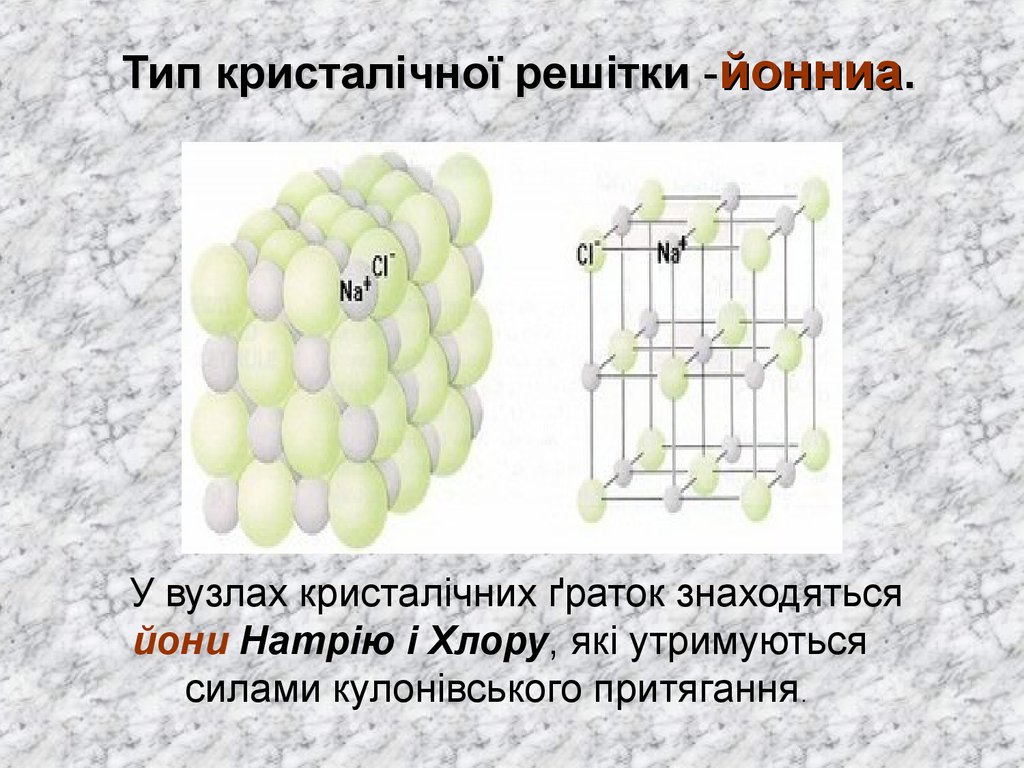
6. Тип кристалічної решітки -йонниа.
У вузлах кристалічних ґраток знаходятьсяйони Натрію і Хлору, які утримуються
силами кулонівського притягання.
7.
• Натрій хлорид (NaCl) – твердий,кристалічний, тугоплавкий, добре
розчинний у воді.
• Хімічний зв’язок - йонний, у вузлах
кристалічних ґраток знаходяться
йони Натрію і Хлору, які
утримуються силами кулонівського
притягання.
• Такий тип кристалічних решіток
називається йонний.
8. Тип кристалічної решітки - атомна
У вузлах кристалічних ґраток знаходятьсяатоми Карбону, які зв’язані між собою
ковалентним полярним зв’язком.
9.
• Графіт (C )- тверда речовина,нерозчинна у воді.
• Хімічний зв'язок - ковалентний
неполярний.
• Тип кристалічної решітки - атомна, у
вузлах кристалічних ґраток знаходяться
атоми Карбону, зв’язані між собою
ковалентним полярним зв’язком.
10. Тип кристалічної решітки – молекулярна
У вузлах кристалічних ґраток знаходятьсямолекули вуглекислого газу.
Зв'язок між ними - міжмолекулярна взаємодія.
11.
• Карбон (IV) оксид (CO2) - за н.у. газ,низькі температури плавлення,
розчинний у воді.
• Хімічний зв’язок - ковалентний
полярний.
• Тип кристалічної решітки –
молекулярна, в вузлах кристалічних
ґраток знаходяться молекули
вуглекислого газу.
• Зв'язок між ними –
• міжмолекулярна взаємодія.
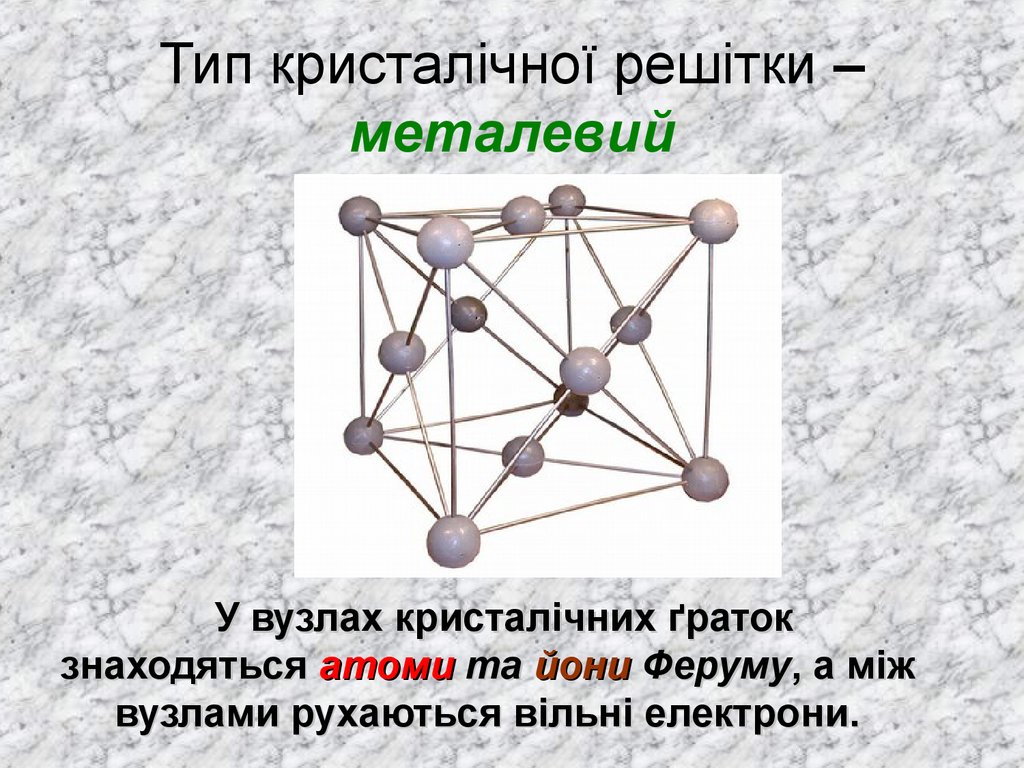
12. Тип кристалічної решітки – металевий
У вузлах кристалічних ґратокзнаходяться атоми та йони Феруму, а між
вузлами рухаються вільні електрони.
13.
• Залізо – високі температури плавлення,нерозчинне у воді.
• Хімічний зв'язок - металічний
• Тип кристалічної решітки –
металевий, у вузлах кристалічних
ґраток знаходяться атоми та йони
Феруму, а між вузлами рухаються вільні
електрони.
14. Інструкція з визначення типу кристалічної гратки
1. Проста речовина – визначити металчи неметал:
– Ме – мають металічну кристалічну
гратку;
– неМе – мають молекулярну кристалічну
гратку;
винятки – деякі неМе мають атомну
кристалічну гратку
15.
2. Складна речовина – визначити класречовини:
– неМехОу – молекулярну кристалічну
гратку; P2O5
– МехОу – йонну кристалічну гратку;
Al2O3
– Ме(ОН)х – йонну кристалічну гратку;
Cu(OH)2
– НхAn – йонну кристалічну гратку; H2SO4
MeхAnу – йонну кристалічну гратку.
Na2SO3
16. Завдання 1
За зразками кристалічних ґраток,з’ясувати, яку речовину ви отримали,
довести це:
Речовини: графіт, алмаз, кухонна
сіль, метал, вода.
17. Завдання 2
Виправити помилки:• Атомна кристалічна градка:
градка Cl2, Fe ,
N2 H2O, C
• Молекулярна кристалічна градка:
градка H2O,
KCl, O2, CO2, Au
• Металічна кристалічна градка:
градка Cu, Na,
Cl, Fe, Al, H2, SiO2
• Йонна кристалічна градка:
градка NaCl,
CaCl2,Br2, NaBr, S
18.
Карбонат кальцію (CaCO3) має йоннукристалічну решітку, тому, можна з певність
спрогнозувати повне розчинення цієї
речовини в кислоті.
19. Домашнє завдання
• 1) Вивчити § підручника,опрацювати конспект.
• 2) Створити просторові моделі
різних кристалічних ґраток; знайти
цікаві данні про використання цих
речовин у побуті.
















 Химия
Химия








