Похожие презентации:
Кислотно-основное титрование. Алкалиметрия
1.
Кислотно-основное титрованиеАцидиметрия – титранты, растворы сильных
кислот HCl, H2SO4, HNO3
Алкалиметрия – титранты, растворы сильных
щелочей NaOH, KOH
1
2.
Алкалиметрия. Стандартизация титрантаNaOH, KOH
1 – 0,5 – 0,1 – 0,05 – 0,02 – 0,01 н.
По точной навеске приготовить нельзя, т.к.
щелочи гигроскопичны и поглощают
углекислый газ воздуха
Готовят раствор щелочи приблизительно
нужной концентрации и проводят стандартизацию по установочным веществам: гидрофталату калия C8H9O4K, щавелевой кислоте
H2C2O4 2H2O, янтарной кислоте H2C4H4O4,
бензойной кислоте C6H5COOH и другим
веществам.
2
3.
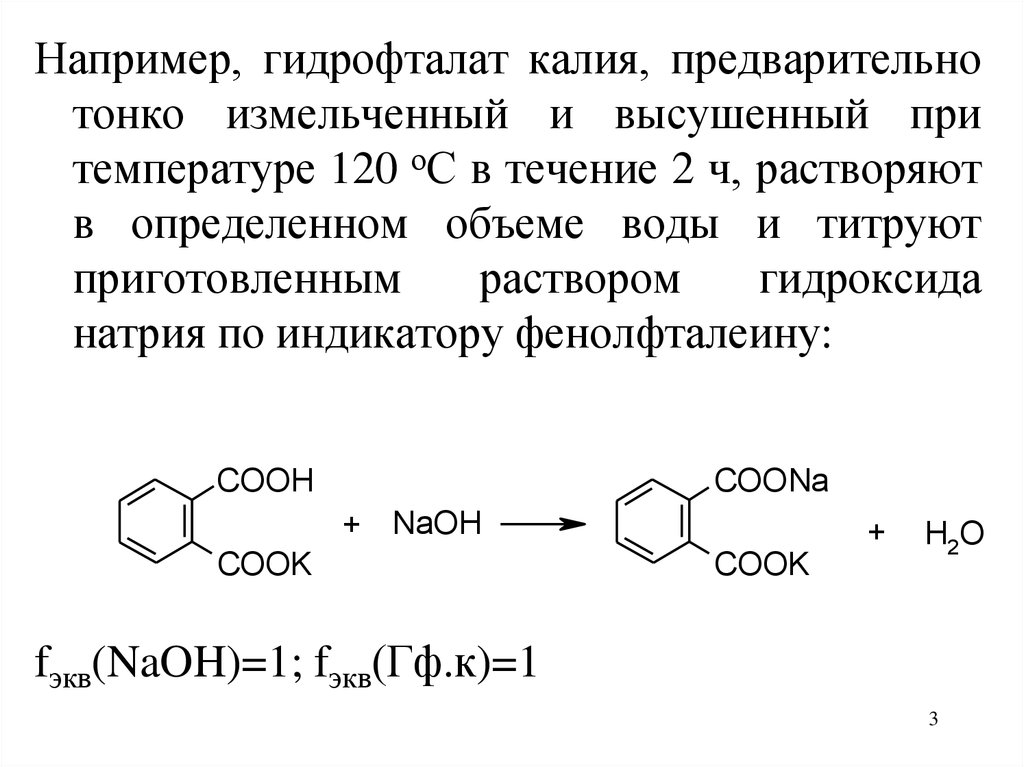
Например, гидрофталат калия, предварительнотонко измельченный и высушенный при
температуре 120 оС в течение 2 ч, растворяют
в определенном объеме воды и титруют
приготовленным
раствором
гидроксида
натрия по индикатору фенолфталеину:
COOH
COONa
+ NaOH
COOK
+
COOK
H2O
fэкв(NaOH)=1; fэкв(Гф.к)=1
3
4.
В общем виде:Сэкв(Y) · Mэкв(Y) · V(мл)
m(Y) = ————————————
1000
m(Y)т.н.. · 1000
Сэкв(Y)практ = ———————
Mэкв(Y) · V(мл)
В алкалиметрии:
Сэкв(Гф.к)теор · Mэкв(Гф.к) · Vм.к.
m(Гф.к) = —————————————
1000
m(Гф.к) · 1000
Сэкв(Гф.к)практ = ———————
Mэкв(Гф.к) · Vм.к.
4
5.
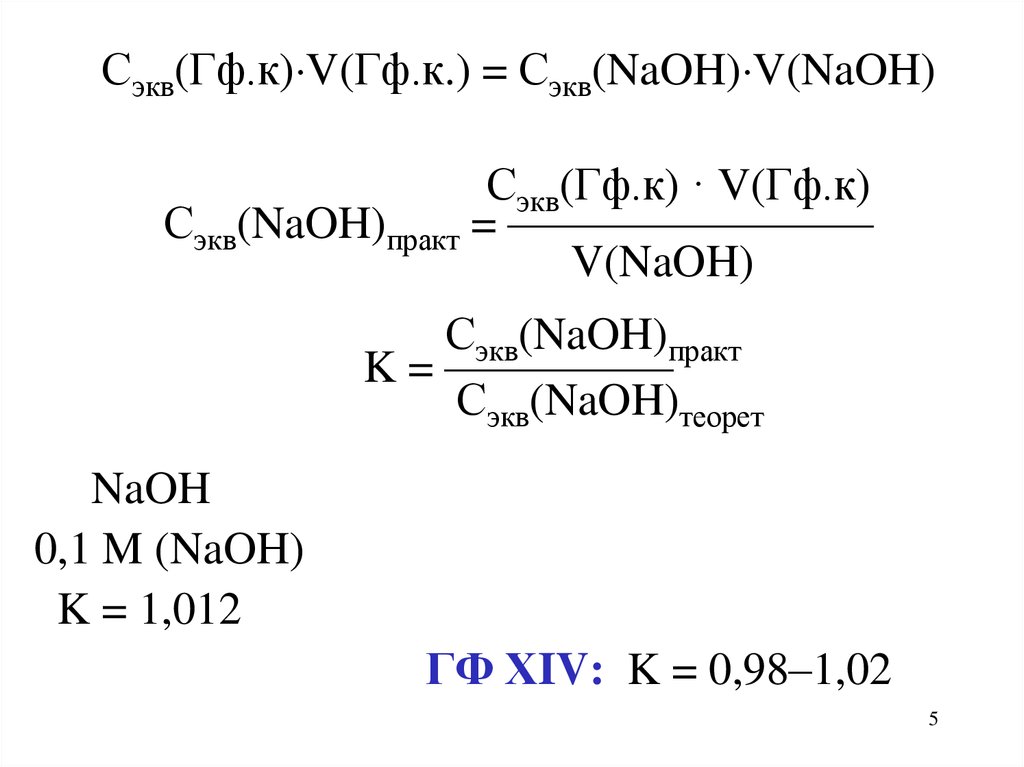
Сэкв(Гф.к) V(Гф.к.) = Сэкв(NaOH) V(NaOH)Сэкв(Гф.к) · V(Гф.к)
Сэкв(NaOH)практ = ————————
V(NaOH)
Сэкв(NaOH)практ
K = —————
Сэкв(NaOH)теорет
NaOH
0,1 M (NaOH)
K = 1,012
ГФ ХIV: K = 0,98–1,02
5
6.
Алкалиметрия применяется для количественного определения сильных и слабых кислот,солей слабых оснований, как правило,
прямым титрованием.
Ион аммония NH4+ очень слабая кислота
(рК=9,24), поэтому прямое титрование его в
водном растворе невозможно. Определяют
аммиак в солях аммония одним из двух
способов: обратным титрованием или
заместительным титрованием.
6
7.
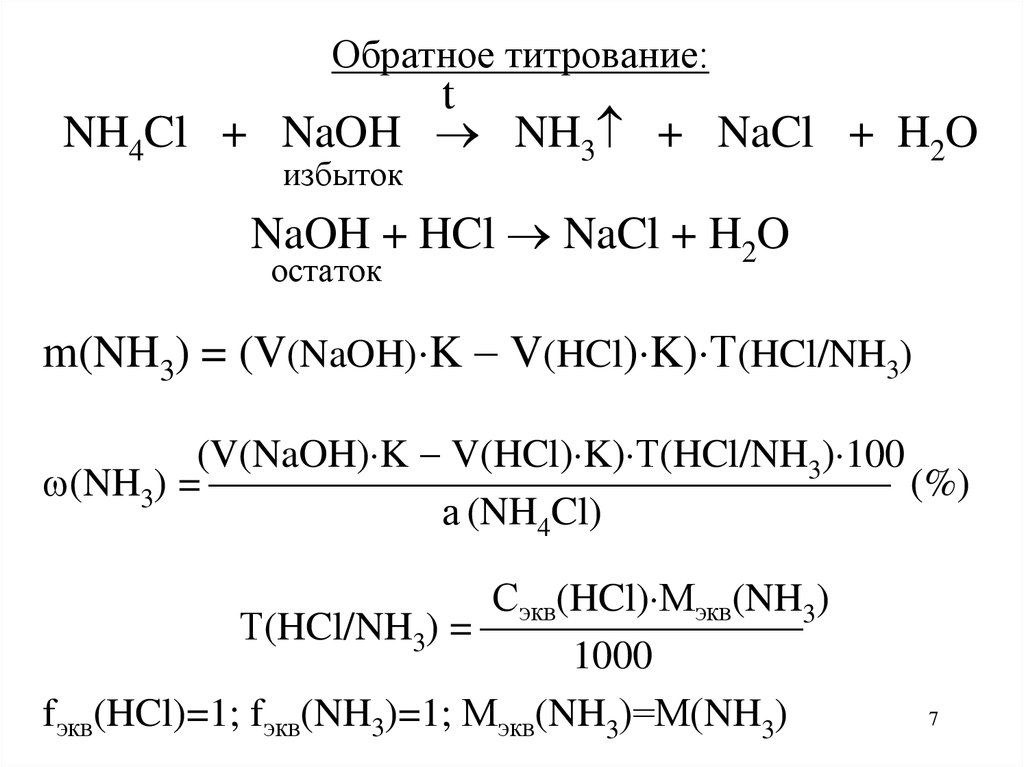
Обратное титрование:t
NH4Cl + NaOH NH3 + NaCl + H2O
избыток
NaOH + HCl NaCl + H2O
остаток
m(NH3) = (V(NaOH) K V(HCl) K) Т(HCl/NH3)
(V(NaOH) K V(HCl) K) Т(HCl/NH3) 100
(NH3) = (%)
а (NH4Cl)
Сэкв(HCl) Мэкв(NH3)
Т(HCl/NH3) =
1000
fэкв(HCl)=1; fэкв(NH3)=1; Мэкв(NH3)=М(NH3)
7
8.
Заместительное титрование4NH4Cl + 6HCOH (CH2)6N4 + 4HCl + 6H2O
Гексаметилентетрамин (ГМТА)
HCl + NaOH NaCl + H2O
m(NH3) = V(NaOH) K Т(NaOH/NH3)
V(NaOH) K Т(NaOH/NH3) 100
(NH3) = (%)
а (NH4Cl)
Сэкв(NaOH) Мэкв(NH3)
Т(NaOH/NH3) =
1000
fэкв(NaOH)=1; fэкв(NH3)=1; Мэкв(NH3)=М(NH3)8
9.
Вфармацевтическом
анализе
прямое
алкалиметрическое титрование применяется
для количественного определения кислот
(хлороводородной, бензойной, салициловой,
аскорбиновой и др. кислот) и солей,
образованных слабым основанием и сильной
кислотой
(новокаин,
гоматропина
гидробромид, тровентол и др. солей).
9
10.
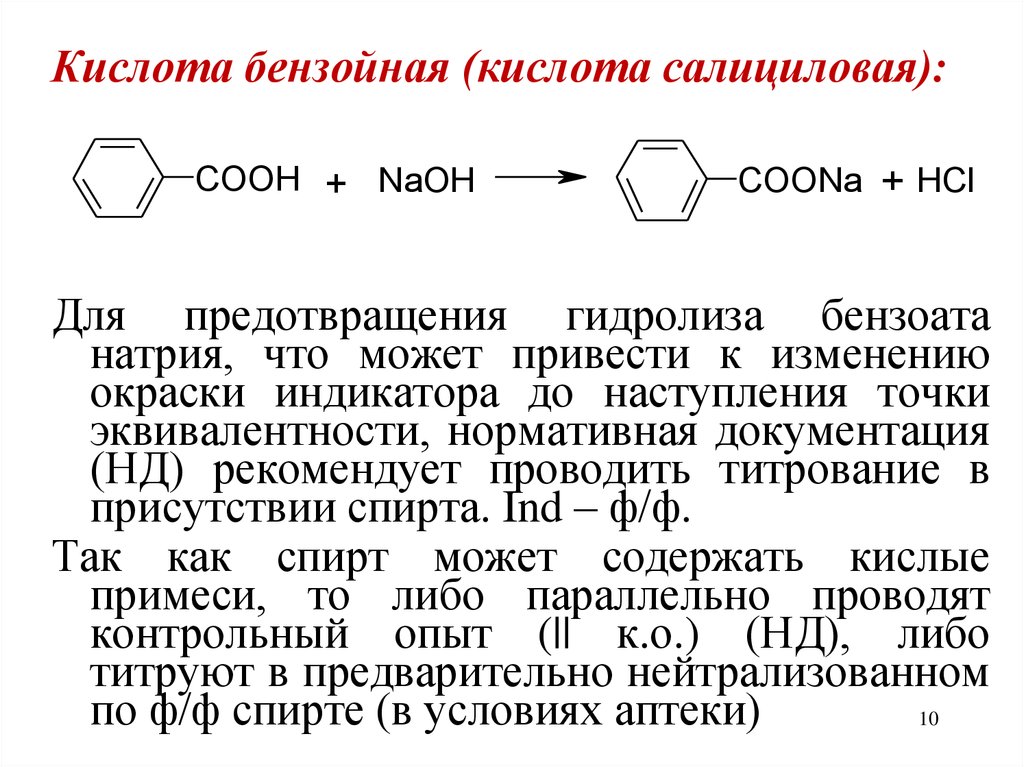
Кислота бензойная (кислота салициловая):COOH + NaOH
COONa + HCl
Для предотвращения гидролиза бензоата
натрия, что может привести к изменению
окраски индикатора до наступления точки
эквивалентности, нормативная документация
(НД) рекомендует проводить титрование в
присутствии спирта. Ind – ф/ф.
Так как спирт может содержать кислые
примеси, то либо параллельно проводят
контрольный опыт (|| к.о.) (НД), либо
титруют в предварительно нейтрализованном
по ф/ф спирте (в условиях аптеки)
10
11.
Расчет массы бензойной кислоты:m(Б.к.) = V(NaOH)·K·T(NaOH/Б.к.)
Расчет массовой доли бензойной кислоты:
V(NaOH)·K·T(NaOH/Б.к.)·100
(Б.к.) = —————————————%
а(Б.к.)
Сэкв(NaOH) · Mэкв(Б.к.)
Т(NaOH/Б.к.) = ————————
1000
fэкв(NaOH)=1; fэкв(Б.к.)=1; Мэкв(Б.к.)=М(Б.к.)
11
12.
Расчет массы и массовой доли с учетомконтрольного опыта:
m(Б.к.) = (V(NaOH)оп –V(NaOH)к.оп)·K·T(NaOH/Б.к.)
(V(NaOH)оп–V(NaOH)к.оп)·K·T(NaOH/Б.к.)·100
(Б.к.) = ——————————————————%
а(Б.к.)
12
13.
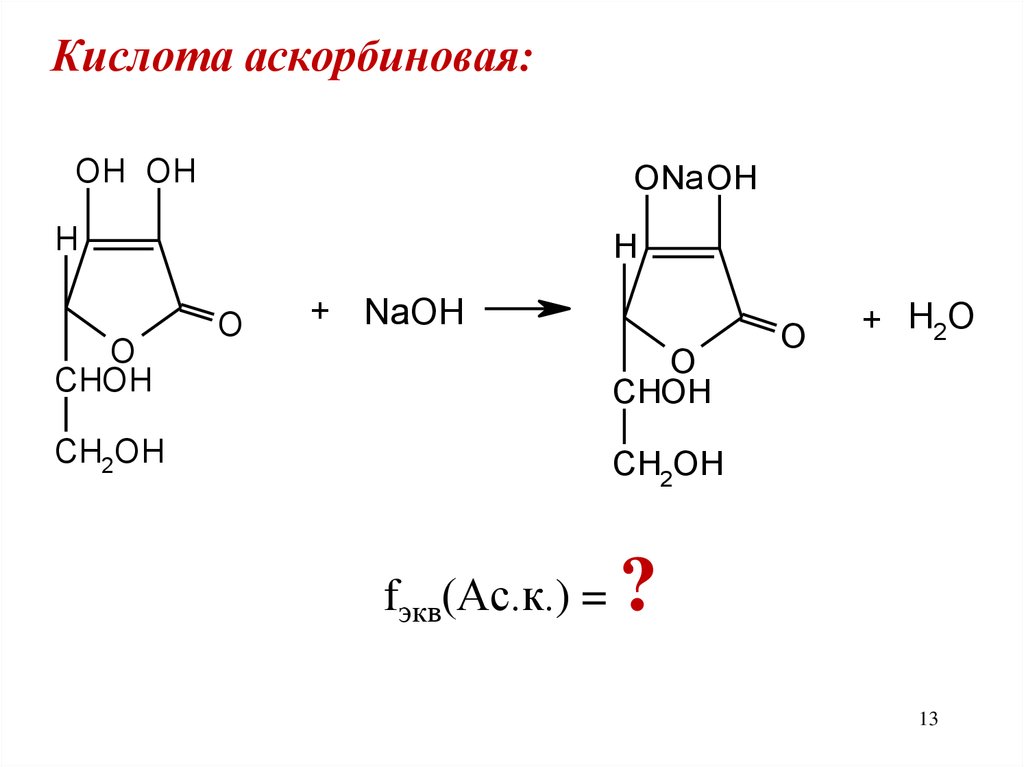
Кислота аскорбиновая:OH OH
ONaOH
H
O
CHOH
H
O
+ NaOH
O
CHOH
CH2OH
O
+ H2O
CH2OH
fэкв(Ас.к.) =
?
13
14.
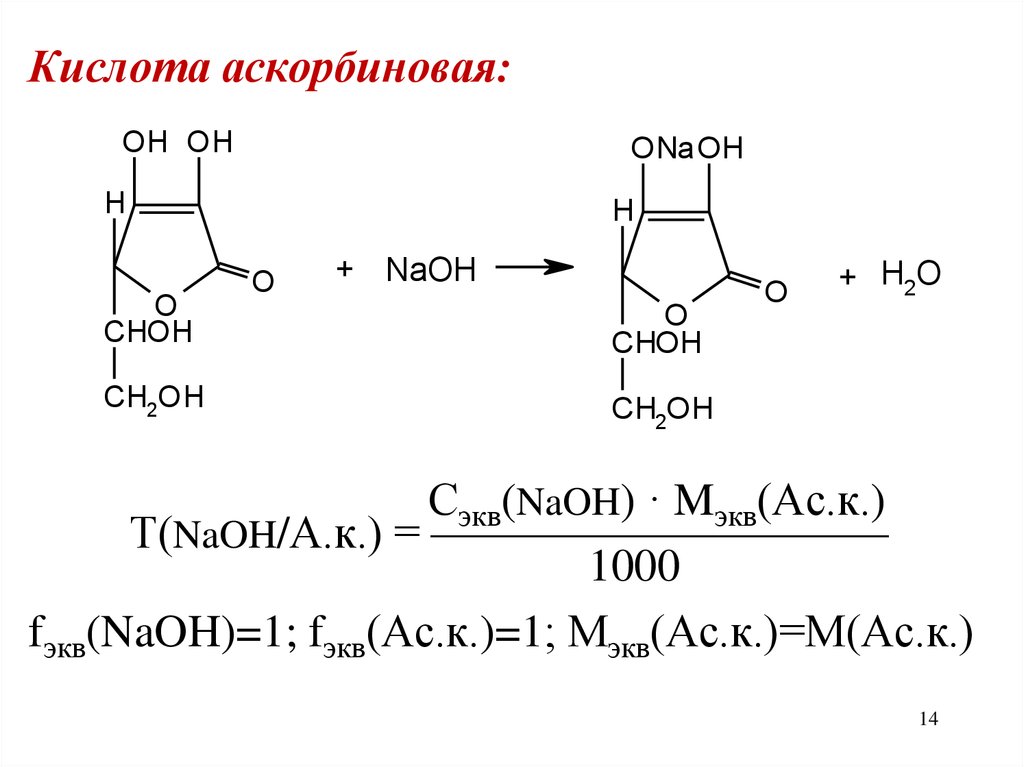
Кислота аскорбиновая:OH OH
ONaOH
H
O
CHOH
CH2OH
H
O
+ NaOH
O
CHOH
O
+ H2O
CH2OH
Сэкв(NaOH) · Mэкв(Ас.к.)
Т(NaOH/А.к.) = ——————————
1000
fэкв(NaOH)=1; fэкв(Ас.к.)=1; Мэкв(Ас.к.)=М(Ас.к.)
14
15.
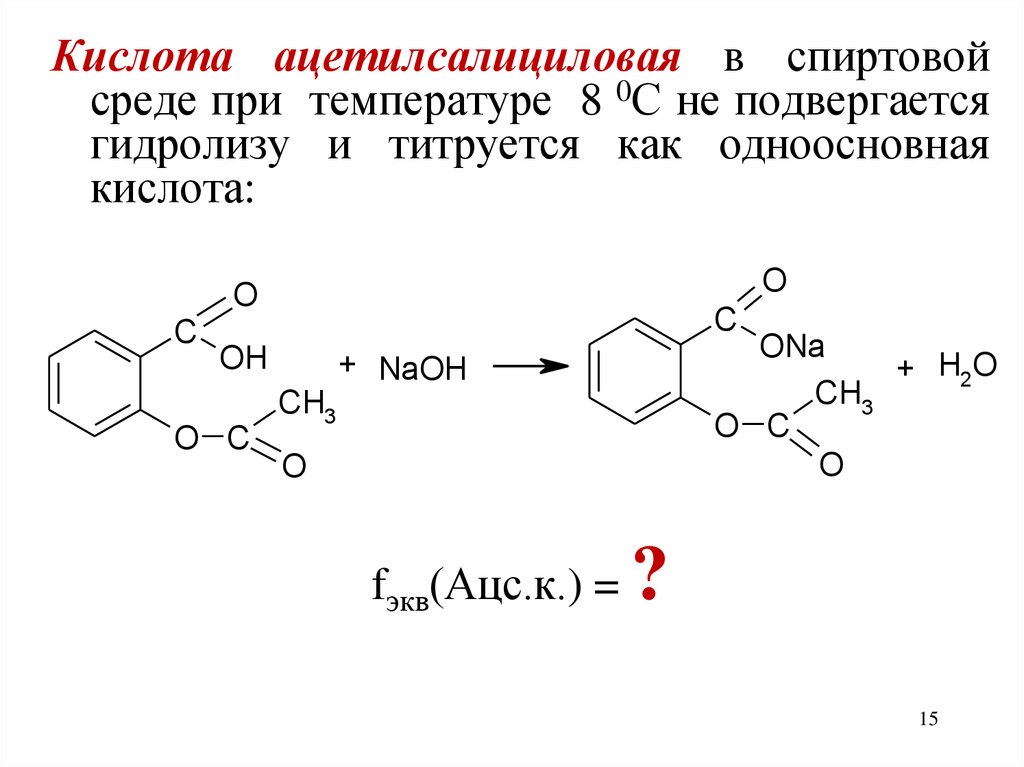
Кислота ацетилсалициловая в спиртовойсреде при температуре 8 0С не подвергается
гидролизу и титруется как одноосновная
кислота:
O
O
C
C
OH
O C
ONa
+ H2O
CH3
O C
O
+ NaOH
CH3
O
fэкв(Ацс.к.) =
?
15
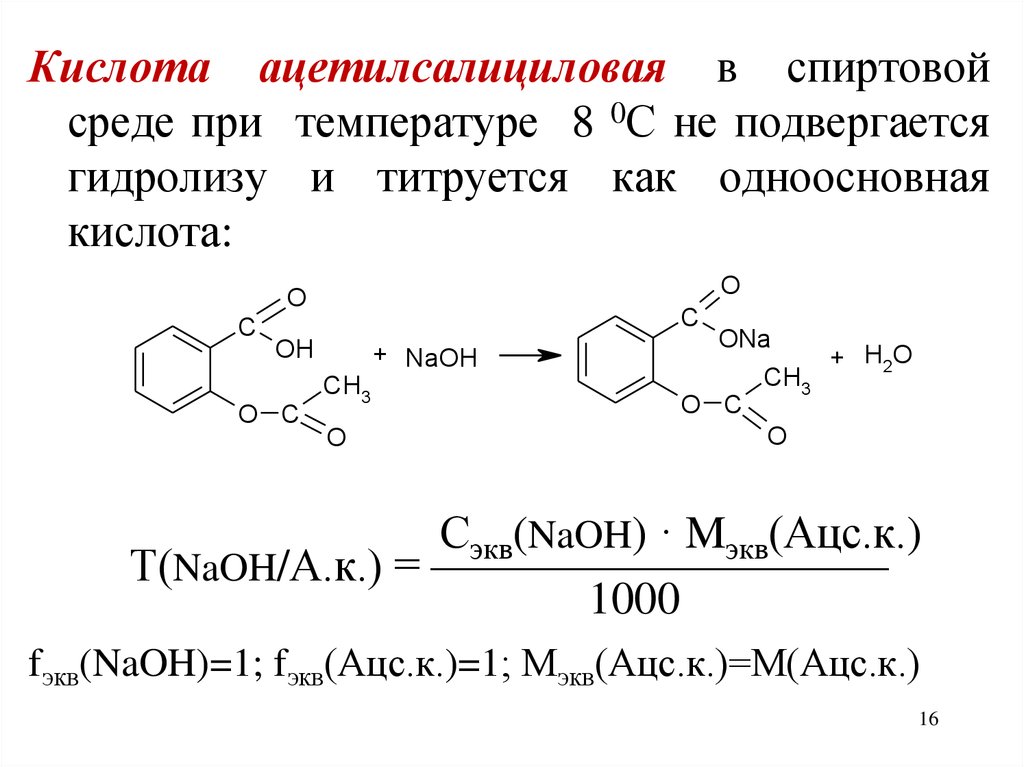
16.
Кислота ацетилсалициловая в спиртовойсреде при температуре 8 0С не подвергается
гидролизу и титруется как одноосновная
кислота:
O
O
C
C
OH
O C
+ NaOH
CH3
O
ONa
+ H2O
CH3
O C
O
Сэкв(NaOH) · Mэкв(Ацс.к.)
Т(NaOH/А.к.) = ——————————
1000
fэкв(NaOH)=1; fэкв(Ацс.к.)=1; Мэкв(Ацс.к.)=М(Ацс.к.)
16
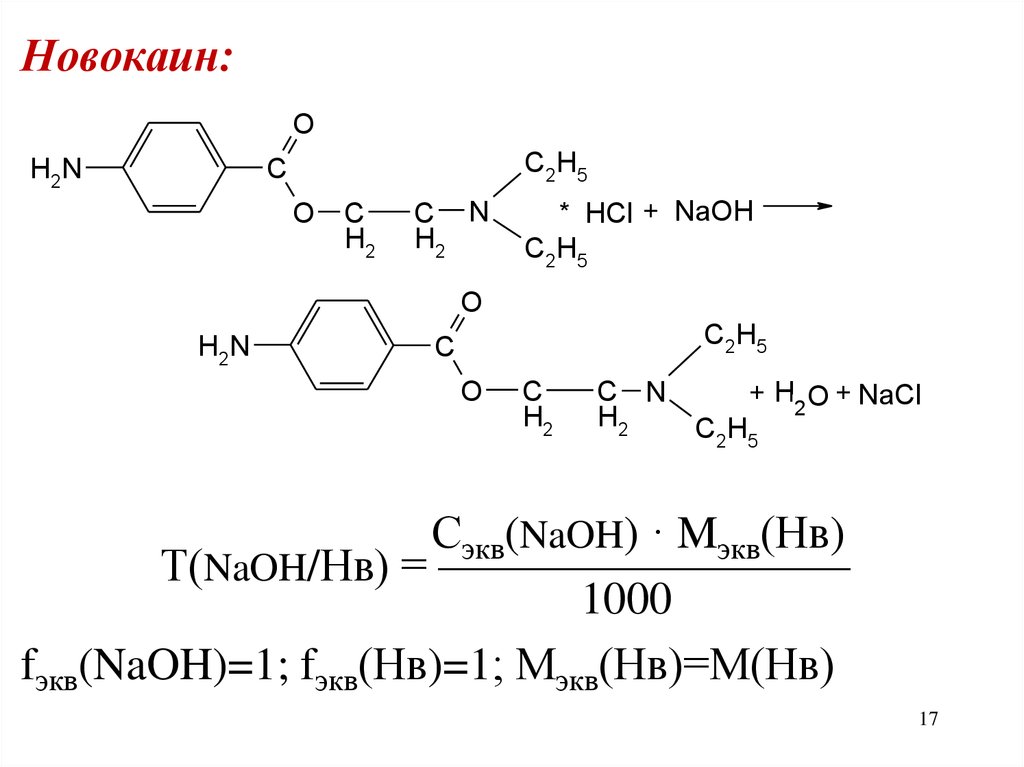
17.
Новокаин:O
H2N
C2H5
C
O
C
H2
C N
H2
* HCl + NaOH
C2H5
O
H2N
C2H5
C
O
C
H2
C N
H2
+ H2 O + NaCl
C2H5
Сэкв(NaOH) · Mэкв(Нв)
Т(NaOH/Нв) = —————————
1000
fэкв(NaOH)=1; fэкв(Нв)=1; Мэкв(Нв)=М(Нв)
17
18.
Обратное алкалиметрическое титрованиеприменяется для количественного определения хлоралгидрата, фенилсалицилата и др.
лекарственных веществ.
Хлоралгидрат:
Cl3C
C
OH
H + NaOH
OH
t
CHCl3 + HCOONa + H2O
NaOH + HCl NaCl + H2O
остаток
18
19.
m(Xг) = (V(NaOH) K – V(HCl) K)·T(HCl/Xг)Сэкв(HCl) · Mэкв(Xг)
Т(HCl/Хг) = ————————
1000
(V(NaOH) K – V(HCl) K)·T(HCl/Xг)·100
(Xг) = ————————————————%
а(Хг)
fэкв(NaOH)=1; fэкв(HCl)=1
fэкв(Хг)=1; Мэкв(Хг)=М(Хг)
19
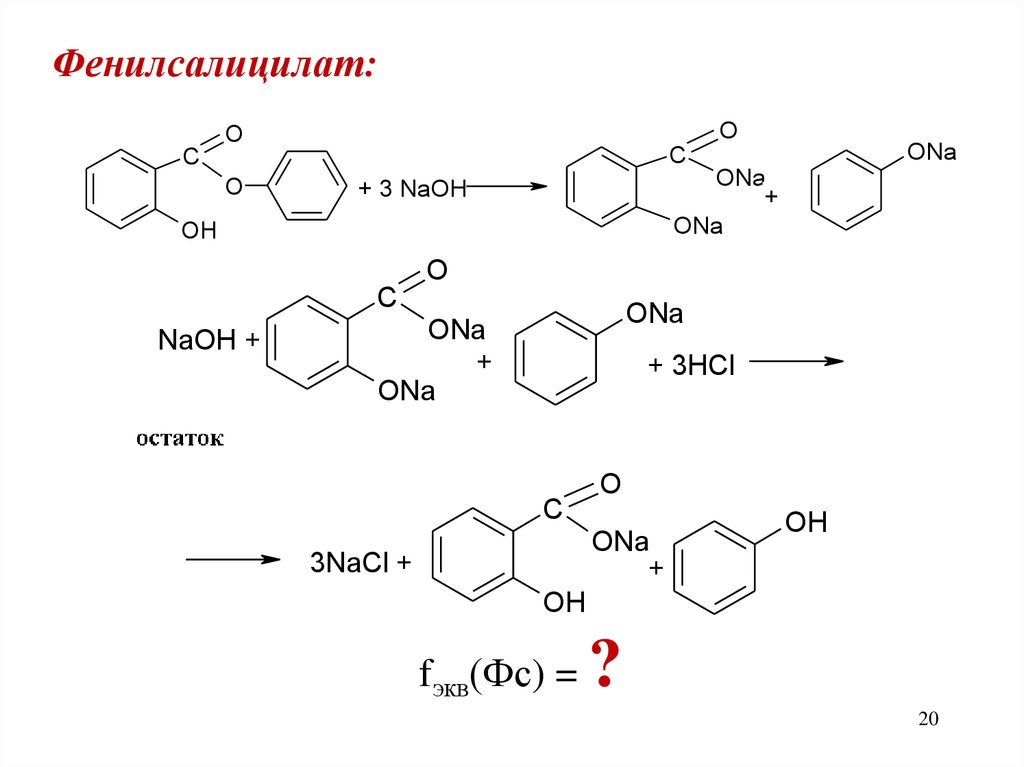
20.
Фенилсалицилат:O
O
O
ONa
C
C
ONa
+
ONa
+ 3 NaOH
OH
O
C
NaOH +
ONa
ONa
+
ONa
+ 3HCl
C
O
ONa
+
3NaCl +
OH
OH
fэкв(Фс) =
?
20
21.
При титровании избытка щелочи одновременнобудут оттитровываться динатривая соль
салициловой кислоты и фенолят натрия.
Изменение окраски фенолфталеина будет
происходить при переходе от динатриевой
соли салицилата в мононатриевую соль
21
22.
m(Фс) = (V(NaOH) K – V(HCl) K)·T(HCl/Фс)Сэкв(HCl) · Mэкв(Фс)
Т(HCl/Фс) = ————————
1000
(V(NaOH) K – V(HCl) K)·T(HCl/Фс)·100
(Фс) = ————————————————%
а(Фс)
fэкв(NaOH)=1; fэкв(HCl)=1
fэкв(Фс)=1; Мэкв(Фс)=М(Фс)
22
23.
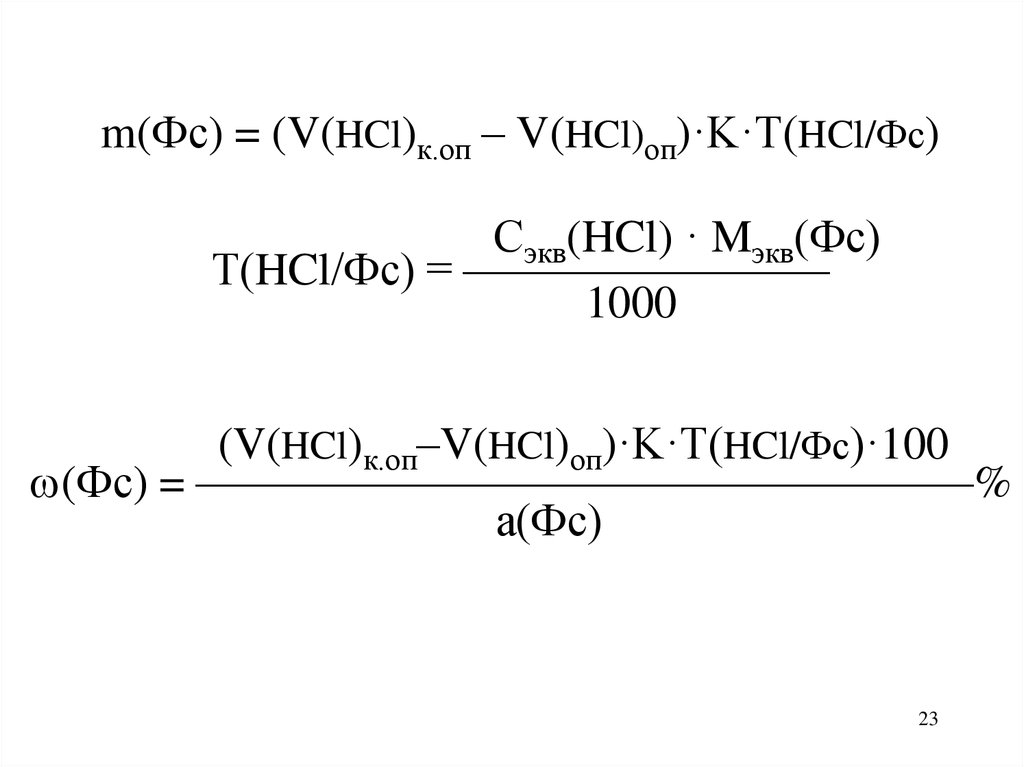
m(Фс) = (V(HCl)к.оп – V(HCl)оп)·K·T(HCl/Фс)Сэкв(HCl) · Mэкв(Фс)
Т(HCl/Фс) = ————————
1000
(V(HCl)к.оп–V(HCl)оп)·K·T(HCl/Фс)·100
(Фс) = —————————————————%
а(Фс)
23
24.
Вариантзаместительного
титрования
(косвенного титрования) применяется для
лекарственных
веществ,
содержащих
гидроксильную группу (глицерин, ментол,
синэстрол, диэтилстильбэстрол и др) (метод
ацетилирования).
24
25.
Метод основан на свойстве веществ за счетспиртовых гидроксилов ацетилироваться
уксусным ангидридом с образованием сложных эфиров и выделением эквивалентного
количества уксусной кислоты, которую
оттитровывают стандартным раствором гидроксида натрия.
Так как одновременно будет оттитровываться
уксусная
кислота,
образующаяся
при
гидролизе избытка уксусного ангидрида,
взятого для ацетилирования, параллельно
проводят контрольный опыт.
25
26.
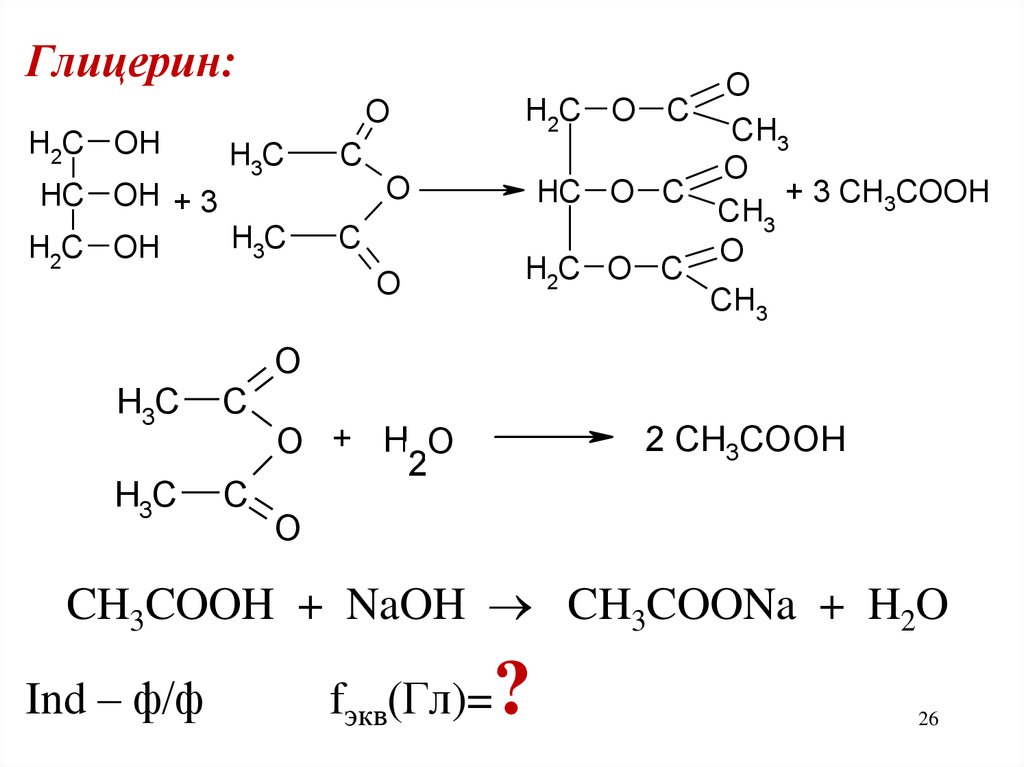
Глицерин:O
H2C OH
H3C
C
HC OH + 3
H3C
H2C OH
C
O
O
O
H2C O C
CH3
O
HC O C
+ 3 CH3COOH
CH3
O
H2C O C
CH3
O
H3C
C
H3C
C
2 CH3COOH
O + H O
2
O
CH3COOH + NaOH CH3COONa + H2O
Ind – ф/ф
fэкв(Гл)=
?
26
27.
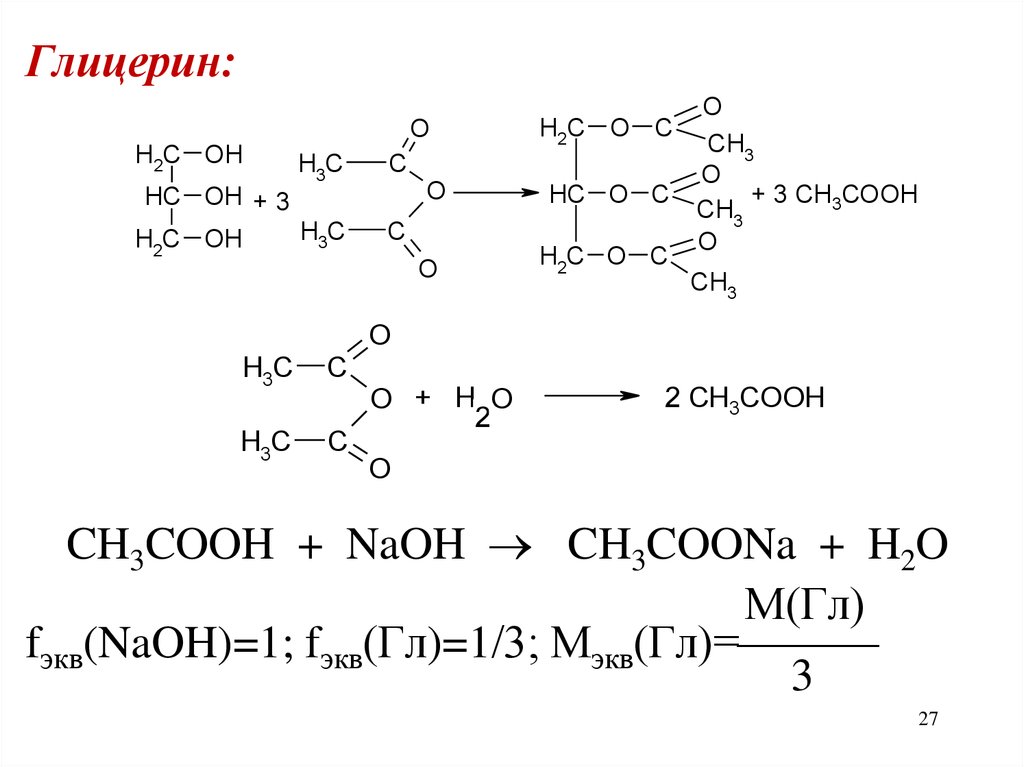
Глицерин:O
H2C OH
H3C
C
HC OH + 3
H3C
H2C OH
C
O
O
O
H2C O C
CH3
O
HC O C
+ 3 CH3COOH
CH3
O
H2C O C
CH3
O
H3C
C
H3C
C
O + H O
2
2 CH3COOH
O
CH3COOH + NaOH CH3COONa + H2O
М(Гл)
fэкв(NaOH)=1; fэкв(Гл)=1/3; Мэкв(Гл)=
3
27
28.
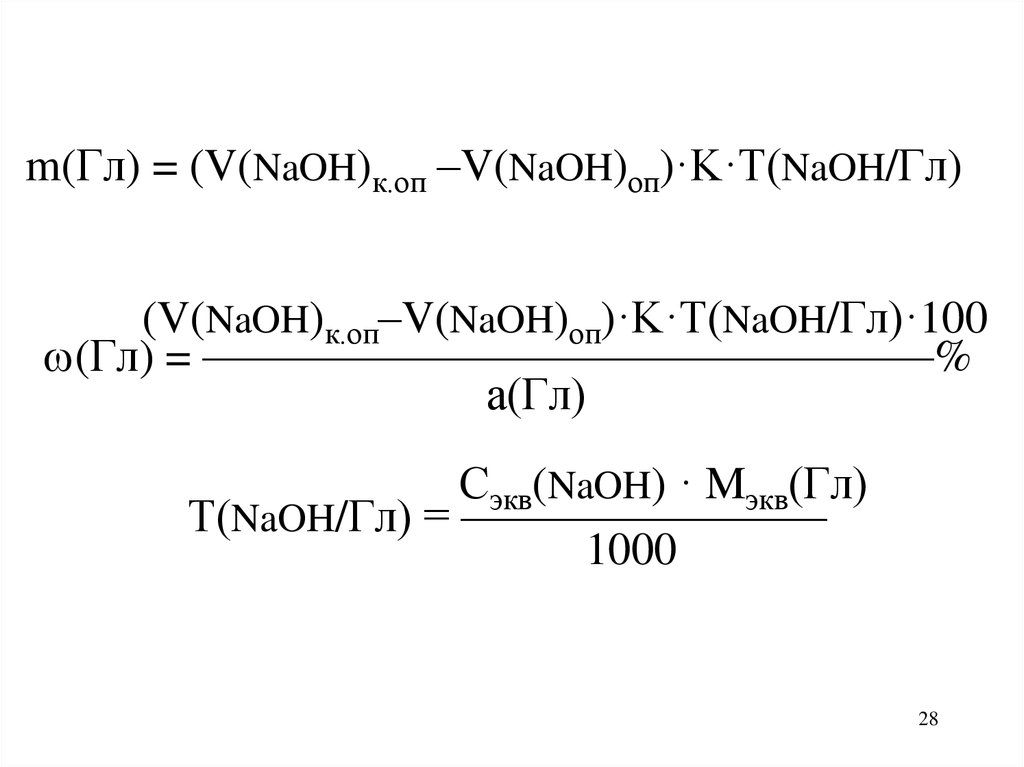
m(Гл) = (V(NaOH)к.оп –V(NaOH)оп)·K·T(NaOH/Гл)(V(NaOH)к.оп–V(NaOH)оп)·K·T(NaOH/Гл)·100
(Гл) = ————————————————%
а(Гл)
Сэкв(NaOH) · Mэкв(Гл)
Т(NaOH/Гл) = ————————
1000
28
29.
Ментол:CH3
CH3
O
H3C C
+
O
O
O
OH H3C C
H3C
C
H
O
CH3
H3C
C
H
Т(NaOH/Мн) =
C
+ CH3COOH
CH3
CH3
?
29
30.
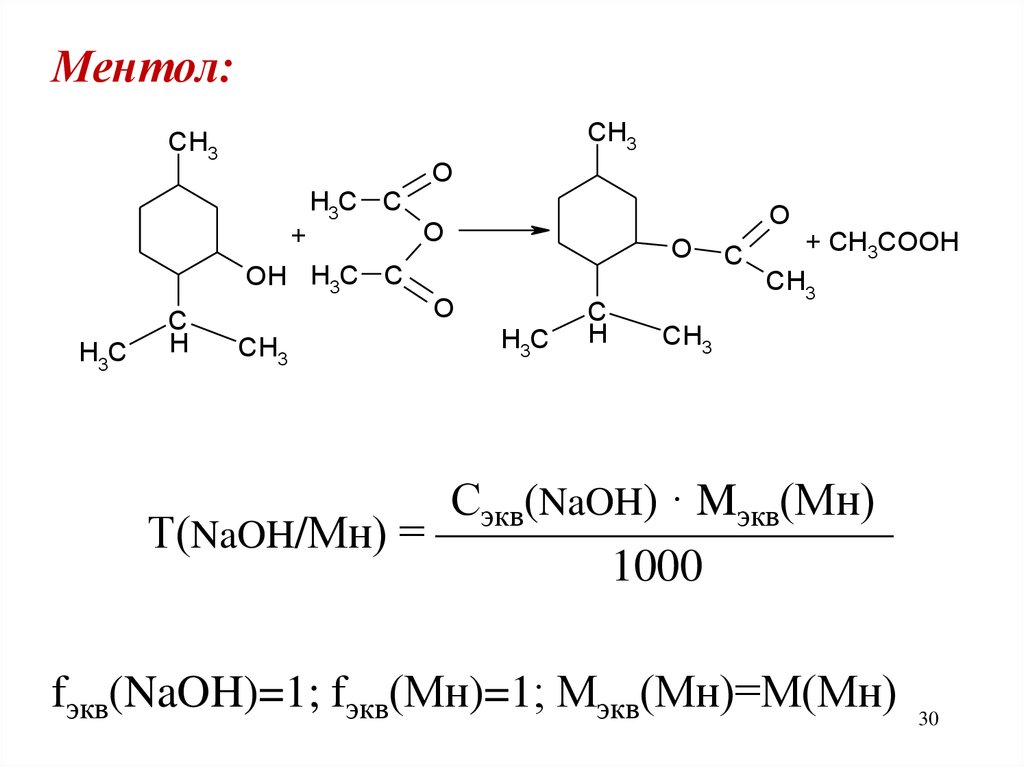
Ментол:CH3
CH3
O
H3C C
+
O
O
O
OH H3C C
H3C
C
H
O
CH3
H3C
C
H
C
+ CH3COOH
CH3
CH3
Сэкв(NaOH) · Mэкв(Мн)
Т(NaOH/Мн) = ——————————
1000
fэкв(NaOH)=1; fэкв(Мн)=1; Мэкв(Мн)=М(Мн)
30
31.
Синэстрол:O
C2H5
HO
H
C C
H
C2H5
OH
H3C
C
O
C
O
C2H5
O
C
H3C
+ 2
H3C
O
O
H
C
C
H
C2H5
Т(NaOH/Сн) =
O
+ 2 CH3COOH
C
CH3
?
31
32.
Синэстрол:O
C2H5
HO
H
C C
H
C2H5
OH
H3C
C
O
C
O
C2H5
O
C
H3C
+ 2
H3C
O
H
C
C
H
C2H5
O
O
+ 2 CH3COOH
C
CH3
Сэкв(NaOH) · Mэкв(Сн)
Т(NaOH/Сн) = ————————
1000
М(Сн)
fэкв(NaOH)=1; fэкв(Сн)=1/2; Мэкв(Сн)=
2 32
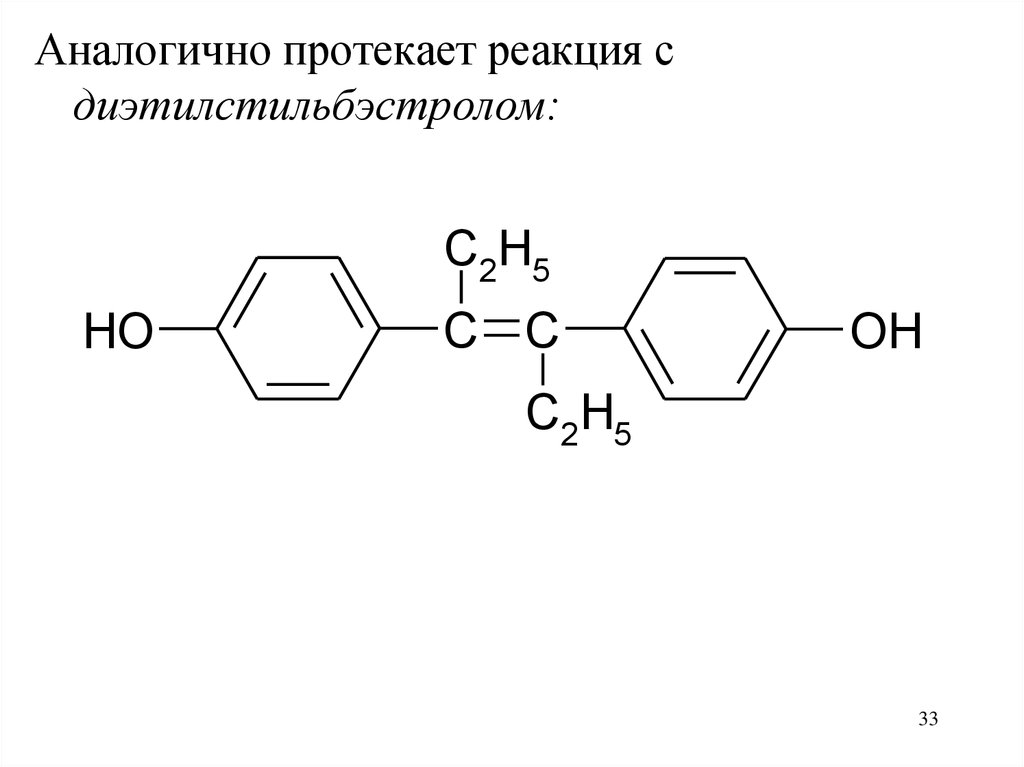
33.
Аналогично протекает реакция сдиэтилстильбэстролом:
C2H5
HO
C C
OH
C2H5
33
34.
Косвенный метод нейтрализации применяется,также, для количественного определения
теобромина и теофиллина. При взаимодействии с нитратом серебра выделяется азотная
кислота, которая оттитровывается стандартным раствором гидроксида натрия.
34
35.
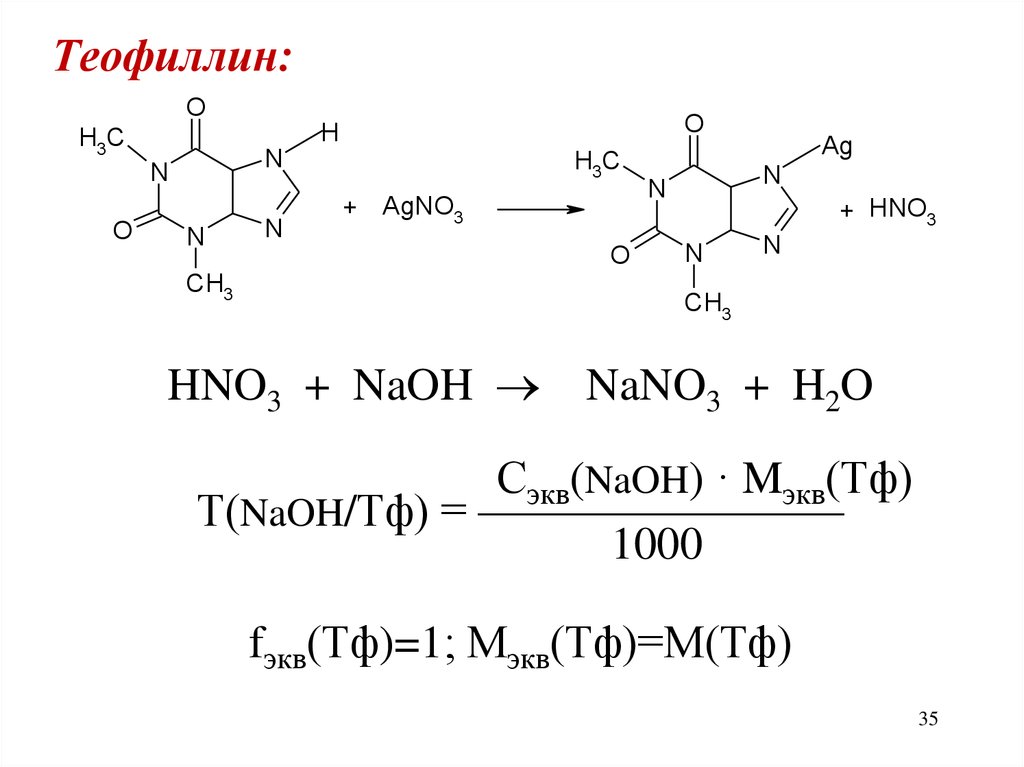
Теофиллин:O
N
N
O
O
H
H3C
N
CH3
N
H3C
+ AgNO3
O
Ag
N
N
+ HNO3
N
N
CH3
HNO3 + NaOH NaNO3 + H2O
Сэкв(NaOH) · Mэкв(Тф)
Т(NaOH/Тф) = ————————
1000
fэкв(Тф)=1; Мэкв(Тф)=М(Тф)
35
36.
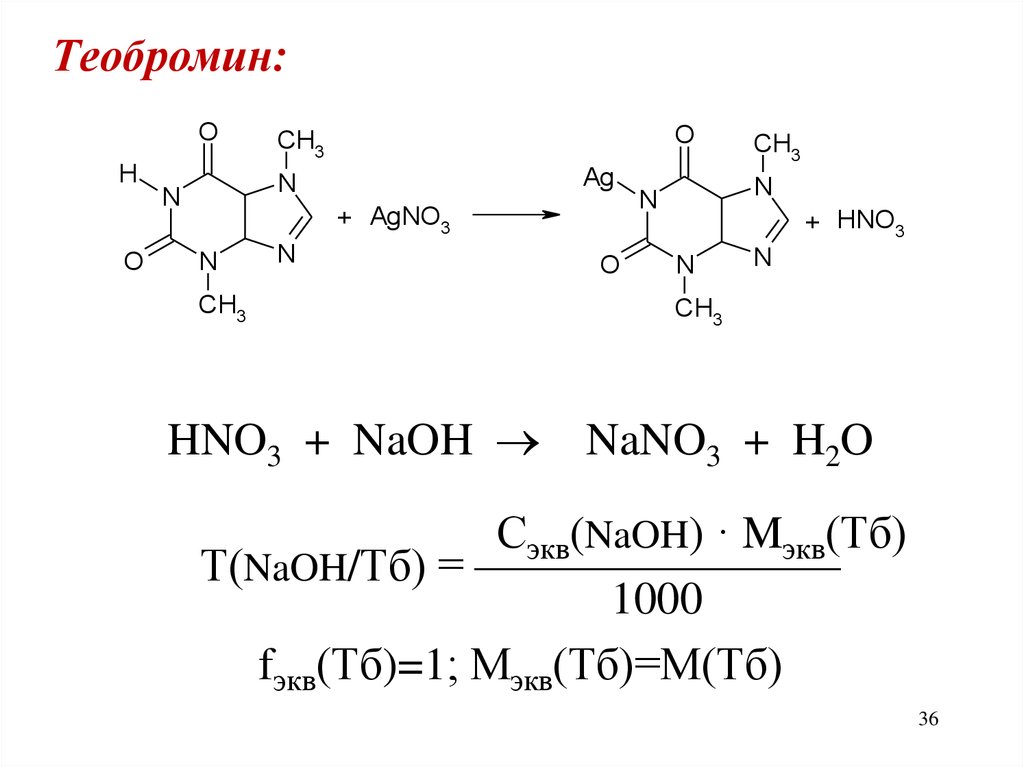
Теобромин:O
H
O
O
CH3
Ag
N
N
+ AgNO3
N
CH3
N
O
CH3
N
N
+ HNO3
N
N
CH3
HNO3 + NaOH NaNO3 + H2O
Сэкв(NaOH) · Mэкв(Тб)
Т(NaOH/Тб) = ————————
1000
fэкв(Тб)=1; Мэкв(Тб)=М(Тб)
36


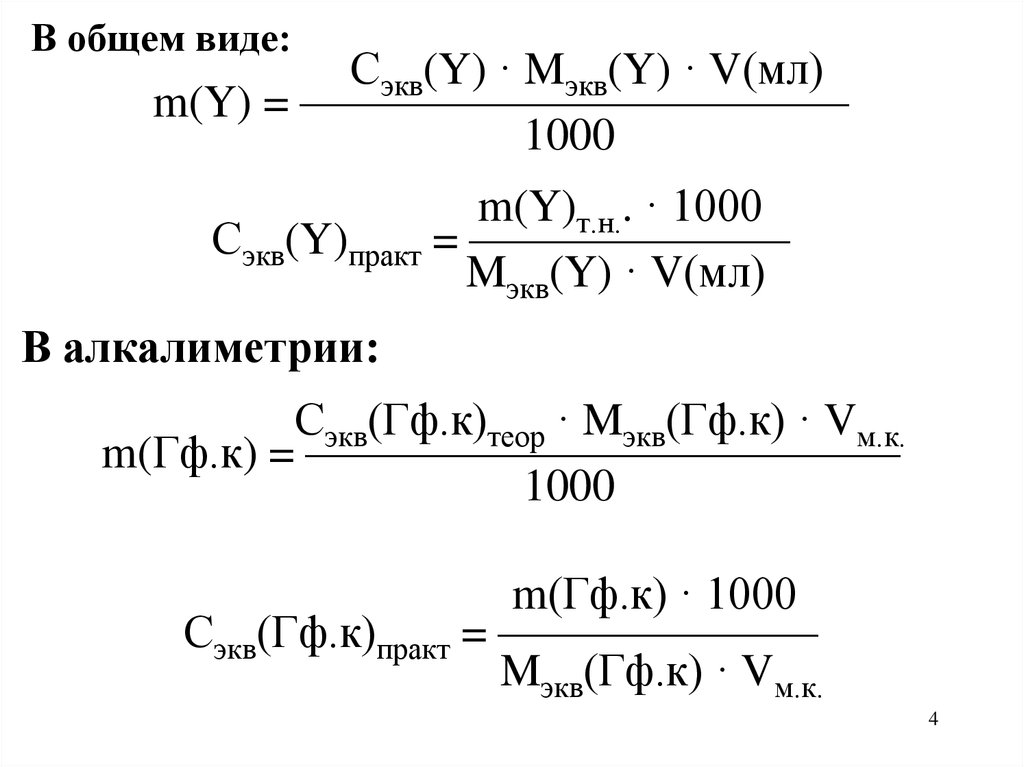






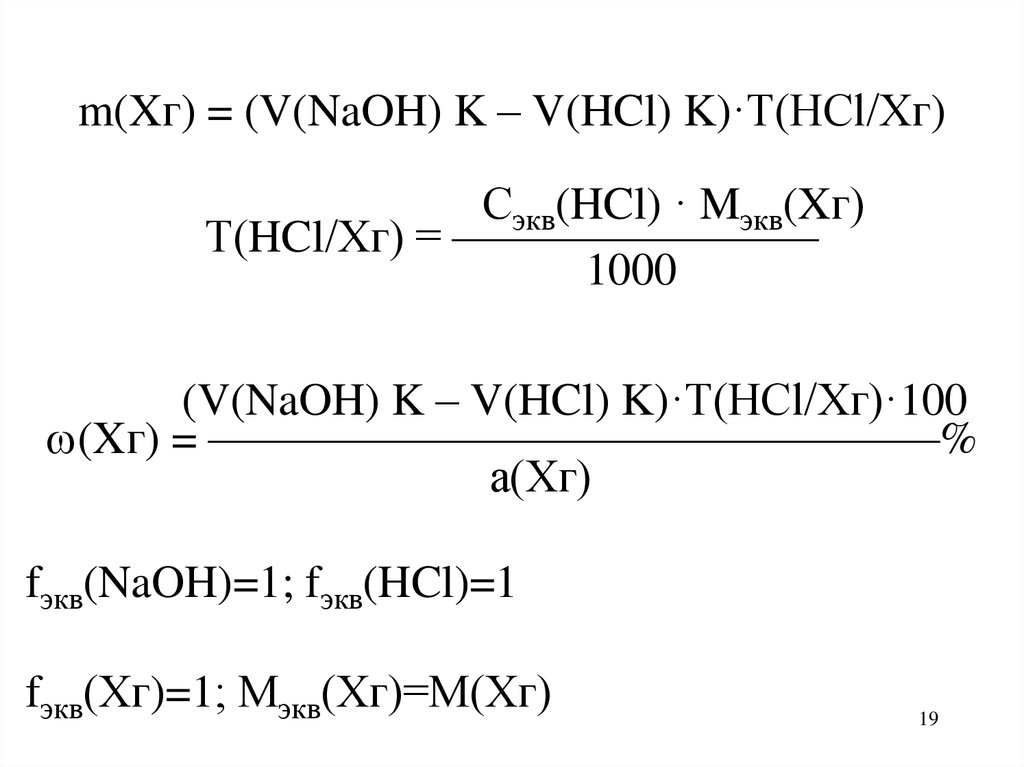









 Химия
Химия








