Похожие презентации:
Кислотно-основное титрование. Аналитическая химия
1.
Аналитическая химияЛекция 4
Кислотно-основное титрование
2.
Инструментальные методы титрования3.
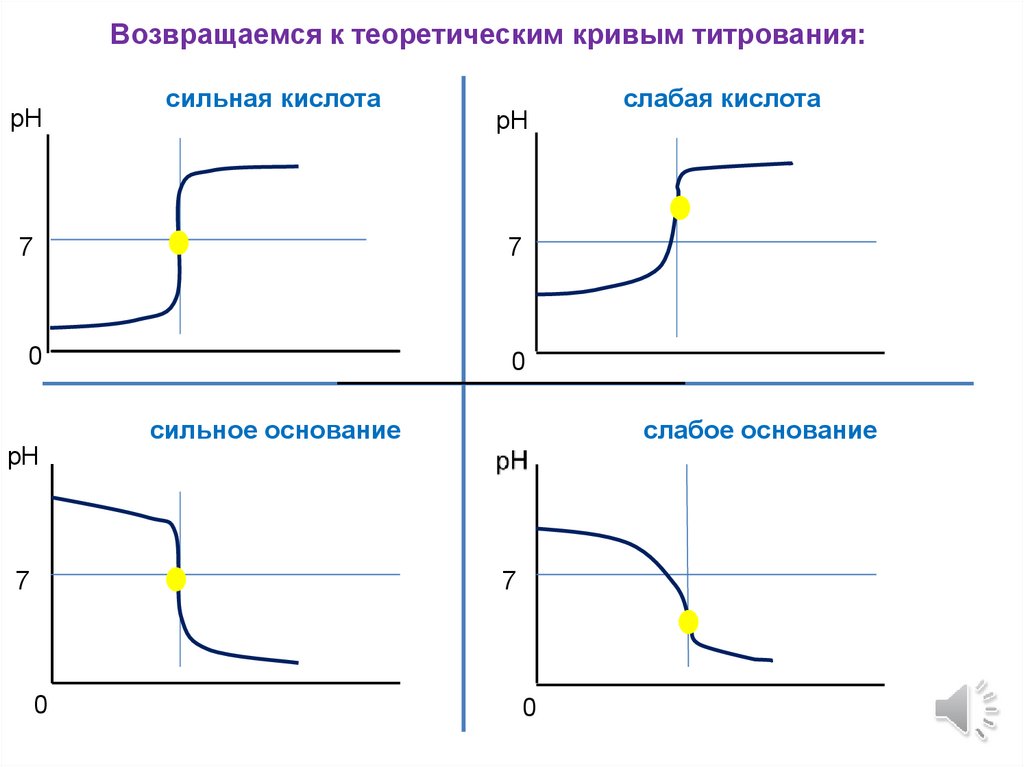
Возвращаемся к теоретическим кривым титрования:рН
сильная кислота
рН
слабая кислота
7
7
0
рН
7
0
сильное основание
слабое основание
7
0
0
4.
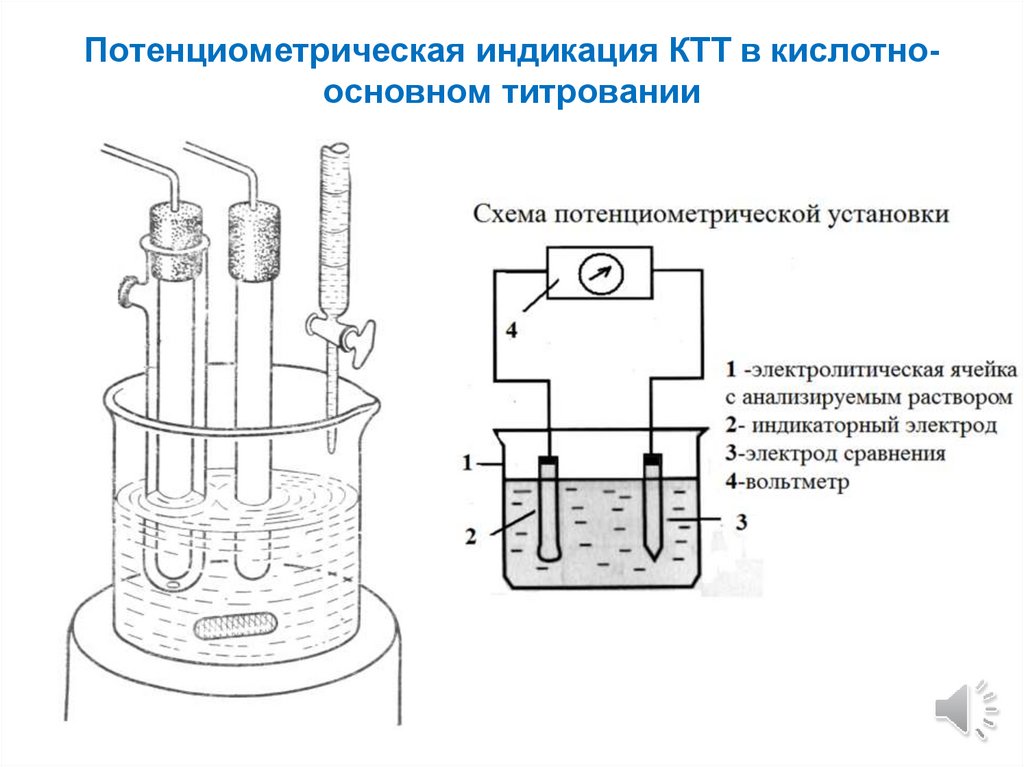
Потенциометрическая индикация КТТ в кислотноосновном титровании5.
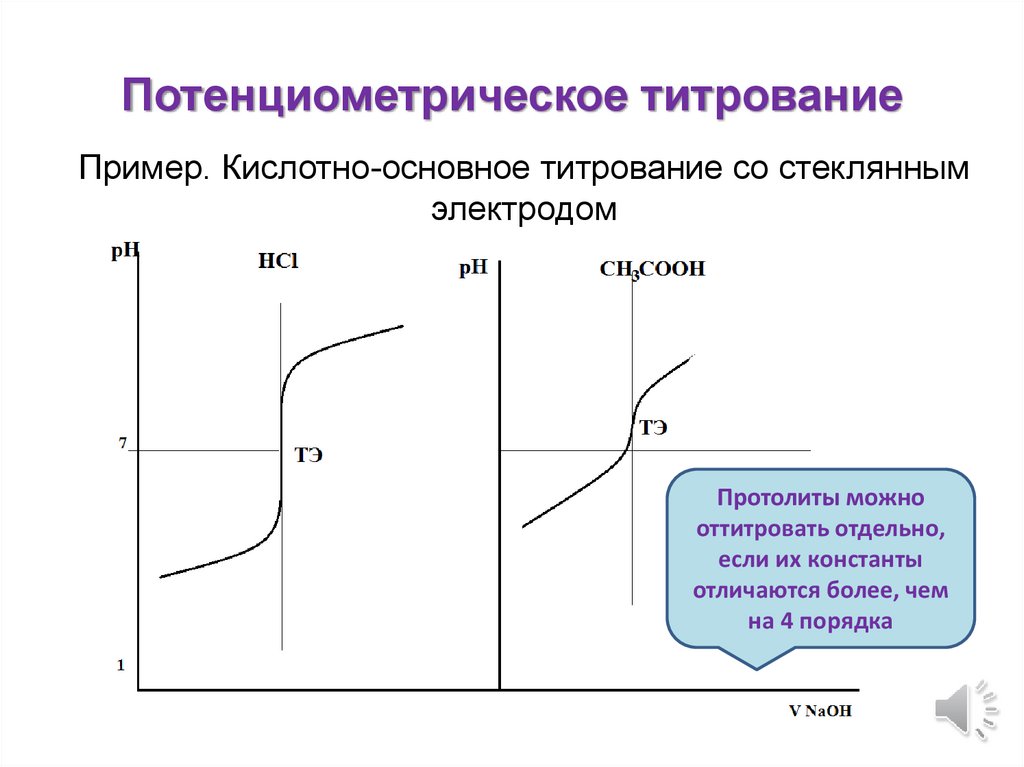
Потенциометрическое титрованиеПример. Кислотно-основное титрование со стеклянным
электродом
Протолиты можно
оттитровать отдельно,
если их константы
отличаются более, чем
на 4 порядка
6.
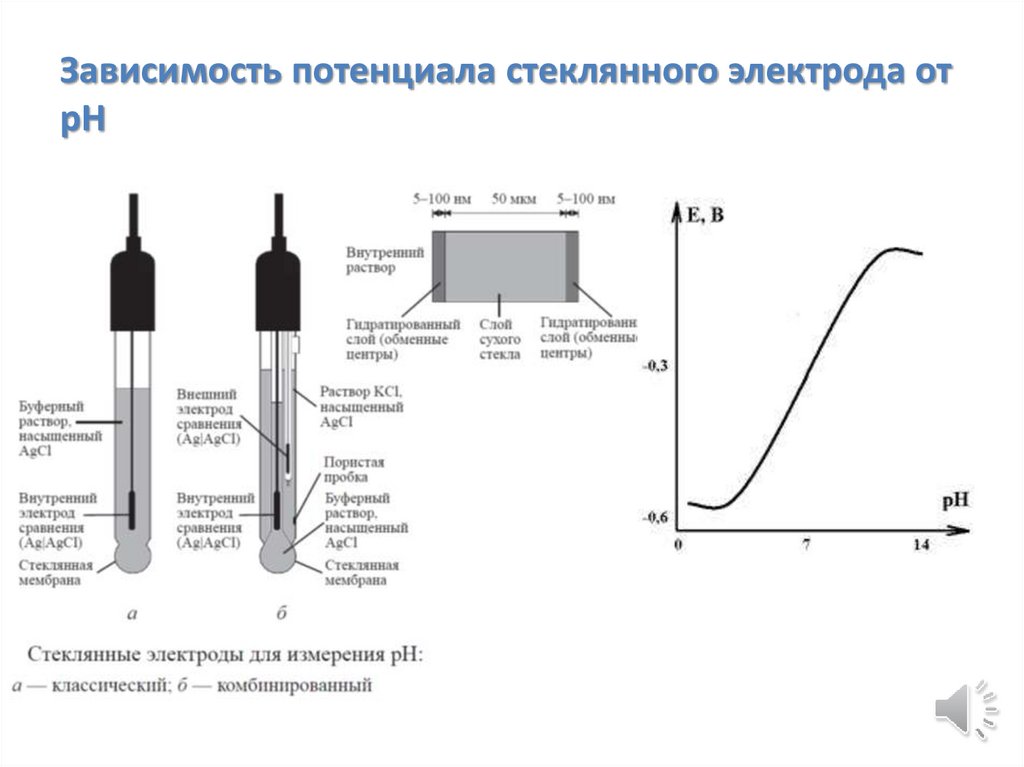
Зависимость потенциала стеклянного электрода отрН
7.
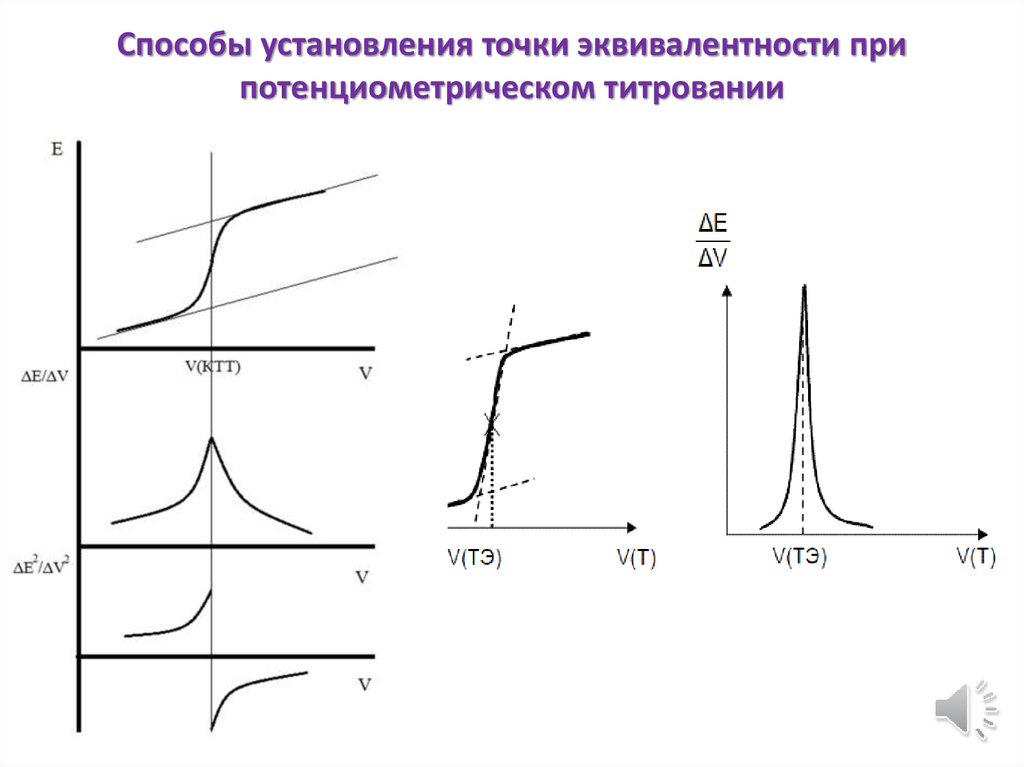
Способы установления точки эквивалентности припотенциометрическом титровании
8.
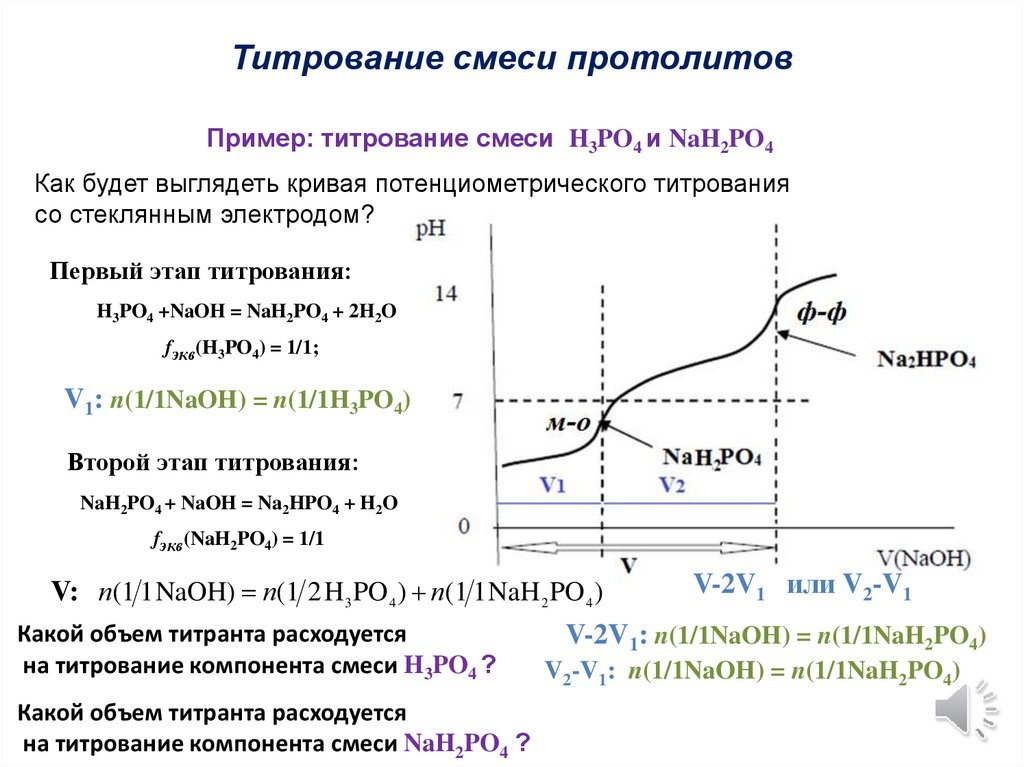
Титрование смеси протолитовПример: титрование смеси H3PO4 и NaH2PO4
Как будет выглядеть кривая потенциометрического титрования
со стеклянным электродом?
Первый этап титрования:
H3PO4 +NaOH = NaH2PO4 + 2H2O
fэкв(H3PO4) = 1/1;
V1: n(1/1NaOH) = n(1/1H3PO4)
Второй этап титрования:
NaH2PO4 + NaOH = Na2HPO4 + H2O
fэкв(NaH2PO4) = 1/1
V: n(1 1 NaOH) n(1 2 H 3 PO 4 ) n(1 1 NaH 2 PO 4 )
Какой объем титранта расходуется
на титрование компонента смеси H3PO4 ?
Какой объем титранта расходуется
на титрование компонента смеси NaH2PO4 ?
V-2V1 или V2-V1
V-2V1: n(1/1NaOH) = n(1/1NaH2PO4)
V2-V1: n(1/1NaOH) = n(1/1NaH2PO4)
9.
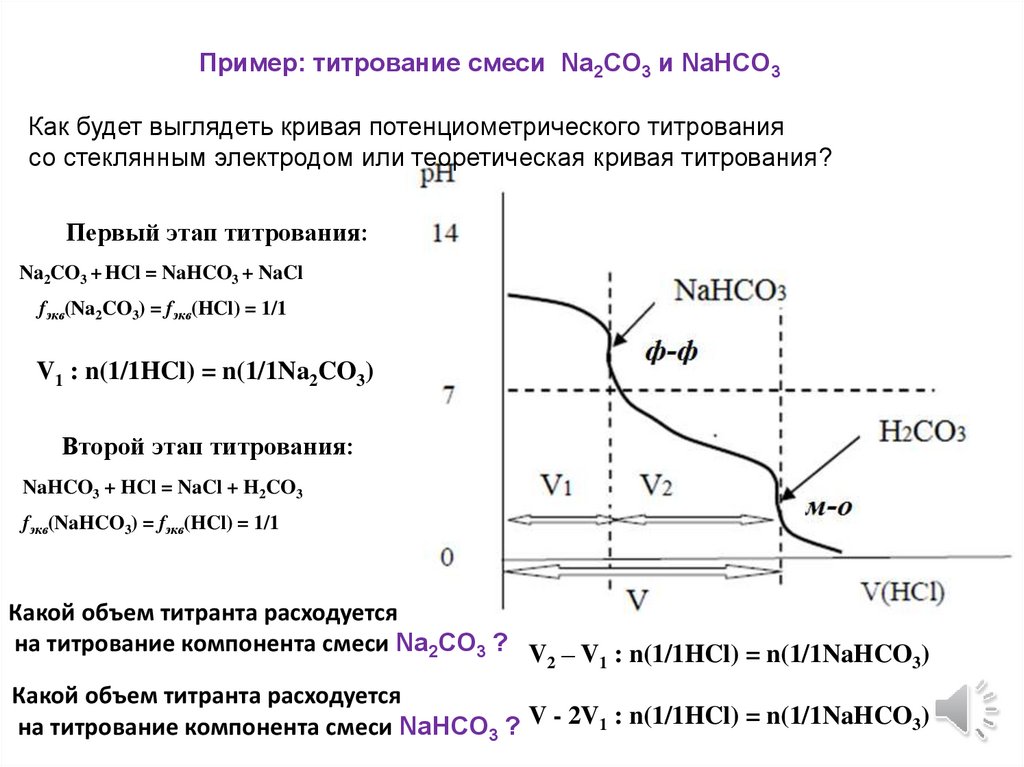
Пример: титрование смеси Na2CO3 и NaHCO3Как будет выглядеть кривая потенциометрического титрования
со стеклянным электродом или теоретическая кривая титрования?
Первый этап титрования:
Na2CO3 + HCl = NaHCO3 + NaCl
fэкв(Na2CO3) = fэкв(HCl) = 1/1
V1 : n(1/1HCl) = n(1/1Na2CO3)
Второй этап титрования:
NaHCO3 + HCl = NaCl + H2CO3
fэкв(NaHCO3) = fэкв(HCl) = 1/1
Какой объем титранта расходуется
на титрование компонента смеси Na2CO3 ? V – V : n(1/1HCl) = n(1/1NaHCO )
2
1
3
Какой объем титранта расходуется
на титрование компонента смеси NaНCO3 ? V - 2V1 : n(1/1HCl) = n(1/1NaHCO3)



 Химия
Химия








