Похожие презентации:
Донорно-акцепторный механизм образования ковалентной связи. Комплексные соединения. Лекция 9
1.
Лекция 9Донорно-акцепторный механизм
образования ковалентной связи.
Комплексные соединения:
классификация, номенклатура, строение.
2.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТКоординационная теория Вернера
Соединения типа: CH4; NH3; H2O; CO2; BF3 и т.д., в который элементы проявляют
обычную максимальную валентность называют валентнонасыщенными соединениями
или соединениями I-го порядка;
При взаимодействии соединений I-го порядка друг с другом образуют соединения
высшего порядка.
Например: гидраты; амиакаты; двойные соли и др.
3.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТПространственное строение координационных соединений
Суммарная степень окисления лигандов или их число превышает валентность или
степень окисления координационного центра (центрального атом).
4.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТЦентральный атом внутренней сферы, вокруг которого группируются ионы или
молекулы лигандов, называется комплексообразователем или ядром комплекса.
Координационное число (КЧ) или координационная валентность (КВ) – это число
мест, во внутренней сфере комплекса, которые могут быть заняты лигандами.
КЧ обычно больше степени окисления комплексообразователя, известны комплексные
соединения со следующими значениями КЧ: 1, 2, 3, 4, 5, 6, 7, 8, 9,12.
Чаще встречаются комплексные соединения с координационной валентностью 2, 4 и 6,
поскольку эти валентности соответствуют наиболее симметричной геометрической
конфигурации комплекса:
КЧ=6 октаэдрической;
КЧ=4 тетраэдрической или квадратной;
КЧ=2 линейной.
КЧ зависит от природы комплексообразователя и лигандов. Незаряженные лиганды в
большем количестве присоединяются к комплексообразователю, чем заряженные.
КЧ зависит от размеров комплексообразователя и размеров лигандов.
5.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТКоординационная емкость лиганда (дентантность лиганда) – это число мест во
внутренней сфере комплекса, занимаемых каждым лигандом. Для большинства
лигандов координационная емкость равна 1, реже 2.
Cl ; Br ; F ; I ; CN ; NH 30 ; H 2 O - занимают одно место и называют монодентантными лигандами;
NH 2 CH 2 CH 2 NH 2 - этилендиамин;
NH 2 NH 2
- гидразин - занимают по два координационных места и
называются бидентантными лигандами:
6.
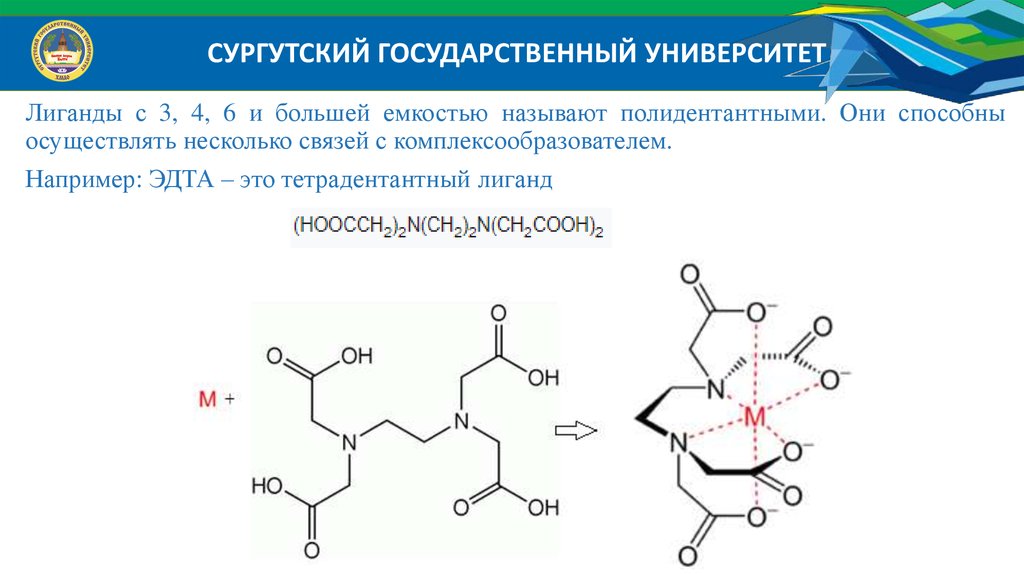
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТЛиганды с 3, 4, 6 и большей емкостью называют полидентантными. Они способны
осуществлять несколько связей с комплексообразователем.
Например: ЭДТА – это тетрадентантный лиганд
7.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТКлассификация координационных соединений
1. Нейтральные, состоящие из координационного центра (КЦ) и лигандов (L):
0
0 0
пентакарбонил железо;
Fe
(CO
)
5
КЦ
L
n
n
n
0
2. Катионные, в которых координационный центр и лиганды имеют положительный
заряд внутренней сферы: КЦ ( L) n m A m
3
0
3
1
Cr
(
NH
)
Cl
3 6
3 трихлорид гексацианохрома;
3. Анионные, в которых координационный центр и лиганды (внутренняя сфера) имеют
отрицательный заряд: Kat m КЦ ( L) n m
4
2
1
K 4 Fe(CN ) 6 гексацианоферрат тетракалия
8.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТНоменклатура координационных соединений
1. Нейтральные комплексы – лиганды (L) называют в любом порядке (слева направо
или справа налево) с умножающими префиксами. Координационный центр (КЦ)
называю в именительном падеже в русской транскрипции:
Cr (C 6 H 6 ) 2 0
дибензолхром;
2. Катионные комплексы – называют анион внешней сферы, далее – лиганды в
любом порядке (слева направо или справа налево) с умножающими префиксами;
координационный центр в родительном падеже русской транскрипции:
Ag ( NH 3 ) 2 1 OH
гидроксид диамминсеребра;
3. Анионные комплексы – называют лиганды в любом порядке (слева направо или
справа налево) с умножающими префиксами, затем КЦ в латинской транскрипции с
суффиксом «–ат» и катион внешней сферы:
3
1
3 1
K 3 Co F 6 гексафторокобальтат трикалия.
9.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ4. Число лигандов обозначается греческими числительными: ди-; три-; тетра-; пента-;
гекса- и т.д.
5. Если лигандов несколько, то сначала называют отрицательно заряженные лиганды, а
затем нейтральные.
Теория кристаллического поля (ТКП)
1. Связь между координационным центром и лигандами ионная или ион-дипольная;
2. Координационный центр рассматривается с детальным учетом электронного
строения;
3. Лиганды – как бесструктурные заряженные точки, создающие кристаллическое поле.
10.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ1.
2.
3.
4.
Метод валентных связей (МВС)
Связь между комплексообразователем (координационным центром) и лигандами
донорно-акцепторная: лиганды доноры (предоставляют электронную пару);
комплексообразователь предоставляет свободную орбиталь. Мерой прочности
служит степень перекрывания орбиталей;
Орбитали координационного центра (КЦ) гибридизуются, тип гибридизации
определяется числом, природой и электронной структурой лигандов, и определяет
геометрию комплекса;
Упрочнение комплекса
происходит за счет образования дополнительных πорбиталей (наряду с σ-связями);
Магнитные свойства, проявляемые комплексом, определяются заселенностью
молекулярных орбиталей соединения. При наличии неспаренных электронов
комплекс парамагнитен; спареность электронов обуславлевает диамагнетизм
комплексного соединения.
11.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТНедостатки МВС
1. Пригоден для описания ограниченного числа координационных соединений;
2. Комплексные соединения с многоцентровыми связями не рассматриваются;
3. Не объясняет
и не предсказывает оптические свойства координационного
соединения, поскольку не учитывает возбужденные состояния.
12.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТУстойчивость комплексных соединений.
Константа нестойкости
При растворении в воде комплексное соединение диссоциирует на ион внешней сферы и
ион внутренней сферы, т.е. внутренняя сфера ведет себя как единое целое:
K [ Ag (CN ) 2 ] K [ Ag (CN ) 2 ]
Однако, в незначительной степени идет диссоциация внутренней сферы комплекса:
[ Ag (CN ) 2 ] Ag 2CN
Для последнего уравнения получаем соотношение, которое называют константой
2
a
a
2
нестойкости комплекса:
Аg
CN
[ Аg ] [CN ]
22
К
К нест
[ Ag (CN ) 2 ]
10
нест
a[ Ag ( CN )
2]
это мера непрочности комплексного соединения. Обратная величина константе
нестойкости, есть константа устойчивости:
1
К уст
К нест
13.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТПрирода связей в координационных соединениях
По природе связи координационные соединения делятся:
1. Соединения с σ-связями:
L – донор электронной плотности;
КЦ – акцептор электронной плотности;
Например: [Cr ( NH ) ]Cl трихлоридгексаамминхрома;
3 6
3
[Co( H 2O) 6 ]Cl2 дихлоридгексааквакобальта
2. Соединения с σ- и π-связями (это наиболее прочные комплексы):
L – донор электронной плотности σ-связи ;
КЦ – акцептор электронной плотности π-связи;
Например: [ Fe(CO ) ] пентакарбонилжелезо;
5
K 4 [ Fe(CN ) 6 ] гексацианоферраттетракалия.
14.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ3. Соединения с π-связями:
L – ароматические, ненасыщенные молекулы соединений,
которые взаимодействуют с КЦ своими π-связями;
Например:
[Cr (C6 H 6 ) 2 ] дибензолхром;
[ Pt (C2 H 4 )Cl2 ] дихлороэтиленплатины;
[ Fe(C5 H 5 ) 2 ] дициклопентадиенилжелезо.
15.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТВажнейшим вопросом является форма и пространственная структура координационного
соединения, которая обусловлена числом лигандов и типом гибридизации орбиталей
координационного центра:
1
1
1
1. K [ Ag (CN ) 2 ]1
1
1
1
[
Ag
(
CN
)
]
Связь рассматривают только для внутренней сферы:
2
Комплексное соединение содержит два (2) лиганда, следовательно молекула линейная,
комплексообразователь проявляет sp-гибридизацию. Пространственная структура
комплексного соединения будет:
L КЦ L
180
16.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ2. [КЦ L3]
Для такого типа соединений характерна плоская тригональная структура, поскольку
координационный центр находится в sp 2 гибридизации:
17.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ3. [КЦ L4] Для такого типа соединений характерна плоская тетраэдрическая структура,
поскольку координационный центр находится в sp 3 гибридизации, что характерно для
Zn, Hg , как координационного центра:
Если sp 2 d гибридизация координационного центра, то для соединения характерна
плоская квадратная форма, что характерно для Pt, Pd , как координационного центра:
18.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ4. [КЦ L5] Для такого типа соединений характерна sp 3 d гибридизации, что характерно
для внешнеорбитального прирамидального или тригонального бипирамидального
комплексного соединения:
Если dsp 3 гибридизация координационного центра, то образуется внутриорбитальное
пирамидальное соединение:
19.
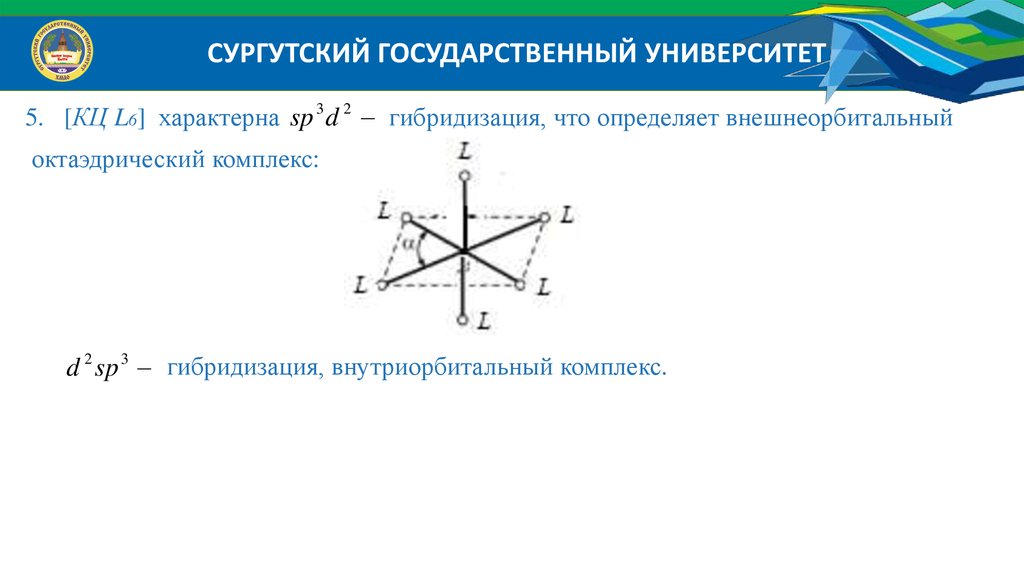
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ5. [КЦ L6] характерна sp 3 d 2 гибридизация, что определяет внешнеорбитальный
октаэдрический комплекс:
d 2 sp 3 гибридизация, внутриорбитальный комплекс.
20.
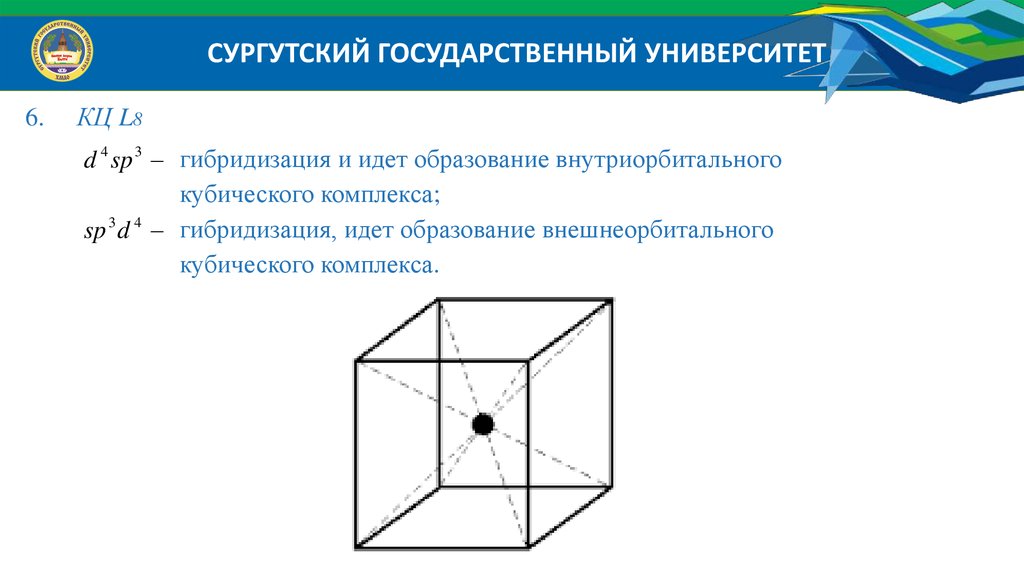
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ6.
КЦ L8
d 4 sp 3 гибридизация и идет образование внутриорбитального
кубического комплекса;
sp 3 d 4 гибридизация, идет образование внешнеорбитального
кубического комплекса.
21.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТВ зависимости от природы лигандов может происходить изменение электронной
структуры координационого центра.
Лиганды обладают разной поляризающей активностью: сильнополяризующие
лиганды приводят к расщеплению d-подуровня на два.
Слабополяризующие лиганды: I Br SCN Cl NO3 F
Лиганды средней поляризующей силы: OH C 2 O42 H 2 O NCS NH 3 F
Сильнополяризующие лиганды: en CN CO органические.молекулы
Например: лиганд (NH3) не расслаивает d-подуровень Cr, а у Co - расслаивает на два
подподуровня. Изменение электронной конфигурации объясняется теорией
кристаллического поля.
22.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТОписание электронной структуры Ϭ-комплекса:
[Cr ( NH 3 ) 6 ]Cl 3 трихлоридгексаамминхрома;
[Co( H 2 O) 6 ]Cl 2 дихлоридгексааквакобальта
Описание электронной структуры Ϭ-π-комплекса:
[ Fe(CO ) 5 ] пентакарбонилжелезо;
K 4 [ Fe(CN ) 6 ] гексацианоферраттетракалия.
Описание электронной структуры π-комплекса:
[Cr (C6 H 6 ) 2 ] дибензолхром;
[ Pt (C2 H 4 )Cl2 ] дихлороэтиленплатины;
[ Fe(C5 H 5 ) 2 ] дициклопентадиенилжелезо.
23.
СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТСпасибо за внимание!
Вопросы?




















 Химия
Химия








