Похожие презентации:
Этапы доказательной медицины в работе с Pico. Четвертый и пятый этапы
1.
Корпоративный фонд “University Medical Center”ЭТАПЫ
доказательной медицины.
Четвертый и пятый этапы
Исатаева Нагима Мухамедрахимовна,
зам. директора ДОМП, к.м.н.
2. 4 и 5 этапы ДМ
• Внедрение результатов критическойоценки в клиническую практику и
оценка результатов проделанной
работы – клинический аудит
3. Guidelines/Рекомендации — это положения, разработанные определенным методом, для того, чтобы помочь врачу и пациенту в принятии решений относи
Guidelines/Рекомендации —это положения, разработанные
определенным методом, для того,
чтобы
помочь врачу и пациенту в
принятии решений относительно
врачебной тактики при
определенных клинических
ситуациях
USA, Institute of Medicine
4. В Республике Казахстан используются клинические протоколы, разработанные на основе международных клинических руководств
5.
• Нужны ли клинические протокола?• Они обязательные? Кем
утверждаются КП?
• Клинические руководства? Их место
в клинической практике?
• А сколько их?
• На все коды МКБ-10 должны быть
КП?
• Кем разрабатываются КП? Каждой
МО?
• Где найти КП?
6.
• Приказ Министра здравоохранения исоциального развития Республики Казахстан
от 30 ноября 2015 года № 926 «О создании
Объединенной комиссии по качеству
медицинских услуг»
(Поручения Президента 100 шагов – 82 шаг)
• Основными задачами Комиссии является
выработка рекомендаций по
совершенствованию:
• клинических протоколов;
• стандартов медицинского образования,
лекарственного обеспечения, системы контроля
качества и доступности услуг в области
здравоохранения.
7.
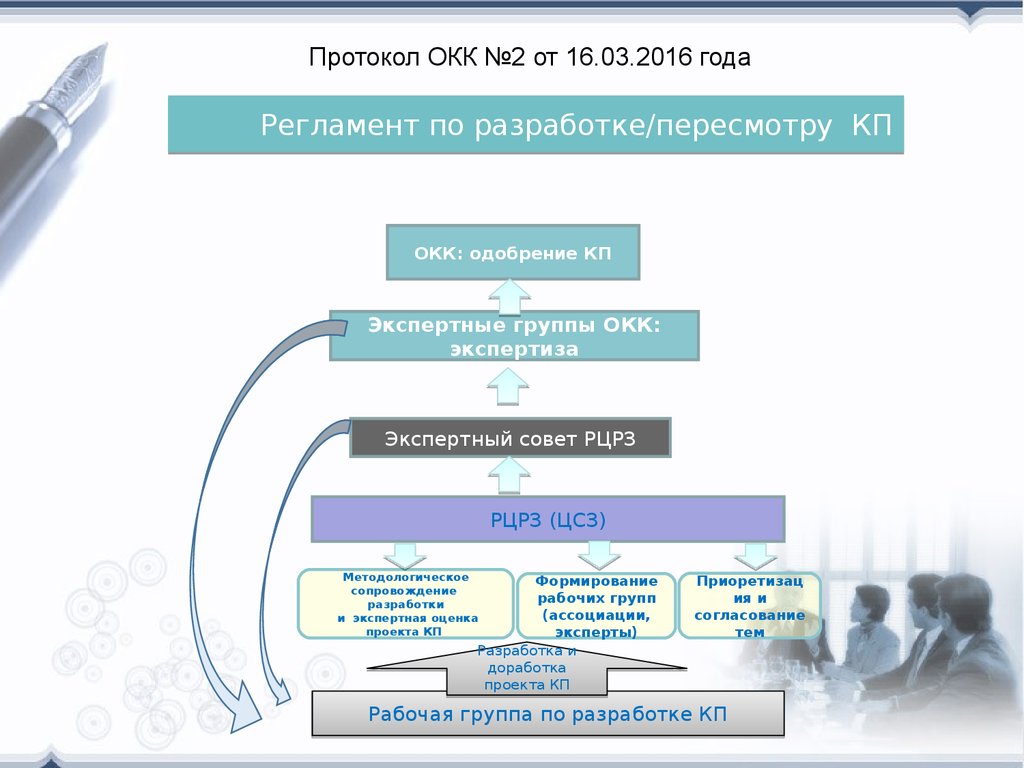
Протокол ОКК №2 от 16.03.2016 годаРегламент по разработке/пересмотру КП
ОКК: одобрение КП
Экспертные группы ОКК:
экспертиза
Экспертный совет РЦРЗ
РЦРЗ (ЦСЗ)
Методологическое
сопровождение
разработки
и экспертная оценка
проекта КП
Формирование
рабочих групп
(ассоциации,
эксперты)
Разработка и
доработка
проекта КП
Приоретизац
ия и
согласование
тем
Рабочая группа по разработке КП
8.
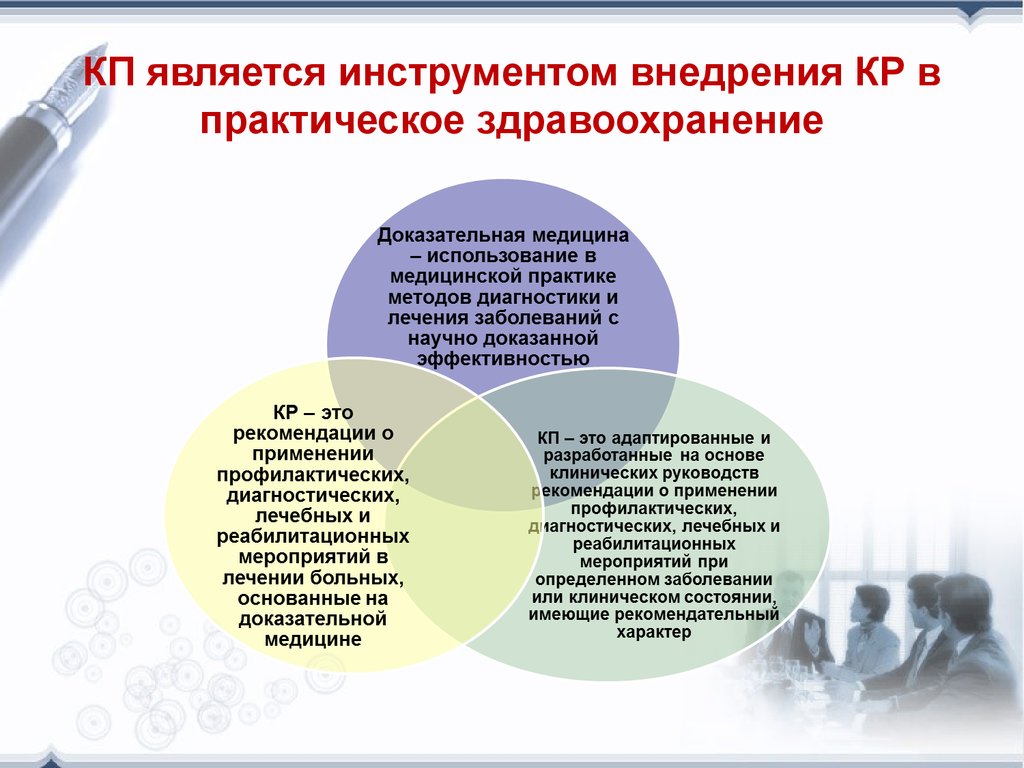
9. КП является инструментом внедрения КР в практическое здравоохранение
10. Клинические протоколы
• адаптированы и разработаны на основеклинических руководств рекомендации
о применении профилактических,
диагностических, лечебных и
реабилитационных мероприятий при
определенном заболевании или
клиническом состоянии
11.
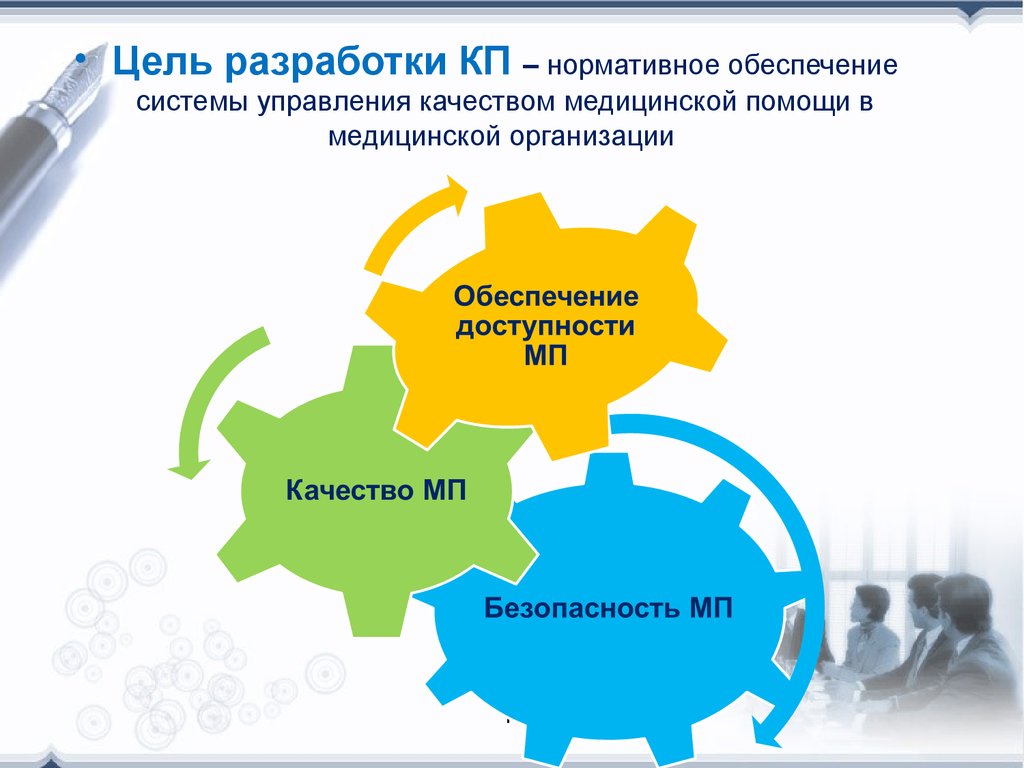
• Цель разработки КП – нормативное обеспечениесистемы управления качеством медицинской помощи в
медицинской организации
11
12. Этапы разработки КП
подача заявки на разработку КП;
приоритезация темы КП;
разработка/пересмотр КП;
рецензирование КП;
экспертиза КП;
согласование КП на ЭС РЦРЗ;
одобрение КП ОКК
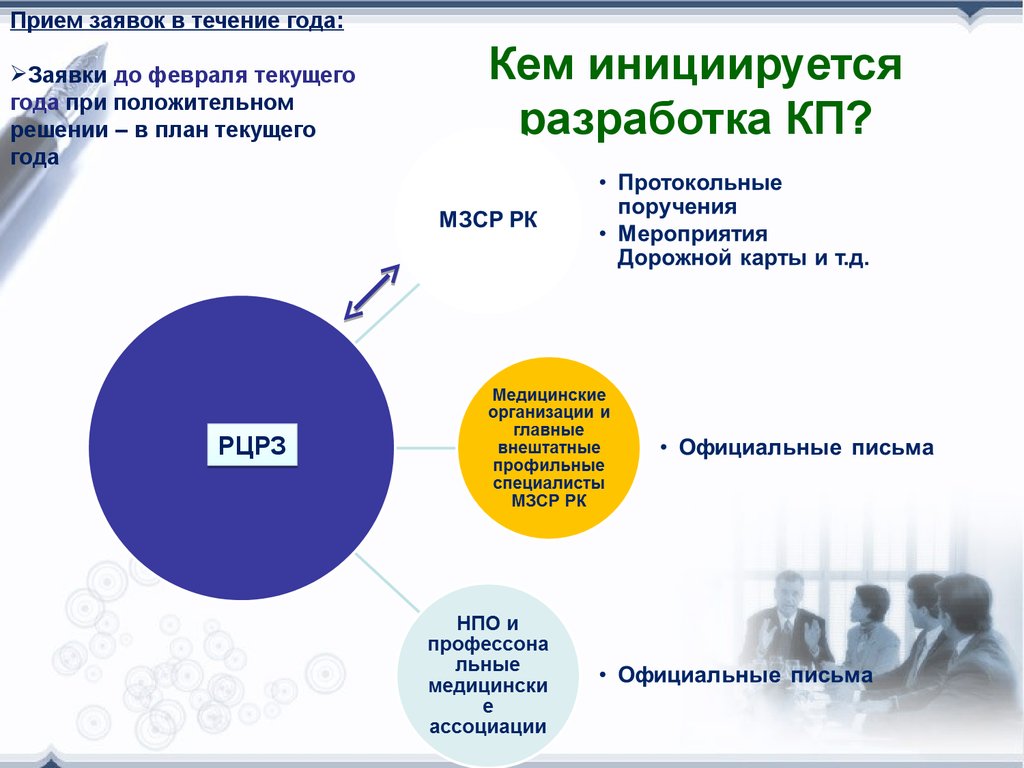
13. Кем инициируется разработка КП?
Прием заявок в течение года:Заявки до февраля текущего
года при положительном
решении – в план текущего
года
РЦРЗ
Кем инициируется
разработка КП?
14.
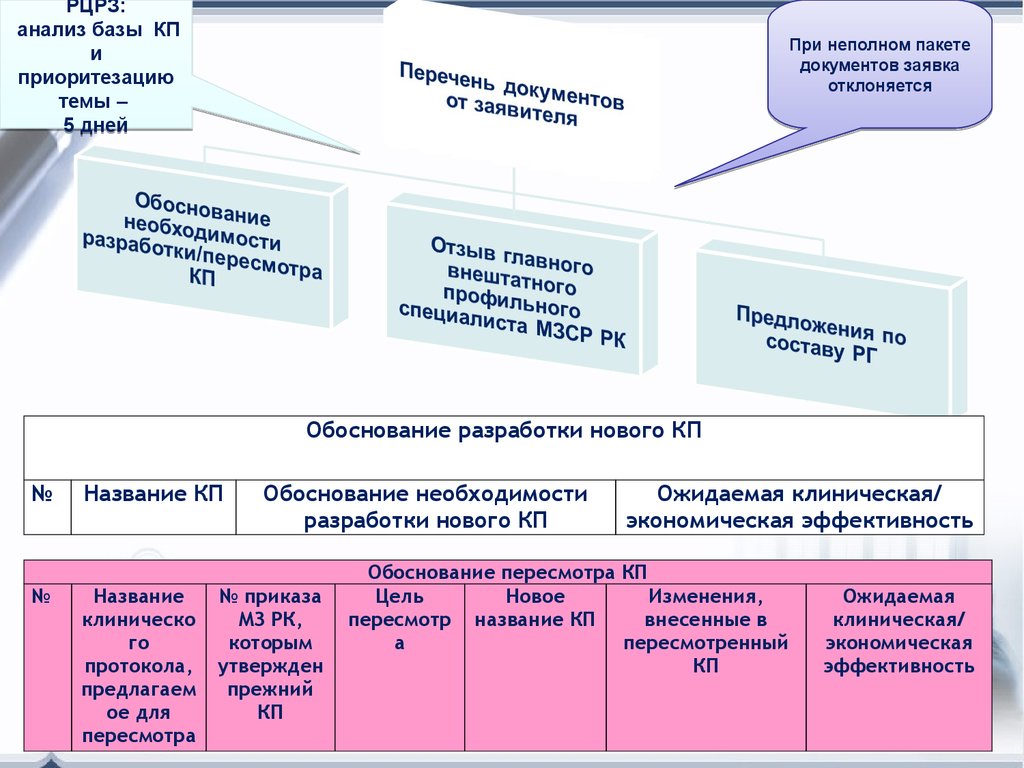
РЦРЗ:анализ базы КП
и
приоритезацию
темы –
5 дней
При неполном пакете
документов заявка
отклоняется
Обоснование разработки нового КП
№
№
Название КП
Название
клиническо
го
протокола,
предлагаем
ое для
пересмотра
Обоснование необходимости
разработки нового КП
№ приказа
МЗ РК,
которым
утвержден
прежний
КП
Ожидаемая клиническая/
экономическая эффективность
Обоснование пересмотра КП
Цель
Новое
Изменения,
пересмотр название КП
внесенные в
а
пересмотренный
КП
Ожидаемая
клиническая/
экономическая
эффективность
15. Критерии приоритезации тем КП
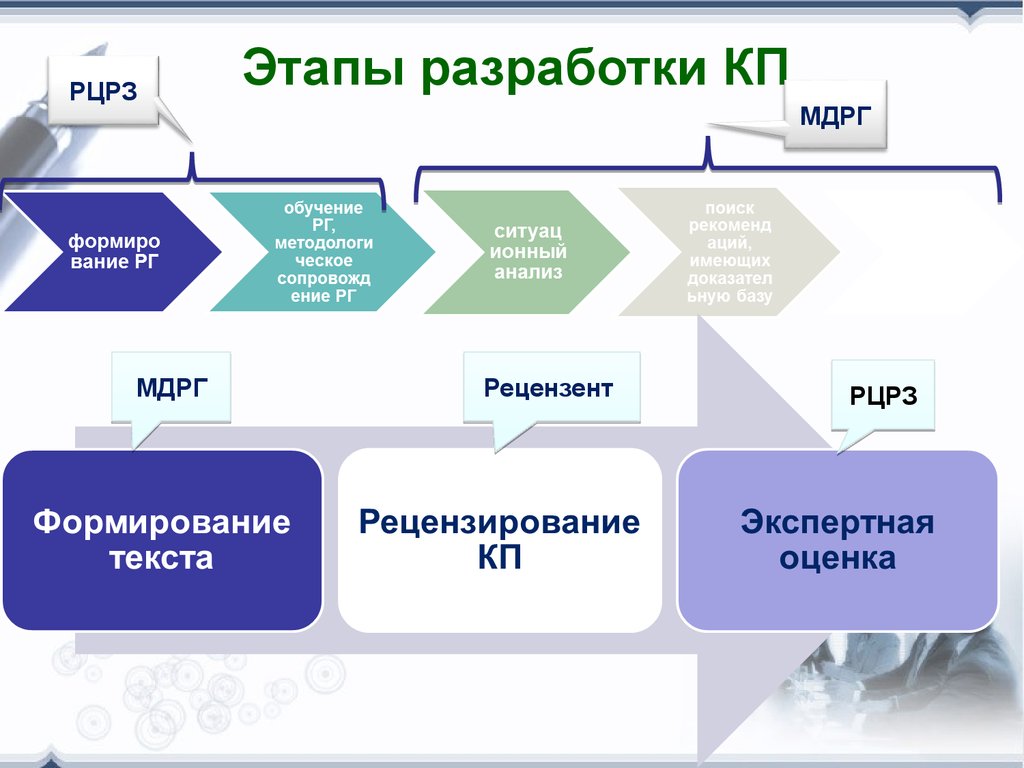
16. Этапы разработки КП
РЦРЗМДРГ
Этапы разработки КП
МДРГ
Рецензент
РЦРЗ
17. Формирование РГ
Включатьспециалистов всех
необходимых
профилей в
соответствии с
темой КП из
медицинских
организаций разного
уровня оказания МП
(не менее 3 МО)
из числа специалистов
научных медицинских
организаций, ВУЗов,
профессиональных ассоциаций
медицинских работников,
неправительственных
организаций;
имеющие стаж работы по
специальности не менее 5 лет;
имеющие научные
публикации по данной теме;
имеющие навыки
экспертной оценки и знания в
области доказательной медицины
информацию о существующих
финансовых
взаимоотношениях с
фармацевтическими
компаниями, производителями
лекарственных средств и
медицинской техники
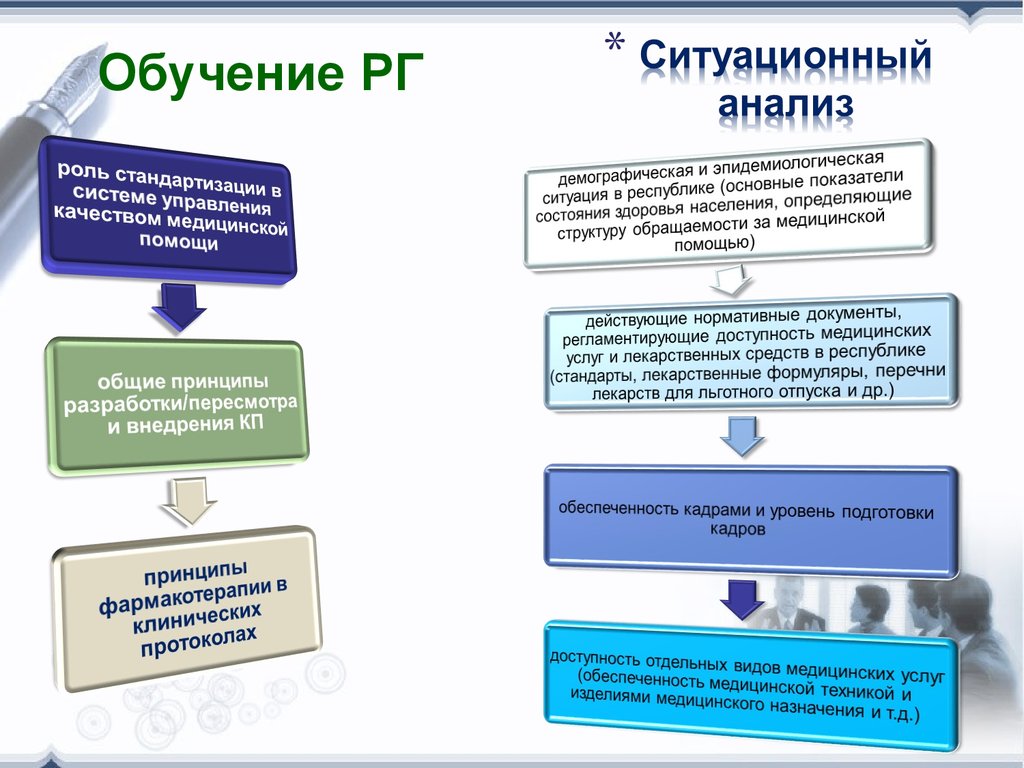
18. Обучение РГ
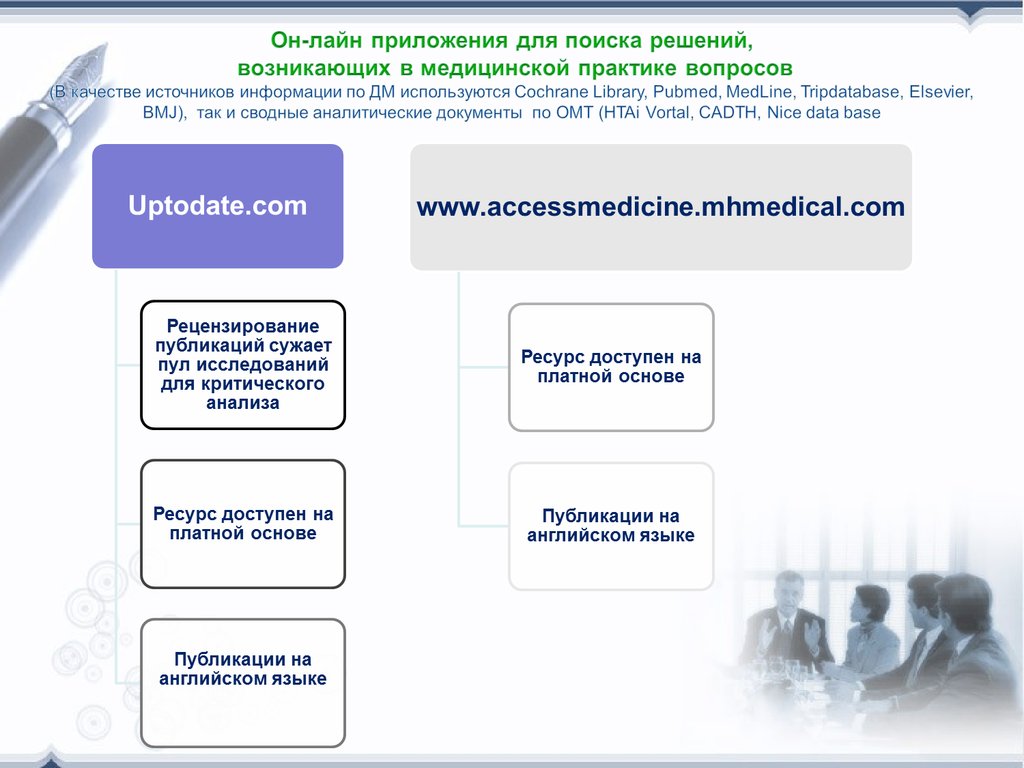
19. Поиск рекомендаций на основе ДМ
20.
21.
22.
23.
Соотношение между степенью убедительности доказательств ивидом научных исследований
Шкала
A
В
Степень убедительности
доказательств
Доказательства убедительны: есть
веские
доказательства
предлагаемому утверждению
Относительная
убедительность
доказательств:
есть
достаточно
доказательств в пользу того, чтобы
рекомендовать данное предложение
C
Достаточных
доказательств
нет:
имеющихся
доказательств
недостаточно
для
вынесения
рекомендации, но рекомендации
могут быть даны с учетом иных
обстоятельств
Виды научных исследований
Высококачественный систематический обзор,
мета-анализ.
Большие
рандомизированные
клинические
исследования с низкой вероятностью ошибок и
однозначными результатами.
Небольшие рандомизированные клинические
исследования с неоднозначными результатами и
средней или высокой вероятностью ошибок.
Большие проспективные сравнительные, но
нерандомизированные исследования.
Качественные ретроспективные исследования
на больших выборках больных с тщательно
подобранными группами сравнения.
Ретроспективные сравнительные исследования.
Исследования на ограниченном числе больных
или на отдельных больных без контрольной
группы.
Личный
неформализованный
опыт
разработчиков.
24.
Методы принятия решенийтся
е
у
з
и
актер
де й
р
и
а
х
х
»
ы
нов
таки
а
м
й
е
о
и
в
н
ния
о
е
е
г
л
ж
з
в
и
о
я
в
«м
по
ыд
Метод разным в оценки до зуется для
ь
об
ой
л
о
к
о
н
с
п
и
е
с
в
ч
И
.
ла
н ой
ти
я
и
д
и
о
р
н
к
я
е
без их ьного реш го решени
ал
ше
оптим ска наилуч блемы.
пои
про
25.
Методы принятия решенийМетод «Липки:
подготовительный этап - поиск и изучение
необходимой литературы, написание отдельных
фрагментов КП, проведение предварительных
рабочих совещаний с постановками вопросов;
этап интерактивного моделирования –
разработчики КП собираются вместе в
изолированном месте на 1-2 дня и в режиме
реального времени, используя компьютерную
технику с электронной версией документа, создают
1-2 модели пациента, при этом оттачиваются
формулировки, рассматриваются доказательства
клинической и экономической эффективности,
ищется согласие по отнесению тех или иных
технологий к обязательным или дополнительным
разделам). При этом используются методы «мозговой
атаки», коллективной генерации идей, построения
сценариев и т.д.;
этап консолидации КП – на основании разработанной
модели, с учетом высказанных мнений, обоснований,
разработчики заканчивают разработку КП, дополняют его
недостающими разделами, после чего он, в
установленном порядке, отправляется на утверждение.
26.
27.
28. Выбор ЛС
29.
30. Внедрение КП для решения следующих задач:
31.
32.
Формирование текста КП33.
Рецензирование КП• Для рецензирования КП проводится отбор рецензентов КП из числа
профильных ведущих отечественных или зарубежных специалистов в
соответствии с профилем КП согласно следующим требованиям:
• специалисты, не принимавшие участия в разработке/пересмотре КП;
• имеющие стаж работы по специальности не менее 10 лет;
• наличие ученой степени (не ниже/равное уровню ученой степени
разработчиков КП);
• имеющие научные публикации по данной теме;
• имеющие навыки и знания в области доказательной медицины.
• Если КП касается нескольких медицинских профилей, то для его
рецензирования привлекаются специалисты соответствующих профилей.
• Кандидатуры рецензентов КП утверждаются на ЭС РЦРЗ (не менее
одного рецензента на один КП).
• РЦРЗ официально
рецензирование.
направляет
рецензентам
проекты
КП
на























 Медицина
Медицина Информатика
Информатика








