Похожие презентации:
Амины. Анилин
1. АМИНЫ
АНИЛИН2.
Амины- это органические соединения,представляющие собой производные
аммиака, в молекуле которого один,
два или три атома водорода замещены
на углеводородный радикал.
3. По числу атомов водорода в молекуле аммиака, замещенных на радикалы, различают:
Первичные амины(в молекуле аммиака на
радикал замещен один
атом водорода)
H3C—NH2
метиламин
Функциональная
группа
-NH2
называется
аминогруппой
C6H5—NH2
фениламин (анилин)
4.
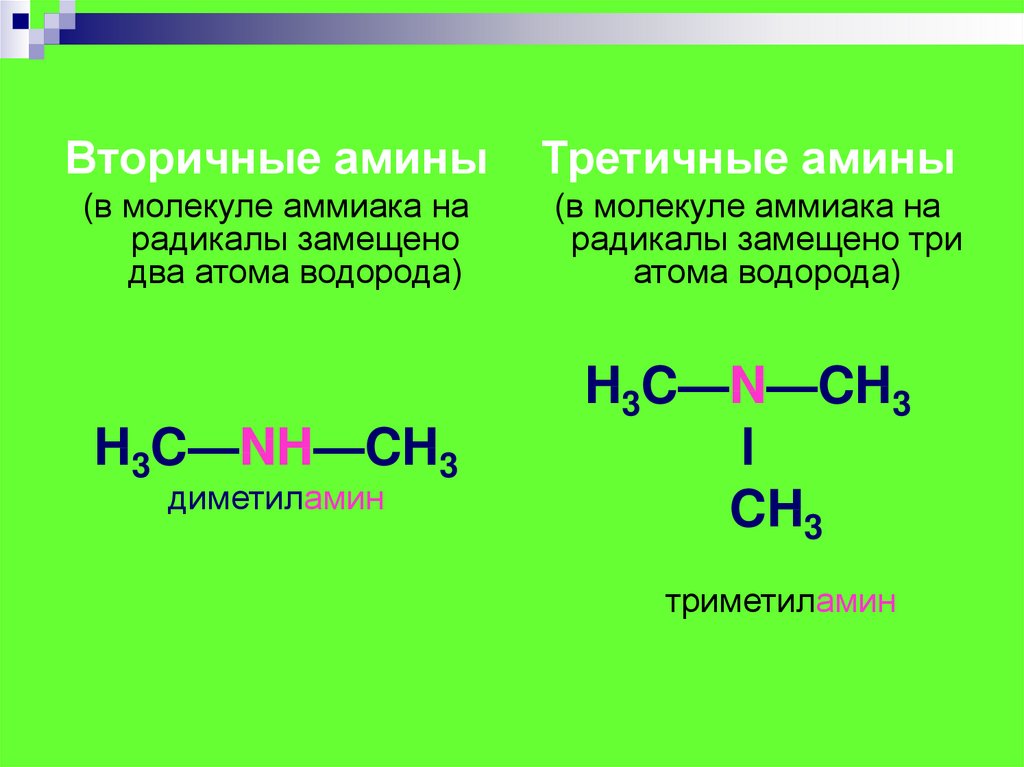
Вторичные амины(в молекуле аммиака на
радикалы замещено
два атома водорода)
H3C—NH—CH3
диметиламин
Третичные амины
(в молекуле аммиака на
радикалы замещено три
атома водорода)
H3C—N—CH3
l
CH3
триметиламин
5.
Физические свойства аминовПростейшие амины (метиламин,
диметиламин, триметиламин)– газообразные
вещества.
Низшие амины– жидкости, которые
хорошо растворяются в воде.
Имеют характерный запах, напоминающий
запах аммиака.
6.
Химические свойства аминовАмины – органические основания.
Атом азота аминогруппы может образовывать
ковалентную связь по донорно-акцепторному
механизму, выступая в роли донора.
H H H C N H
H 3C N
2
3
3
донор
акцептор
ион метиламмония
1) Растворы аминов в воде дают щелочную реакцию:
CH3—CH2—NH2 + H2O → CH3—CH2—NH3 + OH-
7.
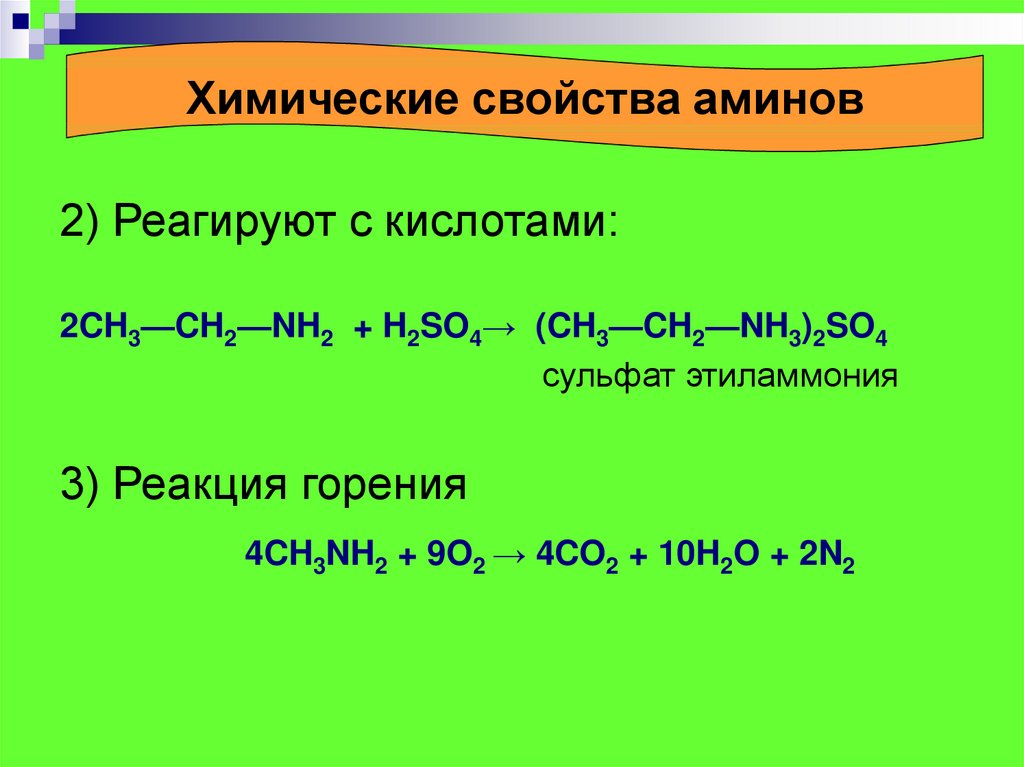
Химические свойства аминов2) Реагируют с кислотами:
2CH3—CH2—NH2 + H2SO4→ (CH3—CH2—NH3)2SO4
сульфат этиламмония
3) Реакция горения
4CH3NH2 + 9O2 → 4CO2 + 10H2O + 2N2
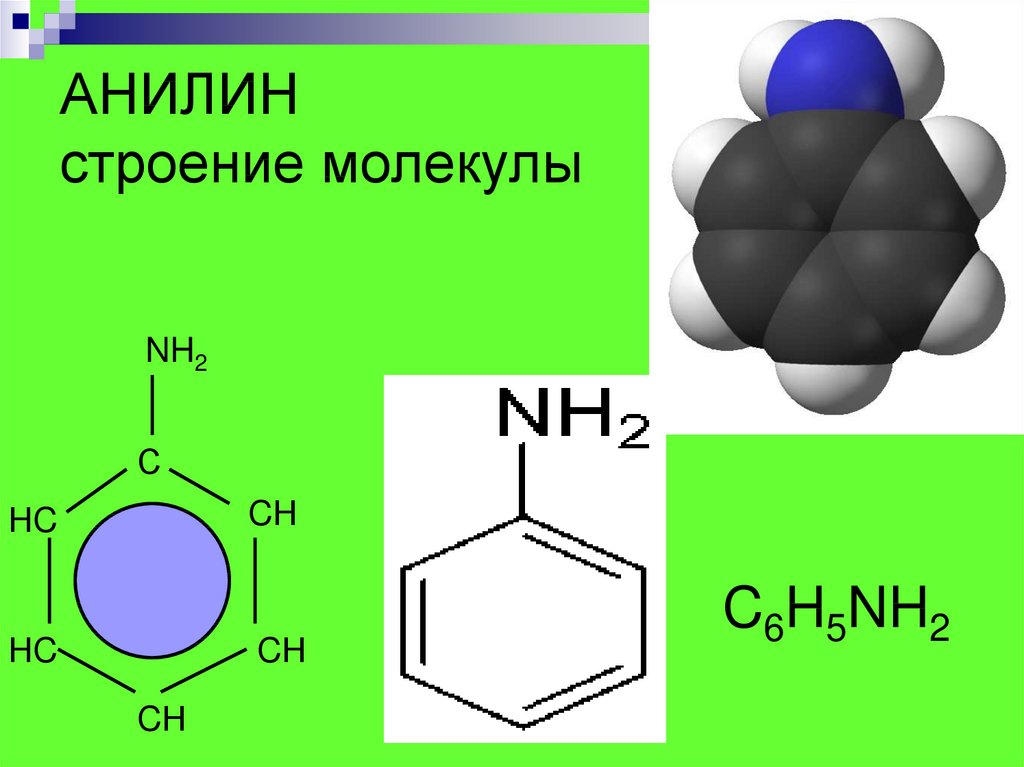
8. АНИЛИН строение молекулы
NH2С
CН
НC
НC
CН
CН
C6H5NH2
9.
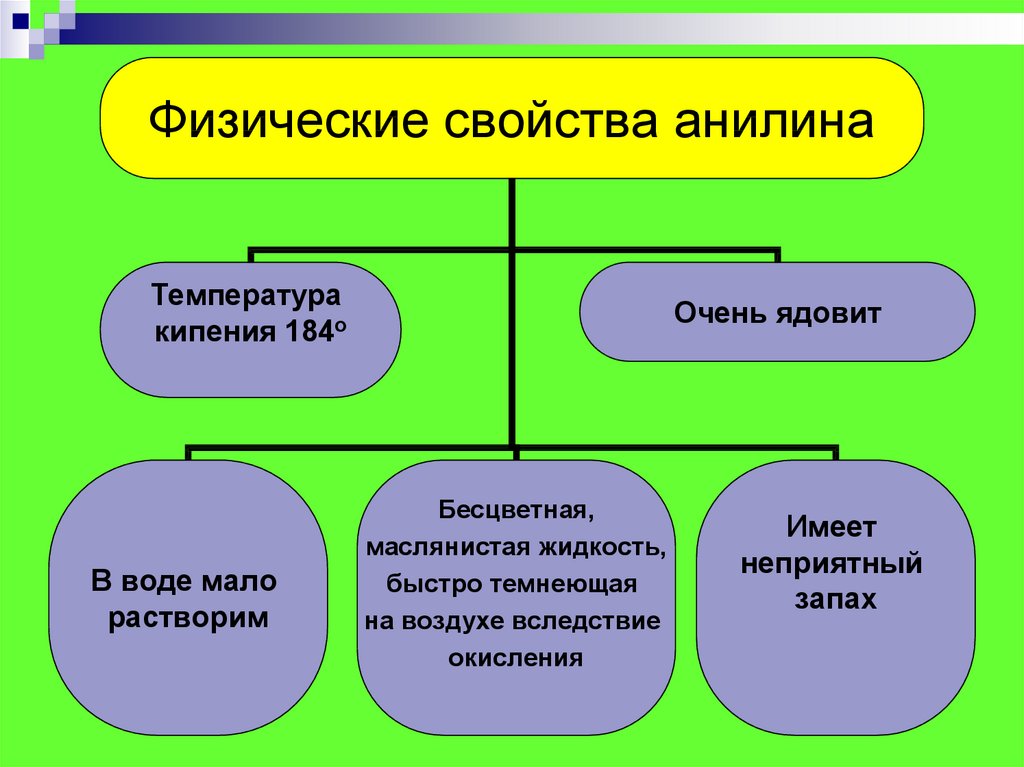
Физические свойства анилинаТемпература
кипения 184о
В воде мало
растворим
Очень ядовит
Бесцветная,
маслянистая жидкость,
быстро темнеющая
на воздухе вследствие
окисления
Имеет
неприятный
запах
10.
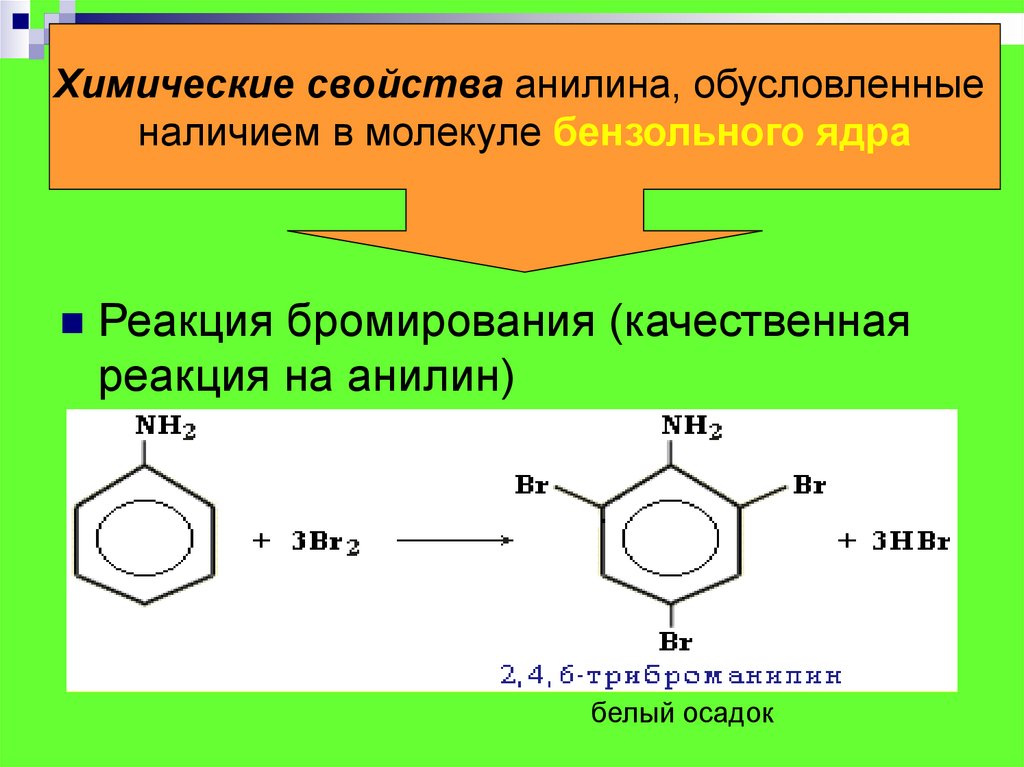
Химические свойства анилина, обусловленныеналичием в молекуле бензольного ядра
Реакция бромирования (качественная
реакция на анилин)
белый осадок
11.
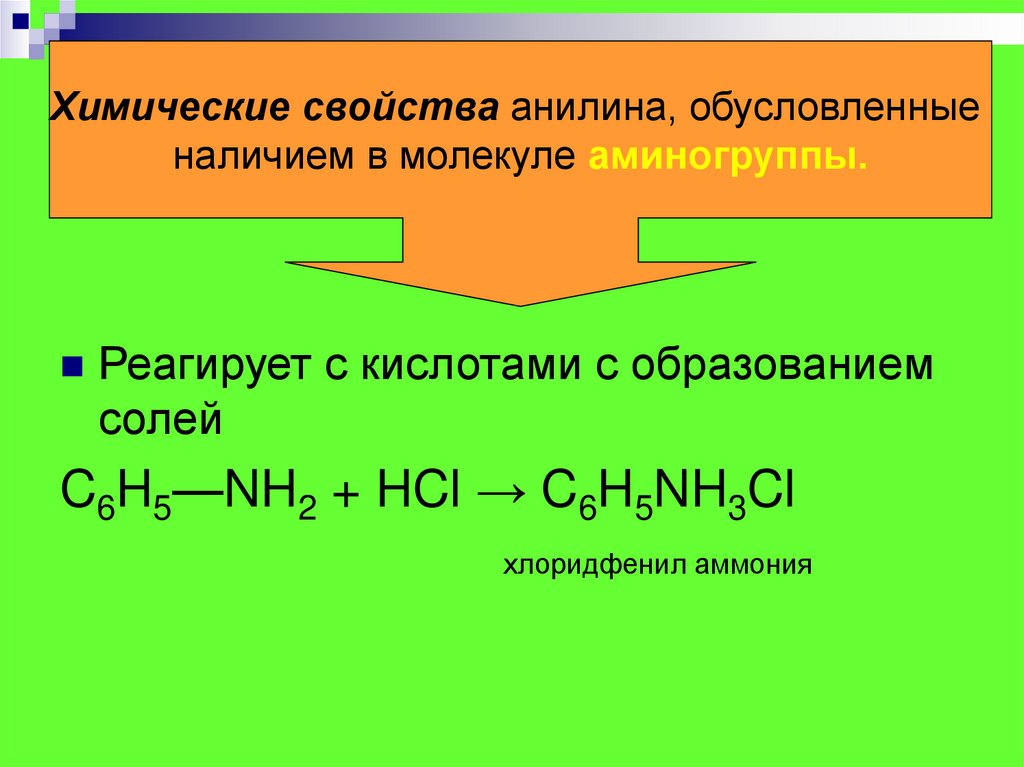
Химические свойства анилина, обусловленныеналичием в молекуле аминогруппы.
Реагирует с кислотами с образованием
солей
C6H5—NH2 + HCl → C6H5NH3Cl
хлоридфенил аммония
12.
Зинин НиколайНиколаевич.
Русский химикорганик,
академик. Открыл
(1842) реакцию
восстановления
ароматических
нитросоединений
и получил анилин.
13. Получение анилина
Реакция ЗининаС6H5NO2 + 6[H]
2 O ,t
Fe
H
C6H5NH2 + 2H2O
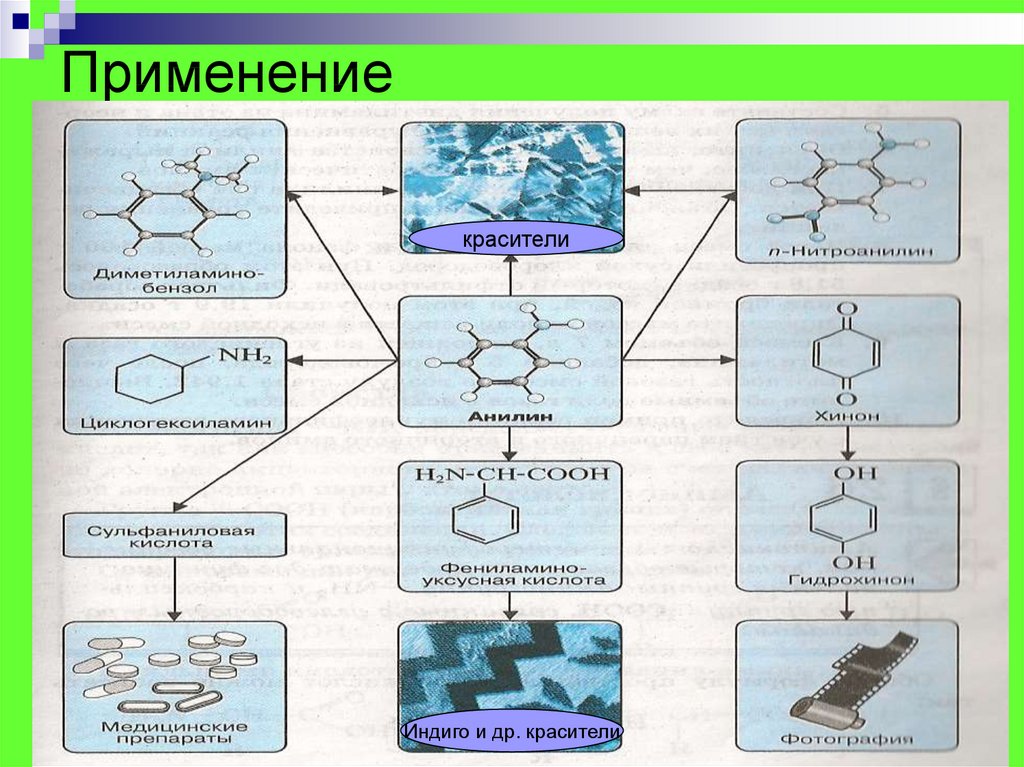
14. Применение
красителиИндиго и др. красители







 Химия
Химия








