Похожие презентации:
Кислородсодержащие органические соединения
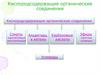
1. КИСЛОРОДСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
2.
КИСЛОРОДСОДЕРЖАЩИЕ
СОЕДИНЕНИЯ
СПИРТЫ
АЛЬДЕГИДЫ
КАРБОНОВЫЕ
КИСЛОТЫ
СЛОЖНЫЕ
ЭФИРЫ
3.
СПИРТЫОДНОАТОМНЫЕ
МНОГОАТОМНЫЕ
4. ОДНОАТОМНЫЕ СПИРТЫ
Сложные вещества с общей формулойСnН2n+1ОН, в которых гидроксильная
группа соединена с углеводородным
радикалом.
5. Правила названия спиртов
Название предельного углеводорода +суффикс -ол.
СН3ОН – метанол (метиловый спирт)
С2Н5ОН – этанол (этиловый спирт)
С3Н7ОН – пропанол
С4Н9ОН – бутанол
6. Метанол СН3ОН
Бесцветная жидкость, с водойсмешивается в любых соотношениях.
Горит бесцветным пламенем.
ОЧЕНЬ ЯДОВИТ!
Небольшое количество – общее
отравление и слепота, большие
количества смертельны.
7. Этанол С2Н5ОН
Бесцветная жидкость со слабым запахом ижгучим вкусом.
Смешивается с водой в любых
соотношениях.
Горит голубоватым пламенем.
8. Получение этанола
1. Гидратация этилена:СН2 = СН2 + Н2О С2Н5ОН
2. Брожение сахаристых веществ:
С6Н12О6 2С2Н5ОН +2СО2
9. Химические свойства спиртов
1. ГорениеС2Н5ОН + 3О2 2СО2 + 3Н2О
2. Окисление
С2Н5ОН + [ O ] CH3 – C=O
|
H
уксусный альдегид
10. Химические свойства спиртов
3. Взаимодействие со щелочнымиметаллами
2С2Н5ОН + 2Na 2С2Н5ОNa + H2
11. Действие этанола на организм человека
Разрушение клеток печени.Общее отравление организма.
Нарушение работы желудочно-кишечного
тракта, сердечно-сосудистой системы.
Деградация личности.
12. Многоатомные спирты
СН2 – ОН|
CH2 – OH
Этиленгликоль
CH2 – OH
|
CH – OH
|
CH2 – OH
Глицерин
Бесцветные, сиропообразные жидкости, сладковатые
на вкус. Ядовиты!
13. Альдегиды
Органические вещества, в молекулахкоторых содержится альдегидная группа
–С=О
|
Н
14. Правила названия альдегидов
Название предельного углеводорода + суффикс –аль.
Н – С = О - метаналь (муравьиный альдегид)
|
H
СН3 – С = О - этаналь (уксусный альдегид)
|
Н
15. Физические свойства альдегидов
Этаналь – бесцветная летучая жидкость срезким запахом. Хорошо растворим в
воде.
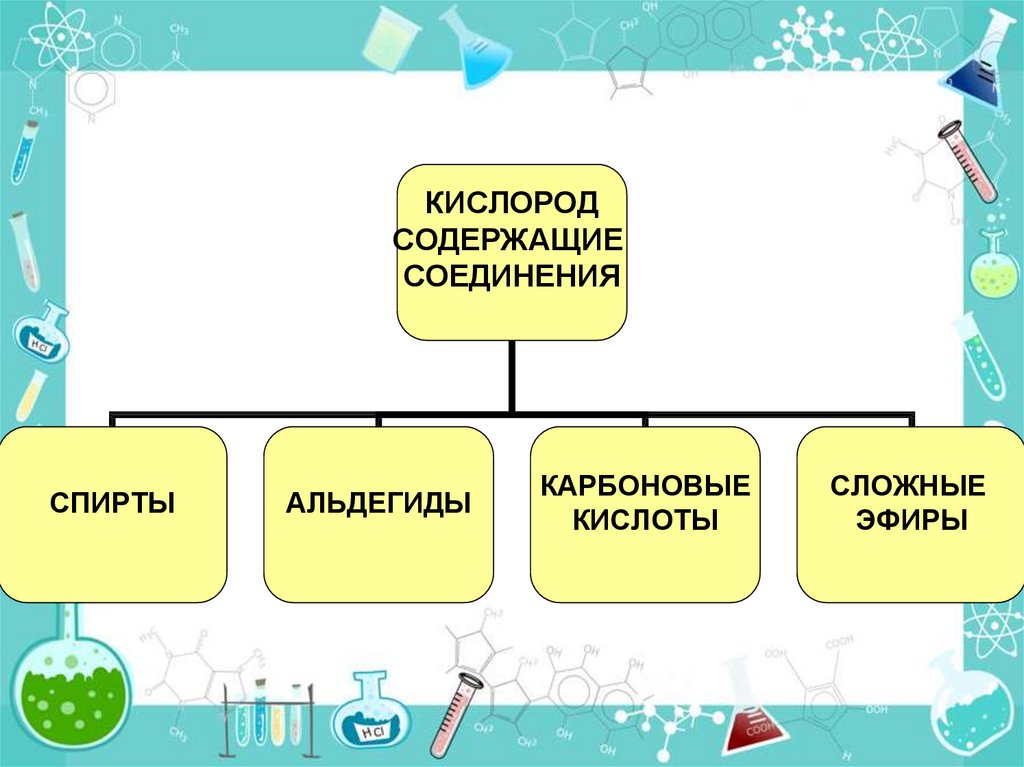
16. Химические свойства альдегидов
Окисление:СН3 – С= О + Ag2O CH3 – C = O + 2Ag
|
|
H
OH
Этаналь
Уксусная кислота
Реакция «серебряного зеркала».
17. Карбоновые кислоты
Органические вещества, в молекулахкоторых содержится карбоксильная
группа – С = О
|
OH
18. Правила названия карбоновых кислот
Название предельного углеводорода + -овая кислота.Н–С= О
метановая кислота (муравьиная)
|
ОН
СН3 – С = О
этановая кислота (уксусная)
|
OH
С17Н35 – С = О
стеариновая кислота
|
OH
19.
Физические свойства уксуснойкислоты
Бесцветная жидкость с резким запахом.
Физические свойства стеариновой
кислоты
Бесцветные кристаллы, нерастворимы в
воде
20. Химические свойства уксусной кислоты
Проявляет характерные свойства кислот.1. Изменяет окраску индикатора:
СН3СООН СН3СОО- + Н+
2. Взаимодействует с металлами:
2СН3СООН + Мg (CH3COO)2Mg + H2
21. Химические свойства уксусной кислоты
3. Взаимодействует с основными оксидами:2СН3СООН + СаО (CH3COO)2Ca + H2O
4. Взаимодействует с основаниями:
СH3COOH + NaOH CH3COONa + H2O
5. Взаимодействует с солями:
2CH3COOH + Na2CO3 2CH3COONa + CO2 + H2O
22.
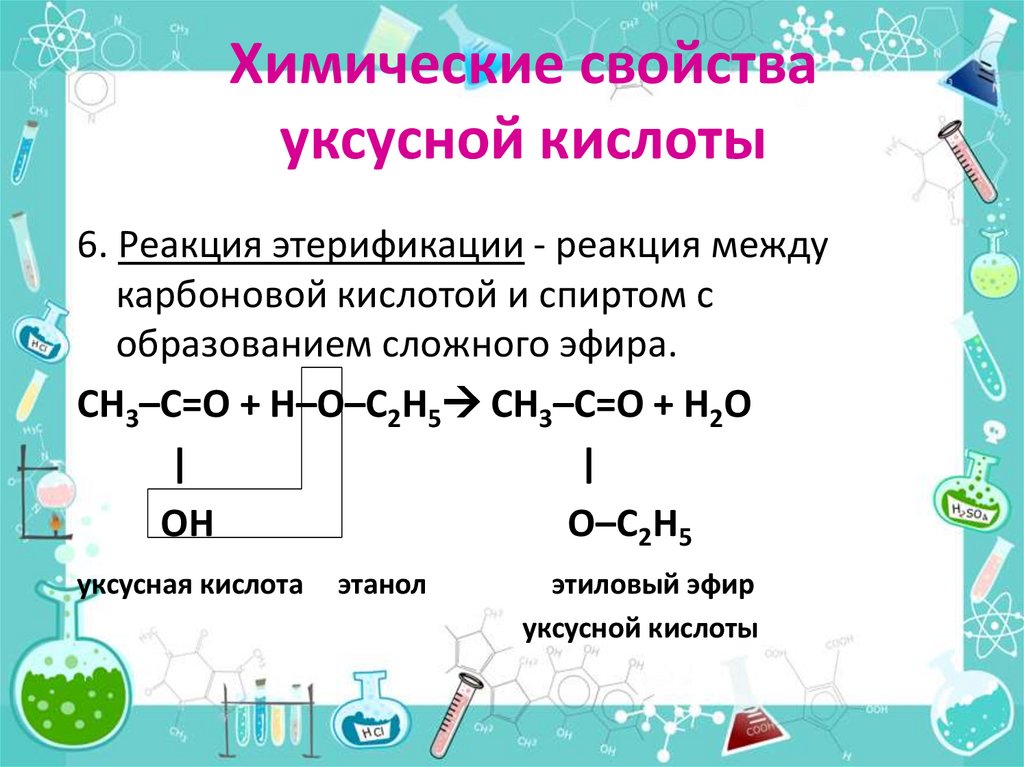
Химические свойствауксусной кислоты
6. Реакция этерификации - реакция между
карбоновой кислотой и спиртом с
образованием сложного эфира.
CH3–C=O + H–O–C2H5 CH3–C=O + Н2О
|
|
OH
O–C2H5
уксусная кислота
этанол
этиловый эфир
уксусной кислоты



















 Химия
Химия