Похожие презентации:
Основные сведения о строении атома. Состав атомных ядер
1.
ОСНОВНЫЕ СВЕДЕНИЯ ОСТРОЕНИИ АТОМА.
СОСТАВ АТОМНЫХ ЯДЕР
2. Эрнест Резерфорд
В 1911 году ЭрнестРезерфорд предложил
планетарную модель
строения атома
Эрнест Резерфорд
3.
Планетарная модель4.
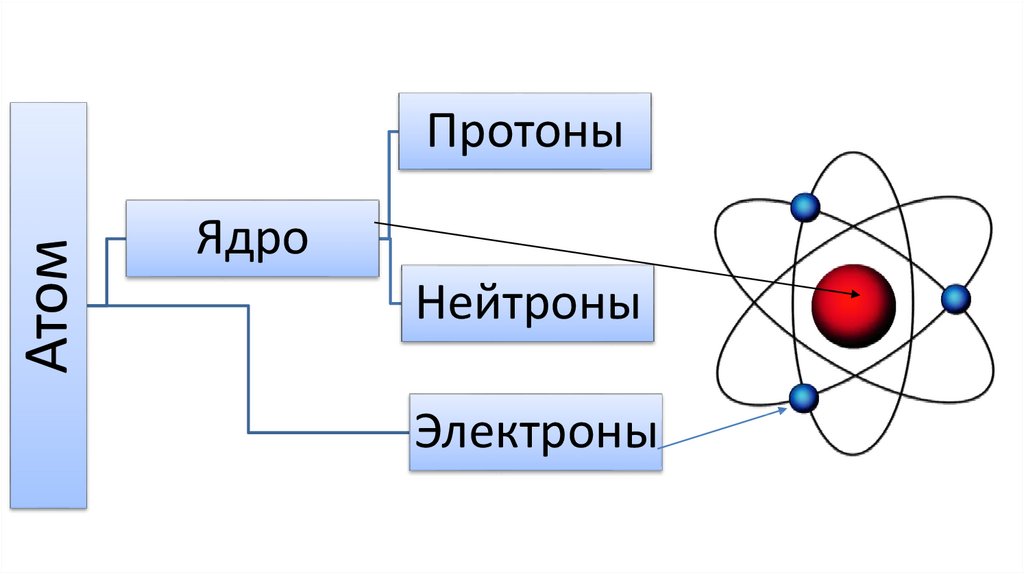
АтомПротоны
Ядро
Нейтроны
Электроны
5.
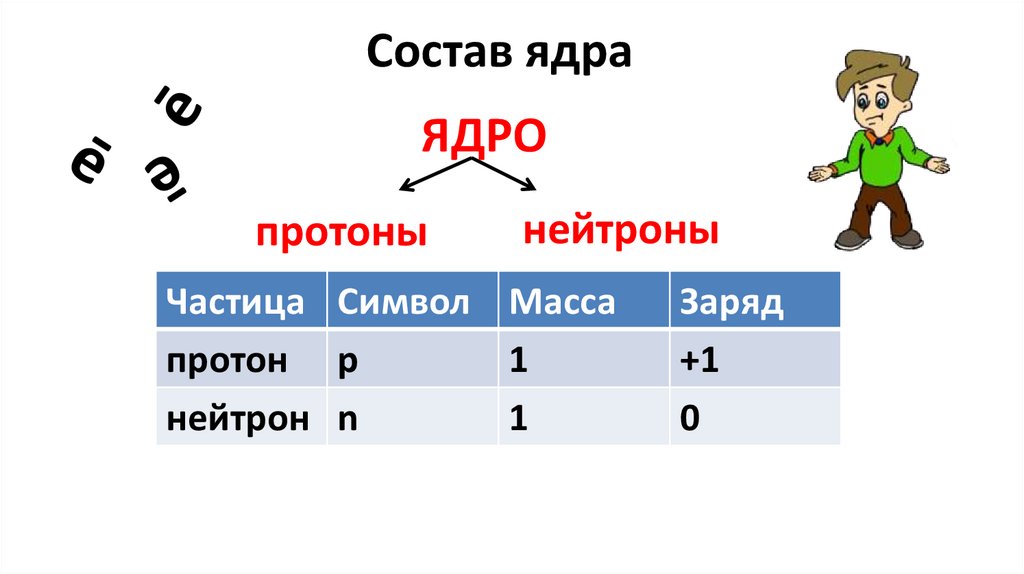
Состав ядраЯДРО
протоны
нейтроны
Частица Символ Масса
протон p
1
нейтрон n
1
Заряд
+1
0
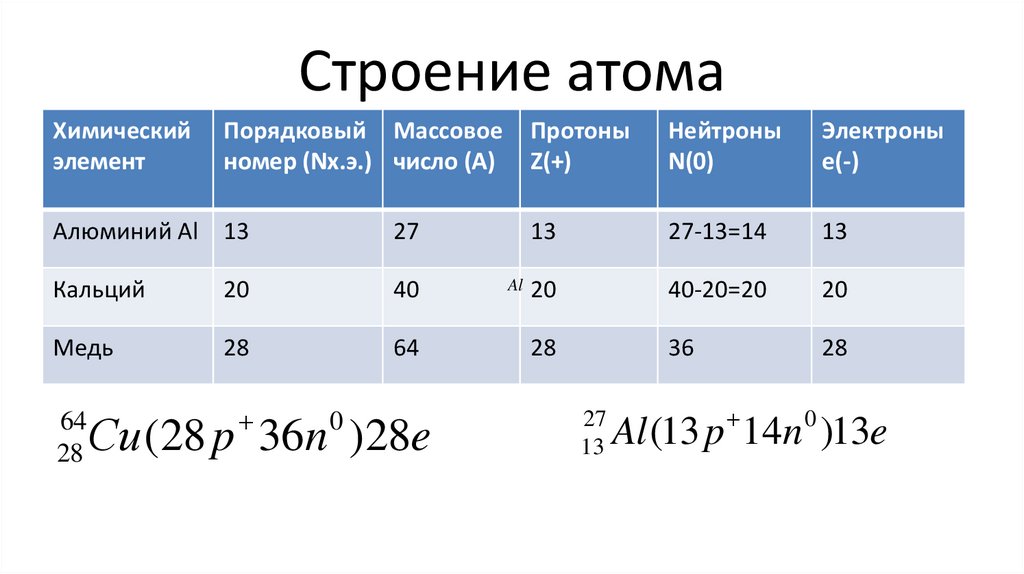
6. Строение атома
Химическийэлемент
Порядковый Массовое
номер (Nх.э.) число (А)
Алюминий Al 13
27
Кальций
20
40
Медь
28
64
64
28
Сu (28 p 36n )28e
0
Al
Протоны
Z(+)
Нейтроны
N(0)
Электроны
e(-)
13
27-13=14
13
20
40-20=20
20
28
36
28
27
13
0
Al (13 p 14n )13e
7.
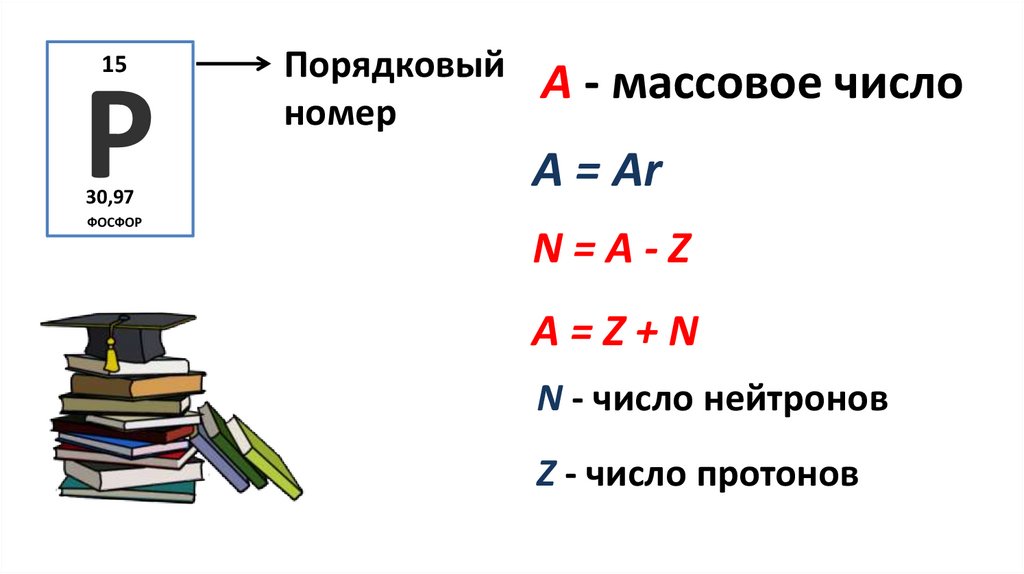
15Р
30,97
ФОСФОР
Порядковый
номер
А - массовое число
А = Ar
N=A-Z
А=Z+N
N - число нейтронов
Z - число протонов
8.
БИННИНГ И РОРЕРНаночастицы
(размер 10-9м)
9. Вывод
1.Суммарное число протонов и нейтронов в ядре называют массовымчислом. Его обозначают латинской буквой А.
2.Заряд ядра численно совпадает с порядковым (атомным) номером
элемента (Z) в периодической системе.
3.Массовое число указывают слева вверху от химического знака
элемента,
12
например, С а заряд ядра — слева внизу, например 6 С
4.Число нейтронов (N) можно вычислить по формуле:
N = А – Z.





 Химия
Химия