Похожие презентации:
Система антиоксидантной защиты
1. система антиоксидантной защиты
Кафедра биохимии и молекулярнойбиологии с курсом КЛД СибГМУ
система антиоксидантной
защиты
Жаворонок Татьяна Васильевна
2. Что такое антиоксиданты и зачем они нужны?
• Редокс-состояние и Редокс-баланс• Окислительный стресс и
Восстановительный стресс
• Соотношение про/антиоксиданты
• Широкое разнообразие антиоксидантов
• Антиоксиданты и
система антиоксидантной защиты
3.
4.
5.
6.
7.
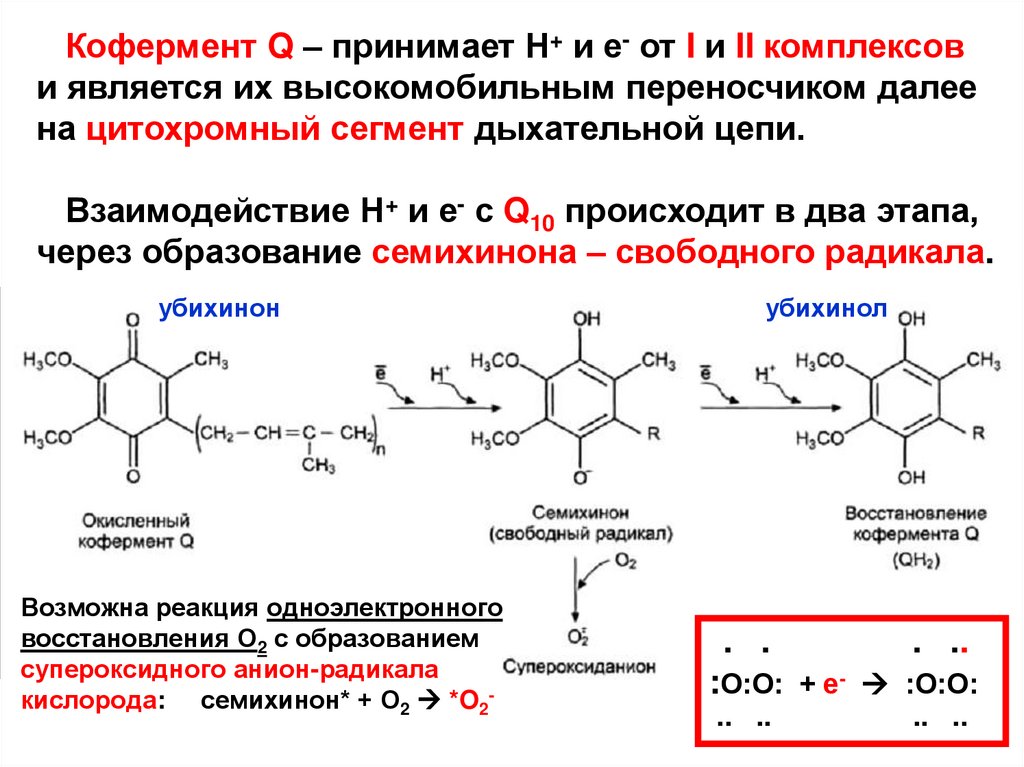
Кофермент Q – принимает Н+ и е- от I и II комплексови является их высокомобильным переносчиком далее
на цитохромный сегмент дыхательной цепи.
Взаимодействие Н+ и е- с Q10 происходит в два этапа,
через образование семихинона – свободного радикала.
убихинон
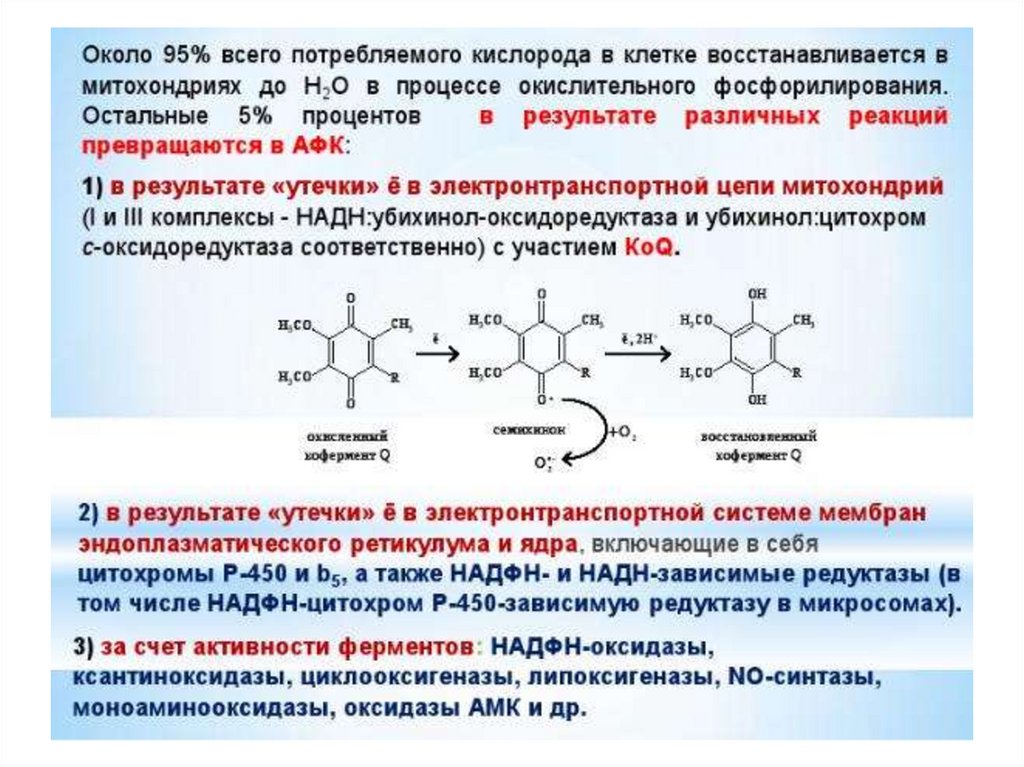
Возможна реакция одноэлектронного
восстановления О2 с образованием
супероксидного анион-радикала
кислорода: семихинон* + О2 *O2-
убихинол
. .
. ..
:О:О: + е- :О:О:
.. ..
.. ..
8. Дисбаланс и окислительный стресс
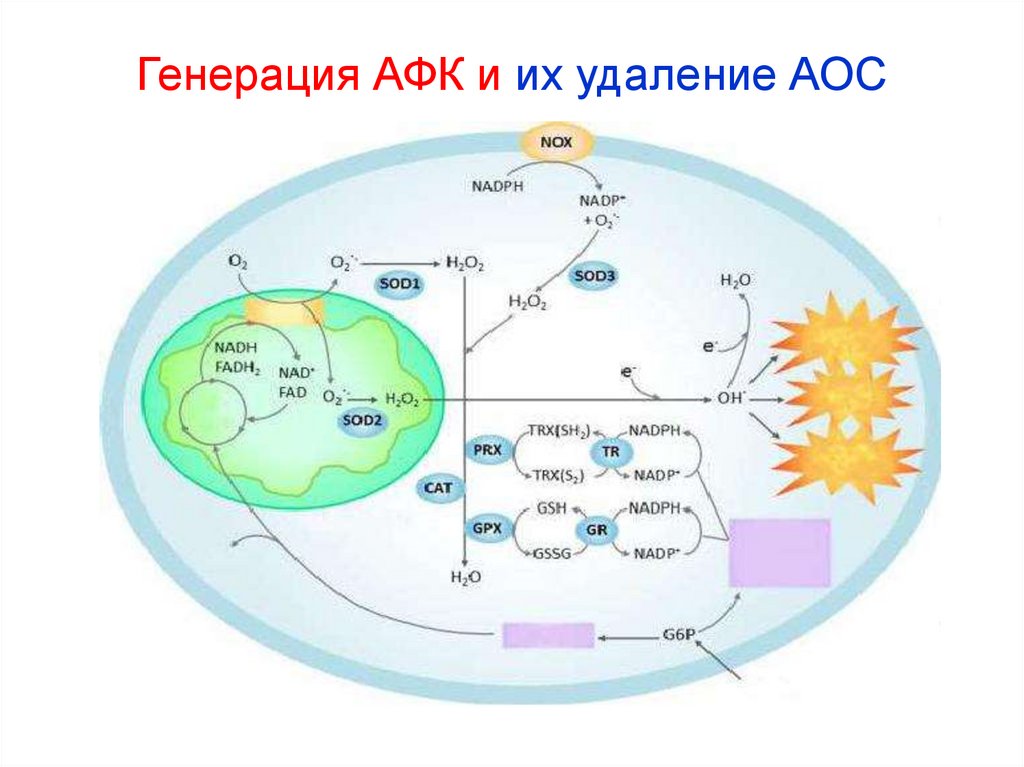
9. Генерация АФК и их удаление АОС
10.
11.
12. Номенклатура антиоксидантов
• Общепринятой единой номенклатурыАО нет. Однако существует широко
известное разделение АО:
1) по механизму действия
2) по химической природе
3) по молекулярной массе
4) по способности к катализу реакций
5) и др.
13. По механизму действия антиокислители делят:
• Антирадикальные ингибиторы, взаимо-действующие с органическими радикалами
• Антиперекисные – разрушающие органические перекиси
• Хелаторы – связывающие катализаторы окисления (ионы металлов переменной валентности Fe,Cu,Zn и др.): металлотионеины до 6 ионов Zn,
Cd,Hg,Cu; сидерофилин, церулоплазмин, ферредоксин
• Тушители – безизлучательно инактивирующие возбуждённые состояния молекул
(например, 1О2 – синглетный кислород).
вспомнить понятия триплетный / синглетный
14.
• 1-й пример определения:Антиоксиданты –
вещества, взаимодействующие с АФК,
органическими свободными радикалами и
останавливающие реакции образования АФК
и окислительной модификации макромолекул
(ОММ).
# вещества, снижающие активность ферментов,
нарабатывающих АФК (аллопуринол)
# противовоспалительные препараты, ингибирующие
реакции метаболического взрыва
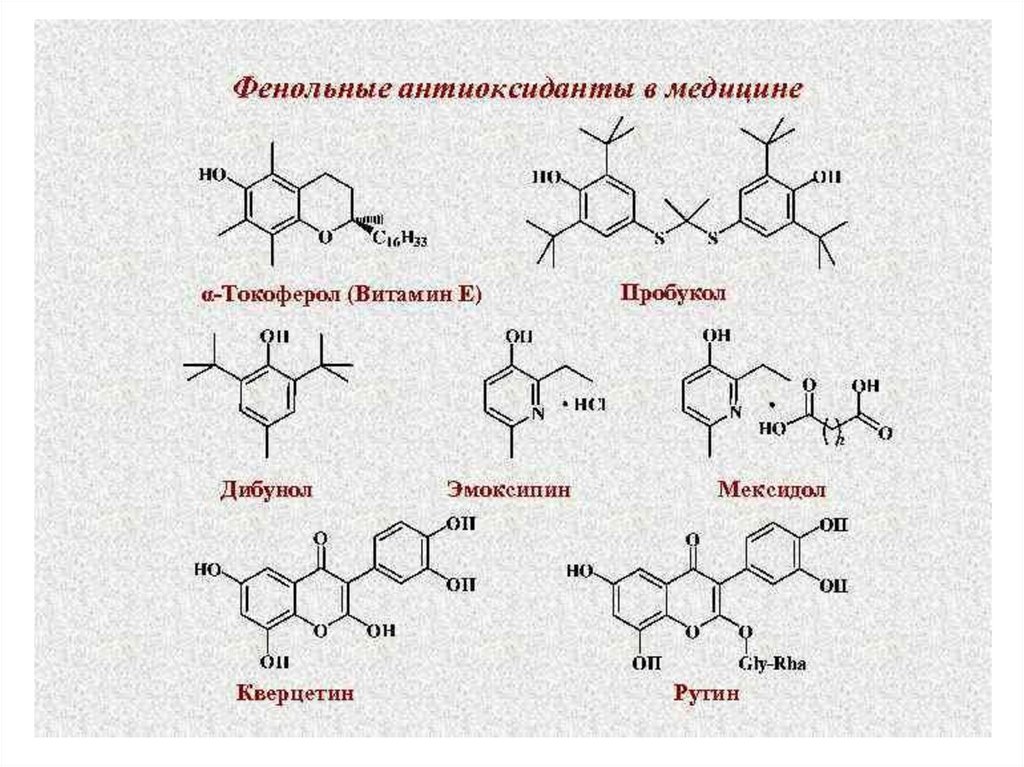
15. По химической природе антиоксиданты бывают:
• Фенолы, полифенолы (токоферолы,пирокатехины и др.)
• Флавоноиды (рутин, кверцетин)
• Стероиды (эстрогены)
• Производные сахаров (аскорбат)
• Аминокислоты (ЦИС, СЕР и др.)
16.
• 2-й пример определения:Антиоксиданты - это широкий класс
веществ различной химической
природы, которые
способны тормозить или устранять
свободно-радикальное окисление
органических соединений
молекулярным кислородом (О2).
• То есть понятия «антиоксиданты» и
«антиоксидантная защита» не вполне
конкретны и достаточно размыты.
17.
• 3-й пример определения:«Антиоксидант – это вещество,
которое, присутствуя в низких по
сравнению с окисляемым
субстратом концентрациях,
существенно задерживает или
полностью ингибирует его
окисление» J.M.Gutteridge (1995)
18. По молекулярной массе антиоксиданты делят:
• Низкомолекулярные (трипептидглутатион G-SH, аскорбат, β-каротин,
токоферол, мочевая кислота и др.)
• Высокомолекулярные, неспособные
проникать через биобарьеры (каталаза,
ферритин, пероксидазы, супероксиддисмутаза, церулоплазмин и др.)
19.
20. По способности к катализу антиоксиданты бывают:
• Неферментативные(витамины Е, С, мочевая кислота и др.)
• Ферментативные
(СОД, каталаза, пероксидазы и др.)
21.
22.
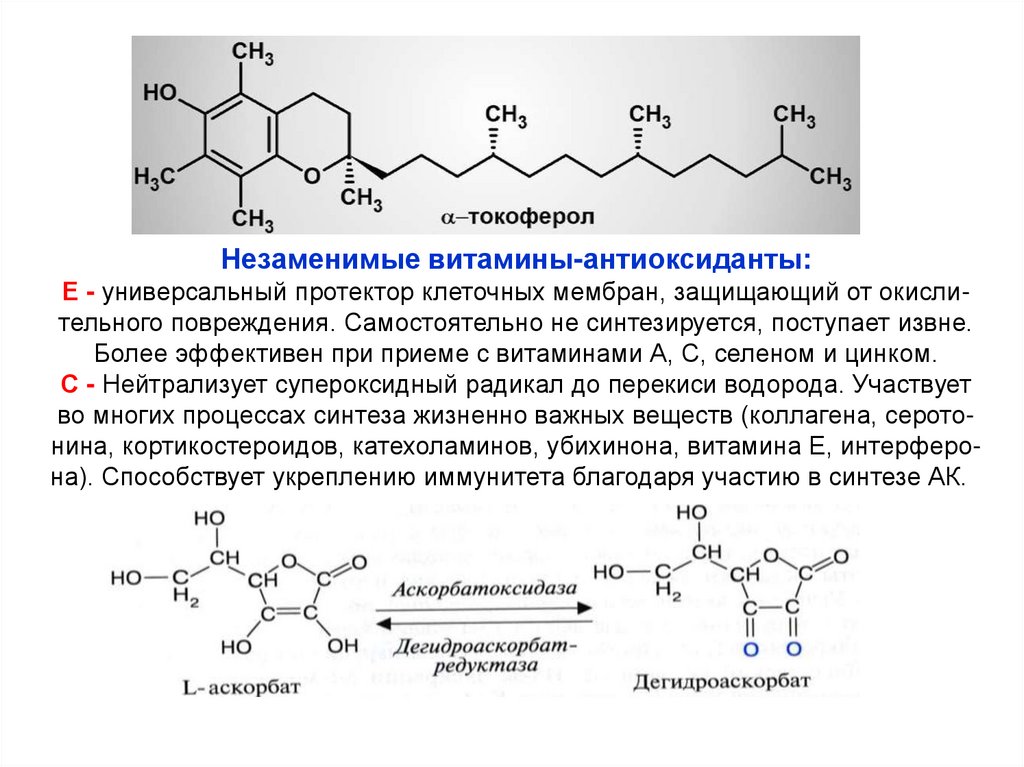
Незаменимые витамины-антиоксиданты:Е - универсальный протектор клеточных мембран, защищающий от окислительного повреждения. Самостоятельно не синтезируется, поступает извне.
Более эффективен при приеме с витаминами А, С, селеном и цинком.
С - Нейтрализует супероксидный радикал до перекиси водорода. Участвует
во многих процессах синтеза жизненно важных веществ (коллагена, серотонина, кортикостероидов, катехоламинов, убихинона, витамина Е, интерферона). Способствует укреплению иммунитета благодаря участию в синтезе АК.
23.
24.
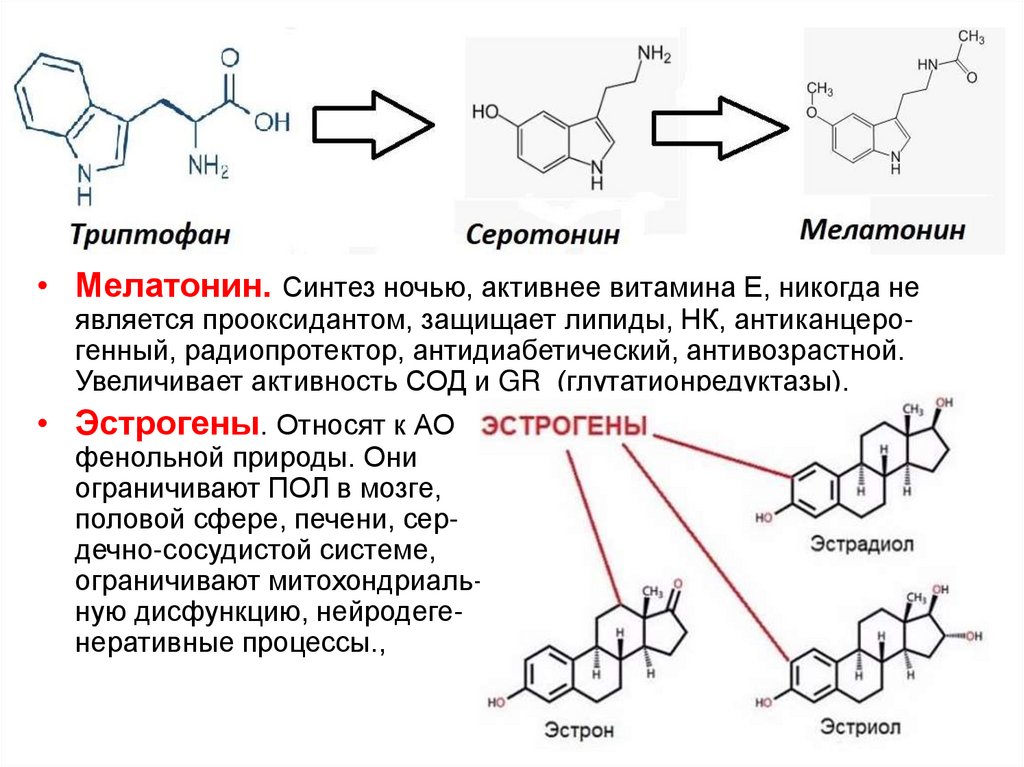
• Мелатонин. Синтез ночью, активнее витамина Е, никогда неявляется прооксидантом, защищает липиды, НК, антиканцерогенный, радиопротектор, антидиабетический, антивозрастной.
Увеличивает активность СОД и GR (глутатионредуктазы).
• Эстрогены. Относят к АО
фенольной природы. Они
ограничивают ПОЛ в мозге,
половой сфере, печени, сердечно-сосудистой системе,
ограничивают митохондриальную дисфункцию, нейродегенеративные процессы.,
25.
26.
27.
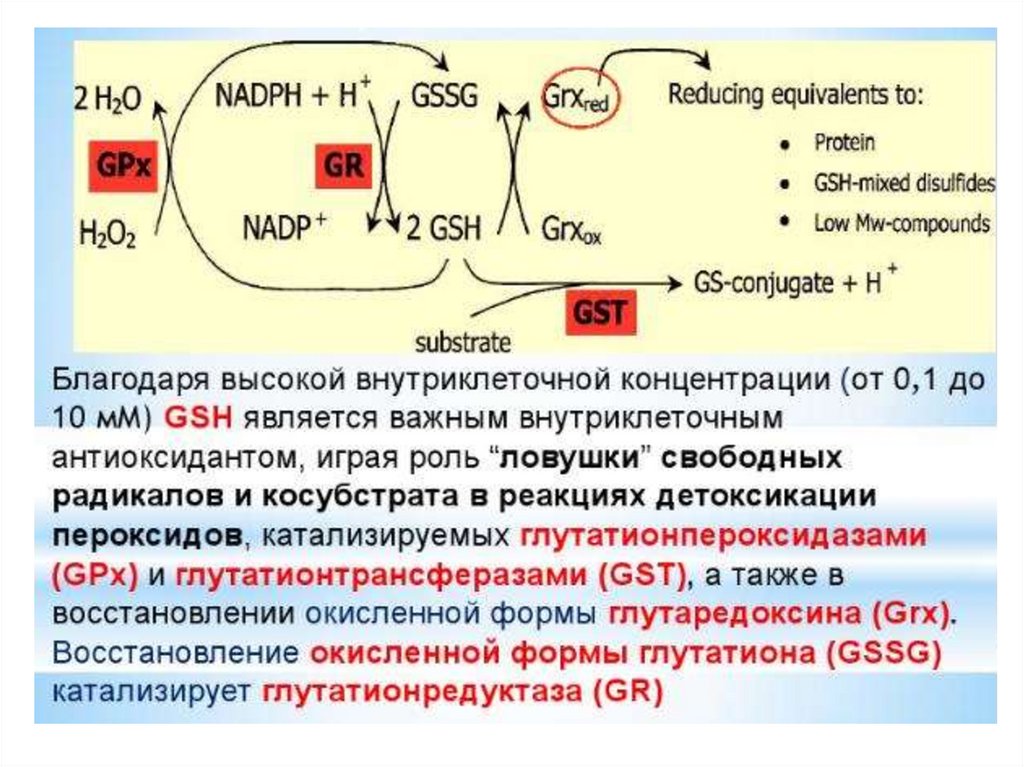
Глутатион и модуляция АФК1. Присутствие в среде АФК (включая H2O2) или
соединений, генерирующих АФК, повышает уровень
GSH за счёт возрастания скорости его синтеза GPX,
которая конкурирует с каталазой за H2O2.
• Редокс цикл глутатиона – защита от «мягкого»
окислительного стресса.
• Каталаза предохраняет от «жёсткого»
окислительного стресса.
• Каталаза имеет меньшее сродство к H2O2, чем GPX.
GPX можно рассматривать как сенсор для H2O2, регулирующий её концентрации в заданных пределах.
2. GSH участвует в обратимом глутатионилировании
функциональных SH-групп белков при защите от ОС.
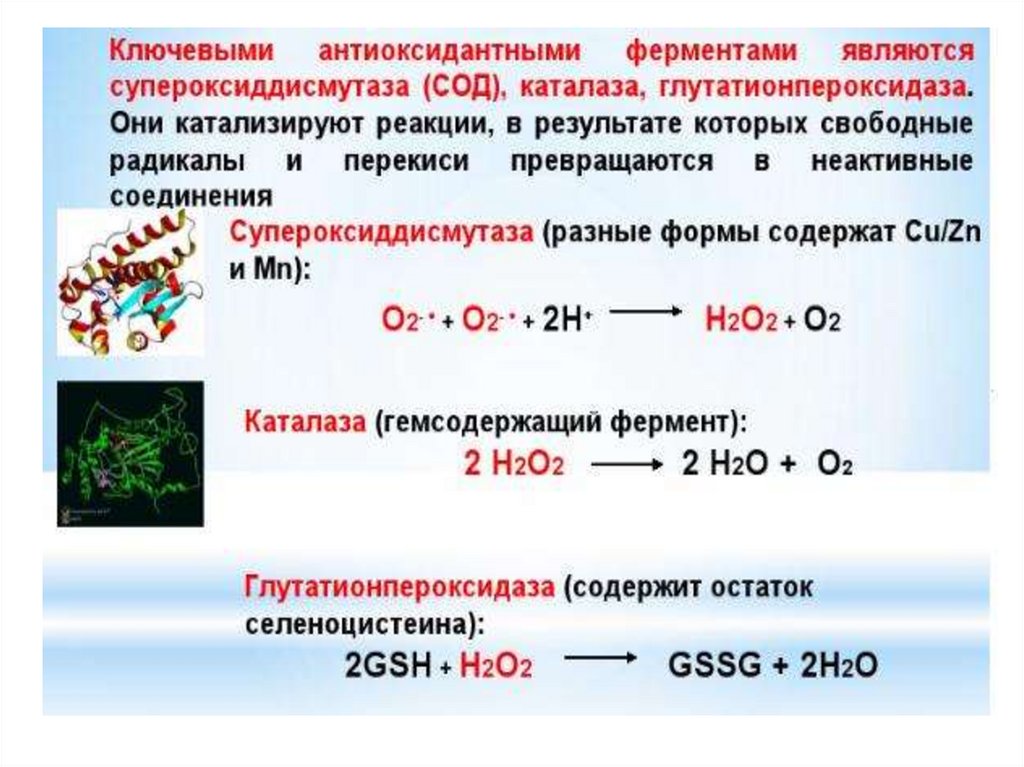
28. СОД – антирадикальный фермент, но продуцирует Н2О2 – субстрат для КАТ и GPX
29.
30.
31. Исходя из роли глутатион-трансферазы становится понятным ещё один принцип разделения в работе АОС:
• Введены понятия первичная АОС и вторичная АОС.• Под вторичной АОС понимают специализированные
ферментативные механизмы устранения окислительных повреждений в клетках (фосфолипазы,
протеиназы, экзо- и эндонуклеазы и др.).
• Поскольку своевременное удаление повреждённых
молекул повышает устойчивость клеток к токсичному
действию АФК и СР, то с позиций биологической
системы и биозначимости свободнорадикальных
окислительных процессов такие ферментативные
системы можно рассматривать как антиоксидантные
в комплексе АОЗ.
32. Системы репарации в АОЗ
• Репарация белков:- протеиназы, протеазы, пептидазы
- протеасомные комплексы (10-20 субъединиц)
- макрооксипротеиназы
• Репарация липидов:
- фосфолипазы,
- ацилтрансферазы (замена ЖК),
- GSH-зависимые пероксидазы/трансферазы
(восстановление ЖК без удаления и замены ЖК)
• Репарация ДНК:
- экзо- и эндоуклеазы (выстригают повреждённые НТ)
- полимеразы, гликозилазы (заполняют промежутки)
- лигазы (итоговая сшивка, завершение репарации)
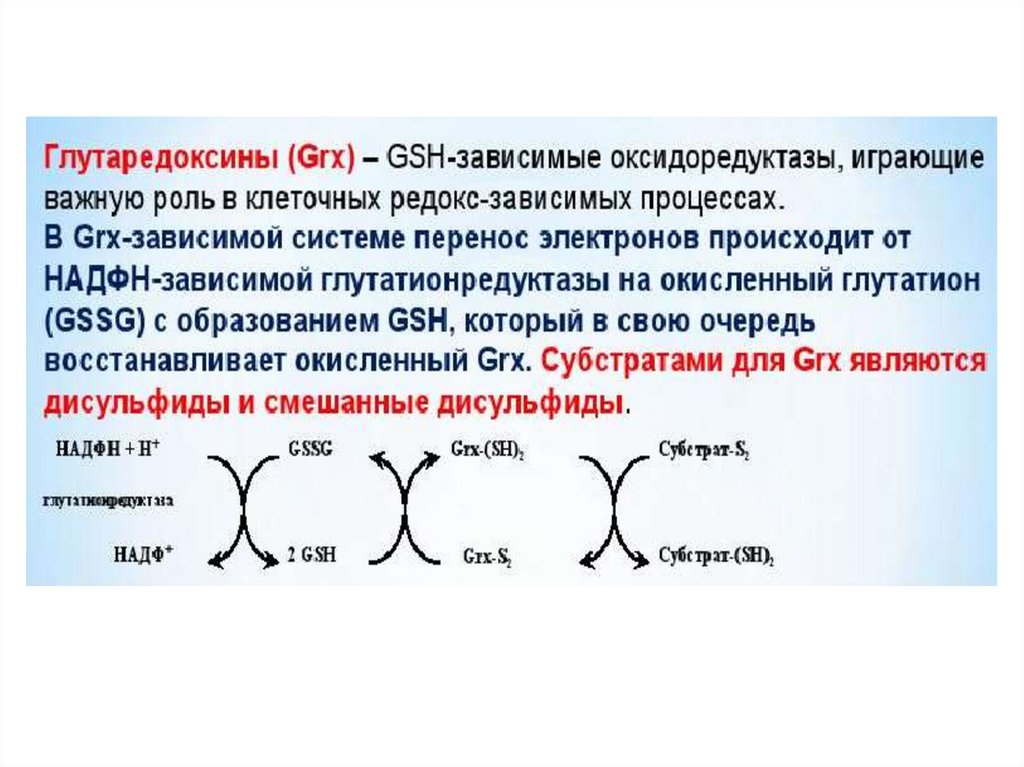
33. Ферментативные редокс-белки
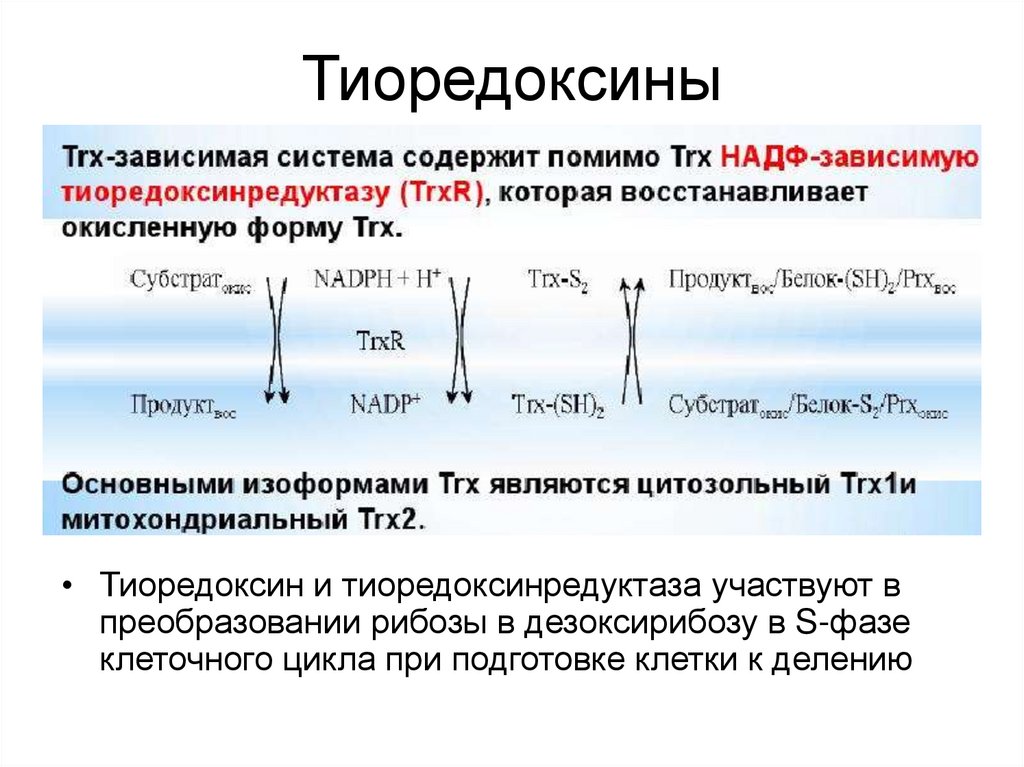
34. Тиоредоксины
• Тиоредоксин и тиоредоксинредуктаза участвуют впреобразовании рибозы в дезоксирибозу в S-фазе
клеточного цикла при подготовке клетки к делению
35.
36.
37.
38. Ферментативные редокс-белки
39.
• В зависимости от ситуации АОмогут быть как синергистами, так и
антагонистами
40.
Препараты Se,АЕвит, кудесан,
Аскорбат,






























 Биология
Биология Химия
Химия








