Похожие презентации:
Органическая химия – химия соединений углерода
1.
2.
Органическая химия – химиясоединений углерода
Кроме углерода и водорода в
составе молекул могут быть:
кислород, азот, сера, фосфор и
другие галогены
3.
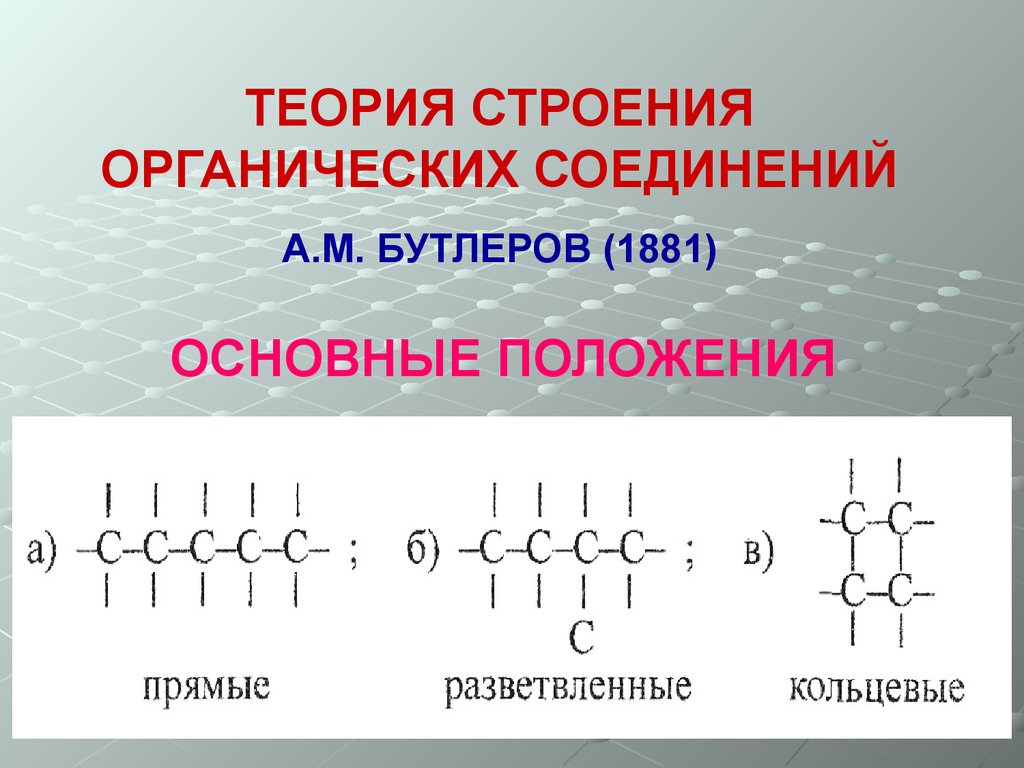
ТЕОРИЯ СТРОЕНИЯОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
А.М. БУТЛЕРОВ (1881)
ОСНОВНЫЕ ПОЛОЖЕНИЯ
1. Углерод в органических
соединениях всегда
четырехвалентен.
4.
ТЕОРИЯ СТРОЕНИЯОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
А.М. БУТЛЕРОВ (1881)
ОСНОВНЫЕ ПОЛОЖЕНИЯ
2. Атомы углерода соединяются
между собой, образуя цепи
атомов.
5.
ТЕОРИЯ СТРОЕНИЯОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
А.М. БУТЛЕРОВ (1881)
ОСНОВНЫЕ ПОЛОЖЕНИЯ
3. Свойства веществ зависят не
только от того, какие атомы и в
каком количестве входят в состав
молекулы, но и от порядка их
соединения.
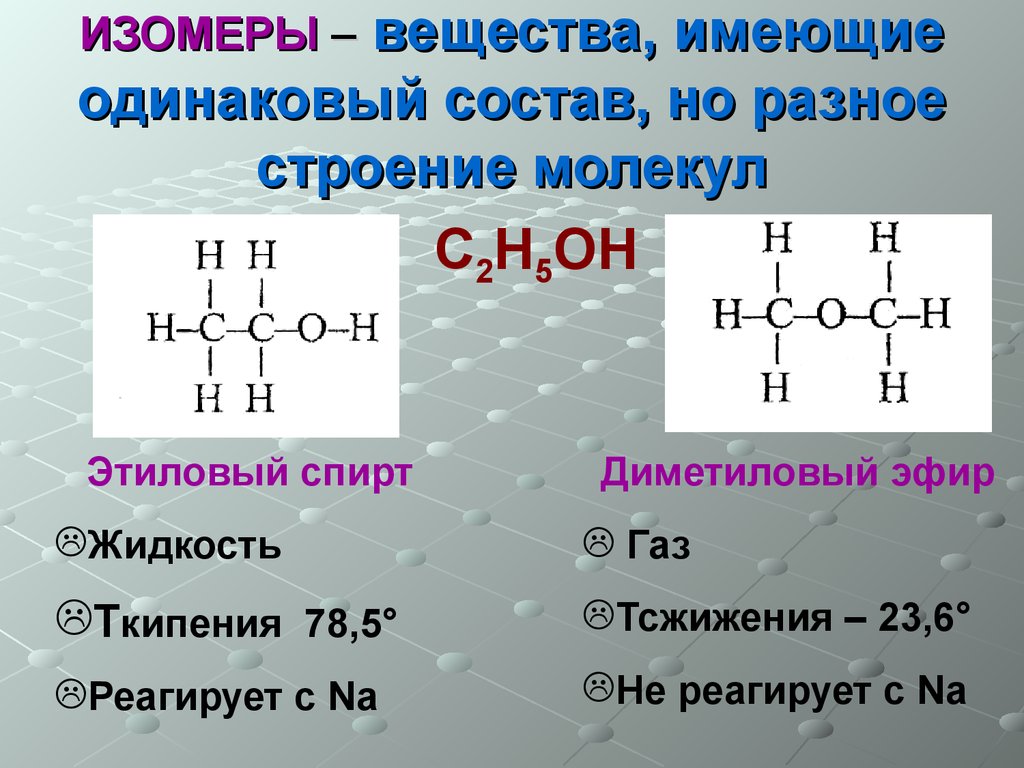
6. ИЗОМЕРЫ – вещества, имеющие одинаковый состав, но разное строение молекул
вещества, имеющиеодинаковый состав, но разное
строение молекул
С2Н5ОН
ИЗОМЕРЫ –
Этиловый спирт
Диметиловый эфир
Жидкость
Газ
Ткипения 78,5°
Тсжижения – 23,6°
Реагирует с Na
Не реагирует с Na
7.
ТЕОРИЯ СТРОЕНИЯОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
А.М. БУТЛЕРОВ (1881)
ОСНОВНЫЕ ПОЛОЖЕНИЯ
4. Атомы в молекуле взаимно
влияют друг на друга, от чего
зависит реакционная способность
молекулы.
8.
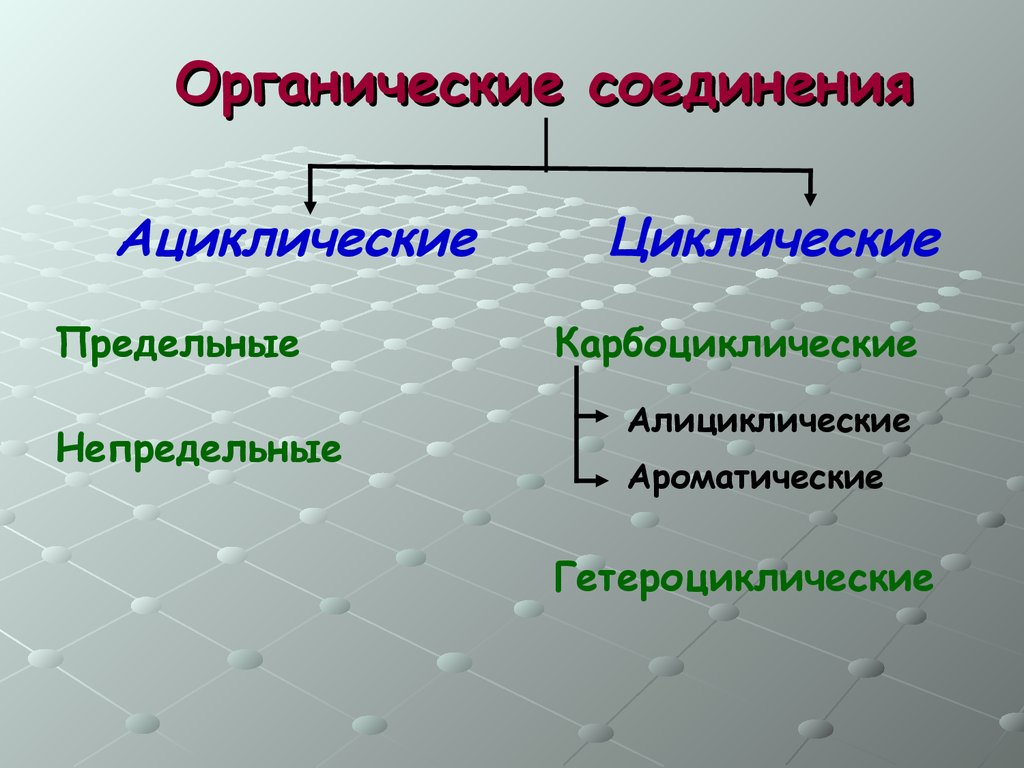
Органические соединенияАциклические
Предельные
Непредельные
Циклические
Карбоциклические
Алициклические
Ароматические
Гетероциклические
9.
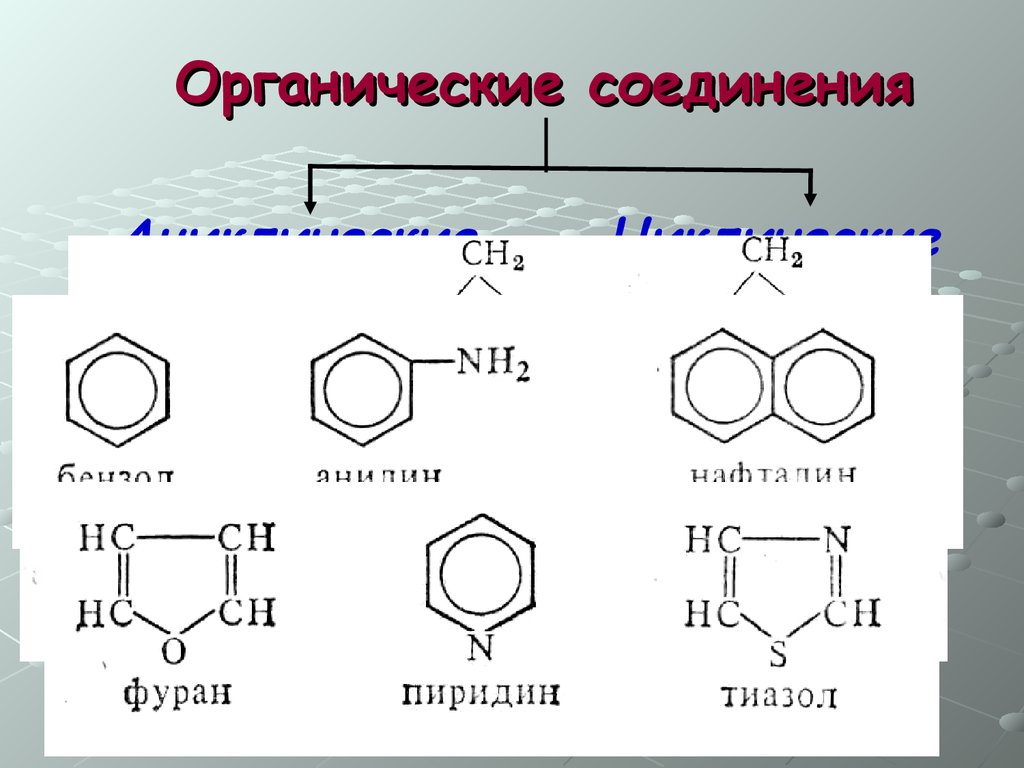
Органические соединенияАциклические
Предельные
Непредельные
Циклические
Карбоциклические
Алициклические
Ароматические
Гетероциклические
10.
Предельные углеводороды(алканы, насыщенные
углеводороды, парафины)
Общая формула СnH2n+2
11.
Предельные углеводородыФизические свойства:
До 4 С – газы, от 5 до 7 С –
жидкости, остальные - твердые.
Нерастворимы в воде.
12.
Предельные углеводородыХимические свойства:
1. Реакции замещения
А) галогенирование
Б) нитрование
13.
Предельные углеводородыХимические свойства:
2. Реакции окисления
А) горение
Б) окисление
14.
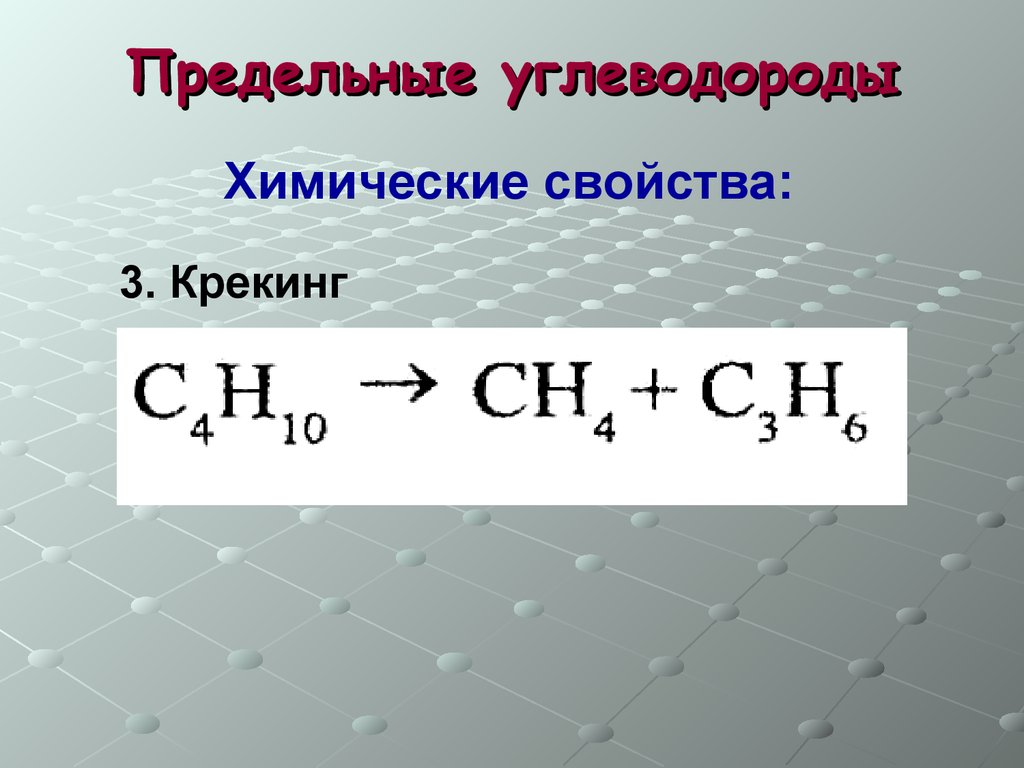
Предельные углеводородыХимические свойства:
3. Крекинг
15.
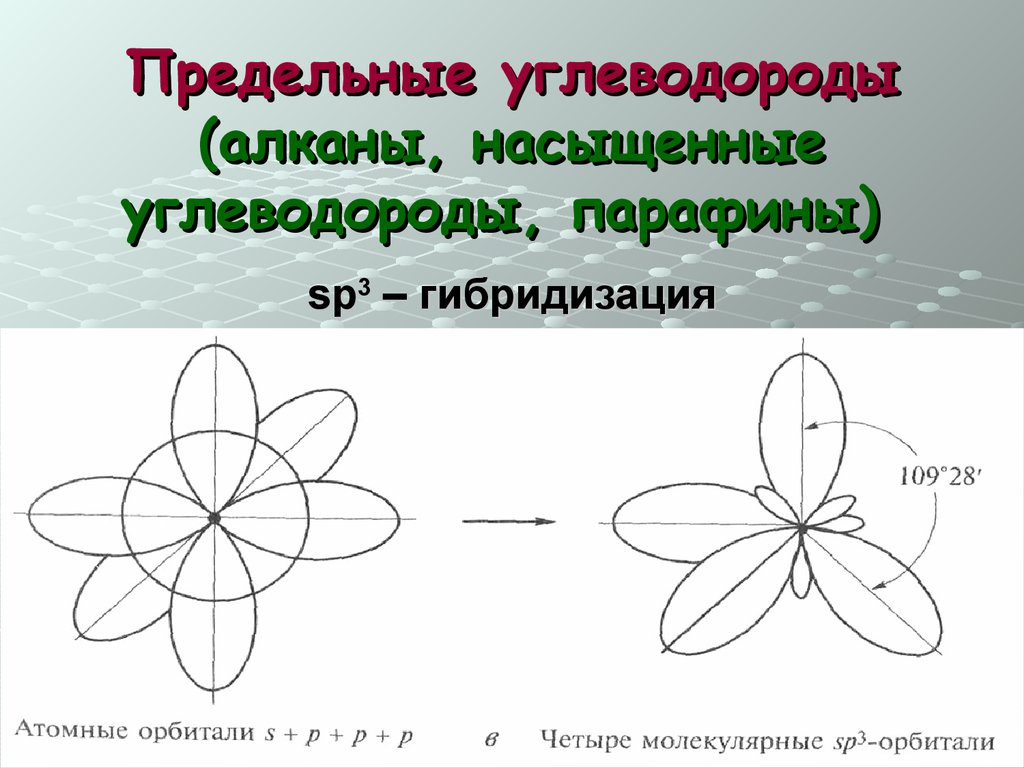
Предельные углеводороды(алканы, насыщенные
углеводороды, парафины)
sp3 – гибридизация
16.
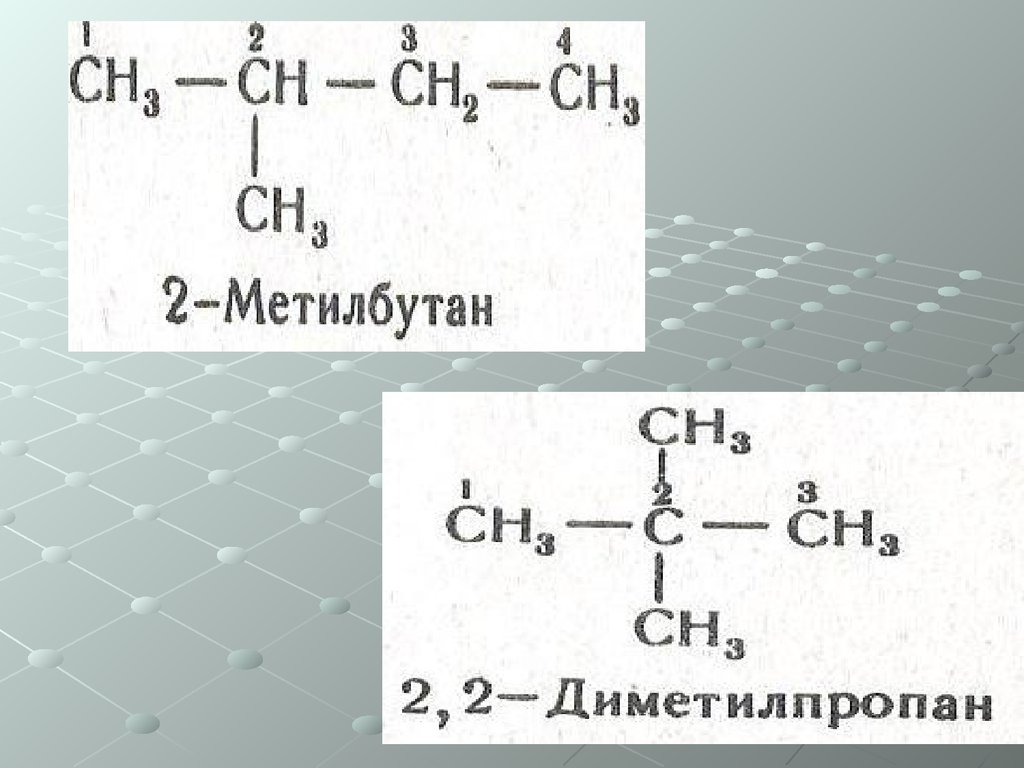
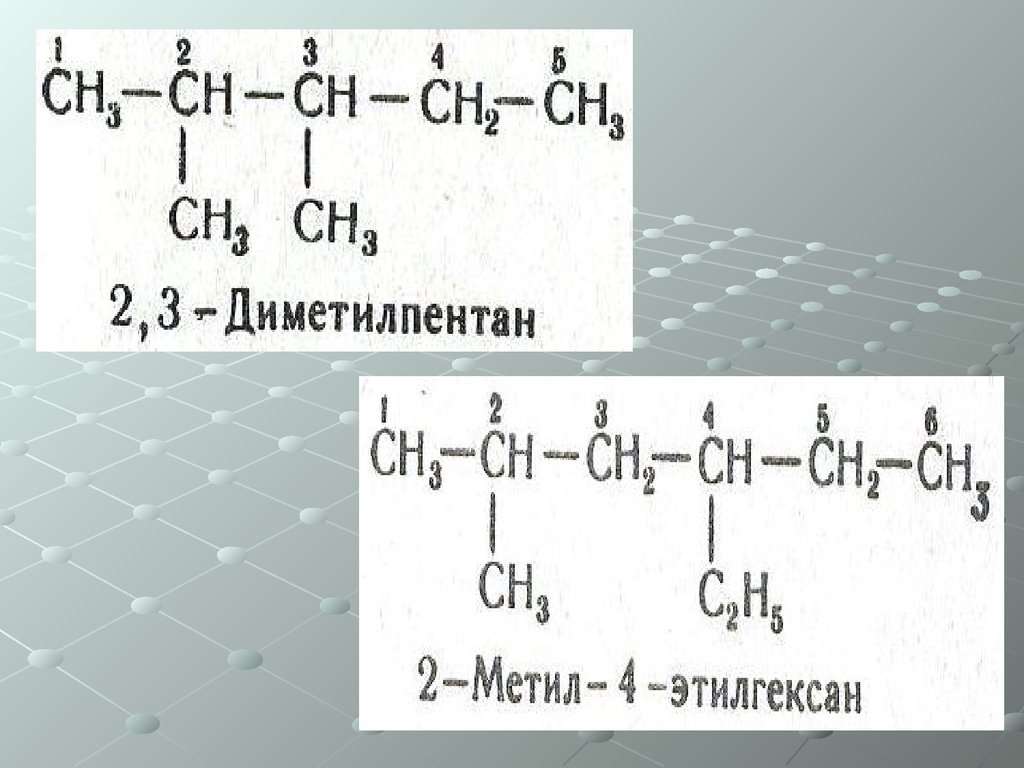
Предельные углеводородыХарактерна изомерия углеродного
скелета
17.
Номенклатура1. Выбирается самая длинная цепь.
2. Нумеруются атомы в главной цепи,
начиная с конца, к которому ближе
расположены разветвления или
ненасыщенные связи.
3. Цифрами указывается
месторасположение радикалов.
4. Называются радикалы по старшинству
(например, сначала метил, а потом этил).
5. Называется основная углеродная цепь.
18.
19.
20.
Непредельные углеводороды(ненасыщенные)
Алкены – одна двойная связь
Общая формула СnH2n
Физические свойства:
До 4 С – газы, от 5 до 8 С –
жидкости, остальные - твердые.
Мало растворимы в воде.
21.
Непредельные углеводородыsp2 – гибридизация
22.
Непредельные углеводородыХимические свойства:
1. Реакции присоединения
А) гидрирование
Б) галогенирование
23.
Непредельные углеводороды(ненасыщенные)
Алкены – одна двойная связь
Общая формула СnH2n
Химические свойства:
1. Реакции присоединения
В) гидрогалогенирование
24.
ПРАВИЛО МАРКОВНИКОВААтом водорода присоединяется к
наиболее гидрированному атому
углерода при двойной связи
(связанному с наибольшим числом
атомов водорода)
25.
Непредельные углеводороды(ненасыщенные)
Алкены – одна двойная связь
Общая формула СnH2n
Химические свойства:
1. Реакции присоединения
Г) гидратация
26.
Непредельные углеводороды(ненасыщенные)
Алкены – одна двойная связь
Общая формула СnH2n
Химические свойства:
2. Реакции полимеризации
27.
Непредельные углеводороды(ненасыщенные)
Алкены – одна двойная связь
Общая формула СnH2n
Химические свойства:
3. Реакции окисления
28.
Непредельные углеводороды(ненасыщенные)
Алкены – одна двойная связь
Общая формула СnH2n
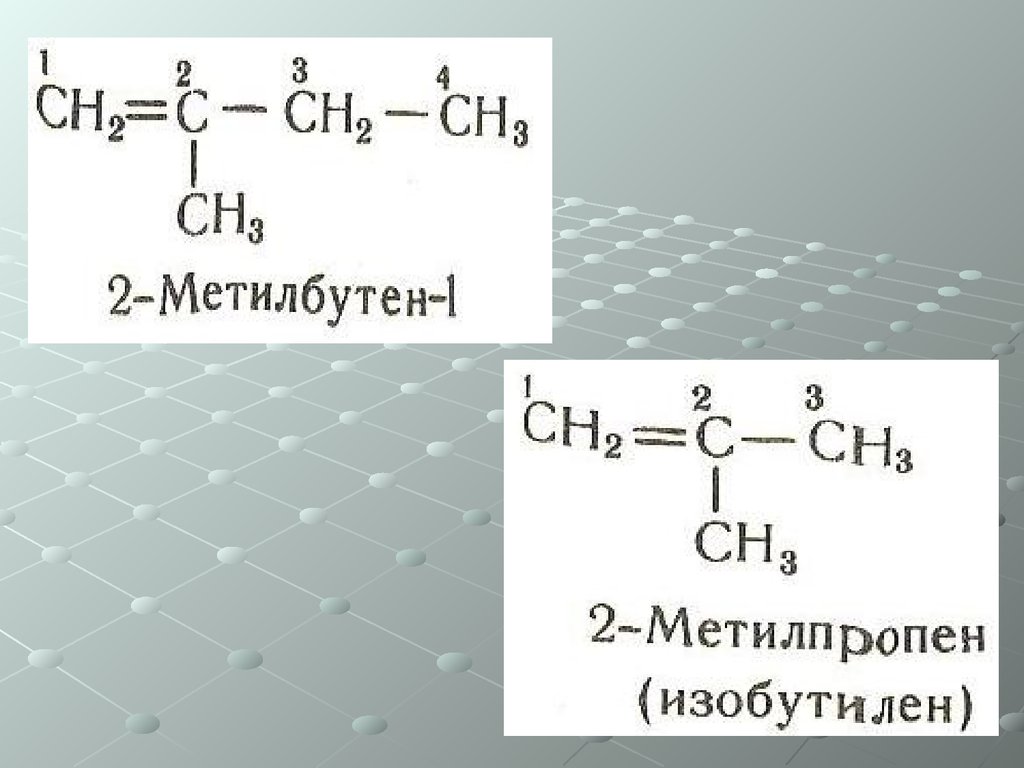
Изомерия:
• Углеродного скелета
• Положения двойной связи
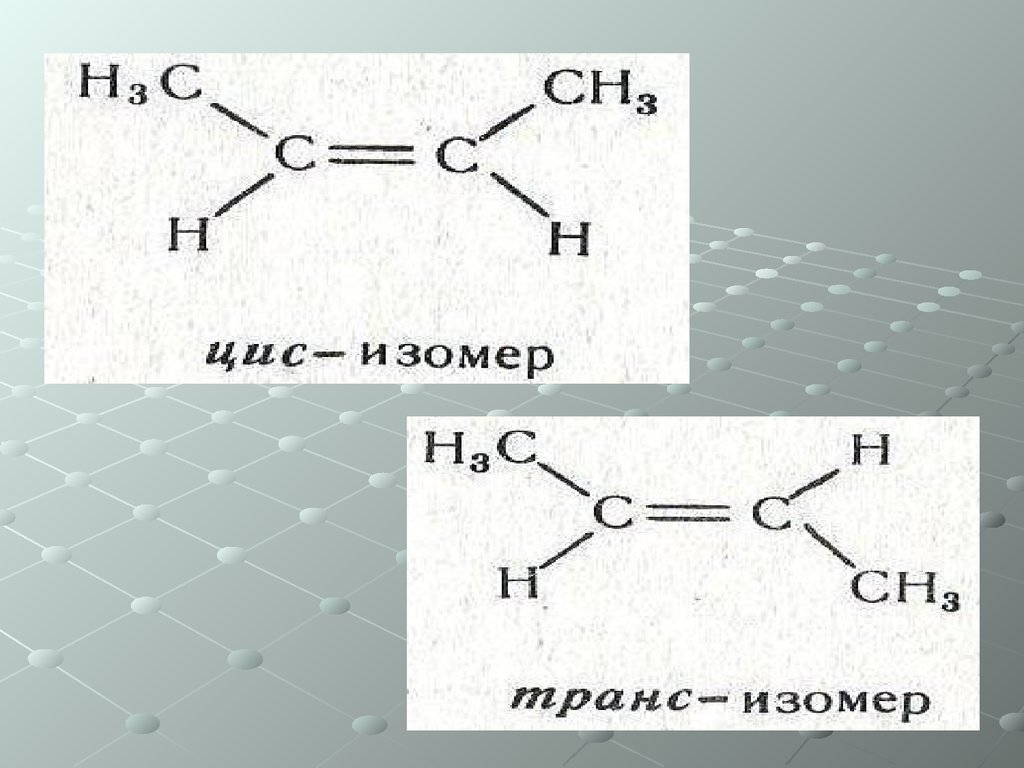
• Геометрическая
29.
30.
31.
32.
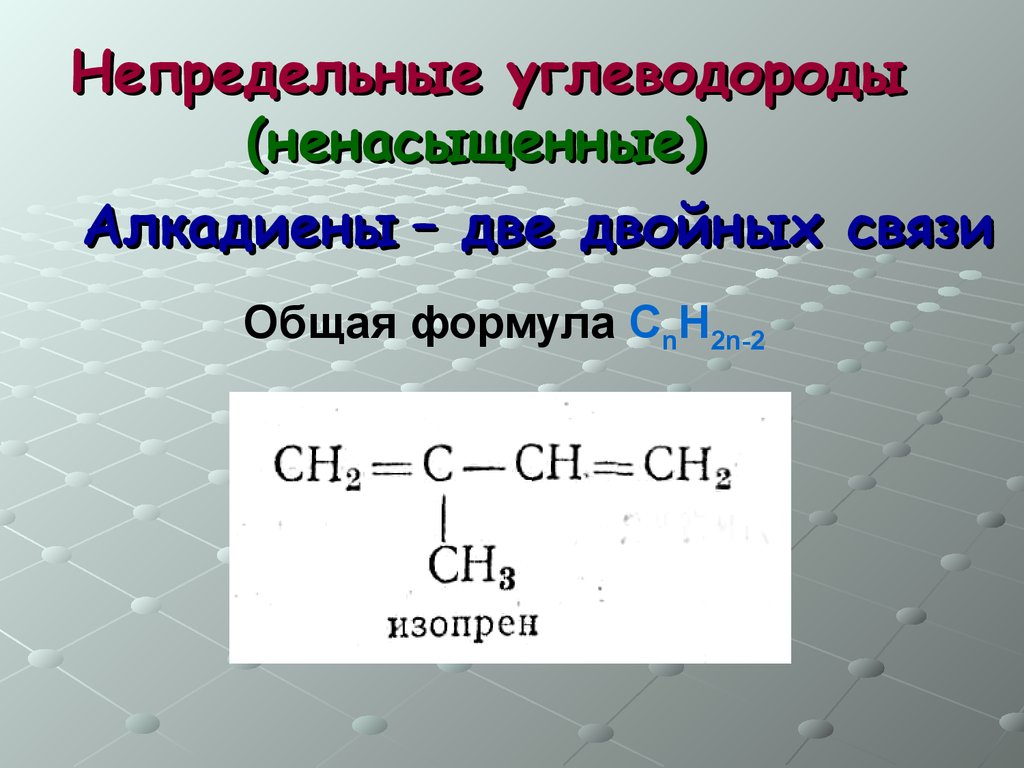
Непредельные углеводороды(ненасыщенные)
Алкадиены – две двойных связи
Общая формула СnH2n-2
33.
Непредельные углеводороды(ненасыщенные)
Алкадиены – две двойных связи
Общая формула СnH2n-2
Изомерия:
•Углеродного скелета
•Положения двойных связей
34.
35.
Непредельные углеводороды(ненасыщенные)
Алкины – одна тройная связь
Общая формула СnH2n-2
36.
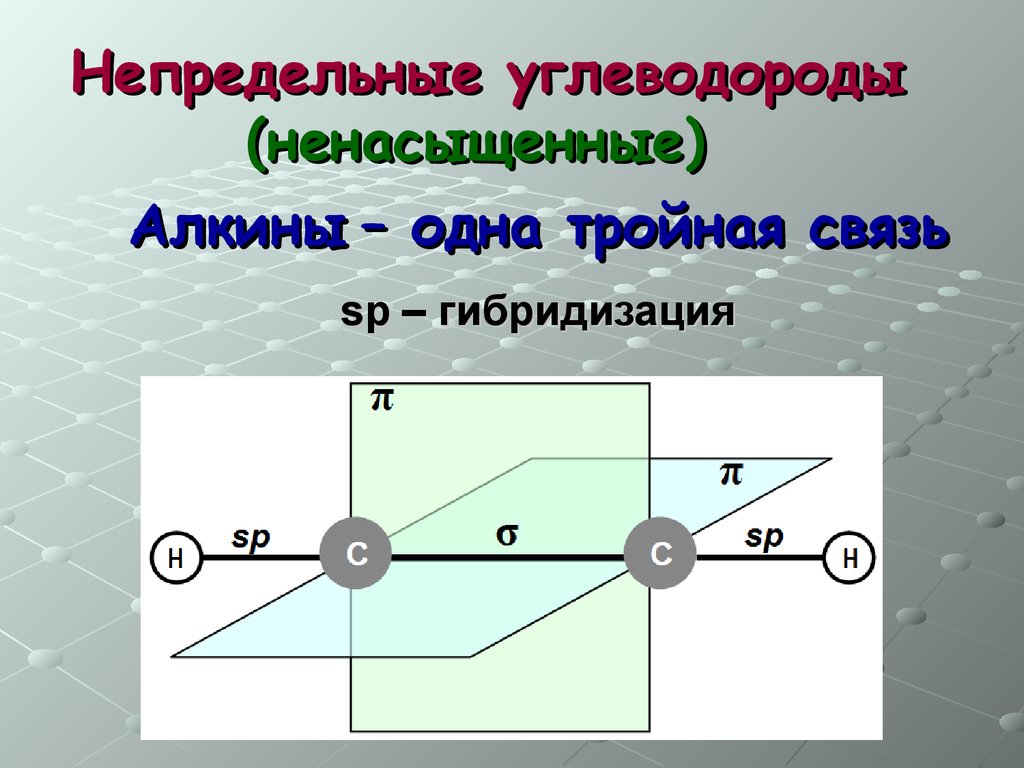
Непредельные углеводороды(ненасыщенные)
Алкины – одна тройная связь
sp – гибридизация
37.
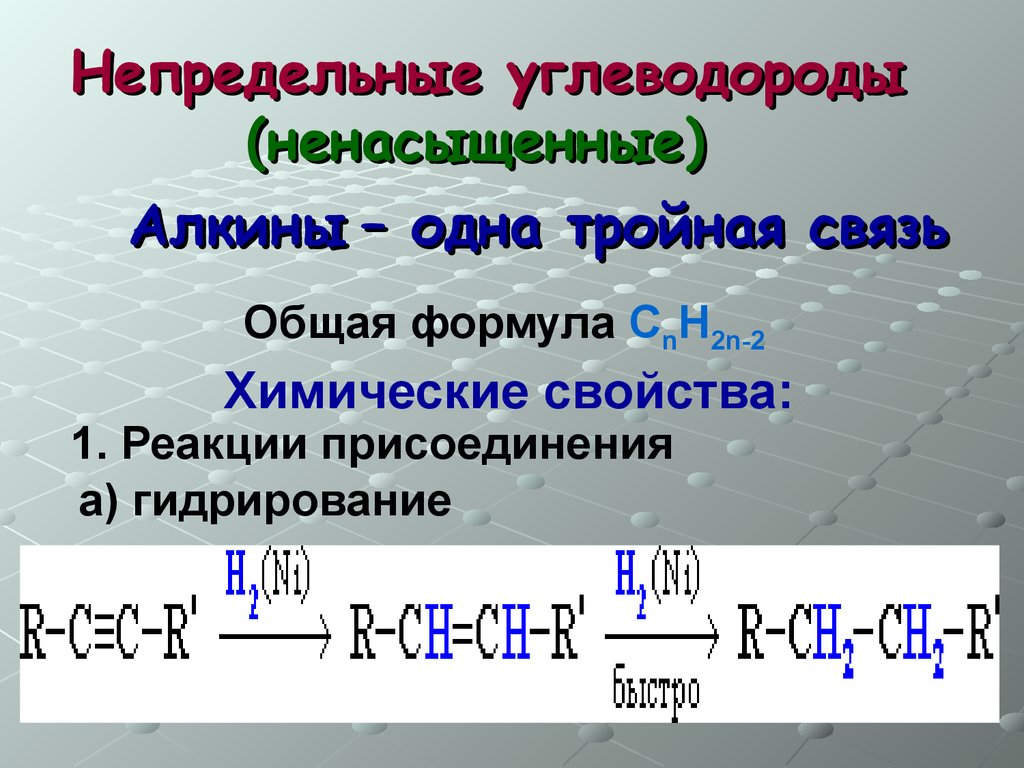
Непредельные углеводороды(ненасыщенные)
Алкины – одна тройная связь
Общая формула СnH2n-2
Химические свойства:
1. Реакции присоединения
а) гидрирование
38.
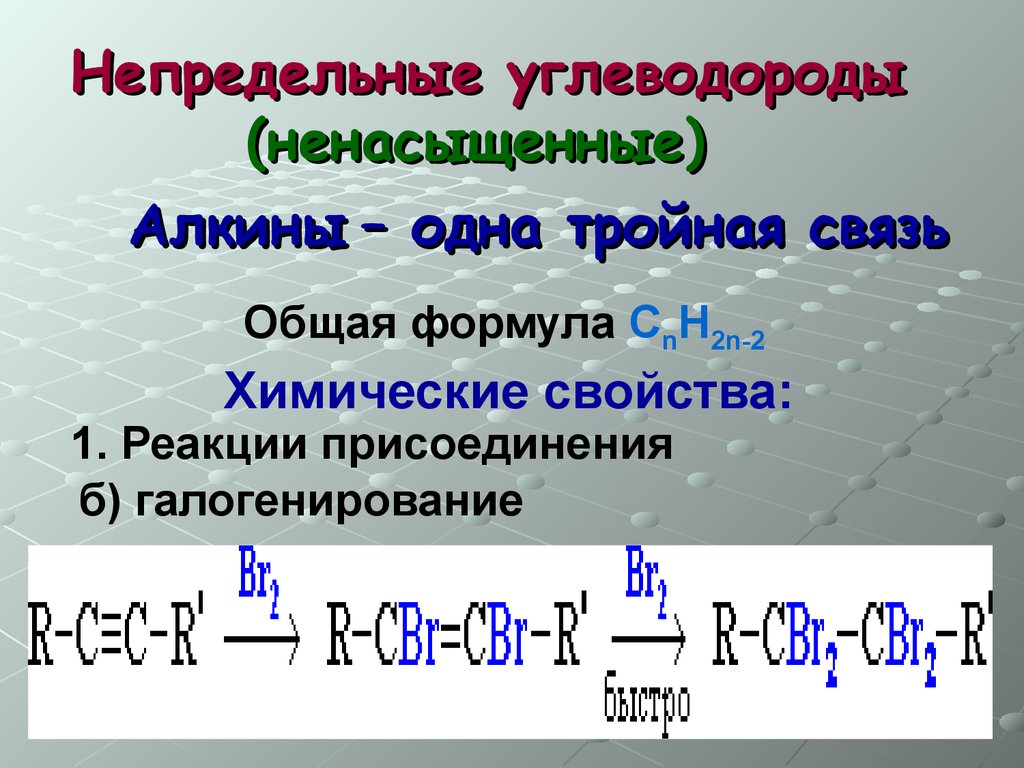
Непредельные углеводороды(ненасыщенные)
Алкины – одна тройная связь
Общая формула СnH2n-2
Химические свойства:
1. Реакции присоединения
б) галогенирование
39.
Непредельные углеводороды(ненасыщенные)
Алкины – одна тройная связь
Общая формула СnH2n-2
Химические свойства:
1. Реакции присоединения
в) гидрогалогенирование
40.
Непредельные углеводороды(ненасыщенные)
Алкины – одна тройная связь
Общая формула СnH2n-2
Химические свойства:
1. Реакции присоединения
г) гидратация (реакция Кучерова)
41.
Непредельные углеводороды(ненасыщенные)
Алкины – одна тройная связь
Общая формула СnH2n-2
Химические свойства:
2. Реакция замещения
Реакция «серебряного зеркала» с
реактивом Толленса
42.
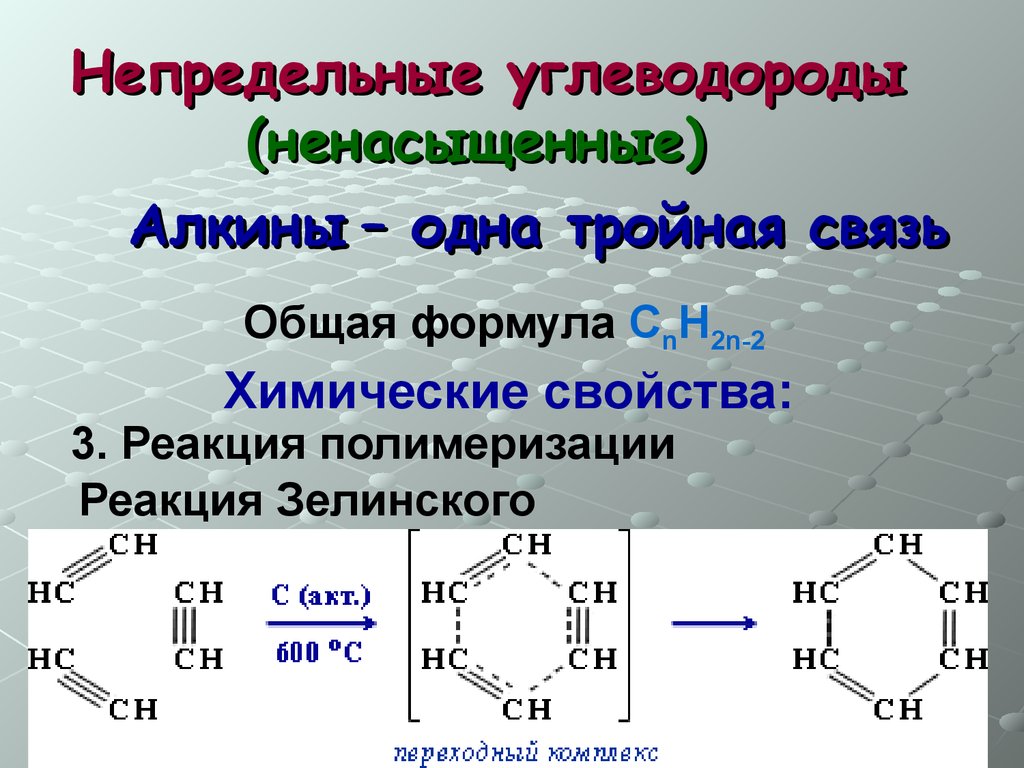
Непредельные углеводороды(ненасыщенные)
Алкины – одна тройная связь
Общая формула СnH2n-2
Химические свойства:
3. Реакция полимеризации
Реакция Зелинского
43.
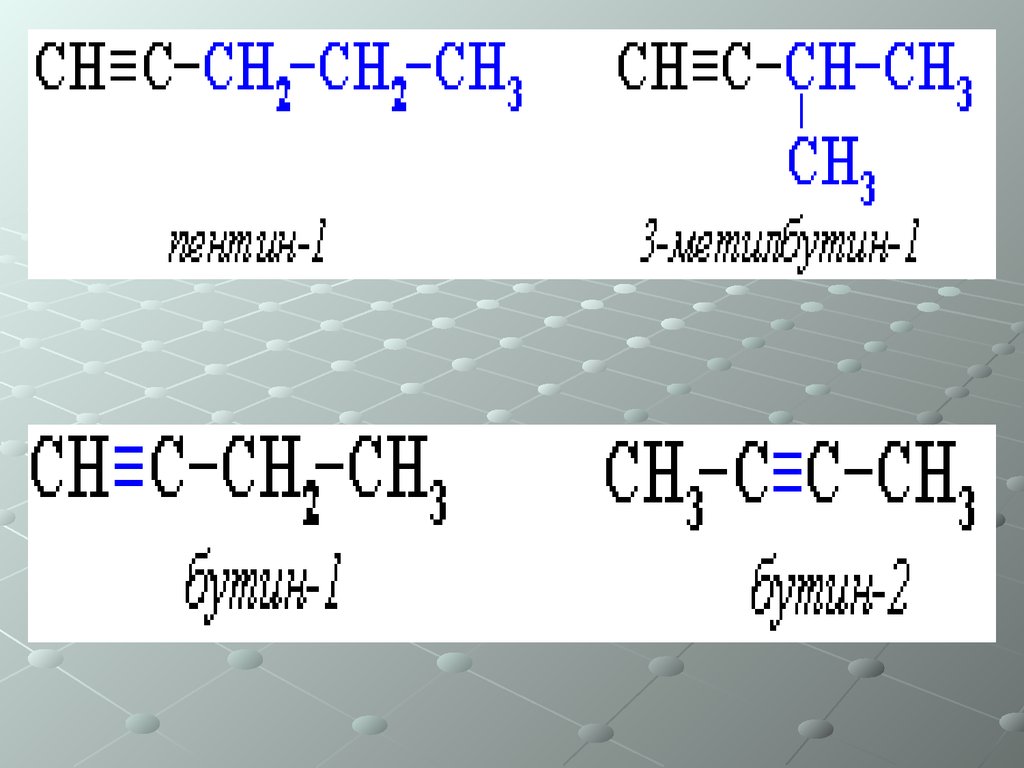
Непредельные углеводороды(ненасыщенные)
Алкины – одна тройная связь
Общая формула СnH2n-2
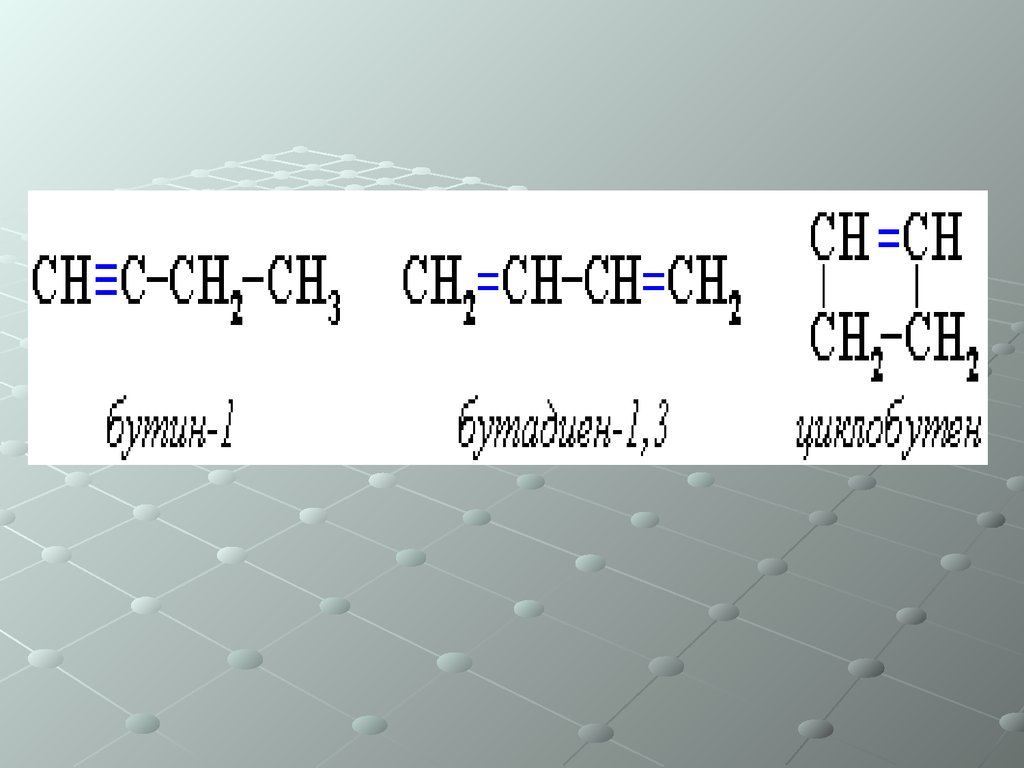
Изомерия:
•Углеродного скелета
•Положения тройной связи
•Межклассовая (с алкадиенами и
циклоалкенами)




























 Химия
Химия








