Похожие презентации:
Водород. Общая характеристика, получение, свойства
1. Водород. Общая характеристика, получение, свойства
2.
Металл+ кислота =
«горючий воздух»
1766
г. Генри
Кавендиш (Англия)
1784
г. А. Лавуазье
(Франция)
Hedrogenium
водород
рождающий воду
3. Положение в ПС
Химическийзнак – Н
Порядковый № 1
Изотопы
протий 11Н
дейтерий 12Н = D
тритий 13Н = Т
Малая
электроотрицательность
– сходство со ЩМ
Простое вещество Н2 –
сходство с галогенами
4. Водород в природе
Содержание в земнойкоре 0,15% по массе (с
учетом гидросферы 1%) –
девятый по
распространенности
Доля атомов 17% второй
после кислорода (52%)
Основной элемент
Вселенной – половина
массы Солнца
Простое вещество в
атмосфере Земли не
встречается
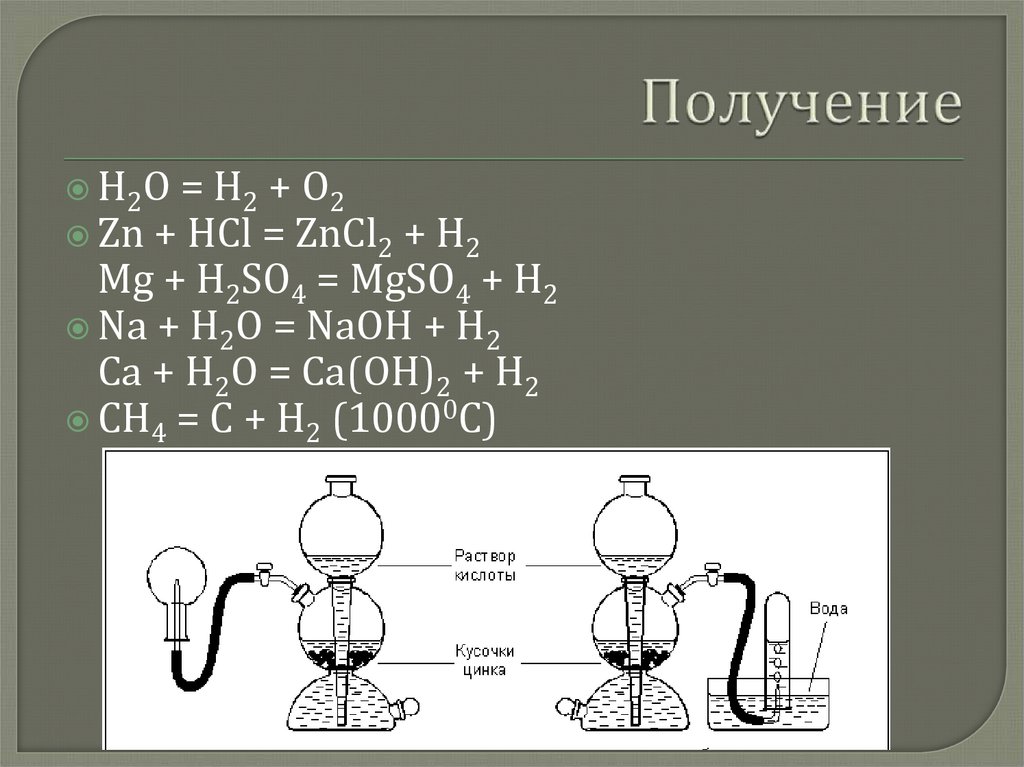
5. Получение
Н2О= Н 2 + О2
Zn + HCl = ZnCl2 + H2
Mg + H2SO4 = MgSO4 + H2
Na + H2O = NaOH + H2
Ca + H2O = Ca(OH)2 + H2
СН4 = С + Н2 (10000С)
6. Свойства водорода
Физическиесвойства
газ без цвета, без
запаха, без вкуса
в 14,5 раз легче
воздуха
Тк = - 252,8 0С
мало растворим в
воде
7. Химические свойства
ОкислительВзаимодействует с металлами (щелочными и
щелочноземельными)
Н2 + Na = NaH
H2 + Ca = CaH2 (гидриды)
Восстановитель
Взаимодействует в неметаллами (кроме As, Р, Si, В)
Н2 + О2 = Н2О "Гремучий газ» : V(H2):V(O2) = 2:1
Н2 + Cl2 = HCl
H2 + N2 = NH3
Взаимодействует с оксидами металлов
H2 + CuO = Cu + H2O
H2 + WO3 = W + H2O







 Химия
Химия








