Похожие презентации:
Общие вопросы опухолевого роста. Эпителиальные опухоли
1. ОБЩИЕ ВОПРОСЫ ОПУХОЛЕВОГО РОСТА
профессор Агеева Т.А.2. АКТУАЛЬНОСТЬ
ОПУХОЛИ уверенно занимают II местов структуре смертности от заболеваний
в России и во всем мире
имеется постоянная тенденция к росту
показателей заболеваемости
опухолевыми заболеваниями
в последние десятилетия в
ОНКОЛОГИИ достигнуты значительные
успехи в понимании молекулярных
механизмов опухолевого роста, что
обусловило значительные успехи в
лечении опухолевых заболеваний
3. ОПУХОЛЬ (новообразование, тумор, бластома) - патологический процесс, характеризующийся безудержным (бесконтрольным, автономным)
ОПУХОЛЬ (новообразование,тумор, бластома) патологический процесс,
характеризующийся безудержным
(бесконтрольным, автономным)
ростом опухолевых клеток, в
которых нарушение роста и
дифференцировки связано с
нарушениями в генетическом
аппарате клеток
4. ОПУХОЛЬ - патологический процесс, характеризующийся безудержным ростом опухолевых клеток, с нарушением их роста и
дифференцировки, что связано снарушениями в структуре генома клеток
5. Нормальное клеточное деление
Пролиферативныйстимул
Активация
антионкогенов
Остановка
пролиферации
Активация
протоонкогенов
Пролиферация
Дифференцировка
6.
7. Основные группы генов, участвующих в регуляции клеточного цикла (пролиферация и дифференцировка)
Протоонкогены - нормальные геныклеток, регулирующие пролиферацию
и дифференцировку клеток
Антионкогены (гены-супрессоры
опухолей) - ингибируют пролиферацию
клеток, регулируют процесс
дифференцировки
Гены, регулирующие процесс апоптоза
Гены, отвечающие за репарацию ДНК
8.
Мутации – внезапно возникающиестойкие изменения генов и хромосом
GGATCTTGCCATATGCAA
CCTAGAACGGTATACGTT
Факторы,
повреждающие
ДНК
GGATCTTGАCATATGCAA
CCTAGAACТGTATACGTT
Изменение структуры и функции
опухолетрансформированной клетки
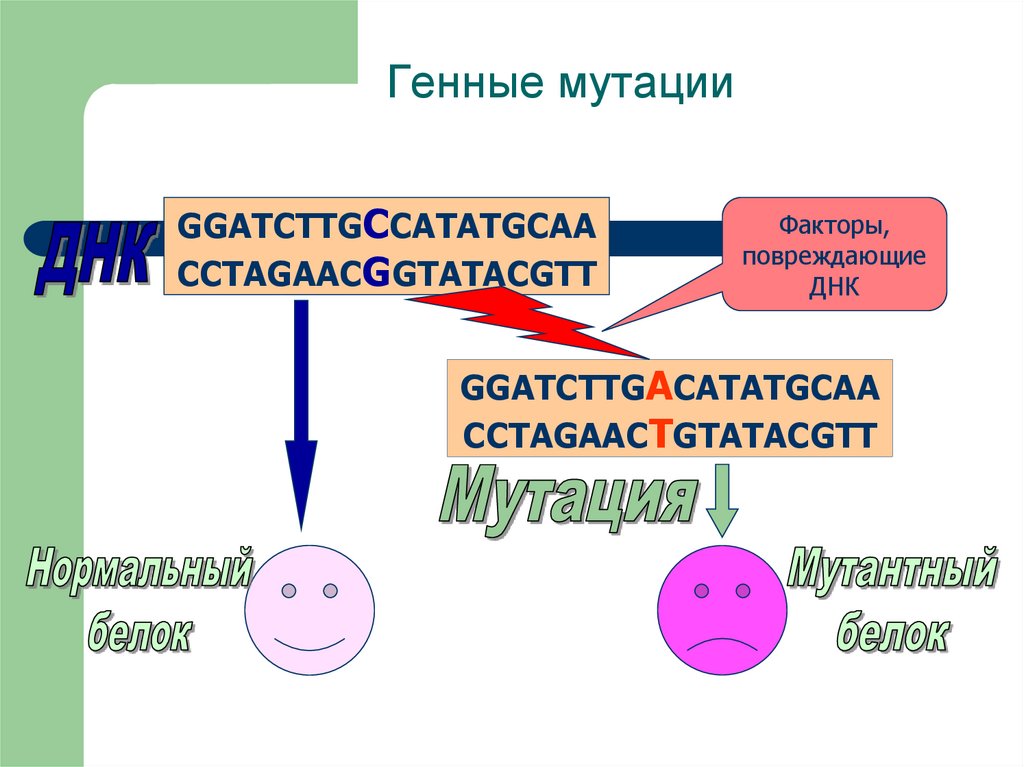
9. Генные мутации
GGATCTTGCCATATGCAACCTAGAACGGTATACGTT
Факторы,
повреждающие
ДНК
GGATCTTGАCATATGCAA
CCTAGAACТGTATACGTT
10. Повреждения (мутации) протоонкогенов
Мутацияпротоонкогена
Активация
онкогена
Нарушение системы
передачи сигналов
Усиленная
пролиферация клеток
(«преимущество пролиферации»)
11. Повреждения (мутации) антионкогенов
Мутацияантионкогена
Инактивация
антионкогена
Нарушение системы
передачи сигналов
Утрата ограничивающих
пролиферацию стимулов
(«преимущество пролиферации»),
нарушение дифференцировки
12. Роль апоптоза в канцерогенезе:
Активацияwр53
МИТОЗ
Ингибирование
wр53
Завершение митоза
«Арест» клетки
в G1
Сканирование
ДНК
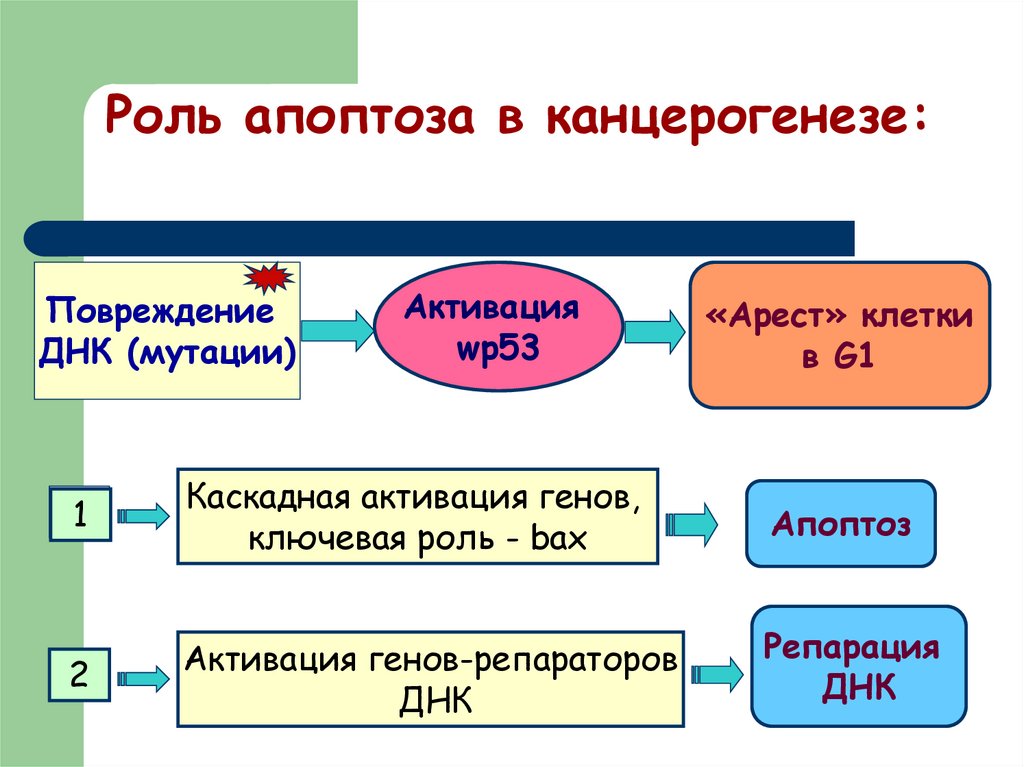
13. Роль апоптоза в канцерогенезе:
ПовреждениеДНК (мутации)
Активация
wр53
«Арест» клетки
в G1
1
Каскадная активация генов,
ключевая роль - bax
Апоптоз
2
Активация генов-репараторов
ДНК
Репарация
ДНК
14. The Intrinsic Apoptosis Pathway
ChemotherapyRadiotherapy
DNA damage
p53
Cell-intrinsic
pathway
PUMA, NOXA
BAX, BAK
BCL2, BCLXL,
MCL1
Mitochondria
Caspase 9
Caspase 3, 6, 7
Cytochrome
c
APAF1
SMAC/DIABLO
IAP
p53
p53
Apoptosis
DNA damage
Adapted from Ashkenazi A. Nat Rev Cancer 2002;2:420–430.
APAF1, apoptotic protease activating factor-1; BAK, BCL2 homologous antagonist/killer; BAX, BCL2-associated protein; BCL2, B-cell
chronic lymphocytic leukemia/lymphoma 2; BCLXL, BCL2-like 1; IAP, inhibitor of apoptosis protein; MCL1, myeloid cell leukemia
sequence 1 (BCL2-related); PUMA, p53-upregulated modulator of apoptosis; SMAC/DIABLO: second mitochondria-derived activator of
caspase/direct IAP binding protein with low pI.
15. Apoptosis is Carried out by Caspases
Pro-apoptotic stimulusInitiator caspases
Caspase
cascade
Effector caspases
Apoptosis
Adapted from Thornberry NA, Lazebnik Y. Science 1998;281:1312–1316.
Caspase, cysteine aspartase.
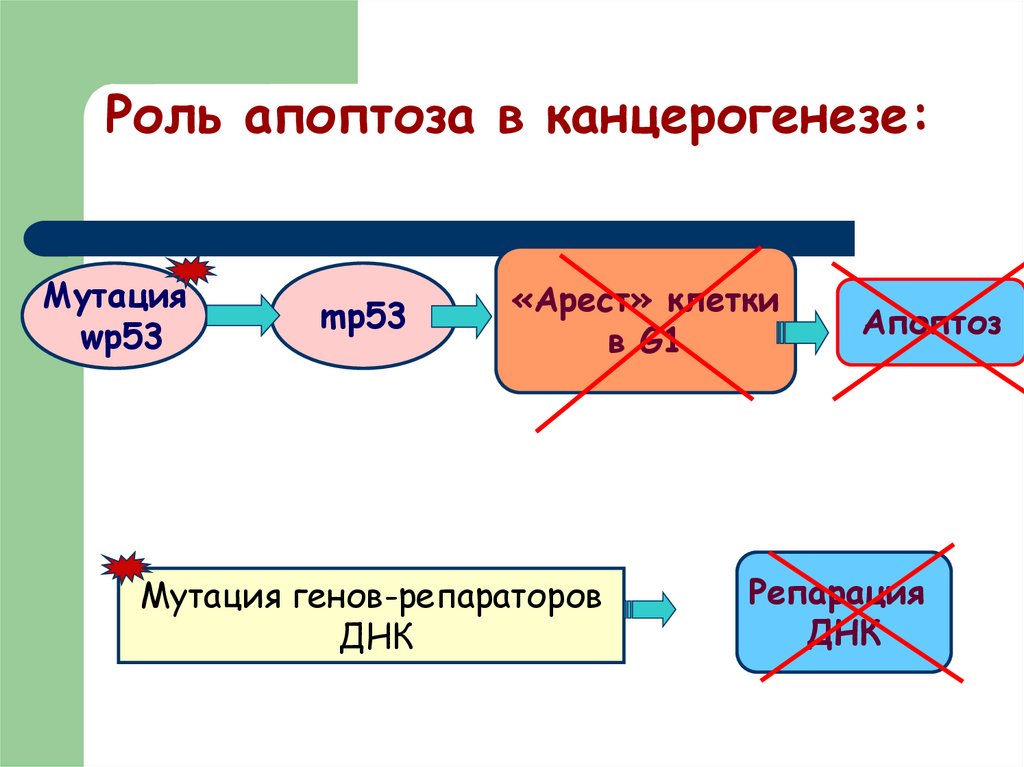
16. Роль апоптоза в канцерогенезе:
Мутацияwр53
mр53
«Арест» клетки
в G1
Мутация генов-репараторов
ДНК
Апоптоз
Репарация
ДНК
17. Основные типы генетических повреждений в канцерогенезе:
Амплификация (her-2-neu)Транслокация (t(8;14) - лимфома Беркитта)
Инсерция (incertion - вставка)
Делеция (del(13q) - Rb)
Инверсия (переворот)
Точечные мутации (р53)
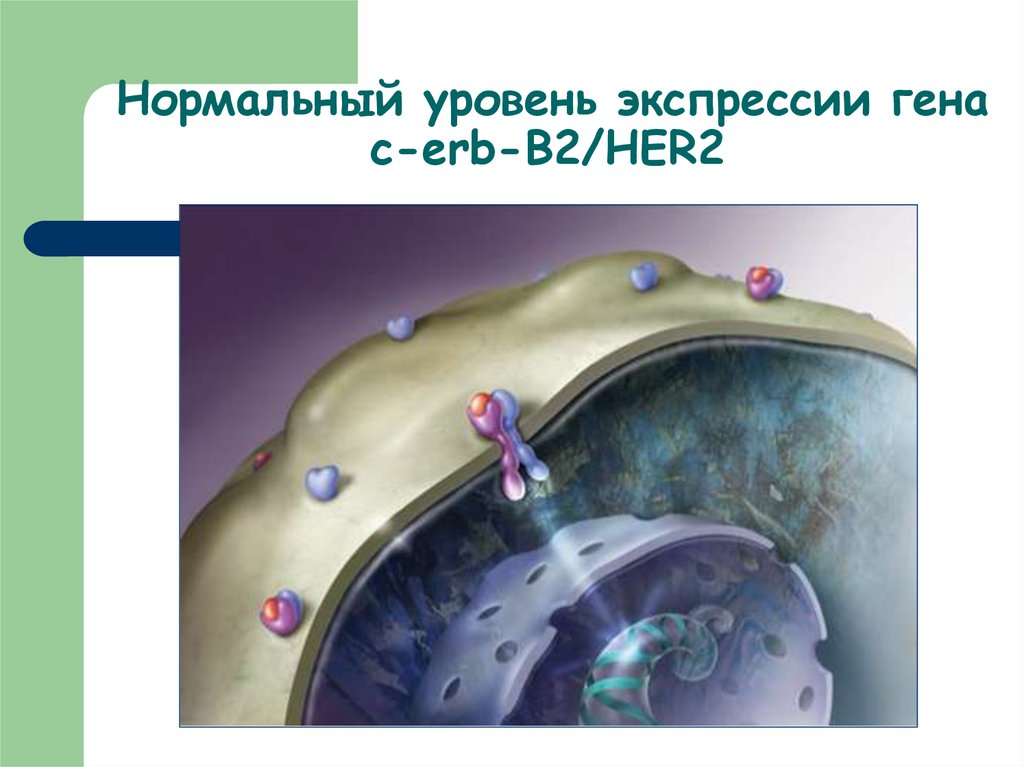
18. Нормальный уровень экспрессии гена c-erb-B2/HER2
19. Амплификация приводит к гиперэкспрессии HER2
20.
Флуоресцентная гибридизацияin-situ (FISH)
Нет амплификации
HER2 -
Амплификация
HER2 +
21. Гиперэкспрессия HER2 приводит к пролиферации клеток опухоли
22. Основные типы генетических повреждений в канцерогенезе:
Амплификация (her-2-neu)Транслокация (t(8;14) - лимфома Беркитта)
Инсерция (incertion - вставка)
Делеция (del(13q) - Rb)
Инверсия (переворот)
Точечные мутации (р53)
23.
t(14;18)Translokation
Kromosom 18
Kromosom 18 q-
Kromosom 14
Kromosom 14 q+
Фолликулярная лимфома
24. FISH: t(14;18)
Normal18
14
14
18
14
18
14
18
t(14;18)
25. Основные типы генетических повреждений в канцерогенезе:
Амплификация (her-2-neu)Транслокация (t(8;14) - лимфома Беркитта)
Инсерция (incertion - вставка)
Делеция (del(13q) - Rb)
Инверсия (переворот)
Точечные мутации (р53)
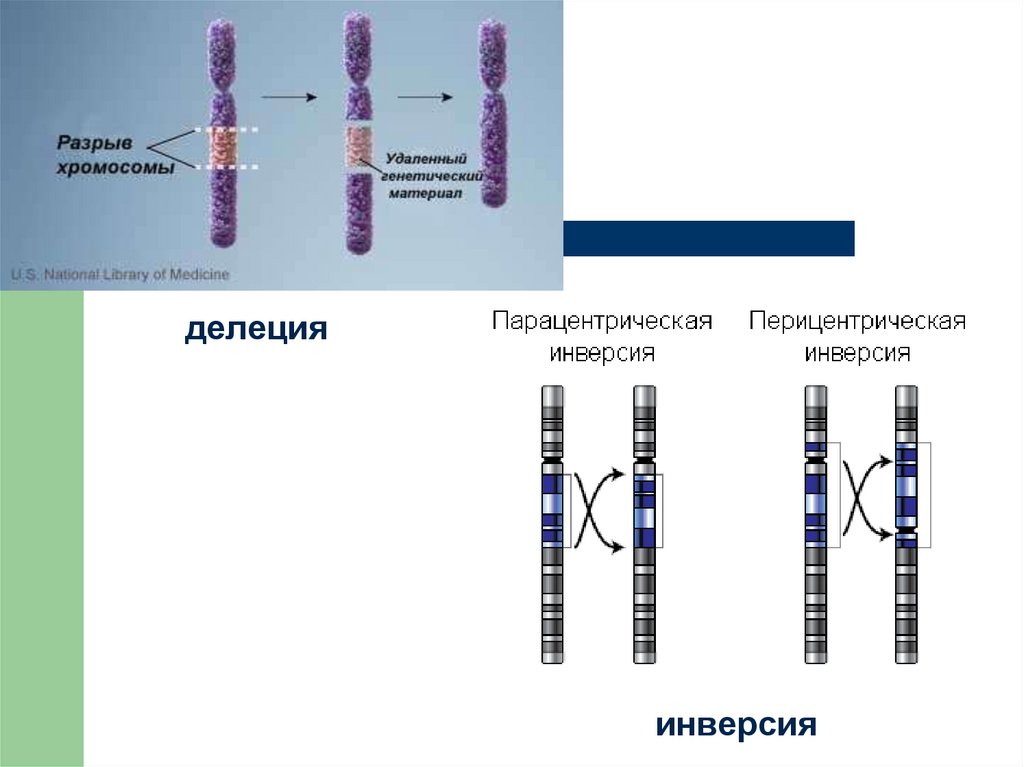
26. делеция
инверсия27. «Теории» опухолевого роста:
Вирусно-генетическаяФизико-химическая
Полиэтиологическая
Дизонтогенетическая
ПОВРЕЖДЕНИЯ ГЕНОМА
28.
HPV (+)29. Опухоль – поэтапно развивающийся процесс
30.
31. Основные свойства опухолей:
Автономный ростАтипизм
Метастазирование
Прогрессирование
32. АТИПИЗМ (atypicus (греч.))- структурные и функциональные признаки, отличающие опухолевую ткань от нормальной
АТИПИЗМ (atypicus (греч.))структурные и функциональныепризнаки, отличающие опухолевую
ткань от нормальной
Морфологический
Биохимический
Гистохимический
Антигенный
Функциональный
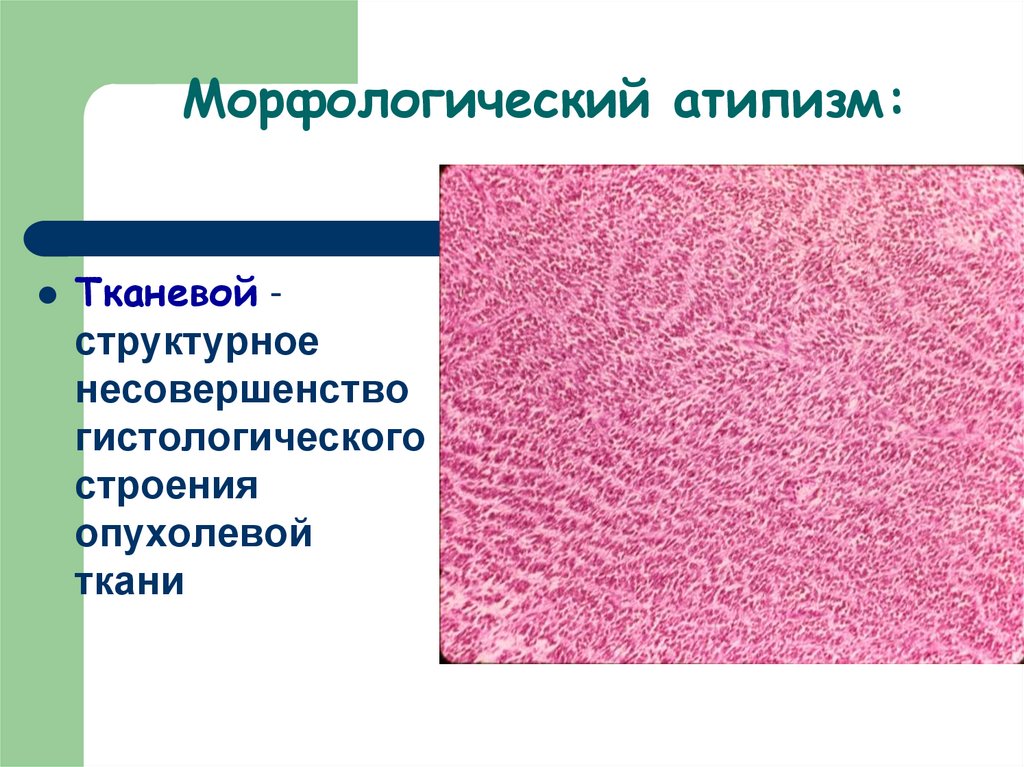
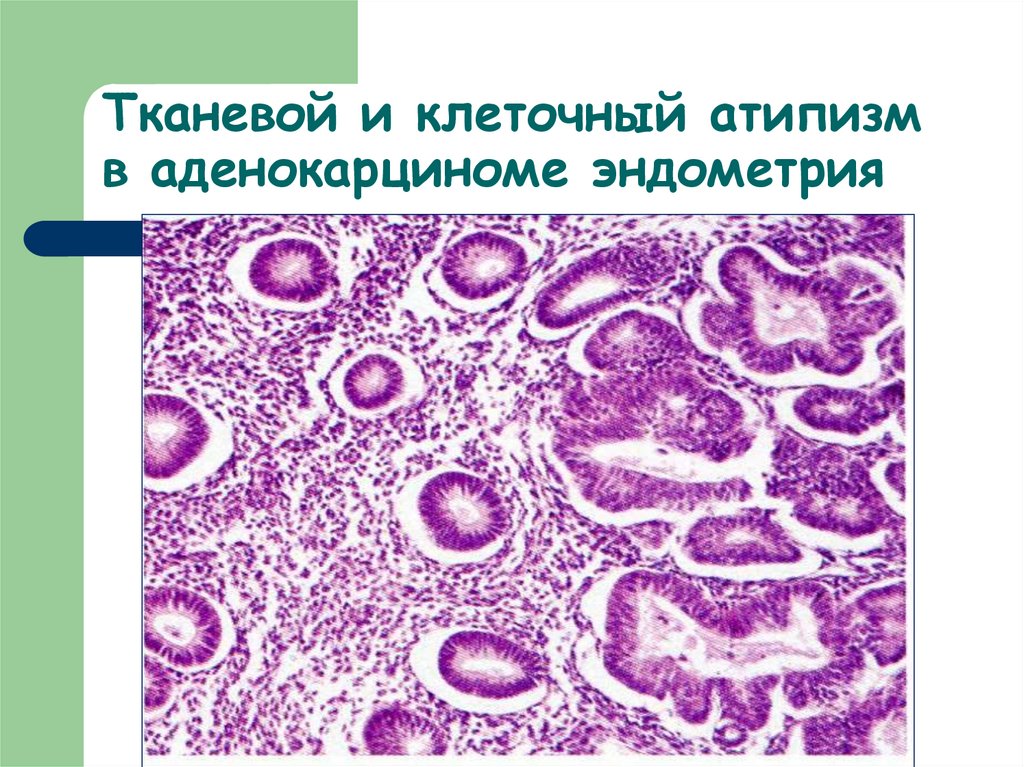
33. Морфологический атипизм:
Тканевой структурноенесовершенство
гистологического
строения
опухолевой
ткани
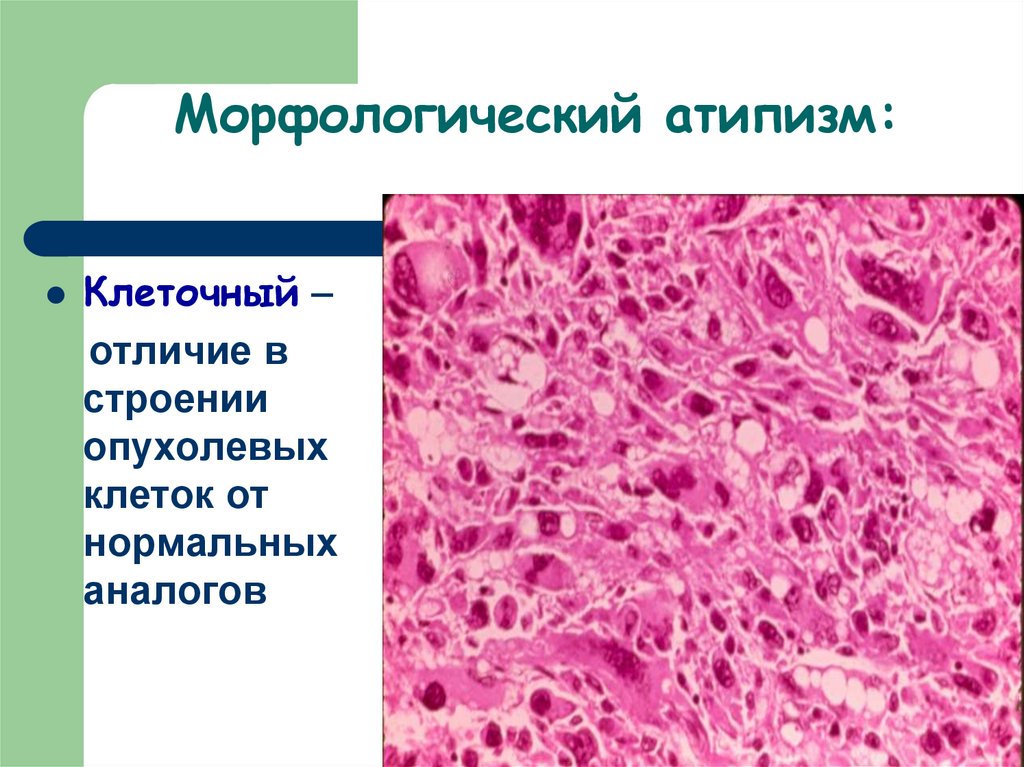
34. Морфологический атипизм:
Клеточный –отличие в
строении
опухолевых
клеток от
нормальных
аналогов
35. Тканевой и клеточный атипизм в аденокарциноме эндометрия
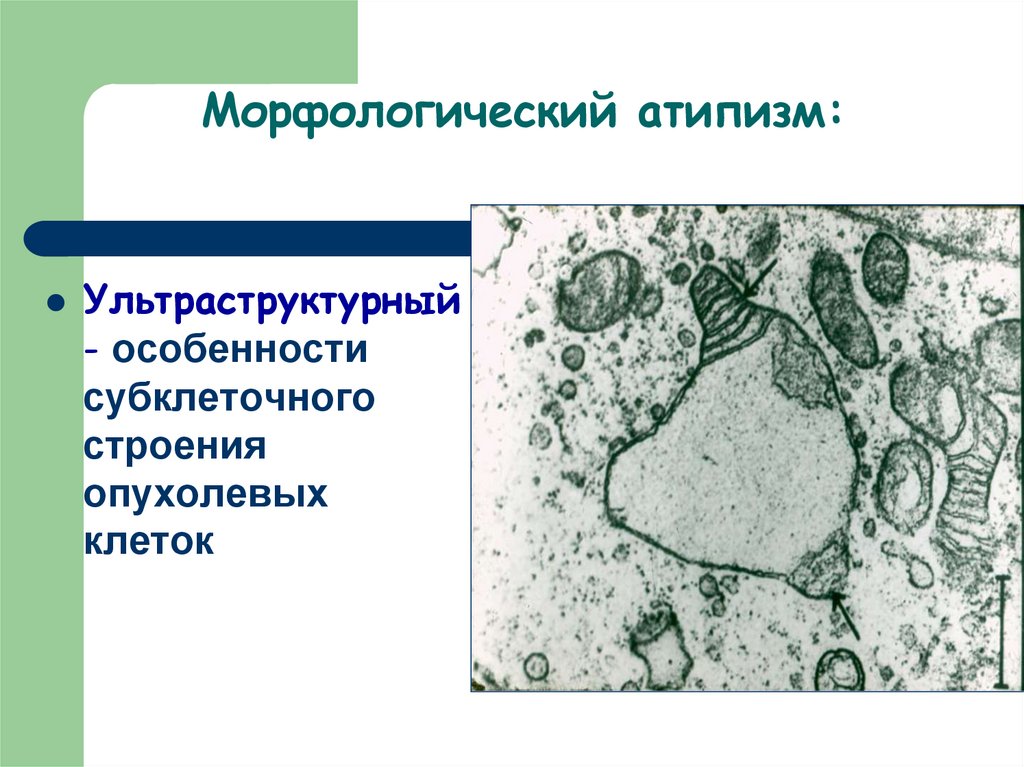
36. Морфологический атипизм:
Ультраструктурный- особенности
субклеточного
строения
опухолевых
клеток
37.
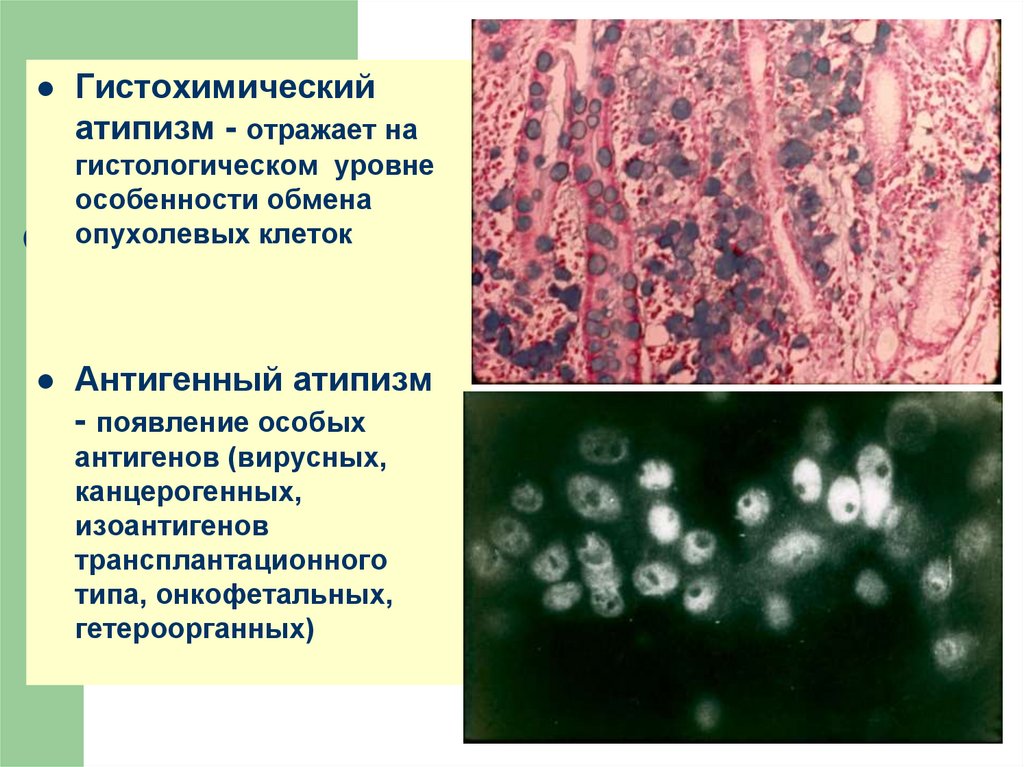
Гистохимическийатипизм - отражает на
гистологическом уровне
особенности обмена
опухолевых клеток
Антигенный атипизм
- появление особых
антигенов (вирусных,
канцерогенных,
изоантигенов
трансплантационного
типа, онкофетальных,
гетероорганных)
38. Влияние опухолей на организм:
ОБЩЕЕ (изменениеобмена,
интоксикация,
гормональная
активность)
МЕСТНОЕ
(сдавливание
органов, сосудов или
нервов, врастание и
разрушение тканей)
39.
Для опухолевых клеток применяюттермины:
- малодифференцированная
- недифференцированная
- дедифференцированная
- бластная
Д.С. Саркисов: «Опухолевая
клетка в своем развитии делает не
шаг назад, а шаг в сторону».
40.
ОПУХОЛИ возникают из любых клетоктканей организма, в любой
локализации, любом возрасте.
ОПУХОЛИ
ДОБРОКАЧЕСТВЕННЫЕ
ЗЛОКАЧЕСТВЕННЫЕ
Основной принцип деления опухолей
на доброкачественные и злокачественные –
степень зрелости (дифференцировки) клеток –
степень их соответствия неопухолевому аналогу!
41.
ПРИЗНАКИДОБРОКАЧЕСТВЕННЫЕ
ЗЛОКАЧЕСТВЕННЫЕ
Генетические
повреждения
Единичные , могут
отсутствовать у
гормонзависимых
Чаще множественные
Степень
дифференцировки
Зрелые,
дифференцированные
Незрелые, недифференцированные
Атипизм
Тканевой
Все виды атипизма
Тип роста
Экспансивный
Инфильтрирующий,
аппозиционный
Метастазирование
Нет
Есть
Рецидивирование
Есть, редко
Есть, часто
Скорость роста
Медленно
Быстро
Влияние на
организм
Местное, общее у
гормональноактивных
Местное и общее
Малигнизация
Малигнизируются
-
42. Гистогенетическая классификация опухолей:
Эпителиальные опухоли без специфическойлокализации (органонеспецифические)
Эпителиальные опухоли экзо- и эндокринных
желез (органоспецифические)
Мезенхимальные опухоли
Опухоли меланинобразующей ткани
Опухоли нервной ткани и оболочек мозга
Опухоли системы крови
Тератомы
43. Роль иммунной системы в канцерогенезе
В организме опухоленосителяобнаруживаются противоопухолевые
антитела и цитотоксические лимфоцитыкиллеры.
По периферии новообразования
формируются скопления
иммунокомпетентных клеток: лимфоцитов,
макрофагов.
Риск развития опухоли значительно
повышается при иммунодефицитных
состояниях
44. Роль иммунной системы в канцерогенезе
Противоопухолевыйиммунитет
Клеточный
иммунитет
Гуморальный
иммунитет
45. Роль иммунной системы в канцерогенезе
Т-киллерПолиморфноклеточная
опухоль
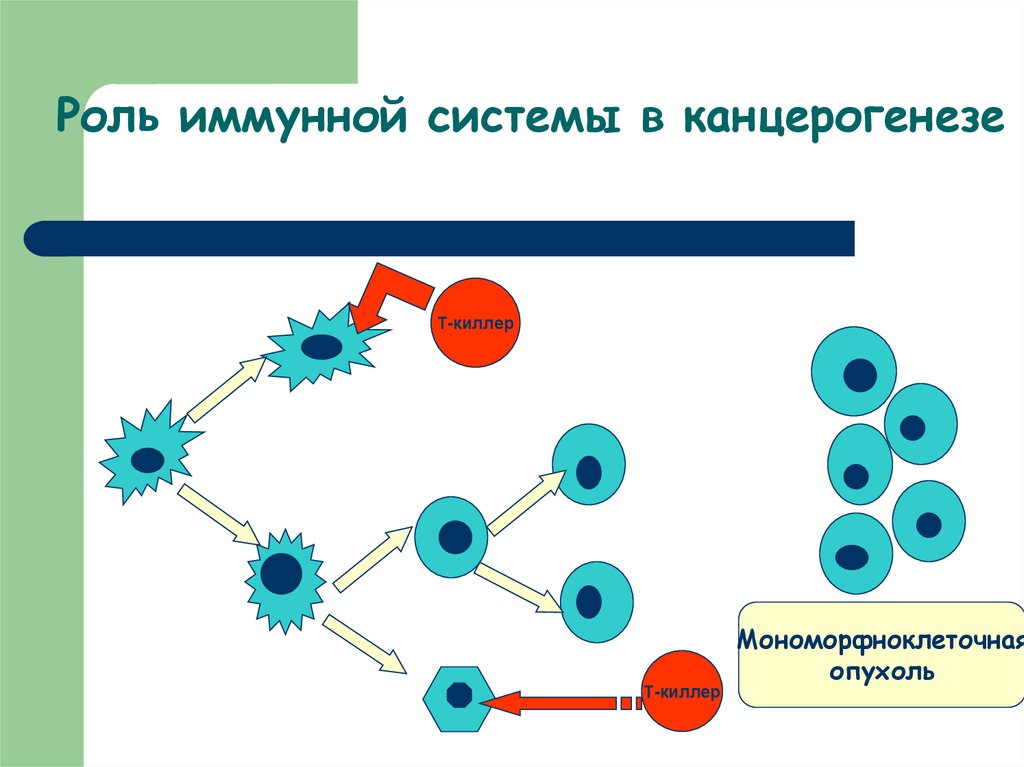
46. Роль иммунной системы в канцерогенезе
Т-киллерТ-киллер
Мономорфноклеточная
опухоль
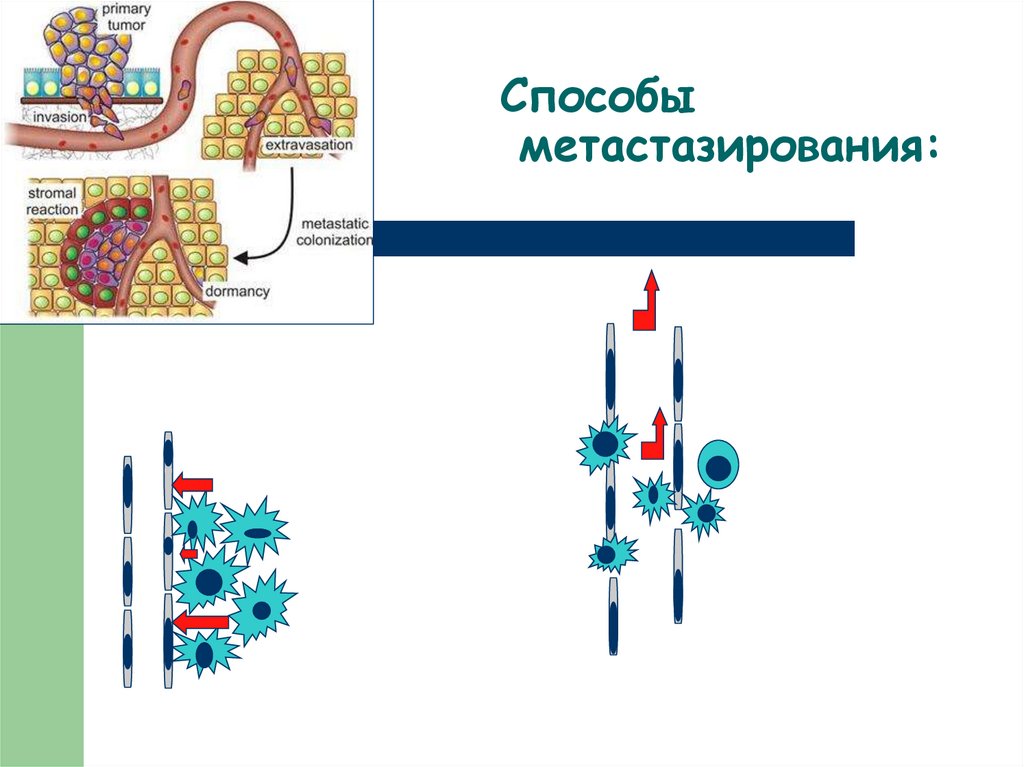
47. МЕТАСТАЗИРОВАНИЕ - распространение опухолевых клеток или их перенос в другие органы и ткани с образованием дочерних опухолевых
узловГематогенный путь
Лимфогенный путь
Контактный
(имплантационный,
«по продолжению»,
«по соприкосновению»)
48. Способы метастазирования:
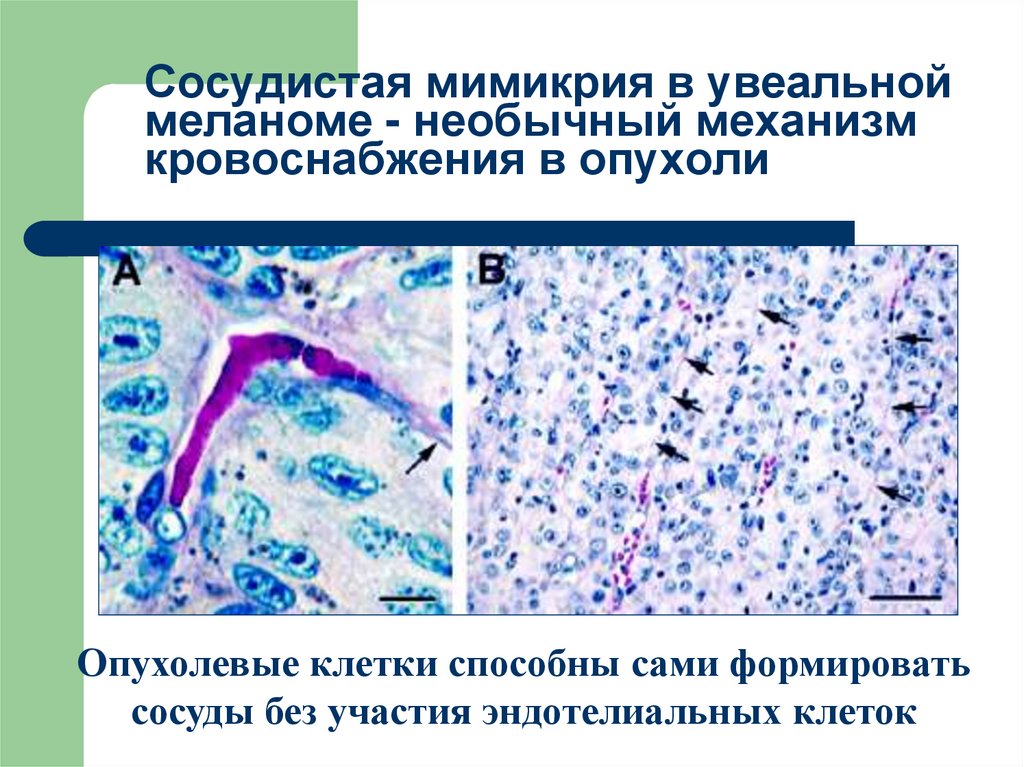
49. Сосудистая мимикрия в увеальной меланоме - необычный механизм кровоснабжения в опухоли
Опухолевые клетки способны сами формироватьсосуды без участия эндотелиальных клеток
50.
Значение неоангиогенезапри злокачественных опухолях
Высокая плотность
микрососудов в опухоли
Гиперэкспрессия
VEGF в опухоли
Прогностическая ценность плотности микрососудов и
экспрессии VEGF в опухоли доказана при раке легкого, яичника,
простаты, мочевого пузыря, пищевода, желудка, толстой кишки,
меланоме
Высокая плотность микрососудов и гиперэкспрессия VEGF
сочетается с агрессивным течением болезни
51. В канцерогенезе описаны два варианта развития злокачественных опухолей:
«de novo» или «c места в карьер»через поэтапное развитие
структурно-функциональных
изменений в ткани, для чего был
введен термин «дисплазия»
(неоплазия)
52. Дисплазия -нарушение пролиферации и дифференцировки эпителиальных клеток, сопровождающееся появлением признаков
морфологического атипизма.Уже регистрируются единичные генетические
перестройки, запускающие избыточную
пролиферацию
Формируется на основе фоновых болезней
Расценивается как предопухолевое состояние
Имеет 3 прогрессирующие степени: легкую,
среднюю и тяжелую.
На тяжелой стадии является необратимой
Прогрессирует в carcinoma in situ.
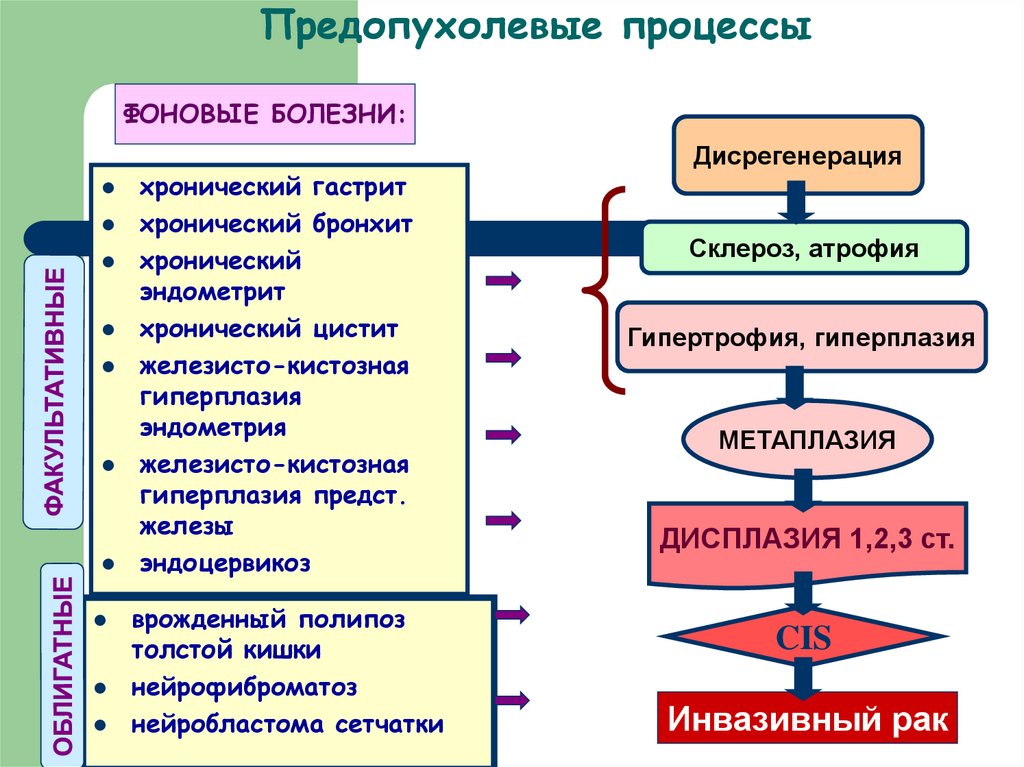
53. Предопухолевые процессы
ФОНОВЫЕ БОЛЕЗНИ:хронический гастрит
хронический бронхит
хронический
эндометрит
хронический цистит
железисто-кистозная
гиперплазия
эндометрия
железисто-кистозная
гиперплазия предст.
железы
эндоцервикоз
врожденный полипоз
толстой кишки
нейрофиброматоз
нейробластома сетчатки
Дисрегенерация
Склероз, атрофия
Гипертрофия, гиперплазия
МЕТАПЛАЗИЯ
ДИСПЛАЗИЯ 1,2,3 ст.
CIS
Инвазивный рак
54. CIN I
CIN II55. CIN I
CIN II56.
CIN IIICIS
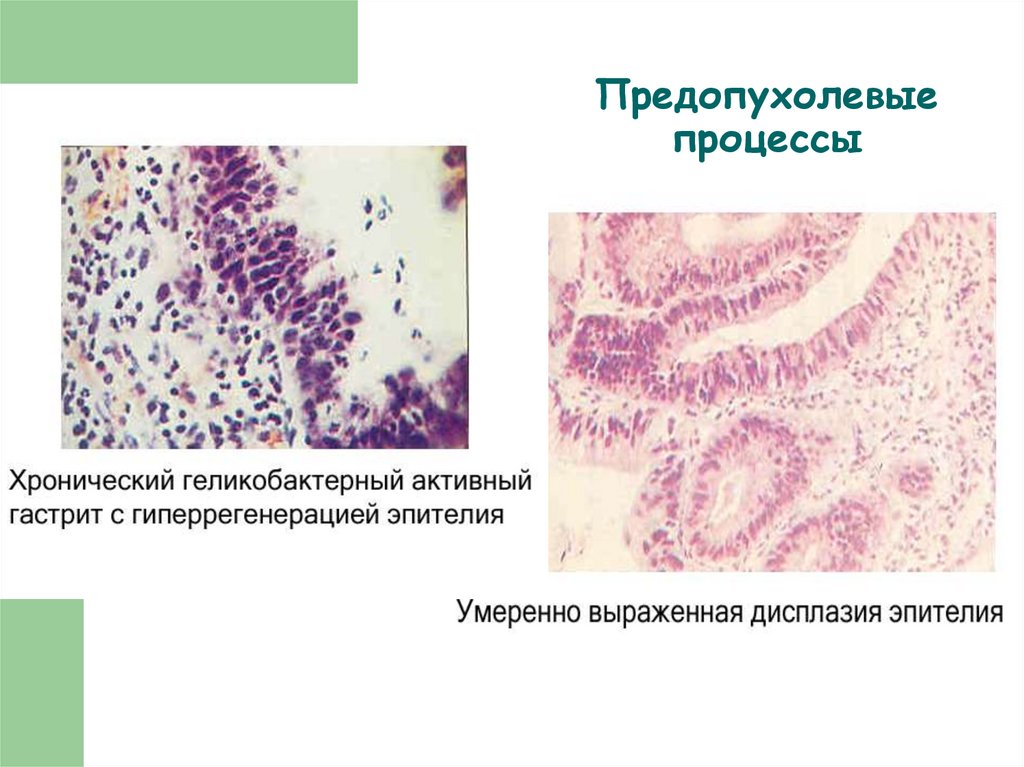
57. Предопухолевые процессы
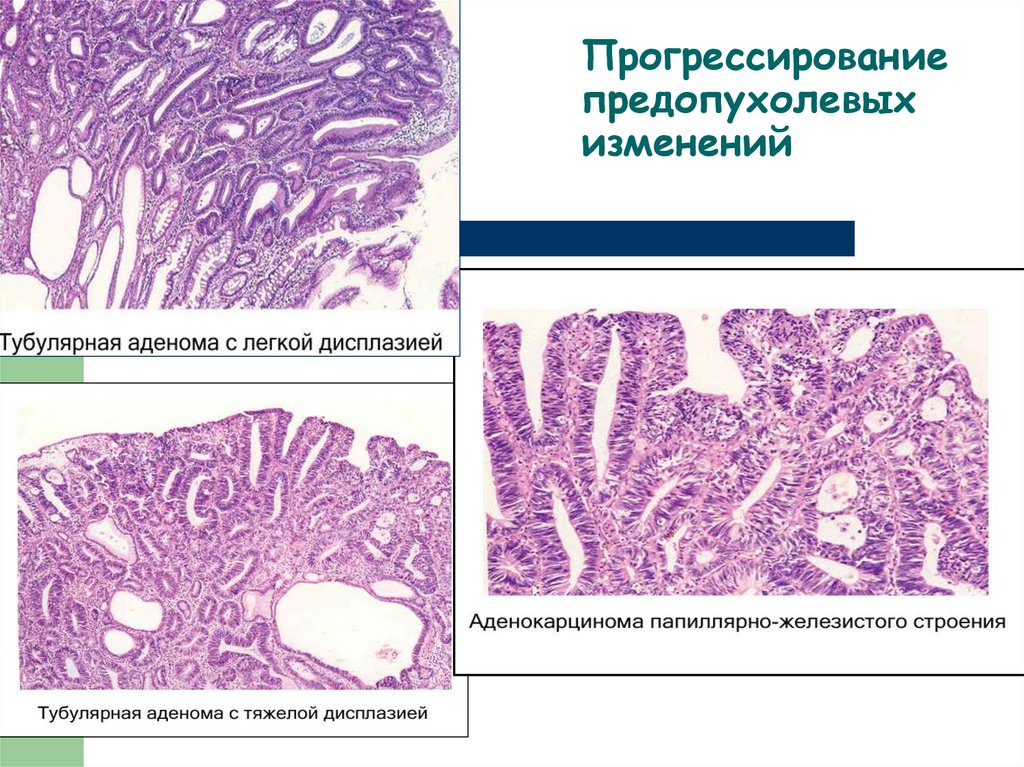
58. Прогрессирование предопухолевых изменений
59.
ПатоморфогенезФенотип
норма
Генотип
фон
мутация АРС гена
дисплазия
«ранняя» аденома
мутация K-ras гена
«средняя» аденома
мутация DCC гена
«поздняя» аденома
мутация p53 гена
неоплазия
дополнительные мутации
метастазы
C.B.Diep et al., 2004
дополнительные мутации
прогрессия
60.
Рак кишечного типаD1S191 нестабильность
Мутации APC, p53,
K-ras
Гиперметилирование
ДНК
Мутации p53/LOH
Экспрессии р27
C-erbB2
pS2
Кишечная
метаплазия
Норм. СО
Аденома
Ранний
рак
Инвазия
метастазы
Cохранение pS2
Хромос. 7q LOH,
1p36 (p73) LOH
cyclin E,
Генетическая
нестабильность
Редукция теломер
Активация
теломеразы,
Абберантная
экспрессия TERT
транскрипция
CD44,
гиперэкспрессия
Cyclin E, CDC25B
Экспрессия р27, nm23
Ранний
рак
Норм. СО
Р53 мутация/LOH
Кадгерин мутация/утрата
Y.Wataru et al., 1999
Экспрессия факторов
роста
Рак диффузного типа
Инвазия
метастазы
К-sam, c-met
61.
Я теперь уже точно знаюкто ты есть,
но я пока еще не знаю,
но скоро узнаю
как тебя успокоить
62. Гиперэкспрессия HER2 приводит к пролиферации клеток опухоли
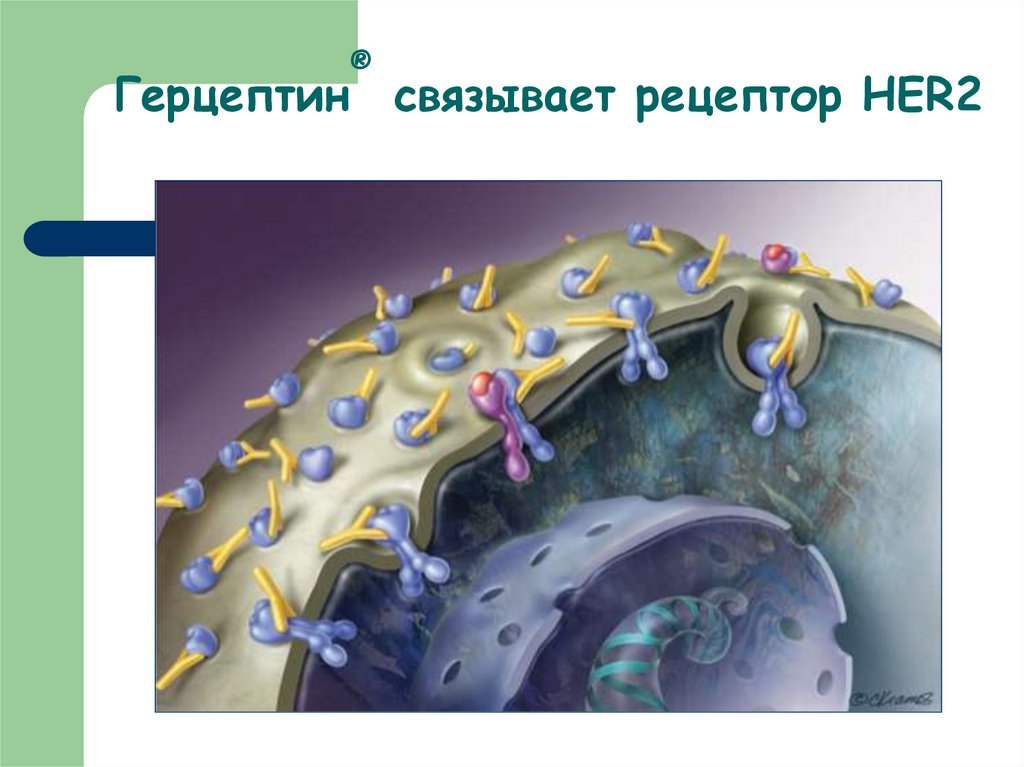
63. Герцептин® связывает рецептор HER2
®Герцептин связывает рецептор HER2
64.
Я теперь уже не толькоточно знаю кто ты есть,
но я уже хорошо
представляю как, а иногда
и могу тебя успокоить











































 Медицина
Медицина








