Похожие презентации:
Моносахариды. Ди- и полисахариды. (Лекция 6)
1. МОНОСАХАРИДЫ. ДИ- и ПОЛИСАХАРИДЫ.
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕУЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ
«БАШКИРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КАФЕДРА ОБЩЕЙ ХИМИИ
Лекция № 6
МОНОСАХАРИДЫ.
ДИ- и ПОЛИСАХАРИДЫ.
2.
Углеводы – это многоатомные альдегидо- иликетоспирты (полиоксикарбонильные
соединения) и их производные с общей
формулой Сn(H2O)m.
• Биологическая роль:
1 - энергетический материал для жизнедеятельности человека;
составляют 55-65% пищи;
2 - структурная функция – входят в состав гликопротеинов,
нуклеиновых кислот, являются компонентами биомембран
клетки;
3 - запасная, резервная функция: гликоген – запасной углевод
организма; при необходимости способен превращаться в жиры
и откладываться;
4 - иммунологические свойства - входят в состав антител (γглобулинов крови);
5 - некоторые проявляют биологическую активность: гепарин
(антикоагулянт крови), сердечные гликозиды (лечебные
препараты), мукополисахариды (связывают воду и ионы).
3.
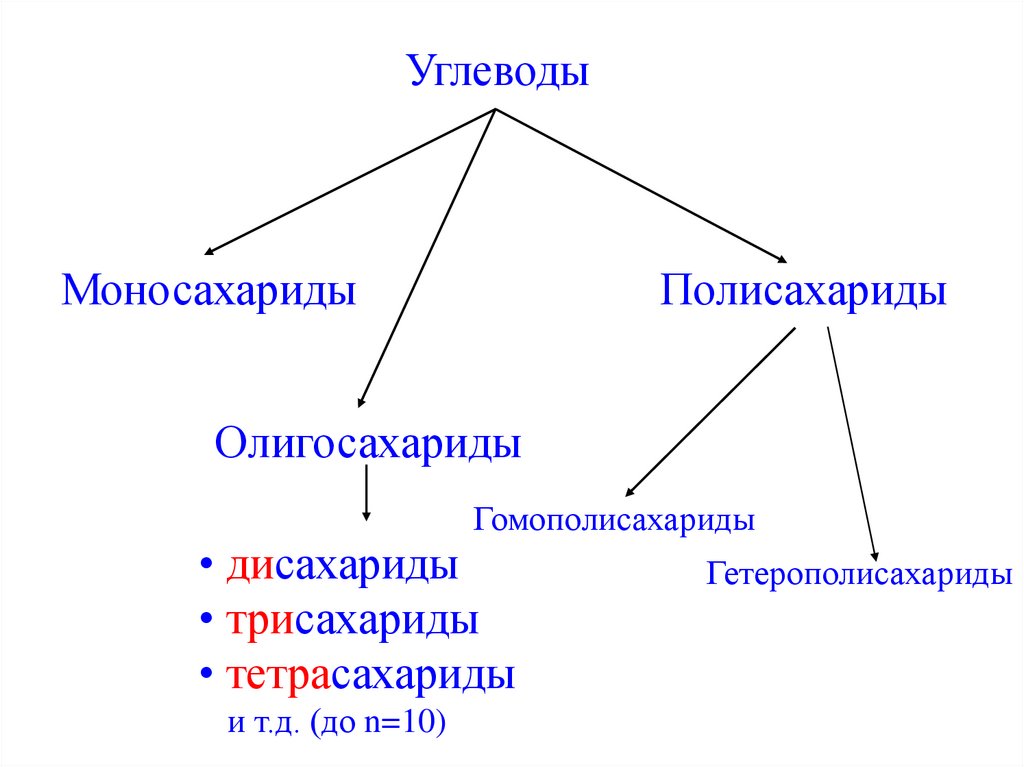
УглеводыМоносахариды
Полисахариды
Олигосахариды
Гомополисахариды
• дисахариды
• трисахариды
• тетрасахариды
и т.д. (до n=10)
Гетерополисахариды
4.
• Моносахариды – это простые углеводы, которые врастворе не гидролизируют.
Классификация.
1. По количеству атомов С на:
а) триозы (С3)
б) тетрозы (С4)
в) пентозы (С5) (рибоза, дезоксирибоза, ксилоза)
г) гексозы (С6) (глюкоза, галактоза, манноза, фруктоза)
2. По главной функциональной группе:
а) альдозы (глюкоза, галактоза, манноза, рибоза, ксилоза)
б) кетозы (фруктоза)
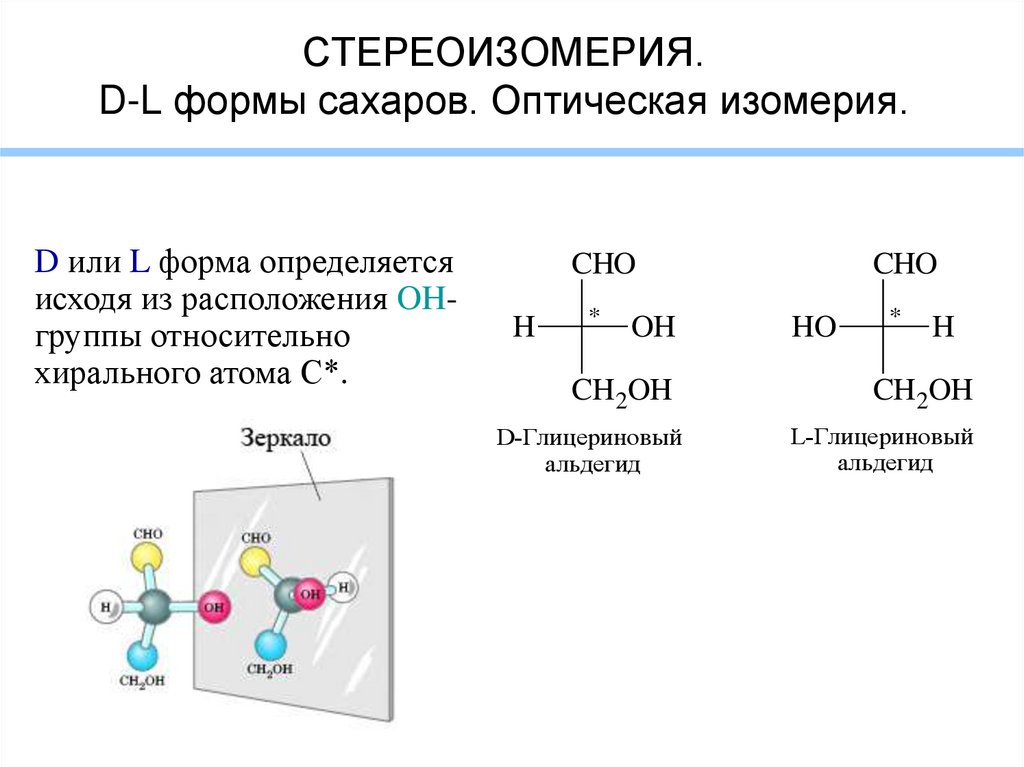
5. СТЕРЕОИЗОМЕРИЯ. D-L формы сахаров. Оптическая изомерия.
D или L форма определяетсяисходя из расположения OHгруппы относительно
хирального атома С*.
CHO
H
*
OH
CH2OH
D-Глицериновый
альдегид
CHO
HO
*
H
CH2OH
L-Глицериновый
альдегид
6.
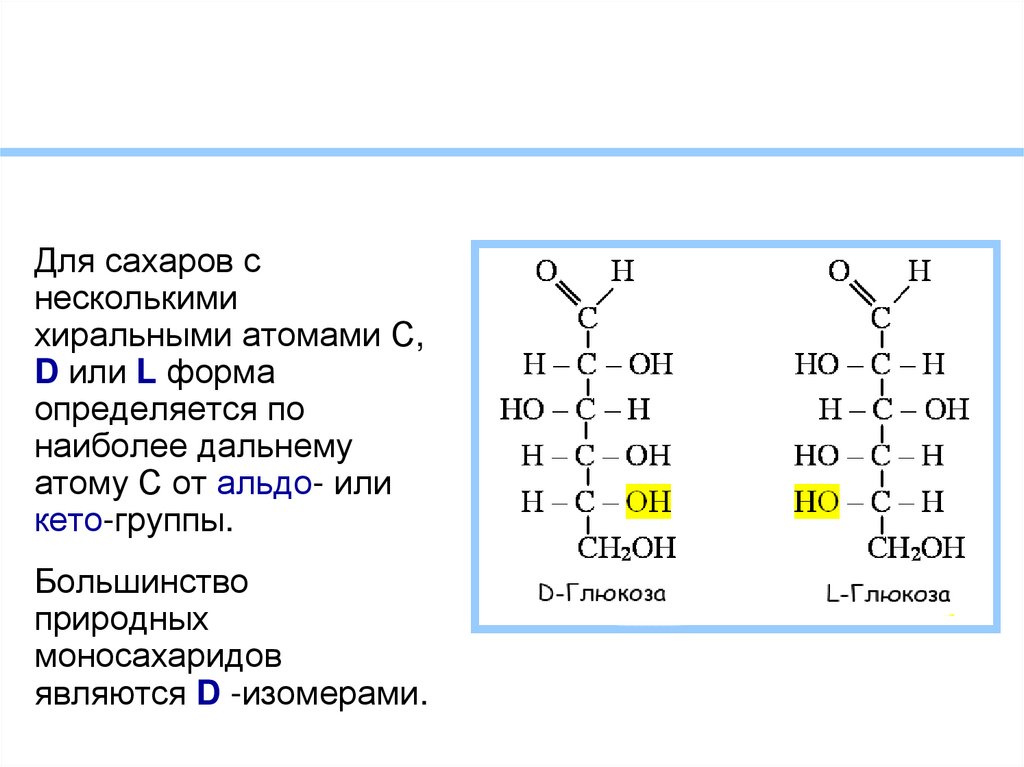
Для сахаров снесколькими
хиральными атомами С,
D или L форма
определяется по
наиболее дальнему
атому С от альдо- или
кето-группы.
Большинство
природных
моносахаридов
являются D -изомерами.
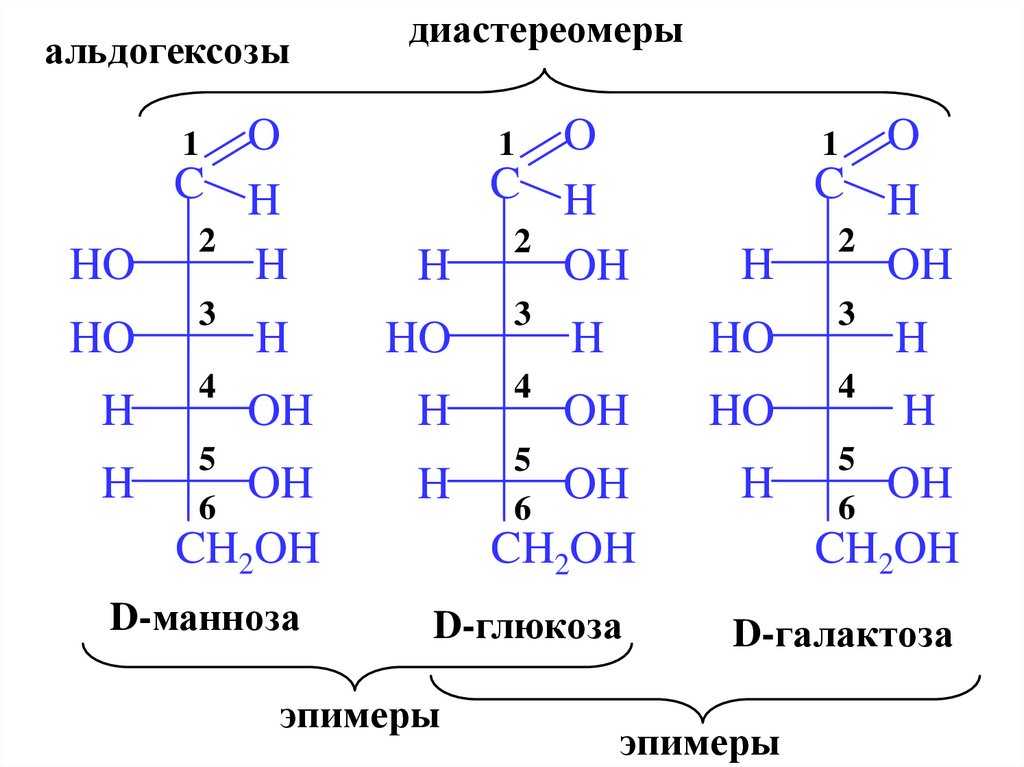
7.
альдогексозыO
C H
2
HO
H
1
HO
H
H
3
4
H
OH
5
6
OH
CH2OH
D-манноза
диастереомеры
O
C H
2
H
OH
O
C H
2
H
OH
3
3
1
HO
H
H
4
H
HO
OH
5
6
OH
CH2OH
D-глюкоза
эпимеры
1
HO
H
4
H
H
5
6
OH
CH2OH
D-галактоза
эпимеры
8.
HO
C H
OH
H
OH
H
OH
HO
H
OH
H
OH
H
CH2OH
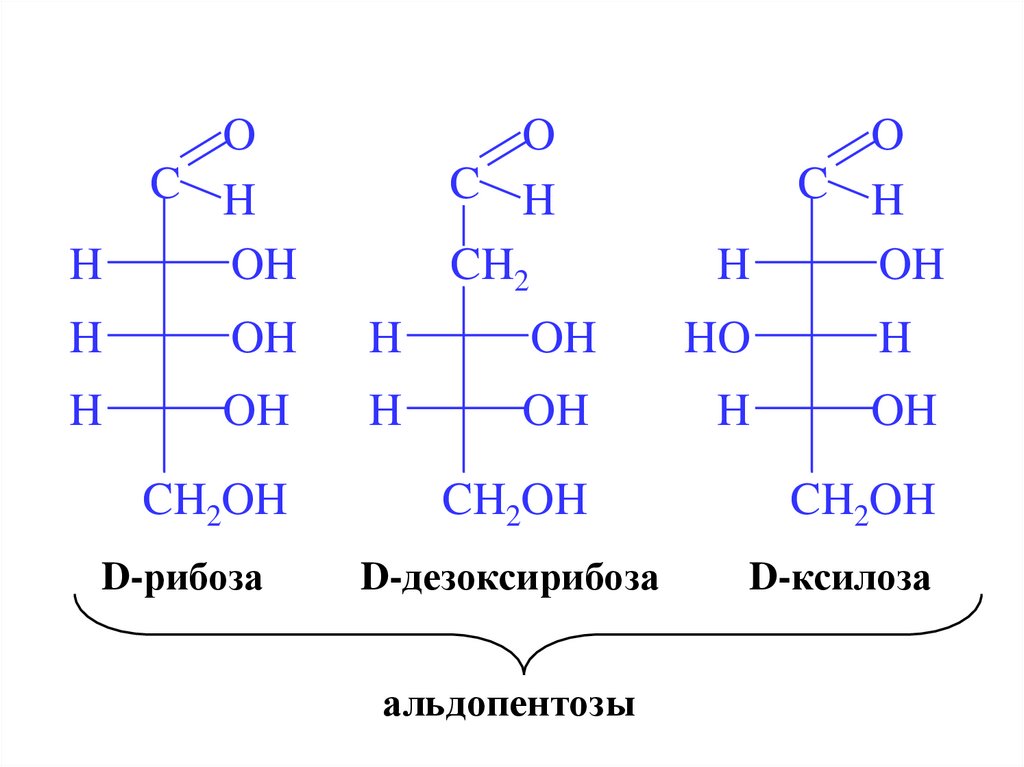
D-рибоза
O
C H
CH2
CH2OH
D-дезоксирибоза
альдопентозы
H
O
C H
OH
H
OH
CH2OH
D-ксилоза
9.
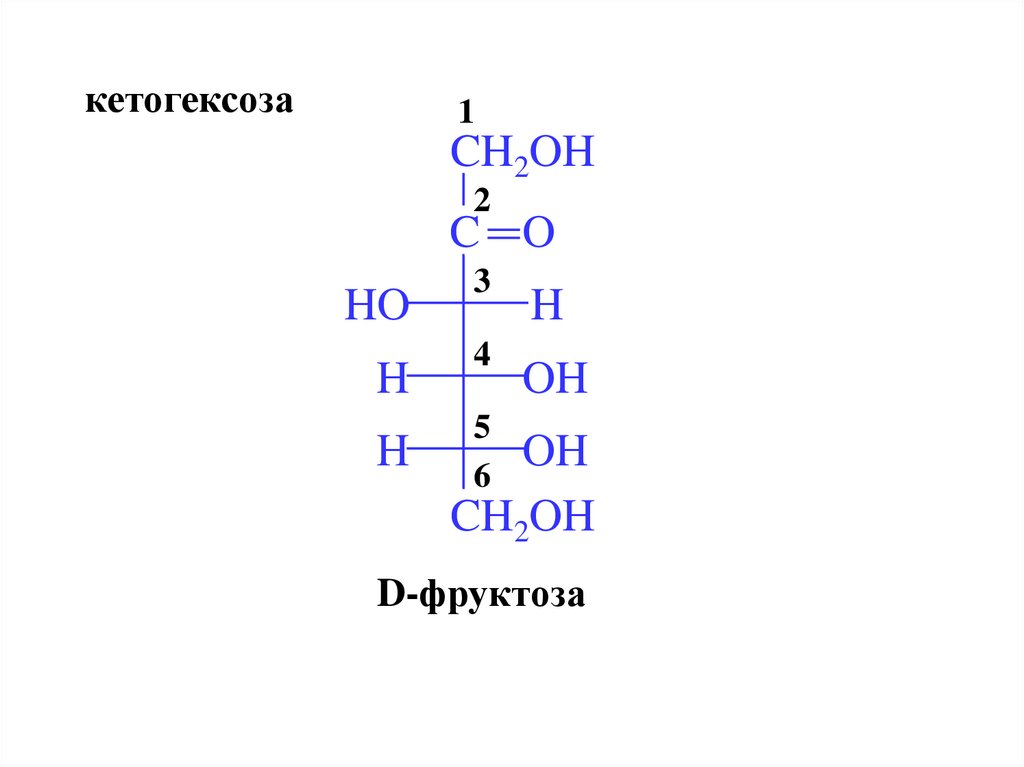
кетогексоза1
CH2OH
2
C O
HO
H
H
3
4
H
OH
5
6
OH
CH2OH
D-фруктоза
10. Цикло-оксо-таутомерия моносахаридов
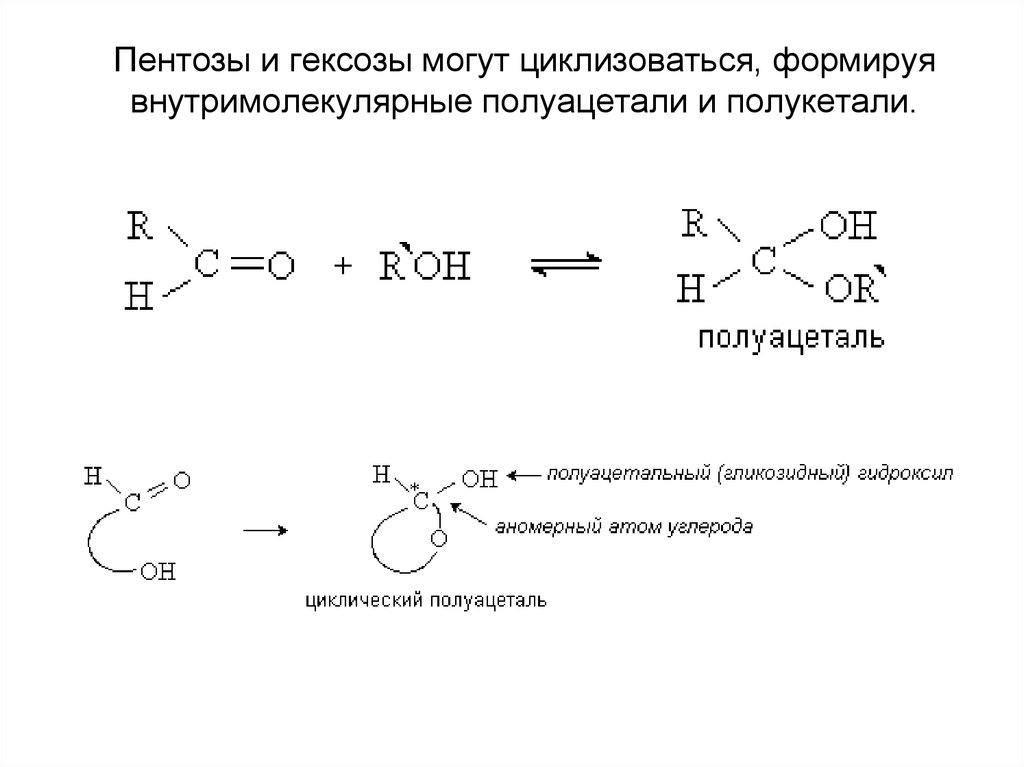
11. Пентозы и гексозы могут циклизоваться, формируя внутримолекулярные полуацетали и полукетали.
12. МОНОСАХАРИДЫ
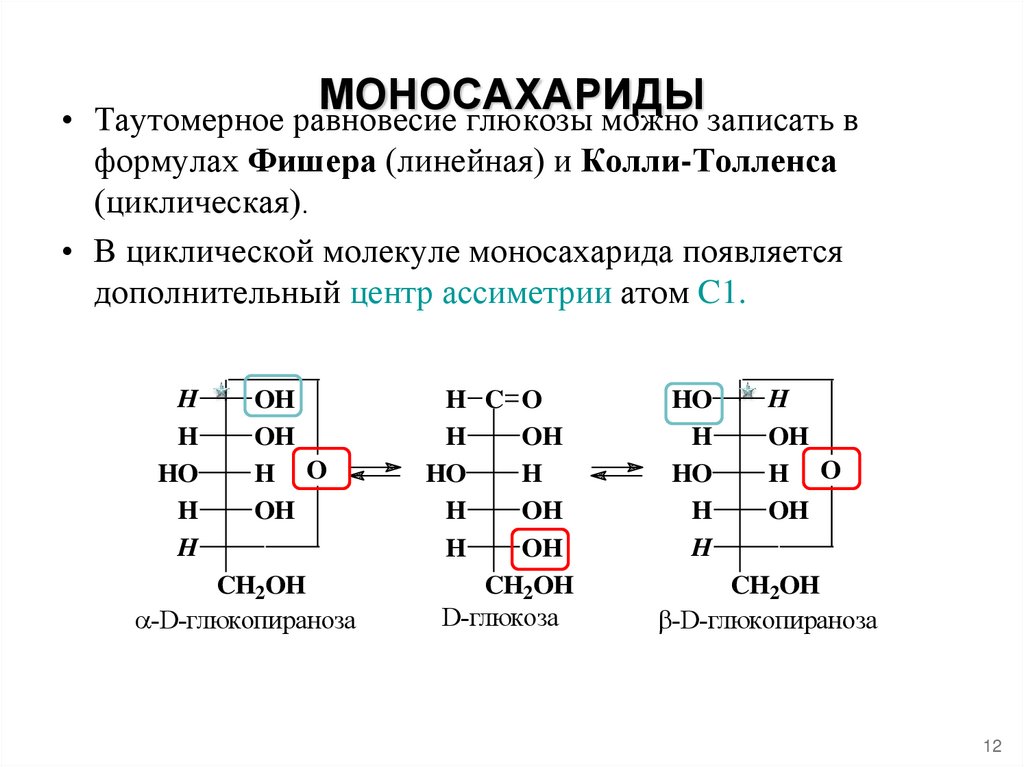
МОНОСАХАРИДЫ
Таутомерное равновесие глюкозы можно записать в
формулах Фишера (линейная) и Колли-Толленса
(циклическая).
• В циклической молекуле моносахарида появляется
дополнительный центр ассиметрии атом C1.
H
H
HO
H
H
OH
OH
H O
OH
CH2OH
-D-глюкопираноза
H C O
H
OH
HO
H
H
OH
H
OH
CH2OH
D-глюкоза
HO
H
HO
H
H
H
OH
H O
OH
CH2OH
-D-глюкопираноза
12
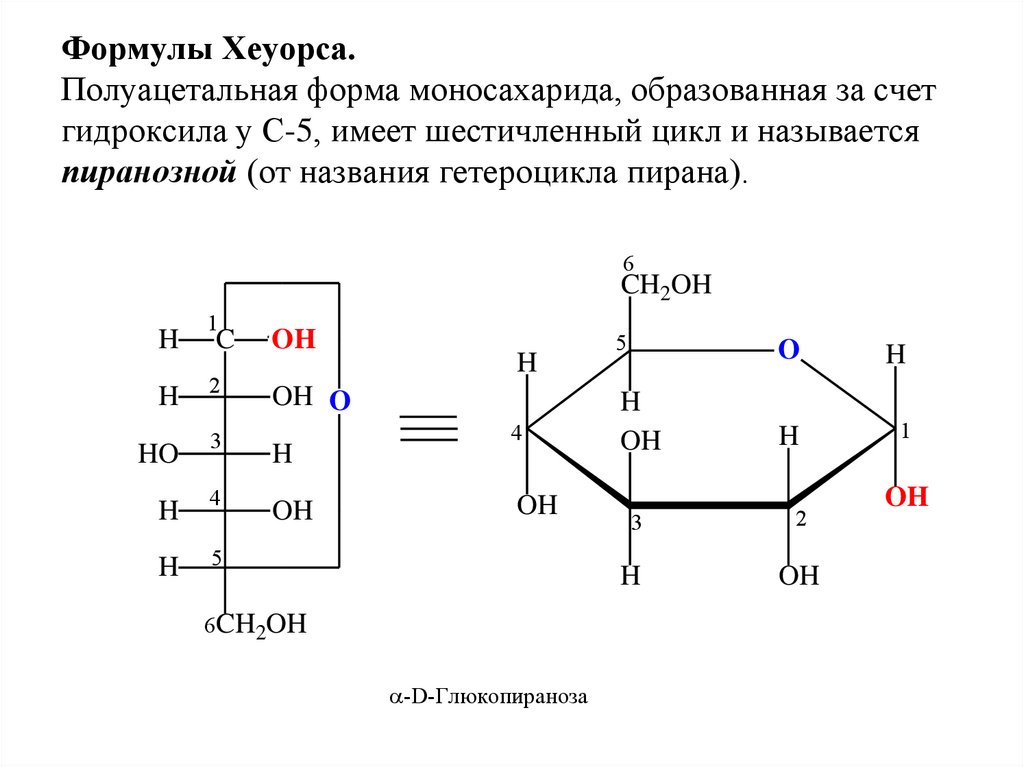
13. Формулы Хеуорса. Полуацетальная форма моносахарида, образованная за счет гидроксила у С-5, имеет шестичленный цикл и называется
пиранозной (от названия гетероцикла пирана).6
CH2OH
H
H
HO
H
H
1
C
2
3
4
OH
H
OH O
H
OH
4
OH
5
5
O
H
H
OH
H
1
3
H
6CH2OH
-D-Глюкопираноза
2
OH
OH
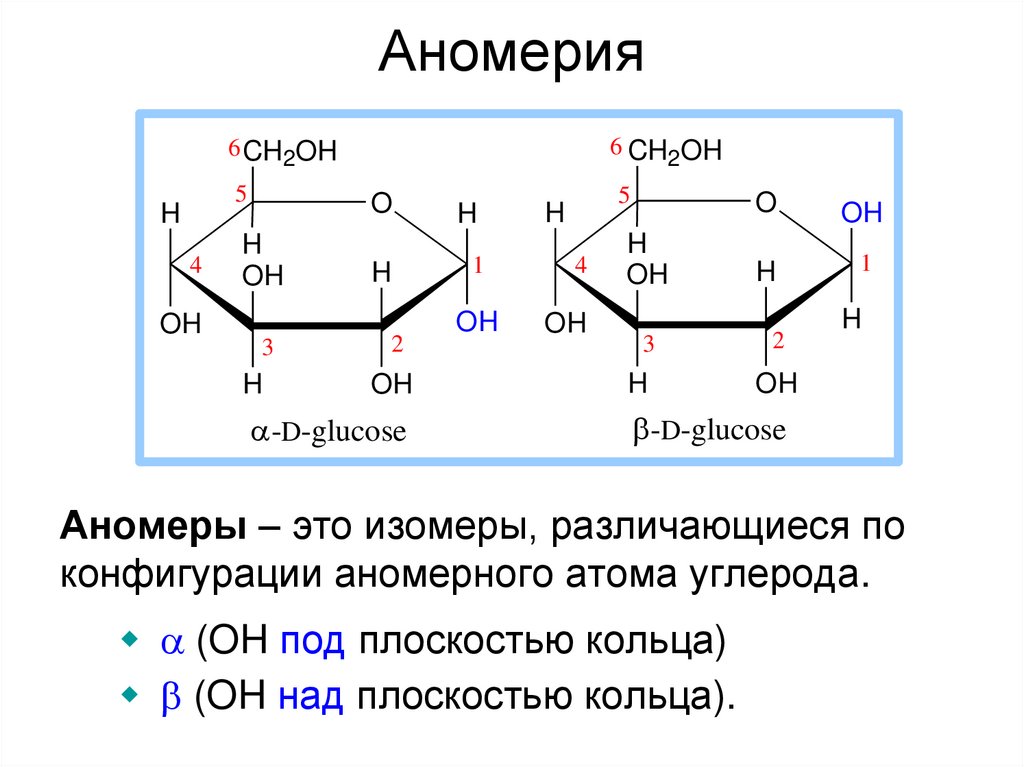
14. Аномерия
6 CH2OH6 CH2OH
5
H
4
OH
O
H
OH
3
H
H
2
OH
-D-glucose
H
1
OH
5
H
4
OH
H
OH
3
H
O
OH
H
1
2
H
OH
-D-glucose
Аномеры – это изомеры, различающиеся по
конфигурации аномерного атома углерода.
(OH под плоскостью кольца)
(OH над плоскостью кольца).
15.
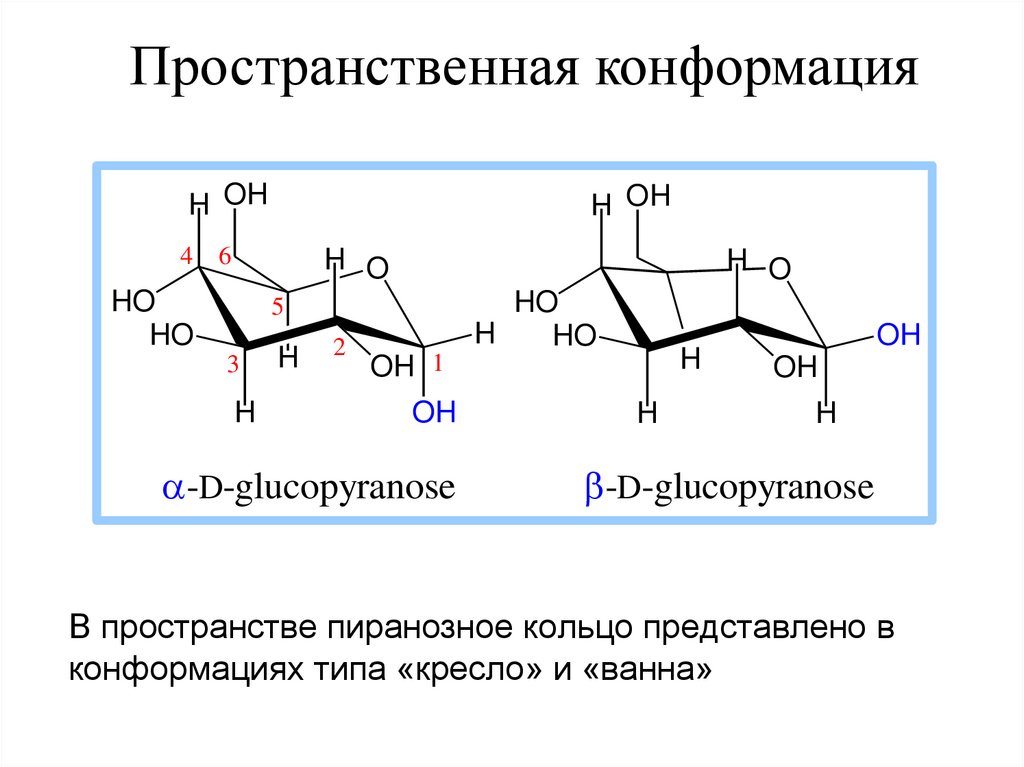
Пространственная конформацияH OH
4
H OH
6
H O
HO
HO
H O
HO
H
HO
5
3
H
H
2
H
OH 1
OH
-D-glucopyranose
H
OH
OH
H
-D-glucopyranose
В пространстве пиранозное кольцо представлено в
конформациях типа «кресло» и «ванна»
16. МОНОСАХАРИДЫ. Химические свойства
• Основные типы реакционной способности моносахаридовопределяются наличием в их таутомерных формах:
карбонильной группы,
полуацетального гидроксила,
спиртовых гидроксилов.
16
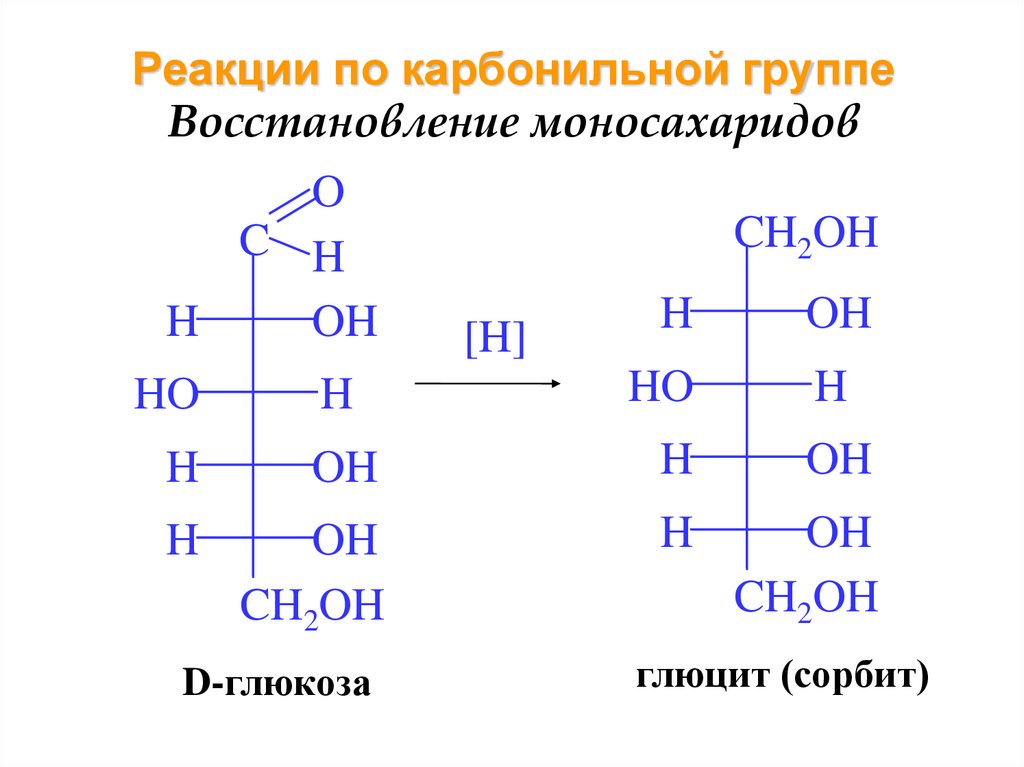
17. Реакции по карбонильной группе Восстановление моносахаридов
OC H
H
OH
HO
H
CH2OH
[H]
H
HO
OH
H
H
OH
H
OH
H
OH
CH2OH
H
OH
CH2OH
D-глюкоза
глюцит (сорбит)
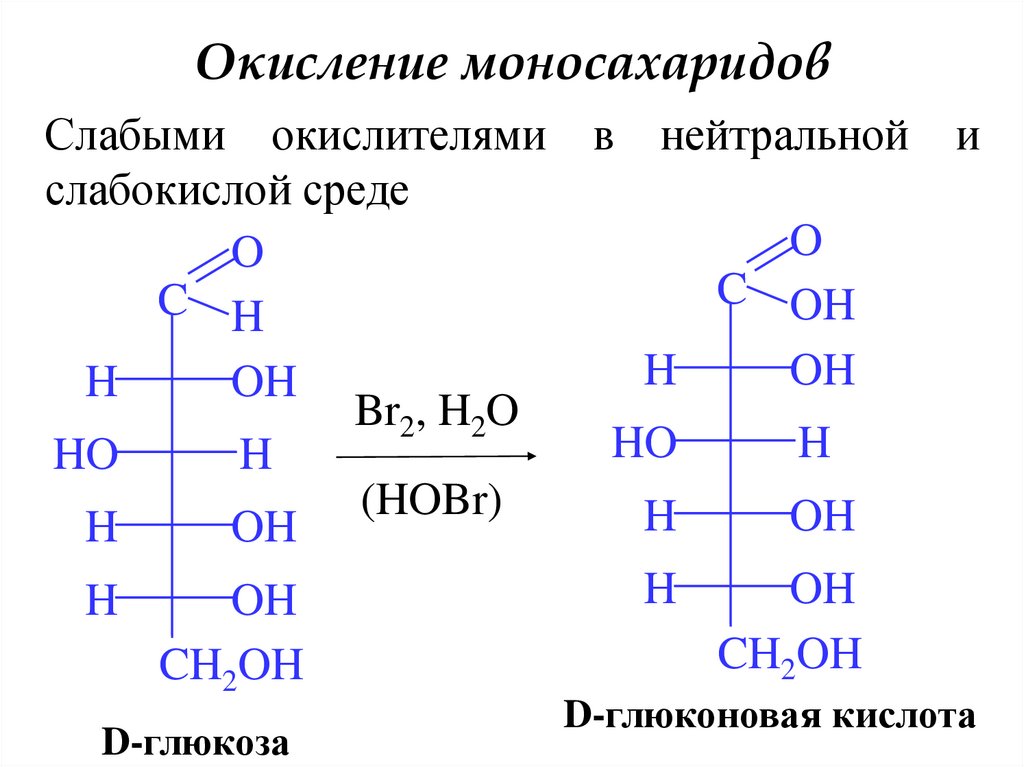
18. Окисление моносахаридов
Слабыми окислителямислабокислой среде
O
C H
H
OH
Br2, H2O
HO
H
(HOBr)
H
OH
H
OH
CH2OH
D-глюкоза
в
нейтральной
и
O
C OH
H
OH
HO
H
H
OH
H
OH
CH2OH
D-глюконовая кислота
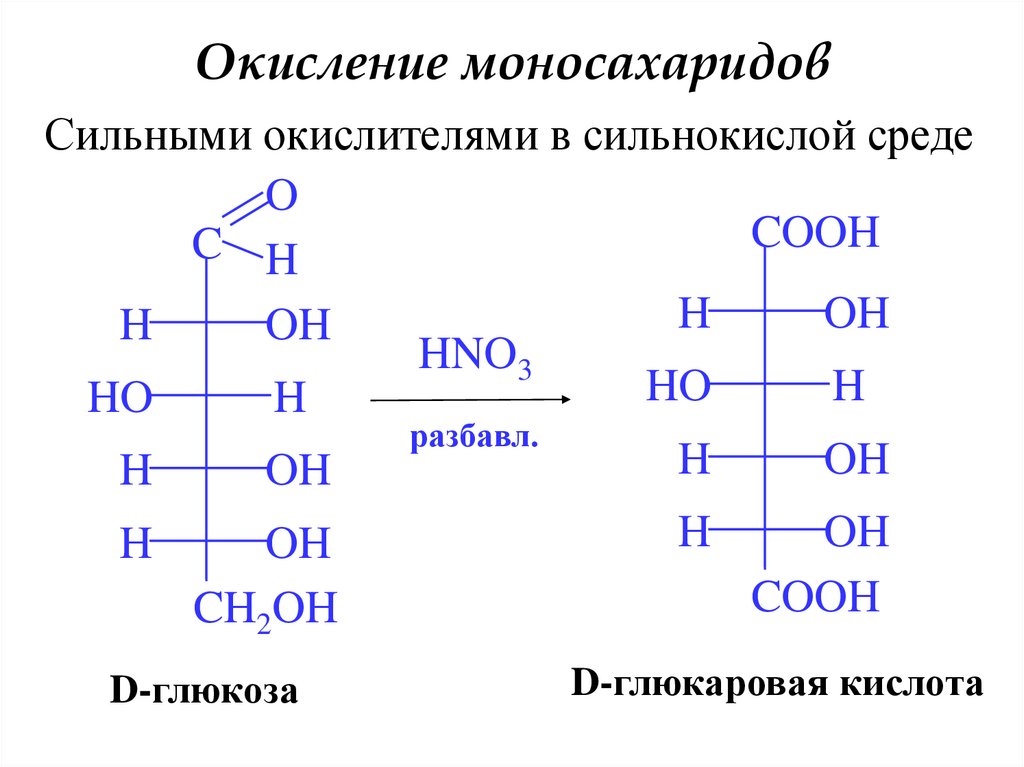
19. Окисление моносахаридов
Сильными окислителями в сильнокислой средеO
COOH
C H
H
OH
H
OH
HNO3
HO
H
HO
H
H
OH
H
OH
CH2OH
D-глюкоза
разбавл.
H
OH
H
OH
COOH
D-глюкаровая кислота
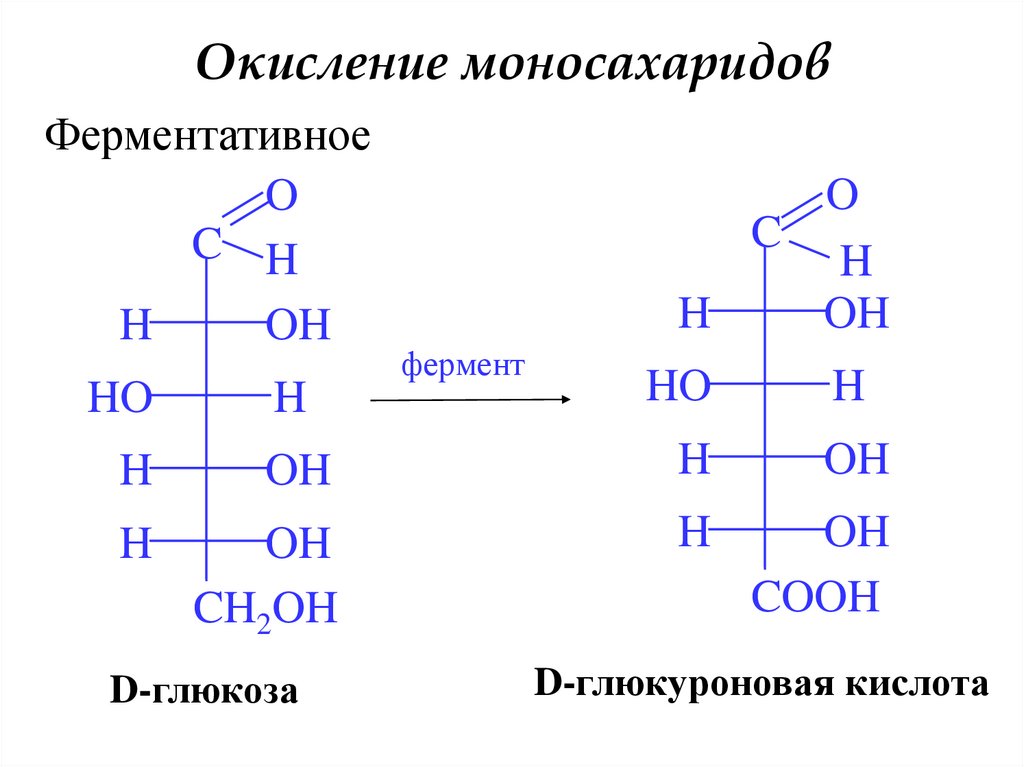
20. Окисление моносахаридов
ФерментативноеO
C H
H
OH
HO
H
O
C
H
H
OH
фермент
HO
H
H
OH
H
OH
H
OH
CH2OH
H
OH
COOH
D-глюкоза
D-глюкуроновая кислота
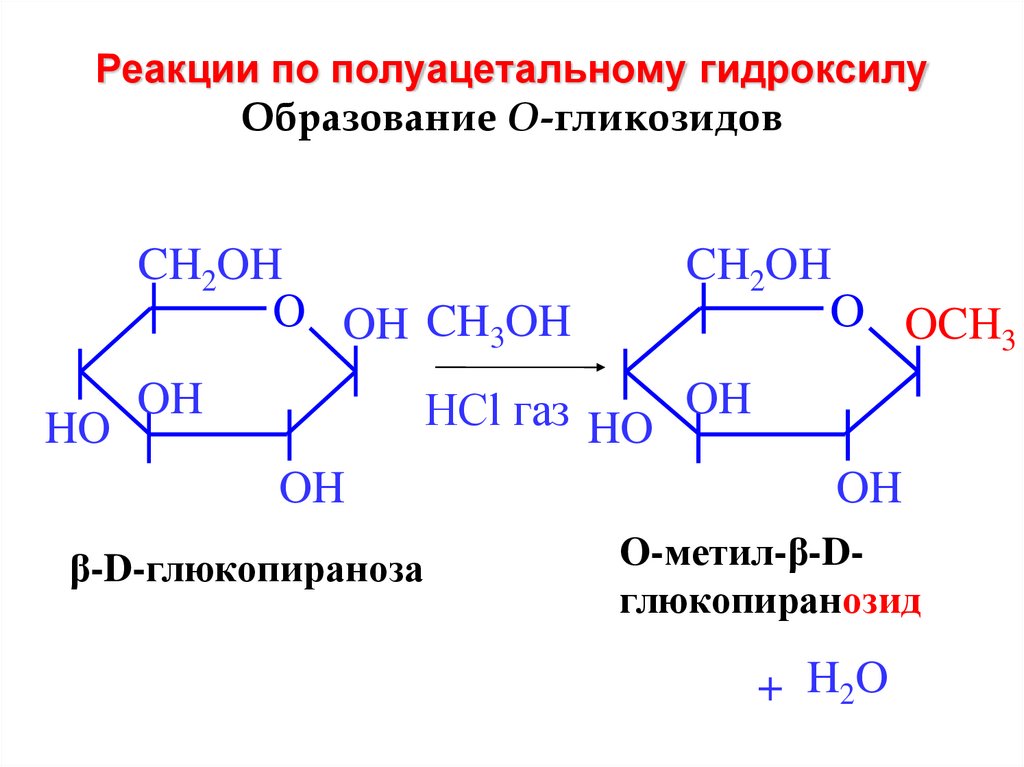
21. Реакции по полуацетальному гидроксилу Образование O-гликозидов
CH2OHO OH CH3OH
HO
OH
CH2OH
O OCH
3
HCl газ HO OH
OH
β-D-глюкопираноза
OH
O-метил-β-Dглюкопиранозид
+ H2O
22. Гидролиз гликозидов
HOCH2OH
O OC H H O
2 5
2
CH2OH
O OH
OH
OH
H+
OH
O-этил-β-Dглюкопиранозид
HO
OH
β-D-глюкопираноза
+ C2H5OH
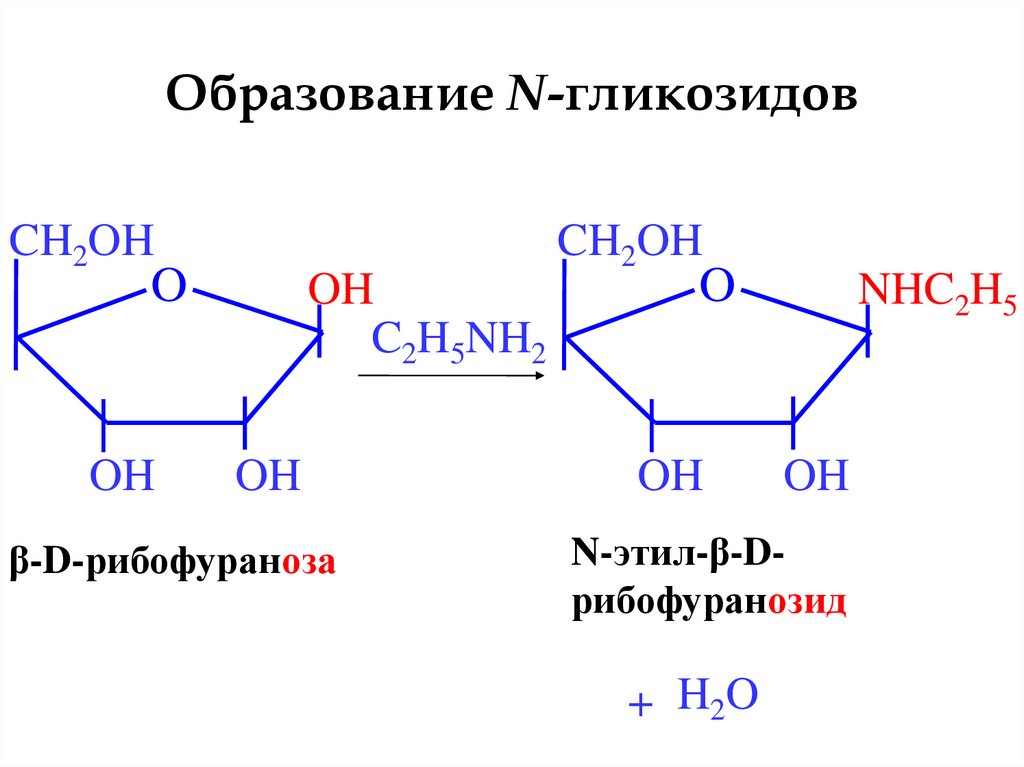
23.
Образование N-гликозидовCH2OH
O
OH
OH
C2H5NH2
OH
β-D-рибофураноза
CH2OH
O
OH
NHC2H5
OH
N-этил-β-Dрибофуранозид
+ H 2O
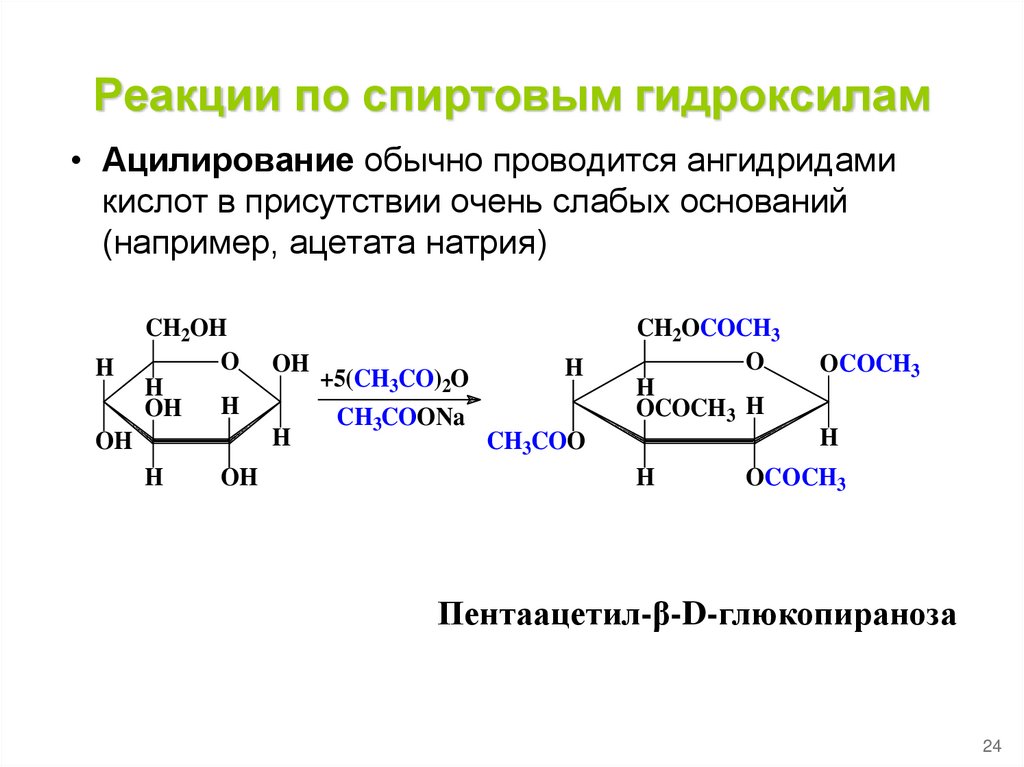
24. Реакции по спиртовым гидроксилам
• Ацилирование обычно проводится ангидридамикислот в присутствии очень слабых оснований
(например, ацетата натрия)
H
CH2OH
O
H
H
OH
OH
H
OH
H
OH
+5(CH3CO)2O
CH3COONa
H
CH2OCOCH3
O
H
OCOCH3 H
OCOCH3
H
CH3COO
H
OCOCH3
Пентаацетил-β-D-глюкопираноза
24
25. Реакции по спиртовым гидроксилам
• Алкилированиеуглеводов
проводят
алкилгалогенидами или диалкилсульфатами:
H
CH2OH
O
H
OH H
OH
H
OH
H
OH
5CH3I
Ag2O
H
CH3O
CH2OCH3
O OCH3
H
HOH
H
OCH3 H
-CH3OH
H
CH3O
H
OCH3
Метил-2,3,4,6-тетра-О-метилβ-D-глюкопиранозид
CH2OCH3
O OH
H
OCH3 H
H
H
OCH3
2,3,4,6-тетра-О-метилβ-D-глюкопираноза
25
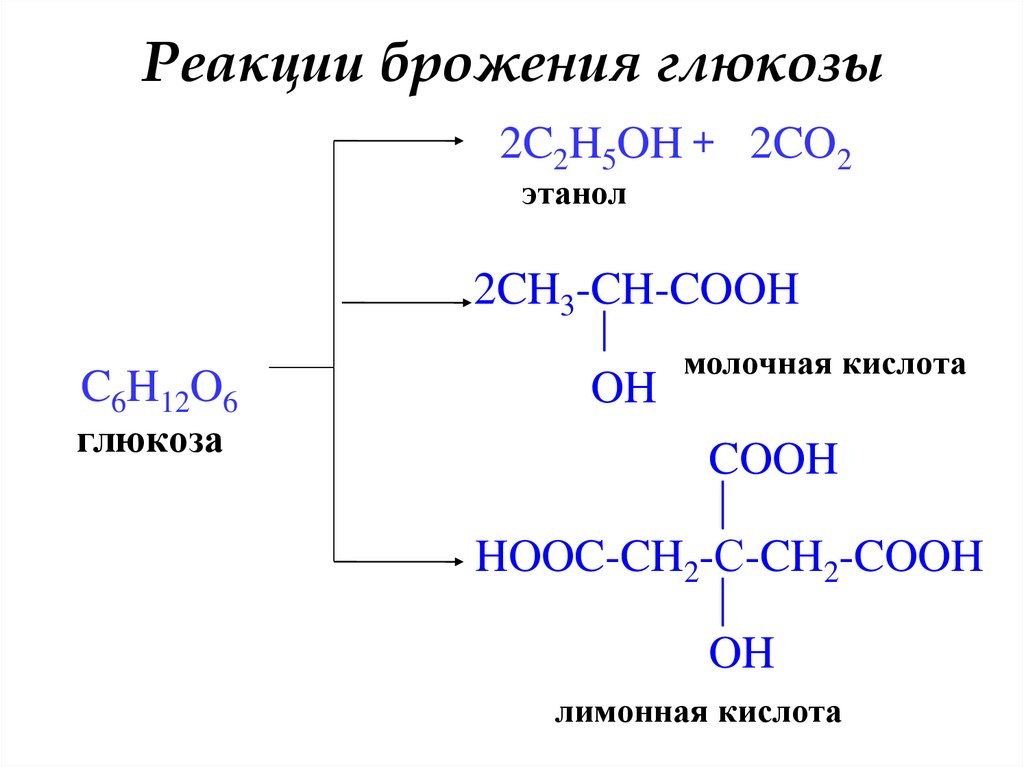
26. Реакции брожения глюкозы
2C2H5OH + 2CO2этанол
2CH3-CH-COOH
C6H12O6
глюкоза
OH
молочная кислота
COOH
HOOC-CH2-С-CH2-COOH
OH
лимонная кислота
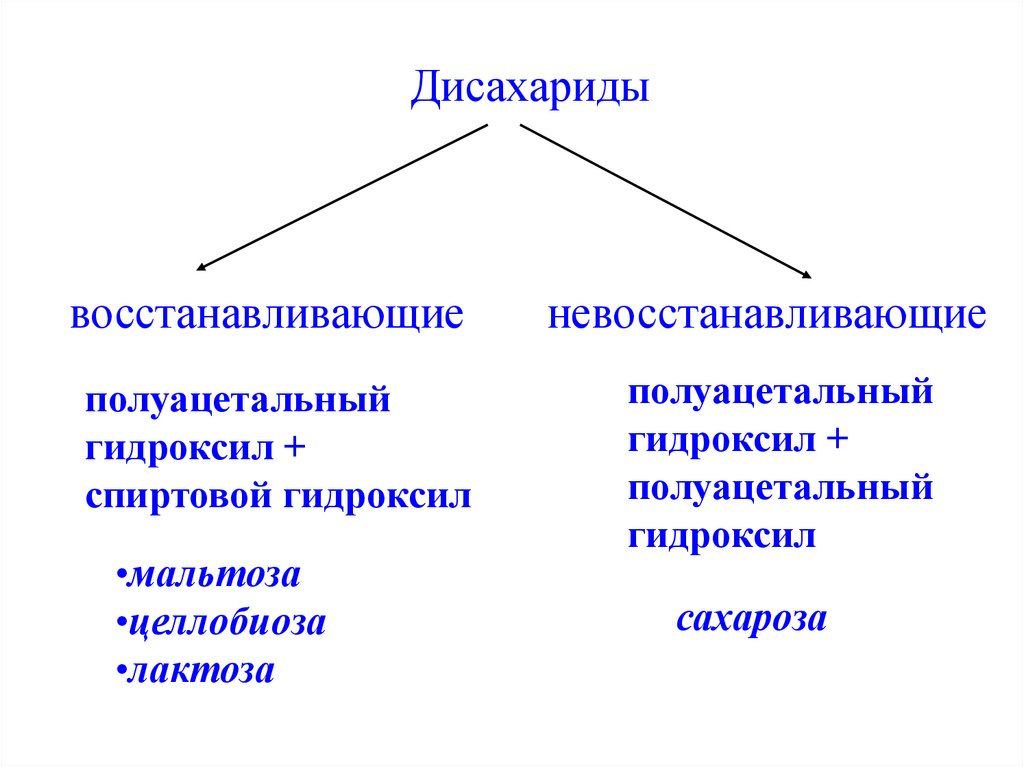
27.
Дисахаридывосстанавливающие
полуацетальный
гидроксил +
спиртовой гидроксил
•мальтоза
•целлобиоза
•лактоза
невосстанавливающие
полуацетальный
гидроксил +
полуацетальный
гидроксил
сахароза
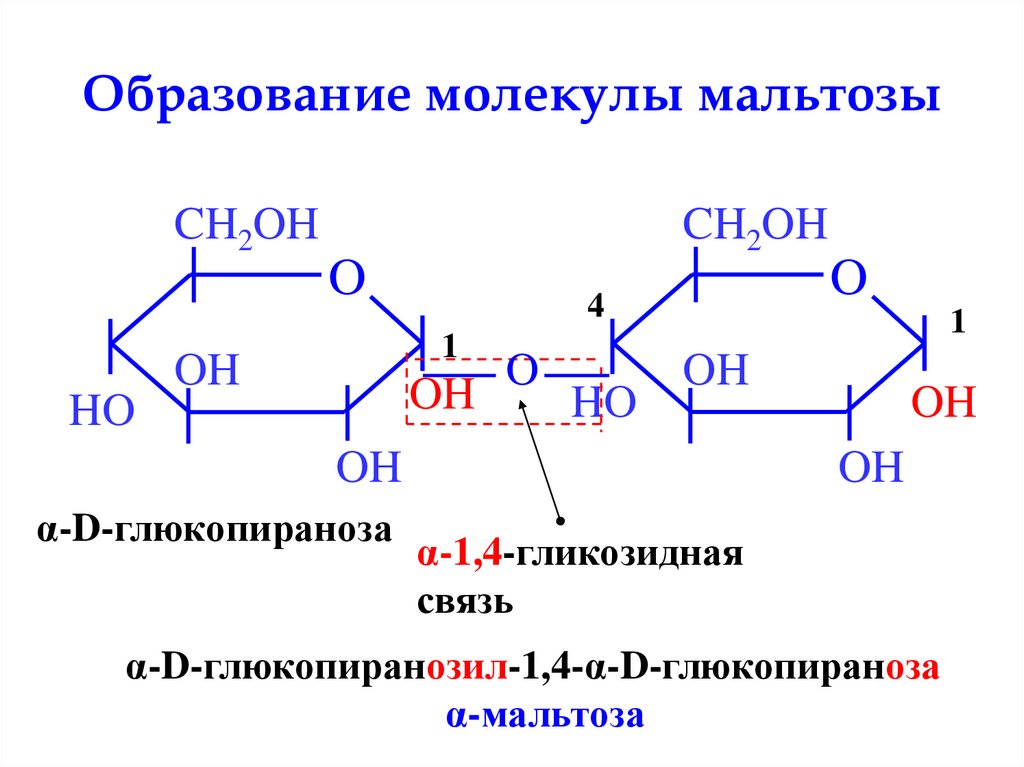
28. Образование молекулы мальтозы
CH2OHCH2OH
O
HO
4
1
OH
O
OH
O
HO
1
OH
OH
OH
α-D-глюкопираноза
OH
α-1,4-гликозидная
связь
α-D-глюкопиранозил-1,4-α-D-глюкопираноза
α-мальтоза
29.
CH2 OHCH2 OH
O
OH
OH
O
HO
OH
Cu(OH)2
to
C
OH
оксо-таутомер мальтозы
Ag(NH3)2OH
to
O
H
OH
продукты окисления
мальтозы + Ag + NH + H O
3
2
продукты окисления
мальтозы + Cu2O + H2O
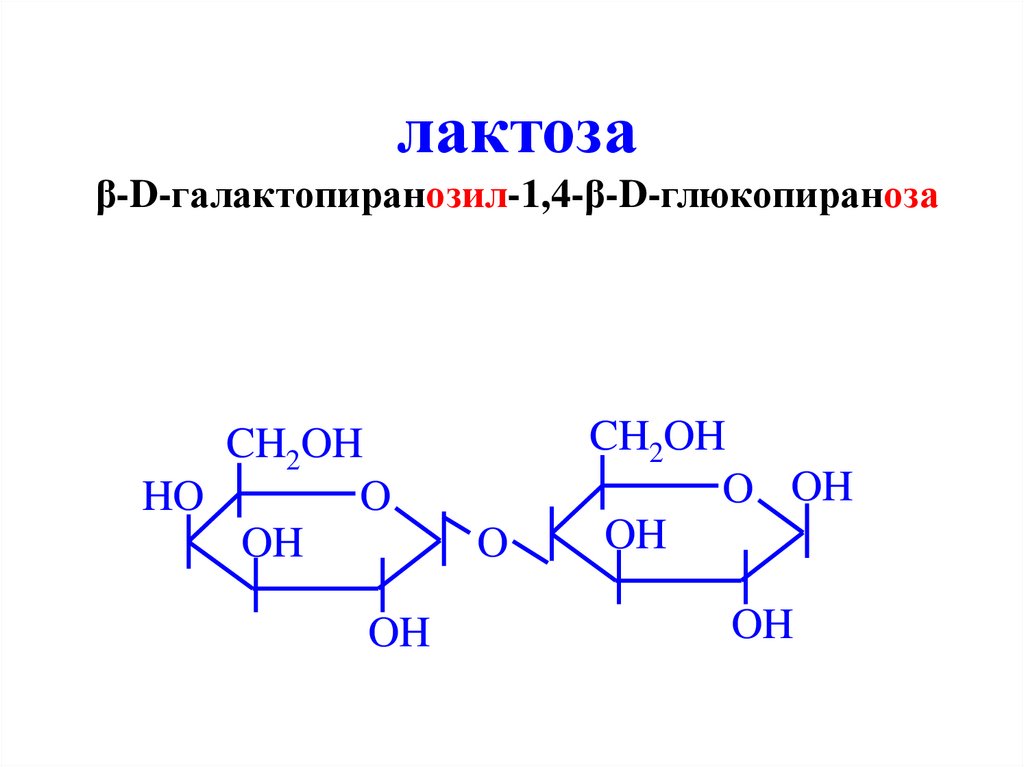
30.
лактозаβ-D-галактопиранозил-1,4-β-D-глюкопираноза
CH2OH
HO
O
OH
OH
O
CH2OH
O OH
OH
OH
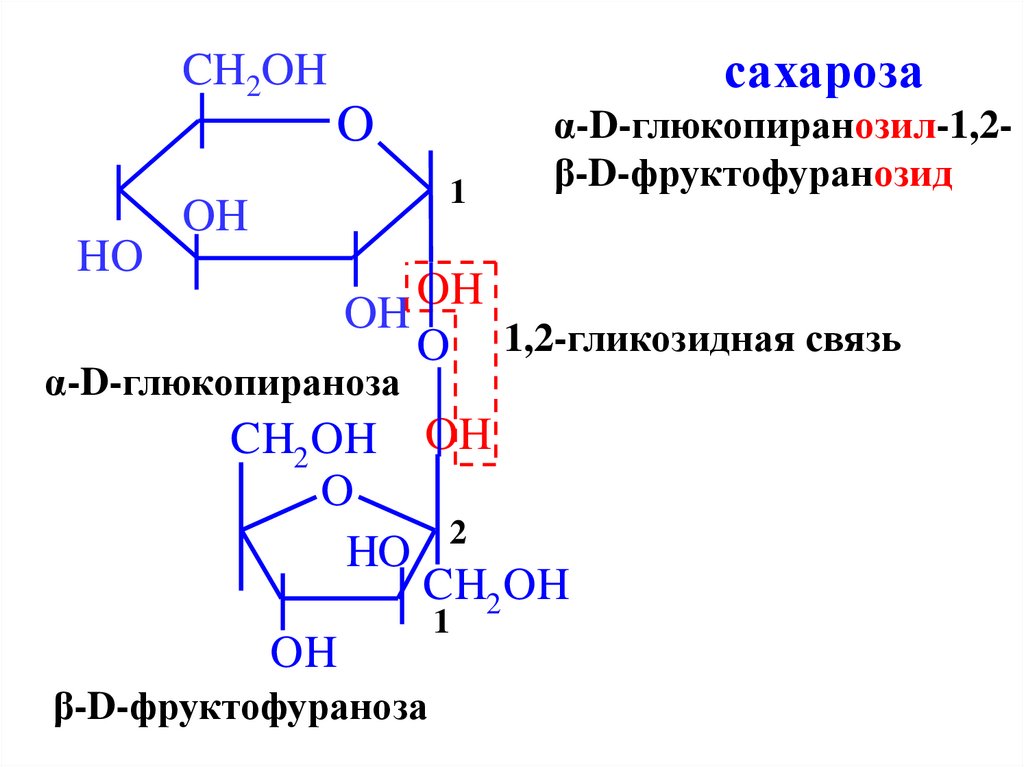
31.
сахарозаCH2OH
O
HO
1
OH
α-D-глюкопиранозил-1,2β-D-фруктофуранозид
OH
OH
O 1,2-гликозидная связь
α-D-глюкопираноза
CH2 OH OH
O
2
HO
CH2 OH
OH
β-D-фруктофураноза
1
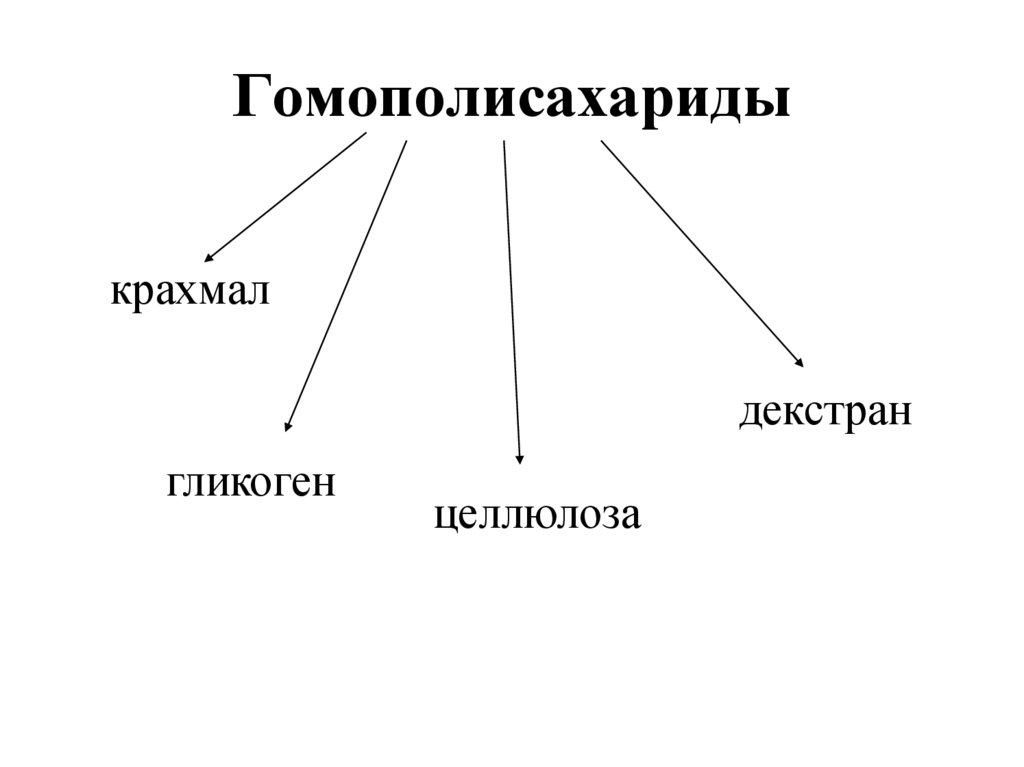
32. Гомополисахариды
крахмалдекстран
гликоген
целлюлоза
33.
Крахмал – гомополимер α-D-глюкозы. (C6H10O5)nНаходится в злаках, бобовых, картофеле
и некоторых других овощах.
Синтезировать крахмал способны почти все растения.
Фракции крахмала:
•амилоза (15-20%)
•амилопектин (80-85%)
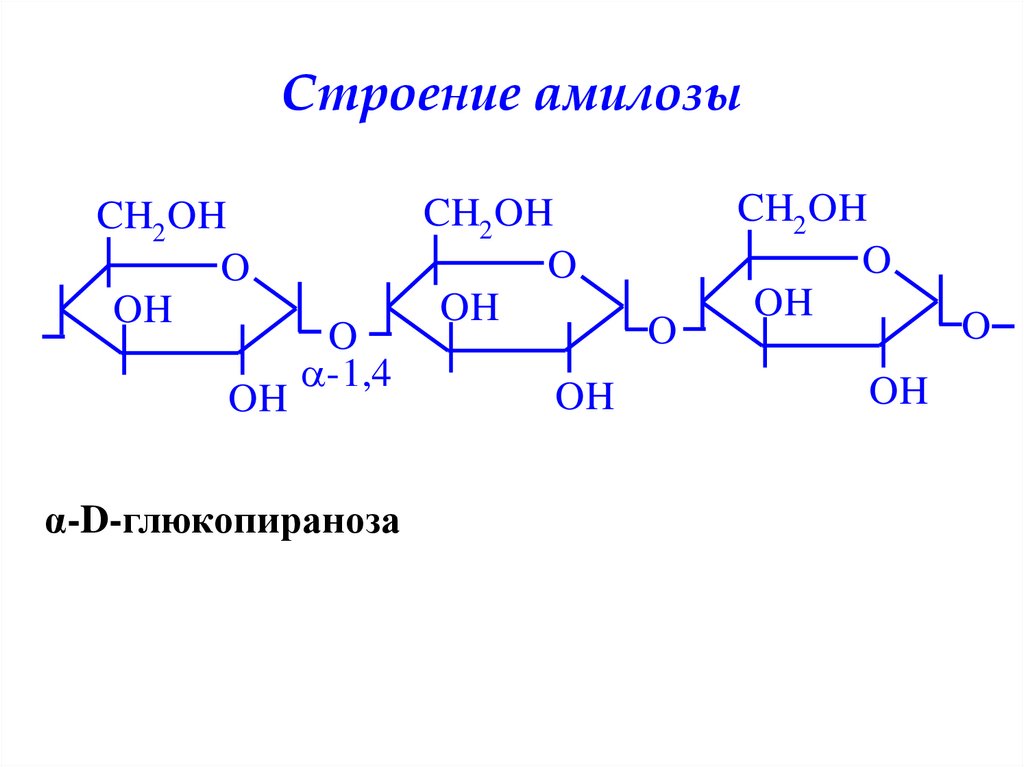
34. Строение амилозы
CH2 OHO
OH
OH
O
-1,4
α-D-глюкопираноза
CH2 OH
O
OH
OH
O
CH2 OH
O
OH
OH
O
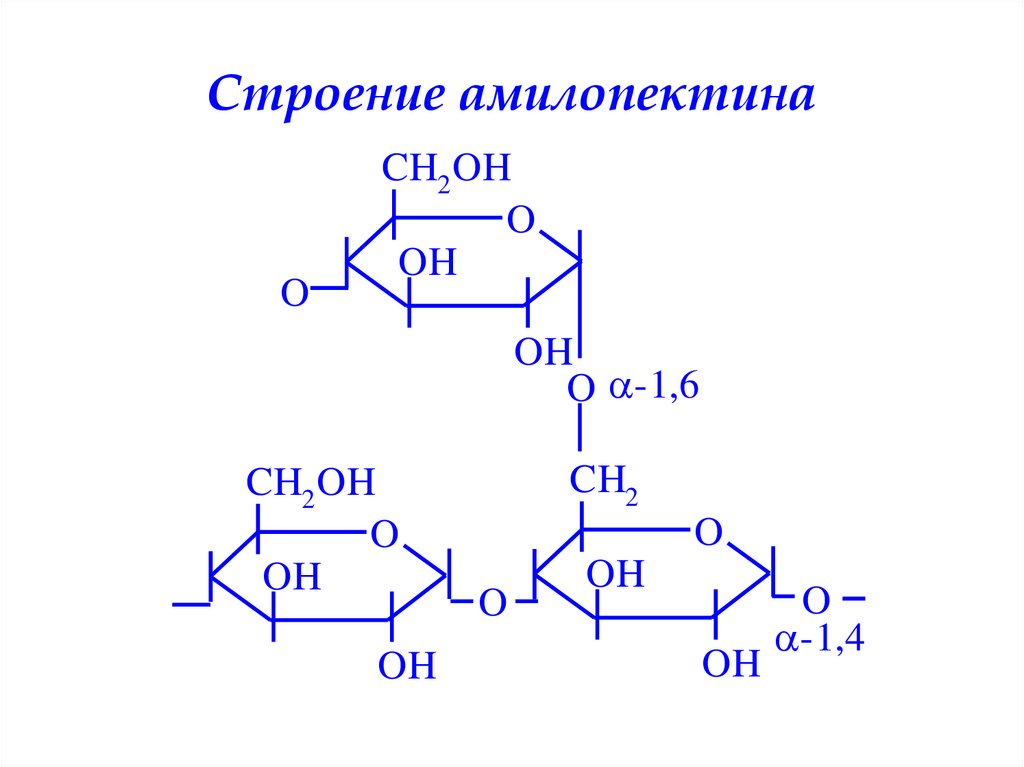
35. Строение амилопектина
OCH2 OH
O
OH
OH
O -1,6
CH2 OH
O
OH
OH
CH2
O
O
OH
OH
O
-1,4
36.
• Гликоген – резервный полисахарид животныхтканей, в наибольшей мере содержится в печени и
мышцах. Структурно он схож с амилопектином,
но длина цепочек меньше – 11-18 остатков
глюкозы, во-вторых, более разветвлен – через
каждые 8-10 остатков. За счет этих особенностей
гликоген более компактно уложен, что
немаловажно для животной клетки.
37.
• Целлюлоза является наиболее распространенныморганическим соединением биосферы. Около
половины всего углерода Земли находится в ее
составе. В отличие от предыдущих полисахаридов
она является внеклеточной молекулой, имеет
волокнистую структуру и абсолютно
нерастворима в воде. Единственной связью в ней
является β-1,4-гликозидная связь.
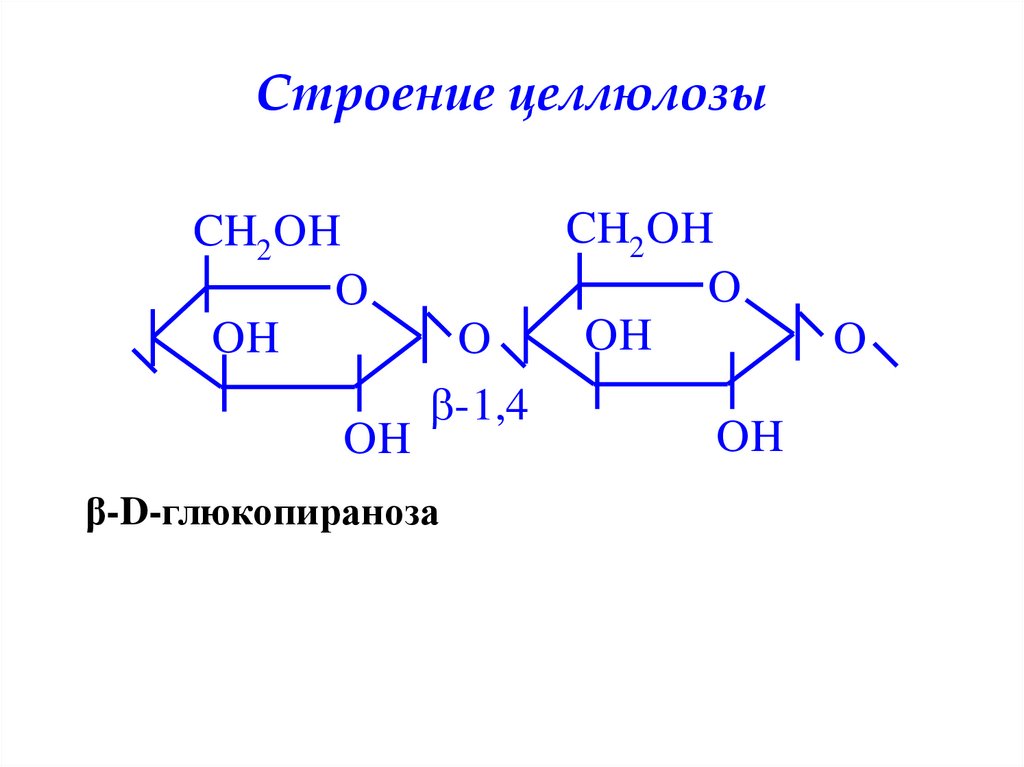
38. Строение целлюлозы
CH2 OHO
OH
OH
O
-1,4
β-D-глюкопираноза
CH2 OH
O
OH
OH
O
39. Гетерополисахариды
ГепаринКамеди
Слизи
Гиалуроновая
кислота
Пектиновые Полисахариды
вещества соединительной
ткани (хондроитинсульфаты)
40.
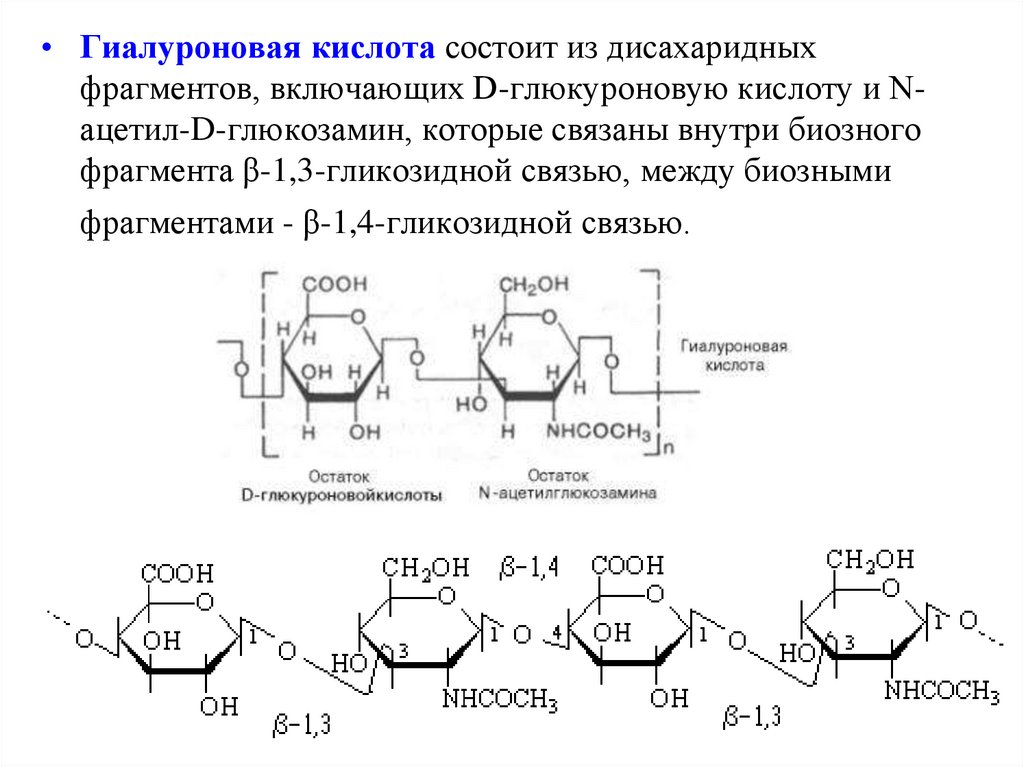
• Гиалуроновая кислота состоит из дисахаридныхфрагментов, включающих D-глюкуроновую кислоту и Nацетил-D-глюкозамин, которые связаны внутри биозного
фрагмента β-1,3-гликозидной связью, между биозными
фрагментами - β-1,4-гликозидной связью.
41.
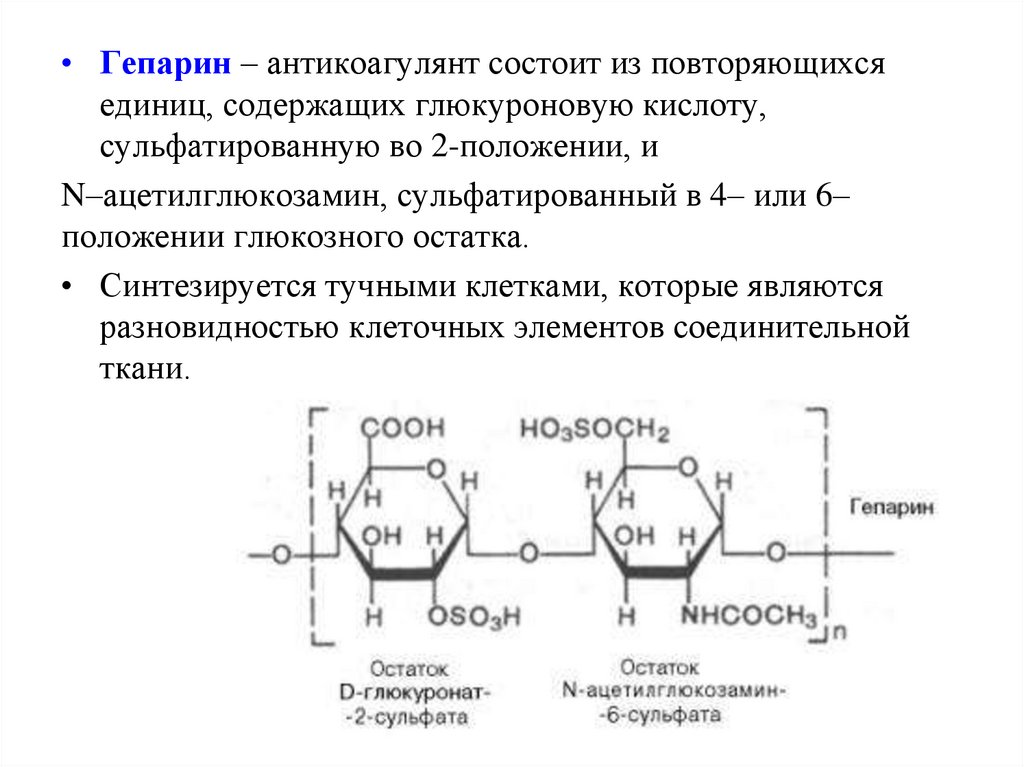
• Гепарин – антикоагулянт состоит из повторяющихсяединиц, содержащих глюкуроновую кислоту,
сульфатированную во 2-положении, и
N–ацетилглюкозамин, сульфатированный в 4– или 6–
положении глюкозного остатка.
• Синтезируется тучными клетками, которые являются
разновидностью клеточных элементов соединительной
ткани.












 Биология
Биология Химия
Химия